Клинический разбор в общей медицине №02 2026
1 Urgench State Medical Institute, Urgench, Uzbekistan;
2 Abu Ali ibn Sino Bukhara State Medical Institute, Bukhara, Uzbekistan
gmatrizayeva@gmail.com
Abstract
Polycystic ovary syndrome (PCOS) is one of the leading causes of endocrine infertility. This study evaluated the effectiveness of conservative, surgical, and combined treatment approaches for restoring reproductive function in women with PCOS.
Aim. To evaluate the effectiveness of various fertility restoration methods in patients with PCOS.
Materials and methods. A prospective study included 70 women with PCOS-associated infertility and 20 healthy controls. Patients were divided into three subgroups based on treatment approach. Clinical, hormonal, metabolic, and ultrasound parameters were analyzed.
Conclusion. Combined conservative and surgical treatment provided more stable and long-term fertility restoration compared to isolated surgical intervention.
Keywords: polycystic ovary syndrome, infertility, fertility restoration, laparoscopy, ovulation induction.
For citation: Matrizaeva G.D., Rajabova G.O., Ikhtiyarova G.A., Khaitov A.O., Ikramova Kh.S. Effectiveness of fertility restoration methods in women with polycystic ovary syndrome. Clinical review for general practice. 2026; 7 (2): 84–91 (In Russ.). DOI: 10.47407/kr2026.7.2.00773
Введение
Синдром поликистозных яичников (СПЯ) по-прежнему остается одной из наиболее значимых и недостаточно изученных проблем гинекологической эндокринологии и репродуктивной медицины. Согласно европейским данным, распространенность СПЯ достигает около 15%. Среди пациенток с эндокринным бесплодием доля женщин с СПЯ составляет до 73% [1, 2], а в структуре бесплодных браков данная патология выявляется в 20–22% случаев, занимая 5–6-е место. Высокая актуальность проблемы обусловлена значительной распространенностью синдрома и его неблагоприятным влиянием на репродуктивную функцию.
Целесообразность применения эндоскопических методов у пациенток с подозрением на СПЯ подтверждена рядом исследований [3, 4]. Лапароскопия позволяет не только визуально оценить состояние яичников, но и выполнить их биопсию, что способствует уточнению диагноза и выбору оптимальной тактики лечения. Преимущества лапароскопического доступа по сравнению с лапаротомией включают минимальную операционную травму, высокую диагностическую информативность, снижение риска спаечного процесса в малом тазу и сокращение сроков госпитализации [5, 6].
Следует подчеркнуть, что эффективность лечения пациенток с СПЯ определяется не столько устранением морфологических изменений яичников, сколько восстановлением овуляторной функции и достижением беременности. Хирургические методы рассматриваются как вторая линия терапии при СПЯ. Несмотря на разнообразие лапароскопических вмешательств, их патогенетическая суть заключается в частичном нарушении целостности овариальной ткани, что приводит к временному снижению андрогенной активности и восстановлению эндокринных регуляторных механизмов [1].
Цель исследования – оценить эффективность различных методов восстановления фертильности у пациенток с СПЯ.
Предмет и объект исследования: обследованы 90 женщин. В проспективное исследование включены 70 женщин с бесплодием и СПЯ, контрольную группу составили 20 женщин репродуктивного возраста с регулярными овуляторными циклами.
В связи с этим женщины, включенные в основную группу, были разделены на три подгруппы в зависимости от применяемых методов лечения:
• Первая подгруппа (А) – 25 пациенток, у которых антиандрогенный эффект достигался путем применения комбинированных оральных контрацептивов (КОК) в течение не менее 3 мес, с последующей индукцией овуляции.
• Вторая подгруппа (Б) – 20 пациенток, которым после применения КОК в течение 3–6 мес было выполнено хирургическое вмешательство на яичниках лапароскопическим методом в объеме дриллинга.
• Третья подгруппа (В) – 25 пациенток, перенесших хирургическое вмешательство в объеме лапароскопического дриллинга без предварительной подготовки.
Под нашим наблюдением находились 70 пациенток с СПЯ в возрасте от 22 до 37 лет (средний возраст – 31,9±1,4 года), страдающих бесплодием продолжительностью от 1 до 10 лет (в среднем 5,3±1,2 года). Во всех случаях были исключены трубный, цервикальный, иммунологический, а также мужской факторы бесплодия.
Методы
Для обследования женщин используют общепринятые методы, включающие сбор анамнеза, жалоб, осмотр и лабораторные исследования: на 2–5-й день менструации – фолликулостимулирующий гормон (ФСГ), лютеинизирующий гормон (ЛГ), пролактин, индекс свободных андрогенов (дегидроэпиандростерон-сульфат – ДГЭА-S, тестостерон) и антимюллеров гормон, ультразвуковое трансвагинальное исследование.
Нарушение метаболизма глюкозы определялось с помощью глюкозотолерантного теста (ГТТ). Кроме того, определялась концентрация инсулина в плазме венозной крови натощак. Критериями инсулинорезистентности служили: индекс I/G (отношение базального уровня инсулина к базальному уровню глюкозы), а также индекс HOMA (Homeostasis Model Assessment): базальный уровень глюкозы (ммоль/л) × базальный уровень инсулина (мкМЕ/мл) / 22,5. Инсулинорезистентность считалась при индексе показателей HOMA>2,77.
Ультразвуковое исследование (УЗИ) для определения состояния органов малого таза проводилось на 5–7-е сутки менструального цикла на аппарате SonoScape 40 (Китай) с трансвагинальным контролем.
Одновременно оценивали морфологию яичников: количество антральных фолликулов (на 2–3-й день менструального цикла), толщину капсулы, эхогенность стромы и объем яичников. Также оценивали размеры матки и толщину эндометрия.
Принципы лечения. при бесплодии на фоне СПЯ базисная терапия проводится в два этапа:
• 1-й подготовительный этап – нормализация основных регуляций репродуктивной системы;
• 2-й этап – стимуляция овуляции.
На подготовительном этапе нормализация обмена веществ, в том числе лечение ожирения, достигается за счет гипокалорийной диеты, физической активности и препарата орлистат – блокатора желудочно-кишечной липазы, 3 капсулы по 120 мг во время или после еды (применение препарата обусловлено отсутствием инкретиновых препаратов в достаточной реальности). При гиперинсулинемии или нарушении толерантности к глюкозе – метформин по 1000 мг два раза в день после еды в течение 6 мес.
С целью нормализации менструального цикла назначались препараты КОК (этинилэстрадиол/дроспиренон 20–30 мкг/3 мг) в течение не менее 3–6 мес.
Овуляцию индуцировали по схеме цитратом кломифена или летрозолом, при необходимости использовали хорионический гонадотропин под ультразвуковым контролем.
Основную группу составила группа пациенток с СПЯ, которая была разделена на 3 подгруппы. В зависимости от этого сравнивалась эффективность консервативной терапии и хирургического лечения.
Результаты
С учетом полиморфизма причин развития СПЯ нами был проведен анализ социальных факторов риска развития заболевания у отобранных групп женщин.
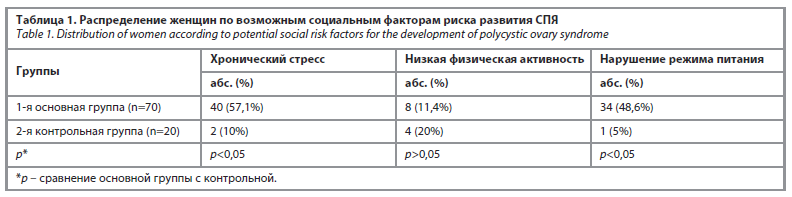
При сравнительном анализе факторов образа жизни между основной и контрольной группами выявлены статистически значимые различия по частоте хронического стресса (p=0,0005) и нарушений режима питания (p=0,0011). Различия по уровню физической активности между группами статистически значимыми не были (p=0,53); табл. 1.
Следует также отметить, что у женщин, занимающихся тяжелым физическим трудом, СПЯ протекал в более выраженной форме. Это может быть связано с относительно повышенной секрецией стероидных гормонов коры надпочечников в условиях физического перенапряжения. У большинства женщин основной группы в подростковом возрасте и в течение последних 3–5 лет в анамнезе были выявлены выраженные психоэмоциональные стрессовые воздействия, сопровождавшиеся состоянием хронического стресса. Известно, что в условиях стресса усиливается секреция стероидных гормонов надпочечников, что, в свою очередь, могло способствовать вторичному развитию СПЯ.
У женщин с СПЯ отмечалось бесплодие, которое само по себе приводит к психоэмоциональной лабильности и тем самым усугубляет течение заболевания.
С точки зрения диагностики рассматриваемого заболевания особый интерес представляют клинические проявления СПЯ.
Клинические проявления СПЯ у обследованных женщин можно условно разделить на три основные группы:
1) нейропсихические изменения, включающие нарушения сна, раздражительность, быструю утомляемость и снижение либидо;
2) вегетативные нарушения, такие как нестабильное артериальное давление, отеки, потливость;
3) метаболические изменения, включая гирсутизм, акне и снижение способности к снижению массы тела.
Анализ выбранных групп женщин показал, что различия в нейропсихических нарушениях между основной и контрольной группами статистически незначимы. Так, возбудимость наблюдалась у 28,6% женщин основной группы и 25% женщин контрольной группы (χ²=0,001; p=0,975), нарушения сна – у 21,4 и 15% соответственно (χ²=0,10; p=0,751), а быстрая утомляемость отмечалась у 24,3% женщин основной группы и у 40% контрольной (χ²=1,21; p=0,271). Таким образом, нейропсихические симптомы сопоставимы между группами, однако наблюдается тенденция к большей усталости в контрольной группе.
Вегетативные нарушения были значительно более выражены у женщин основной группы. Нестабильное артериальное давление отмечалось у 64,3% пациенток основной группы по сравнению с 5% контрольной (χ²=19,57; p<0,0001). Отеки встречались у 44,3% женщин основной группы и лишь у 10% контрольной (χ²=6,47; p=0,011), а повышенная потливость наблюдалась у 37 и 5% соответственно (χ²=6,20; p=0,013). Эти результаты свидетельствуют о статистически значимом увеличении частоты вегетативных нарушений у женщин основной группы, что может быть связано с длительным стрессовым воздействием и эндокринными нарушениями.
Метаболические проявления СПЯ также были значительно выражены в основной группе. Акне регистрировалось у 82,9% женщин основной группы и только у 5% контрольной (χ²=38,38; p<0,0001), гирсутизм – у 85,7% против 20% соответственно (χ²=29,58; p<0,0001), а трудности с похудением отмечались у 51,4% пациенток основной группы и лишь у 15% контрольной (χ²=6,99; p=0,008). Эти данные подчеркивают выраженное влияние СПЯ на проявления гиперандрогенного синдрома и метаболические показатели.
Таким образом, комплексный анализ клинических проявлений показывает, что у женщин основной группы нейропсихические изменения статистически не различались с контрольной группой, однако вегетативные и метаболические нарушения были достоверно более выражены.
Известно, что индекс массы тела (ИМТ) характеризует метаболические изменения, характерные для СПЯ. В исследовании участницы основной группы (n=70) и контрольной группы (n=20) были распределены по категориям ИМТ.
У женщин основной группы нормальная масса тела (ИМТ 18,5–25) наблюдалась у 24 (34,3%) пациенток, тогда как в контрольной группе эта категория преобладала – 17 (85%) женщин. Избыточная масса тела (ИМТ 25–30) отмечалась у 21 (30%) женщины основной группы и 2 (10%) женщин контрольной группы. Первую степень ожирения (ИМТ 30–35) имели 15 (21,4%) женщин основной группы и 1 (5%) женщина контрольной. Вторую степень ожирения (ИМТ 35–40) имели 6 (8,6%) женщин основной группы, третью степень (ИМТ>40) – 4 (5,7%) женщины, в контрольной группе этих категорий не наблюдалось.
Статистический анализ показал, что различия между основной и контрольной группой были статистически значимыми для категории нормальной массы тела (χ²=14,15; p=0,00017), что указывает на значительное преобладание нормальной массы тела в контрольной группе. Различия по остальным категориям (избыточная масса тела, I–III степень ожирения) статистически значимы не были (p>0,05), хотя тенденция к большей распространенности ожирения у женщин основной группы очевидна.
Таким образом, у женщин с СПЯ наблюдается тенденция к увеличению доли избыточной массы тела и ожирения, что подчеркивает значимость контроля веса и метаболических факторов в комплексной терапии данного синдрома.
Опрос 70 пациенток с СПЯ показал, что у большинства из них с самого начала менструаций отмечались различные нарушения менструального цикла.
Нормальная менструация встречалась у 30% женщин основной группы и у всех женщин контрольной группы, различие статистически значимо (p<0,0001). Олигоменорея и аменорея значительно чаще наблюдались у женщин основной группы.
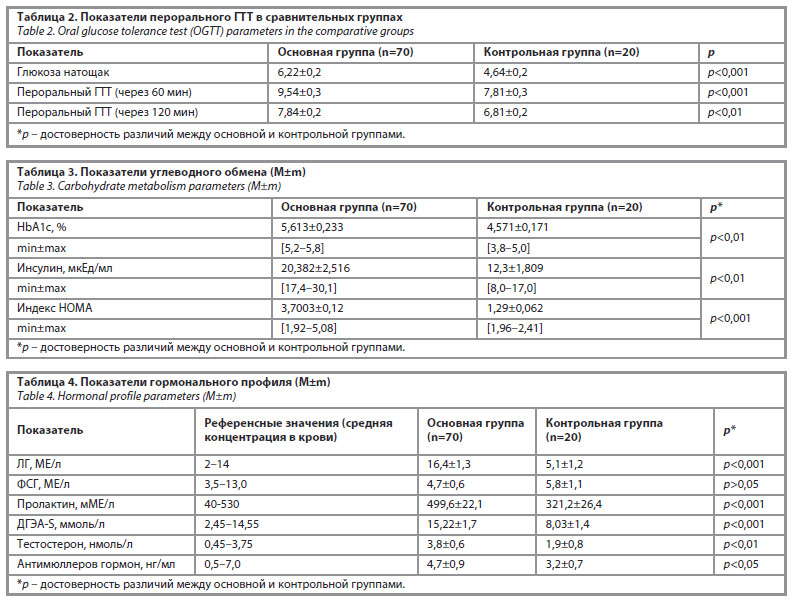
Изучение уровня глюкозы показало, что у 42 женщин основной группы отмечалось повышение ее концентрации в крови, а после проведения теста толерантности к глюкозе данный показатель увеличился до 56 пациенток и в среднем составил 6,22±0,2 ммоль/л. В группе сравнения практически у всех женщин уровень глюкозы натощак находился в пределах нормы и в среднем составлял 4,64 ммоль/л.
После проведения ГТТ существенных изменений не наблюдалось: в основной группе через 60 мин после начала нагрузки средний уровень глюкозы составил 9,54±0,3 ммоль/л, в группе сравнения – 7,81±0,3 ммоль/л (p<0,001).
Через 120 мин гипергликемия в основной группе сохранялась на уровне 7,84±0,2 ммоль/л, тогда как в группе сравнения средний показатель составил 5,4 ммоль/л (табл. 2). Остальные биохимические показатели у данных пациенток находились в пределах нормативных значений.
Как видно из представленных данных, во всех временных точках показатели перорального ГТТ в основной группе были статистически значимо выше по сравнению с контрольной группой (p<0,001), что свидетельствует о наличии выраженных нарушений углеводного обмена у пациенток основной группы.
Анализ показал, что в основной группе уровни гликированного гемоглобина (HbA1c) и инсулина были статистически значимо выше по сравнению с контрольной группой (p<0,01), что свидетельствует о выраженных нарушениях углеводного обмена. Индекс HOMA в основной группе превышал показатели контрольной группы почти в 3 раза, при этом выявленные различия носили высокодостоверный характер (p<0,001), что указывает на наличие выраженной инсулинорезистентности (табл. 3).
В дальнейшем нами были проведены гормональные исследования, результаты которых представлены в табл. 4.
Представленный анализ гормонального профиля показал наличие достоверных различий между основной и контрольной группами по ряду ключевых показателей. В частности, уровень ЛГ в основной группе был статистически значимо выше по сравнению с контрольной группой (16,4±1,3 МЕ/л против 5,1±1,2 МЕ/л; p<0,001), что указывает на выраженные нарушения гипоталамо-гипофизарной регуляции репродуктивной системы.
Концентрация пролактина у пациенток основной группы также была достоверно выше, чем в контрольной группе (499,6±22,1 мМЕ/л и 321,2±26,4 мМЕ/л соответственно; p<0,001), что свидетельствует о наличии гиперпролактинемии и ее возможном влиянии на репродуктивную функцию. Аналогичная тенденция отмечена и в отношении уровня дегидроэпиандростерон-сульфата (ДГЭА-S), который в основной группе превышал показатели контрольной группы более чем в 1,8 раза (15,22±1,7 ммоль/л против 8,03±1,4 ммоль/л; p<0,001), указывая на признаки гиперандрогении надпочечникового генеза.
Уровень тестостерона в основной группе также был статистически значимо выше по сравнению с контрольной группой (3,8±0,6 и 1,9±0,8 нмоль/л соответственно; p<0,01), что подтверждает наличие андрогенного дисбаланса у обследованных пациенток. При этом уровень антимюллерова гормона в основной группе достоверно превышал аналогичный показатель контрольной группы (4,7±0,9 нг/мл против 3,2±0,7 нг/мл; p<0,05), отражая особенности овариального резерва и функционального состояния яичников.
Согласно полученным нами данным, у пациенток с СПЯ наиболее неблагоприятным фактором является сочетание повышения уровня ЛГ, отражающего наличие инсулинорезистентности, связанной с увеличением объема яичников и способствующей их поликистозной трансформации, а также комплекса клинико-лабораторных параметров.
Полученные данные свидетельствуют о синергическом воздействии инсулина и ЛГ, что, в свою очередь, приводит к формированию поликистозных яичников.
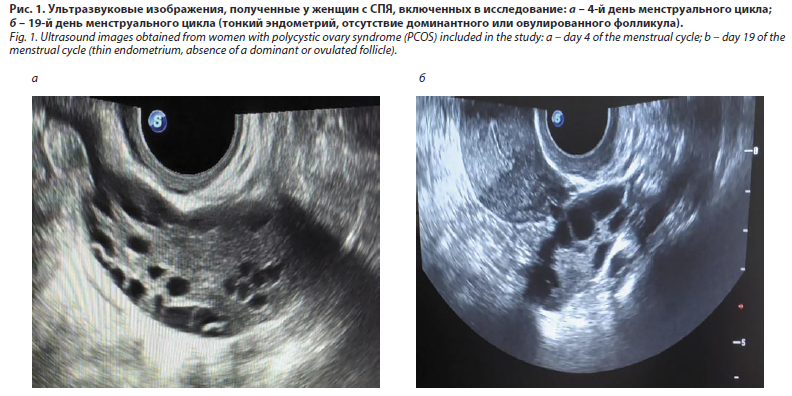
Критерии диагностики СПЯ включают эхографические признаки УЗИ (рис. 1). Основными проявлениями заболевания являются увеличение объема яичников (свыше 10 см3), наличие гиперпластической стромы не менее 25%, наличие атретических фолликулов диаметром более 10 мм, а также уменьшение переднезаднего размера матки.
Переднезадний размер матки составил в 1-й группе 32,0–34,0 мм, во 2-й группе – от 35,0 до 42,0 мм, при этом выявлена статистически значимая разница между группами.
Анализ эхографических размеров яичников показал, что у женщин с СПЯ все параметры (длина, толщина, ширина, объем яичников, диаметр фолликулов и количество антральных фолликулов) были статистически значимо выше по сравнению с контрольной группой (p<0,05). Эти данные подтверждают наличие поликистозной трансформации яичников у пациенток основной группы.
Особенно заметно различие в объеме яичников, который в основной группе превышал таковой у контрольной группы более чем в 5 раз (37,064±3,049 см3 против 7,371±0,809 см3; p<0,05), что является ключевым ультразвуковым признаком СПЯ.
При сравнительном анализе соотношения объема яичников к объему матки у пациенток 1-й группы объем обоих яичников приближался к объему матки: в среднем 97,3%. У женщин контрольной группы объем яичников составлял 31,1%, т.е. примерно треть объема матки (p<0,05). У 68 (97,1%) пациенток 1-й группы этот показатель превышал 50%. В контрольной группе у 96% женщин с объемом яичников менее 50% от объема матки наблюдались нормальные яичники.
Было выявлено статистически значимое положительное корреляционное соотношение между объемом яичников и уровнями ЛГ и инсулина в крови (p<0,05).
УЗИ показало увеличение объема яичников у 93,22% пациенток, при этом у женщин с СПЯ отмечалось диффузное расположение фолликулов в 65,57% случаев. Этот показатель существенно не зависел от наличия или отсутствия ожирения.
В последние годы у женщин с СПЯ были выявлены высокая вероятность резистентности к индукции овуляции с использованием кломифена цитрата или летрозола, а также повышенный риск развития синдрома гиперстимуляции яичников при терапии гонадотропинами. По этой причине в последние годы возрос интерес к хирургическим методам лечения СПЯ. Кроме того, совершенствование эндоскопических техник привело к широкому распространению минимально инвазивных вмешательств.
Целью данного исследования является восстановление репродуктивного здоровья у пациенток с СПЯ посредством оптимизации консервативных и хирургических методов лечения с учетом клинических, морфологических и эндокринно-метаболических особенностей заболевания.
В нашем исследовании мы выявили различные клинические и морфологические формы СПЯ на основании ультразвуковых, эндоскопических и морфологических исследований. Для выбранных вариантов СПЯ мы изучили гормональный и метаболический гомеостаз у пациенток, уточнили показания к хирургическому лечению и провели сравнительный анализ эффективности дриллинга яичников.
Хирургическое лечение эндоскопическим методом было выполнено у 45 пациенток под спинальной анестезией с использованием аппарата фирмы «Storz».
Таким образом, основные моменты декортикации яичников включают:
• выбор места, правильное удержание и фиксацию яичника;
• сохранение фолликулярного аппарата при проведении дриллинга яичников;
• обеспечение адекватного гемостаза и тщательное промывание брюшной полости.
С учетом этих рекомендаций риск при выполнении операции был минимальным, и во время вмешательства не наблюдалось никаких осложнений. Проходимость маточных труб была проверена. После завершения хирургического вмешательства брюшная полость промывалась физиологическим раствором. Продолжительность операции в среднем составила 20–30 мин. Общая кровопотеря не превышала 50 мл. Осложнения не отмечались. Пациентки вставали с постели через 6–8 ч после операции. В дальнейшем, на 2–3-и сутки после хирургического вмешательства, пациентки выписывались из стационара в удовлетворительном состоянии.
При лапароскопическом исследовании у женщин с СПЯ выявлены характерные признаки: жемчужно-серый цвет, гладкая, блестящая, растянутая поверхность с характерным сосудистым рисунком или петлевидными сосудами, наличие субкапсулярных прозрачных кист диаметром от 0,3 до 2,0 см, плотная или равномерно утолщенная капсула.
На разрезе яичников обнаруживались мелкие прозрачные или желтоватые кисты диаметром 0,3–2,0 см (обычно от 10 до 15 кист на каждый яичник).
Яичники имели различные размеры: от слегка увеличенных (4,5×2,5×4,5 см) до значительно увеличенных (11,4×5,7×8,6 см). У 82,1% пациенток яичники были увеличены, у 17,9% – в пределах нормы (верхняя граница нормального размера яичников: 4×1,5×3 см). Одностороннее увеличение наблюдалось только у 19 пациенток, у остальных – двустороннее. У 30 (66,7%) пациенток яичники имели шаровидную форму, у 15 (31,2%) пациенток – овальную форму.
Во всех 45 наблюдениях выявлены 5 и более характерных признаков СПЯ, включая увеличение яичников, гладкую блестящую поверхность с сосудистым рисунком на мембране, растянутую поверхность и субкапсулярные кисты, а также наличие мелких кист на разрезе.
У 42 (93,3%) пациенток в заднем своде матки свободной жидкости в брюшной полости не обнаружено. Аналогичные данные на лапароскопической картине указывают на отсутствие овуляции. Следует отметить, что при различной природе нарушений менструального цикла эндоскопическая картина яичников у пациенток с СПЯ не имела различий.
После лечения были повторно обследованы гормональные показатели только у подгрупп А и Б основной группы. Причина в том, что группа В и контрольная группа не получали никакой медикаментозной терапии.
Подгруппы А и Б были повторно обследованы после шестимесячного курса лечения на уровни ЛГ, ФСГ и глюкозы в крови (табл. 5). У женщин с гиперинсулинемией уровень глюкозы в крови полностью нормализовался.
После проведенного лечения у пациенток с СПЯ показатели ЛГ и соотношение ЛГ/ФСГ изменились в зависимости от примененного метода терапии.
Подгруппа А, получавшая только КОК, показала умеренное снижение ЛГ и ЛГ/ФСГ (2,3±0,3; p<0,01), при этом уровень ФСГ изменился незначительно.
Подгруппа Б, где применялась комбинированная терапия – КОК с последующим лапароскопическим дриллингом яичников, продемонстрировала наиболее выраженную нормализацию гормонального фона. Уровень ЛГ снизился до 9,5±0,5 МЕ/л, а соотношение ЛГ/ФСГ – до 2,1±0,5 (p<0,01), что подчеркивает высокую эффективность комбинированного подхода.
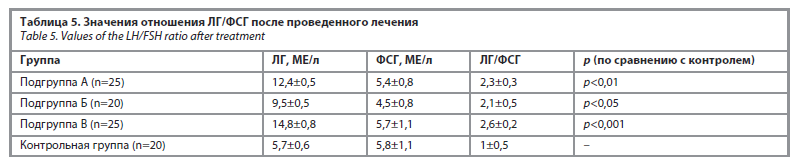
В подгруппе В, где проводилось только лапароскопическое вмешательство, показатели ЛГ и ЛГ/ФСГ оставались высокими (2,6±0,2; p<0,001), что указывает на ограниченный эффект монотерапии без предварительной консервативной подготовки.
Таким образом, данные подтверждают, что комбинация КОК с лапароскопическим дриллингом (подгруппа Б) обеспечивает наиболее стабильную нормализацию гормонального баланса у пациенток с СПЯ.
Согласно результатам обследования, у пациенток подгрупп А и Б отмечалось значительное изменение уровней ЛГ и ФСГ: уровень ЛГ снизился в 2 раза, при этом уровень ФСГ достиг нормальных значений. Соотношение ЛГ/ФСГ уменьшилось до границ 1,5–1,2. Это свидетельствует о возможности перехода к следующему этапу лечения.
У пациенток 1-й группы фолликулогенез был обеспечен при помощи кломифена цитрата или летрозола, а овуляция стимулировалась хорионическим гонадотропином.
Кломифен цитрат по 50 мг или летрозол 2,5 мг назначались по 1 таблетке с 5-го дня менструального цикла, при этом в каждом последующем месяце доза могла быть увеличена до 3 раз в день в зависимости от эффекта предыдущего месяца. Хорионический гонадотропин рекомендован в дозах от 3000 до 10 000 МЕ.
В результате проведенного лечения были достигнуты следующие показатели, представленные на рис. 2.
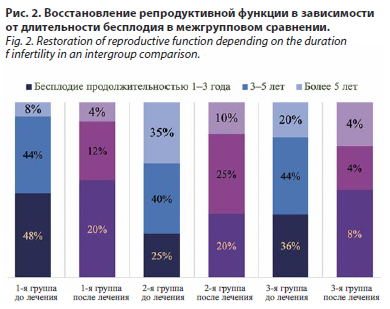 В наблюдаемых группах восстановление репродуктивной функции в зависимости от длительности бесплодия распределялось следующим образом (табл. 6): в группе А бесплодие длительностью до 1–3 лет наблюдалось у 48% женщин, после проведенного лечения беременность наступила у 20% из них; при длительности бесплодия 3–5 лет, выявленной у 44% пациенток, восстановление фертильности отмечено у 12% женщин; при бесплодии продолжительностью более 5 лет, зарегистрированном у 8% женщин, беременность наступила у 4% пациенток. В группе Б бесплодие продолжительностью 1–3 года отмечалось у 25% женщин, из них в 20% случаев наблюдалось восстановление фертильности; при бесплодии длительностью 3–5 лет, выявленном у 40% пациенток, беременность наступила у 25% женщин; при бесплодии более 5 лет, зарегистрированном у 35% пациенток, восстановление репродуктивной функции отмечено у 10% пациенток. У женщин группы B, которым проводилось исключительно лапароскопическое вмешательство, частота наступления беременности была ниже по сравнению с другими группами.
В наблюдаемых группах восстановление репродуктивной функции в зависимости от длительности бесплодия распределялось следующим образом (табл. 6): в группе А бесплодие длительностью до 1–3 лет наблюдалось у 48% женщин, после проведенного лечения беременность наступила у 20% из них; при длительности бесплодия 3–5 лет, выявленной у 44% пациенток, восстановление фертильности отмечено у 12% женщин; при бесплодии продолжительностью более 5 лет, зарегистрированном у 8% женщин, беременность наступила у 4% пациенток. В группе Б бесплодие продолжительностью 1–3 года отмечалось у 25% женщин, из них в 20% случаев наблюдалось восстановление фертильности; при бесплодии длительностью 3–5 лет, выявленном у 40% пациенток, беременность наступила у 25% женщин; при бесплодии более 5 лет, зарегистрированном у 35% пациенток, восстановление репродуктивной функции отмечено у 10% пациенток. У женщин группы B, которым проводилось исключительно лапароскопическое вмешательство, частота наступления беременности была ниже по сравнению с другими группами.
У женщин подгруппы А в течение 1 года после проведенного лечения было зарегистрировано 9 (45%) беременностей, однако лишь 3 (12%) из них завершились срочными родами, а 2 (8%) случая – преждевременными родами. У 2 (8%) женщин была выявлена неразвивающаяся беременность, еще у 2 (8%) пациенток отмечено самопроизвольное прерывание беременности на ранних сроках. Вскоре после потери беременности у 2 женщин вновь наступила беременность. У 3 пациенток, у которых роды завершились успешно, повторная беременность наступила: у одной – через 40 дней после родов, у второй – через 3,5 мес, у третьей – через 6 мес. Несмотря на короткий межродовой интервал, у 2 женщин беременность была пролонгирована. В одном случае, учитывая кесарево сечение в анамнезе и наступление беременности в течение 40 дней после родов, с целью профилактики акушерских осложнений беременность была прервана по медицинским показаниям.
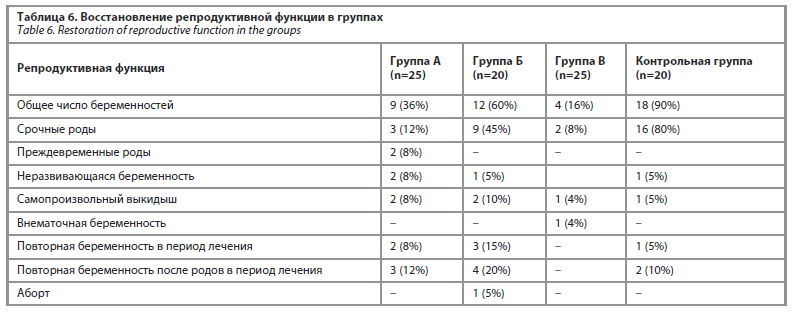
В группе Б общее число беременностей составило 12 (60%) случаев. Наиболее благоприятные исходы отмечены именно в данной группе: 9 (45%) беременностей завершились срочными родами. Неразвивающаяся беременность выявлена у 1 (5%) женщины, самопроизвольный выкидыш – у 2 (10%) пациенток. Повторная беременность в период лечения зарегистрирована у 3 (15%) женщин, а повторная беременность после родов – у 4 (20%) пациенток, что свидетельствует о высокой эффективности проведенного комплексного лечения и восстановлении репродуктивной функции.
В группе B, где применялось преимущественно хирургическое (лапароскопическое) лечение, зарегистрировано 4 (16%) беременности. Из них лишь 2 (8%) случая завершились срочными родами. У 1 (4%) женщины наблюдался самопроизвольный выкидыш, в 1 случае (4%) диагностирована внематочная беременность. Повторных беременностей в период лечения и после родов в данной группе не отмечено, что указывает на более низкие показатели восстановления фертильности по сравнению с группами А и Б.
Таким образом, наилучшие показатели восстановления репродуктивной функции отмечены в группе Б, где наблюдалась наибольшая частота наступления беременности и срочных родов. В группе А репродуктивные исходы были менее стабильными, с более высокой частотой осложненных и прервавшихся беременностей.
В группе В показатели фертильности оставались наиболее низкими, тогда как контрольная группа характеризовалась максимальной частотой благоприятных исходов беременности.
Заключение
У женщин с СПЯ эффективность хирургического лечения без предварительной коррекции эндокринной функции оказалась низкой. Выбор тактики лечения с учетом длительности бесплодия показал высокую эффективность. Комбинированный подход к лечению СПЯ, включающий консервативную терапию с последующим хирургическим вмешательством, обеспечивал более устойчивое и отдаленное восстановление фертильности по сравнению с изолированным хирургическим лечением.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Финансирование. Исследование не имело внешнего финансирования или спонсорской поддержки.
Funding. The study received no external funding or sponsorship.
Вклад авторов. Г.Д. Матризаева, Г.О. Ражабова, Г.А. Ихтиярова, А.О. Хаитов, Х.С. Икрамова – формулирование концепции исследования и разработка его дизайна; Г.Д. Матризаева, Г.О. Ражабова – сбор клинического и лабораторного материала; Г.Д. Матризаева, Г.О. Ражабова, Х.С. Икрамова – анализ и интерпретация полученных результатов; А.О. Хаитов – обзор литературы и статистическая обработка данных; Г.Д. Матризаева, Г.О. Ражабова, Г.А. Ихтиярова – написание первоначального варианта рукописи и подготовка ее окончательной редакции; Г.Д. Матризаева, Г.О. Ражабова, Г.А. Ихтиярова, А.О. Хаитов, Х.С. Икрамова – критический пересмотр рукописи с внесением существенного интеллектуального вклада. Все авторы одобрили окончательный вариант статьи перед публикацией и несут полную ответственность за все ее разделы, что подразумевает надлежащее изучение и разрешение всех вопросов, связанных с точностью и добросовестностью представленных данных.
Author contributions. G.D. Matrizaeva, G.O. Rajabova, G.A. Ikhtiyarova, A.O. Khaitov and Kh.S. Ikramova contributed to the formulation of the research concept and study design; G.D. Matrizaeva and G.O. Rajabova were responsible for the collection of clinical and laboratory data; G.D. Matrizaeva, G.O. Rajabova, Kh.S. Ikramova performed the analysis and interpretation of the obtained results; A.O. Khaitov conducted the literature review and statistical data analysis; G.D. Matrizaeva, G.O. Rajabova, and G.A. Ikhtiyarova drafted the initial version of the manuscript and prepared the final version; G.D. Matrizaeva, G.O. Rajabova, G.A. Ikhtiyarova, A.O. Khaitov and Kh.S. Ikramova critically revised the manuscript and provided substantial intellectual input. All authors approved the final version of the manuscript prior to publication and take full responsibility for all aspects of the work, ensuring the accuracy and integrity of the presented data.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Матризаева Гульнара Джуманиязовна – д-р мед. наук, доц., зав. каф. акушерства и гинекологии, онкологии, Ургенчский ГМИ. E-mail: gmatrizayeva@gmail.com ORCID: 0009-0001-2796-8041
Gulnara J. Matrizaeva – Dr. Sci. (Med.), Associate Professor, Urgench State Medical Institute.
E-mail: gmatrizayeva@gmail.com; ORCID: 0009-0001-2796-8041
Ражабова Гулзода Ойбековна – ассистент каф. акушерства и гинекологии, онкологии,
Ургенчский ГМИ. E-mail: angelina14dc@gmail.com; ORCID: 0009-0000-3422-3227
Gulzoda O. Rajabova – Assistant, Urgench State Medical Institute.
E-mail: angelina14dc@gmail.com; ORCID: 0009-0000-3422-3227
Ихтиярова Гулчехра Акмаловна – д-р мед. наук, проф., зав. каф. акушерства и гинекологии, БухГосМИ. E-mail: ixtiyarova7272@mail.ru; ORCID: 0000-0002-2398-3711
Gulchekhra A. Ikhtiyarova – Dr. Sci. (Med.), Professor, Abu Ali ibn Sino Bukhara State Medical Institute. E-mail: ixtiyarova7272@mail.ru; ORCID: 0000-0002-2398-3711
Хаитов Акбар Октамбаевич – канд. мед. наук, доц., морфолог, Ургенчский ГМИ.
E-mail: akbarshox033087@gmail.com; ORCID: 0009-0001-3051-565Х
Akbar O. Khaitov – Cand. Sci. (Med.), Associate Professor, Urgench State Medical Institute.
E-mail: akbarshox033087@gmail.com; ORCID: 0009-0001-3051-565X
Икрамова Холидажон Сахибовна – канд. мед. наук, доц. каф. акушерства и гинекологии, онкологии, Ургенчский ГМИ. E-mail: xolidajonikramova@gmail.com; ORCID: 0009-0007-1896-5205
Kholidajon S. Ikramova – Cand. Sci. (Med.), Associate Professor, Urgench State Medical Institute. E-mail: xolidajonikramova@gmail.com; ORCID: 0009-0007-1896-5205
Поступила в редакцию: 05.02.2026
Поступила после рецензирования: 09.02.2026
Принята к публикации: 12.02.2026
Received: 05.02.2026
Revised: 09.02.2026
Accepted: 12.02.2026
Клинический разбор в общей медицине №02 2026
Эффективность методов восстановления фертильности у женщин с синдромом поликистозных яичников
Номера страниц в выпуске:84-91
Аннотация
Синдром поликистозных яичников (СПЯ) является одной из ведущих причин эндокринного бесплодия. В работе оценена эффективность консервативных, хирургических и комбинированных методов лечения СПЯ.
Цель. Оценить эффективность различных методов восстановления фертильности у пациенток с СПЯ.
Материалы и методы. В проспективное исследование включены 70 женщин с бесплодием на фоне СПЯ и 20 женщин контрольной группы. Проведен анализ клинико-гормональных, метаболических и ультразвуковых показателей.
Выводы. Комбинированный подход, включающий консервативную терапию с последующим хирургическим вмешательством, обеспечивает более устойчивое восстановление репродуктивной функции.
Ключевые слова: синдром поликистозных яичников, бесплодие, фертильность, лапароскопия, стимуляция овуляции.
Для цитирования: Матризаева Г.Д., Ражабова Г.О., Ихтиярова Г.А., Хаитов А.О., Икрамова Х.С. Эффективность методов восстановления фертильности у женщин с синдромом поликистозных яичников.. Клинический разбор в общей медицине. 2026; 7 (2): 84–91. DOI: 10.47407/kr2026.7.2.00773
Синдром поликистозных яичников (СПЯ) является одной из ведущих причин эндокринного бесплодия. В работе оценена эффективность консервативных, хирургических и комбинированных методов лечения СПЯ.
Цель. Оценить эффективность различных методов восстановления фертильности у пациенток с СПЯ.
Материалы и методы. В проспективное исследование включены 70 женщин с бесплодием на фоне СПЯ и 20 женщин контрольной группы. Проведен анализ клинико-гормональных, метаболических и ультразвуковых показателей.
Выводы. Комбинированный подход, включающий консервативную терапию с последующим хирургическим вмешательством, обеспечивает более устойчивое восстановление репродуктивной функции.
Ключевые слова: синдром поликистозных яичников, бесплодие, фертильность, лапароскопия, стимуляция овуляции.
Для цитирования: Матризаева Г.Д., Ражабова Г.О., Ихтиярова Г.А., Хаитов А.О., Икрамова Х.С. Эффективность методов восстановления фертильности у женщин с синдромом поликистозных яичников.. Клинический разбор в общей медицине. 2026; 7 (2): 84–91. DOI: 10.47407/kr2026.7.2.00773
Effectiveness of fertility restoration methods in women with polycystic ovary syndrome
Gulnara D. Matrizaeva1, Gulzoda O. Rajabova1, Gulchekhra A. Ikhtiyarova2, Akbar O. Khaitov1, Holidajon S. Ikramova11 Urgench State Medical Institute, Urgench, Uzbekistan;
2 Abu Ali ibn Sino Bukhara State Medical Institute, Bukhara, Uzbekistan
gmatrizayeva@gmail.com
Abstract
Polycystic ovary syndrome (PCOS) is one of the leading causes of endocrine infertility. This study evaluated the effectiveness of conservative, surgical, and combined treatment approaches for restoring reproductive function in women with PCOS.
Aim. To evaluate the effectiveness of various fertility restoration methods in patients with PCOS.
Materials and methods. A prospective study included 70 women with PCOS-associated infertility and 20 healthy controls. Patients were divided into three subgroups based on treatment approach. Clinical, hormonal, metabolic, and ultrasound parameters were analyzed.
Conclusion. Combined conservative and surgical treatment provided more stable and long-term fertility restoration compared to isolated surgical intervention.
Keywords: polycystic ovary syndrome, infertility, fertility restoration, laparoscopy, ovulation induction.
For citation: Matrizaeva G.D., Rajabova G.O., Ikhtiyarova G.A., Khaitov A.O., Ikramova Kh.S. Effectiveness of fertility restoration methods in women with polycystic ovary syndrome. Clinical review for general practice. 2026; 7 (2): 84–91 (In Russ.). DOI: 10.47407/kr2026.7.2.00773
Введение
Синдром поликистозных яичников (СПЯ) по-прежнему остается одной из наиболее значимых и недостаточно изученных проблем гинекологической эндокринологии и репродуктивной медицины. Согласно европейским данным, распространенность СПЯ достигает около 15%. Среди пациенток с эндокринным бесплодием доля женщин с СПЯ составляет до 73% [1, 2], а в структуре бесплодных браков данная патология выявляется в 20–22% случаев, занимая 5–6-е место. Высокая актуальность проблемы обусловлена значительной распространенностью синдрома и его неблагоприятным влиянием на репродуктивную функцию.
Целесообразность применения эндоскопических методов у пациенток с подозрением на СПЯ подтверждена рядом исследований [3, 4]. Лапароскопия позволяет не только визуально оценить состояние яичников, но и выполнить их биопсию, что способствует уточнению диагноза и выбору оптимальной тактики лечения. Преимущества лапароскопического доступа по сравнению с лапаротомией включают минимальную операционную травму, высокую диагностическую информативность, снижение риска спаечного процесса в малом тазу и сокращение сроков госпитализации [5, 6].
Следует подчеркнуть, что эффективность лечения пациенток с СПЯ определяется не столько устранением морфологических изменений яичников, сколько восстановлением овуляторной функции и достижением беременности. Хирургические методы рассматриваются как вторая линия терапии при СПЯ. Несмотря на разнообразие лапароскопических вмешательств, их патогенетическая суть заключается в частичном нарушении целостности овариальной ткани, что приводит к временному снижению андрогенной активности и восстановлению эндокринных регуляторных механизмов [1].
Цель исследования – оценить эффективность различных методов восстановления фертильности у пациенток с СПЯ.
Предмет и объект исследования: обследованы 90 женщин. В проспективное исследование включены 70 женщин с бесплодием и СПЯ, контрольную группу составили 20 женщин репродуктивного возраста с регулярными овуляторными циклами.
В связи с этим женщины, включенные в основную группу, были разделены на три подгруппы в зависимости от применяемых методов лечения:
• Первая подгруппа (А) – 25 пациенток, у которых антиандрогенный эффект достигался путем применения комбинированных оральных контрацептивов (КОК) в течение не менее 3 мес, с последующей индукцией овуляции.
• Вторая подгруппа (Б) – 20 пациенток, которым после применения КОК в течение 3–6 мес было выполнено хирургическое вмешательство на яичниках лапароскопическим методом в объеме дриллинга.
• Третья подгруппа (В) – 25 пациенток, перенесших хирургическое вмешательство в объеме лапароскопического дриллинга без предварительной подготовки.
Под нашим наблюдением находились 70 пациенток с СПЯ в возрасте от 22 до 37 лет (средний возраст – 31,9±1,4 года), страдающих бесплодием продолжительностью от 1 до 10 лет (в среднем 5,3±1,2 года). Во всех случаях были исключены трубный, цервикальный, иммунологический, а также мужской факторы бесплодия.
Методы
Для обследования женщин используют общепринятые методы, включающие сбор анамнеза, жалоб, осмотр и лабораторные исследования: на 2–5-й день менструации – фолликулостимулирующий гормон (ФСГ), лютеинизирующий гормон (ЛГ), пролактин, индекс свободных андрогенов (дегидроэпиандростерон-сульфат – ДГЭА-S, тестостерон) и антимюллеров гормон, ультразвуковое трансвагинальное исследование.
Нарушение метаболизма глюкозы определялось с помощью глюкозотолерантного теста (ГТТ). Кроме того, определялась концентрация инсулина в плазме венозной крови натощак. Критериями инсулинорезистентности служили: индекс I/G (отношение базального уровня инсулина к базальному уровню глюкозы), а также индекс HOMA (Homeostasis Model Assessment): базальный уровень глюкозы (ммоль/л) × базальный уровень инсулина (мкМЕ/мл) / 22,5. Инсулинорезистентность считалась при индексе показателей HOMA>2,77.
Ультразвуковое исследование (УЗИ) для определения состояния органов малого таза проводилось на 5–7-е сутки менструального цикла на аппарате SonoScape 40 (Китай) с трансвагинальным контролем.
Одновременно оценивали морфологию яичников: количество антральных фолликулов (на 2–3-й день менструального цикла), толщину капсулы, эхогенность стромы и объем яичников. Также оценивали размеры матки и толщину эндометрия.
Принципы лечения. при бесплодии на фоне СПЯ базисная терапия проводится в два этапа:
• 1-й подготовительный этап – нормализация основных регуляций репродуктивной системы;
• 2-й этап – стимуляция овуляции.
На подготовительном этапе нормализация обмена веществ, в том числе лечение ожирения, достигается за счет гипокалорийной диеты, физической активности и препарата орлистат – блокатора желудочно-кишечной липазы, 3 капсулы по 120 мг во время или после еды (применение препарата обусловлено отсутствием инкретиновых препаратов в достаточной реальности). При гиперинсулинемии или нарушении толерантности к глюкозе – метформин по 1000 мг два раза в день после еды в течение 6 мес.
С целью нормализации менструального цикла назначались препараты КОК (этинилэстрадиол/дроспиренон 20–30 мкг/3 мг) в течение не менее 3–6 мес.
Овуляцию индуцировали по схеме цитратом кломифена или летрозолом, при необходимости использовали хорионический гонадотропин под ультразвуковым контролем.
Основную группу составила группа пациенток с СПЯ, которая была разделена на 3 подгруппы. В зависимости от этого сравнивалась эффективность консервативной терапии и хирургического лечения.
Результаты
С учетом полиморфизма причин развития СПЯ нами был проведен анализ социальных факторов риска развития заболевания у отобранных групп женщин.

При сравнительном анализе факторов образа жизни между основной и контрольной группами выявлены статистически значимые различия по частоте хронического стресса (p=0,0005) и нарушений режима питания (p=0,0011). Различия по уровню физической активности между группами статистически значимыми не были (p=0,53); табл. 1.
Следует также отметить, что у женщин, занимающихся тяжелым физическим трудом, СПЯ протекал в более выраженной форме. Это может быть связано с относительно повышенной секрецией стероидных гормонов коры надпочечников в условиях физического перенапряжения. У большинства женщин основной группы в подростковом возрасте и в течение последних 3–5 лет в анамнезе были выявлены выраженные психоэмоциональные стрессовые воздействия, сопровождавшиеся состоянием хронического стресса. Известно, что в условиях стресса усиливается секреция стероидных гормонов надпочечников, что, в свою очередь, могло способствовать вторичному развитию СПЯ.
У женщин с СПЯ отмечалось бесплодие, которое само по себе приводит к психоэмоциональной лабильности и тем самым усугубляет течение заболевания.
С точки зрения диагностики рассматриваемого заболевания особый интерес представляют клинические проявления СПЯ.
Клинические проявления СПЯ у обследованных женщин можно условно разделить на три основные группы:
1) нейропсихические изменения, включающие нарушения сна, раздражительность, быструю утомляемость и снижение либидо;
2) вегетативные нарушения, такие как нестабильное артериальное давление, отеки, потливость;
3) метаболические изменения, включая гирсутизм, акне и снижение способности к снижению массы тела.
Анализ выбранных групп женщин показал, что различия в нейропсихических нарушениях между основной и контрольной группами статистически незначимы. Так, возбудимость наблюдалась у 28,6% женщин основной группы и 25% женщин контрольной группы (χ²=0,001; p=0,975), нарушения сна – у 21,4 и 15% соответственно (χ²=0,10; p=0,751), а быстрая утомляемость отмечалась у 24,3% женщин основной группы и у 40% контрольной (χ²=1,21; p=0,271). Таким образом, нейропсихические симптомы сопоставимы между группами, однако наблюдается тенденция к большей усталости в контрольной группе.
Вегетативные нарушения были значительно более выражены у женщин основной группы. Нестабильное артериальное давление отмечалось у 64,3% пациенток основной группы по сравнению с 5% контрольной (χ²=19,57; p<0,0001). Отеки встречались у 44,3% женщин основной группы и лишь у 10% контрольной (χ²=6,47; p=0,011), а повышенная потливость наблюдалась у 37 и 5% соответственно (χ²=6,20; p=0,013). Эти результаты свидетельствуют о статистически значимом увеличении частоты вегетативных нарушений у женщин основной группы, что может быть связано с длительным стрессовым воздействием и эндокринными нарушениями.
Метаболические проявления СПЯ также были значительно выражены в основной группе. Акне регистрировалось у 82,9% женщин основной группы и только у 5% контрольной (χ²=38,38; p<0,0001), гирсутизм – у 85,7% против 20% соответственно (χ²=29,58; p<0,0001), а трудности с похудением отмечались у 51,4% пациенток основной группы и лишь у 15% контрольной (χ²=6,99; p=0,008). Эти данные подчеркивают выраженное влияние СПЯ на проявления гиперандрогенного синдрома и метаболические показатели.
Таким образом, комплексный анализ клинических проявлений показывает, что у женщин основной группы нейропсихические изменения статистически не различались с контрольной группой, однако вегетативные и метаболические нарушения были достоверно более выражены.
Известно, что индекс массы тела (ИМТ) характеризует метаболические изменения, характерные для СПЯ. В исследовании участницы основной группы (n=70) и контрольной группы (n=20) были распределены по категориям ИМТ.
У женщин основной группы нормальная масса тела (ИМТ 18,5–25) наблюдалась у 24 (34,3%) пациенток, тогда как в контрольной группе эта категория преобладала – 17 (85%) женщин. Избыточная масса тела (ИМТ 25–30) отмечалась у 21 (30%) женщины основной группы и 2 (10%) женщин контрольной группы. Первую степень ожирения (ИМТ 30–35) имели 15 (21,4%) женщин основной группы и 1 (5%) женщина контрольной. Вторую степень ожирения (ИМТ 35–40) имели 6 (8,6%) женщин основной группы, третью степень (ИМТ>40) – 4 (5,7%) женщины, в контрольной группе этих категорий не наблюдалось.
Статистический анализ показал, что различия между основной и контрольной группой были статистически значимыми для категории нормальной массы тела (χ²=14,15; p=0,00017), что указывает на значительное преобладание нормальной массы тела в контрольной группе. Различия по остальным категориям (избыточная масса тела, I–III степень ожирения) статистически значимы не были (p>0,05), хотя тенденция к большей распространенности ожирения у женщин основной группы очевидна.
Таким образом, у женщин с СПЯ наблюдается тенденция к увеличению доли избыточной массы тела и ожирения, что подчеркивает значимость контроля веса и метаболических факторов в комплексной терапии данного синдрома.
Опрос 70 пациенток с СПЯ показал, что у большинства из них с самого начала менструаций отмечались различные нарушения менструального цикла.
Нормальная менструация встречалась у 30% женщин основной группы и у всех женщин контрольной группы, различие статистически значимо (p<0,0001). Олигоменорея и аменорея значительно чаще наблюдались у женщин основной группы.

Изучение уровня глюкозы показало, что у 42 женщин основной группы отмечалось повышение ее концентрации в крови, а после проведения теста толерантности к глюкозе данный показатель увеличился до 56 пациенток и в среднем составил 6,22±0,2 ммоль/л. В группе сравнения практически у всех женщин уровень глюкозы натощак находился в пределах нормы и в среднем составлял 4,64 ммоль/л.
После проведения ГТТ существенных изменений не наблюдалось: в основной группе через 60 мин после начала нагрузки средний уровень глюкозы составил 9,54±0,3 ммоль/л, в группе сравнения – 7,81±0,3 ммоль/л (p<0,001).
Через 120 мин гипергликемия в основной группе сохранялась на уровне 7,84±0,2 ммоль/л, тогда как в группе сравнения средний показатель составил 5,4 ммоль/л (табл. 2). Остальные биохимические показатели у данных пациенток находились в пределах нормативных значений.
Как видно из представленных данных, во всех временных точках показатели перорального ГТТ в основной группе были статистически значимо выше по сравнению с контрольной группой (p<0,001), что свидетельствует о наличии выраженных нарушений углеводного обмена у пациенток основной группы.
Анализ показал, что в основной группе уровни гликированного гемоглобина (HbA1c) и инсулина были статистически значимо выше по сравнению с контрольной группой (p<0,01), что свидетельствует о выраженных нарушениях углеводного обмена. Индекс HOMA в основной группе превышал показатели контрольной группы почти в 3 раза, при этом выявленные различия носили высокодостоверный характер (p<0,001), что указывает на наличие выраженной инсулинорезистентности (табл. 3).
В дальнейшем нами были проведены гормональные исследования, результаты которых представлены в табл. 4.
Представленный анализ гормонального профиля показал наличие достоверных различий между основной и контрольной группами по ряду ключевых показателей. В частности, уровень ЛГ в основной группе был статистически значимо выше по сравнению с контрольной группой (16,4±1,3 МЕ/л против 5,1±1,2 МЕ/л; p<0,001), что указывает на выраженные нарушения гипоталамо-гипофизарной регуляции репродуктивной системы.
Концентрация пролактина у пациенток основной группы также была достоверно выше, чем в контрольной группе (499,6±22,1 мМЕ/л и 321,2±26,4 мМЕ/л соответственно; p<0,001), что свидетельствует о наличии гиперпролактинемии и ее возможном влиянии на репродуктивную функцию. Аналогичная тенденция отмечена и в отношении уровня дегидроэпиандростерон-сульфата (ДГЭА-S), который в основной группе превышал показатели контрольной группы более чем в 1,8 раза (15,22±1,7 ммоль/л против 8,03±1,4 ммоль/л; p<0,001), указывая на признаки гиперандрогении надпочечникового генеза.
Уровень тестостерона в основной группе также был статистически значимо выше по сравнению с контрольной группой (3,8±0,6 и 1,9±0,8 нмоль/л соответственно; p<0,01), что подтверждает наличие андрогенного дисбаланса у обследованных пациенток. При этом уровень антимюллерова гормона в основной группе достоверно превышал аналогичный показатель контрольной группы (4,7±0,9 нг/мл против 3,2±0,7 нг/мл; p<0,05), отражая особенности овариального резерва и функционального состояния яичников.
Согласно полученным нами данным, у пациенток с СПЯ наиболее неблагоприятным фактором является сочетание повышения уровня ЛГ, отражающего наличие инсулинорезистентности, связанной с увеличением объема яичников и способствующей их поликистозной трансформации, а также комплекса клинико-лабораторных параметров.
Полученные данные свидетельствуют о синергическом воздействии инсулина и ЛГ, что, в свою очередь, приводит к формированию поликистозных яичников.
Критерии диагностики СПЯ включают эхографические признаки УЗИ (рис. 1). Основными проявлениями заболевания являются увеличение объема яичников (свыше 10 см3), наличие гиперпластической стромы не менее 25%, наличие атретических фолликулов диаметром более 10 мм, а также уменьшение переднезаднего размера матки.
Переднезадний размер матки составил в 1-й группе 32,0–34,0 мм, во 2-й группе – от 35,0 до 42,0 мм, при этом выявлена статистически значимая разница между группами.
Анализ эхографических размеров яичников показал, что у женщин с СПЯ все параметры (длина, толщина, ширина, объем яичников, диаметр фолликулов и количество антральных фолликулов) были статистически значимо выше по сравнению с контрольной группой (p<0,05). Эти данные подтверждают наличие поликистозной трансформации яичников у пациенток основной группы.
Особенно заметно различие в объеме яичников, который в основной группе превышал таковой у контрольной группы более чем в 5 раз (37,064±3,049 см3 против 7,371±0,809 см3; p<0,05), что является ключевым ультразвуковым признаком СПЯ.
При сравнительном анализе соотношения объема яичников к объему матки у пациенток 1-й группы объем обоих яичников приближался к объему матки: в среднем 97,3%. У женщин контрольной группы объем яичников составлял 31,1%, т.е. примерно треть объема матки (p<0,05). У 68 (97,1%) пациенток 1-й группы этот показатель превышал 50%. В контрольной группе у 96% женщин с объемом яичников менее 50% от объема матки наблюдались нормальные яичники.
Было выявлено статистически значимое положительное корреляционное соотношение между объемом яичников и уровнями ЛГ и инсулина в крови (p<0,05).
УЗИ показало увеличение объема яичников у 93,22% пациенток, при этом у женщин с СПЯ отмечалось диффузное расположение фолликулов в 65,57% случаев. Этот показатель существенно не зависел от наличия или отсутствия ожирения.

В последние годы у женщин с СПЯ были выявлены высокая вероятность резистентности к индукции овуляции с использованием кломифена цитрата или летрозола, а также повышенный риск развития синдрома гиперстимуляции яичников при терапии гонадотропинами. По этой причине в последние годы возрос интерес к хирургическим методам лечения СПЯ. Кроме того, совершенствование эндоскопических техник привело к широкому распространению минимально инвазивных вмешательств.
Целью данного исследования является восстановление репродуктивного здоровья у пациенток с СПЯ посредством оптимизации консервативных и хирургических методов лечения с учетом клинических, морфологических и эндокринно-метаболических особенностей заболевания.
В нашем исследовании мы выявили различные клинические и морфологические формы СПЯ на основании ультразвуковых, эндоскопических и морфологических исследований. Для выбранных вариантов СПЯ мы изучили гормональный и метаболический гомеостаз у пациенток, уточнили показания к хирургическому лечению и провели сравнительный анализ эффективности дриллинга яичников.
Хирургическое лечение эндоскопическим методом было выполнено у 45 пациенток под спинальной анестезией с использованием аппарата фирмы «Storz».
Таким образом, основные моменты декортикации яичников включают:
• выбор места, правильное удержание и фиксацию яичника;
• сохранение фолликулярного аппарата при проведении дриллинга яичников;
• обеспечение адекватного гемостаза и тщательное промывание брюшной полости.
С учетом этих рекомендаций риск при выполнении операции был минимальным, и во время вмешательства не наблюдалось никаких осложнений. Проходимость маточных труб была проверена. После завершения хирургического вмешательства брюшная полость промывалась физиологическим раствором. Продолжительность операции в среднем составила 20–30 мин. Общая кровопотеря не превышала 50 мл. Осложнения не отмечались. Пациентки вставали с постели через 6–8 ч после операции. В дальнейшем, на 2–3-и сутки после хирургического вмешательства, пациентки выписывались из стационара в удовлетворительном состоянии.
При лапароскопическом исследовании у женщин с СПЯ выявлены характерные признаки: жемчужно-серый цвет, гладкая, блестящая, растянутая поверхность с характерным сосудистым рисунком или петлевидными сосудами, наличие субкапсулярных прозрачных кист диаметром от 0,3 до 2,0 см, плотная или равномерно утолщенная капсула.
На разрезе яичников обнаруживались мелкие прозрачные или желтоватые кисты диаметром 0,3–2,0 см (обычно от 10 до 15 кист на каждый яичник).
Яичники имели различные размеры: от слегка увеличенных (4,5×2,5×4,5 см) до значительно увеличенных (11,4×5,7×8,6 см). У 82,1% пациенток яичники были увеличены, у 17,9% – в пределах нормы (верхняя граница нормального размера яичников: 4×1,5×3 см). Одностороннее увеличение наблюдалось только у 19 пациенток, у остальных – двустороннее. У 30 (66,7%) пациенток яичники имели шаровидную форму, у 15 (31,2%) пациенток – овальную форму.
Во всех 45 наблюдениях выявлены 5 и более характерных признаков СПЯ, включая увеличение яичников, гладкую блестящую поверхность с сосудистым рисунком на мембране, растянутую поверхность и субкапсулярные кисты, а также наличие мелких кист на разрезе.
У 42 (93,3%) пациенток в заднем своде матки свободной жидкости в брюшной полости не обнаружено. Аналогичные данные на лапароскопической картине указывают на отсутствие овуляции. Следует отметить, что при различной природе нарушений менструального цикла эндоскопическая картина яичников у пациенток с СПЯ не имела различий.
После лечения были повторно обследованы гормональные показатели только у подгрупп А и Б основной группы. Причина в том, что группа В и контрольная группа не получали никакой медикаментозной терапии.
Подгруппы А и Б были повторно обследованы после шестимесячного курса лечения на уровни ЛГ, ФСГ и глюкозы в крови (табл. 5). У женщин с гиперинсулинемией уровень глюкозы в крови полностью нормализовался.
После проведенного лечения у пациенток с СПЯ показатели ЛГ и соотношение ЛГ/ФСГ изменились в зависимости от примененного метода терапии.
Подгруппа А, получавшая только КОК, показала умеренное снижение ЛГ и ЛГ/ФСГ (2,3±0,3; p<0,01), при этом уровень ФСГ изменился незначительно.
Подгруппа Б, где применялась комбинированная терапия – КОК с последующим лапароскопическим дриллингом яичников, продемонстрировала наиболее выраженную нормализацию гормонального фона. Уровень ЛГ снизился до 9,5±0,5 МЕ/л, а соотношение ЛГ/ФСГ – до 2,1±0,5 (p<0,01), что подчеркивает высокую эффективность комбинированного подхода.

В подгруппе В, где проводилось только лапароскопическое вмешательство, показатели ЛГ и ЛГ/ФСГ оставались высокими (2,6±0,2; p<0,001), что указывает на ограниченный эффект монотерапии без предварительной консервативной подготовки.
Таким образом, данные подтверждают, что комбинация КОК с лапароскопическим дриллингом (подгруппа Б) обеспечивает наиболее стабильную нормализацию гормонального баланса у пациенток с СПЯ.
Согласно результатам обследования, у пациенток подгрупп А и Б отмечалось значительное изменение уровней ЛГ и ФСГ: уровень ЛГ снизился в 2 раза, при этом уровень ФСГ достиг нормальных значений. Соотношение ЛГ/ФСГ уменьшилось до границ 1,5–1,2. Это свидетельствует о возможности перехода к следующему этапу лечения.
У пациенток 1-й группы фолликулогенез был обеспечен при помощи кломифена цитрата или летрозола, а овуляция стимулировалась хорионическим гонадотропином.
Кломифен цитрат по 50 мг или летрозол 2,5 мг назначались по 1 таблетке с 5-го дня менструального цикла, при этом в каждом последующем месяце доза могла быть увеличена до 3 раз в день в зависимости от эффекта предыдущего месяца. Хорионический гонадотропин рекомендован в дозах от 3000 до 10 000 МЕ.
В результате проведенного лечения были достигнуты следующие показатели, представленные на рис. 2.
 В наблюдаемых группах восстановление репродуктивной функции в зависимости от длительности бесплодия распределялось следующим образом (табл. 6): в группе А бесплодие длительностью до 1–3 лет наблюдалось у 48% женщин, после проведенного лечения беременность наступила у 20% из них; при длительности бесплодия 3–5 лет, выявленной у 44% пациенток, восстановление фертильности отмечено у 12% женщин; при бесплодии продолжительностью более 5 лет, зарегистрированном у 8% женщин, беременность наступила у 4% пациенток. В группе Б бесплодие продолжительностью 1–3 года отмечалось у 25% женщин, из них в 20% случаев наблюдалось восстановление фертильности; при бесплодии длительностью 3–5 лет, выявленном у 40% пациенток, беременность наступила у 25% женщин; при бесплодии более 5 лет, зарегистрированном у 35% пациенток, восстановление репродуктивной функции отмечено у 10% пациенток. У женщин группы B, которым проводилось исключительно лапароскопическое вмешательство, частота наступления беременности была ниже по сравнению с другими группами.
В наблюдаемых группах восстановление репродуктивной функции в зависимости от длительности бесплодия распределялось следующим образом (табл. 6): в группе А бесплодие длительностью до 1–3 лет наблюдалось у 48% женщин, после проведенного лечения беременность наступила у 20% из них; при длительности бесплодия 3–5 лет, выявленной у 44% пациенток, восстановление фертильности отмечено у 12% женщин; при бесплодии продолжительностью более 5 лет, зарегистрированном у 8% женщин, беременность наступила у 4% пациенток. В группе Б бесплодие продолжительностью 1–3 года отмечалось у 25% женщин, из них в 20% случаев наблюдалось восстановление фертильности; при бесплодии длительностью 3–5 лет, выявленном у 40% пациенток, беременность наступила у 25% женщин; при бесплодии более 5 лет, зарегистрированном у 35% пациенток, восстановление репродуктивной функции отмечено у 10% пациенток. У женщин группы B, которым проводилось исключительно лапароскопическое вмешательство, частота наступления беременности была ниже по сравнению с другими группами.У женщин подгруппы А в течение 1 года после проведенного лечения было зарегистрировано 9 (45%) беременностей, однако лишь 3 (12%) из них завершились срочными родами, а 2 (8%) случая – преждевременными родами. У 2 (8%) женщин была выявлена неразвивающаяся беременность, еще у 2 (8%) пациенток отмечено самопроизвольное прерывание беременности на ранних сроках. Вскоре после потери беременности у 2 женщин вновь наступила беременность. У 3 пациенток, у которых роды завершились успешно, повторная беременность наступила: у одной – через 40 дней после родов, у второй – через 3,5 мес, у третьей – через 6 мес. Несмотря на короткий межродовой интервал, у 2 женщин беременность была пролонгирована. В одном случае, учитывая кесарево сечение в анамнезе и наступление беременности в течение 40 дней после родов, с целью профилактики акушерских осложнений беременность была прервана по медицинским показаниям.

В группе Б общее число беременностей составило 12 (60%) случаев. Наиболее благоприятные исходы отмечены именно в данной группе: 9 (45%) беременностей завершились срочными родами. Неразвивающаяся беременность выявлена у 1 (5%) женщины, самопроизвольный выкидыш – у 2 (10%) пациенток. Повторная беременность в период лечения зарегистрирована у 3 (15%) женщин, а повторная беременность после родов – у 4 (20%) пациенток, что свидетельствует о высокой эффективности проведенного комплексного лечения и восстановлении репродуктивной функции.
В группе B, где применялось преимущественно хирургическое (лапароскопическое) лечение, зарегистрировано 4 (16%) беременности. Из них лишь 2 (8%) случая завершились срочными родами. У 1 (4%) женщины наблюдался самопроизвольный выкидыш, в 1 случае (4%) диагностирована внематочная беременность. Повторных беременностей в период лечения и после родов в данной группе не отмечено, что указывает на более низкие показатели восстановления фертильности по сравнению с группами А и Б.
Таким образом, наилучшие показатели восстановления репродуктивной функции отмечены в группе Б, где наблюдалась наибольшая частота наступления беременности и срочных родов. В группе А репродуктивные исходы были менее стабильными, с более высокой частотой осложненных и прервавшихся беременностей.
В группе В показатели фертильности оставались наиболее низкими, тогда как контрольная группа характеризовалась максимальной частотой благоприятных исходов беременности.
Заключение
У женщин с СПЯ эффективность хирургического лечения без предварительной коррекции эндокринной функции оказалась низкой. Выбор тактики лечения с учетом длительности бесплодия показал высокую эффективность. Комбинированный подход к лечению СПЯ, включающий консервативную терапию с последующим хирургическим вмешательством, обеспечивал более устойчивое и отдаленное восстановление фертильности по сравнению с изолированным хирургическим лечением.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Финансирование. Исследование не имело внешнего финансирования или спонсорской поддержки.
Funding. The study received no external funding or sponsorship.
Вклад авторов. Г.Д. Матризаева, Г.О. Ражабова, Г.А. Ихтиярова, А.О. Хаитов, Х.С. Икрамова – формулирование концепции исследования и разработка его дизайна; Г.Д. Матризаева, Г.О. Ражабова – сбор клинического и лабораторного материала; Г.Д. Матризаева, Г.О. Ражабова, Х.С. Икрамова – анализ и интерпретация полученных результатов; А.О. Хаитов – обзор литературы и статистическая обработка данных; Г.Д. Матризаева, Г.О. Ражабова, Г.А. Ихтиярова – написание первоначального варианта рукописи и подготовка ее окончательной редакции; Г.Д. Матризаева, Г.О. Ражабова, Г.А. Ихтиярова, А.О. Хаитов, Х.С. Икрамова – критический пересмотр рукописи с внесением существенного интеллектуального вклада. Все авторы одобрили окончательный вариант статьи перед публикацией и несут полную ответственность за все ее разделы, что подразумевает надлежащее изучение и разрешение всех вопросов, связанных с точностью и добросовестностью представленных данных.
Author contributions. G.D. Matrizaeva, G.O. Rajabova, G.A. Ikhtiyarova, A.O. Khaitov and Kh.S. Ikramova contributed to the formulation of the research concept and study design; G.D. Matrizaeva and G.O. Rajabova were responsible for the collection of clinical and laboratory data; G.D. Matrizaeva, G.O. Rajabova, Kh.S. Ikramova performed the analysis and interpretation of the obtained results; A.O. Khaitov conducted the literature review and statistical data analysis; G.D. Matrizaeva, G.O. Rajabova, and G.A. Ikhtiyarova drafted the initial version of the manuscript and prepared the final version; G.D. Matrizaeva, G.O. Rajabova, G.A. Ikhtiyarova, A.O. Khaitov and Kh.S. Ikramova critically revised the manuscript and provided substantial intellectual input. All authors approved the final version of the manuscript prior to publication and take full responsibility for all aspects of the work, ensuring the accuracy and integrity of the presented data.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Матризаева Гульнара Джуманиязовна – д-р мед. наук, доц., зав. каф. акушерства и гинекологии, онкологии, Ургенчский ГМИ. E-mail: gmatrizayeva@gmail.com ORCID: 0009-0001-2796-8041
Gulnara J. Matrizaeva – Dr. Sci. (Med.), Associate Professor, Urgench State Medical Institute.
E-mail: gmatrizayeva@gmail.com; ORCID: 0009-0001-2796-8041
Ражабова Гулзода Ойбековна – ассистент каф. акушерства и гинекологии, онкологии,
Ургенчский ГМИ. E-mail: angelina14dc@gmail.com; ORCID: 0009-0000-3422-3227
Gulzoda O. Rajabova – Assistant, Urgench State Medical Institute.
E-mail: angelina14dc@gmail.com; ORCID: 0009-0000-3422-3227
Ихтиярова Гулчехра Акмаловна – д-р мед. наук, проф., зав. каф. акушерства и гинекологии, БухГосМИ. E-mail: ixtiyarova7272@mail.ru; ORCID: 0000-0002-2398-3711
Gulchekhra A. Ikhtiyarova – Dr. Sci. (Med.), Professor, Abu Ali ibn Sino Bukhara State Medical Institute. E-mail: ixtiyarova7272@mail.ru; ORCID: 0000-0002-2398-3711
Хаитов Акбар Октамбаевич – канд. мед. наук, доц., морфолог, Ургенчский ГМИ.
E-mail: akbarshox033087@gmail.com; ORCID: 0009-0001-3051-565Х
Akbar O. Khaitov – Cand. Sci. (Med.), Associate Professor, Urgench State Medical Institute.
E-mail: akbarshox033087@gmail.com; ORCID: 0009-0001-3051-565X
Икрамова Холидажон Сахибовна – канд. мед. наук, доц. каф. акушерства и гинекологии, онкологии, Ургенчский ГМИ. E-mail: xolidajonikramova@gmail.com; ORCID: 0009-0007-1896-5205
Kholidajon S. Ikramova – Cand. Sci. (Med.), Associate Professor, Urgench State Medical Institute. E-mail: xolidajonikramova@gmail.com; ORCID: 0009-0007-1896-5205
Поступила в редакцию: 05.02.2026
Поступила после рецензирования: 09.02.2026
Принята к публикации: 12.02.2026
Received: 05.02.2026
Revised: 09.02.2026
Accepted: 12.02.2026
Список исп. литературыСкрыть список1. Иванова А.Ю., Мохорт Т.В. Синдром поликистозных яичников: обновленные рекомендации международного научно обоснованного руководства 2023 года. М., 2024.
Ivanova A.Yu., Mokhort T.V. Polycystic ovary syndrome: updated recommendations of the international scientifically based guidelines for 2023. Moscow, 2024. (in Russian).
2. Matrizayeva G.D, Ikramova X.S, Xaitov A.O. Assisment of quality of life indicators in hormonal infertility in women and determine the value of melatonin in treatment. Research journal of trauma and disability studies. 2022;01 (Issue: 10). ISSN: 2720–6866.
3. Матризаева Г.Д., Икрамова Х.С., Ражабова Г.О. Оценить кумулятивную эффективность стимуляции моноовуляции у женщин с синдромом Штейна Левенталя в различных возрастных группах. Тиббиетда янги кун. 2020;1(29):273-5.
Matrizayeva G.D., Ikramova H.S., Razhabova G.O. To evaluate the cumulative effectiveness of monoovulation stimulation in women with Stein Leventhal syndrome in various age groups. Tibbietda yangi kun. 2020;1(29):273-5 (in Russian).
4. Можейко Л.Ф., Потоцкая А.А. Синдром поликистозных яичников: современный взгляд на проблему (обзор литературы). Репродуктивное здоровье. Восточная Европа. 2022;12(3):390-403. DOI: 10.34883/PI.2022.12.3.010
Mozheyko L.F., Potocka A.A. Polycystic ovary syndrome: a modern view of the problem (literature review). Reproductive health. Eastern Europe. 2022;12(3):390-403. DOI: 10.34883/PI.2022.12.3.010 (in Russian).
5. Адамян Л.В. и др. Синдром поликистозных яичников. Клинические рекомендации. Проблемы эндокринологии. 2022;68(2):112-27.
Adamyan L.V. et al. Polycystic ovary syndrome. Clinical recommendations. Problems of endocrinology. 2022;68(2):112-27 (in Russian).
6. Соснова, Е.А., Грачева, Т.С. Результаты хирургического лечения синдрома поликистозных яичников у женщин репродуктивного возраста. Архив акушерства и гинекологии им. В Ф. Снегирева. 2023;10(2):105-111. DOI: 10.17816/2313-8726-2023-10-2-105-111
7. Рязанова Д.Э., Иванова Е.Г. Современный взгляд на патогенез синдрома поликистозных яичников (обзор литературы). Вектор научной мысли. 2023;(5):5.
Ryazanova D.E., Ivanova E.G. A modern view on the pathogenesis of polycystic ovary syndrome (literature review). The vector of scientific thought. 2023;(5):5 (in Russian).
Sosnova, E.A., Gracheva, T.S. Results of surgical treatment of polycystic ovary syndrome in women of reproductive age. Archive of Obstetrics and Gynecology named after V. F. Snegireva. 2023;10(2):105-111. DOI: 10.17816/2313-8726-2023-10-2-105-111 (in Russian).
8. Турчинец А.И. и др. Таргетная терапия синдрома поликистозных яичников. Медицинский совет. 2023;17(5):7-13.
Turchinets A.I. and others. Targeted therapy of polycystic ovary syndrome. Medical advice. 2023;17(5):7-13. (in Russian).
9. Xie J et al. The role of lncRNA HUPCOS in androgen metabolism and follicle growth arrest in polycystic ovary syndrome. Cell Biology and Toxicology. 2025;41(1):105.
