Клинический разбор в общей медицине №02 2026
Olga V. Budilovskaya, Kira V. Shalepo, Alevtina M. Savicheva, Natalia I. Tapilskaya, Igor Yu. Kogan
Ott Research Institute of Obstetrics, Gynecology and Reproductology, Saint Petersburg, Russia
tapnatalia@yandex.ru
Abstract
Background. Chronic endometritis (CE) is a factor of endometrial receptivity impairment and one of the causes of recurrent implantation failure when using assisted reproductive technologies. Persistence of genital mycoplasmas and uterine cavity dysbiosis maintain chronic inflammation, which substantiates the need for antimicrobial therapy.
Aim. To assess josamycin efficacy in patients with CE and recurrent implantation failure.
Materials and methods. A total of 106 patients diagnosed with infertility and recurrent implantation failure were included in the study. A total of 33 patients with CE confirmed by immunohistochemistry and genital mycoplasmas in the endometrium and/or vagina only were selected for the study based on the examination results. Vaginal and endometrial microbiota was assessed by real-time polymerase chain reaction (Femoflor 16), and local inflammation was assessed based on cytokine expression (ImmunoQuantex) before and 1 month after josamycin therapy (500 mg 3 times a day, 10 days).
Results. Eradication of genital mycoplasmas was achieved in 100% of cases. The decreased frequency of detecting facultative and obligate anaerobes in the uterine cavity was reported. A significant decrease in expression of interleukin-1β (p=0.0027), interleukin-18 (p=0.011), TLR4 (p=0.0489), along with the increase in the GATA3 transcription factor levels (p<0.001), was reported after treatment. The integrated assessment of the test cytokine transcript levels showed the decrease in the mean inflammation index from 86.2±18.7 to 45.2±0.6% (t=3.942, p=0.003) after the josamycin therapy course.
Conclusions. The use of josamycin ensures complete eradication of genital mycoplasmas (Ureaplasma spp., Mycoplasma hominis, Mycoplasma genitalium), it is associated with the decrease in the prevalence of opportunistic microflora persistence in the uterine cavity, as well as with the decreased local inflammation severity. This makes it possible to regard it as a promising component of comprehensive CE treatment in patients with recurrent implantation failure.
Keywords: chronic endometritis, recurrent implantation failure, infertility, genital mycoplasmas, endometrial microbiota, josamycin, antimicrobial therapy, endometrial inflammation.
For citation: Obiedkova K.V., Khalenko V.V., Krysanova A.A., Khusnutdinova T.A., Budilovskaya O.V., Shalepo K.V., Savicheva A.M., Tapilskaya N.I., Kogan I.Yu. Efficacy of antimicrobial therapy for chronic endometritis in patients with recurrent implantation failure. Clinical review for general practice. 2026; 7 (2): 92–100 (In Russ.). DOI: 10.47407/kr2026.7.2.00774
Введение
Развитие вспомогательных репродуктивных технологий позволяет под другим углом зрения рассматривать сопутствующие заболевания у пациенток с бесплодием. Повторные неудачи имплантации вскрыли проблему нарушения рецептивности эндометрия и хронического эндометрита – ХЭ [1]: при отсутствии исследований эндометрия в рутинной практике частота патологии эндометрия среди пациенток репродуктивного возраста с повторными неудачами имплантации по различным диагностическим критериям превышает 50% [2, 3].
Воспалительный характер ХЭ, где микробные агенты выступают триггером или модулятором всей палитры патогенетических нарушений ткани эндометрия, а также накопленные данные об эффективности антибиотикотерапии [4] позволяют предположить, что выявление патогена имеет решающее значение для диагностики и целенаправленной терапии в комплексном лечении патологии эндометрия [5]. В настоящее время формирование критериев сбалансированной микробиоты полости матки находится на этапе накопления научных знаний [6, 7], однако сформированные представления о патогенности тех или иных таксономических групп микроорганизмов и возможность их длительной персистенции в составе моно- или поликомпонентной биопленки определяют необходимость эрадикации инфектов из полости матки для повышения эффективности процедур вспомогательных репродуктивных технологий.
Цель исследования – оценка эффективности применения джозамицина у пациенток с ХЭ и повторными неудачами имплантации.
Первичная точка исследования – оценка элиминации микроорганизмов, в том числе генитальных микоплазм (Ureaplasma spp., и/или Mycoplasma hominis, и/или Mycoplasma genitalium) после терапии джозамицином.
Вторичные точки исследования:
• оценка микробиоты полости матки до и после терапии джозамицином;
• оценка индекса воспаления эндометрия до и после терапии джозамицином.
Материалы и методы
Общий дизайн исследования
Проведено проспективное исследование по оценке эффективности противомикробной терапии джозамицином (препарат Джозафен®, ОАО «Фармстандарт-Лексредства», Россия) в комплексном лечении ХЭ, ассоциированного с генитальными микоплазмами у пациенток с бесплодием. В исследование были включены 33 пациентки репродуктивного возраста (от 28 до 38 лет, средний возраст 33,0±0,6 года), которые были выбраны из 81 обследованной женщины с диагнозом ХЭ, у которых в полости матки были обнаружены Ureaplasma spp., и/или M. hominis, и/или M. genitalium в отделяемом полости матки и/или влагалища.
У всех включенных в исследование женщин установлен диагноз ХЭ на основании иммуногистохимического исследования. При включении в исследование на этапе скрининга, а также после проведенного исследования оценивали микробиоту влагалища и эндометрия с использованием теста Фемофлор-16 («ДНК-технология», Россия), а также индекс воспаления и локальный иммунный статус с помощью тест-системы ИммуноКвантекс («ДНК-технология», Россия).
Критерии включения в исследование:
• возраст от 20 до 38 лет на момент включения в протокол;
• диагноз бесплодия с двумя и более неудачными попытками имплантации;
• иммуногистохимически подтвержденный ХЭ;
• выявление Ureaplasma spp., и/или M. hominis, и/или M. genitalium в отделяемом полости матки и/или влагалища;
• подписанное информированное согласие на участие в исследовании.
Критерии исключения из исследования:
• наступление беременности во время проведения исследования;
• наличие любого значимого клинического события, которое способно отразиться на данных исследования;
• отзыв информированного согласия.
Отбор пациенток в исследование, назначение лечения
В исследование были выбраны пациентки среди 106 женщин с бесплодием и неудачными попытками имплантации в анамнезе. У 25 женщин диагноз ХЭ не подтвердился. Среди 81 пациентки с ХЭ в исследование были включены 33 пациентки, у которых в полости матки и/или во влагалище были обнаружены генитальные микоплазмы (Ureaplasma spp., и/или M. hominis, и/или M. genitalium). Все женщины получали противомикробную химиотерапию джозамицином (препарат Джозафен®, ОАО «Фармстандарт-Лексредства», Россия) по 500 мг 3 раза в сутки 10 дней. Джозамицин (Джозафен®) – антибиотик группы макролидов, оказывает бактериостатическое действие, обусловленное ингибированием синтеза белка бактериями. При создании в очаге воспаления высоких концентраций оказывает бактерицидное действие. Высокоактивен в отношении внутриклеточных микроорганизмов (Chlamydia trachomatis и Chlamydia pneumoniae, Mycoplasma pneumoniae, M. hominis, Ureaplasma urealyticum, Legionella pneumophila), грамположительных аэробных бактерий (Staphylococcus aureus, Streptococcus pyogenes и Streptococcus pneumoniae (pneumococcus), Corynebacterium diphtheriae); грамотрицательных аэробных бактерий (Neisseria meningitidis, Neisseria gonorrhoeae, Haemophilus influenzae, Bordetella pertussis), некоторых анаэробных бактерий (Peptococcus, Peptostreptococcus, Clostridium perfringens) [8]. Контрольное исследование с оценкой клинической и микробиологической эффективности терапии проводили через 1 мес после окончания терапии.
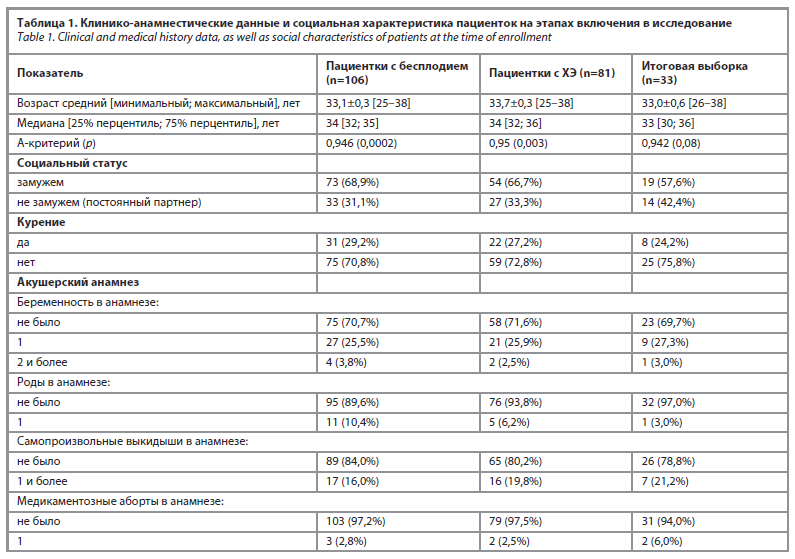
На первом этапе исследования с целью формирования итоговой выборки у всех пациенток были оценены клинико-анамнестические данные и данные иммуногистохимического обследования. Полученные данные представлены в табл. 1. В итоге сформирована группа пациенток с ХЭ и неудачами имплантации, у которых во влагалище и/или полости матки были обнаружены генитальные микоплазмы. Этим пациенткам была назначена антибактериальная терапия препаратом с торговым названием Джозафен®. В случае обнаружения облигатных анаэробов, бактерий семейства Enterobacteriaceae или дрожжеподобных грибов была дополнительно проведена этиотропная терапия.
Получение клинического материала
На 19–21-й день менструального цикла у пациенток, включенных в исследование, эндометрий получали при помощи эндобраша (Endobrash Standard For Endometrial Cytology, Laboratorie C.C.D., Франция) с предварительной обработкой шейки матки антисептиком. Отделяемое влагалища получали с боковых сводов с помощью стерильного ватного тупфера и помещали в транспортную среду с муколитиком.
Молекулярно-биологические исследования
Молекулярно-биологическое исследование микробиоты в биоптате эндометрия и отделяемом влагалища проводили с использованием мультиплексного теста на основе полимеразной цепной реакции в режиме реального времени Фемофлор-16. С помощью данного теста детектировали общую концентрацию бактериальной ДНК, соответствующую общей бактериальной массе, а также наличие следующих групп микроорганизмов: Lactobacillus spp., Enterobacteriaceae, Streptococcus spp., Staphylococcus spp., Gardnerella vaginalis, Eubacterium, Sneathia/Leptotrichia/Fusobacterium, Megasphaera/Veillonella/Dialister, Lachnobacterium spp./Clostridium, Mobiluncus spp./Corynebacterium, Peptostreptococcus, Atopobium (Fannyhessea) vaginae, а также M. hominis, Ureaplasma spp., M. genitalium и дрожжеподобных грибов рода Candida.
Оценку локальной воспалительной реакции в эндометрии проводили путем определения уровней транскриптов (матричных РНК) маркеров локального иммунного ответа: интерлейкина (ИЛ)-1β, ИЛ-10, ИЛ-18, толл-подобных рецепторов 4-го типа (TLR4), фактора транскрипции GATA3, CD68+, B2M и фактора некроза опухоли α, – с использованием диагностических наборов ИммуноКвантекс. По результатам исследования уровней транскриптов провоспалительных и противовоспалительных цитокинов проводился автоматический расчет индекса воспаления (%) с заключением о наличии локальной воспалительной реакции.
Выделение ДНК из полученного биоматериала проводили с использованием комплекта реагентов Проба-ГС («ДНК-технология», Россия), для постановки реакции амплификации нуклеиновых кислот использовали детектирующие амплификаторы DTprime («ДНК-Технология», Россия).
Статистический анализ результатов исследования
Качественные признаки представлены в виде абсолютных (количество) и относительных (удельный вес/частота, %) данных, количественные ‒ в зависимости от варианта распределения признака (по тесту Т. Андерсона и Д. Дарлинга) в виде среднего значения ± стандартное отклонение (нормальное распределение) или в виде медианы с границами 25% и 75% перцентиля (отличное от ненормального распределение). Значимость различий проверяли в зависимости от вида распределения с использованием t-теста Стьюдента или непараметрических признаков: U-критерия Манна−Уитни (для несвязанных выборок) или Т-критерия Вилкоксона (для связанных выборок) соответственно. Соотношение частот при расщеплении признаков в группах проводили с использованием критерия хи-квадрат Пирсона (χ2). Коэффициент парной конкордантности для идентифицируемого микроорганизма при его наличии/отсутствии в полости матки и во влагалище рассчитывали по формуле: K = С/(С+D), где С – число конкордантных пар, D – число дискордантных пар. Критический уровень достоверности нулевой статистической гипотезы (об отсутствии значимых различий или факторных влияний) принимали равным 0,05.
Этические правила и нормы
Исследование выполнено в полном соответствии с принципами Хельсинкской декларации Всемирной медицинской ассоциации «Этические принципы научных и медицинских исследований с участием человека», действующими порядками и стандартами оказания медицинской помощи и другими регуляторными требованиями к проведению клинических исследований и наблюдательных программ в Российской Федерации.
Результаты
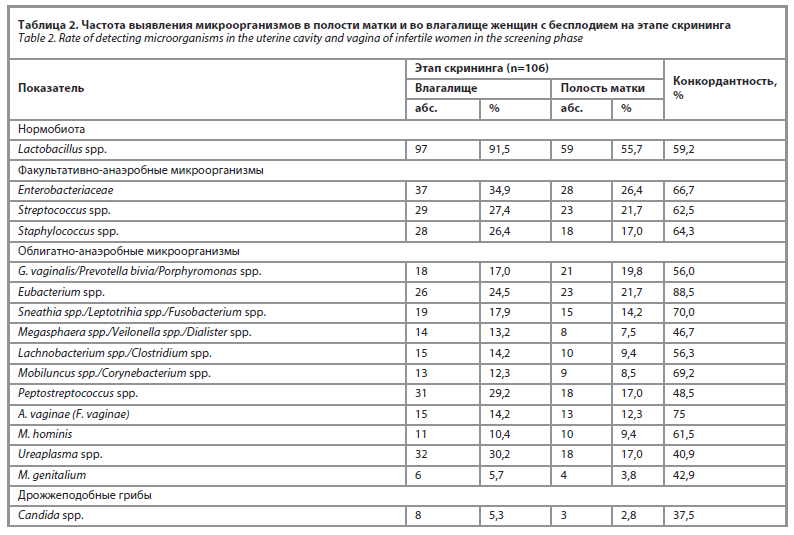
На этапе скрининга у 106 обследованных пациенток с бесплодием наиболее часто (91,5%) во влагалище обнаруживались лактобациллы (табл. 2). Кроме того, достаточно часто выявлялись бактерии семейства Enterobacteriaceae – 34,9% (n=37), Peptostreptococcus spp. – 29,2% (n=31) и Streptococcus spp. – 27,4% (n=29). В полости матки видовой состав микробиоты практически соответствовал микробиоте влагалища с конкордантностью от 40,9 до 88,5%, при этом наиболее частыми микроорганизмами были лактобациллы (55,7%). Кроме того, частота обнаружения бактерий семейства Enterobacteriaceae составила 26,4% (n=28), Eubacterium spp. – 21,7% (n=23) и Streptococcus spp. – 21,7% (n=23). Во влагалище M. hominis были выявлены в 10,4% случаев (n=11), Ureaplasma spp. – в 30,2% (n=32). В полости матки M. hominis были обнаружены в 9,4% случаев (n=10), Ureaplasma spp. – 17% (n=18). Следует отметить, что M. genitalium были выявлены во влагалище у
6 женщин, в эндометрии – у 4.
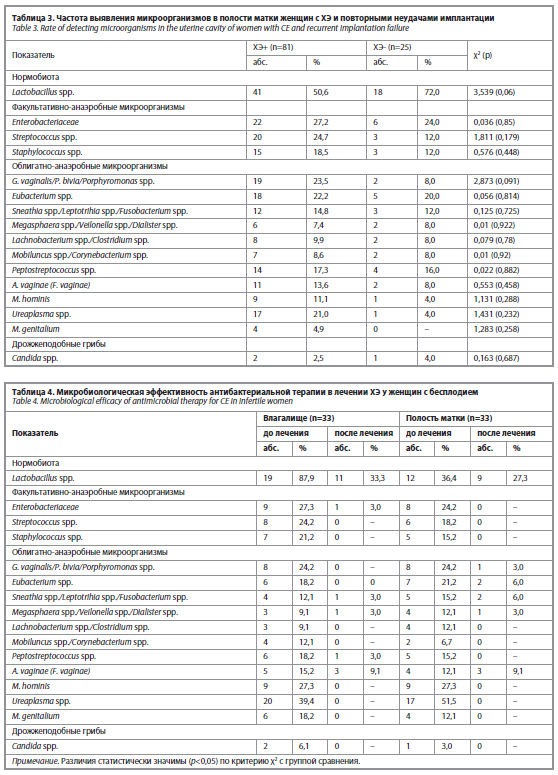
По результатам иммуногистохимического исследования у 81 (76,4%) пациентки с бесплодием диагностирован ХЭ. Статистически значимых различий по частоте идентификации отдельных микроорганизмов у пациенток с ХЭ и без воспалительных изменений в эндометрии не установлено (табл. 3), однако следует отметить, что лактобациллы у пациенток с ХЭ в полости матки обнаруживались реже по сравнению с женщинами без ХЭ – 50,6% и 72% соответственно (χ2=3,539, р=0,06). Среди женщин с ХЭ в полости матки M. hominis были выявлены в 11,1% случаев (n=9), Ureaplasma spp. – 21,0% (n=17), M. genitalium – 4,9% (n=4). Во влагалище этих женщин также были выявлены генитальные микоплазмы: M. genitalium – 7,4% (n=6), M. hominis – 12,4% (n=10), Ureaplasma spp. – 18,5% (n=15), у двух женщин одновременно выявлялись M. hominis и Ureaplasma spp. (2,5%).
Лечение джозамицином получали 33 пациентки с бесплодием, которые по результатам исследования имели иммуногистохимически подтвержденный ХЭ и у которых были обнаружены генитальные микоплазмы (Ureaplasma spp., и/или M. hominis, и/или M. genitalium). У всех этих женщин было две и более неудачных попытки переноса эмбриона. Следует отметить, что у двух женщин во влагалище обнаруживались одновременно уреаплазмы и M. hominis. Микробиологическую эффективность джозамицина оценивали по эрадикации генитальных микоплазм (Ureaplasma spp., и/или M. hominis, и/или M. genitalium), которая составила 100% (табл. 4).
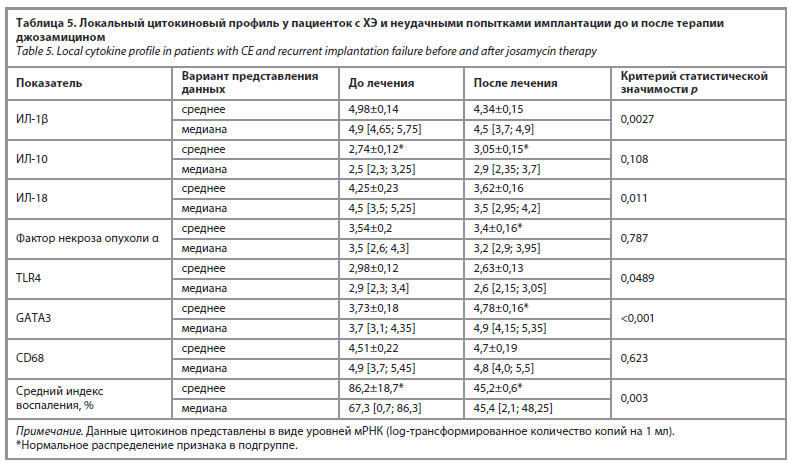
Важным этапом исследования была оценка локального цитокинового профиля и индекса воспаления. Эти данные представлены в табл. 5.
Как видно из табл. 5, по результатам оценки локального цитокинового профиля в ткани эндометрия посредством определения мРНК про- и противовоспалительных цитокинов после лечения отмечалось статистически значимое снижение уровня транскриптов ИЛ-1β, ИЛ-18 и TLR4 при одновременном повышении уровня фактора транскрипции GATA3. При интегральной оценке уровня транскриптов исследуемых цитокинов было установлено снижение среднего индекса воспаления с 86,2±18,7 до 45,2±0,6% (t=3,942, p=0,003) после лечения курсом джозамицина.
Таким образом, лечение ХЭ у женщин с неудачными попытками имплантации – очень сложная задача. Проведение антибактериальной терапии у таких пациенток является обязательным условием. При этом имеет значение этиологический фактор ХЭ, который устанавливается по результатам молекулярно-биологического исследования. В случае выявления генитальных микоплазм мы наблюдали хороший эффект джозамицина (Джозафен®). В случае обнаружения облигатных анаэробов, бактерий семейства Enterobacteriaceae и/или дрожжеподобных грибов необходимо проведение соответствующей этиотропной терапии.
Обсуждение
Несмотря на то что персистирующие в урогенитальном тракте микоплазмы/уреаплазмы нечасто дают клинические проявления, эпидемиологические данные демонстрируют, что их наличие ассоциировано с широким спектром негативных гинекологических, акушерских и репродуктивных исходов [9–11].
При этом ставшая глобальной проблема противомикробной резистентности не обошла стороной и генитальные микоплазмы. По данным проспективного когортного исследования (Афины, Греция), выполненного с 2005 по 2019 г. с включением 8336 небеременных пациенток с симптомами вагинита в возрасте от 18 до 46 лет, количество положительных изолятов на наличие U. urealyticum и/или M. hominis составило 25,1% (n=2093). При этом наиболее высокая эффективность эрадикации внутриклеточных агентов имела место у доксициклина (97,6%), пристинамицина (97,6%) и джозамицина (95,1%), в то время как для офлоксацина, ципрофлоксацина и азитромицина микробиологическая эффективность составила 73,2%, 20,7 и 21,6% соответственно.
По данным выполненного в КНР (Ханчжоу, провинция Чжэцзян) проспективного исследования с включением 5577 пациенток, обследованных в период с 2018 по 2024 г., превалентность U. urealyticum среди обращавшихся за амбулаторной медицинской помощью с наличием клинических проявлений и для профилактического осмотра составила 49,11%. При этом некоторые макролиды продемонстрировали высокую микробиологическую эффективность в отношении данных микроорганизмов: 95,5% для джозамицина и 87,0% для кларитромицина, – в то время как для азитромицина микробиологическая эффективность составила всего 50,5% [12].
Итальянское проспективное исследование, выполненное с 2017 по 2021 г. с включением 21 210 человек, проживающих в двух коммунах (Болонья и Лекко), продемонстрировало, что частота обнаружения генитальных микоплазм в урогенитальном тракте составила 22,3%, при этом Ureaplasma spp. были идентифицированы в 62,3% случаев, M. hominis – в 8,3%, оба микроорганизма – в 29,4%. Ureaplasma spp. в 39,5% случаев были резистентны к ципрофлоксацину, M. hominis – в 60% случаев резистентны к азитромицину и рокситромицину. Резистентность менее 7% отмечалась только у двух препаратов: миноциклина и джозамицина, которые авторами исследования были рекомендованы в качестве препаратов 1-й линии эмпирической терапии [13].
В нашем исследовании на относительно небольшой выборке пациенток получена 100% микробиологическая эффективность джозамицина в отношении генитальных микоплазм (Ureaplasma spp., M. hominis и M. genitalium), обнаруженных как в отделяемом из влагалища, так и в эндометрии.
В исследовании E. Cicinelli и соавт. [14] выбор антибактериальных препаратов определялся в соответствии с бактериологическим профилем эндометрия. При наличии грамотрицательных и грамположительных бактерий применялись ципрофлоксацин (1000 мг в день в течение 10 дней) и амоксициллин с клавулановой кислотой (2 г в день в течение 8 дней) соответственно. Пациенткам, у которых выявлены Mycoplasma spp. или Ureaplasma spp., назначали джозамицин (2 г в день в течение 12 дней). Если после проведенного лечения по результатам биопсии эндометрия определялись плазматические клетки, то назначался повторный курс антибиотиков. В итоге в 76% случаев гистологическая картина была в норме, что свидетельствовало об эффективности терапии антибиотиками.
Следует отметить, что одним из преимуществ джозамицина является низкий профиль его лекарственной токсичности. Так, по данным фармакоэпидемиологического исследования с использованием базы данных фармаконадзора Всемирной организации здравоохранения в период с 1968 по 2023 г., среди наиболее часто назначаемых макролидов джозамицин обладает самым низким профилем токсичности [15].
Одним из преимуществ макролидов является системное противовоспалительное действие, которое имеет большое значение при лечении ХЭ. В нашем исследовании отмечалось снижение индекса воспаления в эндометриальной ткани в течение месяца после курса терапии джозамицином. Исследования на культурах клеток демонстрируют, что джозамицин ингибирует снижение уровня CD34 и повышение ИЛ-6, ИЛ-11 и BMP6, что обеспечивает противовоспалительный эффект и предотвращение прогрессирования фибротических изменений в функциональных тканях [16]. Клинические исследования демонстрируют эффективность макролидов как антифибротического средства при легочном фиброзе, при этом молекулярные механизмы действия заключаются в ингибировании сигнальных путей TGF-β/Smad и JNK/c-Jun. Кроме того, макролиды таргетно ингибируют высвобождение профибротических цитокинов, модуляцию поляризации макрофагов в сторону антифибротических фенотипов M2 и индукцию апоптоза в стареющих клетках [17]. Данные свойства макролида джозамицина могут сделать его препаратом выбора при лечении ХЭ в сочетании с синдромом тонкого эндометрия, где преобладают фибротические изменения функциональной ткани.
Заключение
При неудачах имплантации и наличии ХЭ необходимо назначение антибактериальных препаратов. Противомикробная терапия, направленная на элиминацию генитальных микоплазм (Ureaplasma spp., M. hominis и M. genitalium) у пациенток с ХЭ и неудачными попытками имплантации, приводит к 100% эрадикации исследуемых агентов. При этом отмечаются снижение превалентности других условно-патогенных микроорганизмов, персистирующих в полости матки, и уменьшение выраженности индекса воспаления, определяемого на основании интегральной оценки транскриптов про- и противовоспалительных цитокинов в эндометриальной ткани.
Финансирование. Работа выполнена в рамках ФНИ «Универсальные и специфические механизмы реализации и нарушений репродуктивной функции в семье» (рег. №1024032800230-9-3.2.2, рук. И.Ю. Коган).
Funding. The work was carried out within the framework of the Fundamental Scientific Research project "Universal and specific mechanisms of realization and disorders of reproductive function in the family" (reg. no. 1024032800230-9-3.2.2, Principal Investigator: I.Yu. Kogan).
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Объедкова Ксения Владимировна – канд. мед. наук, ст. науч. сотр. отд. репродуктологии ФГБНУ «НИИ АГиР им. Д.О. Отта». ORCID: 0000-0002-2056-7907
Ksenia V. Obiedkova – Cand. Sci. (Med.), Senior Researcher, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0002-2056-7907
Халенко Владислава Валерьевна – мл. науч. сотр. отд. репродуктологии ФГБНУ «НИИ АГиР им. Д.О. Отта». ORCID: 0000-0001-5313-2259
Vladislava V. Khalenko – Junior Researcher, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0001-5313-2259
Крысанова Анна Александровна – канд. мед. наук, ст. науч. сотр. группы экспериментальной микробиологии ФГБНУ «НИИ АГиР им. Д.О. Отта». ORCID: 0000-0003-4798-1881
Anna A. Krysanova – Cand. Sci. (Med.), Senior Researcher, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0003-4798-1881
Хуснутдинова Татьяна Алексеевна – канд. мед. наук, ст. науч. сотр. группы экспериментальной микробиологии ФГБНУ «НИИ АГиР им. Д.О. Отта». ORCID: 0000-0002-2742-2655
Tatiana A. Khusnutdinova – Cand. Sci. (Med.), Senior Researcher, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0002-2742-2655
Будиловская Ольга Викторовна – канд. мед. наук, ст. науч. сотр. группы экспериментальной микробиологии ФГБНУ «НИИ АГиР им. Д.О. Отта». ORCID: 0000-0001-7673-6274
Olga V. Budilovskaya – Cand. Sci. (Med.), Senior Researcher, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0001-7673-6274
Шалепо Кира Валентиновна – канд. биол. наук, ст. науч. сотр. группы экспериментальной микробиологии ФГБНУ «НИИ АГиР им. Д.О. Отта». ORCID: 0000-0002-3002-3874
Kira V. Shalepo – Cand. Sci. (Biol.), Senior Researcher, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0002-3002-3874
Савичева Алевтина Михайловна – д-р мед. наук, проф., зав. отд. медицинской микробиологии ФГБНУ «НИИ АГиР им. Д.О. Отта», засл. деят. науки РФ. ORCID: 0000-0003-3870-5930
Alevtina M. Savicheva – Dr. Sci. (Med.), Professor, Head of the Department, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0003-3870-5930
Тапильская Наталья Игоревна – д-р мед. наук, проф., вед. науч. сотр. отд. репродукции ФГБНУ «НИИ АГиР им. Д.О. Отта». E-mail: tapnatalia@yandex.ru; ORCID: 0000-0001-5309-0087
Natalia I. Tapilskaya – Dr. Sci. (Med.), Professor, Leading Researcher, Ott Research Institute of Obstetrics, Gynecology and Reproductology. E-mail: tapnatalia@yandex.ru;
ORCID: 0000-0001-5309-0087
Коган Игорь Юрьевич – чл.-кор. РАН, д-р мед. наук, проф., дир. ФГБНУ «НИИ АГиР им.
Д.О. Отта». ORCID: 0000-0002-7351-6900
Igor Yu. Kogan – Corr. Memb. RAS, Dr. Sci. (Med.), Professor, Director, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0002-7351-6900
Поступила в редакцию: 06.02.2026
Поступила после рецензирования: 10.02.2026
Принята к публикации: 12.02.2026
Received: 06.02.2026
Revised: 10.02.2026
Accepted: 12.02.2026
Клинический разбор в общей медицине №02 2026
Эффективность противомикробной терапии хронического эндометрита у пациенток с повторными неудачами имплантации
Номера страниц в выпуске:92-100
Аннотация
Актуальность. Хронический эндометрит (ХЭ) является фактором нарушения рецептивности эндометрия и одной из причин повторных неудач имплантации при применении вспомогательных репродуктивных технологий. Персистенция генитальных микоплазм и дисбиотические изменения микробиоты полости матки поддерживают хроническое воспаление, что обосновывает необходимость антибактериальной терапии.
Цель. Оценка эффективности применения джозамицина у пациенток с ХЭ и повторными неудачами имплантации.
Материалы и методы. В исследование включены 106 пациенток с диагнозом «бесплодие» и повторными неудачами имплантации. По результатам обследования с целью оценки эффективности терапии были отобраны 33 пациентки только с иммуногистохимически подтвержденным ХЭ и наличием генитальных микоплазм в эндометрии и/или влагалище. Проводили оценку микробиоты влагалища и эндометрия методом полимеразной цепной реакции в реальном времени (Фемофлор-16), а также локального воспалительного ответа по экспрессии цитокинов (ИммуноКвантекс) до и через 1 мес после терапии джозамицином (500 мг 3 раза в сутки, 10 дней).
Результаты. Эрадикация генитальных микоплазм достигнута в 100% случаев. Отмечено снижение частоты выявления факультативных и облигатных анаэробов в полости матки. После лечения выявлено достоверное уменьшение экспрессии интерлейкина-1β (p=0,0027), интерлейкина-18 (p=0,011), TLR4 (p=0,0489) при одновременном повышении уровня фактора транскрипции GATA3 (p<0,001). При интегральной оценке уровня транскриптов исследуемых цитокинов было установлено снижение среднего индекса воспаления с 86,2±18,7 до 45,2±0,6% (t=3,942, p=0,003) после лечения курсом джозамицина.
Выводы. Применение джозамицина обеспечивает полную эрадикацию генитальных микоплазм (Ureaplasma spp., Mycoplasma hominis, Mycoplasma genitalium), сопровождается снижением превалентности условно-патогенной микрофлоры, персистирующей в полости матки, и уменьшением выраженности локального воспалительного ответа, что позволяет рассматривать его как перспективный компонент комплексной терапии ХЭ у пациенток с повторными неудачами имплантации.
Ключевые слова: хронический эндометрит, повторные неудачи имплантации, бесплодие, генитальные микоплазмы, микробиота эндометрия, джозамицин, антибактериальная терапия, воспаление эндометрия.
Для цитирования: Объедкова К.В., Халенко В.В., Крысанова А.А., Хуснутдинова Т.А., Будиловская О.В., Шалепо К.В., Савичева А.М., Тапильская Н.И., Коган И.Ю. Эффективность противомикробной терапии хронического эндометрита у пациенток с повторными неудачами имплантации. Клинический разбор в общей медицине. 2026; 7 (2): 92–100. DOI: 10.47407/kr2026.7.2.00774
Актуальность. Хронический эндометрит (ХЭ) является фактором нарушения рецептивности эндометрия и одной из причин повторных неудач имплантации при применении вспомогательных репродуктивных технологий. Персистенция генитальных микоплазм и дисбиотические изменения микробиоты полости матки поддерживают хроническое воспаление, что обосновывает необходимость антибактериальной терапии.
Цель. Оценка эффективности применения джозамицина у пациенток с ХЭ и повторными неудачами имплантации.
Материалы и методы. В исследование включены 106 пациенток с диагнозом «бесплодие» и повторными неудачами имплантации. По результатам обследования с целью оценки эффективности терапии были отобраны 33 пациентки только с иммуногистохимически подтвержденным ХЭ и наличием генитальных микоплазм в эндометрии и/или влагалище. Проводили оценку микробиоты влагалища и эндометрия методом полимеразной цепной реакции в реальном времени (Фемофлор-16), а также локального воспалительного ответа по экспрессии цитокинов (ИммуноКвантекс) до и через 1 мес после терапии джозамицином (500 мг 3 раза в сутки, 10 дней).
Результаты. Эрадикация генитальных микоплазм достигнута в 100% случаев. Отмечено снижение частоты выявления факультативных и облигатных анаэробов в полости матки. После лечения выявлено достоверное уменьшение экспрессии интерлейкина-1β (p=0,0027), интерлейкина-18 (p=0,011), TLR4 (p=0,0489) при одновременном повышении уровня фактора транскрипции GATA3 (p<0,001). При интегральной оценке уровня транскриптов исследуемых цитокинов было установлено снижение среднего индекса воспаления с 86,2±18,7 до 45,2±0,6% (t=3,942, p=0,003) после лечения курсом джозамицина.
Выводы. Применение джозамицина обеспечивает полную эрадикацию генитальных микоплазм (Ureaplasma spp., Mycoplasma hominis, Mycoplasma genitalium), сопровождается снижением превалентности условно-патогенной микрофлоры, персистирующей в полости матки, и уменьшением выраженности локального воспалительного ответа, что позволяет рассматривать его как перспективный компонент комплексной терапии ХЭ у пациенток с повторными неудачами имплантации.
Ключевые слова: хронический эндометрит, повторные неудачи имплантации, бесплодие, генитальные микоплазмы, микробиота эндометрия, джозамицин, антибактериальная терапия, воспаление эндометрия.
Для цитирования: Объедкова К.В., Халенко В.В., Крысанова А.А., Хуснутдинова Т.А., Будиловская О.В., Шалепо К.В., Савичева А.М., Тапильская Н.И., Коган И.Ю. Эффективность противомикробной терапии хронического эндометрита у пациенток с повторными неудачами имплантации. Клинический разбор в общей медицине. 2026; 7 (2): 92–100. DOI: 10.47407/kr2026.7.2.00774
Efficacy of antimicrobial therapy for chronic endometritis in patients with recurrent implantation failure
Ksenia V. Obiedkova, Vladislava V. Khalenko, Anna A. Krysanova, Tatiana A. Khusnutdinova,Olga V. Budilovskaya, Kira V. Shalepo, Alevtina M. Savicheva, Natalia I. Tapilskaya, Igor Yu. Kogan
Ott Research Institute of Obstetrics, Gynecology and Reproductology, Saint Petersburg, Russia
tapnatalia@yandex.ru
Abstract
Background. Chronic endometritis (CE) is a factor of endometrial receptivity impairment and one of the causes of recurrent implantation failure when using assisted reproductive technologies. Persistence of genital mycoplasmas and uterine cavity dysbiosis maintain chronic inflammation, which substantiates the need for antimicrobial therapy.
Aim. To assess josamycin efficacy in patients with CE and recurrent implantation failure.
Materials and methods. A total of 106 patients diagnosed with infertility and recurrent implantation failure were included in the study. A total of 33 patients with CE confirmed by immunohistochemistry and genital mycoplasmas in the endometrium and/or vagina only were selected for the study based on the examination results. Vaginal and endometrial microbiota was assessed by real-time polymerase chain reaction (Femoflor 16), and local inflammation was assessed based on cytokine expression (ImmunoQuantex) before and 1 month after josamycin therapy (500 mg 3 times a day, 10 days).
Results. Eradication of genital mycoplasmas was achieved in 100% of cases. The decreased frequency of detecting facultative and obligate anaerobes in the uterine cavity was reported. A significant decrease in expression of interleukin-1β (p=0.0027), interleukin-18 (p=0.011), TLR4 (p=0.0489), along with the increase in the GATA3 transcription factor levels (p<0.001), was reported after treatment. The integrated assessment of the test cytokine transcript levels showed the decrease in the mean inflammation index from 86.2±18.7 to 45.2±0.6% (t=3.942, p=0.003) after the josamycin therapy course.
Conclusions. The use of josamycin ensures complete eradication of genital mycoplasmas (Ureaplasma spp., Mycoplasma hominis, Mycoplasma genitalium), it is associated with the decrease in the prevalence of opportunistic microflora persistence in the uterine cavity, as well as with the decreased local inflammation severity. This makes it possible to regard it as a promising component of comprehensive CE treatment in patients with recurrent implantation failure.
Keywords: chronic endometritis, recurrent implantation failure, infertility, genital mycoplasmas, endometrial microbiota, josamycin, antimicrobial therapy, endometrial inflammation.
For citation: Obiedkova K.V., Khalenko V.V., Krysanova A.A., Khusnutdinova T.A., Budilovskaya O.V., Shalepo K.V., Savicheva A.M., Tapilskaya N.I., Kogan I.Yu. Efficacy of antimicrobial therapy for chronic endometritis in patients with recurrent implantation failure. Clinical review for general practice. 2026; 7 (2): 92–100 (In Russ.). DOI: 10.47407/kr2026.7.2.00774
Введение
Развитие вспомогательных репродуктивных технологий позволяет под другим углом зрения рассматривать сопутствующие заболевания у пациенток с бесплодием. Повторные неудачи имплантации вскрыли проблему нарушения рецептивности эндометрия и хронического эндометрита – ХЭ [1]: при отсутствии исследований эндометрия в рутинной практике частота патологии эндометрия среди пациенток репродуктивного возраста с повторными неудачами имплантации по различным диагностическим критериям превышает 50% [2, 3].
Воспалительный характер ХЭ, где микробные агенты выступают триггером или модулятором всей палитры патогенетических нарушений ткани эндометрия, а также накопленные данные об эффективности антибиотикотерапии [4] позволяют предположить, что выявление патогена имеет решающее значение для диагностики и целенаправленной терапии в комплексном лечении патологии эндометрия [5]. В настоящее время формирование критериев сбалансированной микробиоты полости матки находится на этапе накопления научных знаний [6, 7], однако сформированные представления о патогенности тех или иных таксономических групп микроорганизмов и возможность их длительной персистенции в составе моно- или поликомпонентной биопленки определяют необходимость эрадикации инфектов из полости матки для повышения эффективности процедур вспомогательных репродуктивных технологий.
Цель исследования – оценка эффективности применения джозамицина у пациенток с ХЭ и повторными неудачами имплантации.
Первичная точка исследования – оценка элиминации микроорганизмов, в том числе генитальных микоплазм (Ureaplasma spp., и/или Mycoplasma hominis, и/или Mycoplasma genitalium) после терапии джозамицином.
Вторичные точки исследования:
• оценка микробиоты полости матки до и после терапии джозамицином;
• оценка индекса воспаления эндометрия до и после терапии джозамицином.
Материалы и методы
Общий дизайн исследования
Проведено проспективное исследование по оценке эффективности противомикробной терапии джозамицином (препарат Джозафен®, ОАО «Фармстандарт-Лексредства», Россия) в комплексном лечении ХЭ, ассоциированного с генитальными микоплазмами у пациенток с бесплодием. В исследование были включены 33 пациентки репродуктивного возраста (от 28 до 38 лет, средний возраст 33,0±0,6 года), которые были выбраны из 81 обследованной женщины с диагнозом ХЭ, у которых в полости матки были обнаружены Ureaplasma spp., и/или M. hominis, и/или M. genitalium в отделяемом полости матки и/или влагалища.
У всех включенных в исследование женщин установлен диагноз ХЭ на основании иммуногистохимического исследования. При включении в исследование на этапе скрининга, а также после проведенного исследования оценивали микробиоту влагалища и эндометрия с использованием теста Фемофлор-16 («ДНК-технология», Россия), а также индекс воспаления и локальный иммунный статус с помощью тест-системы ИммуноКвантекс («ДНК-технология», Россия).
Критерии включения в исследование:
• возраст от 20 до 38 лет на момент включения в протокол;
• диагноз бесплодия с двумя и более неудачными попытками имплантации;
• иммуногистохимически подтвержденный ХЭ;
• выявление Ureaplasma spp., и/или M. hominis, и/или M. genitalium в отделяемом полости матки и/или влагалища;
• подписанное информированное согласие на участие в исследовании.
Критерии исключения из исследования:
• наступление беременности во время проведения исследования;
• наличие любого значимого клинического события, которое способно отразиться на данных исследования;
• отзыв информированного согласия.

Отбор пациенток в исследование, назначение лечения
В исследование были выбраны пациентки среди 106 женщин с бесплодием и неудачными попытками имплантации в анамнезе. У 25 женщин диагноз ХЭ не подтвердился. Среди 81 пациентки с ХЭ в исследование были включены 33 пациентки, у которых в полости матки и/или во влагалище были обнаружены генитальные микоплазмы (Ureaplasma spp., и/или M. hominis, и/или M. genitalium). Все женщины получали противомикробную химиотерапию джозамицином (препарат Джозафен®, ОАО «Фармстандарт-Лексредства», Россия) по 500 мг 3 раза в сутки 10 дней. Джозамицин (Джозафен®) – антибиотик группы макролидов, оказывает бактериостатическое действие, обусловленное ингибированием синтеза белка бактериями. При создании в очаге воспаления высоких концентраций оказывает бактерицидное действие. Высокоактивен в отношении внутриклеточных микроорганизмов (Chlamydia trachomatis и Chlamydia pneumoniae, Mycoplasma pneumoniae, M. hominis, Ureaplasma urealyticum, Legionella pneumophila), грамположительных аэробных бактерий (Staphylococcus aureus, Streptococcus pyogenes и Streptococcus pneumoniae (pneumococcus), Corynebacterium diphtheriae); грамотрицательных аэробных бактерий (Neisseria meningitidis, Neisseria gonorrhoeae, Haemophilus influenzae, Bordetella pertussis), некоторых анаэробных бактерий (Peptococcus, Peptostreptococcus, Clostridium perfringens) [8]. Контрольное исследование с оценкой клинической и микробиологической эффективности терапии проводили через 1 мес после окончания терапии.
На первом этапе исследования с целью формирования итоговой выборки у всех пациенток были оценены клинико-анамнестические данные и данные иммуногистохимического обследования. Полученные данные представлены в табл. 1. В итоге сформирована группа пациенток с ХЭ и неудачами имплантации, у которых во влагалище и/или полости матки были обнаружены генитальные микоплазмы. Этим пациенткам была назначена антибактериальная терапия препаратом с торговым названием Джозафен®. В случае обнаружения облигатных анаэробов, бактерий семейства Enterobacteriaceae или дрожжеподобных грибов была дополнительно проведена этиотропная терапия.
Получение клинического материала
На 19–21-й день менструального цикла у пациенток, включенных в исследование, эндометрий получали при помощи эндобраша (Endobrash Standard For Endometrial Cytology, Laboratorie C.C.D., Франция) с предварительной обработкой шейки матки антисептиком. Отделяемое влагалища получали с боковых сводов с помощью стерильного ватного тупфера и помещали в транспортную среду с муколитиком.
Молекулярно-биологические исследования
Молекулярно-биологическое исследование микробиоты в биоптате эндометрия и отделяемом влагалища проводили с использованием мультиплексного теста на основе полимеразной цепной реакции в режиме реального времени Фемофлор-16. С помощью данного теста детектировали общую концентрацию бактериальной ДНК, соответствующую общей бактериальной массе, а также наличие следующих групп микроорганизмов: Lactobacillus spp., Enterobacteriaceae, Streptococcus spp., Staphylococcus spp., Gardnerella vaginalis, Eubacterium, Sneathia/Leptotrichia/Fusobacterium, Megasphaera/Veillonella/Dialister, Lachnobacterium spp./Clostridium, Mobiluncus spp./Corynebacterium, Peptostreptococcus, Atopobium (Fannyhessea) vaginae, а также M. hominis, Ureaplasma spp., M. genitalium и дрожжеподобных грибов рода Candida.

Оценку локальной воспалительной реакции в эндометрии проводили путем определения уровней транскриптов (матричных РНК) маркеров локального иммунного ответа: интерлейкина (ИЛ)-1β, ИЛ-10, ИЛ-18, толл-подобных рецепторов 4-го типа (TLR4), фактора транскрипции GATA3, CD68+, B2M и фактора некроза опухоли α, – с использованием диагностических наборов ИммуноКвантекс. По результатам исследования уровней транскриптов провоспалительных и противовоспалительных цитокинов проводился автоматический расчет индекса воспаления (%) с заключением о наличии локальной воспалительной реакции.
Выделение ДНК из полученного биоматериала проводили с использованием комплекта реагентов Проба-ГС («ДНК-технология», Россия), для постановки реакции амплификации нуклеиновых кислот использовали детектирующие амплификаторы DTprime («ДНК-Технология», Россия).
Статистический анализ результатов исследования
Качественные признаки представлены в виде абсолютных (количество) и относительных (удельный вес/частота, %) данных, количественные ‒ в зависимости от варианта распределения признака (по тесту Т. Андерсона и Д. Дарлинга) в виде среднего значения ± стандартное отклонение (нормальное распределение) или в виде медианы с границами 25% и 75% перцентиля (отличное от ненормального распределение). Значимость различий проверяли в зависимости от вида распределения с использованием t-теста Стьюдента или непараметрических признаков: U-критерия Манна−Уитни (для несвязанных выборок) или Т-критерия Вилкоксона (для связанных выборок) соответственно. Соотношение частот при расщеплении признаков в группах проводили с использованием критерия хи-квадрат Пирсона (χ2). Коэффициент парной конкордантности для идентифицируемого микроорганизма при его наличии/отсутствии в полости матки и во влагалище рассчитывали по формуле: K = С/(С+D), где С – число конкордантных пар, D – число дискордантных пар. Критический уровень достоверности нулевой статистической гипотезы (об отсутствии значимых различий или факторных влияний) принимали равным 0,05.
Этические правила и нормы
Исследование выполнено в полном соответствии с принципами Хельсинкской декларации Всемирной медицинской ассоциации «Этические принципы научных и медицинских исследований с участием человека», действующими порядками и стандартами оказания медицинской помощи и другими регуляторными требованиями к проведению клинических исследований и наблюдательных программ в Российской Федерации.

Результаты
На этапе скрининга у 106 обследованных пациенток с бесплодием наиболее часто (91,5%) во влагалище обнаруживались лактобациллы (табл. 2). Кроме того, достаточно часто выявлялись бактерии семейства Enterobacteriaceae – 34,9% (n=37), Peptostreptococcus spp. – 29,2% (n=31) и Streptococcus spp. – 27,4% (n=29). В полости матки видовой состав микробиоты практически соответствовал микробиоте влагалища с конкордантностью от 40,9 до 88,5%, при этом наиболее частыми микроорганизмами были лактобациллы (55,7%). Кроме того, частота обнаружения бактерий семейства Enterobacteriaceae составила 26,4% (n=28), Eubacterium spp. – 21,7% (n=23) и Streptococcus spp. – 21,7% (n=23). Во влагалище M. hominis были выявлены в 10,4% случаев (n=11), Ureaplasma spp. – в 30,2% (n=32). В полости матки M. hominis были обнаружены в 9,4% случаев (n=10), Ureaplasma spp. – 17% (n=18). Следует отметить, что M. genitalium были выявлены во влагалище у
6 женщин, в эндометрии – у 4.
По результатам иммуногистохимического исследования у 81 (76,4%) пациентки с бесплодием диагностирован ХЭ. Статистически значимых различий по частоте идентификации отдельных микроорганизмов у пациенток с ХЭ и без воспалительных изменений в эндометрии не установлено (табл. 3), однако следует отметить, что лактобациллы у пациенток с ХЭ в полости матки обнаруживались реже по сравнению с женщинами без ХЭ – 50,6% и 72% соответственно (χ2=3,539, р=0,06). Среди женщин с ХЭ в полости матки M. hominis были выявлены в 11,1% случаев (n=9), Ureaplasma spp. – 21,0% (n=17), M. genitalium – 4,9% (n=4). Во влагалище этих женщин также были выявлены генитальные микоплазмы: M. genitalium – 7,4% (n=6), M. hominis – 12,4% (n=10), Ureaplasma spp. – 18,5% (n=15), у двух женщин одновременно выявлялись M. hominis и Ureaplasma spp. (2,5%).
Лечение джозамицином получали 33 пациентки с бесплодием, которые по результатам исследования имели иммуногистохимически подтвержденный ХЭ и у которых были обнаружены генитальные микоплазмы (Ureaplasma spp., и/или M. hominis, и/или M. genitalium). У всех этих женщин было две и более неудачных попытки переноса эмбриона. Следует отметить, что у двух женщин во влагалище обнаруживались одновременно уреаплазмы и M. hominis. Микробиологическую эффективность джозамицина оценивали по эрадикации генитальных микоплазм (Ureaplasma spp., и/или M. hominis, и/или M. genitalium), которая составила 100% (табл. 4).
Важным этапом исследования была оценка локального цитокинового профиля и индекса воспаления. Эти данные представлены в табл. 5.
Как видно из табл. 5, по результатам оценки локального цитокинового профиля в ткани эндометрия посредством определения мРНК про- и противовоспалительных цитокинов после лечения отмечалось статистически значимое снижение уровня транскриптов ИЛ-1β, ИЛ-18 и TLR4 при одновременном повышении уровня фактора транскрипции GATA3. При интегральной оценке уровня транскриптов исследуемых цитокинов было установлено снижение среднего индекса воспаления с 86,2±18,7 до 45,2±0,6% (t=3,942, p=0,003) после лечения курсом джозамицина.

Таким образом, лечение ХЭ у женщин с неудачными попытками имплантации – очень сложная задача. Проведение антибактериальной терапии у таких пациенток является обязательным условием. При этом имеет значение этиологический фактор ХЭ, который устанавливается по результатам молекулярно-биологического исследования. В случае выявления генитальных микоплазм мы наблюдали хороший эффект джозамицина (Джозафен®). В случае обнаружения облигатных анаэробов, бактерий семейства Enterobacteriaceae и/или дрожжеподобных грибов необходимо проведение соответствующей этиотропной терапии.
Обсуждение
Несмотря на то что персистирующие в урогенитальном тракте микоплазмы/уреаплазмы нечасто дают клинические проявления, эпидемиологические данные демонстрируют, что их наличие ассоциировано с широким спектром негативных гинекологических, акушерских и репродуктивных исходов [9–11].
При этом ставшая глобальной проблема противомикробной резистентности не обошла стороной и генитальные микоплазмы. По данным проспективного когортного исследования (Афины, Греция), выполненного с 2005 по 2019 г. с включением 8336 небеременных пациенток с симптомами вагинита в возрасте от 18 до 46 лет, количество положительных изолятов на наличие U. urealyticum и/или M. hominis составило 25,1% (n=2093). При этом наиболее высокая эффективность эрадикации внутриклеточных агентов имела место у доксициклина (97,6%), пристинамицина (97,6%) и джозамицина (95,1%), в то время как для офлоксацина, ципрофлоксацина и азитромицина микробиологическая эффективность составила 73,2%, 20,7 и 21,6% соответственно.
По данным выполненного в КНР (Ханчжоу, провинция Чжэцзян) проспективного исследования с включением 5577 пациенток, обследованных в период с 2018 по 2024 г., превалентность U. urealyticum среди обращавшихся за амбулаторной медицинской помощью с наличием клинических проявлений и для профилактического осмотра составила 49,11%. При этом некоторые макролиды продемонстрировали высокую микробиологическую эффективность в отношении данных микроорганизмов: 95,5% для джозамицина и 87,0% для кларитромицина, – в то время как для азитромицина микробиологическая эффективность составила всего 50,5% [12].
Итальянское проспективное исследование, выполненное с 2017 по 2021 г. с включением 21 210 человек, проживающих в двух коммунах (Болонья и Лекко), продемонстрировало, что частота обнаружения генитальных микоплазм в урогенитальном тракте составила 22,3%, при этом Ureaplasma spp. были идентифицированы в 62,3% случаев, M. hominis – в 8,3%, оба микроорганизма – в 29,4%. Ureaplasma spp. в 39,5% случаев были резистентны к ципрофлоксацину, M. hominis – в 60% случаев резистентны к азитромицину и рокситромицину. Резистентность менее 7% отмечалась только у двух препаратов: миноциклина и джозамицина, которые авторами исследования были рекомендованы в качестве препаратов 1-й линии эмпирической терапии [13].
В нашем исследовании на относительно небольшой выборке пациенток получена 100% микробиологическая эффективность джозамицина в отношении генитальных микоплазм (Ureaplasma spp., M. hominis и M. genitalium), обнаруженных как в отделяемом из влагалища, так и в эндометрии.
В исследовании E. Cicinelli и соавт. [14] выбор антибактериальных препаратов определялся в соответствии с бактериологическим профилем эндометрия. При наличии грамотрицательных и грамположительных бактерий применялись ципрофлоксацин (1000 мг в день в течение 10 дней) и амоксициллин с клавулановой кислотой (2 г в день в течение 8 дней) соответственно. Пациенткам, у которых выявлены Mycoplasma spp. или Ureaplasma spp., назначали джозамицин (2 г в день в течение 12 дней). Если после проведенного лечения по результатам биопсии эндометрия определялись плазматические клетки, то назначался повторный курс антибиотиков. В итоге в 76% случаев гистологическая картина была в норме, что свидетельствовало об эффективности терапии антибиотиками.
Следует отметить, что одним из преимуществ джозамицина является низкий профиль его лекарственной токсичности. Так, по данным фармакоэпидемиологического исследования с использованием базы данных фармаконадзора Всемирной организации здравоохранения в период с 1968 по 2023 г., среди наиболее часто назначаемых макролидов джозамицин обладает самым низким профилем токсичности [15].
Одним из преимуществ макролидов является системное противовоспалительное действие, которое имеет большое значение при лечении ХЭ. В нашем исследовании отмечалось снижение индекса воспаления в эндометриальной ткани в течение месяца после курса терапии джозамицином. Исследования на культурах клеток демонстрируют, что джозамицин ингибирует снижение уровня CD34 и повышение ИЛ-6, ИЛ-11 и BMP6, что обеспечивает противовоспалительный эффект и предотвращение прогрессирования фибротических изменений в функциональных тканях [16]. Клинические исследования демонстрируют эффективность макролидов как антифибротического средства при легочном фиброзе, при этом молекулярные механизмы действия заключаются в ингибировании сигнальных путей TGF-β/Smad и JNK/c-Jun. Кроме того, макролиды таргетно ингибируют высвобождение профибротических цитокинов, модуляцию поляризации макрофагов в сторону антифибротических фенотипов M2 и индукцию апоптоза в стареющих клетках [17]. Данные свойства макролида джозамицина могут сделать его препаратом выбора при лечении ХЭ в сочетании с синдромом тонкого эндометрия, где преобладают фибротические изменения функциональной ткани.
Заключение
При неудачах имплантации и наличии ХЭ необходимо назначение антибактериальных препаратов. Противомикробная терапия, направленная на элиминацию генитальных микоплазм (Ureaplasma spp., M. hominis и M. genitalium) у пациенток с ХЭ и неудачными попытками имплантации, приводит к 100% эрадикации исследуемых агентов. При этом отмечаются снижение превалентности других условно-патогенных микроорганизмов, персистирующих в полости матки, и уменьшение выраженности индекса воспаления, определяемого на основании интегральной оценки транскриптов про- и противовоспалительных цитокинов в эндометриальной ткани.
Финансирование. Работа выполнена в рамках ФНИ «Универсальные и специфические механизмы реализации и нарушений репродуктивной функции в семье» (рег. №1024032800230-9-3.2.2, рук. И.Ю. Коган).
Funding. The work was carried out within the framework of the Fundamental Scientific Research project "Universal and specific mechanisms of realization and disorders of reproductive function in the family" (reg. no. 1024032800230-9-3.2.2, Principal Investigator: I.Yu. Kogan).
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Объедкова Ксения Владимировна – канд. мед. наук, ст. науч. сотр. отд. репродуктологии ФГБНУ «НИИ АГиР им. Д.О. Отта». ORCID: 0000-0002-2056-7907
Ksenia V. Obiedkova – Cand. Sci. (Med.), Senior Researcher, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0002-2056-7907
Халенко Владислава Валерьевна – мл. науч. сотр. отд. репродуктологии ФГБНУ «НИИ АГиР им. Д.О. Отта». ORCID: 0000-0001-5313-2259
Vladislava V. Khalenko – Junior Researcher, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0001-5313-2259
Крысанова Анна Александровна – канд. мед. наук, ст. науч. сотр. группы экспериментальной микробиологии ФГБНУ «НИИ АГиР им. Д.О. Отта». ORCID: 0000-0003-4798-1881
Anna A. Krysanova – Cand. Sci. (Med.), Senior Researcher, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0003-4798-1881
Хуснутдинова Татьяна Алексеевна – канд. мед. наук, ст. науч. сотр. группы экспериментальной микробиологии ФГБНУ «НИИ АГиР им. Д.О. Отта». ORCID: 0000-0002-2742-2655
Tatiana A. Khusnutdinova – Cand. Sci. (Med.), Senior Researcher, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0002-2742-2655
Будиловская Ольга Викторовна – канд. мед. наук, ст. науч. сотр. группы экспериментальной микробиологии ФГБНУ «НИИ АГиР им. Д.О. Отта». ORCID: 0000-0001-7673-6274
Olga V. Budilovskaya – Cand. Sci. (Med.), Senior Researcher, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0001-7673-6274
Шалепо Кира Валентиновна – канд. биол. наук, ст. науч. сотр. группы экспериментальной микробиологии ФГБНУ «НИИ АГиР им. Д.О. Отта». ORCID: 0000-0002-3002-3874
Kira V. Shalepo – Cand. Sci. (Biol.), Senior Researcher, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0002-3002-3874
Савичева Алевтина Михайловна – д-р мед. наук, проф., зав. отд. медицинской микробиологии ФГБНУ «НИИ АГиР им. Д.О. Отта», засл. деят. науки РФ. ORCID: 0000-0003-3870-5930
Alevtina M. Savicheva – Dr. Sci. (Med.), Professor, Head of the Department, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0003-3870-5930
Тапильская Наталья Игоревна – д-р мед. наук, проф., вед. науч. сотр. отд. репродукции ФГБНУ «НИИ АГиР им. Д.О. Отта». E-mail: tapnatalia@yandex.ru; ORCID: 0000-0001-5309-0087
Natalia I. Tapilskaya – Dr. Sci. (Med.), Professor, Leading Researcher, Ott Research Institute of Obstetrics, Gynecology and Reproductology. E-mail: tapnatalia@yandex.ru;
ORCID: 0000-0001-5309-0087
Коган Игорь Юрьевич – чл.-кор. РАН, д-р мед. наук, проф., дир. ФГБНУ «НИИ АГиР им.
Д.О. Отта». ORCID: 0000-0002-7351-6900
Igor Yu. Kogan – Corr. Memb. RAS, Dr. Sci. (Med.), Professor, Director, Ott Research Institute of Obstetrics, Gynecology and Reproductology. ORCID: 0000-0002-7351-6900
Поступила в редакцию: 06.02.2026
Поступила после рецензирования: 10.02.2026
Принята к публикации: 12.02.2026
Received: 06.02.2026
Revised: 10.02.2026
Accepted: 12.02.2026
Список исп. литературыСкрыть список1. Puente E, Alonso L, Laganà AS et al. Chronic Endometritis: Old problem, novel insights and future challenges. Int J Fertil Steril 2020;13(4):250-6. DOI: 10.22074/ijfs.2020.5779
2. Espinós JJ, Fabregues F, Fontes J et al. Impact of chronic endometritis in infertility: a SWOT analysis. Reprod BioMed Online 2021;42(5):939-51. DOI: 10.1016/j.rbmo.2021.02.003
3. Yan X, Jiao J, Wang X. The pathogenesis, diagnosis, and treatment of chronic endometritis: a comprehensive review. Front Endocrinol 2025;(16):1603570. DOI: 10.3389/fendo.2025.1603570
4. Hiratsuka D, Matsuo M, Kashiwabara K et al. Comparison of diagnostic tests for chronic endometritis and endometrial dysbiosis in recurrent implantation failure: Impact on pregnancy outcomes. Sci Rep 2025;15(1):8272. DOI: 10.1038/s41598-025-92906-9
5. Sánchez-Ruiz R, Hernández-Chico I, Lara-Del-Río B et al. Chronic endometritis and fertility: A binomial linked by microorganisms. Eur J Obstet Gynecol Reprod Biol 2025;(305):86-91. DOI: 10.1016/j.ejogrb.2024.11.032
6. Iwami N, Komiya S, Asada Y et al. Shortening time to pregnancy in infertile women by personalizing treatment of microbial imbalance through Emma & Alice: A multicenter prospective study. Reprod Med Biol 2025;24(1):e12634. DOI: 10.1002/rmb2.12634
7. Karadbhajne P, More A, Dzoagbe HY. The Role of Endometrial Microbiota in Fertility and Reproductive Health: A Narrative Review. Cureus 2025;17(2):e78982. DOI: 10.7759/cureus.78982
8. Инструкция по медицинскому применению лекарственного препарата Джозафен®.
Instructions for medical use of the medicinal product Josafen® (in Russian).
9. Peretz A, Tameri O, Azrad M et al. Mycoplasma and Ureaplasma carriage in pregnant women: the prevalence of transmission from mother to newborn. BMC Pregnancy Childbirth 2020;20(1):456. DOI: 10.1186/s12884-020-03147-9
10. Noda-Nicolau NM, Tantengco OAG, Polettini J et al. Genital Mycoplasmas and Biomarkers of Inflammation and Their Association With Spontaneous Preterm Birth and Preterm Prelabor Rupture of Membranes: A Systematic Review and Meta-Analysis. Front Microbiol 2022;(13):859732. DOI: 10.3389/fmicb.2022.859732
11. Cutoiu A, Boda D. Prevalence of Ureaplasma urealyticum, Mycoplasma hominis and Chlamydia trachomatis in symptomatic and asymptomatic patients. Biomed Rep 2023;19(4):74. DOI: 10.3892/br.2023.1656
12. Zhang Y, Lou C, Mao L et al. Epidemiological characteristics of Ureaplasma urealyticum, Chlamydia trachomatis, Neisseria gonorrhoeae, and herpes simplex virus among 5,577 gynecological outpatients in the Xihu district of Hangzhou, China. BMC Womens Health 2025;25(1):572. DOI: 10.1186/s12905-025-04119-x
13. Pavoni M, Principe L, Foschi C et al. Antimicrobial Resistance of Genital Mycoplasma and Ureaplasma: A Multicentre Study Over a 5-Year Period in Italy (2017-2021). Microb Drug Resist 2024;30(1):55-60. DOI: 10.1089/mdr.2023.0202
14 Cicinelli E, Matteo M, Tinelli R et al. Prevalence of chronic endometritis in repeated unexplained implantation failure and the IVF success rate after antibiotic therapy. Hum Reprod 2015;(30):323-30.
15. Kono Y, Niimura T, Goda M et al. Cardiovascular Toxicity Profile of Macrolides Investigated Using VigiBase Data: A Pharmacovigilance Study. Cardiovasc Toxicol 2025;25(3):498-506. DOI: 10.1007/s12012-025-09970-w
16. Kuepfer L, Fuellen G, Stahnke T. Quantitative systems pharmacology of the eye: Tools and data for ocular QSP. CPT Pharmacometrics Syst Pharmacol 2023;12(3):288-99. DOI: 10.1002/psp4.12918
17. Jia Q, Wang Q, Zhou Q et al. The value of macrolides in the adjuvant treatment of pulmonary fibrosis: maybe a panacea. Ther Adv Respir Dis 2025;(19):17534666251346108. DOI: 10.1177/17534666251346108
21 апреля 2026
Количество просмотров: 88
