Клинический разбор в общей медицине №02 2026
Roman E. Orekhov1, Irina A. Mullina4, Rina Yu. Mitrelis2, Svetlana V. Ivanova5
1 Patrice Lumumba Peoples' Friendship University of Russia, Moscow, Russia;
2 Avtsyn Research Institute of Human Morphology of Petrovsky National Research Centre of Surgery, Moscow, Russia;
3 Clinical Hospital “Lapino”, Moscow, Russia;
4 Semashko Clinical Hospital “Russian Railways-Medicine”, Moscow, Russia;
5 52 Clinical Diagnostic Center, Moscow, Russia
omekan@mail.ru
Abstract
Chronic inflammation disturbs endometrial cyclic biotransformation and receptivity, which are of key importance for successful implantation of the embryo and determine the clinical significance of this disease entity for reproductive medicine. Today, the chronic endometritis diagnosis efficacy and pathogenetic therapy selection remain the issues that are still relevant. The necessity of using bovhyaluronidase azoximer in combination treatment regimens for chronic endometritis has been proven. The use of bovhyaluronidase azoximer in a dose of 3000 IU once every 3 days for a month reduces dysmenorrhea severity, improves local hemodynamics at the level of uterine blood vessels, significantly decreases the inflammatory marker expression, up to complete elimination.
Keywords: chronic endometritis, chronic inflammation, receptivity, bovhyaluronidase azoximer.
For citation: Orazov M.R., Radzinskiy V.E., Mikhaleva L.M., Silantyeva E.S., Orekhov R.E., Mullina I.A., Mitrelis R.Yu., Ivanova S.V. New treatment options for chronic endometritis. Clinical review for general practice. 2026; 7 (2): 18–22 (In Russ.). DOI: 10.47407/kr2026.7.2.00765
Актуальность проблемы
Хронический эндометрит (ХЭ) представляет собой клинико-морфологический синдром, характеризующийся персистирующим воспалением слизистой оболочки матки с развитием множественных вторичных морфофункциональных изменений эндометрия. Согласно современным представлениям ХЭ возникает как ответная реакция эндометрия на различные повреждающие факторы, преимущественно инфекционной природы. Хроническое воспаление нарушает циклическую биотрансформацию и рецептивность эндометрия, что имеет ключевое значение для успешной имплантации эмбриона и определяет клиническую значимость ХЭ в репродуктивной медицине [1–3].
Эпидемиологические данные демонстрируют высокую распространенность ХЭ у пациенток репродуктивного возраста. В общей популяции частота патологии варьирует от 2,8 до 46%, достигая максимальных значений у женщин с бесплодием (14–67,5%), повторными неудачами имплантации и привычным невынашиванием беременности [3–6, 38]. У женщин с привычным невынашиванием беременности частота ХЭ достигает 73% [1]. По данным метаанализа C. Ticconi и соавт. (2024 г.), ХЭ ассоциирован с почти трехкратным повышением риска бесплодия [7].
ХЭ не только причина снижения рецептивности эндометрия и, как следствие, фертильности женщины, это заболевание, способствующее развитию других факторов бесплодия, таких как внутриматочные синехии, эндометриоз, внутриматочные полипы и др. [13–16].
Клиническое значение ХЭ подчеркивается его ассоциацией с внутриматочными синехиями, являющимися одним из факторов бесплодия маточного генеза. Проспективное исследование L. Liu и соавт. (2019 г.) продемонстрировало распространенность ХЭ при внутриматочных синехиях на уровне 46% [13]. Исследование K. Kuroda и соавт. (2022 г.) выявило наиболее высокую частоту ассоциации ХЭ именно с синехиями (78,9%) среди прочих гинекологических заболеваний [14].
В ряде исследований отмечается высокая коморбидность ХЭ с эндометриозом. Систематический обзор и метаанализ D. Kalaitzopoulos и соавт. (2025 г.) установил общую распространенность ХЭ у женщин с эндометриозом на уровне 28%, при этом при тяжелых формах эндометриоза (rASRM III–IV) показатель достигал 43% [15]. Исследование E. Cicinelli и соавт. (2017 г.) выявило распространенность ХЭ при эндометриозе у 38,5% пациенток, что в 2,7 раза выше результатов группы контроля (14,1%) [16].
Роль воспаления в норме и при патологических состояниях
В норме процесс созревания эндометрия сопровождается строго регулируемым воспалением. Физиологически эндометрий содержит большое разнообразие иммунокомпетентных стромальных клеток, включая естественные киллеры (NK), макрофаги, Т-клетки и нейтрофилы. Представленность иммунных клеток и их количество в эндометрии колеблются в течение менструального цикла (МЦ). Нормальный эндометрий содержит до 70% uNK-клеток в секреторной фазе и менее 1% B-лимфоцитов (преимущественно в базальном слое). Лейкоциты составляют менее 10% стромальных клеток в пролиферативной и ранней секреторной фазах, но их количество резко возрастает начиная со средней секреторной фазы. Исследования показали, что популяции лейкоцитов эндометрия женщин с невынашиванием беременности качественно и количественно отличаются от женщин c нормальной фертильностью [24]. Имплантация эмбриона представляет собой провоспалительный Th1-зависимый процесс, сменяющийся Th2-гуморальным ответом для поддержания беременности. ХЭ приводит к персистирующему воспалению, которое нарушает баланс Th1/Th2 [22]. Нарушение естественных процессов иммунной регуляции при ХЭ проявляется патологической инфильтрацией эндометрия иммунокомпетентными клетками (CD138+, CD20+, CD56+) с одновременным снижением популяции uNK-клеток. По данным K. Kitaya и соавт. (2018 г.), ключевым маркером ХЭ является персистирующая инфильтрация плазматическими клетками (CD138+). Также наблюдаются повышение уровня провоспалительных цитокинов (фактора некроза опухоли α – ФНО-α, интерлейкинов – ИЛ-1β, ИЛ-6), снижение экспрессии ИЛ-11 (нарушение децидуализации) и CCL-4 (нарушение рекрутирования NK-клеток) [22, 23].
В последние 10 лет картина ХЭ характеризуется преимущественно субклиническим течением и преобладанием среди возбудителей представителей факультативной флоры. По данным Е. Cicinelli и соавт., у 58% пациенток с диагностированным ХЭ в качестве возбудителя были обнаружены представители условно-патогенной флоры. Наиболее часто выявляемые патогены у пациенток с ХЭ: Escherichia coli, Enterococcus faecalis, Streptococcus spp., Staphylococcus spp., Mycoplasma/Ureaplasma [17–21].
Терапией 1-й линии бактериального ХЭ является доксициклин (100 мг 2 раза в сутки) в течение 14 дней, ее эффективность составляет от 68,5 до 71,3% после одного курса и до 88,3% после двух курсов [26]. Рандомизированное контролируемое исследование D. Song и соавт. (2021 г.) продемонстрировало также эффективность комбинации левофлоксацина (500 мг/сут) и тинидазола (1000 мг/сут) в течение 14 дней на уровне 89,3% излечения против 12,7% спонтанного разрешения в контрольной группе [27]. При неэффективности 1-й линии рекомендуется комбинация ципрофлоксацина (500 мг) и метронидазола (500 мг) дважды в сутки в течение 14 дней [28].
Однако персистирующий ХЭ сохраняется у 18,75% пациенток даже после трех курсов антибиотиков [29], что обусловлено растущей антибиотикорезистентностью. По данным E. Cicinelli и соавт. (2025 г.), резистентность E. coli к фторхинолонам достигает более 50% в ряде стран, а 33,6% изолятов Klebsiella pneumoniae резистентны к фторхинолонам [30]. Это диктует необходимость поиска альтернативных терапевтических подходов, включая иммуномодуляторы, регенеративные методы и физические факторы [27, 31–33].
Обсуждается роль не только инфекционных, но и неинфекционных факторов, включая иммунные нарушения [17–19, 24]. Приблизительно 27% случаев ХЭ являются культурально-негативными, что предполагает возможные аутоиммунные механизмы воспаления [25]. Аутоиммунная теория развития ХЭ предполагает перекрестную реакцию между антигенами длительно персистирующего инфекционного агента и тканями эндометрия. Аутоиммунное воспаление приводит ко вторичному повреждению внутренней оболочки матки, не купируется антибиотикотерапией, способно длительно оставаться недиагностированным, снижая репродуктивный потенциал женщины. Поиск эффективной терапии ХЭ без верифицируемого инфекта, как и возможности увеличения эффективности антибиотикотерапии ХЭ с выявленным возбудителем, является актуальной темой в современной гинекологии.
 Новые протоколы лечения
Новые протоколы лечения
В связи с ограниченной эффективностью стандартной антибиотикотерапии исследовательский интерес представляет бовгиалуронидаза азоксимер (БА) – конъюгат гиалуронидазы с азоксимера бромидом. Препарат обладает противовоспалительным, иммуномодулирующим и выраженным противофиброзным действием, а также разрушает биопленки микроорганизмов, повышая эффективность и биодоступность антибактериальной терапии [36–38].
Нами было выполнено открытое независимое сравнительное рандомизированное клиническое исследование Life Cradle с целью оценки клинико-морфологической эффективности и безопасности использования БА (3000 ME) в комплексной терапии ХЭ у пациенток, страдающих бесплодием маточного генеза, под руководством академика РАН В.Е. Радзинского.
В исследование были включены 160 женщин с ХЭ и бесплодием в возрасте 18–45 лет с двумя и более неудачами имплантации в анамнезе. В зависимости от наличия (И+) или отсутствия (И-) внутриматочной доказанной/значимой инфекции пациентки были разделены на две когорты по 80 человек. Все участницы получали курс физиотерапии (ФТ), пациентки с наличием причинно-значимого инфекта получали антимикробную терапию (АМТ) с использованием группы тетрациклинов в комбинации с 5-нитроимидазолами. Внутри когорт пациентки были рандомизированы в соотношении 1:1 для получения или неполучения БА по схеме: 3000 МЕ внутримышечно 1 раз в три дня в течение 28 дней (всего 10 инъекций).
Первичной конечной точкой исследования было изменение числа плазматических клеток CD138+ в эндометрии в пролиферативной фазе МЦ. Вторичные конечные точки включали динамику экспрессии маркеров CD56+, CD20+, MUC1, HOXA-10, трансформирующего фактора роста β, фактора роста эндотелия сосудов (VEGF), ФНО-α, результаты гистероскопии, патоморфологического исследования, ультразвукового исследования с допплерометрией и оценку выраженности дисменореи.
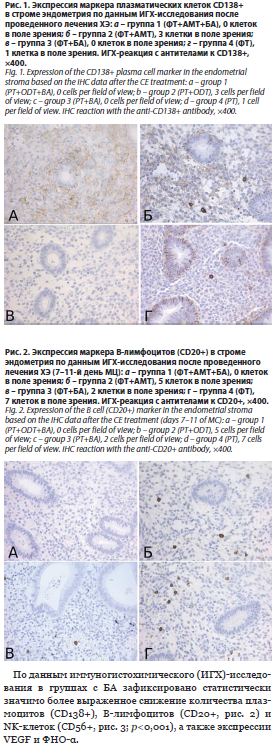
Во всех группах отмечено снижение числа плазматических клеток CD138+, однако добавление БА к базисной терапии обеспечило достоверно высокую эффективность: в когорте И+ плазматические клетки CD138+ отсутствовали у 77,5% пациенток против 2,5% в контрольной группе (p<0,001), в когорте И- – у 30% против 0% (p<0,001, рис. 1).
Морфологическая эффективность (достижение целевого уровня CD138+<5 единиц в поле зрения) в когорте без инфекта составила 82,5% в группе ФТ+БА против 52,5% в группе ФТ (p=0,008).
Комплексная терапия с использованием БА значимо снизила выраженность дисменореи: медиана снижения интенсивности боли по визуальной аналоговой шкале в группе АМТ+ФТ+БА составила -3 балла против -2 в группе АМТ+ФТ (p=0,024). В когорте без инфекта различие было еще более выраженным: -4 балла в группе ФТ+БА против -1,5 балла в группе ФТ (p=0,009).
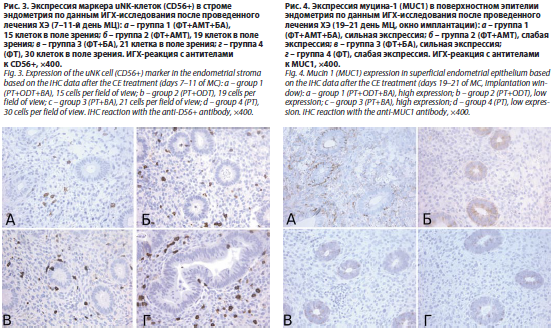
По данным иммуногистохимического (ИГХ)-исследования в группах с БА зафиксировано статистически значимо более выраженное снижение количества плазмоцитов (CD138+), В-лимфоцитов (CD20+, рис. 2) и NK-клеток (CD56+, рис. 3; p<0,001), а также экспрессии VEGF и ФНО-α.
В секреторную фазу цикла в группах с БА отмечено достоверное повышение экспрессии MUC1 (p<0,001, рис. 4), что указывает на улучшение рецептивности эндометрия.
Результаты ультразвукового исследования с допплерометрией продемонстрировали значительное улучшение маточного кровотока в группах с БА. В когорте с инфектом зафиксировано более выраженное снижение максимальной скорости кровотока в маточной артерии (p=0,013) и индекса резистентности в спиральных артериях (p=0,021). В когорте без инфекта выявлено достоверное снижение индексов резистентности и пульсации в маточной, дуговой, базальной и спиральной артериях (p<0,001–0,016).
По данным патоморфологического исследования, в группе ФТ+БА наблюдались статистически значимое снижение частоты лимфоидной инфильтрации (с 87,5 до 22,5%) по сравнению с контрольной группой (с 87,5 до 55%, p=0,005) и уменьшение очагового фиброза стромы (с 42,5 до 12,5%).
Во всех группах не зафиксировано нежелательных явлений, связанных с исследуемым препаратом, включая серьезные и аллергические реакции. Комплаентность пациенток к процедурам исследования составила 100%.
Заключение
Эффективность диагностики и выбор патогенетической терапии ХЭ остаются вопросами, не теряющими актуальности. При лечении бактериальных инфекций во всех областях медицины отмечается рост резистентности возбудителей к антибиотикотерапии. Персистирующее воспаление и инфильтрация эндометрия иммунокомпетентными клетками не просто активируют процессы фиброзообразования (формирование внутриматочных синехий), но также нарушают условия нормального созревания эндометрия и его рецептивности.
Для лечения ХЭ и возвращения женщины к нормальной фертильности критически важны как эффективная антибиотикотерапия, так и регуляция воспаления. Полученные нами клинические данные исследования Life Cradle подтверждают необходимость использования БА в терапевтических схемах лечения ХЭ вне зависимости от наличия или отсутствия инфекции в матке.
На основании результатов исследования установлено, что на фоне комплексной терапии ХЭ с использованием лиофилизата БА в дозе 3000 МЕ по схеме 1 раз в 3 дня в течение 1 мес происходят значимое снижение выраженности дисменореи, нормализация показателей маточного кровотока, кратное снижение числа патологических находок при гистероскопии и выраженное снижение маркеров ХЭ вплоть до полной элиминации.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Оразов Мекан Рахимбердыевич – д-р мед. наук, проф., проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: omekan@mail.ru; ORCID: 0000-0002-5342-8129
Mekan R. Orazov – Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: omekan@mail.ru; ORCID: 0000-0002-5342-8129
Радзинский Виктор Евсеевич – акад. РАН, д-р мед. наук, проф., зав. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН, засл. деят. науки РФ. E-mail: radzinskiy@mail.ru; ORCID: 0000-0002-7428-0469
Viktor E. Radzinskiy – Acad. RAS, Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: radzinskiy@mail.ru; ORCID: 0000-0002-7428-0469
Михалева Людмила Михайловна – чл.-кор. РАН, д-р мед. наук, проф., дир. НИИМЧ им. акад. А.П. Авцына ФГБНУ «РНЦХ им. акад. Б.В. Петровского», засл. деят. науки РФ.
E-mail: mikhalevam@yandex.ru; ORCID: 0000-0003-2052-914X
Liudmila M. Mikhaleva – Corr. Memb. RAS, Dr. Sci. (Med.), Professor, Director of Avtsyn Research Institute of Human Morphology of Petrovsky National Research Centre of Surgery. E-mail: mikhalevam@yandex.ru; ORCID: 0000-0003-2052-914X
Силантьева Елена Сергеевна – д-р мед. наук, зам. глав. врача КГ «Лапино». E-mail: essdoktor@yandex.ru; ORCID: 0000-0002-7667-3231
Elena S. Silantyeva – Dr. Sci. (Med.), Deputy Chief Doctor, Clinical Hospital “Lapino”. E-mail: essdoktor@yandex.ru; ORCID: 0000-0002-7667-3231
Орехов Роман Евгеньевич – канд. мед. наук, доц. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: romanorekhovv@ya.ru
Roman E. Orekhov – Cand. Sci. (Med.), Associate Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: romanorekhovv@ya.ru
Муллина Ирина Александровна – канд. мед. наук, врач акушер-гинеколог гинекологического отд-ния ЧУЗ «КБ “РЖД-Медицина” им. Н.А. Семашко». E-mail: 211irina2111@gmail.com
Irina A. Mullina – Cand. Sci. (Med.), Semashko Clinical Hospital “Russian Railways-Medicine”.
E-mail: 211irina2111@gmail.com
Митрелис Рина Юрьевна – аспирантка НИИМЧ им. акад. А.П. Авцына ФГБНУ «РНЦХ им. акад. Б.В. Петровского». Е-mail: abelyarrin@yandexl.ru
Rina Yu. Mitrelis – Graduate Student, Avtsyn Research Institute of Human Morphology of Petrovsky National Research Centre of Surgery. Е-mail: abelyarrin@yandexl.ru
Иванова Светлана Владимировна – врач акушер-гинеколог, зав. гинекологическим отд-нием филиала ФГБУ «52 КДЦ». Е-mail: 1606010@gmail.com; ORCID: 0009-0001-6415-1508
Svetlana V. Ivanova – gynecologist, head of department, 52 Clinical Diagnostic Center. Е-mail: 1606010@gmail.com; ORCID: 0009-0001-6415-1508
Поступила в редакцию: 05.02.2026
Поступила после рецензирования: 06.02.2026
Принята к публикации: 12.02.2026
Received: 05.02.2026
Revised: 06.02.2026
Accepted: 12.02.2026
Клинический разбор в общей медицине №02 2026
Новые возможности терапии хронического эндометрита
Номера страниц в выпуске:18-22
Аннотация
Хроническое воспаление нарушает циклическую биотрансформацию и рецептивность эндометрия, что имеет ключевое значение для успешной имплантации эмбриона и определяет клиническую значимость данной нозологии в репродуктивной медицине. В настоящее время эффективность диагностики и выбор патогенетической терапии хронического эндометрита остаются вопросами, не теряющими актуальности. Установлена необходимость использования бовгиалуронидазы азоксимера в комплексных терапевтических схемах лечения хронического эндометрита. Использование бовгиалуронидазы азоксимера в дозе 3000 МЕ по схеме 1 раз в 3 дня в течение 1 мес снижает выраженность дисменореи, повышает локальную гемодинамику на уровне маточных сосудов, значимо снижает экспрессию маркеров воспаления вплоть до полной элиминации.
Ключевые слова: хронический эндометрит, хроническое воспаление, рецептивность, бовгиалуронидаза азоксимер.
Для цитирования: Оразов М.Р., Радзинский В.Е., Михалева Л.М., Силантьева Е.С., Орехов Р.Е., Муллина И.А., Митрелис Р.Ю., Иванова С.В. Новые возможности терапии хронического эндометрита. Клинический разбор в общей медицине. 2026; 7 (2): 18–22. DOI: 10.47407/kr2026.7.2.00765
Хроническое воспаление нарушает циклическую биотрансформацию и рецептивность эндометрия, что имеет ключевое значение для успешной имплантации эмбриона и определяет клиническую значимость данной нозологии в репродуктивной медицине. В настоящее время эффективность диагностики и выбор патогенетической терапии хронического эндометрита остаются вопросами, не теряющими актуальности. Установлена необходимость использования бовгиалуронидазы азоксимера в комплексных терапевтических схемах лечения хронического эндометрита. Использование бовгиалуронидазы азоксимера в дозе 3000 МЕ по схеме 1 раз в 3 дня в течение 1 мес снижает выраженность дисменореи, повышает локальную гемодинамику на уровне маточных сосудов, значимо снижает экспрессию маркеров воспаления вплоть до полной элиминации.
Ключевые слова: хронический эндометрит, хроническое воспаление, рецептивность, бовгиалуронидаза азоксимер.
Для цитирования: Оразов М.Р., Радзинский В.Е., Михалева Л.М., Силантьева Е.С., Орехов Р.Е., Муллина И.А., Митрелис Р.Ю., Иванова С.В. Новые возможности терапии хронического эндометрита. Клинический разбор в общей медицине. 2026; 7 (2): 18–22. DOI: 10.47407/kr2026.7.2.00765
New treatment options for chronic endometritis
Mekan R. Orazov1, Viktor E. Radzinskiy1, Liudmila M. Mikhaleva2, Elena S. Silantyeva3,Roman E. Orekhov1, Irina A. Mullina4, Rina Yu. Mitrelis2, Svetlana V. Ivanova5
1 Patrice Lumumba Peoples' Friendship University of Russia, Moscow, Russia;
2 Avtsyn Research Institute of Human Morphology of Petrovsky National Research Centre of Surgery, Moscow, Russia;
3 Clinical Hospital “Lapino”, Moscow, Russia;
4 Semashko Clinical Hospital “Russian Railways-Medicine”, Moscow, Russia;
5 52 Clinical Diagnostic Center, Moscow, Russia
omekan@mail.ru
Abstract
Chronic inflammation disturbs endometrial cyclic biotransformation and receptivity, which are of key importance for successful implantation of the embryo and determine the clinical significance of this disease entity for reproductive medicine. Today, the chronic endometritis diagnosis efficacy and pathogenetic therapy selection remain the issues that are still relevant. The necessity of using bovhyaluronidase azoximer in combination treatment regimens for chronic endometritis has been proven. The use of bovhyaluronidase azoximer in a dose of 3000 IU once every 3 days for a month reduces dysmenorrhea severity, improves local hemodynamics at the level of uterine blood vessels, significantly decreases the inflammatory marker expression, up to complete elimination.
Keywords: chronic endometritis, chronic inflammation, receptivity, bovhyaluronidase azoximer.
For citation: Orazov M.R., Radzinskiy V.E., Mikhaleva L.M., Silantyeva E.S., Orekhov R.E., Mullina I.A., Mitrelis R.Yu., Ivanova S.V. New treatment options for chronic endometritis. Clinical review for general practice. 2026; 7 (2): 18–22 (In Russ.). DOI: 10.47407/kr2026.7.2.00765
Актуальность проблемы
Хронический эндометрит (ХЭ) представляет собой клинико-морфологический синдром, характеризующийся персистирующим воспалением слизистой оболочки матки с развитием множественных вторичных морфофункциональных изменений эндометрия. Согласно современным представлениям ХЭ возникает как ответная реакция эндометрия на различные повреждающие факторы, преимущественно инфекционной природы. Хроническое воспаление нарушает циклическую биотрансформацию и рецептивность эндометрия, что имеет ключевое значение для успешной имплантации эмбриона и определяет клиническую значимость ХЭ в репродуктивной медицине [1–3].
Эпидемиологические данные демонстрируют высокую распространенность ХЭ у пациенток репродуктивного возраста. В общей популяции частота патологии варьирует от 2,8 до 46%, достигая максимальных значений у женщин с бесплодием (14–67,5%), повторными неудачами имплантации и привычным невынашиванием беременности [3–6, 38]. У женщин с привычным невынашиванием беременности частота ХЭ достигает 73% [1]. По данным метаанализа C. Ticconi и соавт. (2024 г.), ХЭ ассоциирован с почти трехкратным повышением риска бесплодия [7].
ХЭ не только причина снижения рецептивности эндометрия и, как следствие, фертильности женщины, это заболевание, способствующее развитию других факторов бесплодия, таких как внутриматочные синехии, эндометриоз, внутриматочные полипы и др. [13–16].
Клиническое значение ХЭ подчеркивается его ассоциацией с внутриматочными синехиями, являющимися одним из факторов бесплодия маточного генеза. Проспективное исследование L. Liu и соавт. (2019 г.) продемонстрировало распространенность ХЭ при внутриматочных синехиях на уровне 46% [13]. Исследование K. Kuroda и соавт. (2022 г.) выявило наиболее высокую частоту ассоциации ХЭ именно с синехиями (78,9%) среди прочих гинекологических заболеваний [14].
В ряде исследований отмечается высокая коморбидность ХЭ с эндометриозом. Систематический обзор и метаанализ D. Kalaitzopoulos и соавт. (2025 г.) установил общую распространенность ХЭ у женщин с эндометриозом на уровне 28%, при этом при тяжелых формах эндометриоза (rASRM III–IV) показатель достигал 43% [15]. Исследование E. Cicinelli и соавт. (2017 г.) выявило распространенность ХЭ при эндометриозе у 38,5% пациенток, что в 2,7 раза выше результатов группы контроля (14,1%) [16].
Роль воспаления в норме и при патологических состояниях
В норме процесс созревания эндометрия сопровождается строго регулируемым воспалением. Физиологически эндометрий содержит большое разнообразие иммунокомпетентных стромальных клеток, включая естественные киллеры (NK), макрофаги, Т-клетки и нейтрофилы. Представленность иммунных клеток и их количество в эндометрии колеблются в течение менструального цикла (МЦ). Нормальный эндометрий содержит до 70% uNK-клеток в секреторной фазе и менее 1% B-лимфоцитов (преимущественно в базальном слое). Лейкоциты составляют менее 10% стромальных клеток в пролиферативной и ранней секреторной фазах, но их количество резко возрастает начиная со средней секреторной фазы. Исследования показали, что популяции лейкоцитов эндометрия женщин с невынашиванием беременности качественно и количественно отличаются от женщин c нормальной фертильностью [24]. Имплантация эмбриона представляет собой провоспалительный Th1-зависимый процесс, сменяющийся Th2-гуморальным ответом для поддержания беременности. ХЭ приводит к персистирующему воспалению, которое нарушает баланс Th1/Th2 [22]. Нарушение естественных процессов иммунной регуляции при ХЭ проявляется патологической инфильтрацией эндометрия иммунокомпетентными клетками (CD138+, CD20+, CD56+) с одновременным снижением популяции uNK-клеток. По данным K. Kitaya и соавт. (2018 г.), ключевым маркером ХЭ является персистирующая инфильтрация плазматическими клетками (CD138+). Также наблюдаются повышение уровня провоспалительных цитокинов (фактора некроза опухоли α – ФНО-α, интерлейкинов – ИЛ-1β, ИЛ-6), снижение экспрессии ИЛ-11 (нарушение децидуализации) и CCL-4 (нарушение рекрутирования NK-клеток) [22, 23].
В последние 10 лет картина ХЭ характеризуется преимущественно субклиническим течением и преобладанием среди возбудителей представителей факультативной флоры. По данным Е. Cicinelli и соавт., у 58% пациенток с диагностированным ХЭ в качестве возбудителя были обнаружены представители условно-патогенной флоры. Наиболее часто выявляемые патогены у пациенток с ХЭ: Escherichia coli, Enterococcus faecalis, Streptococcus spp., Staphylococcus spp., Mycoplasma/Ureaplasma [17–21].
Терапией 1-й линии бактериального ХЭ является доксициклин (100 мг 2 раза в сутки) в течение 14 дней, ее эффективность составляет от 68,5 до 71,3% после одного курса и до 88,3% после двух курсов [26]. Рандомизированное контролируемое исследование D. Song и соавт. (2021 г.) продемонстрировало также эффективность комбинации левофлоксацина (500 мг/сут) и тинидазола (1000 мг/сут) в течение 14 дней на уровне 89,3% излечения против 12,7% спонтанного разрешения в контрольной группе [27]. При неэффективности 1-й линии рекомендуется комбинация ципрофлоксацина (500 мг) и метронидазола (500 мг) дважды в сутки в течение 14 дней [28].
Однако персистирующий ХЭ сохраняется у 18,75% пациенток даже после трех курсов антибиотиков [29], что обусловлено растущей антибиотикорезистентностью. По данным E. Cicinelli и соавт. (2025 г.), резистентность E. coli к фторхинолонам достигает более 50% в ряде стран, а 33,6% изолятов Klebsiella pneumoniae резистентны к фторхинолонам [30]. Это диктует необходимость поиска альтернативных терапевтических подходов, включая иммуномодуляторы, регенеративные методы и физические факторы [27, 31–33].
Обсуждается роль не только инфекционных, но и неинфекционных факторов, включая иммунные нарушения [17–19, 24]. Приблизительно 27% случаев ХЭ являются культурально-негативными, что предполагает возможные аутоиммунные механизмы воспаления [25]. Аутоиммунная теория развития ХЭ предполагает перекрестную реакцию между антигенами длительно персистирующего инфекционного агента и тканями эндометрия. Аутоиммунное воспаление приводит ко вторичному повреждению внутренней оболочки матки, не купируется антибиотикотерапией, способно длительно оставаться недиагностированным, снижая репродуктивный потенциал женщины. Поиск эффективной терапии ХЭ без верифицируемого инфекта, как и возможности увеличения эффективности антибиотикотерапии ХЭ с выявленным возбудителем, является актуальной темой в современной гинекологии.
 Новые протоколы лечения
Новые протоколы леченияВ связи с ограниченной эффективностью стандартной антибиотикотерапии исследовательский интерес представляет бовгиалуронидаза азоксимер (БА) – конъюгат гиалуронидазы с азоксимера бромидом. Препарат обладает противовоспалительным, иммуномодулирующим и выраженным противофиброзным действием, а также разрушает биопленки микроорганизмов, повышая эффективность и биодоступность антибактериальной терапии [36–38].
Нами было выполнено открытое независимое сравнительное рандомизированное клиническое исследование Life Cradle с целью оценки клинико-морфологической эффективности и безопасности использования БА (3000 ME) в комплексной терапии ХЭ у пациенток, страдающих бесплодием маточного генеза, под руководством академика РАН В.Е. Радзинского.
В исследование были включены 160 женщин с ХЭ и бесплодием в возрасте 18–45 лет с двумя и более неудачами имплантации в анамнезе. В зависимости от наличия (И+) или отсутствия (И-) внутриматочной доказанной/значимой инфекции пациентки были разделены на две когорты по 80 человек. Все участницы получали курс физиотерапии (ФТ), пациентки с наличием причинно-значимого инфекта получали антимикробную терапию (АМТ) с использованием группы тетрациклинов в комбинации с 5-нитроимидазолами. Внутри когорт пациентки были рандомизированы в соотношении 1:1 для получения или неполучения БА по схеме: 3000 МЕ внутримышечно 1 раз в три дня в течение 28 дней (всего 10 инъекций).
Первичной конечной точкой исследования было изменение числа плазматических клеток CD138+ в эндометрии в пролиферативной фазе МЦ. Вторичные конечные точки включали динамику экспрессии маркеров CD56+, CD20+, MUC1, HOXA-10, трансформирующего фактора роста β, фактора роста эндотелия сосудов (VEGF), ФНО-α, результаты гистероскопии, патоморфологического исследования, ультразвукового исследования с допплерометрией и оценку выраженности дисменореи.
Во всех группах отмечено снижение числа плазматических клеток CD138+, однако добавление БА к базисной терапии обеспечило достоверно высокую эффективность: в когорте И+ плазматические клетки CD138+ отсутствовали у 77,5% пациенток против 2,5% в контрольной группе (p<0,001), в когорте И- – у 30% против 0% (p<0,001, рис. 1).
Морфологическая эффективность (достижение целевого уровня CD138+<5 единиц в поле зрения) в когорте без инфекта составила 82,5% в группе ФТ+БА против 52,5% в группе ФТ (p=0,008).
Комплексная терапия с использованием БА значимо снизила выраженность дисменореи: медиана снижения интенсивности боли по визуальной аналоговой шкале в группе АМТ+ФТ+БА составила -3 балла против -2 в группе АМТ+ФТ (p=0,024). В когорте без инфекта различие было еще более выраженным: -4 балла в группе ФТ+БА против -1,5 балла в группе ФТ (p=0,009).

По данным иммуногистохимического (ИГХ)-исследования в группах с БА зафиксировано статистически значимо более выраженное снижение количества плазмоцитов (CD138+), В-лимфоцитов (CD20+, рис. 2) и NK-клеток (CD56+, рис. 3; p<0,001), а также экспрессии VEGF и ФНО-α.
В секреторную фазу цикла в группах с БА отмечено достоверное повышение экспрессии MUC1 (p<0,001, рис. 4), что указывает на улучшение рецептивности эндометрия.
Результаты ультразвукового исследования с допплерометрией продемонстрировали значительное улучшение маточного кровотока в группах с БА. В когорте с инфектом зафиксировано более выраженное снижение максимальной скорости кровотока в маточной артерии (p=0,013) и индекса резистентности в спиральных артериях (p=0,021). В когорте без инфекта выявлено достоверное снижение индексов резистентности и пульсации в маточной, дуговой, базальной и спиральной артериях (p<0,001–0,016).
По данным патоморфологического исследования, в группе ФТ+БА наблюдались статистически значимое снижение частоты лимфоидной инфильтрации (с 87,5 до 22,5%) по сравнению с контрольной группой (с 87,5 до 55%, p=0,005) и уменьшение очагового фиброза стромы (с 42,5 до 12,5%).
Во всех группах не зафиксировано нежелательных явлений, связанных с исследуемым препаратом, включая серьезные и аллергические реакции. Комплаентность пациенток к процедурам исследования составила 100%.
Заключение
Эффективность диагностики и выбор патогенетической терапии ХЭ остаются вопросами, не теряющими актуальности. При лечении бактериальных инфекций во всех областях медицины отмечается рост резистентности возбудителей к антибиотикотерапии. Персистирующее воспаление и инфильтрация эндометрия иммунокомпетентными клетками не просто активируют процессы фиброзообразования (формирование внутриматочных синехий), но также нарушают условия нормального созревания эндометрия и его рецептивности.
Для лечения ХЭ и возвращения женщины к нормальной фертильности критически важны как эффективная антибиотикотерапия, так и регуляция воспаления. Полученные нами клинические данные исследования Life Cradle подтверждают необходимость использования БА в терапевтических схемах лечения ХЭ вне зависимости от наличия или отсутствия инфекции в матке.
На основании результатов исследования установлено, что на фоне комплексной терапии ХЭ с использованием лиофилизата БА в дозе 3000 МЕ по схеме 1 раз в 3 дня в течение 1 мес происходят значимое снижение выраженности дисменореи, нормализация показателей маточного кровотока, кратное снижение числа патологических находок при гистероскопии и выраженное снижение маркеров ХЭ вплоть до полной элиминации.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Оразов Мекан Рахимбердыевич – д-р мед. наук, проф., проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: omekan@mail.ru; ORCID: 0000-0002-5342-8129
Mekan R. Orazov – Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: omekan@mail.ru; ORCID: 0000-0002-5342-8129
Радзинский Виктор Евсеевич – акад. РАН, д-р мед. наук, проф., зав. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН, засл. деят. науки РФ. E-mail: radzinskiy@mail.ru; ORCID: 0000-0002-7428-0469
Viktor E. Radzinskiy – Acad. RAS, Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: radzinskiy@mail.ru; ORCID: 0000-0002-7428-0469
Михалева Людмила Михайловна – чл.-кор. РАН, д-р мед. наук, проф., дир. НИИМЧ им. акад. А.П. Авцына ФГБНУ «РНЦХ им. акад. Б.В. Петровского», засл. деят. науки РФ.
E-mail: mikhalevam@yandex.ru; ORCID: 0000-0003-2052-914X
Liudmila M. Mikhaleva – Corr. Memb. RAS, Dr. Sci. (Med.), Professor, Director of Avtsyn Research Institute of Human Morphology of Petrovsky National Research Centre of Surgery. E-mail: mikhalevam@yandex.ru; ORCID: 0000-0003-2052-914X
Силантьева Елена Сергеевна – д-р мед. наук, зам. глав. врача КГ «Лапино». E-mail: essdoktor@yandex.ru; ORCID: 0000-0002-7667-3231
Elena S. Silantyeva – Dr. Sci. (Med.), Deputy Chief Doctor, Clinical Hospital “Lapino”. E-mail: essdoktor@yandex.ru; ORCID: 0000-0002-7667-3231
Орехов Роман Евгеньевич – канд. мед. наук, доц. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: romanorekhovv@ya.ru
Roman E. Orekhov – Cand. Sci. (Med.), Associate Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: romanorekhovv@ya.ru
Муллина Ирина Александровна – канд. мед. наук, врач акушер-гинеколог гинекологического отд-ния ЧУЗ «КБ “РЖД-Медицина” им. Н.А. Семашко». E-mail: 211irina2111@gmail.com
Irina A. Mullina – Cand. Sci. (Med.), Semashko Clinical Hospital “Russian Railways-Medicine”.
E-mail: 211irina2111@gmail.com
Митрелис Рина Юрьевна – аспирантка НИИМЧ им. акад. А.П. Авцына ФГБНУ «РНЦХ им. акад. Б.В. Петровского». Е-mail: abelyarrin@yandexl.ru
Rina Yu. Mitrelis – Graduate Student, Avtsyn Research Institute of Human Morphology of Petrovsky National Research Centre of Surgery. Е-mail: abelyarrin@yandexl.ru
Иванова Светлана Владимировна – врач акушер-гинеколог, зав. гинекологическим отд-нием филиала ФГБУ «52 КДЦ». Е-mail: 1606010@gmail.com; ORCID: 0009-0001-6415-1508
Svetlana V. Ivanova – gynecologist, head of department, 52 Clinical Diagnostic Center. Е-mail: 1606010@gmail.com; ORCID: 0009-0001-6415-1508
Поступила в редакцию: 05.02.2026
Поступила после рецензирования: 06.02.2026
Принята к публикации: 12.02.2026
Received: 05.02.2026
Revised: 06.02.2026
Accepted: 12.02.2026
Список исп. литературыСкрыть список1. Серебренникова К.Г., Арутюнян Н.А., Алексин А.И. Диагностика и клинические критерии хронического эндометрита. Гинекология. 2018;20(6):53-9. DOI: 10.26442/20795696.2018.6.180070
Serebrennikova K.G., Arutyunyan N.A., Aleksin A.I. Diagnostics and clinical criteria of chronic endometritis. Gynecology. 2018; 20(6):53–9. DOI: 10.26442/20795696.2018.6.180070 (in Russian).
2. Воспалительные болезни женских тазовых органов. Клинические рекомендации Минздрава России. М.: Российское общество акушеров-гинекологов, 2024.
Inflammatory diseases of the female pelvic organs. Clinical guidelines of the Russian Ministry of Health. Moscow: Russian Society of Obstetricians and Gynecologists, 2024 (in Russian).
3. Прегравидарная подготовка. Клинический протокол МАРС. Версия 3.0. М.: StatusPraesens, 2023.
Preconception Preparation. MARS Clinical Protocol. Version 3.0. Moscow: StatusPraesens, 2023 (in Russian).
4. Cicinelli E, Cicinelli R, Vitagliano A. Antibiotic therapy for chronic endometritis and its reproductive implications: a step forward, with some uncertainties. Fertil Steril 2021;115(6):1445-6. DOI: 10.1016/j.fertnstert.2021.03.025
5. Lee H, Kim J, Choi D et al. Chronic endometritis prevalence, associated factors and pregnancy outcome among infertile women. Hum Reprod 2024;39(Suppl.1):deae108.684. DOI: 10.1093/humrep/deae108.684
6. Bouet PE, El Hachem H, Monceau E et al. Chronic endometritis in women with recurrent pregnancy loss and recurrent implantation failure: prevalence and role of office hysteroscopy and immunohistochemistry in diagnosis. Fertil Steril 2016;105(1):106-10. DOI: 10.1016/j.fertnstert.2015.09.025
7. Ticconi C, Di Simone N, Campagnolo L et al. Chronic endometritis and recurrent reproductive failure: a systematic review and meta-analysis. Front Immunol 2024;(15):1427454. DOI: 10.3389/fimmu. 2024.1427454
8. Cicinelli E, Resta L, Loizzi V et al. Antibiotic therapy versus no treatment for chronic endometritis: a case-control study. Fertil Steril 2021;115(6):1541-8. DOI: 10.1016/j.fertnstert.2021.01.018
9. Di Pasqua A, Galimberti A, Capitanio E et al. Chronic endometritis in infertile patients: diagnosis, treatment and follow-up. Hum Reprod 2025;40(Suppl.1):deaf097.630. DOI: 10.1093/humrep/deaf097.630
10. Liu L, Yang H, Guo Y et al. The impact of chronic endometritis on endometrial fibrosis and reproductive prognosis in patients with moderate and severe intrauterine adhesions: a prospective cohort study. Fertil Steril 2019;111(5):1002-1010.e2. DOI: 10.1016/j.fertnstert.2019.01.006
11. Локшин В.Н., Кущенко И.Н., Боровиков И.О. и др. Хронический эндометрит и инфертильность – исходы ЭКО (систематический обзор и метаанализ). Кубанский научный медицинский вестник. 2023;30(5):15-40. DOI: 10.25207/1608-6228-2023-30-5-15-40
Lokshin V.N., Kushchenko I.N., Borovikov I.O. et al. Chronic endometritis and infertility – IVF outcomes (systematic review and meta-analysis). Kuban Scientific Medical Bulletin. 2023; 30(5):15–40. DOI: 10.25207/1608-6228-2023-30-5-15-40 (in Russian).
12. McQueen DB, Perfetto CO, Hazard FK, Lathi RB. Pregnancy outcomes in women with chronic endometritis and recurrent pregnancy loss. Fertil Steril 2015;104(4):927-31. DOI: 10.1016/j.fertnstert.2015.06.044
13. Liu L, Yang H, Guo Y et al. The impact of chronic endometritis on endometrial fibrosis and reproductive prognosis. Fertil Steril 2019;111(5):1002-1010.e2.
14. Kuroda K, Ikemoto Y, Ochiai A et al. Prevalence of and risk factors for chronic endometritis in patients with intrauterine disorders after hysteroscopic surgery. Fertil Steril 2022;118(3):568-75. DOI: 10.1016/j.fertnstert.2022.06.013
15. Kalaitzopoulos DR, Samartzis N, Daniilidis A et al. Chronic Endometritis and Endometriosis: Two Sides of the Same Coin? Reprod Sci 2025. DOI: 10.1007/s43032-025-01785-y
16. Cicinelli E, Matteo M, Tinelli R et al. Chronic endometritis due to common bacteria is prevalent in women with recurrent miscarriage as confirmed by improved pregnancy outcome after antibiotic treatment. Reprod Sci 2014;21(5):640-7.
17. Cicinelli E, Di Gennaro F, Gesario A et al. Unified diagnostic criteria for chronic endometritis at fluid hysteroscopy. Fertil Steril 2019;112(1):162-173.e2. DOI: 10.1016/j.fertnstert.2019.03.004
18. Furui M, Ito A, Fukuda Y et al. Endometrial congestion is the only hysteroscopic finding indicative of chronic endometritis. PLoS ONE 2024;19(6):e0303041. DOI: 10.1371/journal.pone.0303041
19. Moreno I, Cicinelli E, Garcia-Grau I et al. The diagnosis of chronic endometritis in infertile asymptomatic women: a comparative study. Am J Obstet Gynecol 2018;218(6):602.e1-602.e16. DOI: 10.1016/j.ajog.2018.02.012
20. Kitaya K, Takeuchi T, Mizuta S et al. Endometritis: new time, new concepts. Fertil Steril 2018;110(3):344-50. DOI: 10.1016/j.fertnstert.2018.04.012
21. Yoneda E, Kim S, Tomita K et al. Evaluation of Lipopolysaccharide and Interleukin-6 as Useful Screening Tool for Chronic Endometritis. Int J Mol Sci 2024;25(4):2017. DOI: 10.3390/ijms25042017
22. Zeng S, Liang Y, Li Y et al. Research update for the immune microenvironment of chronic endometritis. J Reprod Immunol 2022;(152):103637. DOI: 10.1016/j.jri.2022.103637
23. Travaglino A, Raffone A, Saccone G et al. The Role of Plasma Cells as a Marker of Chronic Endometritis: A Systematic Review and Meta-Analysis. Biomedicines 2023;11(6):1714. DOI: 10.3390/biomedicines11061714
24. Liu Y, Zhao Z, Jiang X et al. Doxycycline vs levofloxacin combined with tinidazole for treating chronic endometritis: a randomized controlled trial. Am J Obstet Gynecol 2025;S0002937825005253. DOI: 10.1016/j.ajog.2025.07.045
25. Yan X, Zhang Y, Zhang L et al. The pathogenesis, diagnosis, and treatment of chronic endometritis: a comprehensive review. Front Endocrinol 2025;(16):1603570. DOI: 10.3389/fendo.2025.1603570
26. HogenEsch E, Franasiak JM. Chronic endometritis treatment. Fertil Steril 2023;120(3 Pt 1):456-64.
27. Song D, He Y, Wang Y et al. Impact of antibiotic therapy on the rate of negative test results for chronic endometritis: a prospective randomized control trial. Fertil Steril 2021;115(6):1549-56. DOI: 10.1016/j.fertnstert.2020.12.019
28. Kitaya K, Matsubayashi H, Takaya Y et al. Clinical background affecting pregnancy outcome following local endometrial injury in infertile patients with repeated implantation failure. Am J Reprod Immunol 2017;78(5):e12727. DOI: 10.1111/aji.12719
29. Cicinelli E, Resta L, Nicoletti R et al. Endometrial micropolyps at fluid hysteroscopy suggest the existence of chronic endometritis. Hum Reprod 2005;20(5):1386-9.
30. Cicinelli E, Di Gennaro F, Gesario A et al. Increasing Antimicrobial Resistance to First-Line Therapies in Chronic Endometritis: A 2020–2024 Cross-Sectional Study. J Clin Med 2025;14(14):4873. DOI: 10.3390/jcm14144873
31. Khalenko V, Obedkova KV, Tapilskaya NI et al. New Approaches to the Treatment of Chronic Endometritis. Hum Reprod 2025;40(Suppl.1):deaf097.196. DOI: 10.1093/humrep/deaf097.196
32. Zhylkova E, Feskov O, Konoplya L et al. Administration of umbilical cord blood and placenta in the treatment of chronic endometritis. Hum Reprod 2025;40(Suppl.1):deaf097.207. DOI: 10.1093/humrep/deaf097.207
33. Di Gennaro F, Cicinelli R, Saracino A et al. Chronic Endometritis and Antimicrobial Resistance: Towards a Multidrug-Resistant Endometritis? Microorganisms 2025;13(1):197. DOI: 10.3390/microorganisms13010197
34. Оразов М.Р., Михалева Л.М., Семенов П.А. Хронический эндометрит: патогенез, диагностика, лечение и его связь с бесплодием. Клиническая и экспериментальная морфология. 2020;9(2):16-25. DOI: 10.31088/CEM2020.9.2.16-25
Orazov M.R., Mikhaleva L.M., Semenov P.A. Chronic endometritis: pathogenesis, diagnosis, treatment, and its relationship with infertility. Clinical and experimental morphology. 2020; 9 (2): 16–25. DOI: 10.31088/CEM2020.9.2.16–25 (in Russian).
35. Wang X, Liu X, Li X et al. Exploring the Relationship between Hyaluronic Acid Size and Biological Activity: A Review. DOI: 10.2139/ssrn.5090479
36. Lu J, Zhao Z, Pan L et al. Hyaluronidase: structure, mechanism of action, diseases and therapeutic targets. Mol Biomedicine 2025;(6):50. DOI: 10.1186/s43556-025-00299-y
37. Тризна Е.Ю., Байдамшина Д.Р., Каюмов А.Р. Влияние in vitro изолированного и сочетанного с антибактериальными средствами применения бовгиалуронидазы азоксимера на целостность бактериальной биопленки. Экспериментальная и клиническая фармакология. 2020;83(2):38-44.
Trizna E.Yu., Baidamshina D.R., Kayumov A.R. Effect of in vitro use of bovhyaluronidase azoximer alone and in combination with antibacterial agents on the integrity of bacterial biofilm. Experimental and Clinical Pharmacology. 2020;83(2):38-44. (in Russian).
38. Тапильская Н.И., Копылова А.А., Будиловская О.В. и др. Оценка эффективности применения бовгиалуронидазы азоксимера в лечении хронического эндометрита у женщин с неудачами имплантации. Женская клиника. 2020;(2):66-72.
Tapilskaya N.I., Kopylova A.A., Budilovskaya O.V. et al. Evaluation of the effectiveness of bovhyaluronidase azoximer in the treatment of chronic endometritis in women with implantation failures. Women's Clinic. 2020;(2):66-72 (in Russian).
39. Радзинский В.Е., Оразов М.Р., Михалева Л.М. и др. Эффективность и безопасность бовгиалуронидазы азоксимера в терапии хронического эндометрита: результаты открытого сравнительного рандомизированного контролируемого исследования Life Cradle. Клинический разбор в общей медицине. 2025;6(12).
Radzinskiy V.E., Orazov M.R., Mikhaleva L.M. et al. Efficacy and safety of bovhyaluronidase azoximer in the treatment of chronic endometritis: results of an open, comparative, randomized, controlled trial Life Cradle. Clinical review for general practice. 2025;6(12) (in Russian).
