Клинический разбор в общей медицине №02 2026
Mekan R. Orazov1, Roman E. Orekhov1, Anastasiia N. Akhmatova1, Irina A. Mullina3
1 Patrice Lumumba Peoples' Friendship University of Russia, Moscow, Russia;
2 Avtsyn Research Institute of Human Morphology of Petrovsky National Research Centre of Surgery, Moscow, Russia;
3 Semashko Clinical Hospital “Russian Railways-Medicine”, Moscow, Russia
omekan@mail.ru
Abstract
Aim. To improve the effectiveness of combination therapy for endometrial hyperplasia without atypia using D-chiro-inositol (DCI).
Materials and methods. This double-blind prospective randomized placebo-controlled trial enrolled 60 patients with morphologically verified endometrial hyperplasia without atypia. Participants were stratified into two groups: Group 1 (n=30) received norethisterone acetate in continuous regimen according to the current prescribing information plus DCI 1200 mg/day; Group 2 (n=30) received norethisterone acetate plus placebo. Treatment duration was 6 months with subsequent follow-up for 6 months. The following outcomes were assessed: morphological regression and recurrence rates, dynamics of immunohistochemical markers (Ki-67, VEGF, p53), cytokine profile and metabolic parameters, and safety profile.
Results. The study demonstrated that complete morphological regression of endometrial hyperplasia without atypia at 6 months was achieved in 86.7% of patients receiving progestogen + DCI compared to 60.0% in patients receiving progestogen + placebo (1.4–fold higher; p=0.020). Furthermore, analysis of recurrence rates at 6 months after treatment completion showed superior outcomes in patients after combination therapy (3.7–fold lower, 10.0% vs 36.7%; p=0.015). Sonographic assessment of endometrial thickness after treatment revealed M-echo of 8.5±2.6 mm in patients receiving progestogen + DCI versus 11.4±2.9 mm in patients receiving progestogen + placebo (p<0.001). Patients receiving progestogen + DCI demonstrated normalization of Ki-67 proliferation index (9.8±4.5% with normal range <10%) and VEGF expression (1.83±0.53 AU with normal range <2.0). DCI as part of combination therapy led to normalization of HOMA-IR index (2.44±0.56 vs 3.23±0.52; p<0.001), improvement in lipid profile (reduction in total cholesterol, LDL, and triglycerides by 1.2–1.4-fold; increase in HDL by 1.3-fold), and 2.0-fold reduction in C-reactive protein levels (p<0.001), as well as proinflammatory cytokines. BMI in patients receiving progestogen + DCI decreased from 30.4±2.3 to 28.9±2.4 kg/m², whereas in patients receiving progestogen + placebo it remained stable (30.6±1.6 → 30.8±2.1 kg/m²; p=0.002).
Conclusion. The results of this randomized placebo-controlled trial indicate that adding DCI at a dose of 1200 mg/day to standard norethisterone acetate therapy significantly improves treatment efficacy for endometrial hyperplasia without atypia in women with overweight and obesity.
Keywords: endometrial hyperplasia, D-chiro-inositol, insulin resistance, progestogens, norethisterone acetate, cytokines, Ki-67.
For citation: Radzinskiy V.E., Mihaleva L.M., Kostin I.N., Khamoshina M.B., Orazov M.R., Orekhov R.E., Akhmatova A.N., Mullina I.A. D-chiro-inositol in combination therapy of endometrial hyperplasia without atypia: results of the double-blind randomized placebo-controlled trial. Clinical review for general practice. 2026; 7 (2): 24–36 (In Russ.). DOI: 10.47407/kr2026.7.2.00766
Введение
Гиперплазия эндометрия (ГЭ) представляет собой патологическое состояние, характеризующееся аномальной пролиферацией эндометриальных желез с увеличением соотношения железистого компонента к строме [1]. Являясь предраковым состоянием, ГЭ требует особого внимания клиницистов, поскольку рак эндометрия занимает лидирующую позицию среди злокачественных новообразований женской репродуктивной системы в развитых странах [2]. По данным эпидемиологических исследований, заболеваемость ГЭ достигает 133 случаев на 100 000 женщин-лет, при этом пик заболеваемости приходится на возраст 50–54 лет [1]. Среди женщин с аномальными маточными кровотечениями распространенность ГЭ составляет от 5 до 20,3% в зависимости от исследуемой популяции [3–5]. Особую тревогу вызывает тенденция к увеличению заболеваемости ГЭ, связанная с глобальным ростом распространенности факторов риска – ожирения, сахарного диабета и метаболического синдрома (МС) [2].
Патогенез ГЭ традиционно связывают с гиперэстрогенией на фоне относительного дефицита прогестерона, что обозначается термином «неопозированное действие эстрогенов» [1, 2]. Однако современные исследования убедительно демонстрируют ключевую роль инсулинорезистентности (ИР) и МС в развитии и прогрессировании пролиферативных заболеваний эндометрия [6, 7]. Гиперинсулинемия, характерная для ожирения и МС, оказывает прямое митогенное воздействие на эндометриальные клетки посредством активации инсулиновых рецепторов, запуская каскад фосфорилирования белков субстрата инсулинового рецептора (IRS) и последующую активацию сигнального пути PI3K/AKT [8]. Синергичное взаимодействие инсулиноподобного фактора роста 1 (IGF-1) и эстрогенов создает особо мощную митогенную среду, способствующую неконтролируемой пролиферации [8]. Кроме того, ИР снижает синтез глобулина, связывающего половые гормоны, что приводит к повышению биодоступности эстрогенов [9].
Хроническое низкоинтенсивное воспаление, ассоциированное с ожирением и ИР, играет существенную роль в патогенезе ГЭ [10]. Повышенные уровни провоспалительных цитокинов (интерлейкины – ИЛ-1β, ИЛ-6, фактор некроза опухоли α – ФНО-α, ИЛ-8, ИЛ-17) и сниженные уровни противовоспалительных медиаторов (ИЛ-4, ИЛ-10, ИЛ-13) формируют провоспалительный фенотип, способствующий пролиферации эндометрия и потенциально – его злокачественной трансформации [11, 12]. С-реактивный белок (СРБ), как маркер системного воспаления, также ассоциирован с повышенным риском развития ГЭ и рака эндометрия [10].
Стандартом консервативного лечения ГЭ без атипии является терапия гестагенами, демонстрирующая регрессию гиперпластических изменений у 70–90% пациенток [13]. Тем не менее существенной проблемой остается высокая частота рецидивов после достижения первичного ответа – до 23–40% в течение длительного наблюдения [14, 15]. По данным последних исследований, частота рецидивов через 12 мес после прекращения терапии может достигать 51,4%, при этом медиана времени до рецидива составляет 15 мес [16]. Ключевыми факторами риска рецидивирования являются ожирение (индекс массы тела – ИМТ≥27 кг/м²), ИР и МС [16, 17]. Исследование Х. Li и соавт. (2021 г.) продемонстрировало, что ИР увеличивает риск рецидива в 9,5 раза (отношение шансов – ОШ 9,5; 95% доверительный интервал – ДИ 3,3–27,0), а МС – в 4,9 раза (ОШ 4,9; 95% ДИ 1,5–15,5) [6]. Данные факты обосновывают необходимость комплексного подхода к терапии ГЭ с воздействием на метаболические нарушения.
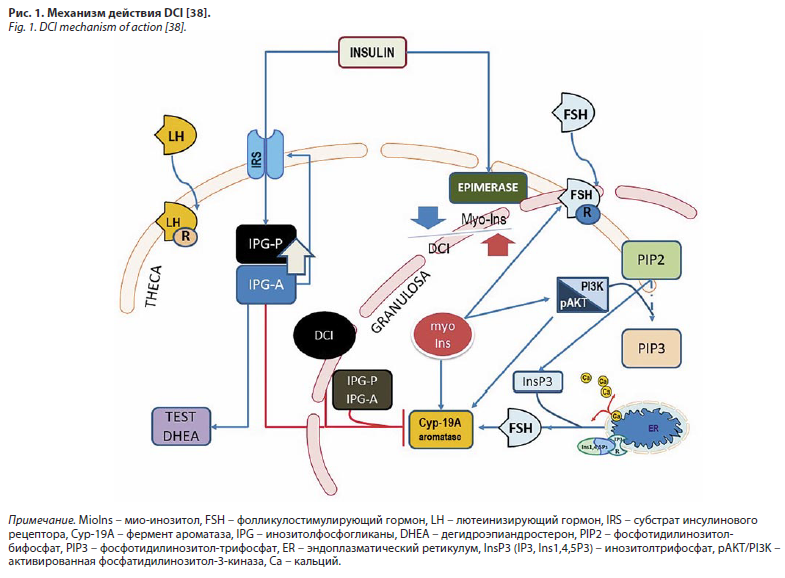
D-хиро-инозитол (D-chiro-inositol – DCI) представляет собой один из девяти стереоизомеров инозитола – циклического шестиуглеродного полиола, широко распространенного в живой природе [18]. DCI является критически важным вторичным мессенджером в сигнальном каскаде инсулина, участвуя в передаче внутриклеточного сигнала после связывания инсулина с рецептором [19]. При активации инсулинового рецептора происходит гидролиз гликозилфосфатидилинозитольных липидов клеточной мембраны с высвобождением инозитолфосфогликановых медиаторов, содержащих DCI и галактозамин, которые активируют ключевые ферменты, контролирующие окислительный и неокислительный метаболизм глюкозы (рис. 1) [20].
Дефицит DCI-содержащих инозитолфосфогликанов признан одним из механизмов развития ИР [21]. У женщин с синдромом поликистозных яичников (СПКЯ) и ИР выявлено трехкратное снижение высвобождения DCI-содержащих инозитолфосфогликанов в ответ на инсулиновую стимуляцию по сравнению со здоровыми женщинами [22]. Эпимеризация мио-инозитола в DCI, осуществляемая специфической эпимеразой, нарушена при сахарном диабете и инсулинорезистентных состояниях [23].
Клинические исследования убедительно подтверждают эффективность DCI в коррекции ИР и метаболических нарушений. В рандомизированном плацебо-контролируемом исследовании J. Nestler и соавт., опубликованном в «New England Journal of Medicine», применение DCI в дозе 1200 мг/сут в течение 6–8 нед у женщин с СПКЯ привело к значительному снижению площади под кривой инсулина (с 13 417±11 572 до 5158±6714 мкЕд/мл×мин; p=0,007) и уровня триглицеридов плазмы (p=0,002), а также повышению частоты овуляции с 27% в группе плацебо до 86% в группе DCI (p<0,001) [20].
DCI реализует свои эффекты через множественные механизмы: инсулиносенситизирующее действие, ингибирование транскрипции ароматазы, модуляцию трансдифференцировки белой жировой ткани в бурую [24]. Систематический обзор и метаанализ 14 рандомизированных контролируемых исследований (РКИ) продемонстрировал, что применение инозитолов у пациентов с метаболическими заболеваниями приводит к статистически значимому снижению уровня триглицеридов (СРС -1,24; 95% ДИ -1,84–-0,64; p<0,001), общего холестерина (СРС -1,09; 95% ДИ -1,83–-0,55; p<0,001) и холестерина липопротеинов низкой плотности – ЛПНП (СРС -1,31; 95% ДИ -2,04–-0,59; p<0,001) [25]. Комбинированная терапия мио-инозитолом и DCI в соотношении 40:1 улучшает показатели липидного профиля, снижает индекс HOMA-IR и уменьшает кардиоваскулярный риск у женщин с СПКЯ [26].
Помимо метаболических эффектов, инозитолы обладают противовоспалительными свойствами. Исследование S. Arefhosseini и соавт. (2023 г.) продемонстрировало, что мио-инозитол снижает экспрессию ФНО-α мРНК у пациентов с неалкогольной жировой болезнью печени [27]. В экспериментальных исследованиях инозитолгексафосфат подавляет экспрессию провоспалительных цитокинов ИЛ-1β и ИЛ-6, индуцированных липополисахаридом [28]. Mиo-инозитол уменьшает воспаление и окислительный стресс в эндотелиальных клетках, подвергшихся хронической гипергликемии, снижая адгезию моноцитов и экспозицию молекул адгезии [29].
Учитывая патогенетическую роль ИР, дислипидемии и хронического воспаления в развитии и рецидивировании ГЭ, а также доказанную эффективность DCI в коррекции данных нарушений, представляется обоснованным изучение возможности применения DCI в составе комплексной терапии ГЭ без атипии. Потенциальное воздействие DCI на множественные патогенетические звенья заболевания может повысить эффективность стандартной гестагенотерапии и снизить риск рецидивирования.
Цель исследования – повысить результативность комплексной терапии ГЭ без атипии с использованием DCI.
Материалы и методы
Настоящее двойное слепое проспективное рандомизированное плацебо-контролируемое исследование было проведено на клинических базах кафедры акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН (заведующий кафедрой – академик РАН, профессор В.Е. Радзинский). Общая продолжительность исследования составила 13 мес: период скрининга – 2 нед, период лечения – 6 мес, период наблюдения после лечения – 6 мес.
Критерии включения:
• возраст 15–49 лет;
• гистологически подтвержденный диагноз ГЭ без атипии;
• индекс массы тела (ИМТ) 24,95–35 кг/м²;
• отсутствие гормональной терапии в течение 3 мес до включения в исследование;
• подписанное информированное согласие.
Критерии исключения:
• атипическая гиперплазия и карцинома эндометрия;
• злокачественные новообразования любой локализации в анамнезе;
• тяжелые соматические заболевания (печеночная, почечная недостаточность, неконтролируемая артериальная гипертензия, сахарный диабет);
• беременность или период лактации;
• острые воспалительные заболевания органов малого таза;
• наличие противопоказаний к приему гестагенов.
В настоящее исследование были включены 60 пациенток, стратифицированных методом слепой рандомизации в две группы. Группа 1 (n=30) получала норэтистерона ацетат в непрерывном режиме + DCI 1200 мг/сут ежедневно в течение 6 мес. Группа 2 (n=30) получала норэтистерона ацетат в непрерывном режиме + плацебо ежедневно в течение 6 мес. В обеих группах пациентки получили информацию по модификации образа жизни согласно действующим клиническим рекомендациям (физические нагрузки и рациональное сбалансированное питание, снижение калоража на 30% для достижения и поддержания нормальной массы тела; физическая активность должна составлять минимум 150 мин/нед, включая упражнения на укрепление мышц в течение 2 дней в неделю).
Антропометрическое обследование включало измерение роста (м) с помощью ростомера и массы тела (кг) на медицинских весах. ИМТ рассчитывали по формуле: масса тела (кг)/рост² (м²).
Всем пациенткам выполнялись:
• стандартное ультразвуковое исследование (УЗИ) органов малого таза с измерением М-эхо на аппарате Voluson E10 (GE Healthcare, США) с использованием трансвагинального датчика частотой 5–9 МГц;
• гистероскопия с прицельной биопсией эндометрия, гистологическое исследование биоптатов эндометрия;
• иммуногистохимическое (ИГХ) исследование с определением экспрессии Ki-67, VEGF, p53;
• иммуноферментный анализ для определения уровней цитокинов в сыворотке крови (ИЛ-4, ИЛ-13, ИЛ-25, ИЛ-37, ИЛ-1β, ФНО-α, ИЛ-8, ИЛ-17);
• биохимический анализ крови (липидный профиль, СРБ, индекс HOMA-IR);
• антропометрия.
Все гистероскопии выполнялись с использованием линзового мини-эндоскопа 2,7 мм с углом обзора 105°, оснащенного двухканальным рабочим зондом 4,5 мм внешнего диаметра (Karl Storz, Германия). Для расширения полости матки использовался физиологический раствор, подаваемый под давлением от системы капельного вливания с высотой подвеса мешка 1 м над уровнем пациентки. Источник света – ксеноновая лампа мощностью 300 Вт, цифровая видеокамера высокого разрешения (Karl Storz). Во время процедуры тщательно осматривались как передняя, так и задняя стенки матки путем продольного проведения гистероскопа вдоль поверхности эндометрия для выявления любых поверхностных изменений.
Полученные образцы биопсии фиксировали в 10% фосфатном буфере с формалином, после чего подвергали гистологической обработке в автоматическом гистопроцессоре Leica ASP 30 (Германия). Далее образцы заливали в парафин на станции Leica EG 1150 (Германия). Срезы толщиной 4 мкм окрашивали гематоксилином и эозином с помощью окрасочной станции Leica ST 5010 (Германия). Микроскопическое исследование препаратов выполняли с использованием микроскопа Leica DMLB и цифровой камеры Leica DFC 420 (Германия). Проводилась патоморфологическая оценка состояния эндометрия в полученных микропрепаратах. Выполняли ИГХ-анализ эндометрия с использованием антител к Ki-67, VEGF, p53. ИГХ-окрашивание выполняли на приборах Ventana BenchMark Ultra IHdSH (США) и Bond-Max (Германия) с использованием системы визуализации Ultra Vision TL-015-HD Lab Vision. Экспрессию изучаемых маркеров анализировали в трех неперекрывающихся полях зрения при увеличении ×400, используя микроскоп Leica DMLB с цифровой камерой Leica DFC 420 (Германия).
Полным морфологическим регрессом считали отсутствие признаков ГЭ по данным гистологического исследования биоптата (нормальный пролиферативный или секреторный эндометрий). Частичным регрессом считали уменьшение степени выраженности гиперпластических изменений/наличие очаговой гиперплазии. Рецидивом ГЭ считали повторное выявление гистологических признаков гиперплазии после ранее достигнутого полного регресса.
Забор венозной крови для биохимического исследования проводился из локтевой вены строго натощак (не менее 12 ч голодания) в утренние часы с использованием вакуумных систем. Определение показателей липидного профиля (ЛПНП, липопротеины высокой плотности – ЛПВП, триглицериды), глюкозы, инсулина, СРБ выполнялось на автоматическом биохимическом анализаторе с расчетом индекса ИР HOMA-IR по формуле: глюкоза натощак (ммоль/л) × инсулин натощак (мкЕд/мл) / 22,5. Определение показателей липидного профиля (общий холестерин, ЛПНП, ЛПВП, триглицериды), глюкозы и СРБ выполнялось на автоматическом биохимическом анализаторе Cobas c311 (Roche Diagnostics, Швейцария); определение инсулина – на иммунохимическом анализаторе Cobas e411 (Roche Diagnostics, Швейцария) методом электрохемилюминесценции.
Уровни цитокинов определяли в периферической крови натощак: ИЛ-4, ИЛ-13, ИЛ-25, ИЛ-37, ИЛ-1β, ФНО-α, ИЛ-8, ИЛ-17 с помощью метода проточной цитофлуорометрии с использованием тест-систем BD Cytometric Bead Array (BD, США) и проточного цитофлуорометра FACStrack (BD, США).
В качестве референсных использовали следующие значения: индекс пролиферации Ki-67<10%, экспрессия VEGF<2,0 у.е., индекс HOMA-IR<2,5. Референсные значения цитокинов: ИЛ-4 2,0–4,0 пг/мл, ИЛ-13 3,0–5,0 пг/мл, ИЛ-25 35–60 пг/мл, ИЛ-37 80–150 пг/мл; для провоспалительных цитокинов: ИЛ-1β<5,0 пг/мл, ФНО-α<8,0 пг/мл, ИЛ-8<15 пг/мл, ИЛ-17<10 пг/мл.
Визиты осуществлялись исходно (В1), через 6 мес терапии (В2) и через 12 мес от начала исследования (В3).
Первичные конечные точки:
• частота морфологического регресса ГЭ через 6 мес терапии (по данным биопсии эндометрия);
• частота рецидива ГЭ в течение 6 мес после окончания лечения.
Вторичные конечные точки:
• динамика толщины эндометрия по данным УЗИ;
• динамика ИГХ-маркеров (Ki-67, VEGF, p53);
• динамика уровней про- и противовоспалительных цитокинов;
• динамика метаболических параметров (индекс HOMA-IR, липидный профиль, СРБ);
• изменение массы тела и ИМТ.
Статистическая обработка данных проводилась с использованием программы Statistica 10.0 (StatSoft Inc., США). Количественные данные представлены в виде M±SD (среднее ± стандартное отклонение) и медианы с интерквартильным размахом. Для сравнения количественных показателей использовался t-критерий Стьюдента или критерий Манна–Уитни в зависимости от характера распределения. Сравнение качественных показателей проводилось с помощью критерия χ². Статистически значимыми считались различия при p<0,05.
Протокол исследования был одобрен локальным этическим комитетом. Все участницы подписали информированное согласие до включения в исследование.
Конфиденциальность данных участниц обеспечивалась присвоением уникальных идентификационных номеров. Все данные хранились в защищенной электронной базе данных с ограниченным доступом. Участницы имели право выйти из исследования в любое время без объяснения причин.
Результаты
В ходе настоящего исследования группы были сопоставимы по основным демографическим и клиническим характеристикам (p≥0,05). Медиана возраста пациенток, принимавших гестаген + DCI, составила 37 лет (диапазон 32–42 года), пациенток, получавших гестаген + плацебо, – 38 лет (диапазон 31–43 года). Антропометрический анализ выявил, что средний ИМТ составил 30,4±2,3 кг/м² и 30,6±1,6 кг/м² соответственно (p=0,78). Исходная толщина эндометрия по данным УЗИ составила 15,6±2,5 мм у пациенток, получавших гестаген + DCI, и 16,1±2,0 мм у пациенток, принимавших гестаген + плацебо (p=0,46).
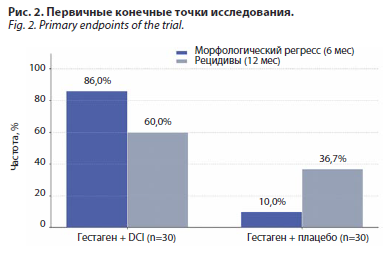
Частота морфологического регресса ГЭ через 6 мес терапии была достоверно выше у пациенток, получавших гестаген + DCI: полный регресс достигнут у 26 (86,7%) из 30 пациенток по сравнению с 18 (60,0%) из 30 у пациенток, принимавших гестаген + плацебо, что соответствует увеличению эффективности в 1,4 раза (χ²=5,46; p=0,020; рис. 2). При оценке частоты рецидивов через 6 мес после окончания терапии рецидив ГЭ зарегистрирован у 3 (10,0%) из 30 пациенток, получавших гестаген + DCI, и у 11 (36,7%) из 30 пациенток, принимавших гестаген + плацебо, что свидетельствует о снижении риска рецидивирования в 3,7 раза на фоне применения DCI (χ²=5,97; p=0,015).
 Динамика толщины эндометрия в ходе настоящего исследования по данным трансвагинального УЗИ представлена в табл. 1. В обеих группах отмечено статистически значимое уменьшение толщины эндометрия на фоне терапии, однако у пациенток, получавших гестаген + DCI, снижение было более выраженным.
Динамика толщины эндометрия в ходе настоящего исследования по данным трансвагинального УЗИ представлена в табл. 1. В обеих группах отмечено статистически значимое уменьшение толщины эндометрия на фоне терапии, однако у пациенток, получавших гестаген + DCI, снижение было более выраженным.
К визиту В3 толщина эндометрия у пациенток, получавших гестаген + DCI, составила 8,5±2,6 мм, у пациенток, принимавших гестаген + плацебо, – 11,4±2,9 мм, что соответствует уменьшению показателя в 1,3 раза по сравнению с плацебо (p<0,001; см. табл. 1).
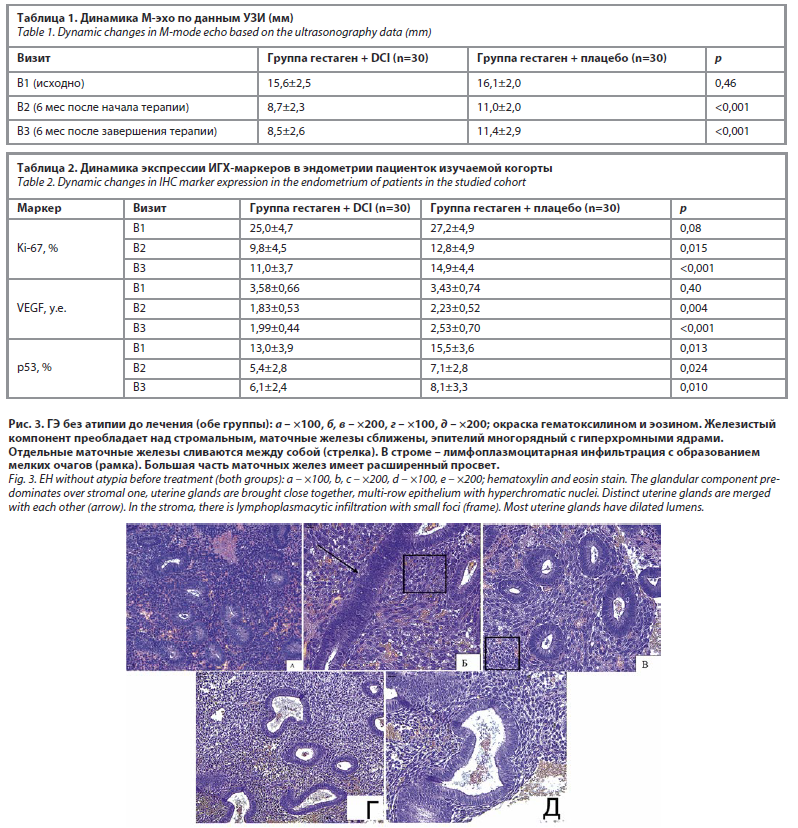
Динамика ИГХ-маркеров представлена в табл. 2. Исходно группы не различались по уровню экспрессии Ki-67 (25,0±4,7% vs 27,2±4,9%; p=0,08). К визиту В2 отмечено снижение индекса Ki-67 в обеих группах, однако у пациенток, получавших гестаген + DCI, показатель достиг референсных значений нормы (9,8±4,5% при норме <10%), тогда как у пациенток, принимавших гестаген + плацебо, оставался незначительно повышенным (12,8±4,9%), что в 1,3 раза выше, чем в группе комбинированной терапии (p=0,015). К визиту В3 различия сохранялись: 11,0±3,7% vs 14,9±4,4%, индекс пролиферации у пациенток, получавших гестаген + плацебо, превышал таковой у пациенток, принимавших гестаген + DCI, в 1,4 раза (p<0,001).
 Экспрессия VEGF исходно была повышена в обеих группах (3,58±0,66 и 3,43±0,74 у.е. при норме <2,0).
Экспрессия VEGF исходно была повышена в обеих группах (3,58±0,66 и 3,43±0,74 у.е. при норме <2,0).
У пациенток, получавших гестаген + DCI, к визиту В2 отмечена нормализация показателя (1,83±0,53 у.е.), тогда как у пациенток, принимавших гестаген + плацебо, экспрессия VEGF оставалась на верхней границе нормы (2,23±0,52 у.е.), превышая значения у пациенток, получавших гестаген + DCI, в 1,2 раза (p=0,004; см. табл. 2).
Аналогичная тенденция прослеживалась для маркера p53 (см. табл. 2).
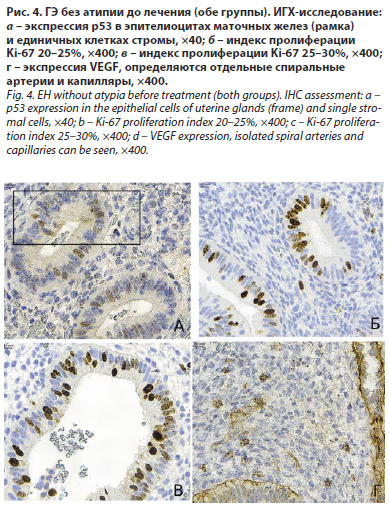
Исходная морфологическая картина ГЭ без атипии в обеих группах характеризовалась преобладанием железистого компонента над стромальным со сближением маточных желез, формированием многорядного железистого эпителия с гиперхромными ядрами и единичными фигурами митоза при сохранной базальной мембране (рис. 3).
В отдельных случаях наблюдалось слияние маточных желез между собой. В строме эндометрия определялась умеренная рассеянная лимфоплазмоцитарная инфильтрация с образованием мелких очагов. Большая часть маточных желез имела расширенный просвет. ИГХ-исследование выявило ядерную экспрессию p53 в эпителиоцитах маточных желез и единичных клетках стромы, индекс пролиферации Ki-67 составлял 20–30%, при оценке VEGF определялись отдельные спиральные артерии и капилляры (рис. 4).
После терапии морфологическая картина эндометрия существенно различалась между группами. Среди пациенток, получавших гестаген + DCI, у большинства (86,7%) достигнут полный морфологический регресс: эндометрий соответствовал средней стадии фазы пролиферации, маточные железы с признаками гиперплазии не выявлялись (рис. 5).
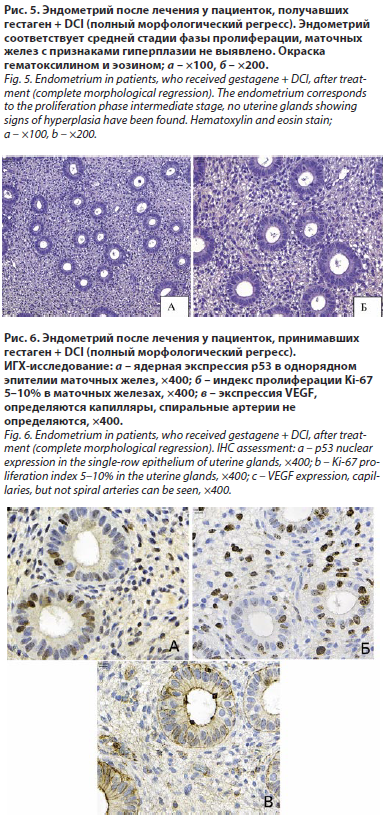 Иммуногистохимически отмечалась ядерная экспрессия p53 в однорядном эпителии маточных желез, индекс пролиферации Ki-67 составлял 5–10%, при оценке VEGF определялись только капилляры, спиральные артерии не определялись (рис. 6).
Иммуногистохимически отмечалась ядерная экспрессия p53 в однорядном эпителии маточных желез, индекс пролиферации Ki-67 составлял 5–10%, при оценке VEGF определялись только капилляры, спиральные артерии не определялись (рис. 6).
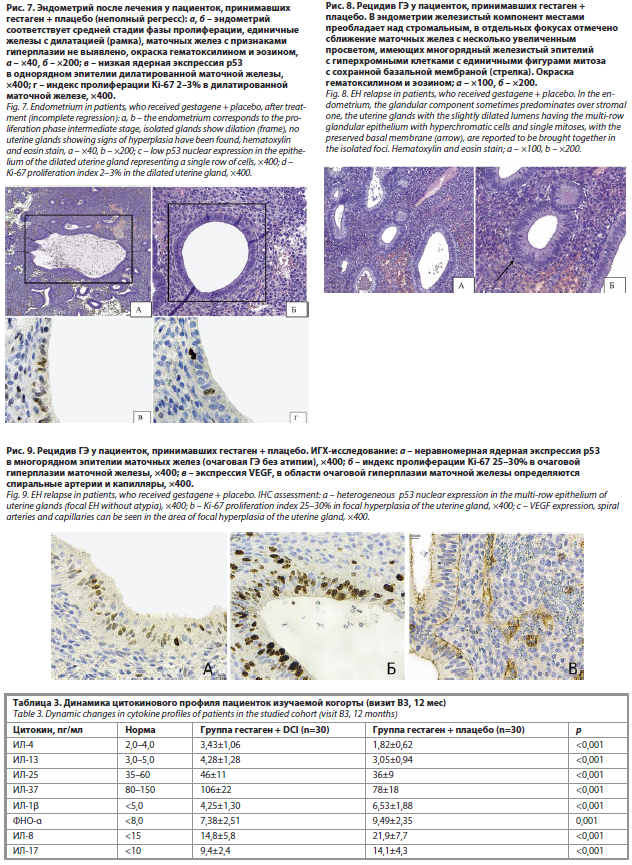
У пациенток, получавших гестаген + плацебо, полный морфологический регресс был достигнут лишь у 60,0%. У 40% пациенток данной группы в биоптатах эндометрия сохранялись единичные железы с дилатацией просвета (рис. 7, а, б) с низкой ядерной экспрессией p53 и минимальным индексом пролиферации Ki-67 2–3% в дилатированных железах, что свидетельствует о неполном морфологическом регрессе ГЭ (рис. 7, в, г).
При рецидиве ГЭ, который среди пациенток, принимавших гестаген + плацебо, регистрировался в 3,7 раза чаще (36,7% против 10,0%), в отдельных фокусах отмечалось сближение маточных желез с увеличенным просветом, имеющих многорядный железистый эпителий с гиперхромными клетками и единичными фигурами митоза при сохранной базальной мембране (рис. 8).
Иммуногистохимически в зонах очаговой гиперплазии выявлялась неравномерная ядерная экспрессия p53, индекс пролиферации Ki-67 достигал 25–30%, определялись спиральные артерии и капилляры (рис. 9).
Исходно в обеих группах отмечался дисбаланс цитокинового профиля: достоверное (p<0,05) снижение уровней противовоспалительных цитокинов (ИЛ-4, ИЛ-13, ИЛ-25, ИЛ-37 ниже референсных значений) и повышение провоспалительных цитокинов (ИЛ-1β, ФНО-α, ИЛ-8, ИЛ-17 выше нормы, табл. 3).
У пациенток, получивших DCI в составе комплексной терапии, к визиту В3 отмечена регуляция/нормализация уровней противовоспалительных цитокинов: ИЛ-4 достиг 3,43±1,06 пг/мл (норма 2,0–4,0 пг/мл), ИЛ-13 – 4,28±1,28 пг/мл (3,0–5,0 пг/мл), ИЛ-25 – 46±11 пг/мл (35–60 пг/мл), ИЛ-37 – 106±22 пг/мл (80–150 пг/мл).
У пациенток, принимавших гестаген + плацебо, показатели оставались ниже нормы (см. табл. 3).
Аналогичная динамика прослеживалась для провоспалительных цитокинов. У пациенток, получавших гестаген + DCI, к визиту В3 отмечено снижение ИЛ-1β до 4,25±1,30 пг/мл (норма <5,0 пг/мл), ФНО-α – до 7,38±2,51 пг/мл (<8,0 пг/мл), ИЛ-8 – до 14,8±5,8 пг/мл (<15), ИЛ-17 – до 9,4±2,4 пг/мл (<10 пг/мл). У пациенток, принимавших гестаген + плацебо, провоспалительные цитокины оставались повышенными, различия между группами были статистически значимы (p<0,001).
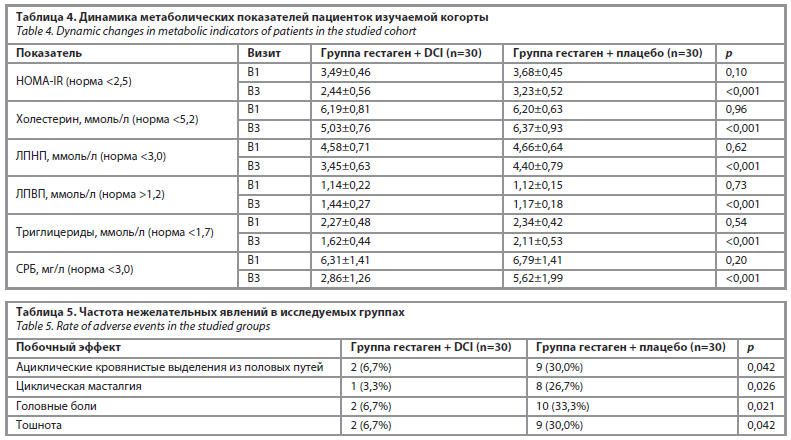
Исходно в обеих группах выявлены признаки ИР и дислипидемии (табл. 4). Индекс HOMA-IR превышал 2,5 у всех пациенток (3,49±0,46 и 3,68±0,45 у пациенток, получавших гестаген + DCI и гестаген + плацебо соответственно). У пациенток, принимавших гестаген + DCI, к визиту В3 отмечена нормализация индекса HOMA-IR (2,44±0,56 при норме <2,5), тогда как у пациенток, получавших гестаген + плацебо, показатель оставался повышенным (3,23±0,52; см. табл. 4), превышая значения в группе комбинированной терапии в 1,3 раза (p<0,001).
Терапия DCI привела к значимому улучшению липидного профиля: снижению общего холестерина с 6,19±0,81 до 5,03±0,76 ммоль/л (в 1,2 раза), ЛПНП – с 4,58±0,71 до 3,45±0,63 ммоль/л (в 1,3 раза), триглицеридов – с 2,27±0,48 до 1,62±0,44 ммоль/л (в 1,4 раза), а также повышению ЛПВП с 1,14±0,22 до 1,44±0,27 ммоль/л (в 1,3 раза). У пациенток, получавших гестаген + плацебо, показатели липидного профиля практически не изменились.
Уровень СРБ у пациенток, принимавших гестаген + DCI, снизился с 6,31±1,41 до 2,86±1,26 мг/л (в 2,2 раза; норма <3,0 мг/л), у пациенток, принимавших гестаген + плацебо, – с 6,79±1,41 до 5,62±1,99 мг/л (в 1,2 раза), при этом конечные значения у пациенток, получавших гестаген + плацебо, были в 2,0 раза выше, чем у пациенток, получавших гестаген + DCI (p<0,001). ИМТ у пациенток, получавших гестаген + DCI, снизился с 30,4±2,3 до 28,9±2,4 кг/м², тогда как у пациенток, получавших гестаген + плацебо, оставался стабильным (30,6±1,6 → 30,8±2,1 кг/м²; p=0,002).
Анализ безопасности продемонстрировал статистически значимо меньшую частоту нежелательных явлений у пациенток, принимавших гестаген + DCI, по сравнению с принимавшими гестаген + плацебо (табл. 5).
Ациклические кровянистые выделения из половых путей у пациенток, получавших гестаген + плацебо, регистрировались в 4,5 раза чаще, чем у пациенток, принимавших гестаген + DCI (p=0,042). Циклическая масталгия отмечалась в 8 раз чаще у пациенток, принимавших гестаген + плацебо (p=0,026). Головные боли наблюдались в 5 раз чаще у пациенток, получавших гестаген + плацебо (p=0,021). Тошнота фиксировалась в 4,5 раза чаще у пациенток, принимавших гестаген + плацебо (p=0,042). Серьезных нежелательных явлений, потребовавших отмены терапии, в обеих группах зарегистрировано не было.
Обсуждение
В настоящее время продолжается поиск новых технологий с целью повышения результативности лечения ГЭ без атипии. Несмотря на достаточно высокую результативность стандартной терапии с использованием гестагенов, частота рецидивов, к сожалению, не меняется, что диктует необходимость научного обоснования использования новых методов терапии ГЭ без атипии.
Результаты рандомизированного плацебо-контролируемого исследования продемонстрировали значительное повышение эффективности терапии ГЭ без атипии при добавлении DCI к стандартной гестагенотерапии. Частота достижения полного морфологического регресса в группе комбинированной терапии составила 86,7%, что статистически значимо превышает показатель группы плацебо (60,0%; p=0,020) и соответствует верхней границе эффективности гестагенотерапии, описанной в международных рекомендациях и систематических обзорах (70–90%) [13, 30].
Полученные нами данные об эффективности монотерапии гестагенами согласуются с результатами крупного метаанализа I. Gallos и соавт., в котором частота регресса ГЭ при применении оральных гестагенов составила около 70% [31]. Согласно рекомендациям Королевского колледжа акушеров и гинекологов (RCOG), стандартная терапия гестагенами обеспечивает регресс гиперплазии у большинства пациенток, однако частота рецидивов остается существенной проблемой [13]. В нашем исследовании добавление DCI позволило не только повысить частоту первичного ответа, но и значительно снизить частоту рецидивирования – с 36,7% до 10,0% (снижение в 3,7 раза; p=0,015).
Высокая частота рецидивов ГЭ после успешной консервативной терапии является одной из ключевых нерешенных проблем современной гинекологии. По данным систематических обзоров, частота рецидивов после достижения первичной ремиссии достигает 23–40% при длительном наблюдении [14], а в отдельных исследованиях – до 51,4% через 12 мес после прекращения терапии [16]. Результаты нашего исследования демонстрируют, что DCI может существенно снижать риск рецидивирования, что имеет важное клиническое значение для долгосрочного ведения пациенток с ГЭ.
Патогенетическое обоснование назначения DCI при ГЭ базируется на современном понимании роли метаболических нарушений в развитии и прогрессировании пролиферативных заболеваний эндометрия. Исследование Х. Li и соавт. убедительно продемонстрировало, что ИР увеличивает риск рецидива атипической ГЭ в 9,5 раза (ОШ 9,5; 95% ДИ 3,3–27,0), а МС – в 4,9 раза (ОШ 4,9; 95% ДИ 1,5–15,5) [6]. Аналогичные данные получены Y. Wu и соавт. (2025 г.), показавшими, что комбинация МС и ИР обладает высокой прогностической ценностью для оценки риска рецидива (AUC=0,818) [32]. Эти данные подчеркивают важность коррекции метаболических нарушений в комплексной терапии ГЭ.
В нашем исследовании применение DCI привело к нормализации индекса HOMA-IR (с 3,49±0,46 до 2,44±0,56 при норме <2,5), тогда как в группе плацебо показатель оставался повышенным (3,23±0,52). Эти результаты согласуются с данными систематического обзора и метаанализа В. Pintaudi и соавт., включавшего 20 РКИ с участием 1239 пациентов, который продемонстрировал статистически значимое снижение HOMA-IR (MD -1,96 ммоль × мкЕд/мл; 95% ДИ -2,62–-1,30) на фоне приема инозитолов [33]. Рандомизированное исследование J. Nestler и соавт., опубликованное в «New England Journal of Medicine», показало, что DCI в дозе 1200 мг/сут приводит к значительному снижению площади под кривой инсулина у женщин с СПКЯ (с 13 417±11 572 до 5158±6714 мкЕд/мл × мин; p=0,007) [20]. Недавнее исследование М. Montt-Guevara и соавт. (2021 г.) подтвердило, что DCI регулирует передачу инсулинового сигнала в адипоцитах человека, что объясняет механизм его инсулиносенситизирующего действия [19].
Помимо коррекции ИР DCI продемонстрировал благоприятное влияние на липидный профиль. В нашем исследовании отмечено статистически значимое снижение общего холестерина (с 6,19±0,81 до 5,03±0,76 ммоль/л), ЛПНП (с 4,58±0,71 до 3,45±0,63 ммоль/л), триглицеридов (с 2,27±0,48 до 1,62±0,44 ммоль/л) и повышение ЛПВП (с 1,14±0,22 до 1,44±0,27 ммоль/л). Эти данные подтверждаются результатами метаанализа R. Tabrizi и соавт., включавшего 14 РКИ, который продемонстрировал значимое снижение триглицеридов (СРС -1,24; 95% ДИ -1,84–-0,64; p<0,001), общего холестерина (СРС -1,09; 95% ДИ -1,83–-0,55; p<0,001) и ЛПНП (СРС -1,31; 95% ДИ -2,04–-0,59; p<0,001) при применении инозитолов у пациентов с метаболическими заболеваниями [25]. Комбинированная терапия мио-инозитолом и DCI, по данным М. Minozzi и соавт., улучшает показатели липидного профиля и снижает кардиоваскулярный риск у женщин с СПКЯ [26].
Важным аспектом патогенеза ГЭ является хроническое низкоинтенсивное воспаление. Исследование А. Kubyshkin и соавт. продемонстрировало, что уровни провоспалительных цитокинов ИЛ-1β, ИЛ-6 и ФНО-α прогрессивно возрастают по мере усиления тяжести ГЭ, что свидетельствует о ключевой роли воспалительных процессов в прогрессировании патологии [34]. В нашем исследовании на фоне применения DCI отмечена нормализация как провоспалительных (ИЛ-1β, ФНО-α, ИЛ-8, ИЛ-17), так и противовоспалительных цитокинов (ИЛ-4, ИЛ-13, ИЛ-25, ИЛ-37). Противовоспалительные свойства инозитолов подтверждены экспериментальными исследованиями Y. Wee и соавт., показавшими, что инозитолгексафосфат подавляет экспрессию провоспалительных цитокинов ИЛ-1β и ИЛ-6, индуцированных липополисахаридом [28]. M. Baldassarre и соавт. продемонстрировали, что мио-инозитол уменьшает воспаление и окислительный стресс в эндотелиальных клетках, подвергшихся хронической гипергликемии [29].
Снижение уровня СРБ с 6,31±1,41 до 2,86±1,26 мг/л (в 2,2 раза) в группе DCI также свидетельствует об уменьшении системного воспаления, что имеет важное значение с учетом связи СРБ с повышенным риском развития ГЭ и рака эндометрия [10]. P. Huang и соавт. показали, что хроническое воспаление, ассоциированное с ожирением, способствует метаболическому репрограммированию глюкозы в эндометрии, создавая условия для пролиферации и злокачественной трансформации [10].
Динамика ИГХ-маркеров в нашем исследовании отражает воздействие DCI на ключевые патогенетические звенья ГЭ. Снижение индекса пролиферации Ki-67 до референсных значений (9,8±4,5% при норме <10%) в группе комбинированной терапии свидетельствует о подавлении избыточной пролиферативной активности эндометрия. Нормализация экспрессии VEGF (1,83±0,53 у.е.) указывает на уменьшение патологического ангиогенеза, который играет существенную роль в прогрессировании гиперпластических процессов эндометрия [8]. Снижение экспрессии p53 в эпителиоцитах маточных желез отражает уменьшение клеточного стресса и восстановление нормальной клеточной регуляции.
Сравнительный анализ с другими подходами к адъювантной терапии ГЭ представляет значительный интерес. Добавление метформина к гестагенотерапии исследовалось в ряде РКИ и метаанализов. Согласно систематическому обзору R. Shao и соавт., комбинированная терапия гестагенами и метформином улучшает частоту полного ответа (ОШ 2,08; 95% ДИ 1,29–3,34; p=0,003) по сравнению с монотерапией гестагенами [35]. Однако влияние метформина на частоту рецидивов остается неоднозначным. В метаанализе J. Chae-Kim и соавт. добавление метформина снижало частоту рецидивов (ОШ 0,46; 95% ДИ 0,24–0,91; p=0,03), но не влияло на частоту ремиссий [36]. Двойное слепое плацебо-контролируемое исследование A. Tehranian и соавт. продемонстрировало, что добавление метформина к мегестролу ацетату повышает частоту ответа с 70,4 до 93,1% при ГЭ без атипии [37]. Наши результаты (86,7% vs 60,0% полного регресса; 10,0% vs 36,7% рецидивов) сопоставимы с эффективностью комбинации гестаген + метформин, что позволяет рассматривать DCI как перспективную альтернативу для адъювантной терапии ГЭ.
Преимуществом DCI является его благоприятный профиль безопасности. В нашем исследовании частота нежелательных явлений была статистически значимо ниже в группе комбинированной терапии: ациклические кровянистые выделения (6,7% vs 30,0%; p=0,042), циклическая масталгия (3,3% vs 26,7%; p=0,026), головные боли (6,7% vs 33,3%; p=0,021), тошнота (6,7% vs 30,0%; p=0,042). Данные результаты согласуются с литературными данными об отличной переносимости инозитолов. Согласно консенсусу экспертной группы EGOI (Experts Group on Inositol in Basic and Clinical Research), инозитолы демонстрируют превосходный профиль безопасности по сравнению с другими инсулиносенситизирующими препаратами, такими как метформин, для которого характерны гастроинтестинальные побочные эффекты [24].
Снижение частоты побочных эффектов гестагенотерапии на фоне приема DCI может объясняться несколькими механизмами. Во-первых, улучшение метаболического профиля и снижение массы тела (ИМТ снизился с 30,4±2,3 до 28,9±2,4 кг/м² в группе DCI) могут способствовать лучшей переносимости гормональной терапии. Во-вторых, противовоспалительное действие DCI может уменьшать выраженность системных побочных эффектов. В-третьих, стабилизация гормонального фона на фоне коррекции ИР может снижать риск ациклических кровотечений и масталгии.
Результаты нашего исследования вносят вклад в развитие концепции мультитаргетной терапии ГЭ, направленной на одновременное воздействие на несколько патогенетических звеньев заболевания. DCI, обладая инсулиносенситизирующим, гиполипидемическим и противовоспалительным действием, воздействует на ключевые метаболические нарушения, лежащие в основе развития и рецидивирования ГЭ. Данный подход соответствует современным тенденциям в онкопрофилактике, подчеркивающим важность коррекции модифицируемых факторов риска [5].
Заключение
Результаты рандомизированного плацебо-контролируемого исследования свидетельствуют о том, что добавление DCI в дозе 1200 мг/сут к стандартной терапии норэтистерона ацетатом значительно повышает эффективность лечения ГЭ без атипии у женщин с избыточной массой тела и ожирением. Комбинированная терапия обеспечивает более высокую частоту полного морфологического регресса (86,7% vs 60,0%) и существенное снижение риска рецидивирования (10,0% vs 36,7%) по сравнению с монотерапией гестагенами. Механизм действия DCI реализуется через коррекцию ИР, нормализацию липидного профиля и цитокинового баланса, что приводит к снижению пролиферативной активности и патологического ангиогенеза в эндометрии. Благоприятный профиль безопасности и снижение частоты побочных эффектов гестагенотерапии позволяют рекомендовать DCI в качестве патогенетически обоснованного компонента комплексной терапии ГЭ без атипии у женщин с метаболическими нарушениями.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Радзинский Виктор Евсеевич – акад. РАН, д-р мед. наук, проф., зав. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН, засл. деят. науки РФ. E-mail: radzinskiy@mail.ru; ORCID: 0000-0002-7428-0469
Viktor E. Radzinskiy – Acad. RAS, Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: radzinskiy@mail.ru; ORCID: 0000-0002-7428-0469
Михалева Людмила Михайловна – чл.-кор. РАН, д-р мед. наук, проф., дир. НИИМЧ им. акад. А.П. Авцына ФГБНУ «РНЦХ им. акад. Б.В. Петровского», засл. деят. науки РФ.
E-mail: mikhalevam@yandex.ru; ORCID: 0000-0003-2052-914X; SPIN-код: 2086-7513
Liudmila M. Mikhaleva – Corr. Memb. RAS, Dr. Sci. (Med.), Professor, Director of Avtsyn Research Institute of Human Morphology of Petrovsky National Research Centre of Surgery. E-mail: mikhalevam@yandex.ru; ORCID: 0000-0003-2052-914X; SPIN code: 2086-7513
Хамошина Марина Борисовна – д-р мед. наук, проф., проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН, засл. деят. науки РФ.
E-mail: khamoshina@mail.ru; ORCID: 0000-0003-1940-4534
Marina B. Khamoshina – Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: khamoshina@mail.ru; ORCID: 0000-0003-1940-4534
Костин Игорь Николаевич – д-р мед. наук, проф., проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: bigbee62@mail.ru
Igor N. Kostin – Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: bigbee62@mail.ru
Оразов Мекан Рахимбердыевич – д-р мед. наук, проф., проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: omekan@mail.ru; ORCID: 0000-0002-5342-8129
Mekan R. Orazov – Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: omekan@mail.ru; ORCID: 0000-0002-5342-8129
Орехов Роман Евгеньевич – канд. мед. наук, доц. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: romanorekhovv@ya.ru
Roman E. Orekhov – Cand. Sci. (Med.), Associate Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: romanorekhovv@ya.ru
Ахматова Анастасия Николаевна – канд. мед. наук, доц. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: achmatova02@mail.ru
Anastasiia N. Akhmatova – Cand. Sci. (Med.), Associate Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: achmatova02@mail.ru
Муллина Ирина Александровна – канд. мед. наук, врач акушер-гинеколог гинекологического отд-ния ЧУЗ «КБ "РЖД-Медицина" им. Н.А. Семашко». E-mail: 211irina2111@gmail.com
Irina A. Mullina – Cand. Sci. (Med.), Semashko Clinical Hospital “Russian Railways-Medicine”.
E-mail: 211irina2111@gmail.com
Поступила в редакцию: 19.01.2026
Поступила после рецензирования: 20.01.2026
Принята к публикации: 22.01.2026
Received: 19.01.2026
Revised: 20.01.2026
Accepted: 22.01.2026
Клинический разбор в общей медицине №02 2026
D-хиро-инозитол в комплексной терапии гиперплазии эндометрия без атипии: результаты двойного слепого рандомизированного плацебо-контролируемого исследования
Номера страниц в выпуске:24-36
Аннотация
Цель. Повысить результативность комплексной терапии гиперплазии эндометрия (ГЭ) без атипии с использованием D-хиро-инозитола (D-chiro-inositol – DCI).
Материалы и методы. В настоящее двойное слепое проспективное рандомизированное плацебо-контролируемое исследование были включены 60 пациенток с морфологически верифицированным диагнозом «ГЭ без атипии». В ходе исследования участницы были стратифицированны на две группы: 1-я (n=30) получала норэтистерона ацетат в непрерывном режиме согласно действующей инструкции и DCI 1200 мг/сут, 2-я (n=30) – норэтистерона ацетат + плацебо. Длительность терапии составила 6 мес с последующим наблюдением в течение 6 мес. Оценивались частота достижения морфологического регресса и рецидивов, динамика иммуногистохимических маркеров (Ki-67, VEGF, p53), цитокинового профиля и метаболических параметров, профиль безопасности.
Результаты. В ходе исследования было установлено, что частота достижения полного морфологического регресса ГЭ без атипии через 6 мес терапии у пациенток, получавших гестаген + DCI, составила 86,7% по сравнению с 60,0% у пациенток, принимавших гестаген + плацебо (в 1,4 раза выше; p=0,020). Вместе с тем анализ частоты рецидивирующего течения ГЭ без атипии через 6 мес после окончания лечения продемонстрировал более высокую результативность у пациенток после комплексной терапии (в 3,7 раза ниже, 10,0% vs 36,7%; p=0,015). Анализ результатов сонографического исследования толщины эндометрия после лечения показал М-эхо 8,5±2,6 мм у пациенток, принимавших гестаген + DCI, и 11,4±2,9 мм у пациенток, получавших гестаген + плацебо (p<0,001). У пациенток, получавших гестаген + DCI, отмечена нормализация индекса пролиферации Ki-67 (9,8±4,5% при норме <10%) и экспрессии VEGF (1,83±0,53 у.е. при норме <2,0). Прием DCI в рамках комплексной терапии привел к нормализации индекса HOMA-IR (2,44±0,56 vs 3,23±0,52; p<0,001), улучшению липидного профиля (снижение общего холестерина, липопротеинов низкой плотности, триглицеридов в 1,2–1,4 раза; повышение липопротеинов высокой плотности в 1,3 раза) и снижению уровня С-реактивного белка в 2,0 раза (p<0,001), а также провоспалительных цитокинов. Индекс массы тела у пациенток, получавших гестаген + DCI, снизился с 30,4±2,3 до 28,9±2,4 кг/м², тогда как у пациенток, принимавших гестаген + плацебо, оставался стабильным (30,6±1,6 → 30,8±2,1 кг/м²; p=0,002).
Заключение. Результаты рандомизированного плацебо-контролируемого исследования свидетельствуют о том, что добавление DCI в дозе 1200 мг/сут к стандартной терапии норэтистерона ацетатом значительно повышает эффективность лечения ГЭ без атипии у женщин с избыточной массой тела и ожирением.
Ключевые слова: гиперплазия эндометрия без атипии, D-хиро-инозитол, инсулинорезистентность, гестагены, норэтистерона ацетат, цитокины, Ki-67.
Для цитирования: Радзинский В.Е., Михалева Л.М., Костин И.Н., Хамошина М.Б., Оразов М.Р., Орехов Р.Е., Ахматова А.Н., Муллина И.А. D-хиро-инозитол в комплексной терапии гиперплазии эндометрия без атипии: результаты двойного слепого рандомизированного плацебо-контролируемого исследования. Клинический разбор в общей медицине. 2026; 7 (2): 24–36. DOI: 10.47407/kr2026.7.2.00766
Цель. Повысить результативность комплексной терапии гиперплазии эндометрия (ГЭ) без атипии с использованием D-хиро-инозитола (D-chiro-inositol – DCI).
Материалы и методы. В настоящее двойное слепое проспективное рандомизированное плацебо-контролируемое исследование были включены 60 пациенток с морфологически верифицированным диагнозом «ГЭ без атипии». В ходе исследования участницы были стратифицированны на две группы: 1-я (n=30) получала норэтистерона ацетат в непрерывном режиме согласно действующей инструкции и DCI 1200 мг/сут, 2-я (n=30) – норэтистерона ацетат + плацебо. Длительность терапии составила 6 мес с последующим наблюдением в течение 6 мес. Оценивались частота достижения морфологического регресса и рецидивов, динамика иммуногистохимических маркеров (Ki-67, VEGF, p53), цитокинового профиля и метаболических параметров, профиль безопасности.
Результаты. В ходе исследования было установлено, что частота достижения полного морфологического регресса ГЭ без атипии через 6 мес терапии у пациенток, получавших гестаген + DCI, составила 86,7% по сравнению с 60,0% у пациенток, принимавших гестаген + плацебо (в 1,4 раза выше; p=0,020). Вместе с тем анализ частоты рецидивирующего течения ГЭ без атипии через 6 мес после окончания лечения продемонстрировал более высокую результативность у пациенток после комплексной терапии (в 3,7 раза ниже, 10,0% vs 36,7%; p=0,015). Анализ результатов сонографического исследования толщины эндометрия после лечения показал М-эхо 8,5±2,6 мм у пациенток, принимавших гестаген + DCI, и 11,4±2,9 мм у пациенток, получавших гестаген + плацебо (p<0,001). У пациенток, получавших гестаген + DCI, отмечена нормализация индекса пролиферации Ki-67 (9,8±4,5% при норме <10%) и экспрессии VEGF (1,83±0,53 у.е. при норме <2,0). Прием DCI в рамках комплексной терапии привел к нормализации индекса HOMA-IR (2,44±0,56 vs 3,23±0,52; p<0,001), улучшению липидного профиля (снижение общего холестерина, липопротеинов низкой плотности, триглицеридов в 1,2–1,4 раза; повышение липопротеинов высокой плотности в 1,3 раза) и снижению уровня С-реактивного белка в 2,0 раза (p<0,001), а также провоспалительных цитокинов. Индекс массы тела у пациенток, получавших гестаген + DCI, снизился с 30,4±2,3 до 28,9±2,4 кг/м², тогда как у пациенток, принимавших гестаген + плацебо, оставался стабильным (30,6±1,6 → 30,8±2,1 кг/м²; p=0,002).
Заключение. Результаты рандомизированного плацебо-контролируемого исследования свидетельствуют о том, что добавление DCI в дозе 1200 мг/сут к стандартной терапии норэтистерона ацетатом значительно повышает эффективность лечения ГЭ без атипии у женщин с избыточной массой тела и ожирением.
Ключевые слова: гиперплазия эндометрия без атипии, D-хиро-инозитол, инсулинорезистентность, гестагены, норэтистерона ацетат, цитокины, Ki-67.
Для цитирования: Радзинский В.Е., Михалева Л.М., Костин И.Н., Хамошина М.Б., Оразов М.Р., Орехов Р.Е., Ахматова А.Н., Муллина И.А. D-хиро-инозитол в комплексной терапии гиперплазии эндометрия без атипии: результаты двойного слепого рандомизированного плацебо-контролируемого исследования. Клинический разбор в общей медицине. 2026; 7 (2): 24–36. DOI: 10.47407/kr2026.7.2.00766
D-chiro-inositol in combination therapy of endometrial hyperplasia without atypia: results of the double-blind randomized placebo-controlled trial
Viktor E. Radzinskiy1, Liudmila M. Mikhaleva2, Igor N. Kostin1, Marina B. Khamoshina1,Mekan R. Orazov1, Roman E. Orekhov1, Anastasiia N. Akhmatova1, Irina A. Mullina3
1 Patrice Lumumba Peoples' Friendship University of Russia, Moscow, Russia;
2 Avtsyn Research Institute of Human Morphology of Petrovsky National Research Centre of Surgery, Moscow, Russia;
3 Semashko Clinical Hospital “Russian Railways-Medicine”, Moscow, Russia
omekan@mail.ru
Abstract
Aim. To improve the effectiveness of combination therapy for endometrial hyperplasia without atypia using D-chiro-inositol (DCI).
Materials and methods. This double-blind prospective randomized placebo-controlled trial enrolled 60 patients with morphologically verified endometrial hyperplasia without atypia. Participants were stratified into two groups: Group 1 (n=30) received norethisterone acetate in continuous regimen according to the current prescribing information plus DCI 1200 mg/day; Group 2 (n=30) received norethisterone acetate plus placebo. Treatment duration was 6 months with subsequent follow-up for 6 months. The following outcomes were assessed: morphological regression and recurrence rates, dynamics of immunohistochemical markers (Ki-67, VEGF, p53), cytokine profile and metabolic parameters, and safety profile.
Results. The study demonstrated that complete morphological regression of endometrial hyperplasia without atypia at 6 months was achieved in 86.7% of patients receiving progestogen + DCI compared to 60.0% in patients receiving progestogen + placebo (1.4–fold higher; p=0.020). Furthermore, analysis of recurrence rates at 6 months after treatment completion showed superior outcomes in patients after combination therapy (3.7–fold lower, 10.0% vs 36.7%; p=0.015). Sonographic assessment of endometrial thickness after treatment revealed M-echo of 8.5±2.6 mm in patients receiving progestogen + DCI versus 11.4±2.9 mm in patients receiving progestogen + placebo (p<0.001). Patients receiving progestogen + DCI demonstrated normalization of Ki-67 proliferation index (9.8±4.5% with normal range <10%) and VEGF expression (1.83±0.53 AU with normal range <2.0). DCI as part of combination therapy led to normalization of HOMA-IR index (2.44±0.56 vs 3.23±0.52; p<0.001), improvement in lipid profile (reduction in total cholesterol, LDL, and triglycerides by 1.2–1.4-fold; increase in HDL by 1.3-fold), and 2.0-fold reduction in C-reactive protein levels (p<0.001), as well as proinflammatory cytokines. BMI in patients receiving progestogen + DCI decreased from 30.4±2.3 to 28.9±2.4 kg/m², whereas in patients receiving progestogen + placebo it remained stable (30.6±1.6 → 30.8±2.1 kg/m²; p=0.002).
Conclusion. The results of this randomized placebo-controlled trial indicate that adding DCI at a dose of 1200 mg/day to standard norethisterone acetate therapy significantly improves treatment efficacy for endometrial hyperplasia without atypia in women with overweight and obesity.
Keywords: endometrial hyperplasia, D-chiro-inositol, insulin resistance, progestogens, norethisterone acetate, cytokines, Ki-67.
For citation: Radzinskiy V.E., Mihaleva L.M., Kostin I.N., Khamoshina M.B., Orazov M.R., Orekhov R.E., Akhmatova A.N., Mullina I.A. D-chiro-inositol in combination therapy of endometrial hyperplasia without atypia: results of the double-blind randomized placebo-controlled trial. Clinical review for general practice. 2026; 7 (2): 24–36 (In Russ.). DOI: 10.47407/kr2026.7.2.00766
Введение
Гиперплазия эндометрия (ГЭ) представляет собой патологическое состояние, характеризующееся аномальной пролиферацией эндометриальных желез с увеличением соотношения железистого компонента к строме [1]. Являясь предраковым состоянием, ГЭ требует особого внимания клиницистов, поскольку рак эндометрия занимает лидирующую позицию среди злокачественных новообразований женской репродуктивной системы в развитых странах [2]. По данным эпидемиологических исследований, заболеваемость ГЭ достигает 133 случаев на 100 000 женщин-лет, при этом пик заболеваемости приходится на возраст 50–54 лет [1]. Среди женщин с аномальными маточными кровотечениями распространенность ГЭ составляет от 5 до 20,3% в зависимости от исследуемой популяции [3–5]. Особую тревогу вызывает тенденция к увеличению заболеваемости ГЭ, связанная с глобальным ростом распространенности факторов риска – ожирения, сахарного диабета и метаболического синдрома (МС) [2].
Патогенез ГЭ традиционно связывают с гиперэстрогенией на фоне относительного дефицита прогестерона, что обозначается термином «неопозированное действие эстрогенов» [1, 2]. Однако современные исследования убедительно демонстрируют ключевую роль инсулинорезистентности (ИР) и МС в развитии и прогрессировании пролиферативных заболеваний эндометрия [6, 7]. Гиперинсулинемия, характерная для ожирения и МС, оказывает прямое митогенное воздействие на эндометриальные клетки посредством активации инсулиновых рецепторов, запуская каскад фосфорилирования белков субстрата инсулинового рецептора (IRS) и последующую активацию сигнального пути PI3K/AKT [8]. Синергичное взаимодействие инсулиноподобного фактора роста 1 (IGF-1) и эстрогенов создает особо мощную митогенную среду, способствующую неконтролируемой пролиферации [8]. Кроме того, ИР снижает синтез глобулина, связывающего половые гормоны, что приводит к повышению биодоступности эстрогенов [9].
Хроническое низкоинтенсивное воспаление, ассоциированное с ожирением и ИР, играет существенную роль в патогенезе ГЭ [10]. Повышенные уровни провоспалительных цитокинов (интерлейкины – ИЛ-1β, ИЛ-6, фактор некроза опухоли α – ФНО-α, ИЛ-8, ИЛ-17) и сниженные уровни противовоспалительных медиаторов (ИЛ-4, ИЛ-10, ИЛ-13) формируют провоспалительный фенотип, способствующий пролиферации эндометрия и потенциально – его злокачественной трансформации [11, 12]. С-реактивный белок (СРБ), как маркер системного воспаления, также ассоциирован с повышенным риском развития ГЭ и рака эндометрия [10].
Стандартом консервативного лечения ГЭ без атипии является терапия гестагенами, демонстрирующая регрессию гиперпластических изменений у 70–90% пациенток [13]. Тем не менее существенной проблемой остается высокая частота рецидивов после достижения первичного ответа – до 23–40% в течение длительного наблюдения [14, 15]. По данным последних исследований, частота рецидивов через 12 мес после прекращения терапии может достигать 51,4%, при этом медиана времени до рецидива составляет 15 мес [16]. Ключевыми факторами риска рецидивирования являются ожирение (индекс массы тела – ИМТ≥27 кг/м²), ИР и МС [16, 17]. Исследование Х. Li и соавт. (2021 г.) продемонстрировало, что ИР увеличивает риск рецидива в 9,5 раза (отношение шансов – ОШ 9,5; 95% доверительный интервал – ДИ 3,3–27,0), а МС – в 4,9 раза (ОШ 4,9; 95% ДИ 1,5–15,5) [6]. Данные факты обосновывают необходимость комплексного подхода к терапии ГЭ с воздействием на метаболические нарушения.

D-хиро-инозитол (D-chiro-inositol – DCI) представляет собой один из девяти стереоизомеров инозитола – циклического шестиуглеродного полиола, широко распространенного в живой природе [18]. DCI является критически важным вторичным мессенджером в сигнальном каскаде инсулина, участвуя в передаче внутриклеточного сигнала после связывания инсулина с рецептором [19]. При активации инсулинового рецептора происходит гидролиз гликозилфосфатидилинозитольных липидов клеточной мембраны с высвобождением инозитолфосфогликановых медиаторов, содержащих DCI и галактозамин, которые активируют ключевые ферменты, контролирующие окислительный и неокислительный метаболизм глюкозы (рис. 1) [20].
Дефицит DCI-содержащих инозитолфосфогликанов признан одним из механизмов развития ИР [21]. У женщин с синдромом поликистозных яичников (СПКЯ) и ИР выявлено трехкратное снижение высвобождения DCI-содержащих инозитолфосфогликанов в ответ на инсулиновую стимуляцию по сравнению со здоровыми женщинами [22]. Эпимеризация мио-инозитола в DCI, осуществляемая специфической эпимеразой, нарушена при сахарном диабете и инсулинорезистентных состояниях [23].
Клинические исследования убедительно подтверждают эффективность DCI в коррекции ИР и метаболических нарушений. В рандомизированном плацебо-контролируемом исследовании J. Nestler и соавт., опубликованном в «New England Journal of Medicine», применение DCI в дозе 1200 мг/сут в течение 6–8 нед у женщин с СПКЯ привело к значительному снижению площади под кривой инсулина (с 13 417±11 572 до 5158±6714 мкЕд/мл×мин; p=0,007) и уровня триглицеридов плазмы (p=0,002), а также повышению частоты овуляции с 27% в группе плацебо до 86% в группе DCI (p<0,001) [20].
DCI реализует свои эффекты через множественные механизмы: инсулиносенситизирующее действие, ингибирование транскрипции ароматазы, модуляцию трансдифференцировки белой жировой ткани в бурую [24]. Систематический обзор и метаанализ 14 рандомизированных контролируемых исследований (РКИ) продемонстрировал, что применение инозитолов у пациентов с метаболическими заболеваниями приводит к статистически значимому снижению уровня триглицеридов (СРС -1,24; 95% ДИ -1,84–-0,64; p<0,001), общего холестерина (СРС -1,09; 95% ДИ -1,83–-0,55; p<0,001) и холестерина липопротеинов низкой плотности – ЛПНП (СРС -1,31; 95% ДИ -2,04–-0,59; p<0,001) [25]. Комбинированная терапия мио-инозитолом и DCI в соотношении 40:1 улучшает показатели липидного профиля, снижает индекс HOMA-IR и уменьшает кардиоваскулярный риск у женщин с СПКЯ [26].
Помимо метаболических эффектов, инозитолы обладают противовоспалительными свойствами. Исследование S. Arefhosseini и соавт. (2023 г.) продемонстрировало, что мио-инозитол снижает экспрессию ФНО-α мРНК у пациентов с неалкогольной жировой болезнью печени [27]. В экспериментальных исследованиях инозитолгексафосфат подавляет экспрессию провоспалительных цитокинов ИЛ-1β и ИЛ-6, индуцированных липополисахаридом [28]. Mиo-инозитол уменьшает воспаление и окислительный стресс в эндотелиальных клетках, подвергшихся хронической гипергликемии, снижая адгезию моноцитов и экспозицию молекул адгезии [29].
Учитывая патогенетическую роль ИР, дислипидемии и хронического воспаления в развитии и рецидивировании ГЭ, а также доказанную эффективность DCI в коррекции данных нарушений, представляется обоснованным изучение возможности применения DCI в составе комплексной терапии ГЭ без атипии. Потенциальное воздействие DCI на множественные патогенетические звенья заболевания может повысить эффективность стандартной гестагенотерапии и снизить риск рецидивирования.
Цель исследования – повысить результативность комплексной терапии ГЭ без атипии с использованием DCI.
Материалы и методы
Настоящее двойное слепое проспективное рандомизированное плацебо-контролируемое исследование было проведено на клинических базах кафедры акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН (заведующий кафедрой – академик РАН, профессор В.Е. Радзинский). Общая продолжительность исследования составила 13 мес: период скрининга – 2 нед, период лечения – 6 мес, период наблюдения после лечения – 6 мес.
Критерии включения:
• возраст 15–49 лет;
• гистологически подтвержденный диагноз ГЭ без атипии;
• индекс массы тела (ИМТ) 24,95–35 кг/м²;
• отсутствие гормональной терапии в течение 3 мес до включения в исследование;
• подписанное информированное согласие.
Критерии исключения:
• атипическая гиперплазия и карцинома эндометрия;
• злокачественные новообразования любой локализации в анамнезе;
• тяжелые соматические заболевания (печеночная, почечная недостаточность, неконтролируемая артериальная гипертензия, сахарный диабет);
• беременность или период лактации;
• острые воспалительные заболевания органов малого таза;
• наличие противопоказаний к приему гестагенов.
В настоящее исследование были включены 60 пациенток, стратифицированных методом слепой рандомизации в две группы. Группа 1 (n=30) получала норэтистерона ацетат в непрерывном режиме + DCI 1200 мг/сут ежедневно в течение 6 мес. Группа 2 (n=30) получала норэтистерона ацетат в непрерывном режиме + плацебо ежедневно в течение 6 мес. В обеих группах пациентки получили информацию по модификации образа жизни согласно действующим клиническим рекомендациям (физические нагрузки и рациональное сбалансированное питание, снижение калоража на 30% для достижения и поддержания нормальной массы тела; физическая активность должна составлять минимум 150 мин/нед, включая упражнения на укрепление мышц в течение 2 дней в неделю).
Антропометрическое обследование включало измерение роста (м) с помощью ростомера и массы тела (кг) на медицинских весах. ИМТ рассчитывали по формуле: масса тела (кг)/рост² (м²).
Всем пациенткам выполнялись:
• стандартное ультразвуковое исследование (УЗИ) органов малого таза с измерением М-эхо на аппарате Voluson E10 (GE Healthcare, США) с использованием трансвагинального датчика частотой 5–9 МГц;
• гистероскопия с прицельной биопсией эндометрия, гистологическое исследование биоптатов эндометрия;
• иммуногистохимическое (ИГХ) исследование с определением экспрессии Ki-67, VEGF, p53;
• иммуноферментный анализ для определения уровней цитокинов в сыворотке крови (ИЛ-4, ИЛ-13, ИЛ-25, ИЛ-37, ИЛ-1β, ФНО-α, ИЛ-8, ИЛ-17);
• биохимический анализ крови (липидный профиль, СРБ, индекс HOMA-IR);
• антропометрия.
Все гистероскопии выполнялись с использованием линзового мини-эндоскопа 2,7 мм с углом обзора 105°, оснащенного двухканальным рабочим зондом 4,5 мм внешнего диаметра (Karl Storz, Германия). Для расширения полости матки использовался физиологический раствор, подаваемый под давлением от системы капельного вливания с высотой подвеса мешка 1 м над уровнем пациентки. Источник света – ксеноновая лампа мощностью 300 Вт, цифровая видеокамера высокого разрешения (Karl Storz). Во время процедуры тщательно осматривались как передняя, так и задняя стенки матки путем продольного проведения гистероскопа вдоль поверхности эндометрия для выявления любых поверхностных изменений.
Полученные образцы биопсии фиксировали в 10% фосфатном буфере с формалином, после чего подвергали гистологической обработке в автоматическом гистопроцессоре Leica ASP 30 (Германия). Далее образцы заливали в парафин на станции Leica EG 1150 (Германия). Срезы толщиной 4 мкм окрашивали гематоксилином и эозином с помощью окрасочной станции Leica ST 5010 (Германия). Микроскопическое исследование препаратов выполняли с использованием микроскопа Leica DMLB и цифровой камеры Leica DFC 420 (Германия). Проводилась патоморфологическая оценка состояния эндометрия в полученных микропрепаратах. Выполняли ИГХ-анализ эндометрия с использованием антител к Ki-67, VEGF, p53. ИГХ-окрашивание выполняли на приборах Ventana BenchMark Ultra IHdSH (США) и Bond-Max (Германия) с использованием системы визуализации Ultra Vision TL-015-HD Lab Vision. Экспрессию изучаемых маркеров анализировали в трех неперекрывающихся полях зрения при увеличении ×400, используя микроскоп Leica DMLB с цифровой камерой Leica DFC 420 (Германия).
Полным морфологическим регрессом считали отсутствие признаков ГЭ по данным гистологического исследования биоптата (нормальный пролиферативный или секреторный эндометрий). Частичным регрессом считали уменьшение степени выраженности гиперпластических изменений/наличие очаговой гиперплазии. Рецидивом ГЭ считали повторное выявление гистологических признаков гиперплазии после ранее достигнутого полного регресса.
Забор венозной крови для биохимического исследования проводился из локтевой вены строго натощак (не менее 12 ч голодания) в утренние часы с использованием вакуумных систем. Определение показателей липидного профиля (ЛПНП, липопротеины высокой плотности – ЛПВП, триглицериды), глюкозы, инсулина, СРБ выполнялось на автоматическом биохимическом анализаторе с расчетом индекса ИР HOMA-IR по формуле: глюкоза натощак (ммоль/л) × инсулин натощак (мкЕд/мл) / 22,5. Определение показателей липидного профиля (общий холестерин, ЛПНП, ЛПВП, триглицериды), глюкозы и СРБ выполнялось на автоматическом биохимическом анализаторе Cobas c311 (Roche Diagnostics, Швейцария); определение инсулина – на иммунохимическом анализаторе Cobas e411 (Roche Diagnostics, Швейцария) методом электрохемилюминесценции.
Уровни цитокинов определяли в периферической крови натощак: ИЛ-4, ИЛ-13, ИЛ-25, ИЛ-37, ИЛ-1β, ФНО-α, ИЛ-8, ИЛ-17 с помощью метода проточной цитофлуорометрии с использованием тест-систем BD Cytometric Bead Array (BD, США) и проточного цитофлуорометра FACStrack (BD, США).
В качестве референсных использовали следующие значения: индекс пролиферации Ki-67<10%, экспрессия VEGF<2,0 у.е., индекс HOMA-IR<2,5. Референсные значения цитокинов: ИЛ-4 2,0–4,0 пг/мл, ИЛ-13 3,0–5,0 пг/мл, ИЛ-25 35–60 пг/мл, ИЛ-37 80–150 пг/мл; для провоспалительных цитокинов: ИЛ-1β<5,0 пг/мл, ФНО-α<8,0 пг/мл, ИЛ-8<15 пг/мл, ИЛ-17<10 пг/мл.
Визиты осуществлялись исходно (В1), через 6 мес терапии (В2) и через 12 мес от начала исследования (В3).
Первичные конечные точки:
• частота морфологического регресса ГЭ через 6 мес терапии (по данным биопсии эндометрия);
• частота рецидива ГЭ в течение 6 мес после окончания лечения.
Вторичные конечные точки:
• динамика толщины эндометрия по данным УЗИ;
• динамика ИГХ-маркеров (Ki-67, VEGF, p53);
• динамика уровней про- и противовоспалительных цитокинов;
• динамика метаболических параметров (индекс HOMA-IR, липидный профиль, СРБ);
• изменение массы тела и ИМТ.
Статистическая обработка данных проводилась с использованием программы Statistica 10.0 (StatSoft Inc., США). Количественные данные представлены в виде M±SD (среднее ± стандартное отклонение) и медианы с интерквартильным размахом. Для сравнения количественных показателей использовался t-критерий Стьюдента или критерий Манна–Уитни в зависимости от характера распределения. Сравнение качественных показателей проводилось с помощью критерия χ². Статистически значимыми считались различия при p<0,05.
Протокол исследования был одобрен локальным этическим комитетом. Все участницы подписали информированное согласие до включения в исследование.
Конфиденциальность данных участниц обеспечивалась присвоением уникальных идентификационных номеров. Все данные хранились в защищенной электронной базе данных с ограниченным доступом. Участницы имели право выйти из исследования в любое время без объяснения причин.
Результаты
В ходе настоящего исследования группы были сопоставимы по основным демографическим и клиническим характеристикам (p≥0,05). Медиана возраста пациенток, принимавших гестаген + DCI, составила 37 лет (диапазон 32–42 года), пациенток, получавших гестаген + плацебо, – 38 лет (диапазон 31–43 года). Антропометрический анализ выявил, что средний ИМТ составил 30,4±2,3 кг/м² и 30,6±1,6 кг/м² соответственно (p=0,78). Исходная толщина эндометрия по данным УЗИ составила 15,6±2,5 мм у пациенток, получавших гестаген + DCI, и 16,1±2,0 мм у пациенток, принимавших гестаген + плацебо (p=0,46).
Частота морфологического регресса ГЭ через 6 мес терапии была достоверно выше у пациенток, получавших гестаген + DCI: полный регресс достигнут у 26 (86,7%) из 30 пациенток по сравнению с 18 (60,0%) из 30 у пациенток, принимавших гестаген + плацебо, что соответствует увеличению эффективности в 1,4 раза (χ²=5,46; p=0,020; рис. 2). При оценке частоты рецидивов через 6 мес после окончания терапии рецидив ГЭ зарегистрирован у 3 (10,0%) из 30 пациенток, получавших гестаген + DCI, и у 11 (36,7%) из 30 пациенток, принимавших гестаген + плацебо, что свидетельствует о снижении риска рецидивирования в 3,7 раза на фоне применения DCI (χ²=5,97; p=0,015).
 Динамика толщины эндометрия в ходе настоящего исследования по данным трансвагинального УЗИ представлена в табл. 1. В обеих группах отмечено статистически значимое уменьшение толщины эндометрия на фоне терапии, однако у пациенток, получавших гестаген + DCI, снижение было более выраженным.
Динамика толщины эндометрия в ходе настоящего исследования по данным трансвагинального УЗИ представлена в табл. 1. В обеих группах отмечено статистически значимое уменьшение толщины эндометрия на фоне терапии, однако у пациенток, получавших гестаген + DCI, снижение было более выраженным.К визиту В3 толщина эндометрия у пациенток, получавших гестаген + DCI, составила 8,5±2,6 мм, у пациенток, принимавших гестаген + плацебо, – 11,4±2,9 мм, что соответствует уменьшению показателя в 1,3 раза по сравнению с плацебо (p<0,001; см. табл. 1).

Динамика ИГХ-маркеров представлена в табл. 2. Исходно группы не различались по уровню экспрессии Ki-67 (25,0±4,7% vs 27,2±4,9%; p=0,08). К визиту В2 отмечено снижение индекса Ki-67 в обеих группах, однако у пациенток, получавших гестаген + DCI, показатель достиг референсных значений нормы (9,8±4,5% при норме <10%), тогда как у пациенток, принимавших гестаген + плацебо, оставался незначительно повышенным (12,8±4,9%), что в 1,3 раза выше, чем в группе комбинированной терапии (p=0,015). К визиту В3 различия сохранялись: 11,0±3,7% vs 14,9±4,4%, индекс пролиферации у пациенток, получавших гестаген + плацебо, превышал таковой у пациенток, принимавших гестаген + DCI, в 1,4 раза (p<0,001).
 Экспрессия VEGF исходно была повышена в обеих группах (3,58±0,66 и 3,43±0,74 у.е. при норме <2,0).
Экспрессия VEGF исходно была повышена в обеих группах (3,58±0,66 и 3,43±0,74 у.е. при норме <2,0). У пациенток, получавших гестаген + DCI, к визиту В2 отмечена нормализация показателя (1,83±0,53 у.е.), тогда как у пациенток, принимавших гестаген + плацебо, экспрессия VEGF оставалась на верхней границе нормы (2,23±0,52 у.е.), превышая значения у пациенток, получавших гестаген + DCI, в 1,2 раза (p=0,004; см. табл. 2).
Аналогичная тенденция прослеживалась для маркера p53 (см. табл. 2).
Исходная морфологическая картина ГЭ без атипии в обеих группах характеризовалась преобладанием железистого компонента над стромальным со сближением маточных желез, формированием многорядного железистого эпителия с гиперхромными ядрами и единичными фигурами митоза при сохранной базальной мембране (рис. 3).
В отдельных случаях наблюдалось слияние маточных желез между собой. В строме эндометрия определялась умеренная рассеянная лимфоплазмоцитарная инфильтрация с образованием мелких очагов. Большая часть маточных желез имела расширенный просвет. ИГХ-исследование выявило ядерную экспрессию p53 в эпителиоцитах маточных желез и единичных клетках стромы, индекс пролиферации Ki-67 составлял 20–30%, при оценке VEGF определялись отдельные спиральные артерии и капилляры (рис. 4).
После терапии морфологическая картина эндометрия существенно различалась между группами. Среди пациенток, получавших гестаген + DCI, у большинства (86,7%) достигнут полный морфологический регресс: эндометрий соответствовал средней стадии фазы пролиферации, маточные железы с признаками гиперплазии не выявлялись (рис. 5).
 Иммуногистохимически отмечалась ядерная экспрессия p53 в однорядном эпителии маточных желез, индекс пролиферации Ki-67 составлял 5–10%, при оценке VEGF определялись только капилляры, спиральные артерии не определялись (рис. 6).
Иммуногистохимически отмечалась ядерная экспрессия p53 в однорядном эпителии маточных желез, индекс пролиферации Ki-67 составлял 5–10%, при оценке VEGF определялись только капилляры, спиральные артерии не определялись (рис. 6).У пациенток, получавших гестаген + плацебо, полный морфологический регресс был достигнут лишь у 60,0%. У 40% пациенток данной группы в биоптатах эндометрия сохранялись единичные железы с дилатацией просвета (рис. 7, а, б) с низкой ядерной экспрессией p53 и минимальным индексом пролиферации Ki-67 2–3% в дилатированных железах, что свидетельствует о неполном морфологическом регрессе ГЭ (рис. 7, в, г).
При рецидиве ГЭ, который среди пациенток, принимавших гестаген + плацебо, регистрировался в 3,7 раза чаще (36,7% против 10,0%), в отдельных фокусах отмечалось сближение маточных желез с увеличенным просветом, имеющих многорядный железистый эпителий с гиперхромными клетками и единичными фигурами митоза при сохранной базальной мембране (рис. 8).
Иммуногистохимически в зонах очаговой гиперплазии выявлялась неравномерная ядерная экспрессия p53, индекс пролиферации Ki-67 достигал 25–30%, определялись спиральные артерии и капилляры (рис. 9).
Исходно в обеих группах отмечался дисбаланс цитокинового профиля: достоверное (p<0,05) снижение уровней противовоспалительных цитокинов (ИЛ-4, ИЛ-13, ИЛ-25, ИЛ-37 ниже референсных значений) и повышение провоспалительных цитокинов (ИЛ-1β, ФНО-α, ИЛ-8, ИЛ-17 выше нормы, табл. 3).
У пациенток, получивших DCI в составе комплексной терапии, к визиту В3 отмечена регуляция/нормализация уровней противовоспалительных цитокинов: ИЛ-4 достиг 3,43±1,06 пг/мл (норма 2,0–4,0 пг/мл), ИЛ-13 – 4,28±1,28 пг/мл (3,0–5,0 пг/мл), ИЛ-25 – 46±11 пг/мл (35–60 пг/мл), ИЛ-37 – 106±22 пг/мл (80–150 пг/мл).
У пациенток, принимавших гестаген + плацебо, показатели оставались ниже нормы (см. табл. 3).
Аналогичная динамика прослеживалась для провоспалительных цитокинов. У пациенток, получавших гестаген + DCI, к визиту В3 отмечено снижение ИЛ-1β до 4,25±1,30 пг/мл (норма <5,0 пг/мл), ФНО-α – до 7,38±2,51 пг/мл (<8,0 пг/мл), ИЛ-8 – до 14,8±5,8 пг/мл (<15), ИЛ-17 – до 9,4±2,4 пг/мл (<10 пг/мл). У пациенток, принимавших гестаген + плацебо, провоспалительные цитокины оставались повышенными, различия между группами были статистически значимы (p<0,001).


Исходно в обеих группах выявлены признаки ИР и дислипидемии (табл. 4). Индекс HOMA-IR превышал 2,5 у всех пациенток (3,49±0,46 и 3,68±0,45 у пациенток, получавших гестаген + DCI и гестаген + плацебо соответственно). У пациенток, принимавших гестаген + DCI, к визиту В3 отмечена нормализация индекса HOMA-IR (2,44±0,56 при норме <2,5), тогда как у пациенток, получавших гестаген + плацебо, показатель оставался повышенным (3,23±0,52; см. табл. 4), превышая значения в группе комбинированной терапии в 1,3 раза (p<0,001).
Терапия DCI привела к значимому улучшению липидного профиля: снижению общего холестерина с 6,19±0,81 до 5,03±0,76 ммоль/л (в 1,2 раза), ЛПНП – с 4,58±0,71 до 3,45±0,63 ммоль/л (в 1,3 раза), триглицеридов – с 2,27±0,48 до 1,62±0,44 ммоль/л (в 1,4 раза), а также повышению ЛПВП с 1,14±0,22 до 1,44±0,27 ммоль/л (в 1,3 раза). У пациенток, получавших гестаген + плацебо, показатели липидного профиля практически не изменились.
Уровень СРБ у пациенток, принимавших гестаген + DCI, снизился с 6,31±1,41 до 2,86±1,26 мг/л (в 2,2 раза; норма <3,0 мг/л), у пациенток, принимавших гестаген + плацебо, – с 6,79±1,41 до 5,62±1,99 мг/л (в 1,2 раза), при этом конечные значения у пациенток, получавших гестаген + плацебо, были в 2,0 раза выше, чем у пациенток, получавших гестаген + DCI (p<0,001). ИМТ у пациенток, получавших гестаген + DCI, снизился с 30,4±2,3 до 28,9±2,4 кг/м², тогда как у пациенток, получавших гестаген + плацебо, оставался стабильным (30,6±1,6 → 30,8±2,1 кг/м²; p=0,002).
Анализ безопасности продемонстрировал статистически значимо меньшую частоту нежелательных явлений у пациенток, принимавших гестаген + DCI, по сравнению с принимавшими гестаген + плацебо (табл. 5).
Ациклические кровянистые выделения из половых путей у пациенток, получавших гестаген + плацебо, регистрировались в 4,5 раза чаще, чем у пациенток, принимавших гестаген + DCI (p=0,042). Циклическая масталгия отмечалась в 8 раз чаще у пациенток, принимавших гестаген + плацебо (p=0,026). Головные боли наблюдались в 5 раз чаще у пациенток, получавших гестаген + плацебо (p=0,021). Тошнота фиксировалась в 4,5 раза чаще у пациенток, принимавших гестаген + плацебо (p=0,042). Серьезных нежелательных явлений, потребовавших отмены терапии, в обеих группах зарегистрировано не было.
Обсуждение
В настоящее время продолжается поиск новых технологий с целью повышения результативности лечения ГЭ без атипии. Несмотря на достаточно высокую результативность стандартной терапии с использованием гестагенов, частота рецидивов, к сожалению, не меняется, что диктует необходимость научного обоснования использования новых методов терапии ГЭ без атипии.
Результаты рандомизированного плацебо-контролируемого исследования продемонстрировали значительное повышение эффективности терапии ГЭ без атипии при добавлении DCI к стандартной гестагенотерапии. Частота достижения полного морфологического регресса в группе комбинированной терапии составила 86,7%, что статистически значимо превышает показатель группы плацебо (60,0%; p=0,020) и соответствует верхней границе эффективности гестагенотерапии, описанной в международных рекомендациях и систематических обзорах (70–90%) [13, 30].
Полученные нами данные об эффективности монотерапии гестагенами согласуются с результатами крупного метаанализа I. Gallos и соавт., в котором частота регресса ГЭ при применении оральных гестагенов составила около 70% [31]. Согласно рекомендациям Королевского колледжа акушеров и гинекологов (RCOG), стандартная терапия гестагенами обеспечивает регресс гиперплазии у большинства пациенток, однако частота рецидивов остается существенной проблемой [13]. В нашем исследовании добавление DCI позволило не только повысить частоту первичного ответа, но и значительно снизить частоту рецидивирования – с 36,7% до 10,0% (снижение в 3,7 раза; p=0,015).
Высокая частота рецидивов ГЭ после успешной консервативной терапии является одной из ключевых нерешенных проблем современной гинекологии. По данным систематических обзоров, частота рецидивов после достижения первичной ремиссии достигает 23–40% при длительном наблюдении [14], а в отдельных исследованиях – до 51,4% через 12 мес после прекращения терапии [16]. Результаты нашего исследования демонстрируют, что DCI может существенно снижать риск рецидивирования, что имеет важное клиническое значение для долгосрочного ведения пациенток с ГЭ.
Патогенетическое обоснование назначения DCI при ГЭ базируется на современном понимании роли метаболических нарушений в развитии и прогрессировании пролиферативных заболеваний эндометрия. Исследование Х. Li и соавт. убедительно продемонстрировало, что ИР увеличивает риск рецидива атипической ГЭ в 9,5 раза (ОШ 9,5; 95% ДИ 3,3–27,0), а МС – в 4,9 раза (ОШ 4,9; 95% ДИ 1,5–15,5) [6]. Аналогичные данные получены Y. Wu и соавт. (2025 г.), показавшими, что комбинация МС и ИР обладает высокой прогностической ценностью для оценки риска рецидива (AUC=0,818) [32]. Эти данные подчеркивают важность коррекции метаболических нарушений в комплексной терапии ГЭ.
В нашем исследовании применение DCI привело к нормализации индекса HOMA-IR (с 3,49±0,46 до 2,44±0,56 при норме <2,5), тогда как в группе плацебо показатель оставался повышенным (3,23±0,52). Эти результаты согласуются с данными систематического обзора и метаанализа В. Pintaudi и соавт., включавшего 20 РКИ с участием 1239 пациентов, который продемонстрировал статистически значимое снижение HOMA-IR (MD -1,96 ммоль × мкЕд/мл; 95% ДИ -2,62–-1,30) на фоне приема инозитолов [33]. Рандомизированное исследование J. Nestler и соавт., опубликованное в «New England Journal of Medicine», показало, что DCI в дозе 1200 мг/сут приводит к значительному снижению площади под кривой инсулина у женщин с СПКЯ (с 13 417±11 572 до 5158±6714 мкЕд/мл × мин; p=0,007) [20]. Недавнее исследование М. Montt-Guevara и соавт. (2021 г.) подтвердило, что DCI регулирует передачу инсулинового сигнала в адипоцитах человека, что объясняет механизм его инсулиносенситизирующего действия [19].
Помимо коррекции ИР DCI продемонстрировал благоприятное влияние на липидный профиль. В нашем исследовании отмечено статистически значимое снижение общего холестерина (с 6,19±0,81 до 5,03±0,76 ммоль/л), ЛПНП (с 4,58±0,71 до 3,45±0,63 ммоль/л), триглицеридов (с 2,27±0,48 до 1,62±0,44 ммоль/л) и повышение ЛПВП (с 1,14±0,22 до 1,44±0,27 ммоль/л). Эти данные подтверждаются результатами метаанализа R. Tabrizi и соавт., включавшего 14 РКИ, который продемонстрировал значимое снижение триглицеридов (СРС -1,24; 95% ДИ -1,84–-0,64; p<0,001), общего холестерина (СРС -1,09; 95% ДИ -1,83–-0,55; p<0,001) и ЛПНП (СРС -1,31; 95% ДИ -2,04–-0,59; p<0,001) при применении инозитолов у пациентов с метаболическими заболеваниями [25]. Комбинированная терапия мио-инозитолом и DCI, по данным М. Minozzi и соавт., улучшает показатели липидного профиля и снижает кардиоваскулярный риск у женщин с СПКЯ [26].
Важным аспектом патогенеза ГЭ является хроническое низкоинтенсивное воспаление. Исследование А. Kubyshkin и соавт. продемонстрировало, что уровни провоспалительных цитокинов ИЛ-1β, ИЛ-6 и ФНО-α прогрессивно возрастают по мере усиления тяжести ГЭ, что свидетельствует о ключевой роли воспалительных процессов в прогрессировании патологии [34]. В нашем исследовании на фоне применения DCI отмечена нормализация как провоспалительных (ИЛ-1β, ФНО-α, ИЛ-8, ИЛ-17), так и противовоспалительных цитокинов (ИЛ-4, ИЛ-13, ИЛ-25, ИЛ-37). Противовоспалительные свойства инозитолов подтверждены экспериментальными исследованиями Y. Wee и соавт., показавшими, что инозитолгексафосфат подавляет экспрессию провоспалительных цитокинов ИЛ-1β и ИЛ-6, индуцированных липополисахаридом [28]. M. Baldassarre и соавт. продемонстрировали, что мио-инозитол уменьшает воспаление и окислительный стресс в эндотелиальных клетках, подвергшихся хронической гипергликемии [29].
Снижение уровня СРБ с 6,31±1,41 до 2,86±1,26 мг/л (в 2,2 раза) в группе DCI также свидетельствует об уменьшении системного воспаления, что имеет важное значение с учетом связи СРБ с повышенным риском развития ГЭ и рака эндометрия [10]. P. Huang и соавт. показали, что хроническое воспаление, ассоциированное с ожирением, способствует метаболическому репрограммированию глюкозы в эндометрии, создавая условия для пролиферации и злокачественной трансформации [10].
Динамика ИГХ-маркеров в нашем исследовании отражает воздействие DCI на ключевые патогенетические звенья ГЭ. Снижение индекса пролиферации Ki-67 до референсных значений (9,8±4,5% при норме <10%) в группе комбинированной терапии свидетельствует о подавлении избыточной пролиферативной активности эндометрия. Нормализация экспрессии VEGF (1,83±0,53 у.е.) указывает на уменьшение патологического ангиогенеза, который играет существенную роль в прогрессировании гиперпластических процессов эндометрия [8]. Снижение экспрессии p53 в эпителиоцитах маточных желез отражает уменьшение клеточного стресса и восстановление нормальной клеточной регуляции.
Сравнительный анализ с другими подходами к адъювантной терапии ГЭ представляет значительный интерес. Добавление метформина к гестагенотерапии исследовалось в ряде РКИ и метаанализов. Согласно систематическому обзору R. Shao и соавт., комбинированная терапия гестагенами и метформином улучшает частоту полного ответа (ОШ 2,08; 95% ДИ 1,29–3,34; p=0,003) по сравнению с монотерапией гестагенами [35]. Однако влияние метформина на частоту рецидивов остается неоднозначным. В метаанализе J. Chae-Kim и соавт. добавление метформина снижало частоту рецидивов (ОШ 0,46; 95% ДИ 0,24–0,91; p=0,03), но не влияло на частоту ремиссий [36]. Двойное слепое плацебо-контролируемое исследование A. Tehranian и соавт. продемонстрировало, что добавление метформина к мегестролу ацетату повышает частоту ответа с 70,4 до 93,1% при ГЭ без атипии [37]. Наши результаты (86,7% vs 60,0% полного регресса; 10,0% vs 36,7% рецидивов) сопоставимы с эффективностью комбинации гестаген + метформин, что позволяет рассматривать DCI как перспективную альтернативу для адъювантной терапии ГЭ.
Преимуществом DCI является его благоприятный профиль безопасности. В нашем исследовании частота нежелательных явлений была статистически значимо ниже в группе комбинированной терапии: ациклические кровянистые выделения (6,7% vs 30,0%; p=0,042), циклическая масталгия (3,3% vs 26,7%; p=0,026), головные боли (6,7% vs 33,3%; p=0,021), тошнота (6,7% vs 30,0%; p=0,042). Данные результаты согласуются с литературными данными об отличной переносимости инозитолов. Согласно консенсусу экспертной группы EGOI (Experts Group on Inositol in Basic and Clinical Research), инозитолы демонстрируют превосходный профиль безопасности по сравнению с другими инсулиносенситизирующими препаратами, такими как метформин, для которого характерны гастроинтестинальные побочные эффекты [24].
Снижение частоты побочных эффектов гестагенотерапии на фоне приема DCI может объясняться несколькими механизмами. Во-первых, улучшение метаболического профиля и снижение массы тела (ИМТ снизился с 30,4±2,3 до 28,9±2,4 кг/м² в группе DCI) могут способствовать лучшей переносимости гормональной терапии. Во-вторых, противовоспалительное действие DCI может уменьшать выраженность системных побочных эффектов. В-третьих, стабилизация гормонального фона на фоне коррекции ИР может снижать риск ациклических кровотечений и масталгии.
Результаты нашего исследования вносят вклад в развитие концепции мультитаргетной терапии ГЭ, направленной на одновременное воздействие на несколько патогенетических звеньев заболевания. DCI, обладая инсулиносенситизирующим, гиполипидемическим и противовоспалительным действием, воздействует на ключевые метаболические нарушения, лежащие в основе развития и рецидивирования ГЭ. Данный подход соответствует современным тенденциям в онкопрофилактике, подчеркивающим важность коррекции модифицируемых факторов риска [5].
Заключение
Результаты рандомизированного плацебо-контролируемого исследования свидетельствуют о том, что добавление DCI в дозе 1200 мг/сут к стандартной терапии норэтистерона ацетатом значительно повышает эффективность лечения ГЭ без атипии у женщин с избыточной массой тела и ожирением. Комбинированная терапия обеспечивает более высокую частоту полного морфологического регресса (86,7% vs 60,0%) и существенное снижение риска рецидивирования (10,0% vs 36,7%) по сравнению с монотерапией гестагенами. Механизм действия DCI реализуется через коррекцию ИР, нормализацию липидного профиля и цитокинового баланса, что приводит к снижению пролиферативной активности и патологического ангиогенеза в эндометрии. Благоприятный профиль безопасности и снижение частоты побочных эффектов гестагенотерапии позволяют рекомендовать DCI в качестве патогенетически обоснованного компонента комплексной терапии ГЭ без атипии у женщин с метаболическими нарушениями.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is not conflict of interests.
Список литературы доступен на сайте журнала https://klin-razbor.ru/
The list of references is available on the journal‘s website https://klin-razbor.ru/
Информация об авторах
Information about the authors
Радзинский Виктор Евсеевич – акад. РАН, д-р мед. наук, проф., зав. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН, засл. деят. науки РФ. E-mail: radzinskiy@mail.ru; ORCID: 0000-0002-7428-0469
Viktor E. Radzinskiy – Acad. RAS, Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: radzinskiy@mail.ru; ORCID: 0000-0002-7428-0469
Михалева Людмила Михайловна – чл.-кор. РАН, д-р мед. наук, проф., дир. НИИМЧ им. акад. А.П. Авцына ФГБНУ «РНЦХ им. акад. Б.В. Петровского», засл. деят. науки РФ.
E-mail: mikhalevam@yandex.ru; ORCID: 0000-0003-2052-914X; SPIN-код: 2086-7513
Liudmila M. Mikhaleva – Corr. Memb. RAS, Dr. Sci. (Med.), Professor, Director of Avtsyn Research Institute of Human Morphology of Petrovsky National Research Centre of Surgery. E-mail: mikhalevam@yandex.ru; ORCID: 0000-0003-2052-914X; SPIN code: 2086-7513
Хамошина Марина Борисовна – д-р мед. наук, проф., проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН, засл. деят. науки РФ.
E-mail: khamoshina@mail.ru; ORCID: 0000-0003-1940-4534
Marina B. Khamoshina – Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: khamoshina@mail.ru; ORCID: 0000-0003-1940-4534
Костин Игорь Николаевич – д-р мед. наук, проф., проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: bigbee62@mail.ru
Igor N. Kostin – Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: bigbee62@mail.ru
Оразов Мекан Рахимбердыевич – д-р мед. наук, проф., проф. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: omekan@mail.ru; ORCID: 0000-0002-5342-8129
Mekan R. Orazov – Dr. Sci. (Med.), Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: omekan@mail.ru; ORCID: 0000-0002-5342-8129
Орехов Роман Евгеньевич – канд. мед. наук, доц. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: romanorekhovv@ya.ru
Roman E. Orekhov – Cand. Sci. (Med.), Associate Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: romanorekhovv@ya.ru
Ахматова Анастасия Николаевна – канд. мед. наук, доц. каф. акушерства и гинекологии с курсом перинатологии Медицинского института ФГАОУ ВО РУДН. E-mail: achmatova02@mail.ru
Anastasiia N. Akhmatova – Cand. Sci. (Med.), Associate Professor, Patrice Lumumba Peoples' Friendship University of Russia. E-mail: achmatova02@mail.ru
Муллина Ирина Александровна – канд. мед. наук, врач акушер-гинеколог гинекологического отд-ния ЧУЗ «КБ "РЖД-Медицина" им. Н.А. Семашко». E-mail: 211irina2111@gmail.com
Irina A. Mullina – Cand. Sci. (Med.), Semashko Clinical Hospital “Russian Railways-Medicine”.
E-mail: 211irina2111@gmail.com
Поступила в редакцию: 19.01.2026
Поступила после рецензирования: 20.01.2026
Принята к публикации: 22.01.2026
Received: 19.01.2026
Revised: 20.01.2026
Accepted: 22.01.2026
Список исп. литературыСкрыть список1. Reed SD, Newton KM, Clinton WL et al. Incidence of endometrial hyperplasia. Am J Obstet Gynecol 2009;200(6):678.e1-678.e6786. DOI: 10.1016/j.ajog.2009.02.032
2. Galani A, Stavros S, Moustakli E et al. Endometrial Hyperplasia: Current Insights into Epidemiology, Risk Factors, and Clinical Management. Cancers 2026;(18):148. DOI: 10.3390/cancers18010148
3. Mikes BA, Vadakekut ES, Sparzak PB. Abnormal Uterine Bleeding. In: StatPearls. Treasure Island (FL): StatPearls Publishing, 2025.
4. Farzaneh F, Mirgaloybayat S, Niazi AA et al. Prevalence of Endometrial Hyperplasia and Its Related Factors in Patients with AUB. J Obstet Gynecol Cancer Res 2024;9(3):311-6. DOI: 10.30699/jogcr.9.3.311
5. Beavis AL, Blechter B, Najjar O et al. Identifying women 45 years and younger at elevated risk for endometrial hyperplasia or cancer. Gynecol Oncol 2023;(174):98-105. DOI: 10.1016/j.ygyno.2023.04.019
6. Li X, Fan Y, Wang J et al. Insulin Resistance and Metabolic Syndrome Increase the Risk of Relapse For Fertility Preserving Treatment in Atypical Endometrial Hyperplasia and Early Endometrial Cancer Patients. Front Oncol 2021;(11):744689. DOI: 10.3389/fonc.2021.744689
7. Li X, Shao R. PCOS and obesity: insulin resistance might be a common etiology for the development of type I endometrial carcinoma. Am J Cancer Res 2014;4(1):73-9.
8. Ordeanu IM, Busuioc CJ, Văduva CC et al. Obesity as a Catalyst for Endometrial Hyperplasia and Cancer Progression: A Narrative Review of Epidemiology, Molecular Pathways, and Prevention. Biomedicines 2025;13(11):2612. DOI: 10.3390/biomedicines13112612
9. Yang X, Wang J. The Role of Metabolic Syndrome in Endometrial Cancer: A Review. Front Oncol 2019;(9):744. DOI: 10.3389/fonc.2019.00744
10. Huang P, Fan X, Yu H et al. Glucose metabolic reprogramming and its therapeutic potential in obesity-associated endometrial cancer. J Transl Med 2023;21(1):94. DOI: 10.1186/s12967-022-03851-4
11. Tylutka A, Walas Ł, Zembron-Lacny A. Level of IL-6, TNF, and IL-1β and age-related diseases: a systematic review and meta-analysis. Front Immunol 2024;(15):1330386. DOI: 10.3389/fimmu.2024.1330386
12. Popko K, Gorska E, Stelmaszczyk-Emmel A et al. Proinflammatory cytokines Il-6 and TNF-α and the development of inflammation in obese subjects. Eur J Med Res 2010;15(Suppl.2):120-2. DOI: 10.1186/2047-783x-15-s2-120
13. Henderson I, Black N, Khattak H; UKARCOG Working Group Authors; Gupta JK, Rimmer MP. Diagnosis and management of endometrial hyperplasia: A UK national audit of adherence to national guidance 2012-2020. PLoS Med 2024;21(2):e1004346. DOI: 10.1371/journal.pmed.1004346
14. Sletten ET, Arnes M, Lysa LM et al. Prediction of Relapse After Therapy Withdrawal in Women with Endometrial Hyperplasia: A Long-term Follow-up Study. Anticancer Res 2017;37(5):2529-36. DOI: 10.21873/anticanres.11595
15. Management of Endometrial Intraepithelial Neoplasia or Atypical Endometrial Hyperplasia: ACOG Clinical Consensus No. 5. Obstet Gynecol 2023;142(3):735-44. DOI: 10.1097/AOG.0000000000005297
16. Choi CH, Lee YY, Lai YL et al. Outcomes of extended progestin therapy in atypical endometrial hyperplasia patients without an initial response to progestin: a retrospective study from two tertiary centers in Korea and Taiwan. J Gynecol Oncol 2025;36(2):e18. DOI: 10.3802/jgo.2025.36.e18
17. Yin J, Ma S, Shan Y et al. Risk Factors for Recurrence in Patients with Atypical Endometrial Hyperplasia and Endometrioid Adenocarcinoma after Fertility-Sparing Treatments. Cancer Prev Res (Phila) 2020;13(4):403-10. DOI: 10.1158/1940-6207.CAPR-19-0399
18. Kalra B, Kalra S, Sharma JB. The inositols and polycystic ovary syndrome. Indian J Endocrinol Metab 2016;20(5):720-4. DOI: 10.4103/2230-8210.189231
19. Montt-Guevara MM, Finiguerra M, Marzi I et al. D-Chiro-Inositol Regulates Insulin Signaling in Human Adipocytes. Front Endocrinol (Lausanne) 2021;(12):660815. DOI: 10.3389/fendo.2021.660815
20. Nestler JE, Jakubowicz DJ, Reamer P et al. Ovulatory and metabolic effects of D-chiro-inositol in the polycystic ovary syndrome. N Engl J Med. 999;340(17):1314-20. DOI: 10.1056/NEJM199904293401703
21. Larner J, Brautigan DL, Thorner MO. D-chiro-inositol glycans in insulin signaling and insulin resistance. Mol Med 2010;16(11-12):543-52. DOI:10.2119/molmed.2010.00107
22. Baillargeon JP, Diamanti-Kandarakis E, Ostlund RE Jr et al. Altered D-chiro-inositol urinary clearance in women with polycystic ovary syndrome. Diabetes Care 2006;29(2):300-5. DOI: 10.2337/diacare. 29.02.06.dc05-1070
23. Sun TH, Heimark DB, Nguygen T et al. Both myo-inositol to chiro-inositol epimerase activities and chiro-inositol to myo-inositol ratios are decreased in tissues of GK type 2 diabetic rats compared to Wistar controls. Biochem Biophys Res Commun 2002;293(3):1092-8. DOI: 10.1016/S0006-291X(02)00313-3
24. Dinicola S et al. Chiro-Inositol in Clinical Practice: A Perspective from the Experts Group on Inositol in Basic and Clinical Research (EGOI). Gynecol Obstet Investig 2024;89(4):284-94. DOI: 10.1159/000536081
25. Tabrizi R, Ostadmohammadi V, Lankarani KB et al. The effects of inositol supplementation on lipid profiles among patients with metabolic diseases: a systematic review and meta-analysis of randomized controlled trials. Lipids Health Dis 2018;17(1):123. DOI: 10.1186/s12944-018-0779-4
26. Minozzi M, Nordio M, Pajalich R. The Combined therapy myo-inositol plus D-Chiro-inositol, in a physiological ratio, reduces the cardiovascular risk by improving the lipid profile in PCOS patients. Eur Rev Med Pharmacol Sci 2013;17(4):537-40.
27. Arefhosseini S, Roshanravan N, Asghari S et al. Expression of inflammatory genes, WBC-derived inflammatory biomarkers and liver function indices: Effects of myo-inositol supplementation in obese patients with NAFLD. J Funct Foods 2023;(104):105524. DOI: 10.1016/j.jff.2023.105524
28. Wee Y, Yang CH, Chen SK et al. Inositol hexaphosphate modulates the behavior of macrophages through alteration of gene expression involved in pathways of pro- and anti-inflammatory responses, and resolution of inflammation pathways. Food Sci Nutr 2021;9(6):3240-9. DOI: 10.1002/fsn3.2286
29. Baldassarre MPA, Di Tomo P, Centorame G et al. Myoinositol Reduces Inflammation and Oxidative Stress in Human Endothelial Cells Exposed In Vivo to Chronic Hyperglycemia. Nutrients 2021;13(7):2210. DOI: 10.3390/nu13072210
30. Gallos ID, Krishan P, Shehmar M et al. LNG-IUS versus oral progestogen treatment for endometrial hyperplasia: a long-term comparative cohort study. Hum Reprod 2013;28(11):2966-71. DOI: 10.1093/humrep/det320
31. Gallos ID, Shehmar M, Thangaratinam S et al. Oral progestogens vs levonorgestrel-releasing intrauterine system for endometrial hyperplasia: a systematic review and metaanalysis. Am J Obstet Gynecol 2010;203(6). DOI: 10.1016/j.ajog.2010.07.037
32. Wu Y, Wang J, Fan Y et al. Metabolic syndrome combined with insulin resistance showed great predictive value in evaluating recurrence in patients with atypical endometrial hyperplasia and early endometrial cancer. BMC Cancer 2025;25(1):1094. DOI: 10.1186/ s12885-025-14481-6
33. Pintaudi B, Di Vieste G, Bonomo M. The Effectiveness of Myo-Inositol and D-Chiro Inositol Treatment in Type 2 Diabetes. Int J Endocrinol 2016;(2016):9132052. DOI: 10.1155/2016/9132052
34. Kubyshkin AV, Aliev LL, Fomochkina II et al. Endometrial hyperplasia-related inflammation: its role in the development and progression of endometrial hyperplasia. Inflamm Res 2016;65(10):785-94. DOI: 10.1007/s00011-016-0960-z
35. Shao F, Li Y, Zhao Y. Progestin plus metformin improves outcomes in patients with endometrial hyperplasia and early endometrial cancer more than progestin alone: a meta-analysis. Front Endocrinol (Lausanne) 2023;(14):1139858. DOI: 10.3389/fendo.2023.1139858
36. Chae-Kim J, Garg G, Gavrilova-Jordan L et al. Outcomes of women treated with progestin and metformin for atypical endometrial hyperplasia and early endometrial cancer: a systematic review and meta-analysis. Int J Gynecol Cancer 2021;31(12):1499-505. DOI: 10.1136/ijgc-2021-002699
37. Tehranian A, Ghahghaei-Nezamabadi A, Arab M et al. The impact of adjunctive metformin to progesterone for the treatment of non-atypical endometrial hyperplasia in a randomized fashion, a placebo-controlled, double blind clinical trial. J Gynecol Obstet Hum Reprod 2021;50(6):101863. DOI: 10.1016/j.jogoh.2020.101863
38. Bizzarri M, Monti N, Piombarolo A et al. Myo-Inositol and D-Chiro-Inositol as Modulators of Ovary Steroidogenesis: A Narrative Review. Nutrients 2023;(15)L1875. DOI: 10.3390/nu15081875
21 апреля 2026
Количество просмотров: 135
