Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№01 2012
Возможность комбинированной терапии депрессий мелатонинергическим и трициклическими антидепрессантами №01 2012
Номера страниц в выпуске:53-56
Полученные в ходе исследования «Время» данные свидетельствуют о том, что комбинированное применение Вальдоксана с амитриптилином в рамках клинической купирующей и поддерживающей терапии умеренных и тяжелых депрессий непсихотического уровня принципиально возможно, является эффективным и не вызывает серьезных побочных эффектов. Это наблюдение представляется важным в свете решения задач по преодолению резистентности к антидепрессивной фармакотерапии, оптимизации длительной поддерживающей (профилактической противорецидивной) терапии аффективных расстройств и повышению показателей приверженности терапии.
Резюме. Полученные в ходе исследования «Время» данные свидетельствуют о том, что комбинированное применение Вальдоксана с амитриптилином в рамках клинической купирующей и поддерживающей терапии умеренных и тяжелых депрессий непсихотического уровня принципиально возможно, является эффективным и не вызывает серьезных побочных эффектов. Это наблюдение представляется важным в свете решения задач по преодолению резистентности к антидепрессивной фармакотерапии, оптимизации длительной поддерживающей (профилактической противорецидивной) терапии аффективных расстройств и повышению показателей приверженности терапии.
Ключевые слова: антидепрессант, комбинированная терапия.
Possibility of combined antidepressive therapy with melatonergic and tricyclic antidepressants
V.E.Medvedev
Russian University of People’s Friendship, Moscow
Summary. According to data received from the study «Vremya» combined therapy of moderate and severe non-psychotic depressions with Valdoxan and amitriptyline (for reduction of depression and maintenance therapy) is possible, effective and doesn’t cause serious adverse events. These facts are of great importance for therapeutic resistance negotiation, for optimization of maintenance therapy of affective disorders and for better compliance.
Key words: antidepressant, combined therapy.
Подбор эффективной психофармакотерапии для лечения тяжелых депрессий до настоящего времени является одной из основных проблем клинической психиатрии. С одной стороны, до 30% больных большой депрессией не поддаются лечению антидепрессантом первого выбора, назначенным в адекватной дозе на период, достаточный для получения лечебного эффекта [2, 12]. При этом эффективность монотерапии антидепрессантами разных поколений не превышает 60–70% [20, 25].
С другой стороны, зачастую достижение клинически значимого эффекта при назначении антидепрессантов ограничивается возникновением нежелательных реакций, приводящих к снижению комплаенса и преждевременному отказу пациентов от терапии [31, 35]. Так, в ряде публикаций сообщается, что в рамках первичной медицинской помощи из-за развития побочных эффектов трициклические антидепрессанты (ТЦА) часто назначаются в меньших дозах, чем рекомендовано по результатам рандомизированных клинических исследований [16]. По этой же причине 88% пациентов принимают ТЦА в дозах ниже рекомендованных национальными стандартами [17].
Еще одной проблемой при лечении депрессий является выбор тактики на этапе поддерживающей (профилактической) терапии, обусловленной желательностью и/или необходимостью перевода на антидепрессант с минимальным спектром побочных эффектов, но высокой эффективностью даже в низких или средних дозировках [22, 31, 32].
Для решения указанных задач обычным в клинической практике является назначение комбинации антидепрессантов [8, 12, 19, 20].
В литературе представлены данные о том, что высокая эффективность при лечении тяжелых депрессий и достижение стойкой ремиссии обеспечивается сочетанным применением ТЦА и селективных ингибиторов обратного захвата серотонина (СИОЗС) [29, 33, 34] или ингибиторов обратного захвата серотонина и норадреналина (СИОЗСН) [14, 23, 32].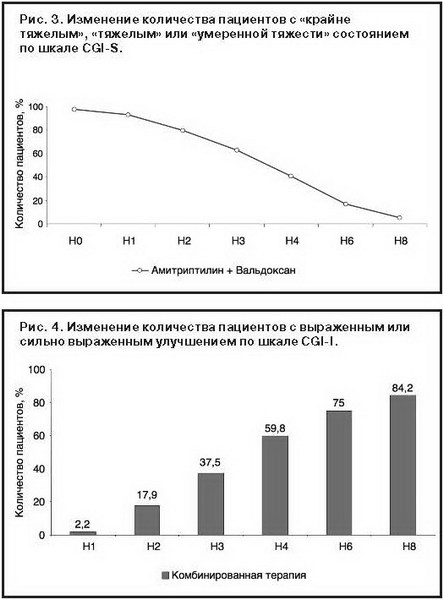 В то же время, по данным ряда исследователей, врачи опасаются применять подобные комбинации из-за возможной плохой переносимости, связанной с нежелательным фармакокинетическим взаимодействием ТЦА и антидепрессантов иных групп [5, 7, 15]. Основной механизм взаимодействия заключается в ингибировании одного из важнейших ферментов метаболизма ТЦА CYP2D6 препаратами СИОЗС и СИОЗСН [9, 13, 30]. Данные исследований in vitro позволяют ранжировать антидепрессанты по силе ингибирования этого фермента в следующем порядке: пароксетин → флуоксетин → сертралин → флувоксамин → венлафаксин → миртазапин [13, 33].
В то же время, по данным ряда исследователей, врачи опасаются применять подобные комбинации из-за возможной плохой переносимости, связанной с нежелательным фармакокинетическим взаимодействием ТЦА и антидепрессантов иных групп [5, 7, 15]. Основной механизм взаимодействия заключается в ингибировании одного из важнейших ферментов метаболизма ТЦА CYP2D6 препаратами СИОЗС и СИОЗСН [9, 13, 30]. Данные исследований in vitro позволяют ранжировать антидепрессанты по силе ингибирования этого фермента в следующем порядке: пароксетин → флуоксетин → сертралин → флувоксамин → венлафаксин → миртазапин [13, 33].
CYP2D6 считается одним из основных ферментов системы цитохрома Р-450 и отвечает за гидроксилирование, деметилирование и дальнейшее выведение ТЦА (в частности, амитриптилина) из организма [13].
Таким образом, подавляя активность CYP2D6, многие антидепрессанты способствуют повышению концентрации ТЦА в плазме крови, увеличивая тем самым риск возникновения серьезных побочных эффектов – тремора, дизартрии, симптомов сердечно-сосудистой токсичности1 [10, 11, 18].
В этой связи представляет особый интерес изучение возможности и эффективности комбинированного применения ТЦА с мелатонинергическим тимолептиком Вальдоксаном (агомелатин), характеризующимся принципиально иным, чем у СИОЗС или СИОЗСН, механизмом действия, хорошей общей переносимостью и отсутствием или минимальным влиянием на основные гемодинамические показатели [3, 4, 24, 26].
В одном из крупнейших исследований эффективности и переносимости Вальдоксана в рамках купирующей и поддерживающей терапии умеренных и тяжелых депрессий непсихотического уровня, назначаемой в рутинной клинической практике психиатрического стационара («Время», национальный координатор – доктор медицинских наук, профессор Б.Д.Цыганков), прошедшем с осени 2009 г. по весну 2010 г. в 50 регионах Российской Федерации, приняли участие 1842 пациента от 18 до 80 лет [520 (28,2%) мужчин, 1322 (71,8%) женщины; средний возраст 44 года] [6]. В исследовании наряду c пациентами, находящимися на монотерапии Вальдоксаном, часть больных (n=171) получали комбинированное лечение амитриптилином и Вальдоксаном.
Для оценки динамики состояния пациентов в ходе 8 нед терапии использовались международные валидизированные шкалы: депрессии Гамильтона (HAMD-21), оценки общего клинического впечатления для оценки тяжести заболевания CGI-S и оценки общего клинического впечатления для оценки изменения состояния пациента CGI-I.
Критериями эффективности считались: снижение балла по шкале HAMD-21 на 50% и более, снижение балла после окончания лечения на 2 пункта и более по шкале CGI-S и/или выставления балла «4» (небольшое улучшение) после 1 и 2-й недели терапии и баллов «5» (выраженное улучшение) и «6» (значительно выраженное улучшение) после 4 и 8-й недели терапии по шкале CGI-I.
В программу не включались больные с основным диагнозом «шизофрения», «шизоаффективное расстройство», «органическое поражение центральной нервной системы», страдающие алкоголизмом или наркоманией, а также пациенты с наличием суицидального риска (более 2 баллов по пункту 3 шкалы HAMD-21 и/или по клинической оценке исследователя).
В группу комбинированной терапии (амитриптилин + Вальдоксан) были включены пациенты 19–72 лет (средний возраст 44,7±12,1 года) обоего пола (70,8% женщин, 29,2% мужчин).
У большинства пациентов этой группы диагностировались: рекуррентное депрессивное расстройство, текущий эпизод средней (F33.1; 28,4%) или тяжелой (F33.2; 17,3%) степени без психотических симптомов, единичный депрессивный эпизод средней (F32.1; 21,8%) или тяжелой (F32.2; 19,9%) степени без психотических симптомов, а также биполярное аффективное расстройство, текущий эпизод средней (F31.3; 6,5%) или тяжелой (F31.4; 4,6%) степени без психотических симптомов. Возраст манифестации аффективного заболевания в группе составлял 17–65 лет (средний возраст 38,3±11,5 года). Длительность психического заболевания – от 0,1 до 41 года (средняя длительность 6,8±7,8 года). Средняя длительность текущего депрессивного эпизода 2,9±3,5 мес.
Возраст манифестации аффективного заболевания в группе составлял 17–65 лет (средний возраст 38,3±11,5 года). Длительность психического заболевания – от 0,1 до 41 года (средняя длительность 6,8±7,8 года). Средняя длительность текущего депрессивного эпизода 2,9±3,5 мес.
Средняя сумма баллов в группе по шкале депрессии Гамильтона при включении в исследование достигала 27,6±7,3 балла.
Полностью завершили 8-недельный курс комбинированной терапии 85,2% пациентов, что косвенно указывает на хорошую переносимость сочетанного применения амитриптилина и агомелатина.
По мнению исследователей, в ходе комбинированной терапии для достижения клинической эффективности 54,6% больных потребовалось увеличение дозы антидепрессанта, которое осуществлялось за счет Вальдоксана (с 25 до 50 мг/ночь).
К моменту окончания исследования средняя сумма баллов по шкале депрессии Гамильтона статистически значимо снизилась в 4,9 раза (с 28,0±7,5 до 5,7±5,1; p<0,00001). При этом сумма баллов статистически достоверно уменьшалась уже начиная с 1-й недели терапии (р<0,00001) (рис.1).
Процент респондеров по принятым в исследовании критериям к концу 8-й недели терапии достиг 92,9% (рис. 2). При этом число ремиттеров (пациентов с суммой баллов не более 7 по шкале депрессии Гамильтона) также прогрессивно увеличивалось в ходе исследования (по данным авторов, до 69,6% [6]).
При анализе результатов психометрической оценки отдельных симптомов депрессии в группе выраженность «депрессивного настроения», «моторной заторможенности» или «ажитации», «психической» и «соматической» тревоги, «ипохондрических страхов», «нарушений работоспособности» и «активности», «чувства вины» и всех типов инсомнии (ранней, средней, поздней) в ходе терапии статистически значимо уменьшалась (р<0,00001), начиная со 2-й недели терапии (р≤0,000029).
Аналогичная тенденция наблюдалась авторами при оценке тяжести общих соматических, а также генитальных и желудочно-кишечных симптомов депрессии. По всем показателям зафиксировано статистически значимое улучшение (р<0,00001) после 1-й недели терапии (р≤0,010).
Помимо прочего, в ходе комбинированной терапии амитриптилином и Вальдоксаном отмечалась постепенная компенсация образовавшейся на фоне депресии потери массы тела (р<0,00001).
Кроме того, после 2 нед (р=0,019) терапии статистически значимо снижалась выраженность суточных колебаний самочувствия пациентов (р<0,00001).
При оценке по шкале CGI-S динамики тяжести депрессивного состояния в ходе терапии комбинацией амитриптилина с Вальдоксаном зарегистрировано статистически значимое уменьшение числа пациентов с «крайне тяжелым», «тяжелым» или «умеренно тяжелым» состоянием (рис. 3).
Сходные данные получены и при анализе влияния терапии на оценку изменения состояния пациентов по шкале CGI-I (рис. 4).
Переносимость терапии
У 32% больных переносимость комбинированной терапии врачи признали «отличной» (нежелательные реакции отсутствуют), у остальных 68% пациентов – «хорошей» (незначительные нежелательные реакции). Оценку «плохо» (выраженные нежелательные реакции) переносимости терапии не выставил никто из врачей.
В свою очередь, 33,2% пациентов оценили переносимость терапии как «отличную» (нежелательные реакции отсутствуют), 66,8% – как «хорошую» (незначительные нежелательные реакции).
Важно отметить, что 91,3% больных выразили желание продолжить курс лечения амитриптилином и Вальдоксаном. Влияние комбинированной терапии на основные соматические показатели пациентов реализовалось статистически достоверным увеличением массы тела (не выходящим, однако, за пределы массы, потерянной на фоне депрессии), незначительным с клинической точки зрения снижением частоты сердечных сокращений и уровня артериального давления.
В исследовании не было установлено статистически значимых изменений аспартатаминотрансферазы, аланинаминотрансферазы, щелочной фосфатазы и общего билирубина на фоне приема двух антидепрессантов.
Обсуждение
Полученные в ходе исследования «Время» данные свидетельствуют о том, что комбинированное применение Вальдоксана с амитриптилином в рамках клинической купирующей и поддерживающей терапии умеренных и тяжелых депрессий непсихотического уровня принципиально возможно, является эффективным и не вызывает серьезных побочных эффектов. Так, полностью завершили 8-недельный курс комбинированной терапии 85,2% пациентов. Средняя сумма баллов по шкале депрессии Гамильтона на протяжение 8 нед лечения статистически достоверно снижается, начиная с 1-й недели терапии
(с 28,0±7,5 до 5,7±5,1; р<0,00001). При этом значение каждого пункта шкалы депрессии Гамильтона статистически достоверно нивелируется, начиная с 1-й недели лечения.
Существенно, что полученные данные сопоставимы с результатами применения в этом же исследовании монотерапии депрессий Вальдоксаном (n=888). Хотя исходно тяжесть аффективного расстройства у пациентов, получавших только Вальдоксан, была статистически достоверно ниже (средняя сумма баллов по шкале депрессии Гамильтона HAMD-21 до начала лечения – 23,6±5,9 балла), чем в группе комбинированной терапии, эффективность терапии (число респондеров по принятым в исследовании критериям) составила 92,88%.
Это наблюдение представляется важным в свете решения задач по преодолению резистентности к антидепрессивной фармакотерапии, оптимизации длительной поддерживающей (профилактической противорецидивной) терапии аффективных расстройств и повышению показателей приверженности терапии (в том числе за счет уменьшения частоты возникновения и выраженности нежелательных реакций на фоне приема ТЦА).
Кроме того, имеющиеся результаты исследования позволяют сделать несколько предварительных допущений. Во-первых, назначение комбинации двух таких антидепрессантов с доказанной высокой эффективностью, как Вальдоксан и амитриптилин, можно осуществлять с тенденцией к уменьшению дозы последнего. Это позволит, не теряя в эффективности терапии, снизить вероятность возникновения нежелательных реакций и повысит комплаенс и приверженность терапии со стороны пациента.
Во-вторых, при уменьшении тяжести депрессивных симптомов на фоне комбинированной терапии возможен постепенный переход на монотерапию Вальдоксаном как препаратом с высокой эффективностью при менее тяжелых аффективных расстройствах и лучшими, чем у ами-триптилина, показателями переносимости.
Необходимо заметить, что обсуждаемое исследование «Время» имело ряд значимых ограничений. В частности, дизайном работы не была предусмотрена дифференцировка депрессивных состояний по ведущему психопатологическому синдрому. Не были собраны или представлены данные об использовавшихся в ходе терапии дозах амитриптилина и о причинах присоединения к схеме лечения Вальдоксана. Также снижает эффективность оценки результатов отсутствие детализации и количественных показателей частоты возникновения и выраженности нежелательных явлений.
Подводя итог, следует еще раз указать, что представленные в настоящем обзоре сведения, безусловно, носят предварительный характер, нуждаются в уточнении и могут приобрести реальный смысл в аспекте эффективной помощи больным только после проведения целенаправленных клинических, фармакоэпидемиологических и фармакоэкономических исследований.
Однако уже сейчас можно констатировать, что на современном этапе развития психофармакологии наметился пересмотр стратегии комбинированного использования антидепрессантов с различными механизмами действия.
Сведения об авторе
Медведев Владимир Эрнстович – канд. мед. наук, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПКМР РУДН. E-mail: melkorcard@mail.ru
Ключевые слова: антидепрессант, комбинированная терапия.
Possibility of combined antidepressive therapy with melatonergic and tricyclic antidepressants
V.E.Medvedev

Russian University of People’s Friendship, Moscow
Summary. According to data received from the study «Vremya» combined therapy of moderate and severe non-psychotic depressions with Valdoxan and amitriptyline (for reduction of depression and maintenance therapy) is possible, effective and doesn’t cause serious adverse events. These facts are of great importance for therapeutic resistance negotiation, for optimization of maintenance therapy of affective disorders and for better compliance.
Key words: antidepressant, combined therapy.
Подбор эффективной психофармакотерапии для лечения тяжелых депрессий до настоящего времени является одной из основных проблем клинической психиатрии. С одной стороны, до 30% больных большой депрессией не поддаются лечению антидепрессантом первого выбора, назначенным в адекватной дозе на период, достаточный для получения лечебного эффекта [2, 12]. При этом эффективность монотерапии антидепрессантами разных поколений не превышает 60–70% [20, 25].
С другой стороны, зачастую достижение клинически значимого эффекта при назначении антидепрессантов ограничивается возникновением нежелательных реакций, приводящих к снижению комплаенса и преждевременному отказу пациентов от терапии [31, 35]. Так, в ряде публикаций сообщается, что в рамках первичной медицинской помощи из-за развития побочных эффектов трициклические антидепрессанты (ТЦА) часто назначаются в меньших дозах, чем рекомендовано по результатам рандомизированных клинических исследований [16]. По этой же причине 88% пациентов принимают ТЦА в дозах ниже рекомендованных национальными стандартами [17].
Еще одной проблемой при лечении депрессий является выбор тактики на этапе поддерживающей (профилактической) терапии, обусловленной желательностью и/или необходимостью перевода на антидепрессант с минимальным спектром побочных эффектов, но высокой эффективностью даже в низких или средних дозировках [22, 31, 32].
Для решения указанных задач обычным в клинической практике является назначение комбинации антидепрессантов [8, 12, 19, 20].
В литературе представлены данные о том, что высокая эффективность при лечении тяжелых депрессий и достижение стойкой ремиссии обеспечивается сочетанным применением ТЦА и селективных ингибиторов обратного захвата серотонина (СИОЗС) [29, 33, 34] или ингибиторов обратного захвата серотонина и норадреналина (СИОЗСН) [14, 23, 32].
 В то же время, по данным ряда исследователей, врачи опасаются применять подобные комбинации из-за возможной плохой переносимости, связанной с нежелательным фармакокинетическим взаимодействием ТЦА и антидепрессантов иных групп [5, 7, 15]. Основной механизм взаимодействия заключается в ингибировании одного из важнейших ферментов метаболизма ТЦА CYP2D6 препаратами СИОЗС и СИОЗСН [9, 13, 30]. Данные исследований in vitro позволяют ранжировать антидепрессанты по силе ингибирования этого фермента в следующем порядке: пароксетин → флуоксетин → сертралин → флувоксамин → венлафаксин → миртазапин [13, 33].
В то же время, по данным ряда исследователей, врачи опасаются применять подобные комбинации из-за возможной плохой переносимости, связанной с нежелательным фармакокинетическим взаимодействием ТЦА и антидепрессантов иных групп [5, 7, 15]. Основной механизм взаимодействия заключается в ингибировании одного из важнейших ферментов метаболизма ТЦА CYP2D6 препаратами СИОЗС и СИОЗСН [9, 13, 30]. Данные исследований in vitro позволяют ранжировать антидепрессанты по силе ингибирования этого фермента в следующем порядке: пароксетин → флуоксетин → сертралин → флувоксамин → венлафаксин → миртазапин [13, 33].
CYP2D6 считается одним из основных ферментов системы цитохрома Р-450 и отвечает за гидроксилирование, деметилирование и дальнейшее выведение ТЦА (в частности, амитриптилина) из организма [13].
Таким образом, подавляя активность CYP2D6, многие антидепрессанты способствуют повышению концентрации ТЦА в плазме крови, увеличивая тем самым риск возникновения серьезных побочных эффектов – тремора, дизартрии, симптомов сердечно-сосудистой токсичности1 [10, 11, 18].
В этой связи представляет особый интерес изучение возможности и эффективности комбинированного применения ТЦА с мелатонинергическим тимолептиком Вальдоксаном (агомелатин), характеризующимся принципиально иным, чем у СИОЗС или СИОЗСН, механизмом действия, хорошей общей переносимостью и отсутствием или минимальным влиянием на основные гемодинамические показатели [3, 4, 24, 26].
В одном из крупнейших исследований эффективности и переносимости Вальдоксана в рамках купирующей и поддерживающей терапии умеренных и тяжелых депрессий непсихотического уровня, назначаемой в рутинной клинической практике психиатрического стационара («Время», национальный координатор – доктор медицинских наук, профессор Б.Д.Цыганков), прошедшем с осени 2009 г. по весну 2010 г. в 50 регионах Российской Федерации, приняли участие 1842 пациента от 18 до 80 лет [520 (28,2%) мужчин, 1322 (71,8%) женщины; средний возраст 44 года] [6]. В исследовании наряду c пациентами, находящимися на монотерапии Вальдоксаном, часть больных (n=171) получали комбинированное лечение амитриптилином и Вальдоксаном.
Для оценки динамики состояния пациентов в ходе 8 нед терапии использовались международные валидизированные шкалы: депрессии Гамильтона (HAMD-21), оценки общего клинического впечатления для оценки тяжести заболевания CGI-S и оценки общего клинического впечатления для оценки изменения состояния пациента CGI-I.
Критериями эффективности считались: снижение балла по шкале HAMD-21 на 50% и более, снижение балла после окончания лечения на 2 пункта и более по шкале CGI-S и/или выставления балла «4» (небольшое улучшение) после 1 и 2-й недели терапии и баллов «5» (выраженное улучшение) и «6» (значительно выраженное улучшение) после 4 и 8-й недели терапии по шкале CGI-I.
В программу не включались больные с основным диагнозом «шизофрения», «шизоаффективное расстройство», «органическое поражение центральной нервной системы», страдающие алкоголизмом или наркоманией, а также пациенты с наличием суицидального риска (более 2 баллов по пункту 3 шкалы HAMD-21 и/или по клинической оценке исследователя).
В группу комбинированной терапии (амитриптилин + Вальдоксан) были включены пациенты 19–72 лет (средний возраст 44,7±12,1 года) обоего пола (70,8% женщин, 29,2% мужчин).
У большинства пациентов этой группы диагностировались: рекуррентное депрессивное расстройство, текущий эпизод средней (F33.1; 28,4%) или тяжелой (F33.2; 17,3%) степени без психотических симптомов, единичный депрессивный эпизод средней (F32.1; 21,8%) или тяжелой (F32.2; 19,9%) степени без психотических симптомов, а также биполярное аффективное расстройство, текущий эпизод средней (F31.3; 6,5%) или тяжелой (F31.4; 4,6%) степени без психотических симптомов.
 Возраст манифестации аффективного заболевания в группе составлял 17–65 лет (средний возраст 38,3±11,5 года). Длительность психического заболевания – от 0,1 до 41 года (средняя длительность 6,8±7,8 года). Средняя длительность текущего депрессивного эпизода 2,9±3,5 мес.
Возраст манифестации аффективного заболевания в группе составлял 17–65 лет (средний возраст 38,3±11,5 года). Длительность психического заболевания – от 0,1 до 41 года (средняя длительность 6,8±7,8 года). Средняя длительность текущего депрессивного эпизода 2,9±3,5 мес.
Средняя сумма баллов в группе по шкале депрессии Гамильтона при включении в исследование достигала 27,6±7,3 балла.
Полностью завершили 8-недельный курс комбинированной терапии 85,2% пациентов, что косвенно указывает на хорошую переносимость сочетанного применения амитриптилина и агомелатина.
По мнению исследователей, в ходе комбинированной терапии для достижения клинической эффективности 54,6% больных потребовалось увеличение дозы антидепрессанта, которое осуществлялось за счет Вальдоксана (с 25 до 50 мг/ночь).
К моменту окончания исследования средняя сумма баллов по шкале депрессии Гамильтона статистически значимо снизилась в 4,9 раза (с 28,0±7,5 до 5,7±5,1; p<0,00001). При этом сумма баллов статистически достоверно уменьшалась уже начиная с 1-й недели терапии (р<0,00001) (рис.1).
Процент респондеров по принятым в исследовании критериям к концу 8-й недели терапии достиг 92,9% (рис. 2). При этом число ремиттеров (пациентов с суммой баллов не более 7 по шкале депрессии Гамильтона) также прогрессивно увеличивалось в ходе исследования (по данным авторов, до 69,6% [6]).
При анализе результатов психометрической оценки отдельных симптомов депрессии в группе выраженность «депрессивного настроения», «моторной заторможенности» или «ажитации», «психической» и «соматической» тревоги, «ипохондрических страхов», «нарушений работоспособности» и «активности», «чувства вины» и всех типов инсомнии (ранней, средней, поздней) в ходе терапии статистически значимо уменьшалась (р<0,00001), начиная со 2-й недели терапии (р≤0,000029).
Аналогичная тенденция наблюдалась авторами при оценке тяжести общих соматических, а также генитальных и желудочно-кишечных симптомов депрессии. По всем показателям зафиксировано статистически значимое улучшение (р<0,00001) после 1-й недели терапии (р≤0,010).
Помимо прочего, в ходе комбинированной терапии амитриптилином и Вальдоксаном отмечалась постепенная компенсация образовавшейся на фоне депресии потери массы тела (р<0,00001).
Кроме того, после 2 нед (р=0,019) терапии статистически значимо снижалась выраженность суточных колебаний самочувствия пациентов (р<0,00001).
При оценке по шкале CGI-S динамики тяжести депрессивного состояния в ходе терапии комбинацией амитриптилина с Вальдоксаном зарегистрировано статистически значимое уменьшение числа пациентов с «крайне тяжелым», «тяжелым» или «умеренно тяжелым» состоянием (рис. 3).
Сходные данные получены и при анализе влияния терапии на оценку изменения состояния пациентов по шкале CGI-I (рис. 4).
Переносимость терапии
У 32% больных переносимость комбинированной терапии врачи признали «отличной» (нежелательные реакции отсутствуют), у остальных 68% пациентов – «хорошей» (незначительные нежелательные реакции). Оценку «плохо» (выраженные нежелательные реакции) переносимости терапии не выставил никто из врачей.
В свою очередь, 33,2% пациентов оценили переносимость терапии как «отличную» (нежелательные реакции отсутствуют), 66,8% – как «хорошую» (незначительные нежелательные реакции).
Важно отметить, что 91,3% больных выразили желание продолжить курс лечения амитриптилином и Вальдоксаном. Влияние комбинированной терапии на основные соматические показатели пациентов реализовалось статистически достоверным увеличением массы тела (не выходящим, однако, за пределы массы, потерянной на фоне депрессии), незначительным с клинической точки зрения снижением частоты сердечных сокращений и уровня артериального давления.
В исследовании не было установлено статистически значимых изменений аспартатаминотрансферазы, аланинаминотрансферазы, щелочной фосфатазы и общего билирубина на фоне приема двух антидепрессантов.
Обсуждение
Полученные в ходе исследования «Время» данные свидетельствуют о том, что комбинированное применение Вальдоксана с амитриптилином в рамках клинической купирующей и поддерживающей терапии умеренных и тяжелых депрессий непсихотического уровня принципиально возможно, является эффективным и не вызывает серьезных побочных эффектов. Так, полностью завершили 8-недельный курс комбинированной терапии 85,2% пациентов. Средняя сумма баллов по шкале депрессии Гамильтона на протяжение 8 нед лечения статистически достоверно снижается, начиная с 1-й недели терапии
(с 28,0±7,5 до 5,7±5,1; р<0,00001). При этом значение каждого пункта шкалы депрессии Гамильтона статистически достоверно нивелируется, начиная с 1-й недели лечения.
Существенно, что полученные данные сопоставимы с результатами применения в этом же исследовании монотерапии депрессий Вальдоксаном (n=888). Хотя исходно тяжесть аффективного расстройства у пациентов, получавших только Вальдоксан, была статистически достоверно ниже (средняя сумма баллов по шкале депрессии Гамильтона HAMD-21 до начала лечения – 23,6±5,9 балла), чем в группе комбинированной терапии, эффективность терапии (число респондеров по принятым в исследовании критериям) составила 92,88%.
Это наблюдение представляется важным в свете решения задач по преодолению резистентности к антидепрессивной фармакотерапии, оптимизации длительной поддерживающей (профилактической противорецидивной) терапии аффективных расстройств и повышению показателей приверженности терапии (в том числе за счет уменьшения частоты возникновения и выраженности нежелательных реакций на фоне приема ТЦА).
Кроме того, имеющиеся результаты исследования позволяют сделать несколько предварительных допущений. Во-первых, назначение комбинации двух таких антидепрессантов с доказанной высокой эффективностью, как Вальдоксан и амитриптилин, можно осуществлять с тенденцией к уменьшению дозы последнего. Это позволит, не теряя в эффективности терапии, снизить вероятность возникновения нежелательных реакций и повысит комплаенс и приверженность терапии со стороны пациента.
Во-вторых, при уменьшении тяжести депрессивных симптомов на фоне комбинированной терапии возможен постепенный переход на монотерапию Вальдоксаном как препаратом с высокой эффективностью при менее тяжелых аффективных расстройствах и лучшими, чем у ами-триптилина, показателями переносимости.
Необходимо заметить, что обсуждаемое исследование «Время» имело ряд значимых ограничений. В частности, дизайном работы не была предусмотрена дифференцировка депрессивных состояний по ведущему психопатологическому синдрому. Не были собраны или представлены данные об использовавшихся в ходе терапии дозах амитриптилина и о причинах присоединения к схеме лечения Вальдоксана. Также снижает эффективность оценки результатов отсутствие детализации и количественных показателей частоты возникновения и выраженности нежелательных явлений.
Подводя итог, следует еще раз указать, что представленные в настоящем обзоре сведения, безусловно, носят предварительный характер, нуждаются в уточнении и могут приобрести реальный смысл в аспекте эффективной помощи больным только после проведения целенаправленных клинических, фармакоэпидемиологических и фармакоэкономических исследований.
Однако уже сейчас можно констатировать, что на современном этапе развития психофармакологии наметился пересмотр стратегии комбинированного использования антидепрессантов с различными механизмами действия.
Сведения об авторе
Медведев Владимир Эрнстович – канд. мед. наук, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПКМР РУДН. E-mail: melkorcard@mail.ru
Список исп. литературыСкрыть список1. Вальдоксан (Агомелатин) в терапии тяжелых и умеренных депрессий непсихотического уровня у пациентов психиатрического стационара. Статистический отчет обсервационного исследования «Время». М., 2010.
2. Иванов М.В., Мазо Г.Э. Полифармакотерапевтический подход к лечению резистентных депрессивных состояний. Усовершенствованная медицинская технология. СПб., 2007.
3. Медведев В.Э. Перспективы использования мелатонинергических препаратов в терапии депрессий у пациентов с сердечно-сосудистыми заболеваниями. Психиатр. и психофармакотер. 2010; 3: 19–23.
4. Медведев В.Э., Епифанов А.В. Инновационный метод терапии депрессий у пациентов с ишемической болезнью сердца. Обозрение психиатрии и мед. психологии им. В.М.Бехтерева. 2010; 3: 31–6.
5. Смулевич А.Б. Дифференцированная терапия при депрессиях и коморбидной патологии. Психиатр. и психофармакотер. 2001; 3: 76–9.
6. Цыганков Б.Д., Ялтонская А.В., Филиппских С.В. Вальдоксан (агомелатин) в терапии тяжелых и умеренных депрессий непсихотического уровня (результаты обсервационного исследования). 2011.
7. Ables AZ, Baughman OL. Antidepressants: update on new agents and indications. Am Family Physician 2003; 67: 547–54.
8. Anderson I, Tomenson B. A meta analysis if the efficacy of serotonin reuptake inhibitors compared to tricyclic antidepressants in depression. Neuropsychopharmacol 1994; 10 (Suppl.): 106.
9. Bymaster FP, Dreshfield A, Threlkeld PG et al. Comparative affinity of duloxetine and venlafaxine for serotonin and norepinephrine transporters in vitro and in vivo, hyman serotonin receptor subtypes, and other neuronal receptors. Neuropsychopharmacol 2001; 25: 871–80.
10. Buckley NA, McManus PR. Fatal toxicity of serotoninergic and other antidepressant drugs: analysis of United Kingdom mortality data. BMJ 2002; 325: 1332–3.
11. Cheeta S, Schifano F, Oyefeso A et al. Antidepressant-related deaths and antidepressant prescriptions in England and Wales, 1998–2000. The British J Psychiat 2004; 184: 41–7.
12. Cowen PJ. Pharmacological management of treatment-resistant depression. Advances in Psychiatric Treatment 1998; 4: 320–7.
13. Crewe HK, Lennard MS, Tucker GT et al. The effect of selective serotonin re-uptake inhibitors on cytochrome P4502D6 (CYP2D6) activity in human liver microsomes. British J Clin Pharmacol 1992; 34: 262–5.
14. Dardennes R, Berdeaux G, Lafuma A, Fagnani F. Comparison of the cost-effectiveness of milnacipran (a SNRI) with TCAs and SSRIs: a modeling approach. Eur Psychiat 1999; 14 (3): 152–62.
15. Depont F, Rambelomanana S, Puil S et al. Antidepressants: psychiatrists’ opinions and clinical practice. Acta Psychiat Scand 2003; 108: 24–31.
16. Donoghue JM, Taylor DM. Suboptimal use of antidepressants in the treatment of depression. CNS Drugs 2000; 13: 365–3.
17. Donoghue JM, Tylee A. The treatment of depression: prescribing patterns of antidepressants in primary care in the UK. Br J Psychiat 1996; 168: 164–8.
18. Drent M, Singh S, Gorgels AP et al. Drug-induced pneumonitis and heart failure simultaneously associated with venlafaxine. Am J Respiratory and Critical Care Med 2003; 167: 958–61.
19. Fava M. Augmentation and combination strategies in treatment-resistant depression. J Clin Psychiat 2001; 62 (Suppl. 18): 4–11.
20. Fava M, McGrath PJ, Sheu WP. Switching to reboxetine: an efficacy and safety study in patients with major depressive disorder unresponsive to fluoxetine. J Clin Psychopharmacol 2003; 23 (4): 365–9.
21. Freeman JW, Mundy GR, Beattie RR et al. Cardiac abnormalities in poisoning with tricyclic antidepressants. BMJ 1969; 2: 610–1.
22. Furukawa TA, McGuire H, Barbui C. Meta-analysis of effects and side effects of low dosage tricyclic antidepressants in depression: systematic review. BMJ 2002; 325: 991–9.
23. Gasto C, Navarro V, Marcos T et al. Single-blind comparison of venlafaxine and nortriptyline in elderly major depression. J Clin Psychopharmacol 2003; 23 (1): 21–6.
24. Kasper S, Lemoine P. Comparative efficacy of the antidepressants agomelatine, venlafaxine and sertraline [abstr.]. In: 21st European College of Neuropsycho-pharmacology Congress 2008; Bareelone, Spain. Eur Neuropsychopharmacol 2008; 18: 331–2.
25. Kennedy SH et al. Treating depression effectively. J Clin Psychiat 2004; 78 (Suppl. 3): 44–9.
26. Lôo H, Daléry J, Macher JP, Payen A. Pilot study comparing in blind the therapeutic effect of two doses of agomelatine, melatonin- agonist and selective 5-HT2C receptors antagonist, in the treatment of major depressive disorders. Encephal 2003; 29 (2): 165–71.
27. Ma Y, Henry JA. The antidotal effect of alpha(1)-acid glycoprotein on amitriptyline toxicity in cardiac myocytes. Toxicol 2001; 169: 133–44.
28. Marshall JB, Forker AD. Cardiovascular effects of tricyclic antidepressant drugs: therapeutic usage, overdose, and management of complications. Am Heart J 1982; 103: 401–14.
29. Parker G. Differential effectiveness of newer and older antidepressants appears mediated by an age effect on the phenotypic expression of depression. Acta Psychiat Scand 2002; 106 (3): 168–70.
30. Rochat B, Amey M, Gillet M et al. Identification of three cytochrome P-450 isozymes involved in N-demethylation of citalopram enantiomers in human liver microsomes. Pharmacogenet 1997; 7: 1–10.
31. Sartorius N, Baghai T, Baldwin D, Brand U. The use and usefulness of antidepressants a technical review of avidance by a tesk forse of the ECNP 2006; 276.
32. Smith D, Dempster C, Glanville J et al. Efficacy and tolerability of venlafaxine compared with selective serotonin reuptake inhibitors and other antidepressants: a meta-analysis. ACP J Club 2002; 137 (3): 101.
33. Vaughan DA. Interaction of fluoxetine with tricyclic antidepressants. Am J of Psychiat 1988; 145: 1478.
34. Vezmar S, Miljkovic B, Vucicevic K et al. Фармакокинетика и клиническая эффективность комбинации флувоксамина и амитриптилина в лечении депрессии. J Pharmacol Sci 2009; 110: 98–104.
35. Witchel HJ, Hancox JC, Nutt DJ. Psychotropic drugs, cardiac arrhythmia, and sudden death. J Clin Psychopharmacol 2003; 23: 58–77.


