Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№02 2010
Венлаксор® (венлафаксин) в терапии депрессивных расстройств (опыт применения в амбулаторной и клинической практике) №02 2010
Номера страниц в выпуске:29-31
В настоящее время назрела необходимость разработки и использования в клинической практике препаратов, фактически промежуточных между селективными ингибиторами обратного захвата серотонина (СИОЗС) и трициклическими антидепрессантами (ТЦА). Последние воздействуют на широкий спектр рецепторов , что, с одной стороны, обусловливает их достаточно высокую эффективность, но с другой – их применение сопровождается высоким риском развития тяжелых нежелательных явлений. Данное обстоятельство существенно ограничивает возможность амбулаторного применения ТЦА для длительной поддерживающей терапии. Что же касается наиболее часто назначаемых антидепрессантов из группы СИОЗС, лишенных многих недостатков ТЦА, то они хотя и отличаются лучшей переносимостью, но, по данным некоторых авторов, проигрывают им в эффективности.
Введение
В настоящее время назрела необходимость разработки и использования в клинической практике препаратов, фактически промежуточных между селективными ингибиторами обратного захвата серотонина (СИОЗС) и трициклическими антидепрессантами (ТЦА). Последние воздействуют на широкий спектр рецепторов (норадреналин/серотонинергические, холинергические, гистаминовые и адренергические), что, с одной стороны, обусловливает их достаточно высокую эффективность, но с другой – их применение сопровождается высоким риском развития тяжелых нежелательных явлений [6]. Данное обстоятельство существенно ограничивает возможность амбулаторного применения ТЦА для длительной поддерживающей терапии [9]. Что же касается наиболее часто назначаемых антидепрессантов из группы СИОЗС [10], лишенных многих недостатков ТЦА, то они хотя и отличаются лучшей переносимостью [23], но, по данным некоторых авторов, проигрывают им в эффективности [20, 22].
Венлаксор® (венлафаксин) относится к группе антидепрессантов III его поколения – современных тимоаналептических средств, классифицируемых как препараты двойного действия (селективные ингибиторы обратного захвата серотонина и норадреналина). Однако следует обратить внимание на то, что в действительности венлафаксин обладает тройным дозозависимым действием. Механизм антидепрессивного действия Венлаксора (венлафаксина) связан с его способностью потенцировать передачу нервного импульса в центральную нервную систему. Венлафаксин и его основной метаболит О-дисметилвенлафаксин (ОДВ) обладают тройным эффектом: являются сильными ингибиторами обратного захвата серотонина и норадреналина и слабыми ингибиторами обратного захвата допамина. Кроме того, венлафаксин и ОДВ снижают b-адренергическую реактивность организма. Таким образом, препарат обладает свойствами комбинированного тимоаналептика, эффекты которого последовательно проявляются при наращивании дозировок в широком терапевтическом диапазоне от 37,5 до 375 мг/сут, в малых и средних дозах влияя на серотонинергическую и норадреналинергическую, а в высоких дозах и на дофаминергическую нейротрансмиттерные системы [1]. Оправдано применение венлафаксина при депрессиях, резистентных к терапии СИОЗС [12, 18]. Венлафаксин патогенетически влияет на основные клинические проявления аффективного расстройства. Это позволяет использовать препарат при лечении разных клинических вариантов депрессии, синдромально различных аффективных нарушений. Следует отметить также благоприятный профиль переносимости и безопасности венлафаксина, минимальный риск развития побочных эффектов, обусловленный отсутствием сродства к мускариновым, холинергическим, гистаминовым (H1), a-адренергическим, опиатным, бензодиазепиновым и фенциклидиновым или М-метил-d-аспартатным (NMDA) рецепторам головного мозга [8, 11–14, 16]. Это свойство, по данным ряда исследований, делает допустимым применение препарата для терапии депрессивных и тревожных расстройств у пациентов общемедицинской сети, страдающих соматической патологией [3, 5, 10, 12, 19, 22].
Целью исследования является оценка терапевтической эффективности и безопасности препарата Венлаксор® (венлафаксин, АО «Гриндекс») у пациентов с депрессивными состояниями разной (легкой и средней) степени тяжести и психопатологической структуры. В работе определялись режим дозирования препарата, сроки наступления терапевтического эффекта, профиль переносимости препарата Венлаксор® (венлафаксин).
Материалы и методы
Исследование проведено на базе клиники отдела по изучению пограничной психической патологии и психосоматических расстройств (руководитель – акад. РАМН проф. А.Б.Смулевич) Научного центра психического здоровья РАМН (директор – акад. РАМН проф. А.С.Тиганов). Выборку исследования формировали из числа больных, проходящих амбулаторное и стационарное лечение в отделе пограничной психической патологии и психосоматических расстройств ГУ НЦПЗ РАМН. Процедура клинического обследования состояла из стандартных процедур анализа психического состояния, сбора субъективных и объективных анамнестических сведений и оформления медицинской документации.
В исследование включили 30 пациентов в возрасте старше 18 лет, давших добровольное информированное согласие на участие в исследовании, состояние которых определялось клинически выраженным депрессивным синдромом (CGI-S>4, HAMD 17>16, HAMA>17, MADRS>28). Депрессивный синдром регистрировался в рамках депрессивного эпизода (F32), рекуррентного депрессивного расстройства (F33) и смешанного депрессивно-тревожного расстройства (F41.2) по критериям МКБ-10. Исключали пациентов, соответствующих любому из следующих критериев: 1) тяжелая депрессия, 2) период беременности и лактации, 3) коморбидность депрессивного эпизода острым психотическим состояниям, 4) хронический алкоголизм, наркомания, тяжелые соматические заболевания в фазе декомпенсации (почечная, печеночная, сердечная недостаточность, неконтролируемая гипергликемия), 5) гиперчувствительность к исследуемому препарату, 6) прием ингибиторов моноаминоксидазы в течение 2 нед, предшествующих включению в исследование.
Для оценки состояния больных и действия препарата использовали следующие формализованные психометрические инструменты:
Регистрировались данные физикального обследования, лабораторных и инструментальных методов исследования, назначаемых пациенту в рамках рутинной практики. Предусматривалась досрочная отмена терапии Венлаксором при отсутствии эффекта к концу 10-го дня терапии при использовании максимальных суточных доз, утяжеления депрессии, выраженных нежелательных явлений, отказа пациента от лечения/утраты контакта с пациентом.
Критерием оценки эффективности лечения наряду с клинически регистрируемым улучшением состояния являлось уменьшение суммы балов по шкалам HAMD>50%, MADRS>50% и HAMA>35%, в качестве дополнительных использовались показатели по шкале CGI-I (существенное, выраженное или умеренное улучшение), а также по CGI-S («нет симптомов» или «пограничное расстройство»).
Все связанные (или возможно связанные) с приемом препарата нежелательные явления, выявленные по спонтанным сообщениям пациентов, результатам целенаправленного расспроса пациента на каждом клиническом визите и в показателях лабораторных/инструментальных методов исследования регистрировались в разделе «Побочные эффекты» индивидуальной регистрационной карты больного.
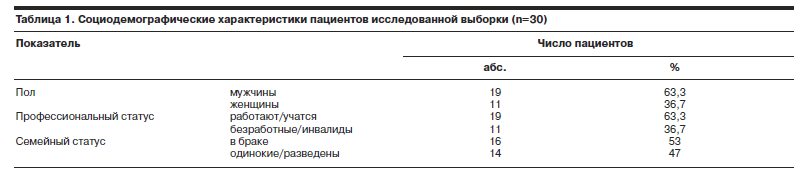
Выборка исследования включала 30 больных (19 мужчин и 11 женщин) в возрасте от 18 до 65 лет (средний возраст 39±5,3 года), госпитализированных в клинику ГУ НЦПЗ РАМН (9 наблюдений) или обратившихся за помощью амбулаторно (21 наблюдение). Социодемографические характеристики пациентов изученной выборки представлены в табл. 1.
В соответствии с критериями МКБ-10 психопатологические нарушения у 24 больных характеризовались наличием признаков депрессивного состояния (F32, F33), у 6 пациентов – смешанного депрессивного и тревожного расстройства (F41.2).
В статусе всех пациентов на момент включения в исследование присутствовали стойкие депрессивные и тревожные расстройства разной степени выраженности, средний стартовый балл по шкале HAMD составил 21,7±6, по MADRS – 29,5±6, по шкале HAMD – 25,86±5,6.
Следует отметить, что психопатологические проявления депрессивных расстройств в изученной выборке характеризовались тревогой (стойкая гипотимия с преобладанием беспредметного беспокойства, внутреннего напряжения, предчувствия несчастья), апатией с дефицитом побуждений и утратой жизненного тонуса, регистрировались смешанные проявления тревоги и апатии. Ряд пациентов вербализовали тоску (подавленность с выраженной витальностью в виде диффузного, протопатического ощущения гнета, тяжести в груди, с суточным ритмом, сопутствующими расстройствами сна, аппетита, изменением массы тела).
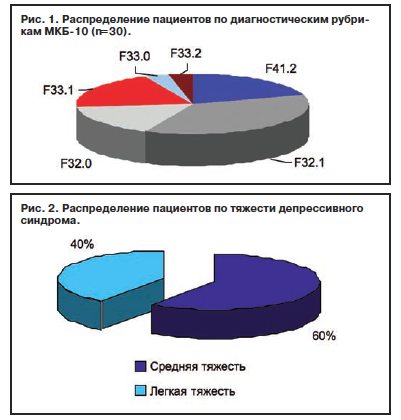
Распределение пациентов в соответствии с диагностическими категориями и выраженностью депрессивных расстройств представлено на рис. 1. В 53,3% случаев у пациентов был диагностирован первый эпизод депрессии (F32), в 20% – впервые возникшее смешанное депрессивное и тревожное расстройство (F41.2), в 26,6% наблюдений депрессивная симптоматика регистрировалась в рамках рекуррентной депрессии.
В выборке преобладали больные с депрессией средней степени тяжести (60%), депрессии легкой степени тяжести составили 40% наблюдений (рис. 2).
Результаты
Успешно курс терапии завершили 27 пациентов, что является высоким показателем тимоаналептической эффективности и переносимости препарата (первоначальный объем выборки – 30 больных). Средняя эффективная доза Венлаксора составила 176,25 мг/сут (от 37,5 до 300 мг). Доля пациентов, получавших максимальные терапевтические дозировки препарата (300 мг/сут), была равна 10% (3 из 30 пациентов, закончивших исследование), что также характеризует переносимость препарата.
Исключение из исследования выполнялось в связи с неэффективностью терапии по оценке состояния на 3-й неделе терапии. К нонреспондерам отнесены 2 пациента с тоскливой витальной депрессией в рамках F32.1 и F33.1 (по МКБ-10). В целом Венлаксор обладает хорошей переносимостью. Выбывание из исследования в связи с побочными эффектами зарегистрировано в одном случае (непереносимая тошнота, непозволяющая нарастить дозу препарата для достижения достаточного антидепрессивного эффекта). Среди участников, завершивших исследование, неблагоприятные лекарственные эффекты зафиксированы в 7 (24,1%) случаях (табл. 2).
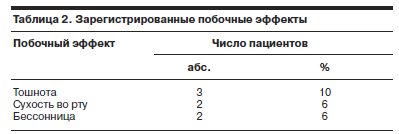
Необходимо отметить, что нежелательные реакции возникали преимущественно на начальном этапе терапии
(1-я неделя), были кратковременными, корригировались симптоматическими средствами или снижением дозы Венлаксора.
Эффективность терапии Венлаксором (количество респондеров по шкалам HAMD>50%, MADRS>50% и HAMA>35%) при промежуточной оценке на 2-й неделе лечения отмечена в 83% случаев (25 пациентов). После завершении курса лечения (1 мес) проводилась шкальная оценка достижения уровня ремиссии (HAMD<7 баллов, MADRS<15 баллов), которая была зарегистрирована в 83,3%, что сопоставимо с результатами большинства исследований.
Уже к концу 1-й недели терапии отмечена выраженная редукция депрессивной симптоматики по шкалам (рис. 3).
В результатах оценки по шкалам общего клинического впечатления – CGI-S и CGI-I – отражается высокая общая эффективность терапии. Стартовый средний суммарный балл по CGI-S, составивший 4,56 (интервал между показателями «умеренно болен» и «явно болен»), снизился через 4 нед терапии до 1,46 (интервал между показателями «здоров, отсутствие психических нарушений» и «пограничное состояние»).
Средний суммарный балл по шкале CGI-I во время финального визита (4-я неделя) составил 1,4 (интервал между показателями «очень хорошее улучшение» – 1 балл и «хорошее улучшение» – 2 балла) (рис. 4).
Наблюдалось выраженное снижение уровня как депрессивных, так и тревожных расстройств с субъективным улучшением настроения, уменьшением колебаний аффекта, повышением уровня профессиональной продуктивности, снижением раздражительности и чувства внутреннего напряжения. Улучшились сон, аппетит, появлялись побуждения к деятельности. Редуцировались проявления психической тревоги, беспокойства, ожидания грядущей катастрофы, что согласуется с данными других исследований [2, 4, 7, 15, 17, 20, 21].
Тимоаналептический эффект характеризовался быстрым наступлением: в 73,3% случаев отмечалась 50% редукция суммы баллов по шкалам HAMD и MADRS уже на 1-й неделе терапии. Гипотимия и тревожные нарушения в структуре депрессивных расстройств редуцировались гармонично. В одном случае наблюдалась инверсия аффекта с переходом в гипоманиакальное состояние, откорректированное уменьшением дозы Венлаксора. Следует отметить, что Венлаксор обладает благоприятным профилем переносимости, высоким уровнем безопасности. Его назначение не сопровождалось токсическими и аллергическими реакциями.
Таким образом, Венлаксор® является современным эффективным и безопасным антидепрессантом тройного дозозависимого действия, который может быть рекомендован как препарат выбора при терапии тревожных и депрессивных расстройств легкой и умеренной степени тяжести, что, учитывая высокую распространенность аффективных расстройств, обусловливает целесообразность его широкого применения как на госпитальном этапе, так и в амбулаторной практике.
В настоящее время назрела необходимость разработки и использования в клинической практике препаратов, фактически промежуточных между селективными ингибиторами обратного захвата серотонина (СИОЗС) и трициклическими антидепрессантами (ТЦА). Последние воздействуют на широкий спектр рецепторов (норадреналин/серотонинергические, холинергические, гистаминовые и адренергические), что, с одной стороны, обусловливает их достаточно высокую эффективность, но с другой – их применение сопровождается высоким риском развития тяжелых нежелательных явлений [6]. Данное обстоятельство существенно ограничивает возможность амбулаторного применения ТЦА для длительной поддерживающей терапии [9]. Что же касается наиболее часто назначаемых антидепрессантов из группы СИОЗС [10], лишенных многих недостатков ТЦА, то они хотя и отличаются лучшей переносимостью [23], но, по данным некоторых авторов, проигрывают им в эффективности [20, 22].
Венлаксор® (венлафаксин) относится к группе антидепрессантов III его поколения – современных тимоаналептических средств, классифицируемых как препараты двойного действия (селективные ингибиторы обратного захвата серотонина и норадреналина). Однако следует обратить внимание на то, что в действительности венлафаксин обладает тройным дозозависимым действием. Механизм антидепрессивного действия Венлаксора (венлафаксина) связан с его способностью потенцировать передачу нервного импульса в центральную нервную систему. Венлафаксин и его основной метаболит О-дисметилвенлафаксин (ОДВ) обладают тройным эффектом: являются сильными ингибиторами обратного захвата серотонина и норадреналина и слабыми ингибиторами обратного захвата допамина. Кроме того, венлафаксин и ОДВ снижают b-адренергическую реактивность организма. Таким образом, препарат обладает свойствами комбинированного тимоаналептика, эффекты которого последовательно проявляются при наращивании дозировок в широком терапевтическом диапазоне от 37,5 до 375 мг/сут, в малых и средних дозах влияя на серотонинергическую и норадреналинергическую, а в высоких дозах и на дофаминергическую нейротрансмиттерные системы [1]. Оправдано применение венлафаксина при депрессиях, резистентных к терапии СИОЗС [12, 18]. Венлафаксин патогенетически влияет на основные клинические проявления аффективного расстройства. Это позволяет использовать препарат при лечении разных клинических вариантов депрессии, синдромально различных аффективных нарушений. Следует отметить также благоприятный профиль переносимости и безопасности венлафаксина, минимальный риск развития побочных эффектов, обусловленный отсутствием сродства к мускариновым, холинергическим, гистаминовым (H1), a-адренергическим, опиатным, бензодиазепиновым и фенциклидиновым или М-метил-d-аспартатным (NMDA) рецепторам головного мозга [8, 11–14, 16]. Это свойство, по данным ряда исследований, делает допустимым применение препарата для терапии депрессивных и тревожных расстройств у пациентов общемедицинской сети, страдающих соматической патологией [3, 5, 10, 12, 19, 22].
Целью исследования является оценка терапевтической эффективности и безопасности препарата Венлаксор® (венлафаксин, АО «Гриндекс») у пациентов с депрессивными состояниями разной (легкой и средней) степени тяжести и психопатологической структуры. В работе определялись режим дозирования препарата, сроки наступления терапевтического эффекта, профиль переносимости препарата Венлаксор® (венлафаксин).
Материалы и методы
Исследование проведено на базе клиники отдела по изучению пограничной психической патологии и психосоматических расстройств (руководитель – акад. РАМН проф. А.Б.Смулевич) Научного центра психического здоровья РАМН (директор – акад. РАМН проф. А.С.Тиганов). Выборку исследования формировали из числа больных, проходящих амбулаторное и стационарное лечение в отделе пограничной психической патологии и психосоматических расстройств ГУ НЦПЗ РАМН. Процедура клинического обследования состояла из стандартных процедур анализа психического состояния, сбора субъективных и объективных анамнестических сведений и оформления медицинской документации.
В исследование включили 30 пациентов в возрасте старше 18 лет, давших добровольное информированное согласие на участие в исследовании, состояние которых определялось клинически выраженным депрессивным синдромом (CGI-S>4, HAMD 17>16, HAMA>17, MADRS>28). Депрессивный синдром регистрировался в рамках депрессивного эпизода (F32), рекуррентного депрессивного расстройства (F33) и смешанного депрессивно-тревожного расстройства (F41.2) по критериям МКБ-10. Исключали пациентов, соответствующих любому из следующих критериев: 1) тяжелая депрессия, 2) период беременности и лактации, 3) коморбидность депрессивного эпизода острым психотическим состояниям, 4) хронический алкоголизм, наркомания, тяжелые соматические заболевания в фазе декомпенсации (почечная, печеночная, сердечная недостаточность, неконтролируемая гипергликемия), 5) гиперчувствительность к исследуемому препарату, 6) прием ингибиторов моноаминоксидазы в течение 2 нед, предшествующих включению в исследование.
Для оценки состояния больных и действия препарата использовали следующие формализованные психометрические инструменты:
• шкалу общего клинического впечатления (CGI) для оценки тяжести заболевания (CGI-S) и улучшения (CGI-I);Венлаксор® назначался после отмены предшествующей психофармакотерапии с периодом «отмывки» минимум 7 дней. Начальная доза Венлаксора составляла 75 мг/сут (двукратный прием по 37,5 мг) с дальнейшим повышением до 150 мг (двукратный прием по 75 мг). При необходимости назначения более высокой стартовой дозы (депрессия средней степени тяжести или госпитализация пациента) титрация дозы начиналась со 150 мг/сут, также разделенной на два приема (по 75 мг). При неудовлетворительном терапевтическом эффекте суточная доза Венлаксора повышалась на 75 мг каждые 2–3 дня до достижения эффективной, максимальная суточная доза – 300 мг, длительность лечения – 4 нед. Был рекомендован прием препарата вместе с пищей.
• шкалу Гамильтона для оценки депрессии (HAMD);
• шкалу Гамильтона для оценки тревоги (HAMA);
• шкалу депрессии Монтгомери–Асберг (MADRS).
Регистрировались данные физикального обследования, лабораторных и инструментальных методов исследования, назначаемых пациенту в рамках рутинной практики. Предусматривалась досрочная отмена терапии Венлаксором при отсутствии эффекта к концу 10-го дня терапии при использовании максимальных суточных доз, утяжеления депрессии, выраженных нежелательных явлений, отказа пациента от лечения/утраты контакта с пациентом.
Критерием оценки эффективности лечения наряду с клинически регистрируемым улучшением состояния являлось уменьшение суммы балов по шкалам HAMD>50%, MADRS>50% и HAMA>35%, в качестве дополнительных использовались показатели по шкале CGI-I (существенное, выраженное или умеренное улучшение), а также по CGI-S («нет симптомов» или «пограничное расстройство»).
Все связанные (или возможно связанные) с приемом препарата нежелательные явления, выявленные по спонтанным сообщениям пациентов, результатам целенаправленного расспроса пациента на каждом клиническом визите и в показателях лабораторных/инструментальных методов исследования регистрировались в разделе «Побочные эффекты» индивидуальной регистрационной карты больного.
Выборка исследования включала 30 больных (19 мужчин и 11 женщин) в возрасте от 18 до 65 лет (средний возраст 39±5,3 года), госпитализированных в клинику ГУ НЦПЗ РАМН (9 наблюдений) или обратившихся за помощью амбулаторно (21 наблюдение). Социодемографические характеристики пациентов изученной выборки представлены в табл. 1.

В соответствии с критериями МКБ-10 психопатологические нарушения у 24 больных характеризовались наличием признаков депрессивного состояния (F32, F33), у 6 пациентов – смешанного депрессивного и тревожного расстройства (F41.2).
В статусе всех пациентов на момент включения в исследование присутствовали стойкие депрессивные и тревожные расстройства разной степени выраженности, средний стартовый балл по шкале HAMD составил 21,7±6, по MADRS – 29,5±6, по шкале HAMD – 25,86±5,6.
Следует отметить, что психопатологические проявления депрессивных расстройств в изученной выборке характеризовались тревогой (стойкая гипотимия с преобладанием беспредметного беспокойства, внутреннего напряжения, предчувствия несчастья), апатией с дефицитом побуждений и утратой жизненного тонуса, регистрировались смешанные проявления тревоги и апатии. Ряд пациентов вербализовали тоску (подавленность с выраженной витальностью в виде диффузного, протопатического ощущения гнета, тяжести в груди, с суточным ритмом, сопутствующими расстройствами сна, аппетита, изменением массы тела).

Распределение пациентов в соответствии с диагностическими категориями и выраженностью депрессивных расстройств представлено на рис. 1. В 53,3% случаев у пациентов был диагностирован первый эпизод депрессии (F32), в 20% – впервые возникшее смешанное депрессивное и тревожное расстройство (F41.2), в 26,6% наблюдений депрессивная симптоматика регистрировалась в рамках рекуррентной депрессии.
В выборке преобладали больные с депрессией средней степени тяжести (60%), депрессии легкой степени тяжести составили 40% наблюдений (рис. 2).
Результаты
Успешно курс терапии завершили 27 пациентов, что является высоким показателем тимоаналептической эффективности и переносимости препарата (первоначальный объем выборки – 30 больных). Средняя эффективная доза Венлаксора составила 176,25 мг/сут (от 37,5 до 300 мг). Доля пациентов, получавших максимальные терапевтические дозировки препарата (300 мг/сут), была равна 10% (3 из 30 пациентов, закончивших исследование), что также характеризует переносимость препарата.
Исключение из исследования выполнялось в связи с неэффективностью терапии по оценке состояния на 3-й неделе терапии. К нонреспондерам отнесены 2 пациента с тоскливой витальной депрессией в рамках F32.1 и F33.1 (по МКБ-10). В целом Венлаксор обладает хорошей переносимостью. Выбывание из исследования в связи с побочными эффектами зарегистрировано в одном случае (непереносимая тошнота, непозволяющая нарастить дозу препарата для достижения достаточного антидепрессивного эффекта). Среди участников, завершивших исследование, неблагоприятные лекарственные эффекты зафиксированы в 7 (24,1%) случаях (табл. 2).

Необходимо отметить, что нежелательные реакции возникали преимущественно на начальном этапе терапии
(1-я неделя), были кратковременными, корригировались симптоматическими средствами или снижением дозы Венлаксора.
Эффективность терапии Венлаксором (количество респондеров по шкалам HAMD>50%, MADRS>50% и HAMA>35%) при промежуточной оценке на 2-й неделе лечения отмечена в 83% случаев (25 пациентов). После завершении курса лечения (1 мес) проводилась шкальная оценка достижения уровня ремиссии (HAMD<7 баллов, MADRS<15 баллов), которая была зарегистрирована в 83,3%, что сопоставимо с результатами большинства исследований.
Уже к концу 1-й недели терапии отмечена выраженная редукция депрессивной симптоматики по шкалам (рис. 3).
В результатах оценки по шкалам общего клинического впечатления – CGI-S и CGI-I – отражается высокая общая эффективность терапии. Стартовый средний суммарный балл по CGI-S, составивший 4,56 (интервал между показателями «умеренно болен» и «явно болен»), снизился через 4 нед терапии до 1,46 (интервал между показателями «здоров, отсутствие психических нарушений» и «пограничное состояние»).
Средний суммарный балл по шкале CGI-I во время финального визита (4-я неделя) составил 1,4 (интервал между показателями «очень хорошее улучшение» – 1 балл и «хорошее улучшение» – 2 балла) (рис. 4).
Наблюдалось выраженное снижение уровня как депрессивных, так и тревожных расстройств с субъективным улучшением настроения, уменьшением колебаний аффекта, повышением уровня профессиональной продуктивности, снижением раздражительности и чувства внутреннего напряжения. Улучшились сон, аппетит, появлялись побуждения к деятельности. Редуцировались проявления психической тревоги, беспокойства, ожидания грядущей катастрофы, что согласуется с данными других исследований [2, 4, 7, 15, 17, 20, 21].
Тимоаналептический эффект характеризовался быстрым наступлением: в 73,3% случаев отмечалась 50% редукция суммы баллов по шкалам HAMD и MADRS уже на 1-й неделе терапии. Гипотимия и тревожные нарушения в структуре депрессивных расстройств редуцировались гармонично. В одном случае наблюдалась инверсия аффекта с переходом в гипоманиакальное состояние, откорректированное уменьшением дозы Венлаксора. Следует отметить, что Венлаксор обладает благоприятным профилем переносимости, высоким уровнем безопасности. Его назначение не сопровождалось токсическими и аллергическими реакциями.
Таким образом, Венлаксор® является современным эффективным и безопасным антидепрессантом тройного дозозависимого действия, который может быть рекомендован как препарат выбора при терапии тревожных и депрессивных расстройств легкой и умеренной степени тяжести, что, учитывая высокую распространенность аффективных расстройств, обусловливает целесообразность его широкого применения как на госпитальном этапе, так и в амбулаторной практике.
Список исп. литературыСкрыть список1. Аведисова А.С. Венлафаксин: результаты международных исследований антидепрессанта III поколения. Психиатр. и психофармакотер. 2006; 11 (2).
2. Волель Б.А., Романов Д.В. Опыт применения венлафаксина (Велафакса) у пациентов с депрессией в амбулаторной и клинической практике. Тер. психич. расстройств. 2007; 2: 48–52.
3. Иванов С.В., Шафигуллин М.Р., Сгилиди И.С. и др. Эфевелон (венлафаксин) в терапии депрессивных расстройств у пациентов с онкологическими заболеваниями. Психосоматич. расстройства. 2007; 2 (3).
4. Ильина Н.А. Опыт применения велаксина (венлафаксина) при тревожных депрессиях в психиатрической практике. Журн. неврол. и психиат. 2007.
5. Медведев В.Э., Добровольский А.В. Лечение депрессий у больных с сердечно-сосудистыми заболеваниями. Опыт применения Велаксина. Психиатр. и психофармакотер. 2007; 3: 14–6.
6. Мосолов С.Н. Клиническое применение антидепрессантов. СПб., 1995.
7. De Nayer A, Geerts S, Ruelens L et al. Venlafaxine compared with fluoxetine in outpatients with depression and concomitant anxiety. Int J Neuropsychopharmacol 2002; 5 (2): 115–20.
8. Amsterdam J. Efficacy and safety of venlafaxine in the treatment of bipolar II major depressive episode. J Clin Psychopharmacol 1998; 18 (5): 414–7.
9. Anderson I, Mortimore C. Discontinuation rates of SSRI\'s and tricyclic antidepressants. Br J Psychiat 1997; 171: 87.
10. Bauer M, Whybrow PC, Angst J et al. World Federation of Societies of Biological Psychiatry (WFSBP) guidelines for biological treatment of unipolar depressive disorders, part 1: acute and continuation treatment of major depressive disorder. Wld J Biol Psychiat 2002; 3: 5–43.
11. Damian D, van der Wee N, van Megen H et al. Double Blind Comparison of Venlafaxine and Paroxetine in Obsessive-Compulsive Disorders. J Clin Psychopharmacol 2003; 23 (6): 568–75.
12. de Montigny C, Silverstone PH, Debonnel G et al. Venlafaxine in treatment-resistant major depression: a Canadian multicenter, open-label trial. J Clin Psychopharmacol 1999; 19 (5): 401–6.
13. Entsuah AR et al. Response and remission rates in different subpopulations with major depressive disorder administered Venlafaxine, selective serotonin reuptake, or placebo. J Clin Psychiat 2001; 62 (11): 869–77.
14. Gasto C, Navarro V, Marcos Т et al. Single-blind comparison of venlafaxme and nor-triptyline in elderly major depression. J Clin Psychopharmacol 2003; 23 (1): 21–6.
15. Gorman J, Laszlo A. Efficacy of Fenlafaxine in mixed Depression-Anxiety States. Depres Anxiety 2000; 12 (1): 77–80.
16. Hunter AM, Leuchter AF, Morgan ML et al. Neurophysiologic correlates of the Side Effects in Normal Subjects Randomized to Venlafaxine or Placebo. Neuropsychopharmacology 2005; 30 (4): 792–9.
17. Judge R, Wagner B. Once-daily venlafaxine XR compared with fluoxetine in outpatientwith depression and anxiety. J Clin Psychiat 1999; 60: 795–6.
18. Poirier MF. Boyer P. Venlafaxine and paroxetine in treatment-resistent depression. Double-blind, randomised comparison. Br J Psychiat 1999; 175: 12–6.
19. Pollack M, Meoni P, Otto MW et al. Predictors of outcome following venlafaxine extended-release treatment of DSM-IV generalized anxiety disorder: a pooled analysis of short- and long-term studies. J Clin Psychopharmacol 2003; 23 (3): 250–9.
20. Roose SP, Glassman AH, Attia E, Woodring S. Comparative efficacy of selective serotonin reuptake inhibitors and tricyclics in the treatment of melancholia. Am J Psychiat 1994; 151 (12): 1735–9.
21. Rudolph RL, Entsuah R, Chitra R. A meta-analysis of the effects of venlafaxine on anxiety associated with depression. J Clin Psychopharmacol 1998; 18 (2): 136–44.
22. Vestergaard P, Gram LF, Kragh-Sorensen P et al. Therapeutic potentials of recently introduced antidepressants. Danish University Antidepressant Group. Psychopharmacol Ser 1993; 10: 190–8.
23. Williams JW, Mulrow CD, Chiquette E et al. A systematic review of newer pharmacotherapies for depression in adults: evidence report summary. Ann Intern Med 2000; 132: 743–56.


