Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№04 2010
Комплексная терапия пациентов с синдромом раздраженного кишечника №04 2010
Номера страниц в выпуске:15-17
Результаты опроса пациентов, страдающих синдромом раздраженного кишечника (СРК) и наблюдавшихся в реабилитационных центрах США и Европы, показали, что качество жизни таких больных страдает, трудоспособность снижена, ведут они себя как больные, страдающие тяжелым органическим заболеванием при удовлетворительном общем состоянии, хорошем внешнем виде и отсутствии признаков прогрессирования болезни, а также могут испытывать трудности в создании доверительных отношений с врачом. В ряде исследований была показана эффективность психотерапии у больных с СРК.
Результаты опроса пациентов, страдающих синдромом раздраженного кишечника (СРК) и наблюдавшихся в реабилитационных центрах США и Европы, показали, что качество жизни таких больных страдает, трудоспособность снижена, ведут они себя как больные, страдающие тяжелым органическим заболеванием при удовлетворительном общем состоянии, хорошем внешнем виде и отсутствии признаков прогрессирования болезни, а также могут испытывать трудности в создании доверительных отношений с врачом [1].
В процессе лечения следует акцентировать внимание пациентов на нормальных результатах исследований и подчеркивать важность отсутствия патологических нарушений для прогноза заболевания. Крайне важна правильная оценка психического состояния больных с СРК, а также своевременное привлечение психологов, психиатров, невропатологов, вегетологов для подбора адекватной психотропной терапии [2].
На практике все методы сводятся к обучению пациента контролировать осознанный ответ на стрессовую ситуацию, чтобы впоследствии научиться давать альтернативный, адаптированный к ситуации ответ. Психологообучающие формы, подобные этим, были предложены в 1989 г. S.Benjamin и лежат в основе биологической обратной связи (Biofeedback), являющейся одним из составных элементов релаксации, применяющимся у больных с изначально нетяжелыми формами функциональных заболеваний пищеварительного тракта. Одним из методов воздействия на болевой синдром явилось создание в 1980 г. программы, получившей название «клиника хронической боли» (Chronic Pain Clinic) [3].
В ряде исследований была показана эффективность психотерапии у больных с СРК [4]. Использовались традиционная динамическая психотерапия, релаксация, гипнотерапия и когнитивная поведенческая терапия [5]. Метод релаксации включает следующие составляющие: приобретение навыков прогрессивной мышечной релаксации, биологическую обратную связь для снятия мышечных судорог, температурной реакции и электродермальной активности, аутогенные тренировки, медитации [6]. Однако высказывалось критическое отношение к результатам этих исследований в связи с отсутствием единого методологического подхода [7].
Фармакологическая коррекция психоневротических нарушений проводится прежде всего антидепрессантами. Традиционно использовался трициклический антидепрессант (ТЦА) амитриптилин, но в последнее время он уступает место препаратам нового поколения [8]. Ряд авторов обнаружили, что миансерина гидрохлорид, обладая сродством к серотониновым рецепторам, также обладает седативным действием, что актуально для больных, страдающих хронической абдоминальной болью и нарушениями сна [9]. Также было продемонстрировано положительное влияние миансерина гидрохлорида на моторику толстого кишечника. При этом отмечается минимальное количество побочных эффектов со стороны желудочно-кишечного тракта (ЖКТ). Положительный эффект миансерина при лечении психосоматических расстройств у больных с функциональными расстройствами со стороны ЖКТ был продемонстрирован в 75% случаев – было получено достоверное уменьшение абдоминальной боли и явлений дистресса с оценкой результатов по шкале общего клинического впечатления Clinical Global Impression Scale [10].
Так, во многих исследованиях была показана эффективность низких доз ТЦА в отношении гастроэнтерологических симптомов при СРК, причем наименьшим количеством побочных эффектов, характерных для данной группы препаратов, обладали вторичные амины – имипрамин и нортриптилин [11, 12]. Антидепрессанты могут взаимодействовать с эндогенными опиоидами и их рецепторами в мозге [13]. Энкефалинсодержащие нейроны и нервные окончания располагаются в 1 и 2-й пластинках дорсального рога, околопроводном сером веществе. А.Biegon и D.Samuel продемонстрировали специфическую взаимосвязь ТЦА и опиатных рецепторов мозга, предположив, что данный феномен лежит в основе анальгетического эффекта [14]. Так, в ряде исследований, как зарубежных, так и проведенных в нашей стране, подтверждена эффективность сульпирида (просульпин, эглонил), относящегося к группе нейролептиков, в группе больных с высоким уровнем тревоги [15].
Влияние препарата на серотониновые рецепторы и гистаминовую активность реализуется и на центральном, и на периферическом уровнях. При исследовании анальгетического действия антидепрессантов выявлено две важные закономерности. Первая – анальгетический эффект наступает при меньших терапевтических дозах, чем антидепрессивное действие препарата. Вторая – анальгетический эффект при применении антидепрессантов, как правило, предшествует антидепрессивному [16].
К числу препаратов выбора для терапии СРК, формирующегося при соучастии депрессивной патологии, можно отнести Коаксил (тианептин) – современный антидепрессант класса селективных стимуляторов обратного захвата серотонина. Эффективность Коаксила в терапии больных с СРК, коморбидным депрессии, подтверждена результатами открытого 6-недельного исследования. В соответствии с показателями шкалы общего клинического впечатления монотерапия Коаксилом достоверно превосходила по эффективности базисную терапию СРК. Полная или значительная редукция симптоматики зарегистрирована у 65% пациентов из группы Коаксила против 10% в группе базисной терапии. Наиболее полно терапевтический эффект Коаксила реализуется в отношении абдоминалгий, а также депрессивной и тревожной симптоматики. Интересно, что Коаксил и базисная терапия в равной степени способствовали снижению показателей нарушений моторной функции толстой кишки (диарея и запоры) [17].
Результаты
Были обследованы 42 пациента с СРК. Всем пациентам был назначен Коаксил (тианептин) в дозе 12,5 мг 3 раза в день. Полный курс терапии продолжительностью 1,5 мес окончили 22 пациента, 7 пациентов не закончили назначенный курс терапии, 13 пациентов повторно проконсультированы вегетологом, где получили рекомендации по дальнейшему лечению (продление сроков лечения от 3 до 6 мес). В течение всего периода лечения у вегетолога все пациенты получали плановую терапию, назаначенную гастроэнтерологом. Повторные визиты осуществлялись через 2 нед от начала лечения – для оценки клинического состояния больных, а также коррекции доз препарата и через месяц – для оценки эффективности препарата и проведения повторного психологического тестирования.
При динамическом наблюдении больных с СРК с преобладанием запоров у 3 пациентов из 9 в течение первых 2 нед наблюдалась положительная динамика. Больные отмечали улучшение самочувствия, сна, уменьшение общей слабости, метеоризма, однако сохранялись тошнота, умеренные боли в животе, запоры на фоне психоэмоциональной нагрузки и без нее. У остальных 5 человек динамики не наблюдалось. При оценке состояния больных спустя 45 дней от начала лечения у одного пациента каких-либо изменений не наблюдалось, у 8 – положительная динамика: пациенты отмечали нормализацию сна, уменьшение выраженности тревоги, внутреннего напряжения, беспокойства, общей слабости; устранение урчания, метеоризма, тошноты. Однако у 3 больных сохранялись запоры, не связанные с психоэмоциональной нагрузкой и погрешностями в диете.
При динамическом наблюдении 11 больных с СРК с преобладанием поносов мы отметили следующее: спустя 2 нед от начала лечения у 3 человек жалобы носили прежний характер. Положительная динамика наблюдалась у 8 пациентов: менее выражены были волнение, чувство тревоги, тошнота; больные отмечали улучшение общего самочувствия, сна. Жалобы на умеренные боли ноющего характера в животе, а также в сердце, изжогу, отрыжку, метеоризм, понос сохранялись. Спустя 45 дней от начала лечения жалобы на боль в животе ноющего характера прежней интенсивности сохранялись у одного человека. У 2 человек жалобы на боль в животе были менее выражены, боли в сердце, не связанные с физической нагрузкой, сохранялись.
Умеренные ноющие боли в животе были менее выражены у 3 пациентов. У одного пациента сохранялся лишь кашицеобразный стул по утрам, в остальном жалоб не предъявлял. У одного пациента из прежних жалоб имели место умеренные боли в левом подреберье и кашицеобразный стул. У одного человека какой-либо динамики не наблюдалось. Отсутствие каких-либо жалоб наблюдалось у 2 пациентов.
При динамическом наблюдении больных с СРК с чередованием поносов и запоров в первом случае спустя 2 нед от начала лечения пациент отмечал улучшение общего самочувствия, боли в животе были менее выражены, метеоризм, урчание не беспокоили, стул нормализовался, однако сохранялись трудности засыпания. Во втором случае жалобы носили прежний характер: сохранялись ноющие боли в околопупочной области, в области сердца, урчание, метеоризм, чередование кашицеобразного стула с запорами после психоэмоциональной нагрузки. Спустя 45 дней от начала лечения в первом случае больной отмечал ухудшение самочувствия: боли в животе, трудности засыпания сохранялись, вновь появились урчание, метеоризм, кашицеобразный стул до 3 раз в сутки. Во втором случае динамики не наблюдалось.
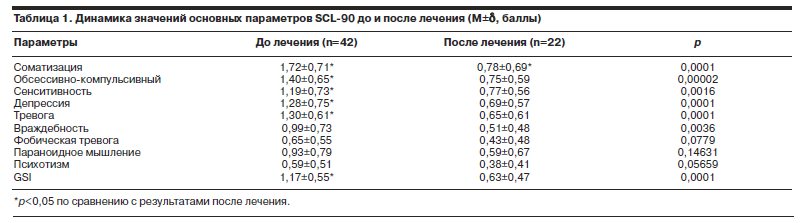
На фоне проведенного лечения распределение средних значений основных параметров шкалы SCL-90 дает возможность говорить о значительном снижении частоты встречаемости случаев высокой выраженности параметров (С – ≥2,0 балла), а соответственно, увеличении частоты встречаемости случаев средней выраженности (В – 1,0–2,0 балла) и, что наиболее важно, – малой выраженности (А – до 0,99 балла; табл. 2).
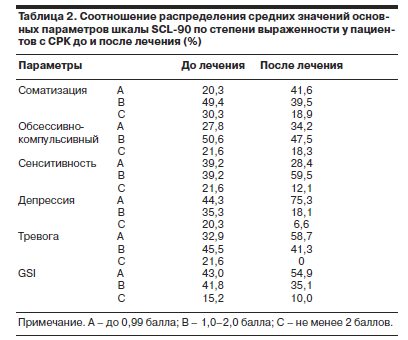
Оценка результатов шкалы HADS после проведенного лечения показала достоверное снижение показателя клинически выраженной тревоги и депрессии и увеличение показателя отсутствия клинически выраженной тревоги и депрессии. При этом показатель клинически выраженной тревоги и депрессии снизился более чем в 2 раза, а показатель отсутствия клинически выраженной тревоги и депрессии вырос более чем в 5 раз. Увеличение показателя субклинически выраженной тревоги и депрессии не было достоверным (табл. 3).
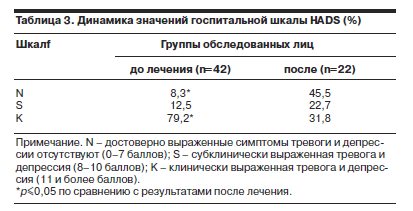
Сравнительная оценка результатов опросника MPQ (для болей в животе) до и после окончания курса лечения продемонстрировала достоверное снижение показателей по большинству шкал, а именно по шкалам суммарного числа выбранных дескрипторов, суммарного рангового числа выбранных дескрипторов, индекса числа выбранных дескрипторов по эмоционально-аффективной шкале, рангового числа выбранных дескрипторов по эмоционально-аффективной шкале, рангового числа выбранных дескрипторов по эвалюативной шкале (табл. 4).
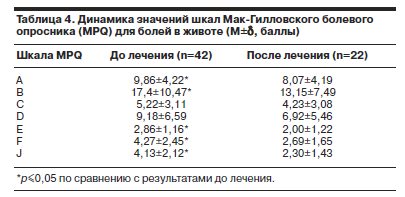
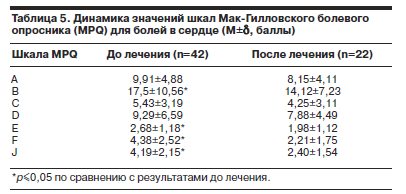
Сравнительная оценка результатов опросника MPQ (для болей в сердце) до и после окончания курса лечения также продемонстрировала достоверное снижение показателей по большинству шкал, а именно: по шкалам суммарного рангового числа выбранных дескрипторов, индекса числа выбранных дескрипторов по эмоционально-аффективной шкале, рангового числа выбранных дескрипторов по эмоционально-аффективной шкале, рангового числа выбранных дескрипторов по эвалюативной шкале (табл. 5).
Таким образом, следует отметить, что назначение терапии, направленной на коррекцию психоэмоциональных нарушений у пациентов с СРК дало выраженный положительный эффект. Большинство пациентов отмечали улучшение общего самочувствия, нормализацию сна, устранение чувства беспокойства, тревоги, волнения, уменьшение, а в ряде случаев полную редукцию болей в животе и сердце. Уменьшились такие проявления, как тошнота, урчание, метеоризм. Нормализовался стул. У больных появилось желание заниматься активной деятельностью, более оптимистическая оценка окружающей ситуации. Произошло достоверное снижение значений по большинству шкал опросника MPQ (для болей в сердце и в животе). Снижение суммарных показателей произошло за счет достоверного снижения значений эмоционально-аффективной и эвалюативной шкал, что свидетельствует о непосредственном влиянии Коаксила на основные составляющие болевого восприятия у пациентов с СРК. Результаты психологического опросника SCL-90, MPQ, а также данные шкалы HADS демонстрируют положительные изменения характера психологического статуса и уменьшение тяжести психоэмоциональных нарушений.
В процессе лечения следует акцентировать внимание пациентов на нормальных результатах исследований и подчеркивать важность отсутствия патологических нарушений для прогноза заболевания. Крайне важна правильная оценка психического состояния больных с СРК, а также своевременное привлечение психологов, психиатров, невропатологов, вегетологов для подбора адекватной психотропной терапии [2].
На практике все методы сводятся к обучению пациента контролировать осознанный ответ на стрессовую ситуацию, чтобы впоследствии научиться давать альтернативный, адаптированный к ситуации ответ. Психологообучающие формы, подобные этим, были предложены в 1989 г. S.Benjamin и лежат в основе биологической обратной связи (Biofeedback), являющейся одним из составных элементов релаксации, применяющимся у больных с изначально нетяжелыми формами функциональных заболеваний пищеварительного тракта. Одним из методов воздействия на болевой синдром явилось создание в 1980 г. программы, получившей название «клиника хронической боли» (Chronic Pain Clinic) [3].
В ряде исследований была показана эффективность психотерапии у больных с СРК [4]. Использовались традиционная динамическая психотерапия, релаксация, гипнотерапия и когнитивная поведенческая терапия [5]. Метод релаксации включает следующие составляющие: приобретение навыков прогрессивной мышечной релаксации, биологическую обратную связь для снятия мышечных судорог, температурной реакции и электродермальной активности, аутогенные тренировки, медитации [6]. Однако высказывалось критическое отношение к результатам этих исследований в связи с отсутствием единого методологического подхода [7].
Фармакологическая коррекция психоневротических нарушений проводится прежде всего антидепрессантами. Традиционно использовался трициклический антидепрессант (ТЦА) амитриптилин, но в последнее время он уступает место препаратам нового поколения [8]. Ряд авторов обнаружили, что миансерина гидрохлорид, обладая сродством к серотониновым рецепторам, также обладает седативным действием, что актуально для больных, страдающих хронической абдоминальной болью и нарушениями сна [9]. Также было продемонстрировано положительное влияние миансерина гидрохлорида на моторику толстого кишечника. При этом отмечается минимальное количество побочных эффектов со стороны желудочно-кишечного тракта (ЖКТ). Положительный эффект миансерина при лечении психосоматических расстройств у больных с функциональными расстройствами со стороны ЖКТ был продемонстрирован в 75% случаев – было получено достоверное уменьшение абдоминальной боли и явлений дистресса с оценкой результатов по шкале общего клинического впечатления Clinical Global Impression Scale [10].
Так, во многих исследованиях была показана эффективность низких доз ТЦА в отношении гастроэнтерологических симптомов при СРК, причем наименьшим количеством побочных эффектов, характерных для данной группы препаратов, обладали вторичные амины – имипрамин и нортриптилин [11, 12]. Антидепрессанты могут взаимодействовать с эндогенными опиоидами и их рецепторами в мозге [13]. Энкефалинсодержащие нейроны и нервные окончания располагаются в 1 и 2-й пластинках дорсального рога, околопроводном сером веществе. А.Biegon и D.Samuel продемонстрировали специфическую взаимосвязь ТЦА и опиатных рецепторов мозга, предположив, что данный феномен лежит в основе анальгетического эффекта [14]. Так, в ряде исследований, как зарубежных, так и проведенных в нашей стране, подтверждена эффективность сульпирида (просульпин, эглонил), относящегося к группе нейролептиков, в группе больных с высоким уровнем тревоги [15].
Влияние препарата на серотониновые рецепторы и гистаминовую активность реализуется и на центральном, и на периферическом уровнях. При исследовании анальгетического действия антидепрессантов выявлено две важные закономерности. Первая – анальгетический эффект наступает при меньших терапевтических дозах, чем антидепрессивное действие препарата. Вторая – анальгетический эффект при применении антидепрессантов, как правило, предшествует антидепрессивному [16].
К числу препаратов выбора для терапии СРК, формирующегося при соучастии депрессивной патологии, можно отнести Коаксил (тианептин) – современный антидепрессант класса селективных стимуляторов обратного захвата серотонина. Эффективность Коаксила в терапии больных с СРК, коморбидным депрессии, подтверждена результатами открытого 6-недельного исследования. В соответствии с показателями шкалы общего клинического впечатления монотерапия Коаксилом достоверно превосходила по эффективности базисную терапию СРК. Полная или значительная редукция симптоматики зарегистрирована у 65% пациентов из группы Коаксила против 10% в группе базисной терапии. Наиболее полно терапевтический эффект Коаксила реализуется в отношении абдоминалгий, а также депрессивной и тревожной симптоматики. Интересно, что Коаксил и базисная терапия в равной степени способствовали снижению показателей нарушений моторной функции толстой кишки (диарея и запоры) [17].
Результаты
Были обследованы 42 пациента с СРК. Всем пациентам был назначен Коаксил (тианептин) в дозе 12,5 мг 3 раза в день. Полный курс терапии продолжительностью 1,5 мес окончили 22 пациента, 7 пациентов не закончили назначенный курс терапии, 13 пациентов повторно проконсультированы вегетологом, где получили рекомендации по дальнейшему лечению (продление сроков лечения от 3 до 6 мес). В течение всего периода лечения у вегетолога все пациенты получали плановую терапию, назаначенную гастроэнтерологом. Повторные визиты осуществлялись через 2 нед от начала лечения – для оценки клинического состояния больных, а также коррекции доз препарата и через месяц – для оценки эффективности препарата и проведения повторного психологического тестирования.
При динамическом наблюдении больных с СРК с преобладанием запоров у 3 пациентов из 9 в течение первых 2 нед наблюдалась положительная динамика. Больные отмечали улучшение самочувствия, сна, уменьшение общей слабости, метеоризма, однако сохранялись тошнота, умеренные боли в животе, запоры на фоне психоэмоциональной нагрузки и без нее. У остальных 5 человек динамики не наблюдалось. При оценке состояния больных спустя 45 дней от начала лечения у одного пациента каких-либо изменений не наблюдалось, у 8 – положительная динамика: пациенты отмечали нормализацию сна, уменьшение выраженности тревоги, внутреннего напряжения, беспокойства, общей слабости; устранение урчания, метеоризма, тошноты. Однако у 3 больных сохранялись запоры, не связанные с психоэмоциональной нагрузкой и погрешностями в диете.
При динамическом наблюдении 11 больных с СРК с преобладанием поносов мы отметили следующее: спустя 2 нед от начала лечения у 3 человек жалобы носили прежний характер. Положительная динамика наблюдалась у 8 пациентов: менее выражены были волнение, чувство тревоги, тошнота; больные отмечали улучшение общего самочувствия, сна. Жалобы на умеренные боли ноющего характера в животе, а также в сердце, изжогу, отрыжку, метеоризм, понос сохранялись. Спустя 45 дней от начала лечения жалобы на боль в животе ноющего характера прежней интенсивности сохранялись у одного человека. У 2 человек жалобы на боль в животе были менее выражены, боли в сердце, не связанные с физической нагрузкой, сохранялись.
Умеренные ноющие боли в животе были менее выражены у 3 пациентов. У одного пациента сохранялся лишь кашицеобразный стул по утрам, в остальном жалоб не предъявлял. У одного пациента из прежних жалоб имели место умеренные боли в левом подреберье и кашицеобразный стул. У одного человека какой-либо динамики не наблюдалось. Отсутствие каких-либо жалоб наблюдалось у 2 пациентов.
При динамическом наблюдении больных с СРК с чередованием поносов и запоров в первом случае спустя 2 нед от начала лечения пациент отмечал улучшение общего самочувствия, боли в животе были менее выражены, метеоризм, урчание не беспокоили, стул нормализовался, однако сохранялись трудности засыпания. Во втором случае жалобы носили прежний характер: сохранялись ноющие боли в околопупочной области, в области сердца, урчание, метеоризм, чередование кашицеобразного стула с запорами после психоэмоциональной нагрузки. Спустя 45 дней от начала лечения в первом случае больной отмечал ухудшение самочувствия: боли в животе, трудности засыпания сохранялись, вновь появились урчание, метеоризм, кашицеобразный стул до 3 раз в сутки. Во втором случае динамики не наблюдалось.

На фоне проведенного лечения распределение средних значений основных параметров шкалы SCL-90 дает возможность говорить о значительном снижении частоты встречаемости случаев высокой выраженности параметров (С – ≥2,0 балла), а соответственно, увеличении частоты встречаемости случаев средней выраженности (В – 1,0–2,0 балла) и, что наиболее важно, – малой выраженности (А – до 0,99 балла; табл. 2).

Оценка результатов шкалы HADS после проведенного лечения показала достоверное снижение показателя клинически выраженной тревоги и депрессии и увеличение показателя отсутствия клинически выраженной тревоги и депрессии. При этом показатель клинически выраженной тревоги и депрессии снизился более чем в 2 раза, а показатель отсутствия клинически выраженной тревоги и депрессии вырос более чем в 5 раз. Увеличение показателя субклинически выраженной тревоги и депрессии не было достоверным (табл. 3).

Сравнительная оценка результатов опросника MPQ (для болей в животе) до и после окончания курса лечения продемонстрировала достоверное снижение показателей по большинству шкал, а именно по шкалам суммарного числа выбранных дескрипторов, суммарного рангового числа выбранных дескрипторов, индекса числа выбранных дескрипторов по эмоционально-аффективной шкале, рангового числа выбранных дескрипторов по эмоционально-аффективной шкале, рангового числа выбранных дескрипторов по эвалюативной шкале (табл. 4).

Сравнительная оценка результатов опросника MPQ (для болей в сердце) до и после окончания курса лечения также продемонстрировала достоверное снижение показателей по большинству шкал, а именно: по шкалам суммарного рангового числа выбранных дескрипторов, индекса числа выбранных дескрипторов по эмоционально-аффективной шкале, рангового числа выбранных дескрипторов по эмоционально-аффективной шкале, рангового числа выбранных дескрипторов по эвалюативной шкале (табл. 5).

Таким образом, следует отметить, что назначение терапии, направленной на коррекцию психоэмоциональных нарушений у пациентов с СРК дало выраженный положительный эффект. Большинство пациентов отмечали улучшение общего самочувствия, нормализацию сна, устранение чувства беспокойства, тревоги, волнения, уменьшение, а в ряде случаев полную редукцию болей в животе и сердце. Уменьшились такие проявления, как тошнота, урчание, метеоризм. Нормализовался стул. У больных появилось желание заниматься активной деятельностью, более оптимистическая оценка окружающей ситуации. Произошло достоверное снижение значений по большинству шкал опросника MPQ (для болей в сердце и в животе). Снижение суммарных показателей произошло за счет достоверного снижения значений эмоционально-аффективной и эвалюативной шкал, что свидетельствует о непосредственном влиянии Коаксила на основные составляющие болевого восприятия у пациентов с СРК. Результаты психологического опросника SCL-90, MPQ, а также данные шкалы HADS демонстрируют положительные изменения характера психологического статуса и уменьшение тяжести психоэмоциональных нарушений.
Список исп. литературыСкрыть список1. Toner BВ, Segal ZV, Emmott S et аl. Cognitive-behavioral group therapy for patients with irritable bowel syndrome. Int J Group Psychother 1998; 48: 215–43 (Medline).
2. Bennet EJ, Piesse C, Palmer K et al. Funсtional gastrointestinal disorders: psychologikal, social and somatic features. Gut 1998; 42: 414–20.
3. Benjamin S. Psychological treatment of chronic pain: a selective review. J Psychosomatic Res 1989; 33: 121–31.
4. Toner BВ. Cognitive-behavioral treatment of functional somatic syndromes: intergrating gender issues. Cognitive and Behavioral Practice 1994; 1: 157–78.
5. Lynch PM, Zamble EA. Controlled behavior treatment study of irritable bowel syndrome. J Consult Clin Psychol 1994; 62: 576–82.
6. Balkom А., Bakker A, Spinhoven A et аl. Allmenn metaanalysis of the treatment of panic disorder with or without agorafhobia: a comparison of psychopharmacological, cognitive-behavioral, and combination treatments. J Nerv Ment Dis 1997; 185: 510–6.
7. Talley NJ, Owen ВК, Boyce Р et. al.Psychological treatment for irritable bowel syndrome: a critique of controlled treatment trials. Am J Gastroenterol 1996; 91: 27–86.
8. Watson CР, Evans RJ, Reed K et аl. Amitriptyline versus placebo in postherpetic neuralgia. Neurology 1982; 32: 671–3.
9. Carman JS, Ahdieh H, Wyatt-Knowles E et аl. A controlled study of mianserin in moderately to severely depressed outpatients. Psychopharmacol Bull 1991; 27 (Suppl. 2): 135–9.
10. Tunum L. Mianserin in chronic abdominal pain. Nord J Psychiatry 1993; 47: 351–4.
11. Magni G. The use of antidepressants in the treatment of chronic pain. A review of the current evidence. Drugs 1991; 42: 730–48.
12. Pilowsky I, Halletts EС, Bassett DL et al. A controlled study of amitriptyline in the treatment of chronic pain. Pain 1982; 14: 169–79.
13. Смулевич А.Б., Сыркин А.Л., Дробижев М.Ю. и др. Диагностика и фармакотерапия депрессий у соматических больных. В кн.: Депрессии и коморбидные расстройства. Под ред. А.Б.Смулевича. 1997; с. 250–60.
14. Biegon A, Samuel D. Interaction of tricyclic antidepressants with opiate receptors. Biochem Pharmacol 1980; 29: 460–2.
15. Смулевич А.Б., Иванов С.В. Терапия психосоматических расстройств. Клинические эффекты Эглонила (сульпирида). Психиатр. и психофармакотер. 2000; 2 (3).
16. Вознесенская Т.Г. Хроническая боль и депрессия. Трудный пациент. 2004; 2 (10): 40–2.
17. Loldrup-Poulsen D, Bech P, Hansen H et аl. Antidepressants in the treatment of chronic pain. Psychopharmacology 1990; 4: B. 7.
20 августа 2010
Количество просмотров: 2273


