Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№03 2003
Депакин: история и перспективы применения в психоневрологической практике №03 2003
Препарат "Депакин-Хроно", представляющий в химическом отношении вальпроевую кислоту и ее натриевую соль, на протяжении последних лет широко используется в практике психиатрии и неврологии не только для лечения различных типов припадков, но и ряда других психических расстройств.
Сам по себе факт этого длительного применения препарата во всем мире свидетельствует однозначно об его эффективности и надежности. Депакин, несмотря на появление на фармацевтическом рынке в течение последних нескольких лет ряда новых антиэпилептических прераратов, остается своего рода “золотым стандартом” монотерапии в эпилептологии, исполняя кроме того роль базисного препарата при использовании нескольких препаратов в лечении резистентных припадков.
Данная обзорная работа знакомит с историей внедрения препарата в эпилептологию и смежные с ней области – неврологию и психиатрию.
История появления вальпроатов как антиконвульсантов берет свое начало в 1962 г., когда у этих соединений P.Eymard чисто случайно обнаружил противосудорожное свойство. Вместе с тем как химическое соединение вальпроевая кислота (di-n-пропилуксусная кислота) была синтезирована на 80 лет раньше – в 1882 г. Burton. Данное соединение на протяжении многих лет использовали в лабораторной биохимической и фармакологической исследовательской работе как липофильный агент для растворения водонерастворимых соединений. В частности, имеются указания на то, что P.Eymard, H.Meunier и Y.Meunier (1963) использовали вальпроевую кислоту для растворения некоторых производных келлина, которые они испытывали с целью изучения у них противосудорожных свойств в так называемом пентилентетразоловом судорожном тесте. К удивлению исследователей, противосудорожными свойствами обладала и сама вальпроевая кислота (W. Losher, 1999).
В первой публикации по исследованию вальпроата указывалось, что вещество оказывает противосудорожное действие в эксперименте на кроликах в диапазоне доз от 200 до 420 мг на 1 кг массы тела животных (H.Meunier и соавт., 1963).
В последующем появились сообщения о том, что вальпроат оказывает противосудорожное действие при моделировании в эксперименте судорожных состояний с помощью электрошока, стрихнина, пикротоксина и при аудиогенных судорогах (W.Losher, 1999). Исходя из этого в исследовательском центре компании “Санофи-Синтелабо” был сделан вывод об универсальном противосудорожном действии вальпроата, и вскоре препарат был впервые испытан в клинических условиях на больных эпилепсией.
Первые результаты клинического противосудорожного эффекта вальпроата натрия были получены G.Carraz и соавт. (1964), и в 1967 г. во Франции препарат был внедрен компанией “Санофи-Синтелабо” на фармацевтический рынок для лечения больных эпилепсией. В последующем он стал применяться более чем в 100 странах мира. В настоящее время вальпроаты выпускаются Санофи-Синтелабо под несколькими названиями в разных странах: депакин, депакан, депакот, депакон, эргенил, эпилим. В дальнейшем появились копии и аналоги: конвулекс, орфирил и др.
Механизм действия Депакина заслуживает специального рассмотрения, поскольку это имеет значение для предсказания его эффективности в клинических условиях.
Вплоть до настоящего времени в экспериментальных изысканиях новых антиконвульсантов используется в основном 3 модели судорожных состояний: модель максимального электрошока (МЭШ), судороги, вызываемые у животных при введении пентилентетразола (иначе пентилентетразоловый тест – ПТЗ) и "киндлинг-модель". Считают, что тест МЭШ, который вызывают двусторонним нанесением электрического разряда через роговицы или уши у животных, позволяет предсказать в клинических условиях эффект, направленный на подавление генерализованных тонико-клонических припадков (ТКП). С другой стороны, ПТЗ-тест представляет экспериментальную модель абсансов и миоклонических судорог. Киндлинг-тест, при котором припадки у животных вызывают за счет раздражения вживленных электродов в область миндалины или гиппокампа, представляет наиболее адекватную модель парциальных припадков у человека, особенно сложных парциальных припадков, характерных для височной эпилепсии. Иными словами, существующие три теста могут смоделировать практически все типы припадков, наблюдаемых в клинических условиях.
Существенно, что Депакин показал эффективность в плане устранения всех трех типов экспериментально вызванных припадков, что априорно позволяет говорить о нем, как об антиконвульсанте широкого спектра действия, эффект которого адресуется практически всем припадкам. Основные данные по этим свойствам препарата отражены в табл.1, составленной по материалам статьи W.Losher (1999).
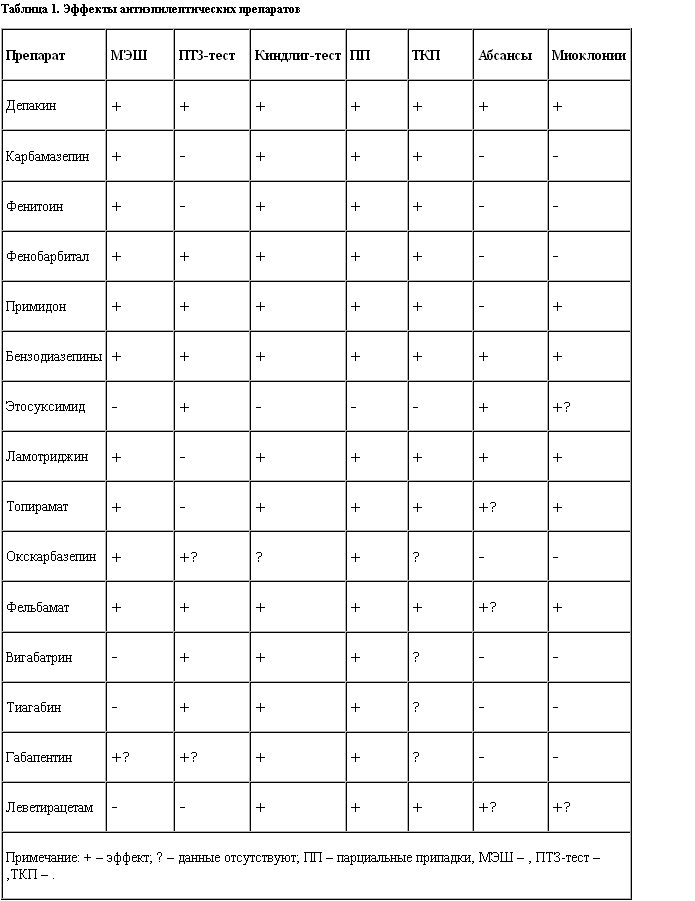
Из таблицы также следует, что Депакин в клинических условиях оказывает эффект в плане устранения практически всех типов припадков. Это позволяет его рассматривать как универсальный антиэпилептический препарат. Эта эффективность Депакина при всех типах припадков и формах эпилепсии объясняется тем, что механизм действия вальпроатов включает несколько компонентов.
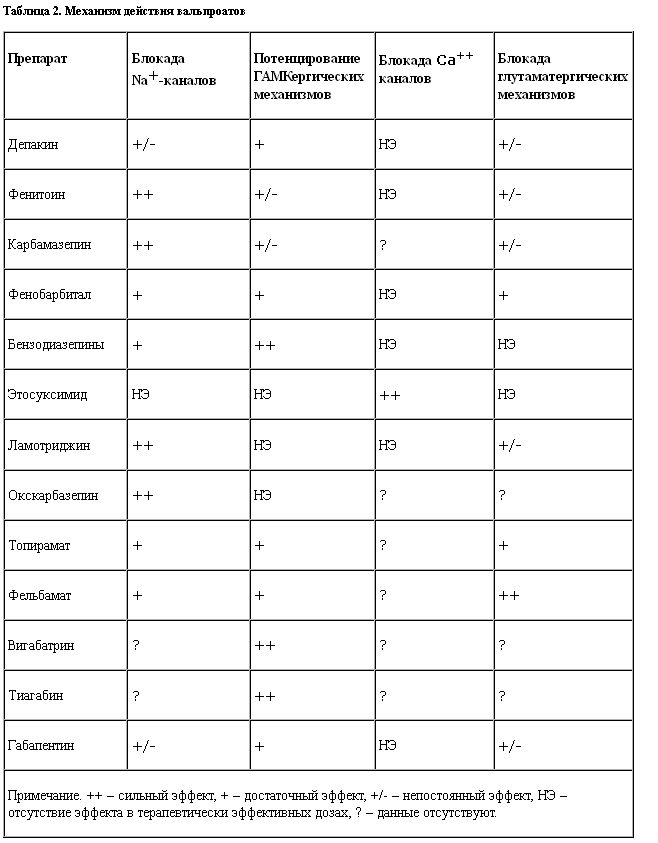
Считается, что в основе собственно антиконвульсивного эффекта препаратов лежит способность предотвращать развитие повторных потенциалов действия в нейронах, что в свою очередь осуществляется за счет блокады вольтажзависимых натриевых каналов. Воздействие на ГАМКергическую систему лежит в основе как антиконвульсивного эффекта, так и определенных психотропных эффектов, связанных с устранением психомоторного возбуждения и наступлением седации (T.Ketter и соавт., 1999), тогда как в основе влияния на абсансы лежит способность блокировать таламические кальциевые каналы (W.Losher,1999). Данная схема носит весьма условный характер, но из нее вытекает, что механизм действия Депакина включает по меньшей мере три компонента. В то же время неясно, почему препарат оказывает антиабсансный эффект, если он лишен способности блокировать кальциевые каналы.
Сопоставление старых и новых антиконвульсантов по механизму действия показывает, что принципиального различия между этими двумя генерациями препаратов нет. Депакин, согласно этой схеме разделяет общий механизм действия с препаратом “Габапентин” и приближается по механизму действия к топирамату и фельбамату. Несмотря на это, Депакин принципиально и в лучшую сторону отличается от габапентина по эффективности в клинических условиях, поскольку в отличие от последнего оказывает эффект в отношении припадков практически любого типа. Топирамат, который по механизму действия только немного отличается от Депакина, по спектру противосудорожной активности приближается в большей степени к вальпроатам, чем габапентин. Из этого следует, что представленные схемы механизма действия антиэпилептических препаратов не могут полностью объяснить всего клинического многообразия эффектов.
Влияние на ГАМКергическую систему является едва ли не основным в сложном механизме действия Депакина. При этом твердо установлено, что препарат повышает концентрацию ГАМК в клинически адекватных дозах, но функциональный смысл этого эффекта еще далек от понимания. Так, повышение уровня ГАМК при действии вальпроатов на пресинаптическом уровне может быть объяснено за счет трех механизмов: а) счет тормозного влияния вальпроатов на распад ГАМК; б) усиления синтеза ГАМК и в) непрямого влияния вальпроатов на синтез и распад ГАМК. Непрямое влияние вальпроатов на пресинаптический уровень ГАМК осуществляется за счет прямого потенцирования постсинаптических ГАМКергических функций. Это приводит по механизму обратной связи к торможению кругооборота ГАМК и тем самым к возрастанию концентрации ГАМК в нервных терминалях (W.Losher, 1999).
Фармакокинетика вальпроатов также заслуживает специального рассмотрения. В настоящее время во всем мире существует фактически 3 химические формы вальпроатов. Они включают собственно вальпроевую кислоту, натриевую соль вальпроевой кислоты и комплекс вальпроевой кислоты и ее натриевой соли в соотношении 1:1. Данные три типа препаратов выпускаются в различных формах: в таблетках, капсулах, растворе, а также в растворе для внутривенных инъекций (D.Shen, 1999).
При приеме внутрь все формы вальпроатов практически полностью всасываются в желудочно-кишечном тракте (более чем на 90%), и прием пищи не влияет на этот процесс.
Абсорбция вальпроевой кислоты из сиропа, обычных таблеток или желатиновых капсул происходит очень быстро. Пик концентрации препарата составляет менее 2 ч. Абсорбция препарата из формы Депакин-энтерик, которая создана для защиты желудочно-кишечного тракта от действия кислоты, составляет несколько больше времени – около 2–3 ч, а максимальная концентрация достигается через 3–5 ч. Прием пищи замедляет абсорбцию активного вещества.
Депакин-Хроно представляет специально разработанную лекарственную форму, состоящую из вальпроевой кислоты и ее натриевой соли в соотношении 1:2. В отличие от других форм вальпроатов, используемых для перорального приема, данная форма характеризуется отсутствием латентного периода времени абсорбции, более удлиненным временем всасывания и более линейной корреляцией между уровнем дозы и концентрацией в плазме. Концентрация препарата при этом имеет более устойчивый характер в течение суток, что выгодно отличает Депакин-Хроно от традиционных форм вальпроатов. Следует подчеркнуть, что Депакин-Хроно в целом имеет гораздо лучшую переносимость, что связывается с отсутствием пиков максимальной концентрации при применении традиционных форм (Bergmannи соавт., 1999). С учетом того, что часть случаев малокурабельной эпилепсии принято связывать с отсутствием стабильного уровня АЭП в плазме крови (В.А. Карлов, 1999), применение формы препарата с медленным высвобождением априорно должно способствовать преодолению резистентности.
Препарат образует несколько активных метаболитов, обладающих противосудорожной активностью (F.Abbott, M.Anari, 1999). Вместе с тем сравнительно недавно установлено, что концентрация активных метаболитов вальпроатов в ликворе у больных эпилепсией находится на более низком уровне, чем концентрация самих вальпроатов. Очевидно, что роль активных метаболитов в наступлении терапевтического эффекта низкая (F.Abbott, M.Anari, 1999).
Примерно 40% вещества от всей дозы вальпроатов подвергается соединению с глюкуроновой кислотой, тогда как около 20–30% – бета-окислению. При полипрагмазии следует помнить, что часть других антиэпилептических препаратов (фенобарбитал, фенитоин, карбамазепин) индуцирует глюкуронозилтрансферазы, что приводит повышению клиренса вальпроатов в 2 раза и, соответственно, к снижению их концентрации в плазме крови.
Сами по себе вальпроаты тормозят по меньшей мере 4 ферментные системы, что может привести к росту концентрации некоторых других препаратов при их комбинированном применении. К ним относятся лоразепам и ламотриджин (A.Yuen и соавт., 1992). При этом время полужизни ламотриджина возрастает с 30 до 60 ч в присутствии вальпроатов. Это может потребовать снижения дозы ламотриджина.
Клиническая эффективность Депакина
Лечение эпилепсий. Уже указывалось, что вальпроевая кислота и ее натриевая соль относятся к антиэпилептическим препаратам широкого спектра действия, что и предопределяет круг показаний для их назначения в психоневрологической практике. В настоящее время вальпроаты продолжают оставаться “золотым стандартом” и базисными препаратами для лечения практически всех форм эпилепсии.
Следует подчеркнуть, что в выборе адекватной противоэпилептической терапии существует несколько правил, которым необходимо следовать.
Во-первых, лечение должно быть направлено не только на купирование припадков, но и, если это возможно, на заболевание или расстройство, которое их вызывает. При этом в случае припадков, возникших при нейроинфекции или сосудистой патологии, должны применяться антиэпилептические препараты для купирования припадков и наряду с этим другие препараты (сосудистые, мочегонные), воздействующие на первичный патологический процесс. Больные с хроническими (повторными) припадками в любом случае должны получать антипиэпилептические препараты.
Во-вторых, лечение должно начинаться с терапии одним антиэпилептическим препаратом, и контроль за приступами должен осуществляться вначале повышением доз препаратов до максимальных. При отсутствии должного эффекта следует назначить другой антиэпилептический препарат с иным механизмом действия.
В-третьих, при изменении доз антиэпилептических препаратов следует руководствоваться реакцией больного на препараты, а не уровнем их концентрации в плазме крови, хотя и его необходимо принимать во внимание. При этом недостаточное снижение частоты припадков будет говорить о необходимости повышения доз, тогда как появление токсических побочных эффектов – напротив, о необходимости снижения уровня доз.
Наблюдение за уровнем препаратов в крови желательно для вальпроатов, как и для карбамазепина, но в случае хорошей переносимости препаратов при хорошем контроле припадков необходимости в подобном мониторинге нет (L. Willmore, 1999).
Депакин является препаратом выбора для лечения как первично генерализованных, так и парциальных припадков с вторичной генерализацией и без нее.
Анализ данных литературы показывает, что Депакин с успехом применяли для терапии абсансов. В открытых и контролируемых исследованиях установлено, что препарат эффективен не менее чем у 75% больных с абасансами. Полное исчезновение абсансов наблюдается не менее чем у половины больных (D.Simon, J.Penry, 1975; A.Richens, S.Ahmad, 1975). В случае простых абсансов контроль за приступами наблюдается не менее чем у 80–90% больных (O.Henriksen, S.Johannessen, 1982; B.Bourgeois и соавт., 1987).
Тонико-клонические припадки (ТКП) у взрослых редко возникают как первичные и гораздо чаще встречаются в результате генерализации эпилептического разряда из первичного фокуса. В этой связи точная дихотомия ТКП на первичные и вторичные не всегда представляется возможной. Вместе с тем в многочисленных исследованиях установлено, что частота ТКП на фоне терапии вальпроатами снижается на 75–100% более чем у половины больных (D.Simon, J.Penry, 1975; R.Davis и соавт.,1994). У детей полный контроль ТКП наблюдали у 34%, у взрослых полный контроль с двухлетней ремиссией – у 72% больных при терапии Депакином и у 56% при лечении фенитоином (D.Turnbull и соавт., 1982, 1985). Полагают, что примерно 70–85% больных различного возраста могут достигнуть полного исчезновения ТКП при терапии Депакином (B.Bourgeois и соавт., 1987).
Парциальные припадки (ПП) у взрослых больных эпилепсией встречаются наиболее часто. Обобщенные данные литературы показывают, что редукции простых и сложных ПП на 75–100% удается достигнуть у 28% больных (L.Willmore, 1999).В большинстве этих исследований вальпроат применялся в качестве дополнительного лекарственного средства к предшествующим антиэпилептическим препаратам.
В одном из исследований, выполненных по двойному слепому методу, проводили сравнение вальпроата с карбамазепином на материале 480 больных со сложными ПП как с вторичной генерализацией, так и без нее (R.Mattson и соавт., 1992). Оба препарата оказались эффективными в плане устранения генерализованных ТКП. Различий между препаратами, если принимать во внимание число больных с вторично генерализованными ТКП, желающих продолжать терапию конкретным препаратом, также установлено не было.
Результаты многочисленных открытых исследований показали, что вальпроаты обладают выраженной эффективностью при терапии сложных ПП, тогда как простые ПП, похоже, гораздо менее реагируют на препарат (А.Covanis и соавт., 1982).
В большинстве исследований подчеркивается, что статистически значимых различий в эффективности между вальпроатами, карбамазепином и фенитоином установлено не было, хотя все эти работы не были безупречными в плане дизайна исследования и не отвечали критериям доказательной медицины.
Едва ли не единственное исследование, которое выполнено в соответствии со строгими критериями доказательной медицины, предполагало сравнение вальпроата с плацебо в качестве дополнительного средства к карбамазепину или фенитоину (L.Willmore и соавт., 1996). В качестве результативного критерия эффективности терапии применяли показатель снижения частоты приступов не менее чем на 50% по сравнению с долечебным уровнем. При этом оказалось 38% респондеров среди больных со сложными ПП.
Миоклонии (миоклонус) представляют собой вариант синдрома, возникающего при переходе от юношеского к взрослому возрасту. В этих случаях устанавливают диагноз юношеской миоклонической эпилепсии. Больные могут страдать подобными припадками на протяжении всей жизни. Депакин является специфическим антиэпилептическим препаратом, который оказывает выраженный эффект при лечении этого эпилептического синдрома. Полного контроля над приступами при этом удается достигнуть не менее чем у 70% больных (А.Covanis и соавт., 1982).
Данными синдромами не ограничивается круг показаний для Депакина. В целом следует подчеркнуть, что эффективность препарата в плане устранения как генерализованных, так и парциальных припадков выгодно отличает его от новой генерации антиэпилептических препаратов. Более того, многие клиницисты считают, что вальпроаты еще долгие годы будут рассматриваться в качестве препаратов выбора для лечения многих эпилепсий, в частности имеющих припадки сложной семиотики и смешанного типа. Примером этого являются атипичные абсансы, генерализованные тонико-клонические и атонические припадки при синдроме Леннокса–Гасто, прогрессирующая миоклоническая эпилепсия, известная также как синдром Унферрихта–Лундборга и синдром Уэста (инфантильный спазм). Во всех этих случаях речь идет о резистентных к терапии пароксизмальных явлениях различной семиотики. С учетом эффективности Депакина при этих различных и неблагоприятных в прогностическом отношении припадков значение его в эпилептологии трудно переоценить (N.Fountain, F.Dreifuss, 1999), поскольку препарат является средством выбора при лечении малокурабельных эпилептических синдромов.
Наряду с этим Депакин является препаратом выбора при лечении миоклонических припадков и ТКП при юношеской миоклонической эпилепсии, детской абсансной эпилепсии и фоточувствительной эпилепсии. В этом отношении с вальпроатом могут соперничать только фельбамат и ламотриджин. Однако с учетом того, что первый из названных препаратов вызывает в качестве побочных эффектов печеночный некроз и апластическую анемию, а второй – токсико-аллергическую сыпь (синдром Стивенса–Джонсона), становится ясно, что главное место в терапии названных эпилептических синдромов остается за вальпроатами.
Говоря о предикторах эффективности терапии Депакином, следует подчеркнуть, что он эффективен, главным образом, при припадках, относимых к генерализованным приступам. Считается, что больные со всем многообразием генерализованных припадков обладают в определенной мере общим механизмом их возникновения, что и объединяет столь разные в семиотическом отношении пароксизмальные состояния, чувствительные к Депакину. Наверняка, существуют и другие типы эпилептических синдромов, имеющих общую патофизиологию и реагирующих на вальпроаты. Например, существует большая группа больных, у которых генерализованные ТКП происходят после пробуждения. D.Janz (1953) для обозначения подобной формы первично генерализованной эпилепсии предложил термин "Auchwach-epilepsie", т.е. эпилепсия пробуждения. Больные этого типа имеют отличительные личностные особенности в виде малой общительности, упрямства, отсутствует целеустремленности, а также небрежности, равнодушия, утраты самоконтроля, нарушений предписаний врача, анозогнозии, стремления к употреблению алкоголя и склонности к девиантному и делинквентному поведению. Наряду с этим их отличает выраженная впечатлительность, достаточно живой ум, легкая эмоциональная вспыльчивость, отсутствие самоуверенности с пониженной самооценкой. Вполне вероятно, что весь этот личностный "букет" будет указывать на больных – кандидатов для терапии Депакином (N.Fountain, F.Dreifuss, 1999). Это, однако, нуждается в проведении специального исследования.
Установлена большая клиническая эффективность Депакина-Хроно по сравнению с традиционными формами при лечении различных малокурабельных форм эпилепсии. При этом общая эффективность терапии возрастает примерно в 1,5 раза (В.А. Карлов, 1999), что позволяет рассматривать форму с медленным высвобождением как средство выбора при лечении рефрактерных форм эпилепсии.
Применение в психиатрии
Наряду с карбамазепином вальпроат выступает как яркий нормотимик при лечении и профилактике биполярного аффективного расстройства (R.Post, 1999). Широкое применение вальпроата в этом качестве началось в 90-е годы ХХ века.
Известно, что на протяжении многих лет в качестве главного нормотимика в психиатрии рассматривались соли лития. Однако клинический опыт показал, что возможности соединений лития при терапии и профилактике биполярных аффективных расстройств далеко не безграничны. В части случаев при этом возникала картина так называемой быстрой смены фаз (rapid cycling), мании с дисфорическим аффектом и коморбидные состояния, включающие тревогу и личностные расстройства (D.Dunner, R.Fieve, 1974; J.Calabrese, G.Delucchi, 1989; R.Post, 1999).
В этой связи и нашел свое место Депакин, который, как и другие нормотимики, применяется при лечении указанных состояний при отсутствии эффекта от солей лития.
Не останавливаясь подробно на этой проблеме, отметим только, что Депакин оказывает отчетливый эффект при лечении острых маниакальных состояний. При этом его эффективность может достигать от 48% (C.Bowden и соавт., 1994) до 80% (H.Emrich и соавт., 1980).
При лечении так называемых дисфорических маний, которые соответствуют смешанным состояниям в отечественной психиатрии, также наблюдается низкая эффективность от солей лития. Подобные состояния составляют примерно около 40% от всех маниакальных состояний. В структуре подобных синдромов наряду с атипичным маниакальным аффектом присутствуют и аффекты других модальностей, в частности тоски и тревоги, могут быть суицидальные тенденции. Вальпроаты являются средствами выбора при лечении и подобных состояний.
Имеется ряд сообщений об эффективности Депакина при лечении острых депрессий, хотя результаты в целом менее убедительные, чем при лечении маниакальных состояний (R.Post, 1999). Вместе с тем указывается, что наибольшего эффекта от вальпроатов можно достичь при лечении депрессий у больных с быстрой сменой фаз либо с биполярным расстройством II подтипа. Так, в исследовании J.Calabrese и соавт.(1993) выраженный терапевтический эффект, под которым понималось полное прекращение циклов (фаз), наблюдали у 21% больного, а умеренный эффект – у 24% больных. С этим контрастируют данные об эффективности вальпроатов в 72% при профилактике фаз депрессий. Из этого следует, что эффективность препарата в плане профилактики выше результатов лечения острых депрессивных состояний (R.Post, 1999).
В работе M.Winsberg и соавт. (1997) установлена очень высокая эффективность вальпроата при лечении биполярной депрессии подтипа II, если больные предварительно не получали терапию антидепрессантами. Из этого следует, что терапия антидепрессантами у больных такого типа нежелательна, поскольку при этом может снизиться способность реагировать на Депакин, хотя в реальных условиях это не принимается во внимание.
Наибольшую эффективность, однако, Депакин показал при профилактике маниакальных и депрессивных фаз у больных с маниакально-депрессивным психозом. По этому разделу существует огромный объем литературы, которую невозможно осветить в настоящей работе.
Из других показаний для назначения Депакина в области психиатрии следует назвать паническое расстройство и посттравматическое стрессовое расстройство. Суточная доза препарата при этом составляет в среднем 20 мг/кг (P.Keck и соавт., 1993). Терапевтический эффект наблюдали примерно у 83% больных, т.е. он был весьма выраженным.
Уровень суточных доз и плазменная концентрация Депакина
В отношении уровня суточных доз препарата при лечении различных форм эпилепсий не может быть стандартных рекомендаций. Рекомендуемый уровень концентрации вальпроата в плазме крови составляет 50–100 мг/л. Тем не менее, как подчеркивалось выше, при выборе оптимальной дозы надо исходить из характера наступления (отсутствия) эффекта и наличия (отсутствия) побочных эффектов. В ряде случаев при отсутствии должного эффекта от формы "Депакин-энтерик" следует перейти к форме "Депакин-хроно". Последняя позволяет добиться более высокого уровня препарата и более длительного его сохранения в плазме крови.
Побочные эффекты и нежелательные явления могут быть причиной недостаточного эффекта препарата у больных эпилепсией. Начальные побочные эффекты включают желудочно-кишечные расстройства в виде тошноты, рвоты, диареи, абдоминальных болей.
Другая категория побочных эффектов связана с прибавкой массы тела. Данное явление возникает примерно у 20–54% больных (L.Willmore, 1999).
Третья разновидность побочных эффектов включает алопецию, которая носит преходящий характер.
Такие тяжелые побочные эффекты, как тромбоцитопения, геморрагии, острые панкреатиты и токсическое поражение печени, встречаются редко и главным образом при высоких дозах препарата.
В заключение нужно отметить, что Депакин является в современных условиях одним из антиэпилептических препаратов первого выбора, поскольку его эффективность была продемонстрирована при большом диапазоне проявлений эпилепсии и судорожных состояний. Безусловно, что тропизм препарата к большинству припадков при эпилепсии придает ему особый статус в клинической эпилептологии. Это обусловлено и особым характером психотропного эффекта Депакина.
Список исп. литературыСкрыть список1. Abbott F., Anari M. Chemistry and biotransformation. Valproate/ W. Lцsher (Ed.). 1999; P.47–75.
2. Bourgeois B, Beaumanoir A, Blajev B et al. Epilepsia 1987; 28 (Suppl. 2): 8–11.
3. Bowden C, Brugger A, Swann A et al. JAMA 1994; 271: 918–24.
4. Сalabrese J, Delucchi G. J Clin Psychiatry 1989; 50: 30–4.
5. Calabrese J, Woyshville M, Kimmel S et al. J Clin Psychopharmacology 1993; 13: 280–3.
6. Carraz G, Darbon M, Lebreton S. et al. Therapy 1964; 19: 468–76.
7. Covanis A, Gupta A, Jeavons P. Epilepsia 1982; 23: 693–720.
8. Davis R, Peters D, McTavish D. Drugs 1994; 47: 332–72.
9. Dunner D, Fieve R. Arch Gen Psychiatry 1974; 30: 561–6.
10. Emrich H, Zerssen D. von, Kissling W et al. Arch Psychiatr Nervenkr 1980; 229: 1–16.
11. Fountain N, Dreifuss F. Valproate /W. Lцsher (Ed.).1999; 265–76.
12. Henriksen O, Johannessen S. Acta Neurol Scand 1982; 65: 504–23.
13. Hooper W, Franklin M, Glue P et al. Epilepsia 1996; 37: 91–7.
14. Janz D. Arch Psychiat Nervenkr 1953; 191: 73–98
15. Keck P, Taylor V, Tugrul K et al. Biol Psychiatry 1993; 33: 542–6.
16. Ketter T, Post R, Theodore W Neurology 1999; 53 (Suppl.2): 53–67.
17. Lцsher W. Valproate /W. Lцsher (Ed.) 1999; 37–45.
18. Lцsher W. Valproate /W. Lцsher (Ed.) 1999; 1–3.
19. Mattson R, Cramer J, Collins J et al. N Engl J. Med 1992; 327: 765–71.
20. Meunier H, Carraz G, Meunier Y еt al. Therapie 1963; 18: 435–8.
21. Post R. Valproate /W. Lцsher (Ed.) 1999; 167–201.
22. Richens A, Ahmad S Brit Med J 1975; 2: 255–6.
23. Sato S, White B, Penry J et al. Neurology 1982; 32: 157–63.
24. Schmidt D Valproate /W. Lцsher (Ed.) 1999; 224–64.
25. Simon D, Penry J Epilepsia 1975; 22: 1701–08.
26. Turnbull D, Howel D, Rawlins M et al. Brit Med J 1985; 290: 815–9.
27. Turnbull D, Rawlins M, Weightman D et al. J Neurol Neurosurg Psychiatry 1982; 45: 55–9.
28. Vajda F, Mihaly G, Miles J et al. Neurology 1978; 28: 897–9.
29. Willmore L. Valproate /W. Lцsher (Ed.) 1999; 154–66.
30. Willmore L, Shu V, Wallin B et al. Neurology 1996; 46: 49–53.
31. Winsberg M, Degolia S, Strong C et al. APA New Research Program and Abstracts 1997; Abstr. NR113: 97.
32. Yuen A, Land G, Weatherley B et al. Brit J Clin Pharmacology 1992; 33: 511–3.


