Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№04 2003
Антаксон: современные подходы к терапии алкогольной зависимости №04 2003
Налтрексона гидрохлорид появился на фармацевтическом рынке и стал использоваться клиницистами более 30 лет назад. Препарат имеет свою завидную, интересную историю. Налтрексона гидрохлорид – это, пожалуй, один из очень немногих препаратов, который изначально был создан для лечения опиатной зависимости. В настоящее время все больше растет интерес исследователей в отношении его использования при алкогольной зависимости [1–10]. Достаточно быстрые темпы развития медицинской биологии в последние два-три десятилетия в значительной мере расширили представления о патогенезе наркологических заболеваний. В настоящее время уже накоплена достаточная теоретическая, экспериментальная и клиническая база для того, чтобы вполне обоснованно с патогенетической точки зрения объяснить применение налтрексона при алкогольной зависимости [11–16].
В эксперименте было показано, что опиоидная (эндорфинная) система тесно связана с дофаминергической системой и отвечает за психотропные эффекты алкоголя [17]. В 80-х годах прошлого века американской ученой Дэвис [18] была предложена концепция развития алкогольной зависимости, реализующаяся через опиатную систему, что указывало на общность механизмов формирования алкогольной и опиатной зависимости. Суть этой концепции заключалась в следующем. Как известно, алкоголь, попадая в организм, под действием соответствующих ферментов претерпевает цепь метаболических реакций и распадается с образованием ацетальдегида. В то же время алкоголь с учетом феномена положительной обратной связи вызывает дополнительное высвобождение из депо дофамина. При больших количествах потребляемого алкоголя в организме накапливается большая концентрация алкоголя и дофамина, происходит их конденсация, в результате чего образуются новые непептидные эндогенные соединения, обладающие опиатоподобным действием: тетрагидропапавералин, салсолинол, тетрагидро-b-карболин. Налтрексон, как известно, способен блокировать как центральные, так и периферические эффекты конденсированных продуктов и, соответственно, подавлять эндорфиноподобное действие алкоголя.
При рассмотрении вопросов патогенетически обоснованного применения налтрексона при алкогольной зависимости, нельзя не упомянуть об одном из важнейших биологических принципов функций рецепторных образований. Речь идет о степени сродства вещества к рецептору. Все вещества, связывающиеся с какими-либо рецепторами, имеют различную степень "сродства" к этим рецепторам. Вещество с более высокой степенью сродства вытесняет с рецепторов вещества с меньшим сродством и препятствует их дальнейшему воздействию на рецепторы и, следовательно, на организм. Налтрексон обладает более высоким сродством к опиатным рецепторам, чем морфин и его производные, и меньшим сродством, чем эндогенные лиганды опиатных рецепторов. Это обеспечивает его высокую безопасность с одной стороны и определенную избирательность действия с другой.
Налтрексон при лечении алкоголизма начал активно использоваться с конца 80-х – начала 90-х годов, и в середине 90-х годов FDA после значительной серии преклинических и клинических испытаний официально рекомендовал применение налтрексона как эффективного дополнительного средства при лечении алкогольной зависимости [10].
Вопрос эффективности применения налтрексона при алкоголизме неоднозначен. Большинство зарубежных авторов делают акцент на том, что эффективность терапии повышается при сочетанном использовании психотерапевтических методов и блокаторов опиатных рецепторов [1, 4, 6, 8]. Но есть и такие работы, в которых эффективность препарата оспаривается по сравнению с социо- и психотерапевтическим лечением (группы поддержки "Анонимные алкоголики" – АА) [19]. Тем не менее нельзя не отметить, что при проведении глобальных, мультицентровых, двойных слепых, контролируемых исследований в различных странах налтрексон показал высокие терапевтические результаты как при изолированном использовании, так и в сочетании с различными психотерапевтическими методами [5, 6, 8, 9]. В этих исследованиях показано, что пациенты, получавшие налтрексон, демонстрируют значительное снижение общего употребления алкоголя и удлинение ремиссий в сравнении с контрольной плацебо-группой. Результаты проведенных исследований подтверждают наряду с высокой терапевтической эффективностью безопасность препарата. Так, из наиболее часто встречающихся побочных эффектов отмечены тошнота, рвота, артралгии, головная боль, беспокойство, головокружение [20, 21].
Несмотря на множество клинических испытаний налтрексона в терапии алкогольной зависимости, можно выделить несколько существенных, охватывающих весь фармакологический спектр препарата [22–26], которые сводятся к следующему: 1) налтрексон уменьшает вызываемую алкоголем эйфорию, 2) как следствие этого, ослабевает влечение к алкоголю, 3) под действием налтрексона происходит уменьшение потребления алкоголя и
4) снижается частота рецидивов у больных алкогольной зависимостью.
В нашей стране до настоящего времени пока еще сохраняется дефицит работ о применении налтрексона при лечении алкоголизма, публикаций и исследований, посвященных данной теме, еще сравнительно мало.
В связи с этим в нашем центре было проведено клиническое исследование препарата "Антаксон" (налтрексона гидрохлорид) при лечении алкогольной зависимости.
Целью предпринятого исследования являлось изучение терапевтической эффективности антаксона при лечении алкогольной зависимости, оценка его влияния на патологическое влечение к алкоголю на различных этапах заболевания. Кроме того, в основные задачи входила оценка действия препарата при возможных рецидивах заболевания, его безопасности при длительном применении.
Материал и методы исследования
Общее число больных, участвующих в открытом контролируемом многоцентровом клиническом испытании антаксона, составило 296 пациентов. В основную группу вошли 150 человек, в контрольную – 146 пациентов. Все пациенты мужского пола.
Критерии включения и исключения из исследования
В исследование были включены следующие пациенты с диагностикой синдрома зависимости по МКБ-10: алкогольная зависимость; психические и поведенческие расстройства, связанные с алкогольной зависимостью; возраст от 18 до 55 лет; пациенты мужского пола.
Из исследования исключали больных: с острыми психотическими состояниями, включая пределириозные расстройства; больных с высоким суицидальным риском; пациентов с хроническими соматическими заболеваниями в стадии обострения; лиц с гиперчувствительностью к препаратам; пациентов, принимавших участие в исследованиях в течение предшествующих 3 мес.
У большинства включенных в исследование больных наблюдали развернутую клиническую картину средней (II) стадии. Это подтверждали следующие клинические проявления: первичное патологическое влечение к алкоголю (осознанное и неосознанное), утрата количественного контроля, максимальная толерантность к алкоголю, сформировавшийся развернутый алкогольный абстинентный синдром, а также заострение преморбидных личностных особенностей. Темп прогредиентности заболевания был квалифицирован как средний у 255 (86%) человек. Сравнительно у небольшого числа пациентов были диагностированы клинические признаки переходной (II–III) и конечной (III) стадий заболевания: снижение толерантности к алкоголю, меняющийся тип пьянства, появление пьянства по типу истинных запоев, признаки алкогольной деградации и энцефалопатии, значительные соматические и социальные последствия. Длительность заболевания варьировала от 4 до 38 лет.
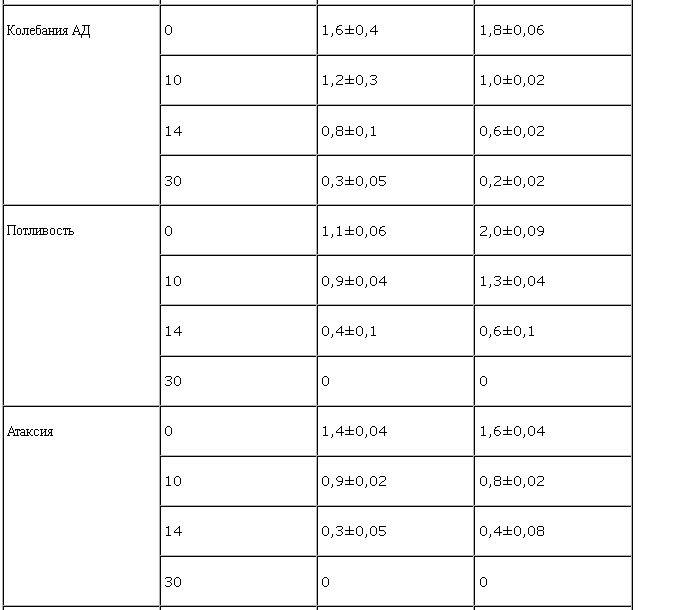
В структуре абстинентного синдрома присутствовали типичные для него соматовегетативные и психопатологические расстройства. Из психопатологических расстройств превалировали подавленное настроение, тревога, дисфория, внутренняя напряженность, беспричинные опасения, нарушения сна и пр. У всех больных отмечены гипергидроз, жажда, тремор, диспепсические нарушения, колебания артериального давления (АД), тахикардия, слабость, разбитость. Степень тяжести абстинентного синдрома была квалифицирована как средняя у 207 (70%) пациентов и как тяжелая у 87 (30%) пациентов.
По основным клинико-социальным характеристикам основная и контрольная группы не отличались, статистически значимых различий между группами не было.
Основным методом обследования являлся клинико-психопатологический. Клиническое исследование антаксона проводили соответственно составленному протоколу, максимально отвечающему международным требованиям GCP (качественных клинических испытаний). При оценке спектра терапевтической активности препарата использовали специально разработанные в отделении клинической психофармакологии шкалы оценки соматовегетативных, психопатологических проявлений в структуре абстинентного синдрома и постабстинентного состояния, шкалу общего клинического впечатления. Безопасность антаксона оценивали по динамике лабораторных показателей (АлАт, АсАт), производили сравнение в начале лечения (0-й день – день поступления) и в конце лечения (30-й день). Обследование больных осуществляли в день поступления (0-й день), в дальнейшем – на 3, 10, 30 и 90-й дни.
Для статистического анализа полученных результатов были использованы компьютерные программы Microsoft Excel 2000; Statistica (версия 5.1), проводили межгрупповое и внутригрупповое сравнение. Проверяли достоверность изменения таких параметров, как патологическое влечение к алкоголю, выраженность аффективных, поведенческих расстройств, вегетативных нарушений. Использовали параметрический t-критерий Стьюдента для уровня значимости pЈ0,05. Для сравнения относительных величин использовали метод определения средних ошибок.
Антаксон назначали в постабстинентном состоянии, суточная доза составляла 50 мг (1 капсула), недельная – 350 мг. Другие препараты с психотропной активностью на данном этапе исследования не использовали. Применяли также индивидуальную и групповую, в основном, рациональную психотерапию.
В контрольной группе применяли традиционную психофармакотерапию: антиконвульсанты (финлепсин), антидепрессанты (амитриптилин, леривон, коаксил), транквилизаторы (преимущественно феназепам) назначали в течение первых 5–7 дней. Проводили индивидуальную и групповую рациональную психотерапию.
Всем больным назначали гепатопротекторы, витамины и вегетотропные средства. Длительность клинического исследования в общем составила 12 нед.
Критерии оценки эффективности препарата
На первом этапе эффект признавали хорошим, если была достигнута 70% редукция симптомов по шкалам оценки соматовегетативных и психопатологических проявлений на 3-й день терапии; показатели шкалы общего клинического впечатления не превышали 2 баллов на 7-й день исследования. На 2-м этапе эффект признавали хорошим, если была достигнута устойчивая полная редукция симптомов по шкалам оценки соматовегетативных и психопатологических проявлений, а также отсутствовали рецидивы в течение 12 нед.
Результаты исследования
Эффективность антаксона оценивали по следующим параметрам: 1) оценка способности препарата поддерживать состояние, свободное от алкоголя; 2) его влияние на формирование более качественных ремиссий; 3) терапевтическое воздействие на патологическое влечение к алкоголю и связанные с ним психопатологические нарушения; 4) оценка безопасности препарата при длительном применении.
После купирования острых проявлений алкогольного абстинентного синдрома на первый план в клинической картине у больных выходили различные психопатологические расстройства. Несомненно, что наиболее стойким, стержневым расстройством заболевания являлось патологическое влечение к алкоголю.
Анализ клинических данных у больных обеих групп показал следующее. На первом этапе исследования (4 нед) у 15 (10%) пациентов из основной группы наблюдали единичные эксцессы употребления алкоголя, не приведшие в дальнейшем к возобновлению привычного характера злоупотребления алкоголем (табл. 1).

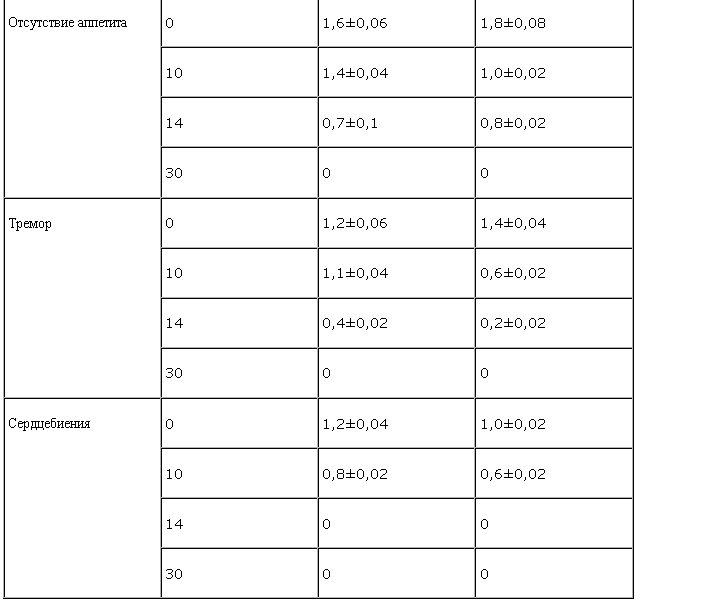
При приеме спиртных напитков на фоне лечения антаксоном были отмечены следующие особенности действия препарата. Органолептические свойства спиртных напитков (как правило, в 90% случаев больные употребляли пиво) сохранялись прежними, привычными, без ощутимых особенностей. У большинства пациентов наблюдали приступы слабой тошноты. По субъективным ощущениям состояние опьянения было достижимо, но достигалось несколько труднее, чем до начала лечения. После единичного употребления алкоголя 13 пациентов в последующем отказались от его дальнейшего употребления. Связывали это как с ухудшимся физическим состоянием, так и с тем, что "желания выпить нет". Ухудшение физического состояния проявлялось, в основном, нарушениями вегетативного характера: возобновлялись потливость, тремор, дрожь в теле (табл. 2). Эти расстройства диагностировали как в состоянии интоксикации, так и в постинтоксикационном периоде, их длительность была небольшой, максимально составляла до 12–16 ч.
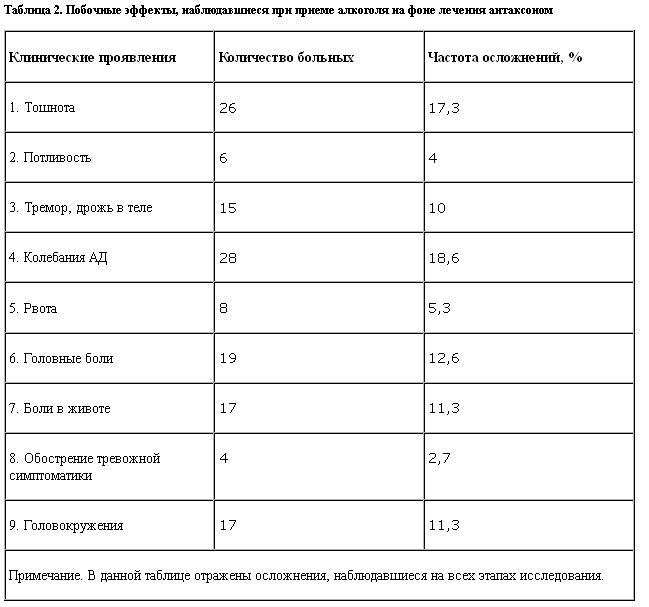
После соответствующей терапевтической коррекции данные расстройства нивелировались. Эти 13 пациентов остались в программе и продолжали прием антаксона.
У 2 пациентов из основной группы наблюдали более выраженные расстройства. При употреблении 350–500 мл водки в течение дня у этих больных к концу алкогольного эксцесса наблюдали выраженную тошноту, многократную обильную рвоту, боли в животе. Опьянение было выраженным, но, так же как и в предыдущих случаях, достигалось значительно труднее, чем до начала лечения. В дальнейшем у них наблюдали выраженное влечение к алкоголю, которое проявлялось тревожно-дисфорической симптоматикой. В связи с тем что в данном случае потребовалось назначение психотропных препаратов (сонапакс, финлепсин и некоторые другие), эти 2 пациента были вынуждены прекратить участие в исследовании (см. табл. 1).
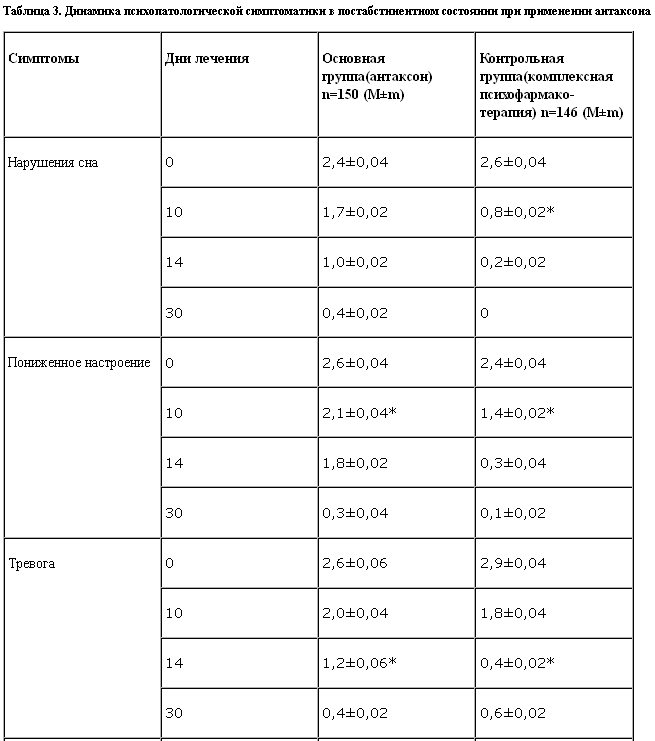
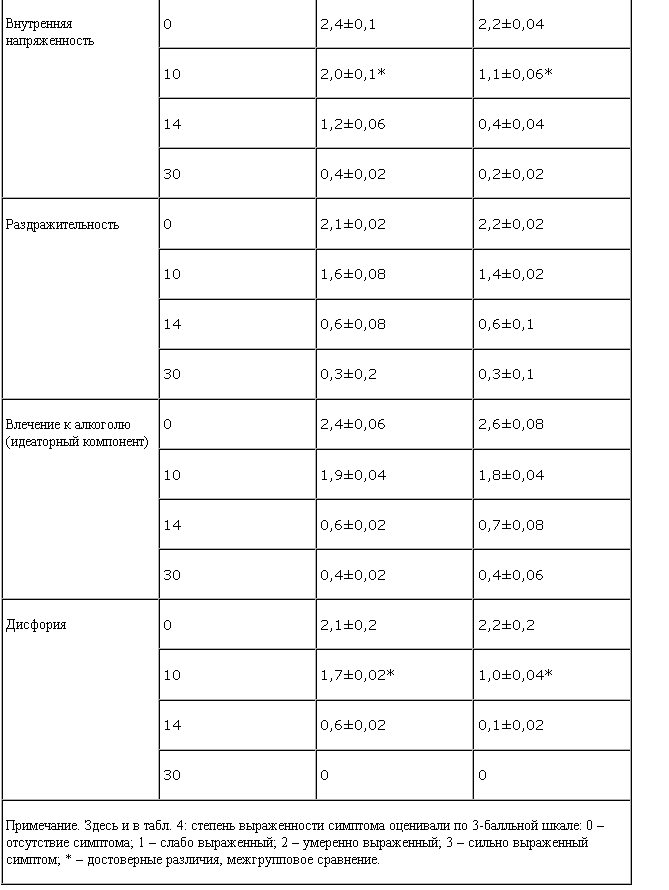
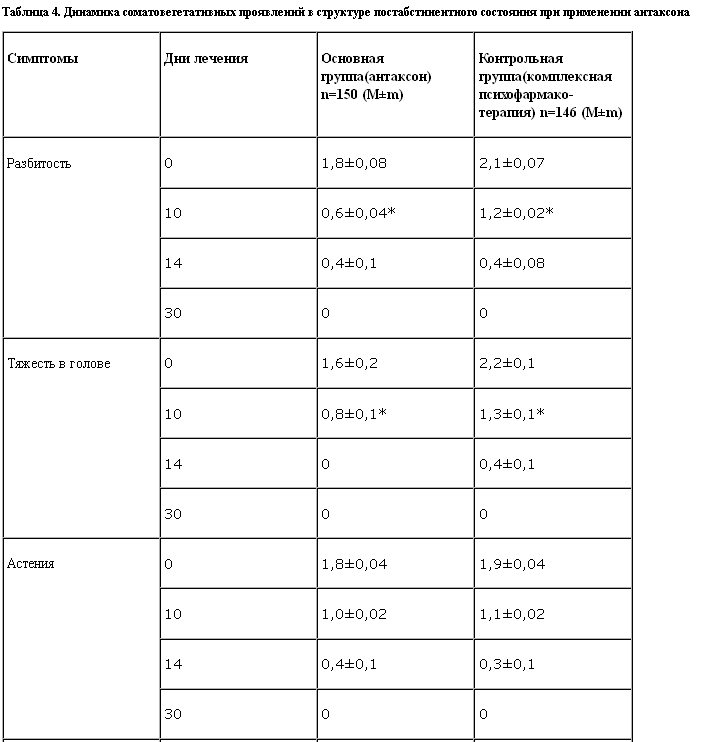
В качестве критерия улучшения состояния и его стабилизации при клиническом исследовании антаксона рассматривали дезактуализацию патологического влечения к алкоголю, полную и стойкую редукцию аффективной (главным образом, тревожной и дисфорической) симптоматики и вегетативных расстройств.
Этап формирования ремиссии
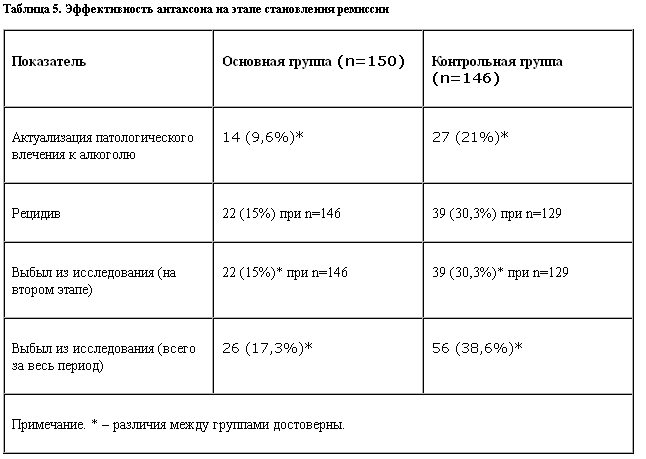
Курс стационарного лечения составлял в среднем, 30–45 дней. В дальнейшем пациентов переводили на амбулаторное наблюдение. Они продолжали принимать антаксон в домашних условиях. Консультации с лечащим доктором происходили 1 раз в 10 дней. На этом этапе лечения как в основной, так и в контрольной группах продолжали проводить индивидуальную и групповую психотерапию, осуществляли тщательный контроль за соматическим состоянием пациентов. На этом этапе из основной группы выбыло из исследования 22 (15%) человека (табл. 5).
Отказались от дальнейшего приема препарата 17 пациентов в связи с тем, что на фоне его приема употребление алкоголя сопровождалось значительными вегетативными расстройствами – тошнотой, многократной рвотой, колебаниями АД и головокружениями. В то же время состояние опьянения достигалось значительно труднее, эйфорическое действие алкогольных напитков проявлялось значительно менее выражено. У 5 человек наблюдали следующий феномен. По самоотчетам больных, период так называемого распивания, т.е. период от первого приема алкоголя до возобновления сформированных псевдозапоев, удлинялся. Если ранее данный период составлял в среднем от 14 до 30 дней, то при приеме антаксона он мог удлиняться до 45–60 дней.
Остальные 124 пациента основной группы отмечали значительное улучшение психофизического состояния на фоне приема антаксона.
В контрольной группе на втором этапе исследования рецидивы наблюдали у 39 (30,3%) пациентов, что значительно больше, чем в основной группе.
При длительном постоянном применении антаксона была отмечена заметная и значительная стабилизация психического состояния пациентов, в течение всего периода приема антаксона больные оставались спокойны, влечение к алкоголю не актуализировалось, сон, аппетит, настроение были ровными, стабильными. Это свидетельствует о значительной терапевтической эффективности препарата на этапе формирования и стабилизации ремиссии. Напротив, в контрольной группе более часто диагностировали колебания настроения, возобновление тревожной и/или дисфорической симптоматики, нарушения сна и снижение аппетита.
Использование шкалы общего клинического впечатления позволило подтвердить достаточный терапевтический эффект антаксона: на 7-й день исследования показатели шкалы не превышали 2 баллов (см. рисунок).
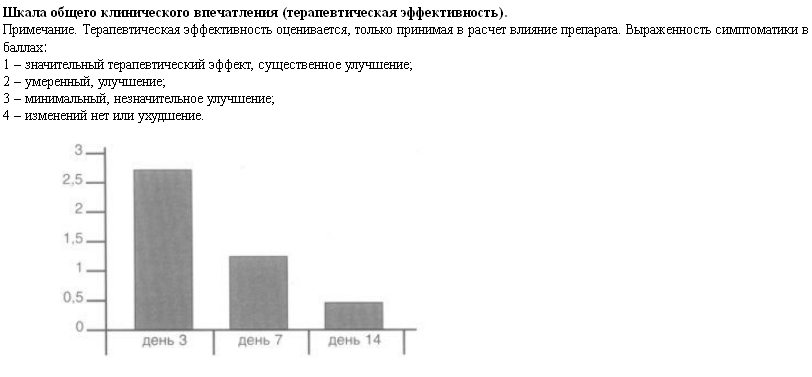
На протяжении всего периода применения антаксона у 17 (11,3%) пациентов наблюдали побочные эффекты вегетативного круга в начальном периоде приема препарата, такие как снижение аппетита, потливость, озноб. У 5 пациентов наблюдали почесывание. Однако эта симптоматика проходила самостоятельно на фоне дальнейшего приема препарата без дополнительной медикаментозной коррекции. Каких-либо осложнений не наблюдали. Динамический контроль лабораторных показателей (АлАт, АсАт, ГГТ, тимоловая проба, Глю и некоторые другие) ни в одном случае не выявил каких либо ухудшений. Это позволяет сделать вывод о безопасности препарата. Случаев привыкания к антаксону также отмечено не было.
Обсуждение
Влияние антаксона на патологическое влечение к алкоголю не вызывает сомнений, оно прослеживается в динамике при постоянном длительном приеме препарата. Терапевтическое действие антаксона увеличивалось при длительном его приеме, наиболее заметной эффективность препарата была на 2–3-м месяце его использования и проявлялась в достоверно меньшем количестве рецидивов по сравнению с контрольной группой. Сравнительно умеренное влияние антаксона на редукцию психопатологической и вегетативной симптоматики в рамках постабстинентного состояния позволяет предположить, что терапевтическая эффективность антаксона будет значительно более выражена при его комплексном применении с психотропными препаратами.
Прием препарата не вызывал значительных побочных эффектов, не влиял на работоспособность и концентрацию внимания, при его применении не наблюдалось каких-либо осложнений и случаев привыкания. Это свидетельствует о безопасности препарата и позволяет использовать его в амбулаторной практике.
Полученные результаты имеют большое значение для лечения больных с алкогольной зависимостью и позволяют рекомендовать антаксон как в комплексном лечении, так и изолировано в стационарных и амбулаторных условиях.


