Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№06 2013
Результаты обсервационной программы ДЖАЗ: «Эффективность препарата агомелатин (Вальдоксан) при лечении пациентов с тревожной депрессией в рамках большого депрессивного расстройства» №06 2013
Номера страниц в выпуске:14-22
Тревожные симптомы – одни из самых распространенных феноменов в структуре депрессивного расстройства, а синдром тревожной депрессии в клинике аффективной патологии занимает особое место. Известно, что включение тревоги приводит к утяжелению депрессивного состояния, более длительному течению заболевания, более значимым нарушениям социальной адаптации пациентов и повышению суицидального риска. Кроме того, тревожные симптомы в структуре большого депрессивного расстройства (БДР) ассоциируются с низким уровнем ответа на антидепрессивную терапию и возрастанием риска обострений.
Резюме. С целью получения дополнительных данных по терапевтической эффективности и переносимости агомелатина у пациентов с тревожной депрессией было проведено обсервационное исследование «ДЖАЗ». При участии 9 клинических центров из различных регионов России в течение 8-недельного периода агомелатин назначался в дозе 25 мг/сут вечером пациентам с симптомами тревоги в структуре большого депрессивного эпизода. Для динамической оценки состояния больных использовались психометрические шкалы: HDRS-17, CGI-I, ShARS, STAI, BSS, LSEQ. В исследование были включены 310 пациентов, из которых 294 полностью завершили программу. Агомелатин показал высокую эффективность (90% ремиссия + респонс) у пациентов с наличием тревожной симптоматики в структуре депрессивного расстройства. Выявлены особенности обратного развития отдельных компонентов тревожной депрессии.
Ключевые слова: агомелатин, тревога, депрессия.
The results of observational studies «JAZZ» – «The efficacy of agomelatine (Valdoxan) in the treatment of patients with anxious depression as part of a major depressive disorder»
A.S.Avedisova, K.V.Zaharova, M.P.Marychev
Serbsky National Research Centre for Social & Forensic Psychiatry
Summary. In order to achieve additional data on the therapeutic efficacy and tolerability of agomelatine in patients with anxious depression was conducted observational study «JAZZ». With the participation of nine clinical centers from different regions of Russia during the 8 week period, agomelatine was administered at a dose of 25 mg/day in the evening in patients with symptoms of anxiety in the structure of a major depressive episode. For dynamic assessment of the patients used psychometric scales: HDRS-17, CGI-I, ShARS, STAI, BSS, LSEQ. The study included 310 patients of whom 294 completed the program. Agomelatine demonstrated high efficiency (90% remission + response) patients the presence of anxiety symptoms in the structure of major depression. Regression shows the features of the individual components of anxious depression.
Key words: agomelatine, anxiety, depression.
Тревожные симптомы – одни из самых распространенных феноменов в структуре депрессивного расстройства [57], а синдром тревожной депрессии в клинике аффективной патологии занимает особое место [12]. Известно, что включение тревоги приводит к утяжелению депрессивного состояния, более длительному течению заболевания, более значимым нарушениям социальной адаптации пациентов и повышению суицидального риска [57, 23]. Кроме того, тревожные симптомы в структуре большого депрессивного расстройства (БДР) ассоциируются с низким уровнем ответа на антидепрессивную терапию и возрастанием риска обострений [21, 22, 54, 57].
К настоящему моменту накоплен большой клинический опыт применения агомелатина (Вальдоксана) при лечении депрессивных расстройств разной степени тяжести. Его эффективность была подтверждена в масштабных международных исследованиях и в Российских наблюдательных программах при лечении больных с БДР униполярного и биполярного течения (биполярное аффективное расстройство типа II – БАР), в том числе при тяжелой депрессии [5–9, 45].
Вместе с тем в серии доклинических исследований на животных [43, 50] выявлен анксиолитический эффект Вальдоксана, механизм которого связывается с особенностями рецепторного аффинитета препарата. Противоречия в оценках исследователей касаются лишь роли рецепторов определенного типа в патогенезе тревожных проявлений при депрессии и реализации фармакологического эффекта агомелатина. Одни авторы, отдавая первенство серотониновым 5НТ2С-рецепторам [29], приводят следующие доказательства: мыши с генетически отсутствующими 5НТ2С-рецепторами демонстрировали редукцию тревоги [18]; в разных исследованиях 5НТ2С-агонисты и антагонисты выявляют, соответственно, анксиогенный и анксиолитический эффекты [17, 19, 26, 33, 34, 42, 44]; антидепрессанты, механизм действия которых связан с антагонизмом к 5НТ2С-рецепторам (Вальдоксан, миртазапин, миансерин), проявляют анксиолитическую активность – как на моделях животных, так и у человека [16, 42, 53]; 1-кратное введение селективных ингибиторов обратного захвата серотонина вызывает у грызунов тревогу посредством косвенной активации 5НТ2С-рецепторов, тогда как их длительный прием уменьшает тревожность вслед за снижением регуляции этих же рецепторов [15, 20], что предполагает их клиническую пользу в долгосрочной терапии тревожных состояний [40].
Другие авторы анксиолитический потенциал агомелатина обосновывают его агонизмом по отношению к мелатониновым рецепторам, в доказательство чего приводят данные о роли мелатонина в патогенезе тревожных расстройств: участие эпифиза в антистрессорной защите организма [4, 14] посредством усиления выработки мелатонина в ответ на разнообразные стрессовые и анксиогенные стимулы [25, 40]; роль мелатонина в хронобиологической регуляции, с учетом патогенетической связи между развитием тревоги и дезорганизацией биологических ритмов [2].
Кроме того, мелатонин проявляет анксиолитические особенности в экспериментах на грызунах [25, 27, 35–37, 47, 48, 51], снижает тревожность у пациентов, готовящихся к хирургической операции [46]. Анксиолитические свойства мелатонина изучались и рядом отечественных авторов [2, 10]. На модели конфликтной ситуации у крыс выявлено сходство противотревожной активности мелатонина с бензодиазепинами (диазепамом, тофизопамом) и b-адреноблокатором (пропранолол) [2]. Наряду с этим применение мелатонина у психически здоровых молодых добровольцев приводило к снижению реактивной тревожности, причем в большей степени у лиц с изначально высокими ее значениями [1, 10].
Небезуспешными оказались попытки объяснить анксиолитический эффект Вальдоксана действием на обе рецепторные системы – мелатонинергическую и серотонинергическую. В серии экспериментов на валидизированных моделях тревоги у грызунов была показана более выраженная эффективность препарата по сравнению с монорецепторными агентами (антагонистами 5НТ2С- и агонистами МT1/MT2-рецепторов) [47].
Число клинических исследований, посвященных влиянию Вальдоксана на тревожную симптоматику, невелико. Имеются данные рандомизированного двойного слепого плацебо-контролируемого исследования с целью изучения эффективности препарата при генерализованном тревожном расстройстве (ГТР) [56]. Результатом терапии 121 пациента с диагнозом ГТР в течение 12 нед явилось превосходство агомелатина по эффективности над плацебо, тогда как по уровню побочных эффектов группы были сопоставимы. Полученные данные были подтверждены в другом исследовании, посвященном эффективности и переносимости агомелатина в предотвращении рецидива у пациентов с ГТР [55].
В течение 6 мес наблюдения число пациентов с рецидивом на терапии агомелатином (22 пациента; 19,5%) было почти в 2 раза меньше, чем в группе плацебо (35 пациентов; 30,7%). Агомелатин также превосходил плацебо в предотвращении рецидивов в подгруппе более тяжелых пациентов (HARS≥25 и CGI-S≥5). Представление об анксиолитической активности Вальдоксана дают также результаты метаанализа 6 многоцентровых двойных слепых рандомизированных исследований (3 плацебо-контролируемых и 3 – с препаратом сравнения: флуоксетином, сертралином и венлафаксином), в которых использовались шкалы HARS и HDRS-17. Вальдоксан превосходил по эффективности как плацебо, так и препараты сравнения по действию на депрессивную и тревожную симптоматику [58].
Имеющиеся в литературе экспериментальные и клинико-фармакологические данные о положительном воздействии Вальдоксана на симптомы тревоги предопределили цель проведения настоящей натуралистической программы – получение данных о терапевтической эффективности и переносимости препарата Вальдоксан (агомелатин) при лечении пациентов с тревожной депрессией в рамках БДР. Дополнительными целями являлись: 1) оценка влияния Вальдоксана на уровень соматической и психической тревоги, 2) оценка влияния Вальдоксана на уровень реактивной тревоги (РТ) и личностной тревоги (ЛТ), 3) выявление зависимости эффективности Вальдоксана от степени редукции тревоги (шкала Шихана) и инсомнии (LEEDS), 4) оценка динамики суицидальных тенденций в процессе терапии.
Материалы и методы
Исследование проводилось в период с 01.02.2012 г. (дата включения 1-го пациента) по 30.06.2012 г. (дата завершения исследования последним пациентом) при участии
9 клинических центров, расположенных в разных регионах РФ:
1. Москва – профессор А.С.Аведисова (ГНЦССП им. В.П.Сербского, руководитель проекта).
2. Москва – академик РАМН А.Б.Смулевич (НЦПЗ РАМН).
3. Санкт-Петербург – профессор Н.Г.Незнанов (НИПНИ им. В.М.Бехтерева).
4. Нижний Новгород – профессор Л.Н.Касимова (Ниж-ГМА).
5. Ставрополь – кандидат психологических наук Г.П.Былим (СГМУ).
6. Красноярск – В.В.Монастырская (заместитель главного врача ККПНД).
7. Томск – доктор медицинских наук Е.Д.Счастный (НИИ психического здоровья СО РАМН).
8. Иркутск – профессор А.С.Бобров (ИГМАПО).
9. Иркутск – профессор В.С.Собенников (ИГМУ).
По своему дизайну проведенное исследование являлось обсервационным, общей продолжительностью 8 нед
(56 дней). В него включались пациенты обоего пола в возрасте от 18 до 65 лет, находящиеся в психиатрическом стационаре или на амбулаторном лечении с диагнозами по Международной классификации болезней 10-го пересмотра (МКБ-10): «Депрессивный эпизод умеренный (F32.1) или тяжелый (F32.2) без психотических симптомов», «Рекуррентное депрессивное расстройство; умеренный (F33.1) или тяжелый (F33.2) депрессивный эпизод без психотических симптомов»; с суммой баллов по шкале HDRS-17 не менее 17, по шкале самооценки тревоги Шихана – не менее 30; имеющие показания для назначения Вальдоксана или в качестве первого антидепрессанта (стандартные показания для терапии антидепрессантами), или в качестве замены предыдущего антидепрессанта в случае его плохой переносимости и/или неудовлетворительной эффективности. Для женщин с сохранной детородной функцией дополнительным условием было применение адекватных медицинских средств контрацепции (гормональная контрацепция, внутриматочная спираль, двойной барьерный метод – презерватив в сочетании со спермицидом). Все пациенты должны были дать письменное информированное согласие на участие в обсервационной программе.
Критерии исключения: наличие суицидального риска (более 2 баллов по пункту 3 шкалы HDRS-17 и/или по клинической оценке исследователя); наличие психотических симптомов (по клинической оценке лечащего врача); резистентность к терапии другими антидепрессантами; шизофрения, шизоаффективное расстройство, органическое поражение центральной нервной системы, деменция, эпилепсия, рассеянный склероз, паркинсонизм, болезнь Альцгеймера, черепно-мозговая травма и ее последствия, биполярное аффективное расстройство; алкоголизм или наркомания в анамнезе; тяжелые или декомпенсированные соматические или неврологические заболевания; печеночная недостаточность; одновременное применение сильных ингибиторов цитохрома CYP1A2 (ципро-флоксацин); беременность или кормление грудью; установленная ранее индивидуальная непереносимость либо неэффективность Вальдоксана в анамнезе при назначении препарата в адекватной дозе (не менее 25 мг/сут) и длительности (не менее 4 нед).
Критерии преждевременного выбывания пациента из исследования: отказ пациента; появление психотических симптомов, суицидального риска или симптомов мании; развитие нежелательных явлений (НЯ) или реакций, препятствующих дальнейшему проведению терапии; нарушение функции печени (повышение аспартатаминотрансферазы, аланинаминотрансферазы или щелочной фосфатазы более чем в 3 раза относительно верхней границы нормы, или повышение общего билирубина более чем в 2 раза относительно верхней границы нормы, или развитие желтухи); возникновение сопутствующих соматических заболеваний/симптомов или обострение хронических заболеваний, не связанных с приемом Вальдоксана; необходимость приема сильных ингибиторов цитохрома CYP1A2 (ципрофлоксацин); несоблюдение режима терапии или беременность.
Вальдоксан назначался в стартовой терапевтической дозе 25 мг (1 таблетка) в соответствии с инструкцией по медицинскому применению. В случае недостаточного, по мнению исследователя, эффекта препарата его доза могла быть повышена до 50 мг (2 таблетки) 1-кратно вечером. Доза 50 мг являлась максимально допустимой.
В ходе 8-недельного периода наблюдения было предусмотрено 7 визитов: визит 1 – фон, визит 2 – на 3-й день терапии, визит 3 – на 7-й день, визит 4 – на 14-й день, визит 5 – на 28-й день, визит 6 – на 42-й день, визит 7 – на
56-й день терапии. Клинические данные регистрировались в индивидуальной регистрационной карте (ИРК).
Помимо психопатологического и общесоматического обследования (включая артериальное давление, частоту сердечных сокращений, биохимический анализ крови, измерение массы тела) в рамках данного исследования использовались следующие шкалы: HDRS-17 (шкала депрессии Гамильтона), CGI-I (шкала общего клинического впечатления для оценки улучшения состояния), шкала самооценки тревоги Шихана (ShARS), шкала самооценки уровня тревожности Спилберга–Ханина (STAI), шкала суицидальных мыслей Бека (BSS), шкала оценки показателей сна (LSEQ); табл. 1.
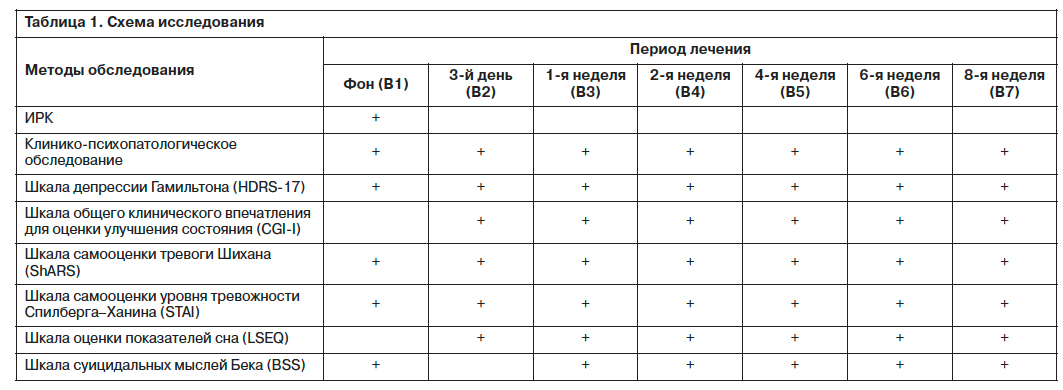
Для оценки эффективности терапии Вальдоксаном были использованы следующие критерии: динамика баллов HDRS-17 на фоне терапии, частота формирования ремиссии, процент респондеров, динамика баллов по ShARS, влияние терапии на оценки РТ и ЛТ (STAI), динамика баллов по BSS, изменение параметров опросника LSEQ на фоне терапии, оценка динамики психического состояния по шкале CGI-I. В конце исследования врачами и пациентами заполнялся краткий опросник, предлагающий оценить эффективность лечения.
Всего в исследование были включены 310 пациентов, социодемографические характеристики которых отображены в табл. 2. Большинство из них женщины – 81,61%; мужчин лишь 18,39%. Средний возраст обследованных 42,5±12,9 года, что указывает на принадлежность изучаемого контингента к наиболее активной в социальном плане части населения. О том же свидетельствует и уровень образования: 58,71% обследованных имели высшее образование, а 5,16 и 21,61% – неоконченное высшее и среднее специальное соответственно, что в совокупности составило 85,48%. Среднее образование получили 10,65% больных, неполное среднее – 0,32%. В 11 (3,55%) случаях данные по уровню образования отсутствовали. Профессионально занятыми среди изученного контингента являлись 67,42% больных, на пенсии – 15,16%, учились – 4,19%, домохозяйки – 7,74% пациентов. Только 4,84% являлись безработными, 1,29% – имели инвалидность по соматическому заболеванию, а 0,65% – по психическому. Более 1/5 (53,55%) больных состояли в браке, 18,39% – одинокие, 16,45% – разведены, 8,06% – вдовы. В остальных случаях (11 человек; 3,55%) эти данные отсутствовали.
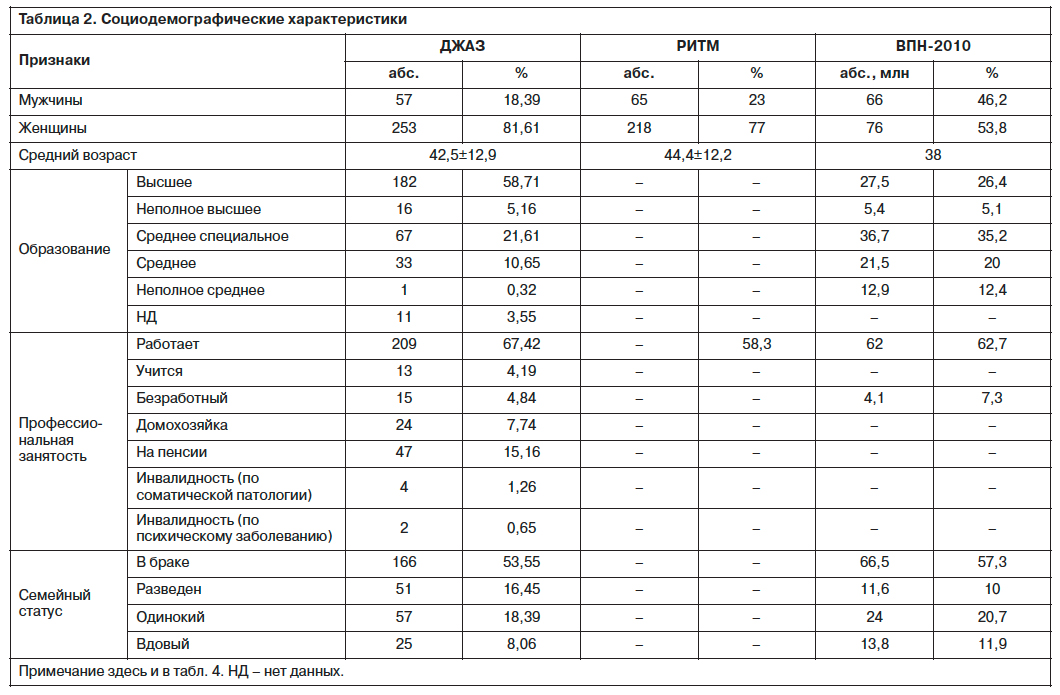
С целью выявления смещения социодемографических показателей исследуемой выборки пациентов с тревожной депрессией от средних в населении РФ и в выборке пациентов с депрессией проводилось сопоставление данных, характеризующих пол, возраст, уровень образования и др. с итогами Всероссийской переписи населения 2010 г. (ВПН-2010), а также с больными, участвующими в обсервационной программе (РИТМ) по изучению эффективности Вальдоксана при депрессивном эпизоде без явлений тревоги [13]. В целом это сравнение обозначило существенное отклонение социодемографических показателей пациентов с депрессией и тревожной депрессией от популяции жителей РФ.
Так, среди пациентов с тревожной депрессией и депрессивным эпизодом значительно преобладали женщины (81,6% и 77% против 53,8% соответственно). Средний возраст жителей РФ составлял 38 лет, тогда как этот показатель для пациентов с тревожной депрессией и с депрессией был выше (42,5±12,9 и 44,4±12,2 соответственно). Для группы ДЖАЗ был характерен высокий процент лиц с высшим образованием – 58,7% (26,4% – ВПН-2010), разведенных – 16,5% (10% – ВПН-2010) при примерно одинаковых характеристиках профессиональной занятости.
С клинической точки зрения, у большинства пациентов диагностировался единичный депрессивный эпизод (63,22%), а у 32,26% больных депрессивные проявления возникали в рамках рекуррентного депрессивного расстройства. При этом средняя степень выраженности депрессии (диагнозы F32.1 и F33.1 по МКБ-10) до начала терапии отмечалась у 84,1% пациентов, тогда как тяжелая степень – у 11,29%. У 4,52% включенных пациентов диагноз указан не был. Средний балл по HDRS-17 на момент включения составил 23,9±4,6 балла, по шкале самооценки тревоги Шихана – 82,5±21,0 балла (тяжелая тревога). Уровень реактивной тревоги, оцениваемый по шкале самооценки Спилберга–Ханина, составлял 59,2±8,6 балла, для ЛТ – 57,2±9,5 балла (табл. 3), что соответствовало высокому уровню тревожности. Большая часть (88,39%) больных, включенных в исследование, не имели суицидальных мыслей или тенденций, тогда как у 11% пациентов баллы по шкале BSS составляли от 1 до 12.
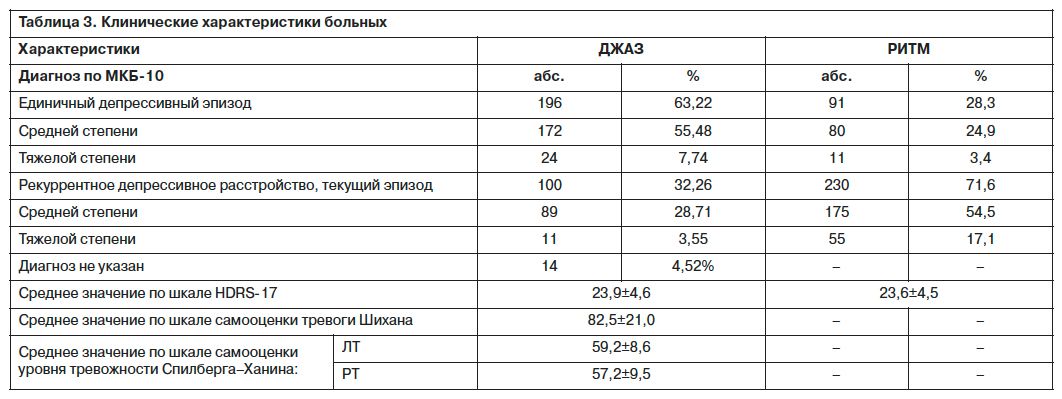
Для выявления вклада отчетливой тревожной симптоматики в клиническую характеристику пациентов с тревожной депрессией было проведено сравнение исследуемой выборки с данными обсервационного исследования РИТМ. Выявлено, что у пациентов с тревожной депрессией в 2 раза (63,2%) чаще диагностировался единичный депрессивный эпизод и в 2 раза (32,2%) реже – рекуррентное депрессивное расстройство по сравнению с группой лиц, принимавших участие в исследовании РИТМ (28,3 и 71,6% соответственно). Депрессии в 2 группах были представлены преимущественно депрессиями средней степени выраженности (84 и 79% соответственно) и существенно меньшим числом больных с тяжелым эпизодом (11 и 20% соответственно). Средний суммарный балл по шкале HDRS-17 не различался между 2 сравниваемыми группами.
Более 1/2 (57,48%) больных, принявших участие в исследовании, получали терапию в психиатрических больницах (как амбулаторно, так и стационарно). 23,13% проходили курс лечения в поликлинике, 13,27% – в консультативно-диагностическом центре. Для 34 (11,56%) больных такие данные отсутствовали. Таким образом, большая часть (82,58%) пациентов находились на амбулаторном режиме лечения, и только 12,26% человек наблюдались стационарно.
При этом 256 (82,58%) больных получали Вальдоксан в качестве первого антидепрессанта для лечения текущего депрессивного эпизода, 33 (10,65%) пациента – как замену предыдущего антидепрессанта, причем у 23 (7,42%) пациентов назначаемый ранее препарат был неудовлетворительным по эффективности, а у 10 (3,23%) – по переносимости. В 6,77% (21 пациент) случаев эти данные отсутствовали. Заменяемым оказался широкий спектр в основном современных антидепрессантов: пароксетин (2,26%), сертралин (1,61%), амитриптилин (1,29%), флуоксетин (0,97%), венлафаксин (0,65%), флувоксамин (0,65%), азафен (0,65%), мапротилин (людиомил) (0,32%), дулоксетин (0,32%), эсциталопрам (0,32%). Для 5 (1,61%) человек принимаемый ранее антидепрессант был неизвестен.
В течение последнего года до включения в исследование 38,71% (120 человек) получали терапию всеми классами психотропных средств и фитотерапией: 19,68% – препаратами растительного происхождения, 16,45% – транквилизаторами, 15,16% – антидепрессантами, 4,84% – нейролептиками, 0,65% – антиконвульсантами.
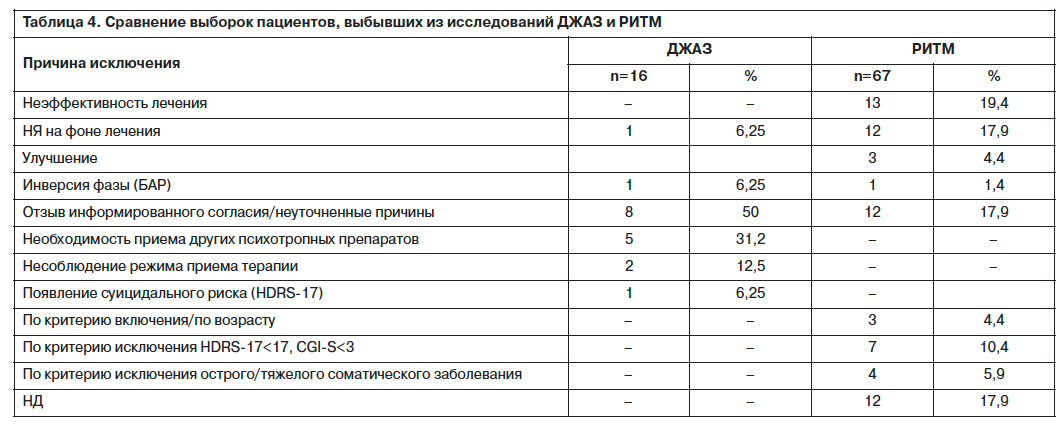
Из всех включенных в исследование 310 пациентов (ВП) полностью завершили программу (ПЗП) 294 (94,8%) человека, что свидетельствует о высоком уровне комплаентности. Только 16 (5,16%) больных по разным причинам преждевременно выбыли (ПВ) из исследования. Сравнительный анализ 3 групп пациентов (ВП, ПВ и ПЗП) показал сопоставимость выборок по социодемографическим и некоторым клиническим показателям (средний балл по шкалам HDRS-17, Шихана, Спилберга–Ханина). В то же время сравнение выборок ПВ и ПЗП показало преобладание в группе ПВ лиц с рекуррентным депрессивным расстройством (p=0,035), получавших в последний год нейролептики (p=0,0077), страдающих сахарным диабетом (p=0,000045), а также пациентов, которым Вальдоксан назначен в качестве замены предыдущего антидепрессанта (p=0,00001). Показатель суицидальности (BSS) был достоверно выше в группе ПВ (p<0,00001).
Если основными причинами преждевременного выбывания у пациентов с тревожной депрессией являлись отказ пациента (50%), необходимость приема других психотропных препаратов (31,2%) и несоблюдение режима терапии (12,5%), то у пациентов с депрессивным эпизодом без явлений тревоги (РИТМ) причины преждевременного отказа располагались в следующем порядке: неэффективность лечения (19,4%), наличие НЯ и неуточненный отказ пациента (по 17,9%); табл. 4. Следует обратить внимание на высокий процент выбывания по причине инверсии аффекта в группе с тревожной депрессией (6,3%) по сравнению с депрессией без явлений тревоги (1,4%), что соответствует представлению некоторых авторов об ассоциированности тревожной депрессии с биполярным спектром [31, 52].
Далее в статье будут рассмотрены только пациенты, полностью завершившие исследование согласно протоколу (294 человека; 94,8%).
В ходе терапии 181 (61,56%) больному Вальдоксан назначался в дозе 25 мг/сут в течение всего периода лечения, 113 (38,44%) – доза препарата была повышена до 50 мг/сут. Последний показатель несколько превосходит таковой в программе РИТМ (27,4%), что свидетельствует о необходимости более частого повышения дозировки препарата при тревожной депрессии. Чаще всего увеличение дозы происходило на 4-м визите терапии (21,43%), реже – на 5-м (13,27%) и для некоторых больных – на 6 (1,02%) и 3-м (0,68%) визитах. В качестве сопутствующей анксиолитической терапии (43 человека; 14,62%) назначался диазепам (6,12%), феназепам (3,06%), гидроксизин (2,38%), медазепам (2,04%), оксазепам (0,34%). Несмотря на то что алпразолам и депакин хроно были запрещены протоколом, их получали 2 пациента (по 0,34%).
Общая эффективность терапии Вальдоксаном
при тревожной депрессии в рамках БДР
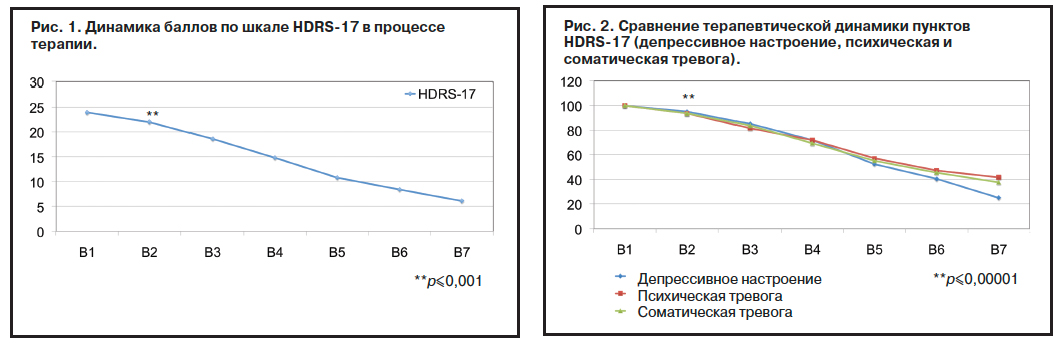 В целом если до лечения средний балл по HDRS-17 составлял 23,9±4,6, то в конце – лишь 6,1±3,6, т.е. его редукция к моменту окончания исследования достигала 74,47%, что свидетельствует о достаточно высоком уровне антидепрессивной активности исследуемого препарата. Сравнение общей эффективности терапии Вальдоксаном в 2 обсервационных программах показало, что у пациентов с тревожной депрессией (ДЖАЗ) процент ремиттеров был выше (69% vs 41,7%), в то время как количество респондеров (21%) и нонреспондеров (9,8%) было ниже аналогичных показателей у пациентов с депрессией без признаков тревоги – РИТМ (37 и 21% соответственно), что, возможно, объясняется меньшим процентом лиц с депрессией тяжелой степени в данной наблюдательной программе.
В целом если до лечения средний балл по HDRS-17 составлял 23,9±4,6, то в конце – лишь 6,1±3,6, т.е. его редукция к моменту окончания исследования достигала 74,47%, что свидетельствует о достаточно высоком уровне антидепрессивной активности исследуемого препарата. Сравнение общей эффективности терапии Вальдоксаном в 2 обсервационных программах показало, что у пациентов с тревожной депрессией (ДЖАЗ) процент ремиттеров был выше (69% vs 41,7%), в то время как количество респондеров (21%) и нонреспондеров (9,8%) было ниже аналогичных показателей у пациентов с депрессией без признаков тревоги – РИТМ (37 и 21% соответственно), что, возможно, объясняется меньшим процентом лиц с депрессией тяжелой степени в данной наблюдательной программе.
Оценка степени улучшения состояния пациентов по шкале CGI-I характеризовалась сходными с предыдущей оценкой процентами: на 7-м визите (56-й день терапии) только у 2 (0,68%) пациентов состояние оставалось без изменений, у 16 (5,44%) больных отмечалось незначительное улучшение, у 87 (29,59%) – существенное улучшение и у 189 (64,29%) – выраженное улучшение.
Помимо редукции депрессивной симптоматики была показана высокая эффективность Вальдоксана в отношении тревожных проявлений. Объективная оценка заключалась в исследовании подпунктов HDRS-17 «психическая» и «соматическая тревога». Уровень «психической тревоги» с высокой статистической достоверностью (p<0,00001) снижался уже после первых 3 дней терапии, аналогичная тенденция отмечалась и в отношении «соматической» тревоги (p<0,00001); рис. 2.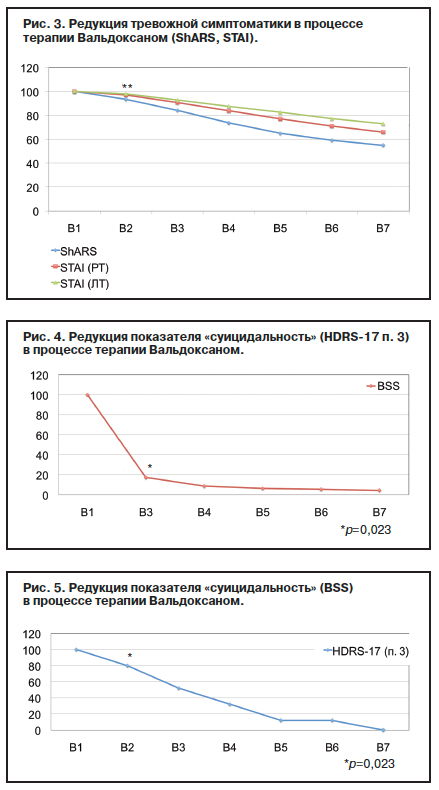
Динамика баллов по ShARS также показала статистически значимую редукцию по сравнению с фоном уже на 3-й день терапии. Высокий темп редукции сохранялся до 7-го визита исследования. Фоновый балл по шкале снижался с 81,3±20,9 (тяжелая тревога) до 44,7±10,3 (тревога средней выраженности) на последнем визите. Менее отчетливые результаты были получены в отношении РТ и ЛТ, оцениваемых по STAI. Средний балл до начала терапии составил 59,2±8,7 для РТ и 57,1±9,5 для ЛТ, что соответствует очень высокому уровню тревожности (более 46 баллов). В конце исследования баллы снизились до 39,1±10,4 и 41,7±10,2 соответственно, что отвечает критериям тревожности среднего уровня. Статистически значимые отличия по сравнению с фоновыми показателями наблюдались, начиная с 3-го дня терапии (рис. 3).
Клиническая оценка суицидальной активности (BSS) больных в фоновом исследовании показала наличие легко выраженной суицидальности у 33 (12,6%) пациентов, которая оценивалась у 16 (5,16%) человек в 1 балл, у 12 (4%) – от 2 до 6 баллов и у 5 (1,7%) – от 7 до 12 баллов. При этом у 3 больных имелись суицидальные попытки в анамнезе. Уже на 3-й день терапии Вальдоксаном суицидальные проявления практически нивелировались, а на 7-м визите исследования только у 4 пациентов сохранялись суицидальные переживания, относящиеся только к 1-му пункту шкалы (пациенты отмечали, что они в слабой степени хотят жить, но не отмечали, что не хотят жить); рис. 4.
Все остальные 18 пунктов достигали нуля. По HDRS-17 наблюдалась сходная, но более растянутая по времени динамика редукции показателя «суицидальность». Статистически достоверная редукция данного пункта отмечалась уже после первых 3 дней терапии (р=0,023), а на 3-м визите (7-й день терапии) фиксировалась практически 2-кратная степень редукции. Причем к окончанию исследования пациенты с наличием суицидальных мыслей отсутствовали (рис. 5). Различие в результатах, оцениваемых «суицидальность» по двум шкалам, вероятно, связано с более дифференцированной оценкой этого явления при помощи BSS.
С целью выявления связи между показателями суицидальности (BSS) и такими параметрами, как заторможенность, ажитация и депрессивное настроение, оцениваемыми по HDRS-17, был проведен корреляционный анализ. Результаты статистической обработки полученных результатов выявили, что сумма баллов по BSS коррелировала с тяжестью п. 1 шкалы HDRS-17 (депрессивное настроение; k=0,2263), но не была связана с пп. 8 («заторможенность») и 9 («ажитация»).
Шкала LSEQ позволила комплексно изучить изменения в процессе терапии Вальдоксаном таких характеристик сна, как «засыпание», «качество сна», «пробуждение», «состояние после сна». Качество засыпания постепенно улучшалось от визита к визиту и к моменту окончания исследования у большинства пациентов достигало доболезненного уровня (р≤0,00001). Качество сна также плавно нормализовалось в процессе лечения: пациенты отмечали, что сон становился более спокойным, уменьшалась частота ночных пробуждений (р≤0,00001). Параметр «пробуждение» оценивался по таким критериям, как легкость и быстрота. Эта составляющая ночного сна нормализовалась более медленно по сравнению с двумя предыдущими характеристиками, тем не менее достигала удовлетворительного уровня к окончанию терапии (р≤0,00001). Состояние после сна оценивалось пациентами на основании самочувствия после пробуждения, по готовности к немедленным действиям, а также по координации движений. В процессе лечения отмечалось статистически достоверное улучшение этого показателя (р≤0,00001); рис. 6.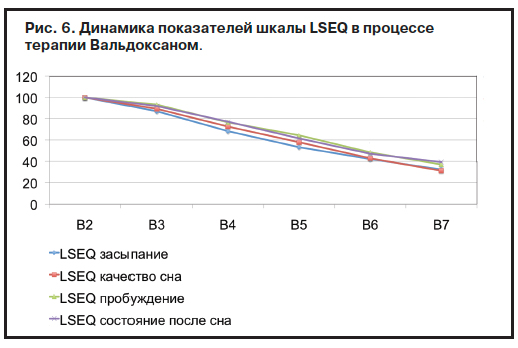
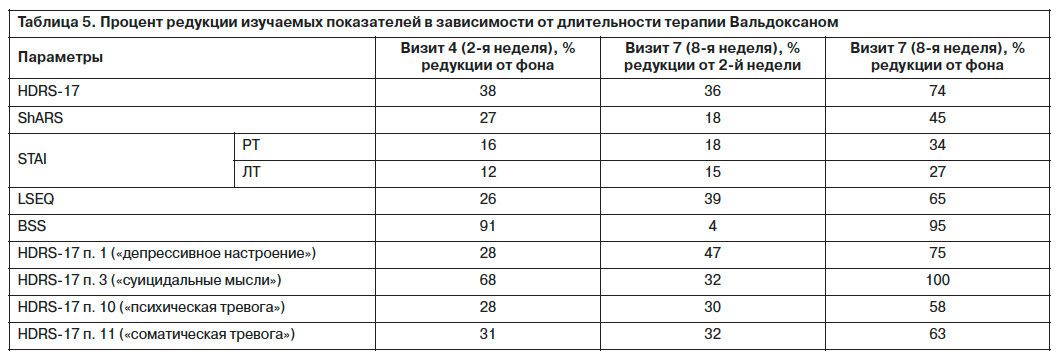
С целью подтверждения предположения о быстроте редукции определенной симптоматики при терапии Вальдоксаном был проведен анализ степени и времени обратного развития тревожной депрессии. При этом сопоставлялась выраженность редукции различных показателей шкал в течение 2 периодов терапии: первые 2 нед и последующие 6 нед. Также оценивались показатели общей редукции всех изучаемых показателей на всем протяжении лечения (табл. 5). Как и предполагалось, процесс обратного развития тревожной депрессии наблюдался преимущественно в первые 2 нед терапии, что подтверждалось значительной редукцией большинства показателей в эти сроки. Особо быстрое снижение баллов в первые 2 нед лечения наблюдалось при оценке суицидальности (на 91% по BSS и 68% по HDRS-17 п. 3). Показатели генерализованной тревоги (ShARS) в большей степени снижались в первые 2 нед (на 27%), чем в последующие 6 нед (на 18%) исследования. Остальные показатели за 2 нед терапии редуцировались практически с той же скоростью, как и за последующие 6 нед (HDRS-17, HDRS-17 пп. 10 и 11), но при этом на первые недели лечения приходилось 50% и более всей отмеченной обратной динамики.
Через 2 нед терапии Вальдоксаном процесс обратного развития симптоматики замедлялся, но показатели таких шкал, как HDRS-17 п. 1 и LSEQ, на этом этапе редуцировались несколько в большей степени. Тревожность как личностная особенность (STAI) подвергалась наименьшей динамике в процессе терапии с примерно равным распределением в 1 и 2-й ее период.
По результатам опросника, оценивающего удовлетворенность терапией врачей и пациентов, было выявлено, что около 1/2 (47,96%) врачей оценили эффективность лечения Вальдоксаном как «отличную», 43,8% – как «хорошую», и только 6,4% считали эффективность «удовлетворительной» и 1,3% – «плохой» (0,3% – данные отсутствуют). 87,4% врачей рекомендовали своим пациентам продолжать терапию этим препаратом. Мнение пациентов было сходным. Так, 42,5% больных оценили эффективность лечения как «отличную», 48,9% – как «хорошую», 6,1% – как «удовлетворительную» и 2,0% – как «плохую» (0,3% – данные отсутствуют); рис. 7. При этом 84% пациентов выразили желание продолжить терапию Вальдоксаном и только 15,6% отказались от продолжения лечения.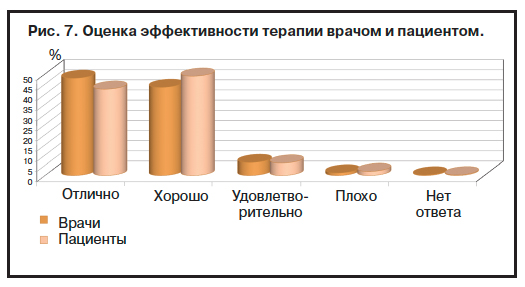
Выводы
Сведения об авторах
А.С.Аведисова – проф., руководитель отд. терапии психических и поведенческих расстройств ФГБУ ГНЦССП им. В.П.Сербского Минздрава России. E-mail: Alla.Avedisova@gmail.com
К.В.Захарова – канд. мед. наук, ст. науч. сотр. отд. терапии психических и поведенческих расстройств ФГБУ ГНЦССП
им. В.П.Сербского Минздрава России. E-mail: ksushkaa@bk.ru
М.П.Марачев – канд. мед. наук, науч. сотр. отд. терапии психических и поведенческих расстройств ФГБУ ГНЦССП
им. В.П.Сербского Минздрава России. E-mail: marachevm@gmail.com
Ключевые слова: агомелатин, тревога, депрессия.
The results of observational studies «JAZZ» – «The efficacy of agomelatine (Valdoxan) in the treatment of patients with anxious depression as part of a major depressive disorder»
A.S.Avedisova, K.V.Zaharova, M.P.Marychev
Serbsky National Research Centre for Social & Forensic Psychiatry
Summary. In order to achieve additional data on the therapeutic efficacy and tolerability of agomelatine in patients with anxious depression was conducted observational study «JAZZ». With the participation of nine clinical centers from different regions of Russia during the 8 week period, agomelatine was administered at a dose of 25 mg/day in the evening in patients with symptoms of anxiety in the structure of a major depressive episode. For dynamic assessment of the patients used psychometric scales: HDRS-17, CGI-I, ShARS, STAI, BSS, LSEQ. The study included 310 patients of whom 294 completed the program. Agomelatine demonstrated high efficiency (90% remission + response) patients the presence of anxiety symptoms in the structure of major depression. Regression shows the features of the individual components of anxious depression.
Key words: agomelatine, anxiety, depression.
Тревожные симптомы – одни из самых распространенных феноменов в структуре депрессивного расстройства [57], а синдром тревожной депрессии в клинике аффективной патологии занимает особое место [12]. Известно, что включение тревоги приводит к утяжелению депрессивного состояния, более длительному течению заболевания, более значимым нарушениям социальной адаптации пациентов и повышению суицидального риска [57, 23]. Кроме того, тревожные симптомы в структуре большого депрессивного расстройства (БДР) ассоциируются с низким уровнем ответа на антидепрессивную терапию и возрастанием риска обострений [21, 22, 54, 57].
К настоящему моменту накоплен большой клинический опыт применения агомелатина (Вальдоксана) при лечении депрессивных расстройств разной степени тяжести. Его эффективность была подтверждена в масштабных международных исследованиях и в Российских наблюдательных программах при лечении больных с БДР униполярного и биполярного течения (биполярное аффективное расстройство типа II – БАР), в том числе при тяжелой депрессии [5–9, 45].
Вместе с тем в серии доклинических исследований на животных [43, 50] выявлен анксиолитический эффект Вальдоксана, механизм которого связывается с особенностями рецепторного аффинитета препарата. Противоречия в оценках исследователей касаются лишь роли рецепторов определенного типа в патогенезе тревожных проявлений при депрессии и реализации фармакологического эффекта агомелатина. Одни авторы, отдавая первенство серотониновым 5НТ2С-рецепторам [29], приводят следующие доказательства: мыши с генетически отсутствующими 5НТ2С-рецепторами демонстрировали редукцию тревоги [18]; в разных исследованиях 5НТ2С-агонисты и антагонисты выявляют, соответственно, анксиогенный и анксиолитический эффекты [17, 19, 26, 33, 34, 42, 44]; антидепрессанты, механизм действия которых связан с антагонизмом к 5НТ2С-рецепторам (Вальдоксан, миртазапин, миансерин), проявляют анксиолитическую активность – как на моделях животных, так и у человека [16, 42, 53]; 1-кратное введение селективных ингибиторов обратного захвата серотонина вызывает у грызунов тревогу посредством косвенной активации 5НТ2С-рецепторов, тогда как их длительный прием уменьшает тревожность вслед за снижением регуляции этих же рецепторов [15, 20], что предполагает их клиническую пользу в долгосрочной терапии тревожных состояний [40].
Другие авторы анксиолитический потенциал агомелатина обосновывают его агонизмом по отношению к мелатониновым рецепторам, в доказательство чего приводят данные о роли мелатонина в патогенезе тревожных расстройств: участие эпифиза в антистрессорной защите организма [4, 14] посредством усиления выработки мелатонина в ответ на разнообразные стрессовые и анксиогенные стимулы [25, 40]; роль мелатонина в хронобиологической регуляции, с учетом патогенетической связи между развитием тревоги и дезорганизацией биологических ритмов [2].
Кроме того, мелатонин проявляет анксиолитические особенности в экспериментах на грызунах [25, 27, 35–37, 47, 48, 51], снижает тревожность у пациентов, готовящихся к хирургической операции [46]. Анксиолитические свойства мелатонина изучались и рядом отечественных авторов [2, 10]. На модели конфликтной ситуации у крыс выявлено сходство противотревожной активности мелатонина с бензодиазепинами (диазепамом, тофизопамом) и b-адреноблокатором (пропранолол) [2]. Наряду с этим применение мелатонина у психически здоровых молодых добровольцев приводило к снижению реактивной тревожности, причем в большей степени у лиц с изначально высокими ее значениями [1, 10].
Небезуспешными оказались попытки объяснить анксиолитический эффект Вальдоксана действием на обе рецепторные системы – мелатонинергическую и серотонинергическую. В серии экспериментов на валидизированных моделях тревоги у грызунов была показана более выраженная эффективность препарата по сравнению с монорецепторными агентами (антагонистами 5НТ2С- и агонистами МT1/MT2-рецепторов) [47].
Число клинических исследований, посвященных влиянию Вальдоксана на тревожную симптоматику, невелико. Имеются данные рандомизированного двойного слепого плацебо-контролируемого исследования с целью изучения эффективности препарата при генерализованном тревожном расстройстве (ГТР) [56]. Результатом терапии 121 пациента с диагнозом ГТР в течение 12 нед явилось превосходство агомелатина по эффективности над плацебо, тогда как по уровню побочных эффектов группы были сопоставимы. Полученные данные были подтверждены в другом исследовании, посвященном эффективности и переносимости агомелатина в предотвращении рецидива у пациентов с ГТР [55].
В течение 6 мес наблюдения число пациентов с рецидивом на терапии агомелатином (22 пациента; 19,5%) было почти в 2 раза меньше, чем в группе плацебо (35 пациентов; 30,7%). Агомелатин также превосходил плацебо в предотвращении рецидивов в подгруппе более тяжелых пациентов (HARS≥25 и CGI-S≥5). Представление об анксиолитической активности Вальдоксана дают также результаты метаанализа 6 многоцентровых двойных слепых рандомизированных исследований (3 плацебо-контролируемых и 3 – с препаратом сравнения: флуоксетином, сертралином и венлафаксином), в которых использовались шкалы HARS и HDRS-17. Вальдоксан превосходил по эффективности как плацебо, так и препараты сравнения по действию на депрессивную и тревожную симптоматику [58].
Имеющиеся в литературе экспериментальные и клинико-фармакологические данные о положительном воздействии Вальдоксана на симптомы тревоги предопределили цель проведения настоящей натуралистической программы – получение данных о терапевтической эффективности и переносимости препарата Вальдоксан (агомелатин) при лечении пациентов с тревожной депрессией в рамках БДР. Дополнительными целями являлись: 1) оценка влияния Вальдоксана на уровень соматической и психической тревоги, 2) оценка влияния Вальдоксана на уровень реактивной тревоги (РТ) и личностной тревоги (ЛТ), 3) выявление зависимости эффективности Вальдоксана от степени редукции тревоги (шкала Шихана) и инсомнии (LEEDS), 4) оценка динамики суицидальных тенденций в процессе терапии.
Материалы и методы
Исследование проводилось в период с 01.02.2012 г. (дата включения 1-го пациента) по 30.06.2012 г. (дата завершения исследования последним пациентом) при участии
9 клинических центров, расположенных в разных регионах РФ:
1. Москва – профессор А.С.Аведисова (ГНЦССП им. В.П.Сербского, руководитель проекта).
2. Москва – академик РАМН А.Б.Смулевич (НЦПЗ РАМН).
3. Санкт-Петербург – профессор Н.Г.Незнанов (НИПНИ им. В.М.Бехтерева).
4. Нижний Новгород – профессор Л.Н.Касимова (Ниж-ГМА).
5. Ставрополь – кандидат психологических наук Г.П.Былим (СГМУ).
6. Красноярск – В.В.Монастырская (заместитель главного врача ККПНД).
7. Томск – доктор медицинских наук Е.Д.Счастный (НИИ психического здоровья СО РАМН).
8. Иркутск – профессор А.С.Бобров (ИГМАПО).
9. Иркутск – профессор В.С.Собенников (ИГМУ).
По своему дизайну проведенное исследование являлось обсервационным, общей продолжительностью 8 нед
(56 дней). В него включались пациенты обоего пола в возрасте от 18 до 65 лет, находящиеся в психиатрическом стационаре или на амбулаторном лечении с диагнозами по Международной классификации болезней 10-го пересмотра (МКБ-10): «Депрессивный эпизод умеренный (F32.1) или тяжелый (F32.2) без психотических симптомов», «Рекуррентное депрессивное расстройство; умеренный (F33.1) или тяжелый (F33.2) депрессивный эпизод без психотических симптомов»; с суммой баллов по шкале HDRS-17 не менее 17, по шкале самооценки тревоги Шихана – не менее 30; имеющие показания для назначения Вальдоксана или в качестве первого антидепрессанта (стандартные показания для терапии антидепрессантами), или в качестве замены предыдущего антидепрессанта в случае его плохой переносимости и/или неудовлетворительной эффективности. Для женщин с сохранной детородной функцией дополнительным условием было применение адекватных медицинских средств контрацепции (гормональная контрацепция, внутриматочная спираль, двойной барьерный метод – презерватив в сочетании со спермицидом). Все пациенты должны были дать письменное информированное согласие на участие в обсервационной программе.
Критерии исключения: наличие суицидального риска (более 2 баллов по пункту 3 шкалы HDRS-17 и/или по клинической оценке исследователя); наличие психотических симптомов (по клинической оценке лечащего врача); резистентность к терапии другими антидепрессантами; шизофрения, шизоаффективное расстройство, органическое поражение центральной нервной системы, деменция, эпилепсия, рассеянный склероз, паркинсонизм, болезнь Альцгеймера, черепно-мозговая травма и ее последствия, биполярное аффективное расстройство; алкоголизм или наркомания в анамнезе; тяжелые или декомпенсированные соматические или неврологические заболевания; печеночная недостаточность; одновременное применение сильных ингибиторов цитохрома CYP1A2 (ципро-флоксацин); беременность или кормление грудью; установленная ранее индивидуальная непереносимость либо неэффективность Вальдоксана в анамнезе при назначении препарата в адекватной дозе (не менее 25 мг/сут) и длительности (не менее 4 нед).
Критерии преждевременного выбывания пациента из исследования: отказ пациента; появление психотических симптомов, суицидального риска или симптомов мании; развитие нежелательных явлений (НЯ) или реакций, препятствующих дальнейшему проведению терапии; нарушение функции печени (повышение аспартатаминотрансферазы, аланинаминотрансферазы или щелочной фосфатазы более чем в 3 раза относительно верхней границы нормы, или повышение общего билирубина более чем в 2 раза относительно верхней границы нормы, или развитие желтухи); возникновение сопутствующих соматических заболеваний/симптомов или обострение хронических заболеваний, не связанных с приемом Вальдоксана; необходимость приема сильных ингибиторов цитохрома CYP1A2 (ципрофлоксацин); несоблюдение режима терапии или беременность.
Вальдоксан назначался в стартовой терапевтической дозе 25 мг (1 таблетка) в соответствии с инструкцией по медицинскому применению. В случае недостаточного, по мнению исследователя, эффекта препарата его доза могла быть повышена до 50 мг (2 таблетки) 1-кратно вечером. Доза 50 мг являлась максимально допустимой.
В ходе 8-недельного периода наблюдения было предусмотрено 7 визитов: визит 1 – фон, визит 2 – на 3-й день терапии, визит 3 – на 7-й день, визит 4 – на 14-й день, визит 5 – на 28-й день, визит 6 – на 42-й день, визит 7 – на
56-й день терапии. Клинические данные регистрировались в индивидуальной регистрационной карте (ИРК).
Помимо психопатологического и общесоматического обследования (включая артериальное давление, частоту сердечных сокращений, биохимический анализ крови, измерение массы тела) в рамках данного исследования использовались следующие шкалы: HDRS-17 (шкала депрессии Гамильтона), CGI-I (шкала общего клинического впечатления для оценки улучшения состояния), шкала самооценки тревоги Шихана (ShARS), шкала самооценки уровня тревожности Спилберга–Ханина (STAI), шкала суицидальных мыслей Бека (BSS), шкала оценки показателей сна (LSEQ); табл. 1.

Для оценки эффективности терапии Вальдоксаном были использованы следующие критерии: динамика баллов HDRS-17 на фоне терапии, частота формирования ремиссии, процент респондеров, динамика баллов по ShARS, влияние терапии на оценки РТ и ЛТ (STAI), динамика баллов по BSS, изменение параметров опросника LSEQ на фоне терапии, оценка динамики психического состояния по шкале CGI-I. В конце исследования врачами и пациентами заполнялся краткий опросник, предлагающий оценить эффективность лечения.
Всего в исследование были включены 310 пациентов, социодемографические характеристики которых отображены в табл. 2. Большинство из них женщины – 81,61%; мужчин лишь 18,39%. Средний возраст обследованных 42,5±12,9 года, что указывает на принадлежность изучаемого контингента к наиболее активной в социальном плане части населения. О том же свидетельствует и уровень образования: 58,71% обследованных имели высшее образование, а 5,16 и 21,61% – неоконченное высшее и среднее специальное соответственно, что в совокупности составило 85,48%. Среднее образование получили 10,65% больных, неполное среднее – 0,32%. В 11 (3,55%) случаях данные по уровню образования отсутствовали. Профессионально занятыми среди изученного контингента являлись 67,42% больных, на пенсии – 15,16%, учились – 4,19%, домохозяйки – 7,74% пациентов. Только 4,84% являлись безработными, 1,29% – имели инвалидность по соматическому заболеванию, а 0,65% – по психическому. Более 1/5 (53,55%) больных состояли в браке, 18,39% – одинокие, 16,45% – разведены, 8,06% – вдовы. В остальных случаях (11 человек; 3,55%) эти данные отсутствовали.

С целью выявления смещения социодемографических показателей исследуемой выборки пациентов с тревожной депрессией от средних в населении РФ и в выборке пациентов с депрессией проводилось сопоставление данных, характеризующих пол, возраст, уровень образования и др. с итогами Всероссийской переписи населения 2010 г. (ВПН-2010), а также с больными, участвующими в обсервационной программе (РИТМ) по изучению эффективности Вальдоксана при депрессивном эпизоде без явлений тревоги [13]. В целом это сравнение обозначило существенное отклонение социодемографических показателей пациентов с депрессией и тревожной депрессией от популяции жителей РФ.
Так, среди пациентов с тревожной депрессией и депрессивным эпизодом значительно преобладали женщины (81,6% и 77% против 53,8% соответственно). Средний возраст жителей РФ составлял 38 лет, тогда как этот показатель для пациентов с тревожной депрессией и с депрессией был выше (42,5±12,9 и 44,4±12,2 соответственно). Для группы ДЖАЗ был характерен высокий процент лиц с высшим образованием – 58,7% (26,4% – ВПН-2010), разведенных – 16,5% (10% – ВПН-2010) при примерно одинаковых характеристиках профессиональной занятости.
С клинической точки зрения, у большинства пациентов диагностировался единичный депрессивный эпизод (63,22%), а у 32,26% больных депрессивные проявления возникали в рамках рекуррентного депрессивного расстройства. При этом средняя степень выраженности депрессии (диагнозы F32.1 и F33.1 по МКБ-10) до начала терапии отмечалась у 84,1% пациентов, тогда как тяжелая степень – у 11,29%. У 4,52% включенных пациентов диагноз указан не был. Средний балл по HDRS-17 на момент включения составил 23,9±4,6 балла, по шкале самооценки тревоги Шихана – 82,5±21,0 балла (тяжелая тревога). Уровень реактивной тревоги, оцениваемый по шкале самооценки Спилберга–Ханина, составлял 59,2±8,6 балла, для ЛТ – 57,2±9,5 балла (табл. 3), что соответствовало высокому уровню тревожности. Большая часть (88,39%) больных, включенных в исследование, не имели суицидальных мыслей или тенденций, тогда как у 11% пациентов баллы по шкале BSS составляли от 1 до 12.

Для выявления вклада отчетливой тревожной симптоматики в клиническую характеристику пациентов с тревожной депрессией было проведено сравнение исследуемой выборки с данными обсервационного исследования РИТМ. Выявлено, что у пациентов с тревожной депрессией в 2 раза (63,2%) чаще диагностировался единичный депрессивный эпизод и в 2 раза (32,2%) реже – рекуррентное депрессивное расстройство по сравнению с группой лиц, принимавших участие в исследовании РИТМ (28,3 и 71,6% соответственно). Депрессии в 2 группах были представлены преимущественно депрессиями средней степени выраженности (84 и 79% соответственно) и существенно меньшим числом больных с тяжелым эпизодом (11 и 20% соответственно). Средний суммарный балл по шкале HDRS-17 не различался между 2 сравниваемыми группами.
Более 1/2 (57,48%) больных, принявших участие в исследовании, получали терапию в психиатрических больницах (как амбулаторно, так и стационарно). 23,13% проходили курс лечения в поликлинике, 13,27% – в консультативно-диагностическом центре. Для 34 (11,56%) больных такие данные отсутствовали. Таким образом, большая часть (82,58%) пациентов находились на амбулаторном режиме лечения, и только 12,26% человек наблюдались стационарно.
При этом 256 (82,58%) больных получали Вальдоксан в качестве первого антидепрессанта для лечения текущего депрессивного эпизода, 33 (10,65%) пациента – как замену предыдущего антидепрессанта, причем у 23 (7,42%) пациентов назначаемый ранее препарат был неудовлетворительным по эффективности, а у 10 (3,23%) – по переносимости. В 6,77% (21 пациент) случаев эти данные отсутствовали. Заменяемым оказался широкий спектр в основном современных антидепрессантов: пароксетин (2,26%), сертралин (1,61%), амитриптилин (1,29%), флуоксетин (0,97%), венлафаксин (0,65%), флувоксамин (0,65%), азафен (0,65%), мапротилин (людиомил) (0,32%), дулоксетин (0,32%), эсциталопрам (0,32%). Для 5 (1,61%) человек принимаемый ранее антидепрессант был неизвестен.
В течение последнего года до включения в исследование 38,71% (120 человек) получали терапию всеми классами психотропных средств и фитотерапией: 19,68% – препаратами растительного происхождения, 16,45% – транквилизаторами, 15,16% – антидепрессантами, 4,84% – нейролептиками, 0,65% – антиконвульсантами.
Из всех включенных в исследование 310 пациентов (ВП) полностью завершили программу (ПЗП) 294 (94,8%) человека, что свидетельствует о высоком уровне комплаентности. Только 16 (5,16%) больных по разным причинам преждевременно выбыли (ПВ) из исследования. Сравнительный анализ 3 групп пациентов (ВП, ПВ и ПЗП) показал сопоставимость выборок по социодемографическим и некоторым клиническим показателям (средний балл по шкалам HDRS-17, Шихана, Спилберга–Ханина). В то же время сравнение выборок ПВ и ПЗП показало преобладание в группе ПВ лиц с рекуррентным депрессивным расстройством (p=0,035), получавших в последний год нейролептики (p=0,0077), страдающих сахарным диабетом (p=0,000045), а также пациентов, которым Вальдоксан назначен в качестве замены предыдущего антидепрессанта (p=0,00001). Показатель суицидальности (BSS) был достоверно выше в группе ПВ (p<0,00001).
Если основными причинами преждевременного выбывания у пациентов с тревожной депрессией являлись отказ пациента (50%), необходимость приема других психотропных препаратов (31,2%) и несоблюдение режима терапии (12,5%), то у пациентов с депрессивным эпизодом без явлений тревоги (РИТМ) причины преждевременного отказа располагались в следующем порядке: неэффективность лечения (19,4%), наличие НЯ и неуточненный отказ пациента (по 17,9%); табл. 4. Следует обратить внимание на высокий процент выбывания по причине инверсии аффекта в группе с тревожной депрессией (6,3%) по сравнению с депрессией без явлений тревоги (1,4%), что соответствует представлению некоторых авторов об ассоциированности тревожной депрессии с биполярным спектром [31, 52].

Далее в статье будут рассмотрены только пациенты, полностью завершившие исследование согласно протоколу (294 человека; 94,8%).
В ходе терапии 181 (61,56%) больному Вальдоксан назначался в дозе 25 мг/сут в течение всего периода лечения, 113 (38,44%) – доза препарата была повышена до 50 мг/сут. Последний показатель несколько превосходит таковой в программе РИТМ (27,4%), что свидетельствует о необходимости более частого повышения дозировки препарата при тревожной депрессии. Чаще всего увеличение дозы происходило на 4-м визите терапии (21,43%), реже – на 5-м (13,27%) и для некоторых больных – на 6 (1,02%) и 3-м (0,68%) визитах. В качестве сопутствующей анксиолитической терапии (43 человека; 14,62%) назначался диазепам (6,12%), феназепам (3,06%), гидроксизин (2,38%), медазепам (2,04%), оксазепам (0,34%). Несмотря на то что алпразолам и депакин хроно были запрещены протоколом, их получали 2 пациента (по 0,34%).
Общая эффективность терапии Вальдоксаном
при тревожной депрессии в рамках БДР
 В целом если до лечения средний балл по HDRS-17 составлял 23,9±4,6, то в конце – лишь 6,1±3,6, т.е. его редукция к моменту окончания исследования достигала 74,47%, что свидетельствует о достаточно высоком уровне антидепрессивной активности исследуемого препарата. Сравнение общей эффективности терапии Вальдоксаном в 2 обсервационных программах показало, что у пациентов с тревожной депрессией (ДЖАЗ) процент ремиттеров был выше (69% vs 41,7%), в то время как количество респондеров (21%) и нонреспондеров (9,8%) было ниже аналогичных показателей у пациентов с депрессией без признаков тревоги – РИТМ (37 и 21% соответственно), что, возможно, объясняется меньшим процентом лиц с депрессией тяжелой степени в данной наблюдательной программе.
В целом если до лечения средний балл по HDRS-17 составлял 23,9±4,6, то в конце – лишь 6,1±3,6, т.е. его редукция к моменту окончания исследования достигала 74,47%, что свидетельствует о достаточно высоком уровне антидепрессивной активности исследуемого препарата. Сравнение общей эффективности терапии Вальдоксаном в 2 обсервационных программах показало, что у пациентов с тревожной депрессией (ДЖАЗ) процент ремиттеров был выше (69% vs 41,7%), в то время как количество респондеров (21%) и нонреспондеров (9,8%) было ниже аналогичных показателей у пациентов с депрессией без признаков тревоги – РИТМ (37 и 21% соответственно), что, возможно, объясняется меньшим процентом лиц с депрессией тяжелой степени в данной наблюдательной программе.
Оценка степени улучшения состояния пациентов по шкале CGI-I характеризовалась сходными с предыдущей оценкой процентами: на 7-м визите (56-й день терапии) только у 2 (0,68%) пациентов состояние оставалось без изменений, у 16 (5,44%) больных отмечалось незначительное улучшение, у 87 (29,59%) – существенное улучшение и у 189 (64,29%) – выраженное улучшение.
Помимо редукции депрессивной симптоматики была показана высокая эффективность Вальдоксана в отношении тревожных проявлений. Объективная оценка заключалась в исследовании подпунктов HDRS-17 «психическая» и «соматическая тревога». Уровень «психической тревоги» с высокой статистической достоверностью (p<0,00001) снижался уже после первых 3 дней терапии, аналогичная тенденция отмечалась и в отношении «соматической» тревоги (p<0,00001); рис. 2.

Динамика баллов по ShARS также показала статистически значимую редукцию по сравнению с фоном уже на 3-й день терапии. Высокий темп редукции сохранялся до 7-го визита исследования. Фоновый балл по шкале снижался с 81,3±20,9 (тяжелая тревога) до 44,7±10,3 (тревога средней выраженности) на последнем визите. Менее отчетливые результаты были получены в отношении РТ и ЛТ, оцениваемых по STAI. Средний балл до начала терапии составил 59,2±8,7 для РТ и 57,1±9,5 для ЛТ, что соответствует очень высокому уровню тревожности (более 46 баллов). В конце исследования баллы снизились до 39,1±10,4 и 41,7±10,2 соответственно, что отвечает критериям тревожности среднего уровня. Статистически значимые отличия по сравнению с фоновыми показателями наблюдались, начиная с 3-го дня терапии (рис. 3).
Клиническая оценка суицидальной активности (BSS) больных в фоновом исследовании показала наличие легко выраженной суицидальности у 33 (12,6%) пациентов, которая оценивалась у 16 (5,16%) человек в 1 балл, у 12 (4%) – от 2 до 6 баллов и у 5 (1,7%) – от 7 до 12 баллов. При этом у 3 больных имелись суицидальные попытки в анамнезе. Уже на 3-й день терапии Вальдоксаном суицидальные проявления практически нивелировались, а на 7-м визите исследования только у 4 пациентов сохранялись суицидальные переживания, относящиеся только к 1-му пункту шкалы (пациенты отмечали, что они в слабой степени хотят жить, но не отмечали, что не хотят жить); рис. 4.
Все остальные 18 пунктов достигали нуля. По HDRS-17 наблюдалась сходная, но более растянутая по времени динамика редукции показателя «суицидальность». Статистически достоверная редукция данного пункта отмечалась уже после первых 3 дней терапии (р=0,023), а на 3-м визите (7-й день терапии) фиксировалась практически 2-кратная степень редукции. Причем к окончанию исследования пациенты с наличием суицидальных мыслей отсутствовали (рис. 5). Различие в результатах, оцениваемых «суицидальность» по двум шкалам, вероятно, связано с более дифференцированной оценкой этого явления при помощи BSS.
С целью выявления связи между показателями суицидальности (BSS) и такими параметрами, как заторможенность, ажитация и депрессивное настроение, оцениваемыми по HDRS-17, был проведен корреляционный анализ. Результаты статистической обработки полученных результатов выявили, что сумма баллов по BSS коррелировала с тяжестью п. 1 шкалы HDRS-17 (депрессивное настроение; k=0,2263), но не была связана с пп. 8 («заторможенность») и 9 («ажитация»).
Шкала LSEQ позволила комплексно изучить изменения в процессе терапии Вальдоксаном таких характеристик сна, как «засыпание», «качество сна», «пробуждение», «состояние после сна». Качество засыпания постепенно улучшалось от визита к визиту и к моменту окончания исследования у большинства пациентов достигало доболезненного уровня (р≤0,00001). Качество сна также плавно нормализовалось в процессе лечения: пациенты отмечали, что сон становился более спокойным, уменьшалась частота ночных пробуждений (р≤0,00001). Параметр «пробуждение» оценивался по таким критериям, как легкость и быстрота. Эта составляющая ночного сна нормализовалась более медленно по сравнению с двумя предыдущими характеристиками, тем не менее достигала удовлетворительного уровня к окончанию терапии (р≤0,00001). Состояние после сна оценивалось пациентами на основании самочувствия после пробуждения, по готовности к немедленным действиям, а также по координации движений. В процессе лечения отмечалось статистически достоверное улучшение этого показателя (р≤0,00001); рис. 6.

С целью подтверждения предположения о быстроте редукции определенной симптоматики при терапии Вальдоксаном был проведен анализ степени и времени обратного развития тревожной депрессии. При этом сопоставлялась выраженность редукции различных показателей шкал в течение 2 периодов терапии: первые 2 нед и последующие 6 нед. Также оценивались показатели общей редукции всех изучаемых показателей на всем протяжении лечения (табл. 5). Как и предполагалось, процесс обратного развития тревожной депрессии наблюдался преимущественно в первые 2 нед терапии, что подтверждалось значительной редукцией большинства показателей в эти сроки. Особо быстрое снижение баллов в первые 2 нед лечения наблюдалось при оценке суицидальности (на 91% по BSS и 68% по HDRS-17 п. 3). Показатели генерализованной тревоги (ShARS) в большей степени снижались в первые 2 нед (на 27%), чем в последующие 6 нед (на 18%) исследования. Остальные показатели за 2 нед терапии редуцировались практически с той же скоростью, как и за последующие 6 нед (HDRS-17, HDRS-17 пп. 10 и 11), но при этом на первые недели лечения приходилось 50% и более всей отмеченной обратной динамики.
Через 2 нед терапии Вальдоксаном процесс обратного развития симптоматики замедлялся, но показатели таких шкал, как HDRS-17 п. 1 и LSEQ, на этом этапе редуцировались несколько в большей степени. Тревожность как личностная особенность (STAI) подвергалась наименьшей динамике в процессе терапии с примерно равным распределением в 1 и 2-й ее период.

По результатам опросника, оценивающего удовлетворенность терапией врачей и пациентов, было выявлено, что около 1/2 (47,96%) врачей оценили эффективность лечения Вальдоксаном как «отличную», 43,8% – как «хорошую», и только 6,4% считали эффективность «удовлетворительной» и 1,3% – «плохой» (0,3% – данные отсутствуют). 87,4% врачей рекомендовали своим пациентам продолжать терапию этим препаратом. Мнение пациентов было сходным. Так, 42,5% больных оценили эффективность лечения как «отличную», 48,9% – как «хорошую», 6,1% – как «удовлетворительную» и 2,0% – как «плохую» (0,3% – данные отсутствуют); рис. 7. При этом 84% пациентов выразили желание продолжить терапию Вальдоксаном и только 15,6% отказались от продолжения лечения.

Выводы
- Полученные данные свидетельствуют о высокой эффективности Вальдоксана (90% ремиссия + респонс) при терапии пациентов с тревожной депрессией, что сопоставимо с результатами некоторых других исследований по оценке его эффективности при депрессии без явлений тревоги. Высокую и хорошую степень эффективности терапии препаратом отметили также более 90% врачей и пациентов.
- В процессе терапии тревожная симптоматика нивелировалась с выраженного уровня до среднего, при этом генерализованная тревога редуцировалась в большей степени, чем реактивная и ЛТ, а уровень РТ снижался значительнее, чем ЛТ. Косвенно противотревожный эффект Вальдоксана подтверждается тем фактом, что в дополнительной анксиолитической терапии нуждались только 14,6% пациентов.
- В процессе терапии отмечалось гармоничное снижение всех показателей, характеризующих качество сна.
- На 3-й день терапии Вальдоксаном выявлена статистически значимая редукция практически всех изучаемых параметров, что свидетельствует о быстроте наступления как антидепрессивного, так и анксиолитического действия препарата.
- В процессе терапии Вальдоксаном отмечалась неравномерная динамика симптоматики тревожной депрессии. Первый тип динамики, при котором скорость редукции показателей в первые 2 нед терапии значительно превосходила таковую в последующие 6 нед, относился к генерализованной тревоге и суицидальности. Второй тип динамики, при котором скорость редукции показателей тревожной депрессии в первые 2 нед терапии практически соответствовала таковой в последующие 6 нед, относилась к общим баллам HDRS-17, соматической и психической тревоге, ЛТ и РТ. Третий тип динамики, при котором основная обратная динамика наблюдалась в основном на более поздних сроках терапии (с 3 по 8-ю неделю), ассоциирован с депрессивным настроением (HDRS-17 п. 1) и инсомнией (LSEQ).
Сведения об авторах
А.С.Аведисова – проф., руководитель отд. терапии психических и поведенческих расстройств ФГБУ ГНЦССП им. В.П.Сербского Минздрава России. E-mail: Alla.Avedisova@gmail.com
К.В.Захарова – канд. мед. наук, ст. науч. сотр. отд. терапии психических и поведенческих расстройств ФГБУ ГНЦССП
им. В.П.Сербского Минздрава России. E-mail: ksushkaa@bk.ru
М.П.Марачев – канд. мед. наук, науч. сотр. отд. терапии психических и поведенческих расстройств ФГБУ ГНЦССП
им. В.П.Сербского Минздрава России. E-mail: marachevm@gmail.com
Список исп. литературыСкрыть список1. Арушанян Э.Б., Байда (Мастягина) О.А., Мастягин С.С. Эксперим. и клин. фармакология. 2006; 69 (1): 21–3.
2. Арушанян Э.Б. Изучение психотропной активности гормона эпифиза мелатонина – оригинальное направление наших исследований. Эксперим. и клин. фармакология. 2007; 70 (6): 55–60.
3. Арушанян Э.Б., Бейер Э.В. Журн. высшей нервной деятельности. 1998; 48 (6): 1065–71.
4. Арушанян Э.Б. Успехи физиол. наук. 1996; 27 (3): 31–50.
5. Бобров А.С., Петрунько О.В., Хамарханова А.А., Швецова А.В. Клинические предикторы реакции на терапию Вальдоксаном при умеренной и тяжелой депрессии. Журн. неврол. и психиатр. 2010; 110 (9): 14.
6. Иванов С.В. Вальдоксан (агомелатин) при терапии умеренных и тяжелых депрессий непсихотического уровня в амбулаторной и госпитальной практике (результаты Российского многоцентрового исследования ХРОНОС). Психиатр. и психофармакотер. 2009; 6: 14–7.
7. Иванов С.В. Вальдоксан в терапии биполярной депрессии: результаты российского многоцентрового натуралистического исследования ХРОНОС. Обозрен. психиатрии и мед. психологии им. Бехтерева. 2011; 2.
8. Марачев М.П. Эффективность агомелатина при терапии атипичной депрессии. Журн. психиатр. и психофармакотер. 2012; 3: 25–30.
9. Мосолов С.Н. Эффективность и переносимость агомелатина при депрессивных состояниях в рамках рекуррентной депрессии и биполярного расстройства: доклад. Вторая Франко-Российская встреча. Париж, 2011.
10. Ованесов К.Б., Ованесова И.М., Арушанян Э.Б. Эксперим. и клин. фармакология. 2006; 69 (6): 17–9.
11. Результаты Всероссийской переписи населения 2010. http://www.perepis-2010.ru
12. Смулевич А.Б., Дубницкая Э.Б. Тревожные депрессии. Мед. газета. 2004; 2.
13. Смулевич А.Б., Андрющенко А.В., Бескова Д.А. Терапия непсихотических депрессий антидепрессантом агомелатином (Вальдоксан): результаты наблюдательного многоцентрового исследования РИТМ. Психиатр. и психофармакотер. 2010; 4: 4–11.
14. Borjigin J, Li X, Snyder SH. The pineal gland and melatonin: molecular and pharmacologic regulation. Ann Rev Pharmacol Toxicol 1999; 39: 53–65.
15. Bristow LJ, O’Connor D, Watts R et al. Evidence for accelerated desensitisation of 5HT2C-receptors following combined treatment with fluoxetine and the 5HT1A-receptor antagonist. WAY100, 635 in the rat. Neuropharmacol 2000; 39: 1222–36.
16. Casacalenda N, Boulenger JP. Pharmacologic treatment effective in both generalized anxiety disorder and major depressive disorder: clinical and theoretical implications. Can J Psychiat 1998; 43: 722–30.
17. Cervo L, Samanin R. 5HT1A-receptor full and partial agonists and 5HT1C (but not 5-HT3) receptor antagonists increase rates of punished responding in rats. Pharmacol Biochem Behav 1995; 52: 671–6.
18. Das S, Tecott L. Diminished anxiety-like responses in 5HT2C-receptor mutant mice. Soc Neurosci Abstr 1996; 22: 811–2.
19. Dekeyne A, Brocco M, Adhumeau A et al. The selective serotonin 5HT1A-receptor ligand, S15535, displays anxiolytic-like effects in the social interaction and Vogel models and suppresses dialy sate levels of 5-HT in the dorsal hippocampus of freely-moving rats: a comparison with other anxiolytic agents. Psychopharmacol 2000; 152: 55–66.
20. Dekeyne A, Denorme B, Monneyron S, Millan MJ. Citalopram reduces social interaction in rats by activation of serotonin (5-HT)2 Creceptors. Neuropharmacol 2000; 39: 1114–7.
21. Fava M, Rush AJ, Alpert JE et al. Difference in treatment outcome in outpatients with anxious vs nonanxious depression: a STAR*D report. Am J Psychiat 2008; 165: 342–51.
22. Fava M, Rush AJ, Alpert JE et al. What clinical and symptom features and comorbid disorders characterize outpatients with anxious major depressive disorder: a replication and extension. Can J Psychiat 2006; 51: 823–35.
23. Fawcett J, Barkin RL. A meta-analysis of eight randomized, double-blind, controlled clinical trials of mirtazapine for the treatment of patients with major depression and symptoms of anxiety. Int Clin Psychopharmacol 2003; 18: 203–10.
24. Golombek DA, Martini M, Cardinali DP. Melatonin as an anxiolytic in rats: time dependence and interaction with the central GABAergic system. Eur J Pharmacol 1993; 237: 231–6.
25. Golombek DA, Pevet P, Cardinali DP. Melatonin effects on behavior: possible mediation by the central GABAergic system. Neurosci Biobehav Res 1996; 20: 403–12.
26. Griebel G, Perrault G, Sanger DJ. A comparative study of the effects of selective and non-selective 5HT2-receptor subtype antagonists in rat and mouse models of anxiety. Neuropharmacol 1997; 36: 793–802.
27. Guardiola-Lemaitre B, Lenegre A, Porsolt RD. Combined effects of diazepam and melatonin in two tests for anxiolytic activity in the mouse. Pharmacol Biochem Behav 1992; 41: 405.
28. Hale A, Corral RM, Mencacci C et al. Superior antidepressant efficacy results of agomelatine vs fluoxetine in severe MDD patients: a randomized, double-blind study. Int Clin Psychopharmacol 2010; 25: 305–14.
29. Heisler LK, Zhou L, Bajwa P et al. Serotonin 5-HT2C-receptors regulate anxiety-like behavior. Gen Brain Behav 2007; 6 (5): 491–6.
30. Kasper S, Hajak G, Wulff K et al. Efficacy of the novel antidepressant agomelatine on the circadian rest-activity cycle and depressive and anxiety symptoms in patients with major depressive disorder: a randomized, double-blind comparison with Sertraline. J Clin Psychiat 2010; 71: 109–20.
31. Katzow JJ, Hsu DJ, Ghaemi SN. The bipolar spectrum: a clinical perspective. Bipolar Disord Vol 2003; 5 (6): 436–42.
32. Kennedy SH, Emsley R. Placebo-controlled trial of agomelatine in the treatments of major depressive disorder. Eur Neuropsychopharmacol 2006; 16: 93–100.
33. Kennett GA, Wood MD, Bright F et al. In vitro and in vivo profile of SB 206553, a potent 5HT2C/5-HT2B-receptor antagonist with anxiolytic-like properties. Br J Pharmacol 1996; 117: 427–34.
34. Kennett GA, Wood MD, Bright F et al. SB 242084, a selective and brain penetrant 5-HT2C-receptor antagonist. Neuropharmacol 1997; 36: 609–20.
35. Kopp C, Vogel E, Rettori MC et al. Effects of melatonin on neophobic responses in different strains in mice. Pharmacol Biochem Behav 1999; 63: 521–6.
36. Kopp C, Vogel E, Rettori MC et al. Anxiolytic-like properties of melatonin receptor agonists in mice: involvement of MT1 and/or MT2-receptors in the regulation of emotional responsiveness. Neuropharmacol 2000; 39: 1865–71.
37. Kopp C, Vogel E, Rettori MC et al. Antagonistic effects of S22153, a new MT1- and MT2-receptor ligand, on the neophobia-reducing properties of melatonin in BALB/c mice. Pharmacol Biochem Behav 1999; 64: 131–6.
38. Lemoine P, Guilleminault C, Alvarez E. Improvement in subjective sleep in major depressive disorder with a novel antidepressant, agomelatine: randomized, double-blind comparison with venlafaxine.
J Clin Psychiat 2007; 68: 1723–32.
39. Loo H, Hale A, D’haenen H. Determination of the dose of agomelatine, a melatoninergic agonist and selective 5-HT2C antagonist, in the treatment of major depressive disorder: a placebo-controlled dose range study. Int Clin Psychopharmacol 2002; 17: 239–47.
40. Millan MJ. The neurobiology and control of anxious states. Prog Neurobiol 2003; 70: 53–244.
41. Millan MJ, Brocco M. The Vogel conflict test: procedural aspects,
g-aminobutyric acid, glutamate and monoamines. Eur J Pharmacol 2003; 463: 67–96.
42. Millan MJ, Brocco M, Gobert A et al. A Anxiolytic properties of the selective, non-peptidergic CRF1-antagonists, CP 154,526 and DMP695: a comparison to other classes of anxiolytic agent. Neuropsychopharmacol 2001; 25: 585–600.
43. Millan MJ, Brocco M, Gobert A, Dekeyne A. Anxiolytic properties of agomelatine, an antidepressant with melatoninergic and serotonergic properties: role of 5HT2C-receptor blockade. Psychopharmacol Berl 2005; 177 (4): 448–58.
44. Millan MJ, Gobert A, Lejeune F et al. The novel melatonin agonist, agomelatine (S20098), is an antagonist at 5-hydroxytryptamine 2C-receptors, blockade of which enhances the activity of front cortical dopaminergic and adrenergic pathways. J Pharmacol Exp Ther 2003; 306: 954–64.
45. Montgomery SA, Kasper S. Severe depression and antidepressants: focus on a pooled analysis of placebo-controlled studies on agomelatine. Int Clin Psychopharmacol 2007; 22 (5): 283–29.
46. Naguib M, Samarkandi AH. The comparative dose – response effects of melatonin and midazolam for premedication of adult patients: a double-blinded, placebo-controlled study. Anesth Analg 2000; 91: 473–9.
47. Nava F, Carta G. Melatonin reduces anxiety induced by lipopolysaccharide in the rat. Neurosci Lett 2001; 307: 57–60.
48. Niles L. Melatonin interaction with the benzodiazepine-GABA receptor complex in the CNS. Adv Exp Med Biol 1991; 294: 267–77.
49. Olie JP, Kasper S. Efficacy of agomelatine, a MT1/MT2-receptor agonist with 5HT2C-antagonistic properties, in major depressive disorder. Int J Neuropsychopharmacol 2007; 10: 661–73.
50. Papp M, Litwa E, Gruca P. Anxiolytic-like activity of agomelatine and melatonin in three animal models of anxiety. Behav Pharmacol 2006; 17 (1): 9–18.
51. Pierrefiche G, Zerbib R, Laborit H. Anxiolytic activity of melatonin in mice: involvement of benzodiazepine receptors. Res Commun Chem Pathol Pharmacol 1993; 82: 131–42.
52. Rihmer Z, Szadoczky E, Furedi J et al. Anxiety disorders comorbidity in bipolar I, bipolar II and unipolar major depression: results from a population-based study in Hungary. J Affect Dis 2001; 67 (1): 175–9.
53. Rocha B, Rigo M, Di Scala G et al. Chronicmianserin or eltoprazine treatment in rats: effects on the elevated plus-maze test and on limbic 5HT2C-receptor levels. Eur J Pharmacol 1994; 262: 125–31.
54. Schosser A, Serretti A, Souery D et al. European Group for the study of Resistant Depression (GSRD). Where have we gone so far: Review of clinical and genetic findings. Eur Neuropsychopharmacol 2012; 22 (7): 453–68.
55. Stein DJ, Ahokas AA, Alabrran C et al. Agomelatine prevents relapse in generalized anxiety disorder: a 6-month randomized, double-blind, placebo-controlled discontinuation study. J Clin Psychiat 2012; 73 (7): 1002–8.
56. Stein DJ, Ahokas AA, Bodinat C. Efficacy of agomelatine in generalized anxiety disorder: a randomized, double-blind, placebo-controlled study. J Clin Psychopharmacol 2008; 28: 561–6.
57. Stein DJ, Hollander E. Anxiety disorders comorbid with depression: social anxiety disorder, post-traumatic stress disorder, generalized anxiety disorder and obsessive-compulsive disorder. Martin Dunitz. London 2002.
58. Stein DJ, Picarel-Blanchot F, Kennedy SH. Efficacy of novel antidepressant agomelatine for anxiety symptoms in major depresson. Hum Psychopharmacol Clin Exp 2013; 28: 151–9.


