Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№06 2013
Оптимизация терапии негативных расстройств при шизофрении рацематом гопантеновой кислоты №06 2013
Номера страниц в выпуске:30-37
Для лечения различных форм и стадий шизофрении используются антипсихотические препараты (нейролептики). Эффективность этой группы лекарственных средств при купировании и профилактике продуктивной симптоматики подтверждается результатами многочисленных исследований разной степени доказательности.
Резюме. В ходе проведенного натуралистического сравнительного исследования установлено, что включение рацемата гопантеновой кислоты (Пантогам актив) в комплексную (наряду с атипичными антипсихотиками) длительную терапию шизофрении, протекающей с преобладанием негативных расстройств, статистически достоверно способствует уменьшению тяжести большинства синдромов первичных негативных расстройств, а также значимому уменьшению вероятности возникновения и выраженности вторичных негативных расстройств. Повышение эффективности и переносимости комбинированной терапии позволяет достичь достоверно более значимого улучшения качества жизни больных.
Ключевые слова: шизофрения, негативные расстройства, Пантогам актив.
Optimization of the treatment of negative symptoms in schizophrenia with hopantenic
acid racemate
V.E.Medvedev1, A.U.Israelyan1,2, E.V.Gushanskaya1,2, V.I.Frolova1
1Chair of Psychiatry, Psychotherapy and Psychosomatic pathology, People’s Friendship University of Russia
2Psychiatric Hospital №13, Moscow
Summary. The results of naturalistic comparative study show that hopantenic acid racemate (Pantogam active) in the complex therapy of schizophrenia with predominant negative symptoms (in addition to atypical antipsychotics) significantly reduces most of the primary negative symptoms. The probability of secondary negative symptoms manifestation and its intensity also decrease. Effectiveness and tolerability of combined therapy allow achieving statistically more significant quality of life improvement.
Key words: schizophrenia, negative symptoms, Pantogam active.
Для лечения различных форм и стадий шизофрении используются антипсихотические препараты (нейролептики). Эффективность этой группы лекарственных средств при купировании и профилактике продуктивной симптоматики подтверждается результатами многочисленных исследований разной степени доказательности [20, 26, 32, 34].
В большинстве исследований также регистрируется благоприятное влияние антипсихотиков последних поколений на выраженность негативных расстройств у больных шизофренией. Последнее обстоятельство имеет не только важное теоретическое, но и практическое значение, поскольку в настоящий момент степень выраженности негативных симптомов (и когнитивной дисфункции) рассматривается в качестве основного предиктора исхода заболевания, детерминирующего семейный и профессиональный прогноз, а также степень социальной адаптации больных шизофренией [1–3, 13, 24].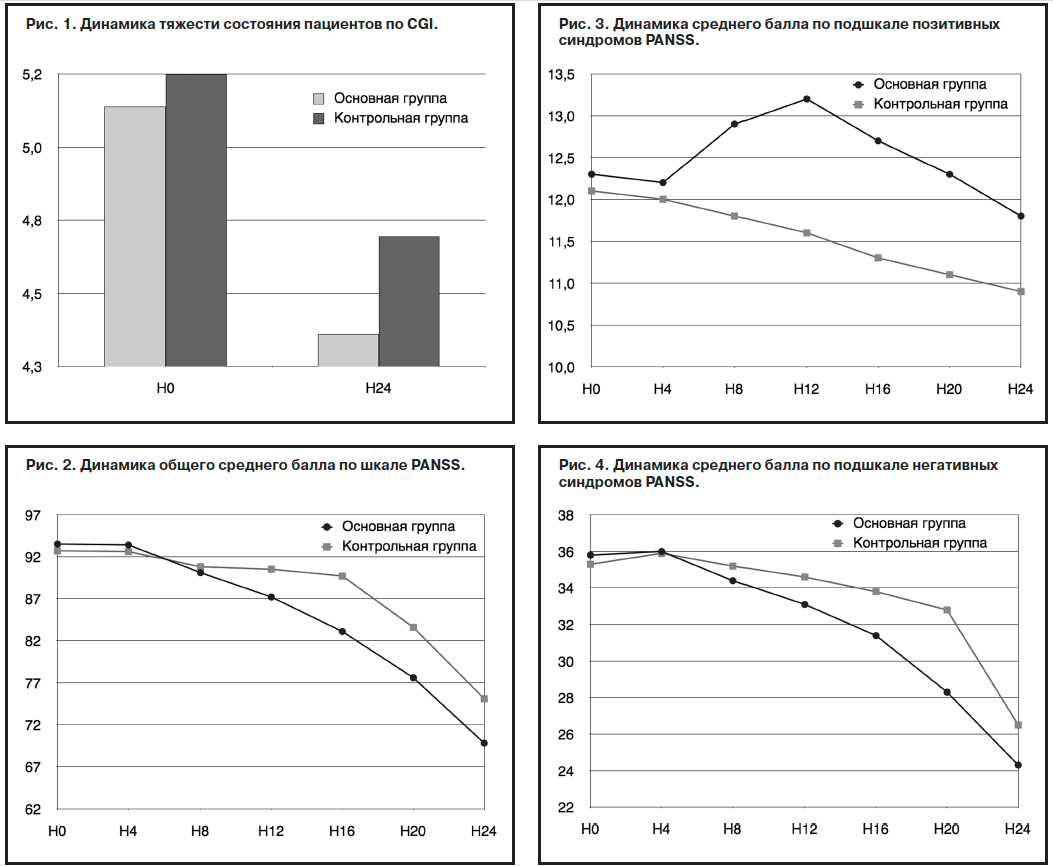
В то же время остается дискуссионным вопрос о механизмах действия и клинических мишенях атипичных антипсихотиков – их влиянии на первичные и/или вторичные негативные расстройства [11, 16, 20, 27]. Многие авторы связывают эффективность атипичных антипсихотических препаратов с редукцией первичной (базисной, «необратимой») негативной симптоматики и нарушений мышления [25, 28, 37]. Другие исследователи, напротив, указывают на тот факт, что применение атипичных антипсихотиков позволяет снизить риск развития вторичной негативной симптоматики, развивающейся, например, в рамках постпсихотической или акинетической депрессии [21, 36], нейролептического паркинсонизма [21, 23].
На этом фоне эффективность антипсихотической терапии негативных расстройств при шизофрении на данном этапе развития психофармакотерапии оценивается большинством авторов как недостаточная [29, 30, 35, 38], что обусловливает поиск лекарственных препаратов или их комбинаций, направленных на повышение переносимости и эффективности антипсихотиков.
Одной из ключевых нейрохимических гипотез развития негативных симптомов при шизофрении является концепция нарушений функционирования ГАМКергической системы, которая регулируется дофаминовыми рецепторами [22, 33]. В пользу этой гипотезы свидетельствуют результаты психофармакотерапии негативных расстройств препаратами, блокирующими дофаминовые рецепторы, а также средствами холинотропного ряда [4, 14, 19].
В этой связи заслуживают внимание данные о применении гопантеновой кислоты и ее рацемической формы в качестве не только корректора экстрапирамидных расстройств (ЭПР) [8, 10], но и дополнительного препарата для лечения шизофрении [5, 15]. Клинико-экспериментальные данные о наличии у рацемата гопантеновой кислоты тимолептического [12, 18], антиастенического [7], нейротрофического [6, 17] эффектов указывают на возможность его применения в качестве адъювантной терапии негативных шизофренических расстройств различного генеза.
Цель натуралистического сравнительного исследования, проведенного в 2012–2013 гг. на кафедре психиатрии, психотерапии и психосоматической патологии факультета повышения квалификации медицинских работников РУДН, – изучение терапевтической эффективности в отношении негативных расстройств и переносимости рацемата гопантеновой кислоты (препарат Пантогам актив) в дозе до 1800 мг/сут при лечении больных шизофренией, протекающей с негативными расстройствами.
Материалы и методы
В исследование включались пациенты обоего пола в возрасте старше 18 лет, обратившиеся за консультацией или госпитализированные в ГПБ №13 (или ее филиалы) г. Москвы (главный врач – кандидат медицинских наук А.Ю.Исраелян), не получавшие антипсихотическую терапию на протяжении предшествующих 6 мес и давшие информированное согласие на участие в исследовании. С целью снижения вероятности наличия латентной или манифестирующей сопутствующей соматической, неврологической и эндокринологической патологии предельный возраст участия в исследовании был ограничен 45 годами. Психиатрический диагноз больных, установленный не менее 5 лет назад, соответствовал диагностическим критериям Международной классификации болезней 10-го пересмотра для шизофрении (F20) и шизотипического расстройства (F21.3–F21.5) с преобладанием негативных расстройств. Также критериями включения являлись результаты скрининговой оценки: не менее 50 баллов по шкале негативных симптомов BPRS, не менее 21 балла по подшкале негативных расстройств шкалы PANSS, не менее 4 баллов по шкале CGI.
Не включались в исследование пациенты с явлениями индивидуальной непереносимости гопантеновой кислоты в анамнезе, страдающие иными, не указанными в критериях включения психопатологическими расстройствами и заболеваниями (в том числе верифицированными по шкале HDRS-21 депрессиями или психотическими расстройствами (более 14 баллов по подшкале позитивных расстройств PANSS [31]), зависимые от психоактивных веществ, беременные и лактирующие. Также ограничениями для включения являлись органическое поражение центральной нервной системы (эпилепсия, деменция, новообразования, рассеянный склероз), пролактинзависимые опухоли гипофиза и молочной железы, феохромоцитома, тяжелая хроническая почечная недостаточность (креатинкиназа менее 10 мл/мин) и другая тяжелая декомпенсированная соматическая патология.
В группе сравнения монотерапия шизофрении с негативными расстройствами осуществлялась атипичными антипсихотиками без назначения препарата Пантогам актив.
При возникновении ЭПР предусматривалось дополнительное в течение не более 7 дней назначение корректора (бипериден). При сохранении ЭПР предполагалось снижение дозы антипсихотика до индивидуально переносимой вплоть до смены антипсихотической терапии.
Эффективность терапии оценивалась на плановых визитах: Н (нед) 0, Н2, Н4, Н8, H12, H16, H20, H24. Инструментами сравнения и основными критериями эффективности препарата в отношении первичных негативных расстройств наряду с клинической оценкой являлась редукция симптоматики по сравнению с исходными баллами шкал BPRS, PANSS, CGI. Для определения динамики когнитивных нарушений использовалась батарея тестов: беглости речевых ответов, Струпа, ассоциативные ряды. Для оценки влияния препарата на вторичные негативные расстройства применялись шкалы HDRS-21 (для выявления нейролептической депрессии), ESRS (для выявления нейролептической заторможенности и паркинсонизма).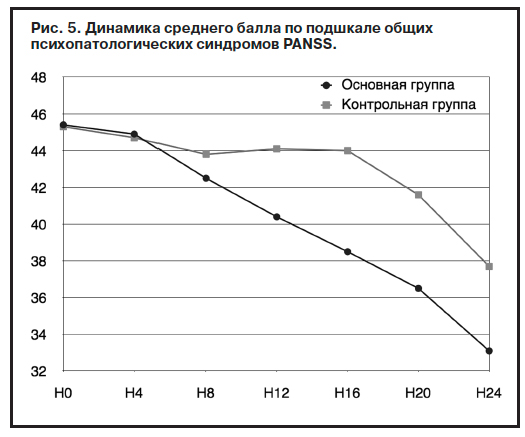
Оценка качества жизни больных проводилась по общей шкале функционирования (GAF) и опроснику SF-36.
Безопасность и переносимость терапии оценивались на основании спонтанных жалоб больного, шкалы побочных эффектов (UKU) и данных клинических и параклинических соматических исследований, включавших регистрацию частоты сердечных сокращений, систолического и диастолического артериального давления в положении сидя, ортостатическую пробу, клинический и биохимический анализы крови, стандартную 12-канальную электрокардиографию в покое.
Дополнительно оценивалась приверженность терапии по показателю соблюдения режима и дозировки назначенного препарата.
Полученный материал обрабатывался с помощью программы Statistica (StatSoft Inc., США). Достоверность различий рассчитывалась при помощи теста Колмогорова– Смирнова.
Результаты исследования
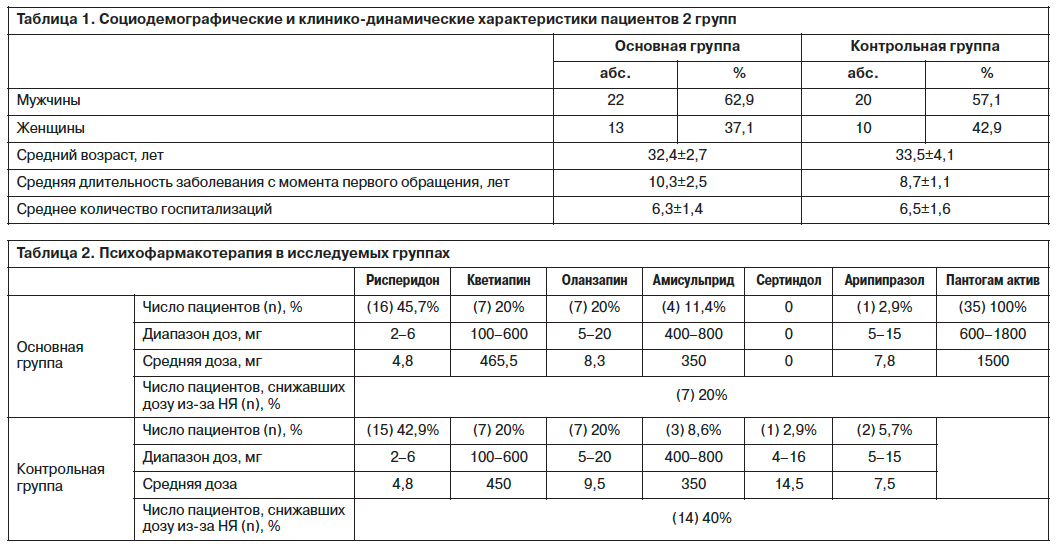
В исследование были включены 70 пациентов (по 35 в основную и контрольную группы). Сходные социодемографические (пол, средний возраст) и клинико-динамические (длительность заболевания, число госпитализаций) характеристики пациентов 2 групп (см. табл. 1) позволяют рассчитывать на валидность полученных результатов.
Основная антипсихотическая терапия, назначаемая пациентам с учетом преобладания в клинической картине заболевания негативных расстройств, включала атипичные антипсихотики последних генераций (см. табл. 2).
Доза Пантогама актив в основной группе достигала максимально допустимой 1800 мг/сут у 12 пациентов. Средняя доза (округляя до целого) – 1500 г/сут.
Согласно шкале CGI-S уменьшение тяжести состояния больных в 2 группах отмечается на 8-й неделе терапии и продолжается в течение 24 нед лечения. В то же время в основной группе статистически значимое уменьшение выраженности психопатологических расстройств фиксируется на 16-й неделе, в то время как в контрольной группе – на 20-й неделе терапии. В целом к окончанию терапии показатель уменьшения тяжести состояния больного в основной группе достоверно превосходит таковой в контрольной (-13,7% vs -9,6%; р<0,05); рис. 1.
Число больных в тяжелом состоянии в основной группе к окончанию исследования снижается достоверно более значимо, чем в контрольной группе (-93,8% vs -58,1%; р<0,01).
Согласно шкале CGI-I с первых месяцев терапии в основной и контрольных группах отмечаются разнонаправленные тенденции: в основной группе уже с первых недель регистрируется «небольшое улучшение» у части больных, в то время как в контрольной группе, напротив, первые
8 нед у части больных (6 на Н4 и 3 на Н8) фиксируется «небольшое ухудшение» состояния, по-видимому, обусловленное нежелательными явлениями (НЯ) антипсихотической терапии.
По шкале PANSS общая редукция баллов в основной группе была статистически более значима, чем в контрольной
(-25,3% vs -20%; р<0,05); табл. 3, рис. 2. При этом в основной группе терапевтический эффект лечения начинал появляться раньше (к 16-й неделе), чем в контрольной, и продолжался на всем протяжении исследования. В контрольной группе снижение общего балла по шкале достигало достоверных значений только к 20-й неделе терапии. Более того, в течение первых 12 нед по отдельным пунктам шкалы (притупленный аффект, пассивно-апатическая социальная отгороженность, нарушение абстрактного мышления, соматическая озабоченность, депрессия, моторная заторможенность, нарушение внимания) регистрировалась отрицательная динамика, обусловленная, по-видимому, развитием вторичных негативных расстройств.
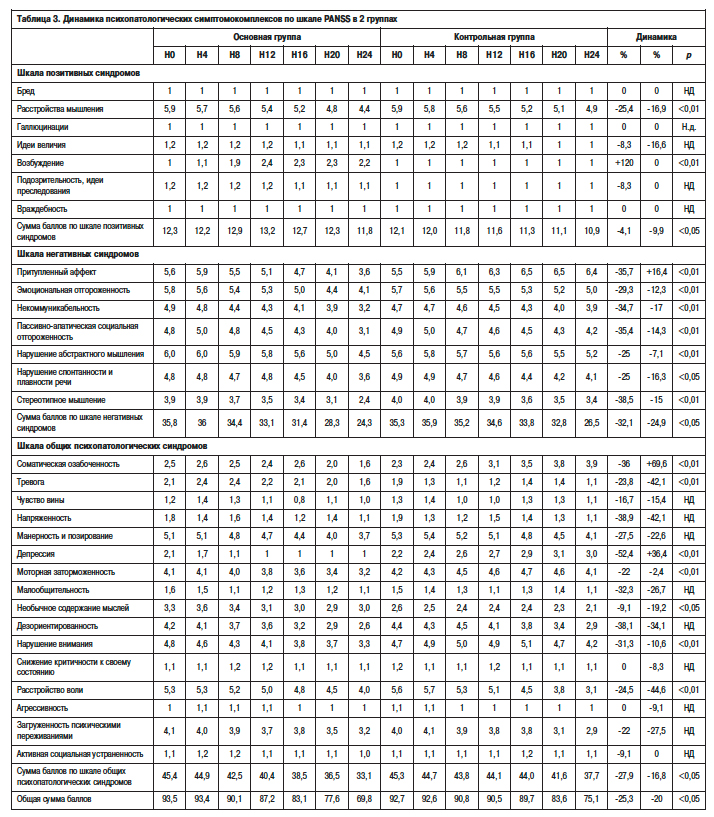
Наибольшая положительная динамика, достоверно превосходящая таковую в контрольной группе, отмечена по подшкалам негативных синдромов (-32,1% vs -24,9%; p<0,05) и общих психопатологических (-27,9% vs 16,8%, р<0,05) синдромов, начиная с 12-й недели лечения (рис. 4, 5).
По шкале позитивных синдромов, напротив, в основной группе в течение 8–20 нед терапии отмечается недостоверное увеличение среднего балла (рис. 3), обусловленное, очевидно, активирующим/психостимулирующим эффектом Пантогама актив (пункт «возбуждение»); см. табл. 3.
В основной группе наибольшей редукции (более 30%) подверглись следующие психопатологические синдромы: притупленный аффект, трудности в общении (некоммуникабельность), пассивно-апатическая социальная отгороженность, стереотипное мышление, соматическая озабоченность, напряженность, депрессия, отказ от сотрудничества, дезориентированность, нарушение внимания. При этом в большинстве случаев (кроме напряженности, отказа от сотрудничества и дезориентированности) редукция являлась статистически более значимой, чем в контрольной группе (см. табл. 3).
Особо следует обратить внимание на разнонаправленность тенденций динамики таких психопатологических синдромов, как притупленный аффект, соматическая озабоченность и депрессия, статистически достоверно уменьшающиеся в основной группе и, напротив, увеличивающиеся в контрольной. Последнее можно также объяснить развитием более выраженных НЯ, что подтверждается психометрической оценкой переносимости терапии.
Таким образом, присоединение к антипсихотической терапии Па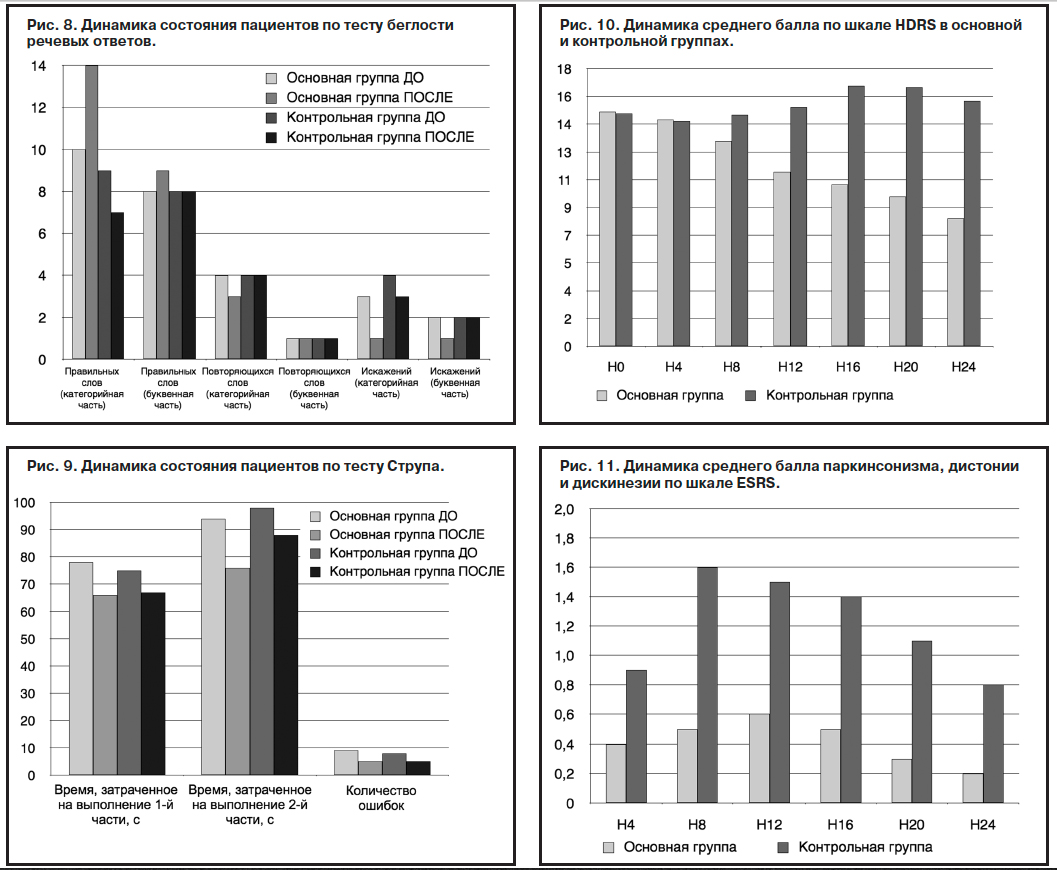 нтогама актив потенцирует терапевтическое влияние нейролептиков на основные проявления первичных негативных расстройств (аналогичные данные получены при анализе результатов оценки состояния пациентов по шкале BPRS; рис. 6, 7), а также уменьшает вероятность возникновения и выраженность вторичных негативных расстройств (нейролептической депрессии, когнитивных нарушений – пункты «бедность экспрессивных жестов», «снижение либидо», «дефицит внимания» и др.). О нейролептическом генезе последних свидетельствуют результаты оценки состояния больных по шкалам HDRS, ESRS, UKU и когнитивных тестов.
нтогама актив потенцирует терапевтическое влияние нейролептиков на основные проявления первичных негативных расстройств (аналогичные данные получены при анализе результатов оценки состояния пациентов по шкале BPRS; рис. 6, 7), а также уменьшает вероятность возникновения и выраженность вторичных негативных расстройств (нейролептической депрессии, когнитивных нарушений – пункты «бедность экспрессивных жестов», «снижение либидо», «дефицит внимания» и др.). О нейролептическом генезе последних свидетельствуют результаты оценки состояния больных по шкалам HDRS, ESRS, UKU и когнитивных тестов.
Динамика когнитивных функций у пациентов 2 групп свидетельствует о более выраженном положительном эффекте терапии с применением Пантогама актив (рис. 8, 9). Монотерапия антипсихотиками на уровне тенденции (но недостоверно) улучшает когнитивные функции либо, напротив, незначительно ухудшает их.

Переносимость терапии
В ходе исследования получены достоверные данные о способности Пантогама актив предупреждать развитие и нивелировать симптомы нейролептической депрессии (рис. 10): средний балл по шкале HDRS в основной группе уменьшается на 45,4% по сравнению с увеличением на 5,3% – в контрольной.
Аналогичным образом включение Пантогама актив в схему терапии негативных шизофренических расстройств позволяет достоверно снизить выраженность развивающихся ЭПР (рис. 11). Особо следует подчеркнуть, что в ходе терапии удалось избежать назначения корректоров ЭПР в 2 группах. Однако число пациентов, которым потребовалась коррекция дозировки антипсихотика в основной группе, оказалось в 2 раза меньше, чем в контрольной (7 наблюдений vs 14 наблюдений).
Спектр НЯ в 2 группах был сходен (рис. 12). При этом выраженность их в основной группе на всем протяжении исследования и на момент его окончания была достоверно меньшей (p<0,01). В основной группе транзиторно наблюдалось в первые 4–8 нед терапии лишь одно НЯ (уменьшение продолжительности сна), не отмечавшееся в контрольной группе.
Соматическое состояние и основные гемодинамические показатели пациентов оставались стабильными (за исключением индекса массы тела – ИМТ и уровня глюкозы в крови), однако к концу терапии наметилась тенденция к меньшему влиянию терапии в основной группе на эти параметры (рис. 13).
Оценка качества повседневного функционирования больного со стороны врача (шкала GAF) и самооценка качества жизни пациента (опросник SF-36) достоверно свидетельствуют о превосходстве комбинированной терапии атипичными антипсихотиками с Пантогамом актив над монотерапией атипичными нейролептиками (рис. 14). Повседневное функционирование пациентов в основной группе улучшается на 60,8% от исходного по сравнению с 35% в контрольной группе (р<0,01), психическое самочувствие по оценке больного – на 73,9% по сравнению с 49,5% (р<0,01), соматическое – на 46,4% по сравнению с 34,4%.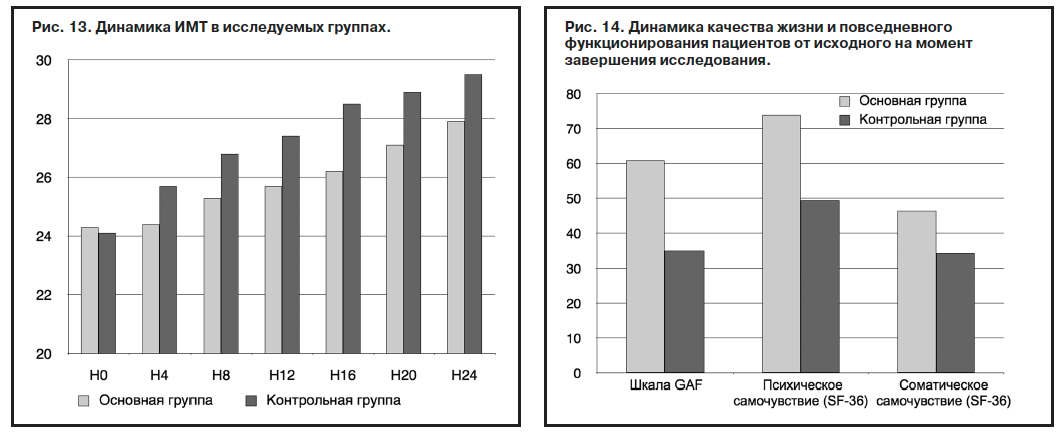
Заключение
Результаты исследования позволяют оптимизировать современные схемы1 терапии шизофрении, протекающей с негативной симптоматикой.
1. Проведенное натуралистическое сравнительное исследование выявило статистически достоверные изменения, подтверждающие, что применение в качестве адъювантного препарата Пантогам актив (МНН: рац-гопантеновая кислода, D,L-гопантеновая кислота) при длительной терапии атипичными антипсихотиками шизофрении, протекающей с преобладанием негативных расстройств, способствует повышению эффективности лечения, о чем свидетельствуют следующие данные:
• Более выраженное, чем в группе сравнения, уменьшение тяжести большинства синдромов негативных расстройств (как первичных, так и вторичных) и улучшение когнитивных функций у пациентов (р<0,05).
• Более быстрое развитие терапевтического эффекта
(в основной группе достоверное снижение тяжести психопатологических симптомокомплексов фиксировалось на 16-й неделе, в то время как в контрольной группе – на 20-й неделе терапии, р<0,05).
• Достоверный профилактический эффект в отношении вторичных негативных (нейролептическая депрессия) и экстрапирамидных расстройств (р<0,05).
• Лучшая переносимость терапии атипичными антипсихотиками по оценке врача и пациента и снижение частоты случаев необходимости коррекции дозировки антипсихотика на фоне приема Пантогама актив в составе комплексной терапии (р<0,01).
2. Результаты данного исследования позволяют предположить, что действие препарата рац-гопантеновой кислоты (Пантогам актив) реализуется не только через ГАМК-ергические механизмы за счет D-изомера гопантеновой кислоты, но и путем блокирования D2-дофаминовых рецепторов L-изомером гопантеновой кислоты [9].
Таким образом, препарат Пантогам актив в средней суточной дозе 1500 мг/сут может быть рекомендован в качестве адъювантного средства, позволяющего повысить эффективность и переносимость терапии шизофрении с негативной симптоматикой при длительном (не менее
24 нед) лечении.
Сведения об авторах
В.Э.Медведев – канд. мед. наук, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПКМР РУДН.
E-mail: melkorcord@mail.ru
А.Ю.Исраелян – канд. мед. наук. глав. врач психиатрической больницы №13 г. Москвы, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПКМР РУДН
Е.В.Гушанская – канд. мед. наук, зав. отд-нием психиатрической больницы №13 г. Москвы, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПКМР РУДН
В.И.Фролова – канд. мед. наук, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПКМР РУДН
Ключевые слова: шизофрения, негативные расстройства, Пантогам актив.
Optimization of the treatment of negative symptoms in schizophrenia with hopantenic
acid racemate
V.E.Medvedev1, A.U.Israelyan1,2, E.V.Gushanskaya1,2, V.I.Frolova1
1Chair of Psychiatry, Psychotherapy and Psychosomatic pathology, People’s Friendship University of Russia
2Psychiatric Hospital №13, Moscow
Summary. The results of naturalistic comparative study show that hopantenic acid racemate (Pantogam active) in the complex therapy of schizophrenia with predominant negative symptoms (in addition to atypical antipsychotics) significantly reduces most of the primary negative symptoms. The probability of secondary negative symptoms manifestation and its intensity also decrease. Effectiveness and tolerability of combined therapy allow achieving statistically more significant quality of life improvement.
Key words: schizophrenia, negative symptoms, Pantogam active.
Для лечения различных форм и стадий шизофрении используются антипсихотические препараты (нейролептики). Эффективность этой группы лекарственных средств при купировании и профилактике продуктивной симптоматики подтверждается результатами многочисленных исследований разной степени доказательности [20, 26, 32, 34].
В большинстве исследований также регистрируется благоприятное влияние антипсихотиков последних поколений на выраженность негативных расстройств у больных шизофренией. Последнее обстоятельство имеет не только важное теоретическое, но и практическое значение, поскольку в настоящий момент степень выраженности негативных симптомов (и когнитивной дисфункции) рассматривается в качестве основного предиктора исхода заболевания, детерминирующего семейный и профессиональный прогноз, а также степень социальной адаптации больных шизофренией [1–3, 13, 24].

В то же время остается дискуссионным вопрос о механизмах действия и клинических мишенях атипичных антипсихотиков – их влиянии на первичные и/или вторичные негативные расстройства [11, 16, 20, 27]. Многие авторы связывают эффективность атипичных антипсихотических препаратов с редукцией первичной (базисной, «необратимой») негативной симптоматики и нарушений мышления [25, 28, 37]. Другие исследователи, напротив, указывают на тот факт, что применение атипичных антипсихотиков позволяет снизить риск развития вторичной негативной симптоматики, развивающейся, например, в рамках постпсихотической или акинетической депрессии [21, 36], нейролептического паркинсонизма [21, 23].
На этом фоне эффективность антипсихотической терапии негативных расстройств при шизофрении на данном этапе развития психофармакотерапии оценивается большинством авторов как недостаточная [29, 30, 35, 38], что обусловливает поиск лекарственных препаратов или их комбинаций, направленных на повышение переносимости и эффективности антипсихотиков.
Одной из ключевых нейрохимических гипотез развития негативных симптомов при шизофрении является концепция нарушений функционирования ГАМКергической системы, которая регулируется дофаминовыми рецепторами [22, 33]. В пользу этой гипотезы свидетельствуют результаты психофармакотерапии негативных расстройств препаратами, блокирующими дофаминовые рецепторы, а также средствами холинотропного ряда [4, 14, 19].
В этой связи заслуживают внимание данные о применении гопантеновой кислоты и ее рацемической формы в качестве не только корректора экстрапирамидных расстройств (ЭПР) [8, 10], но и дополнительного препарата для лечения шизофрении [5, 15]. Клинико-экспериментальные данные о наличии у рацемата гопантеновой кислоты тимолептического [12, 18], антиастенического [7], нейротрофического [6, 17] эффектов указывают на возможность его применения в качестве адъювантной терапии негативных шизофренических расстройств различного генеза.
Цель натуралистического сравнительного исследования, проведенного в 2012–2013 гг. на кафедре психиатрии, психотерапии и психосоматической патологии факультета повышения квалификации медицинских работников РУДН, – изучение терапевтической эффективности в отношении негативных расстройств и переносимости рацемата гопантеновой кислоты (препарат Пантогам актив) в дозе до 1800 мг/сут при лечении больных шизофренией, протекающей с негативными расстройствами.
Материалы и методы
В исследование включались пациенты обоего пола в возрасте старше 18 лет, обратившиеся за консультацией или госпитализированные в ГПБ №13 (или ее филиалы) г. Москвы (главный врач – кандидат медицинских наук А.Ю.Исраелян), не получавшие антипсихотическую терапию на протяжении предшествующих 6 мес и давшие информированное согласие на участие в исследовании. С целью снижения вероятности наличия латентной или манифестирующей сопутствующей соматической, неврологической и эндокринологической патологии предельный возраст участия в исследовании был ограничен 45 годами. Психиатрический диагноз больных, установленный не менее 5 лет назад, соответствовал диагностическим критериям Международной классификации болезней 10-го пересмотра для шизофрении (F20) и шизотипического расстройства (F21.3–F21.5) с преобладанием негативных расстройств. Также критериями включения являлись результаты скрининговой оценки: не менее 50 баллов по шкале негативных симптомов BPRS, не менее 21 балла по подшкале негативных расстройств шкалы PANSS, не менее 4 баллов по шкале CGI.
Не включались в исследование пациенты с явлениями индивидуальной непереносимости гопантеновой кислоты в анамнезе, страдающие иными, не указанными в критериях включения психопатологическими расстройствами и заболеваниями (в том числе верифицированными по шкале HDRS-21 депрессиями или психотическими расстройствами (более 14 баллов по подшкале позитивных расстройств PANSS [31]), зависимые от психоактивных веществ, беременные и лактирующие. Также ограничениями для включения являлись органическое поражение центральной нервной системы (эпилепсия, деменция, новообразования, рассеянный склероз), пролактинзависимые опухоли гипофиза и молочной железы, феохромоцитома, тяжелая хроническая почечная недостаточность (креатинкиназа менее 10 мл/мин) и другая тяжелая декомпенсированная соматическая патология.

В группе сравнения монотерапия шизофрении с негативными расстройствами осуществлялась атипичными антипсихотиками без назначения препарата Пантогам актив.
При возникновении ЭПР предусматривалось дополнительное в течение не более 7 дней назначение корректора (бипериден). При сохранении ЭПР предполагалось снижение дозы антипсихотика до индивидуально переносимой вплоть до смены антипсихотической терапии.
Эффективность терапии оценивалась на плановых визитах: Н (нед) 0, Н2, Н4, Н8, H12, H16, H20, H24. Инструментами сравнения и основными критериями эффективности препарата в отношении первичных негативных расстройств наряду с клинической оценкой являлась редукция симптоматики по сравнению с исходными баллами шкал BPRS, PANSS, CGI. Для определения динамики когнитивных нарушений использовалась батарея тестов: беглости речевых ответов, Струпа, ассоциативные ряды. Для оценки влияния препарата на вторичные негативные расстройства применялись шкалы HDRS-21 (для выявления нейролептической депрессии), ESRS (для выявления нейролептической заторможенности и паркинсонизма).

Оценка качества жизни больных проводилась по общей шкале функционирования (GAF) и опроснику SF-36.
Безопасность и переносимость терапии оценивались на основании спонтанных жалоб больного, шкалы побочных эффектов (UKU) и данных клинических и параклинических соматических исследований, включавших регистрацию частоты сердечных сокращений, систолического и диастолического артериального давления в положении сидя, ортостатическую пробу, клинический и биохимический анализы крови, стандартную 12-канальную электрокардиографию в покое.
Дополнительно оценивалась приверженность терапии по показателю соблюдения режима и дозировки назначенного препарата.
Полученный материал обрабатывался с помощью программы Statistica (StatSoft Inc., США). Достоверность различий рассчитывалась при помощи теста Колмогорова– Смирнова.
Результаты исследования
В исследование были включены 70 пациентов (по 35 в основную и контрольную группы). Сходные социодемографические (пол, средний возраст) и клинико-динамические (длительность заболевания, число госпитализаций) характеристики пациентов 2 групп (см. табл. 1) позволяют рассчитывать на валидность полученных результатов.
Основная антипсихотическая терапия, назначаемая пациентам с учетом преобладания в клинической картине заболевания негативных расстройств, включала атипичные антипсихотики последних генераций (см. табл. 2).
Доза Пантогама актив в основной группе достигала максимально допустимой 1800 мг/сут у 12 пациентов. Средняя доза (округляя до целого) – 1500 г/сут.
Согласно шкале CGI-S уменьшение тяжести состояния больных в 2 группах отмечается на 8-й неделе терапии и продолжается в течение 24 нед лечения. В то же время в основной группе статистически значимое уменьшение выраженности психопатологических расстройств фиксируется на 16-й неделе, в то время как в контрольной группе – на 20-й неделе терапии. В целом к окончанию терапии показатель уменьшения тяжести состояния больного в основной группе достоверно превосходит таковой в контрольной (-13,7% vs -9,6%; р<0,05); рис. 1.
Число больных в тяжелом состоянии в основной группе к окончанию исследования снижается достоверно более значимо, чем в контрольной группе (-93,8% vs -58,1%; р<0,01).

Согласно шкале CGI-I с первых месяцев терапии в основной и контрольных группах отмечаются разнонаправленные тенденции: в основной группе уже с первых недель регистрируется «небольшое улучшение» у части больных, в то время как в контрольной группе, напротив, первые
8 нед у части больных (6 на Н4 и 3 на Н8) фиксируется «небольшое ухудшение» состояния, по-видимому, обусловленное нежелательными явлениями (НЯ) антипсихотической терапии.
По шкале PANSS общая редукция баллов в основной группе была статистически более значима, чем в контрольной
(-25,3% vs -20%; р<0,05); табл. 3, рис. 2. При этом в основной группе терапевтический эффект лечения начинал появляться раньше (к 16-й неделе), чем в контрольной, и продолжался на всем протяжении исследования. В контрольной группе снижение общего балла по шкале достигало достоверных значений только к 20-й неделе терапии. Более того, в течение первых 12 нед по отдельным пунктам шкалы (притупленный аффект, пассивно-апатическая социальная отгороженность, нарушение абстрактного мышления, соматическая озабоченность, депрессия, моторная заторможенность, нарушение внимания) регистрировалась отрицательная динамика, обусловленная, по-видимому, развитием вторичных негативных расстройств.
Наибольшая положительная динамика, достоверно превосходящая таковую в контрольной группе, отмечена по подшкалам негативных синдромов (-32,1% vs -24,9%; p<0,05) и общих психопатологических (-27,9% vs 16,8%, р<0,05) синдромов, начиная с 12-й недели лечения (рис. 4, 5).
По шкале позитивных синдромов, напротив, в основной группе в течение 8–20 нед терапии отмечается недостоверное увеличение среднего балла (рис. 3), обусловленное, очевидно, активирующим/психостимулирующим эффектом Пантогама актив (пункт «возбуждение»); см. табл. 3.
В основной группе наибольшей редукции (более 30%) подверглись следующие психопатологические синдромы: притупленный аффект, трудности в общении (некоммуникабельность), пассивно-апатическая социальная отгороженность, стереотипное мышление, соматическая озабоченность, напряженность, депрессия, отказ от сотрудничества, дезориентированность, нарушение внимания. При этом в большинстве случаев (кроме напряженности, отказа от сотрудничества и дезориентированности) редукция являлась статистически более значимой, чем в контрольной группе (см. табл. 3).
Особо следует обратить внимание на разнонаправленность тенденций динамики таких психопатологических синдромов, как притупленный аффект, соматическая озабоченность и депрессия, статистически достоверно уменьшающиеся в основной группе и, напротив, увеличивающиеся в контрольной. Последнее можно также объяснить развитием более выраженных НЯ, что подтверждается психометрической оценкой переносимости терапии.

Таким образом, присоединение к антипсихотической терапии Па
 нтогама актив потенцирует терапевтическое влияние нейролептиков на основные проявления первичных негативных расстройств (аналогичные данные получены при анализе результатов оценки состояния пациентов по шкале BPRS; рис. 6, 7), а также уменьшает вероятность возникновения и выраженность вторичных негативных расстройств (нейролептической депрессии, когнитивных нарушений – пункты «бедность экспрессивных жестов», «снижение либидо», «дефицит внимания» и др.). О нейролептическом генезе последних свидетельствуют результаты оценки состояния больных по шкалам HDRS, ESRS, UKU и когнитивных тестов.
нтогама актив потенцирует терапевтическое влияние нейролептиков на основные проявления первичных негативных расстройств (аналогичные данные получены при анализе результатов оценки состояния пациентов по шкале BPRS; рис. 6, 7), а также уменьшает вероятность возникновения и выраженность вторичных негативных расстройств (нейролептической депрессии, когнитивных нарушений – пункты «бедность экспрессивных жестов», «снижение либидо», «дефицит внимания» и др.). О нейролептическом генезе последних свидетельствуют результаты оценки состояния больных по шкалам HDRS, ESRS, UKU и когнитивных тестов.
Динамика когнитивных функций у пациентов 2 групп свидетельствует о более выраженном положительном эффекте терапии с применением Пантогама актив (рис. 8, 9). Монотерапия антипсихотиками на уровне тенденции (но недостоверно) улучшает когнитивные функции либо, напротив, незначительно ухудшает их.

Переносимость терапии
В ходе исследования получены достоверные данные о способности Пантогама актив предупреждать развитие и нивелировать симптомы нейролептической депрессии (рис. 10): средний балл по шкале HDRS в основной группе уменьшается на 45,4% по сравнению с увеличением на 5,3% – в контрольной.
Аналогичным образом включение Пантогама актив в схему терапии негативных шизофренических расстройств позволяет достоверно снизить выраженность развивающихся ЭПР (рис. 11). Особо следует подчеркнуть, что в ходе терапии удалось избежать назначения корректоров ЭПР в 2 группах. Однако число пациентов, которым потребовалась коррекция дозировки антипсихотика в основной группе, оказалось в 2 раза меньше, чем в контрольной (7 наблюдений vs 14 наблюдений).
Спектр НЯ в 2 группах был сходен (рис. 12). При этом выраженность их в основной группе на всем протяжении исследования и на момент его окончания была достоверно меньшей (p<0,01). В основной группе транзиторно наблюдалось в первые 4–8 нед терапии лишь одно НЯ (уменьшение продолжительности сна), не отмечавшееся в контрольной группе.
Соматическое состояние и основные гемодинамические показатели пациентов оставались стабильными (за исключением индекса массы тела – ИМТ и уровня глюкозы в крови), однако к концу терапии наметилась тенденция к меньшему влиянию терапии в основной группе на эти параметры (рис. 13).
Оценка качества повседневного функционирования больного со стороны врача (шкала GAF) и самооценка качества жизни пациента (опросник SF-36) достоверно свидетельствуют о превосходстве комбинированной терапии атипичными антипсихотиками с Пантогамом актив над монотерапией атипичными нейролептиками (рис. 14). Повседневное функционирование пациентов в основной группе улучшается на 60,8% от исходного по сравнению с 35% в контрольной группе (р<0,01), психическое самочувствие по оценке больного – на 73,9% по сравнению с 49,5% (р<0,01), соматическое – на 46,4% по сравнению с 34,4%.

Заключение
Результаты исследования позволяют оптимизировать современные схемы1 терапии шизофрении, протекающей с негативной симптоматикой.
1. Проведенное натуралистическое сравнительное исследование выявило статистически достоверные изменения, подтверждающие, что применение в качестве адъювантного препарата Пантогам актив (МНН: рац-гопантеновая кислода, D,L-гопантеновая кислота) при длительной терапии атипичными антипсихотиками шизофрении, протекающей с преобладанием негативных расстройств, способствует повышению эффективности лечения, о чем свидетельствуют следующие данные:
• Более выраженное, чем в группе сравнения, уменьшение тяжести большинства синдромов негативных расстройств (как первичных, так и вторичных) и улучшение когнитивных функций у пациентов (р<0,05).
• Более быстрое развитие терапевтического эффекта
(в основной группе достоверное снижение тяжести психопатологических симптомокомплексов фиксировалось на 16-й неделе, в то время как в контрольной группе – на 20-й неделе терапии, р<0,05).
• Достоверный профилактический эффект в отношении вторичных негативных (нейролептическая депрессия) и экстрапирамидных расстройств (р<0,05).
• Лучшая переносимость терапии атипичными антипсихотиками по оценке врача и пациента и снижение частоты случаев необходимости коррекции дозировки антипсихотика на фоне приема Пантогама актив в составе комплексной терапии (р<0,01).
2. Результаты данного исследования позволяют предположить, что действие препарата рац-гопантеновой кислоты (Пантогам актив) реализуется не только через ГАМК-ергические механизмы за счет D-изомера гопантеновой кислоты, но и путем блокирования D2-дофаминовых рецепторов L-изомером гопантеновой кислоты [9].
Таким образом, препарат Пантогам актив в средней суточной дозе 1500 мг/сут может быть рекомендован в качестве адъювантного средства, позволяющего повысить эффективность и переносимость терапии шизофрении с негативной симптоматикой при длительном (не менее
24 нед) лечении.
Сведения об авторах
В.Э.Медведев – канд. мед. наук, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПКМР РУДН.
E-mail: melkorcord@mail.ru
А.Ю.Исраелян – канд. мед. наук. глав. врач психиатрической больницы №13 г. Москвы, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПКМР РУДН
Е.В.Гушанская – канд. мед. наук, зав. отд-нием психиатрической больницы №13 г. Москвы, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПКМР РУДН
В.И.Фролова – канд. мед. наук, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПКМР РУДН
Список исп. литературыСкрыть список1. Белоусов Ю.Б., Зырянов С.К., Белоусов Д.Ю. Фармакоэкономическая эффективность атипичных антипсихотиков у больных шизофренией. Качественная клин. практика. 2011; 1: 51–7.
2. Бомов П.О. Дефицитарные расстройства у больных шизофренией с дебютом в позднем возрасте (клинико-нейропсихологический и реабилитационный аспекты). Автореф. дис. … канд. мед. наук. Оренбург, 2007.
3. Воробьев В.Ю. Шизофренический дефект (на модели шизофрении, протекающей с преобладанием негативных расстройств). Автореф. дис. … д-ра мед. наук. М., 1988.
4. Дэвис Дж.М. Шизофрения: выбор антипсихотической терапии. Соц. и клин. психиатрия. 2006; 3: 77–80.
5. Джуга Н.П. и др. Влияние гопантеновой кислоты и глицина на эффективность галоперидола при терапии пациентов с параноидной шизофренией. Психиатр. и психофармакотер. 2012; 2: 23–9.
6. Дума С.Н. Оценка клинической эффективности нейропротекторов, влияющих на систему g-аминомасляной кислоты, при лечении когнитивных расстройств у пациентов с дисциркуляторной энцефалопатией I–II стадии. Фарматека. 2010; 15: 96–100.
7. Канаева Л.С., Вазагаева Т.И., Ястребова В.В. Перспективы применения препарата Пантогам актив у больных с астеническими расстройствами. Психиатр. и психофармакотер. 2009; 6: 34–9.
8. Катунина Е.А., Малыхина Е.А., Аванесова О.В. и др. Применение Пантогама актив в комплексном лечении дистонических гиперкинезов. Журн. неврол. и психиатр. 2010; 11: 2.
9. Ковалев Г.И., Старикова Н.А. Пантогам актив: механизм фармакологического действия. РМЖ. 2010; 21: 2–4.
10. Концевой В.А., Ротштейн В.Г., Богдан М.Н. и др. Пантогам в повседневной психиатрической практике. Журн. неврол. и психиатр им. С.С.Корсакова. 2007; 12: 34–9.
11. Медведев В.Э. Негативные расстройства: понятие и терапия. Психиатр. и психофармакотер. 2011; 6: 16–21.
12. Медведев В.Э., Епифанов А.В. Терапия невротических, связанных со стрессом и соматоформных расстройств у пациентов с гипертонической болезнью препаратом Пантогам актив. Рос. психиатр. журн. 2011; 1: 55–61.
13. Мелехов Д.Е. К проблеме резидуальных и дефектных состояний при шизофрении (в связи с задачами клинического и социально-трудового прогноза). Журн. невропатол. и психиат. 1981; 1: 128–38.
14. Морозова М.А., Бениашвили А.Г., Бурминский Д.С. Шизофренический дефект как терапевтическая мишень. Психиатрия. 2008; 3: 13–20.
15. Попов М.Ю. Адъювантная терапия параноидной шизофрении: оптимизация клинического действия галоперидола. Автореф. дис. … д-ра мед. наук. СПб., 2012.
16. Снедков Е.В. Атипичные антипсихотики: поиск решения старых и новых проблем. Психиатр. и психофармакотер. 2006; 4: 45–50.
17. Собенникова В.В. и др. Сравнительная оценка эффективности препарата Пантогам актив в терапии когнитивных расстройств. Психиатрия. 2010; 5: 41–6.
18. Сухотина Н.К. Пантогам как средство лечения пограничных нервно-психических расстройств. Медлайн экспресс. 2006; 4 (187): 44–5.
19. Сыропятов О.Г. Современное лечение шизофрении. Нейронауки (UA). 2007; 2.
20. Цыганков Б.Д., Агасарян Э.Т. Анализ эффективности и безопасности современных и классических антипсихотических препаратов. Журн. неврол. и психиатр. 2010; 9: 64–70.
21. Шток В.Н., Иванова-Смоленская И.А., Левин О.С. Экстрапирамидные расстройства. М., 2002.
22. Alphs L. An industry perspective on the NIMH consensus statement on negative symptoms. Schizophr Bull 2006; 32: 225–30.
23. Ananth J, Parameswaran S, Gunatilake S et al. Neuroleptic malignant syndrome and atypical antipsychotic drugs. J Clin Psychiat 2004; 65 (4): 464–70.
24. Аndreasen NC, Carpenter WT, Kane JM et al. Remission in schizophrenia: proposed criteria and rational for consensus. Am J Psychiat 2005; 162: 441–9.
25. Arango C, Buchanan RW, Kirkpatrick B, Carpenter WT. The deficit syndrome in schizophrenia: implications for the treatment of negative symptoms. Eur Psychiat 2004; 19: 21–6.
26. Bodkin JA, Siris SG, Bermanzohn PC et al. Double-blind, placebo-controlled, multicenter trial of selegiline augmentation of antipsychotic medication to treat negative symptoms in outpatients with schizophrenia. Am J Psychiat 2005; 162: 388–90.
27. Buchanan RW. Persistent Negative Symptoms in Schizophrenia: An Overview. Schizophrenia Bull 2007; 4: 1013–22.
28. Goldberg SC. Negative and deficit symptoms in schizophrenia do respond to neuroleptics. Schizophr Bull 1985; 11: 453–6.
29. Harrow M, Jobe TH. Factors involved in outcome and recovery in schizophrenia patients not on antipsychotic medications: a 15-year multifollow-up study. J Nerv Ment Dis 2007; 195 (5): 404–6.
30. Kabinoff GS, Toalson PA, Healey KM et al. Вопросы метаболизма, связанные с применяемыми в психиатрии атипичными нейролептиками: мифы и факты. Психиатр. и психофармакотер. 2003; 3.
31. Kay SR, Fiszbein A, Opler LA. The Positive and Negative Syndrome Scale (PANSS) for schizophrenia. Schizophr Bull 1987; 13: 261–76.
32. Lieberman JA, Stroup TS, McEvoy JP et al. Effectiveness of antipsychotic drugs in patients with chronic schizophrenia. N Engl J Med 2005; 353 (12): 1209–23.
33. Lieberman JA. Dopamine partial agonists: a new class of antipsychotic. CNS Drugs 2005; 18 (4): 251–67.
34. Meisenzahl EM, Scheuerecker J, Zipse M et al. Effects of treatment with the atypical neuroleptic quetiapine on working memory function: a functional MRI follow-up investigation. Eur Arch Psychiat Clin Neur 2006; 256 (8): 522–31.
35. Murphy BP et al. Pharmacological treatment of primary negative symptoms in schizophrenia: a systematic review. Schizophr Res 2006; 88: 5–25.
36. Rosenheck RA. Effectiveness vs efficacy of second-generation antipsychotics: haloperidol without anticholinergics as a comparator. Psychiat Serv 2005; 56: 85–92.
37. Stip E. Cognition, schizophrenia and the effect of antipsychotics. Encephale 2006; 32 (3 Pt. 1): 341–50.
38. Taylor DM, McAskill R. Atypical antipsychotics and weight gain a systematic review. Acta Psychiat Scand 2000; 101: 416–32.


