Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№05 2014
Эффективность терапии атипичными антипсихотиками больных шизофренией в ремиссии №05 2014
Номера страниц в выпуске:43-48
В последние годы активно обсуждается вопрос об обоснованности применения атипичных антипсихотиков при лечении шизофрении. Неоднозначные результаты клинических исследований, зачастую подвергающие сомнению эффективность препаратов этого ряда при терапии негативных расстройств, трудно корригируемые метаболические нежелательные явления (НЯ), сравнительная дороговизна ограничивают широкое применение атипичных антипсихотиков.
Резюме. Проведено перекрестное сравнительное психофармакотерапевтическое исследование эффективности терапии атипичных антипсихотиков при шизофрении. Установлены клинические предикторы эффективности арипипразола и оланзапина при разных вариантах неполной ремиссии. Спектр нежелательных эффектов препаратов отличается и также влияет на возможность назначения различным категориям больных.
Ключевые слова: ремиссия, шизофрения, арипипразол, оланзапин.
The effectiveness of treatment with atypical antipsychotics in patients with schizophrenia in remission
V.E.Medvedev1, V.I.Frolova1, A.Yu.Ter-Israelian1,2, E.V.Gushanskaya1,2
1Russian Peoples' Friendship University;
2City Psychiatric Hospital №13 Moscow
Summary. Conducted cross-comparative psychopharmacotheurapeutic study of the efficacy of atypical antipsychotics in schizophrenia. Established clinical predictors of the efficacy of aripiprazole and olanzapine in different variants of partial remission. The spectrum of adverse effects of drugs is different and also affects the ability to assign different categories of patients.
Key words: remission, schizophrenia, aripiprazole, olanzapine.
В последние годы активно обсуждается вопрос об обоснованности применения атипичных антипсихотиков при лечении шизофрении [1–3]. Неоднозначные результаты клинических исследований, зачастую подвергающие сомнению эффективность препаратов этого ряда при терапии негативных расстройств [4–7], трудно корригируемые метаболические нежелательные явления (НЯ) [8, 9], сравнительная дороговизна ограничивают широкое применение атипичных антипсихотиков.
Возможными объяснениями противоречивых результатов применения атипичных антипсихотиков при негативных шизофренических расстройствах являются как различные патогенетические механизмы развития симптоматики [10–12], так и отличающиеся рецепторные профили большинства антипсихотиков последних поколений
[1, 13, 14]. Существенную роль, по-видимому, играет и отсутствие дифференцированных предикторов (клинико-динамических, биологических) эффективности и показаний при назначении нейролептиков.
Цель натуралистического открытого сравнительного фармакотерапевтического исследования – изучение эффективности и переносимости среднесрочной (24 нед) терапии атипичными антипсихотиками больных шизофренией с клинически отличающимися вариантами неполной лекарственной ремиссии (дефекта).
Препаратами сравнения были выбраны имеющие различающийся рецепторный профиль и механизм действия нейролептики последних поколений: оланзапин (Парнасан) и арипипразол (Амдоал). Арипипразол – парциальный агонист D2-рецепторов, ингибирующий обратный захват серотонина (агонист 5-НТ1А- и антагонист 5-НТ2А- и 5-НТ2С-рецепторов) [14–16]. Оланзапин – полный антагонист D2-дофаминовых, а также 5-HT2A-, 5-HT2C-, 5-HT3-, 5-HT6-, 5-HT7-серотониновых и H1-гистаминовых рецепторов [16, 17].
Работа проведена в 2013–2014-е годы на базе отделений клинической базы кафедры психиатрии, психотерапии и психосоматической патологии ФПК МР ФГБОУ ВПО РУДН – МБУЗ ГПБ №13 г. Москвы.
Для уменьшения вероятности влияния сопутствующих соматических, неврологических, эндокринных заболеваний, климактерического синдрома в исследование включались больные не старше 45 лет, не обнаруживающие при физикальном и инструментальном обследованиях симптомов соматических заболеваний в тяжелой степени или в стадии декомпенсации.
Критерии исключения: индивидуальная непереносимость оланзапина или арипипразола в анамнезе, высокий суицидальный риск (по шкале суицидального риска), зависимость от психоактивных веществ, беременность, лактация, органическое поражение центральной нервной системы (эпилепсия, деменция, новообразования, рассеянный склероз и т.п.), пролактинзависимые новообразования (пролактинома гипофиза и рак молочной железы), феохромоцитома, сопутствующий прием агонистов дофамина.
Набор пациентов, удовлетворяющих критериям включения, осуществлялся попеременно в группу принимающих арипипразол до 15 мг/сут (1-я группа) или оланзапин до 10 мг/сут (2-я группа) из числа наблюдавшихся в стационаре или амбулатории и стабильно получавших не менее предшествовавших 8 нед атипичные или «классические» нейролептики в форме монотерапии.
Основаниями для перехода на новую терапию с отменой исходной служили недостаточная эффективность и/или переносимость, а также низкая приверженность предшествовавшей терапии. Стартовая доза, схема приема и порядок перекрестной титрации препарата подбирались с учетом индивидуальной переносимости. Длительность исследования составляла 24 нед.
Сопутствующая психотропная терапия исключалась. При возникновении легких экстрапирамидных расстройств (ЭПР) дополнительно в течение не более 7 дней допускалось назначение корректора. При сохранении ЭПР доза антипсихотика снижалась до индивидуально переносимой вплоть до отмены терапии и исключения пациента из исследования. Оценка динамики состояния и эффективности терапии проводилась на плановых визитах: месяц (М) 0 (состояние до начала исследования), М1, М2, М3, М4, М5 и М6.
Инструментами сравнения и основными критериями эффективности наряду с клинической оценкой являлись редукция симптоматики по шкалам PANSS, SANS, CGI, батареи когнитивных тестов (тест беглости речевых ответов, тест Струпа, ассоциативные ряды). Для оценки влияния терапии на повседневное функционирование использовалась шкала функционирования GAF.
Безопасность и переносимость терапии оценивались на основании спонтанных жалоб больного, шкалы побочных эффектов (UKU) и данных клинических и параклинических соматических исследований, включающих регистрацию основных гемодинамических показателей, электрокардиографию, клинический и биохимический анализы крови (включая определение уровня пролактина), индекс массы тела. Для изучения влияния терапии на «вторичные» негативные расстройства (нейролептическая депрессия, паркинсоническая заторможенность и др.) на каждом визите применялись шкалы HADS и Симпсона–Ангуса.
Оценка результатов проводилась стандартными методами статистического анализа (однофакторный дисперсионный анализ повторных измерений с апостериорным тестом минимальных значимых различий, метод переноса данных последнего наблюдения, парный t-тест, корреляции по смешанным моментам Пирсона) с использованием программы Statistica.
Из табл. 1 следует, что, несмотря на стабильное психическое состояние, качество ремиссии следует признать невысоким, так как социальное функционирование большинства больных существенно ограничено. В каждую из групп были включены по 20 пациентов, ранее принимавших
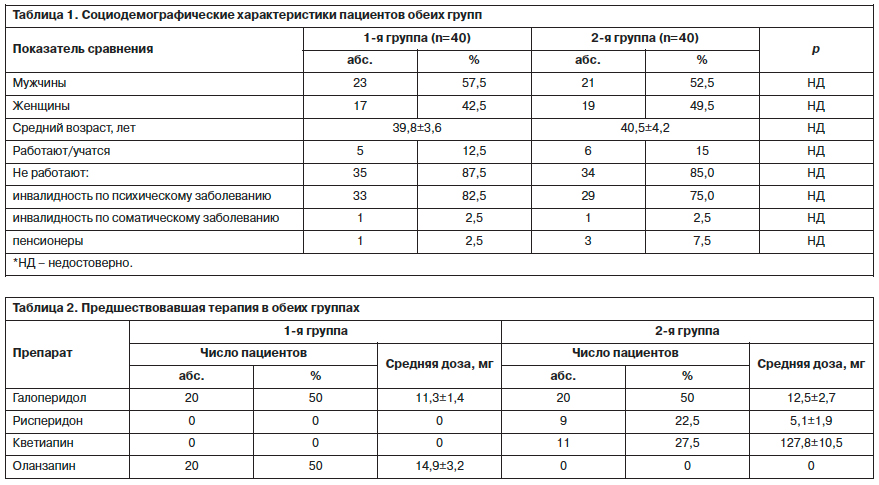
галоперидол. Остальные 20 больных в 1-й группе до включения в исследование принимали оланзапин; во 2-й группе 9 пациентов в качестве терапии до исследования получали рисперидон, 11 пациентов – кветиапин (табл. 2).
Средняя доза арипипразола в 1-й группе достигала 13,2±1,7 мг/сут, оланзапина во 2-й группе – 8,4±1,6 мг/сут. Клинически были дифференцированы два варианта ремиссии больных: дефицитарное состояние с остаточными продуктивными симптомами (17 пациентов в 1-й группе и 22 пациента во 2-й группе) и без таковых (23 пациента в 1-й группе и 18 пациентов во 2-й группе) [18].
Психопатологические проявления дефекта без продуктивных симптомов составляли симптомы редукции энергетического потенциала и эмоционального дефицита.
Доминировали жалобы на ощущение физической и психической слабости, быстрой утомляемости, снижение инициативности, способности самостоятельно принимать решения, планировать. Самостоятельная деятельность больных не превышала 2–3 ч в сутки и ограничивалась монотонной однообразной работой по дому.
При осмотре выявлялись мимическое, речевое и эмоциональное обеднение, снижение круга интересов, социальных контактов, когнитивные расстройства (формальность, амбивалентность, трудности в формулировании ответов, сосредоточения, концентрации внимания, снижение памяти).
У больных с остаточной продуктивной симптоматикой (не определявшей в целом клиническую картину и поведение пациентов) на фоне тех же симптомов редукции энергетического потенциала обнаруживались изолированные ретроспективные монотематические бредовые убеждения, которые относились, как правило, к отдельным событиям отдаленного прошлого (подозрительность только в определенной ситуации или по отношению к конкретному человеку, персекуторная оценка единственного события
и т.п.). Аффективный фон все пациенты оценивали как «обычный», «привычный» для них, «неизмененный».
Исходно средний балл по шкале PANSS составил 94,7±2,7 и 90,9±3,8 в 1 и 2-й группах (p<0,05), по подшкале негативных расстройств – 28,5±8,1 и 27,3±4,9 балла соответственно (p<0,05). Средний исходный балл по шкале SANS достигал 86,1±6,3 и 82,5±4,7 балла соответственно. Таким образом, сходство пациентов обеих групп по основным социодемографическим и клинико-динамическим показателям позволяет рассчитывать на валидность полученных данных.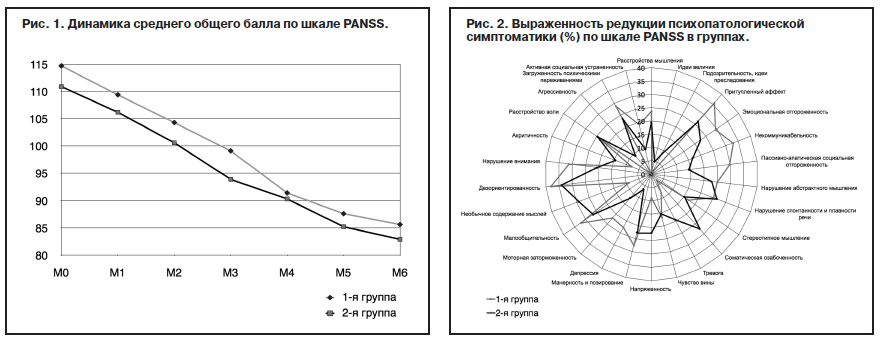
достигало 25,4%, оланзапина (Парнасана) – 25,2% (разница недостоверна).
При оценке влияния терапии на клиническую картину двух клинических вариантов дефекта установлены следующие общие для обоих препаратов эффекты. Так, положительная динамика состояния у больных с неполной ремиссией без остаточной продуктивной симптоматики при приеме и арипипразола (Амдоала) и оланзапина (Парнасана) реализовалась уменьшением интенсивности психической и физической утомляемости, «анергии», трудности сосредоточения, когнитивных расстройств. Постепенно увеличивалась эмоциональная вовлеченность больных в общение с близкими, в события не только собственной, но и общественной жизни, расширялся круг общения и интересов. Пациенты задумывались о возможности трудоустройства. Однако к концу исследования у больных сохранялись мотивационные и волевые расстройства, не позволившие ни одному из неработающих пациентов устроиться на работу.
При терапии дефицитарных состояний с остаточными продуктивными симптомами, помимо описанного выше положительного влияния на астено-когнитивные и эмоциональные расстройства, удалось достичь некоторого снижения выраженности бредовых ретроспекций. Так, в части (29 из 39 пациентов) случаев больные начинали подвергать сомнению свою прежнюю патологическую интерпретацию событий, менее болезненно реагировали на упоминания или воспоминания о них и даже пытались сами инициировать обсуждение их с врачом и членами семьи.
В то же время следует отметить, что у 10 пациентов с остаточными продуктивными симптомами из 1-й группы на фоне оживления эмоциональности и побуждений отмечалось увеличение реактивной лабильности, тревожно-ипохондрических фобий без усиления психотической симптоматики (рис. 2).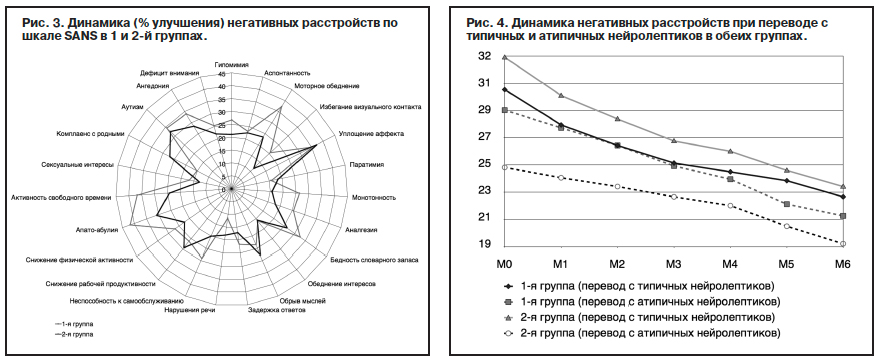
При дифференцированной оценке влияния терапии арипипразолом (Амдоалом) и оланзапином (Парнасаном) на негативные расстройства по шкале SANS также установлено, что достоверные отличия (p<0,001) в спектре действия препаратов касаются таких симптомов, как моторное обеднение, бедность словарного запаса, способность к самообслуживанию и активность в свободное время – для арипипразола, взаимопонимание и доверие с родными, снижение рабочей продуктивности – для оланзапина (рис. 3).
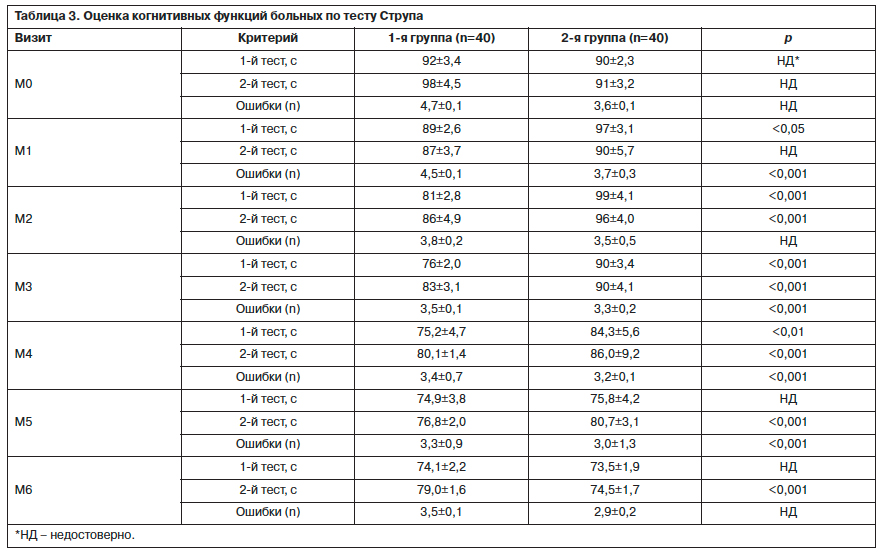
Согласно когнитивным тестам среднее улучшение состояния больных было сопоставимо и составляло 19,1% от исходного в 1-й группе и 18,3% – во 2-й группе. Однако динамика результатов тестов в 2 группах носила не единообразный характер (представлена на примере теста Струпа); табл. 3. Так, в 1-й группе улучшение фиксировалось уже на визите М1 и постепенно увеличивалось к концу исследования. Во 2-й группе выраженность когнитивных расстройств в первые 2 мес (М1 и М2) незначительно увеличивалась, а затем начала прогрессивно снижаться.
С большой долей вероятности речь идет о проявлениях седативного эффекта оланзапина [19–21].
Отдельной оценки заслуживает влияние терапии на негативные и когнитивные расстройства у пациентов, переведенных с терапии типичными (галоперидол) и атипичными антипсихотиками на препараты исследования.
В случаях предшествующего приема галоперидола в первые 2 мес выраженность негативных и когнитивных расстройств существенно уменьшалась, затем скорость нарастания терапевтического эффекта снижалась и вновь нарастала к концу 6-го месяца лечения. При смене терапии с других атипичных антипсихотиков на арипипразол
(Амдоал) и оланзапин (Парнасан) нивелирование негативных расстройств носило плавно-поступательный характер на всем протяжении исследования (рис. 4).
Данный эффект при отмене галоперидола может быть отчасти объяснен редукцией в первые месяцы «вторичных» негативных расстройств (что подтверждается соответствующей динамикой средних баллов по шкалам HADS и Симпсона–Ангуса) и нарастанием положительного влияния арипипразола и оланзапина на «первичные» дефицитарные расстройства с течением времени. Такое объяснение находит подтверждение в результатах других клинических исследований [18, 22, 23].
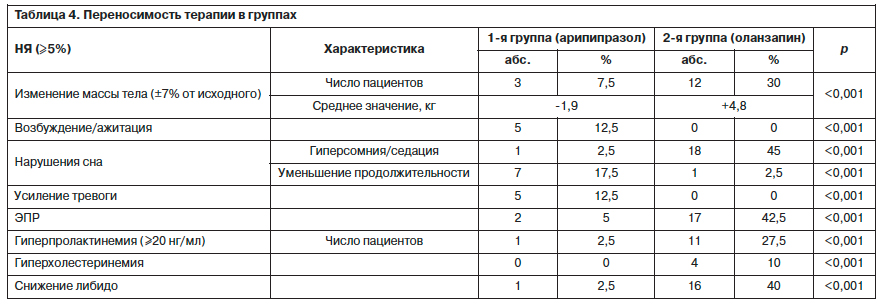
В 1-й группе НЯ отмечены у 19 (47,5%) пациентов, во 2-й группе – у 25 (62,5%). Наиболее частыми НЯ арипипразола являлись усиление тревоги, возбуждение, уменьшение продолжительности сна, оланзапина – гиперсомния, снижение либидо и ЭПР. При этом в 1-й группе дополнительное временное назначение корректоров ЭПР не потребовалось ни разу, во 2-й группе – у 17 (42,5%) пациентов.
По показателю изменения массы тела пациенты обеих групп существенно отличались: за 6 мес терапии в 1-й группе в целом отмечена тенденция к снижению массы тела (-1,9 кг), увеличение (+2,9 кг) зарегистрировано у 3 пациентов. Во 2-й группе, напротив, средняя масса тела увеличивалась, превышая на визите М6 7% от исходной у 12 больных.
Статистически значимых отличий между группами по основным гемодинамическим показателям, уровню липидов и глюкозы в крови не выявлено. Все изменения исходных значений уровня холестерина, липопротеидов низкой и высокой плотности, глюкозы не выходили за рамки установленных физиологических норм.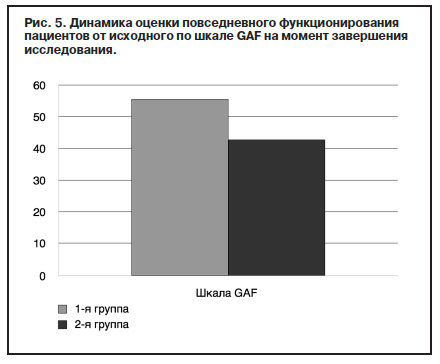
Скорость и динамика развития антинегативного (в отношении «первичных» и «вторичных» негативных расстройств) и прокогнитивного эффекта атипичных нейролептиков определяются не только механизмами рецепторного взаимодействия, но и характером предшествующей терапии и ее переносимости. Так, частичный агонист
D2-дофаминовых рецепторов арипипразол (Амдоал) может рассматриваться в качестве альтернативы нейролептикам, лечение которыми ассоциировано с жалобами на седацию и гиперсомнию, а также у пациентов с избыточной массой тела и/или тенденцией к ее увеличению, сахарным диабетом, сердечно-сосудистыми заболеваниями при наличии склонности к развитию ЭПР.
Полученные данные в практическом плане позволяют осуществлять более дифференцированный подход к назначению современных антипсихотиков с целью повышения эффективности и приверженности длительной терапии, сокращения финансовых затрат (на смену терапии, повторные госпитализации), повышения ресоциализации хронических больных шизофренией. Положительный субъективный опыт и отношение к антипсихотику сильно коррелируют с комплаентностью и благоприятным долговременным прогнозом.
Фролова Вероника Игоревна – канд. мед. наук, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПК МР ФГБОУ ВПО РУДН
Тер-Исраелян Алексей Юрьевич – канд. мед. наук, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПК МР ФГБОУ ВПО РУДН, глав. врач МБУЗ ГПБ №13 г. Москвы
Гушанская Екатерина Владимировна – канд. мед. наук, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПК МР ФГБОУ ВПО РУДН, зав. отд-нием МБУЗ ГПБ №13 г. Москвы
Ключевые слова: ремиссия, шизофрения, арипипразол, оланзапин.
The effectiveness of treatment with atypical antipsychotics in patients with schizophrenia in remission
V.E.Medvedev1, V.I.Frolova1, A.Yu.Ter-Israelian1,2, E.V.Gushanskaya1,2
1Russian Peoples' Friendship University;
2City Psychiatric Hospital №13 Moscow
Summary. Conducted cross-comparative psychopharmacotheurapeutic study of the efficacy of atypical antipsychotics in schizophrenia. Established clinical predictors of the efficacy of aripiprazole and olanzapine in different variants of partial remission. The spectrum of adverse effects of drugs is different and also affects the ability to assign different categories of patients.
Key words: remission, schizophrenia, aripiprazole, olanzapine.
В последние годы активно обсуждается вопрос об обоснованности применения атипичных антипсихотиков при лечении шизофрении [1–3]. Неоднозначные результаты клинических исследований, зачастую подвергающие сомнению эффективность препаратов этого ряда при терапии негативных расстройств [4–7], трудно корригируемые метаболические нежелательные явления (НЯ) [8, 9], сравнительная дороговизна ограничивают широкое применение атипичных антипсихотиков.
Возможными объяснениями противоречивых результатов применения атипичных антипсихотиков при негативных шизофренических расстройствах являются как различные патогенетические механизмы развития симптоматики [10–12], так и отличающиеся рецепторные профили большинства антипсихотиков последних поколений
[1, 13, 14]. Существенную роль, по-видимому, играет и отсутствие дифференцированных предикторов (клинико-динамических, биологических) эффективности и показаний при назначении нейролептиков.
Цель натуралистического открытого сравнительного фармакотерапевтического исследования – изучение эффективности и переносимости среднесрочной (24 нед) терапии атипичными антипсихотиками больных шизофренией с клинически отличающимися вариантами неполной лекарственной ремиссии (дефекта).
Препаратами сравнения были выбраны имеющие различающийся рецепторный профиль и механизм действия нейролептики последних поколений: оланзапин (Парнасан) и арипипразол (Амдоал). Арипипразол – парциальный агонист D2-рецепторов, ингибирующий обратный захват серотонина (агонист 5-НТ1А- и антагонист 5-НТ2А- и 5-НТ2С-рецепторов) [14–16]. Оланзапин – полный антагонист D2-дофаминовых, а также 5-HT2A-, 5-HT2C-, 5-HT3-, 5-HT6-, 5-HT7-серотониновых и H1-гистаминовых рецепторов [16, 17].
Работа проведена в 2013–2014-е годы на базе отделений клинической базы кафедры психиатрии, психотерапии и психосоматической патологии ФПК МР ФГБОУ ВПО РУДН – МБУЗ ГПБ №13 г. Москвы.
Дизайн исследования
В исследование включались пациенты обоего пола в возрасте от 18 лет, соответствующие диагностическим критериям Международной классификации болезней 10-го пересмотра для неполной ремиссии шизофрении (F20.х4), диагностированной не менее 5 лет назад, и имеющие не менее 21 балла по подшкале негативных расстройств и не более 14 баллов по подшкале позитивных расстройств шкалы PANSS.Для уменьшения вероятности влияния сопутствующих соматических, неврологических, эндокринных заболеваний, климактерического синдрома в исследование включались больные не старше 45 лет, не обнаруживающие при физикальном и инструментальном обследованиях симптомов соматических заболеваний в тяжелой степени или в стадии декомпенсации.
Критерии исключения: индивидуальная непереносимость оланзапина или арипипразола в анамнезе, высокий суицидальный риск (по шкале суицидального риска), зависимость от психоактивных веществ, беременность, лактация, органическое поражение центральной нервной системы (эпилепсия, деменция, новообразования, рассеянный склероз и т.п.), пролактинзависимые новообразования (пролактинома гипофиза и рак молочной железы), феохромоцитома, сопутствующий прием агонистов дофамина.
Набор пациентов, удовлетворяющих критериям включения, осуществлялся попеременно в группу принимающих арипипразол до 15 мг/сут (1-я группа) или оланзапин до 10 мг/сут (2-я группа) из числа наблюдавшихся в стационаре или амбулатории и стабильно получавших не менее предшествовавших 8 нед атипичные или «классические» нейролептики в форме монотерапии.
Основаниями для перехода на новую терапию с отменой исходной служили недостаточная эффективность и/или переносимость, а также низкая приверженность предшествовавшей терапии. Стартовая доза, схема приема и порядок перекрестной титрации препарата подбирались с учетом индивидуальной переносимости. Длительность исследования составляла 24 нед.
Сопутствующая психотропная терапия исключалась. При возникновении легких экстрапирамидных расстройств (ЭПР) дополнительно в течение не более 7 дней допускалось назначение корректора. При сохранении ЭПР доза антипсихотика снижалась до индивидуально переносимой вплоть до отмены терапии и исключения пациента из исследования. Оценка динамики состояния и эффективности терапии проводилась на плановых визитах: месяц (М) 0 (состояние до начала исследования), М1, М2, М3, М4, М5 и М6.
Инструментами сравнения и основными критериями эффективности наряду с клинической оценкой являлись редукция симптоматики по шкалам PANSS, SANS, CGI, батареи когнитивных тестов (тест беглости речевых ответов, тест Струпа, ассоциативные ряды). Для оценки влияния терапии на повседневное функционирование использовалась шкала функционирования GAF.
Безопасность и переносимость терапии оценивались на основании спонтанных жалоб больного, шкалы побочных эффектов (UKU) и данных клинических и параклинических соматических исследований, включающих регистрацию основных гемодинамических показателей, электрокардиографию, клинический и биохимический анализы крови (включая определение уровня пролактина), индекс массы тела. Для изучения влияния терапии на «вторичные» негативные расстройства (нейролептическая депрессия, паркинсоническая заторможенность и др.) на каждом визите применялись шкалы HADS и Симпсона–Ангуса.
Оценка результатов проводилась стандартными методами статистического анализа (однофакторный дисперсионный анализ повторных измерений с апостериорным тестом минимальных значимых различий, метод переноса данных последнего наблюдения, парный t-тест, корреляции по смешанным моментам Пирсона) с использованием программы Statistica.
Результаты исследования
Общее число пациентов, включенных в каждую группу, составило 40. Средняя длительность эндогенного заболевания в группах, по данным медицинской документации, составила 12,4±3,6 и 11,1±4,2 года (1 и 2-я группа соответственно; p<0,05). Основные социодемографические показатели больных 2 групп представлены в табл. 1.
Из табл. 1 следует, что, несмотря на стабильное психическое состояние, качество ремиссии следует признать невысоким, так как социальное функционирование большинства больных существенно ограничено. В каждую из групп были включены по 20 пациентов, ранее принимавших
галоперидол. Остальные 20 больных в 1-й группе до включения в исследование принимали оланзапин; во 2-й группе 9 пациентов в качестве терапии до исследования получали рисперидон, 11 пациентов – кветиапин (табл. 2).

Средняя доза арипипразола в 1-й группе достигала 13,2±1,7 мг/сут, оланзапина во 2-й группе – 8,4±1,6 мг/сут. Клинически были дифференцированы два варианта ремиссии больных: дефицитарное состояние с остаточными продуктивными симптомами (17 пациентов в 1-й группе и 22 пациента во 2-й группе) и без таковых (23 пациента в 1-й группе и 18 пациентов во 2-й группе) [18].
Психопатологические проявления дефекта без продуктивных симптомов составляли симптомы редукции энергетического потенциала и эмоционального дефицита.
Доминировали жалобы на ощущение физической и психической слабости, быстрой утомляемости, снижение инициативности, способности самостоятельно принимать решения, планировать. Самостоятельная деятельность больных не превышала 2–3 ч в сутки и ограничивалась монотонной однообразной работой по дому.
При осмотре выявлялись мимическое, речевое и эмоциональное обеднение, снижение круга интересов, социальных контактов, когнитивные расстройства (формальность, амбивалентность, трудности в формулировании ответов, сосредоточения, концентрации внимания, снижение памяти).
У больных с остаточной продуктивной симптоматикой (не определявшей в целом клиническую картину и поведение пациентов) на фоне тех же симптомов редукции энергетического потенциала обнаруживались изолированные ретроспективные монотематические бредовые убеждения, которые относились, как правило, к отдельным событиям отдаленного прошлого (подозрительность только в определенной ситуации или по отношению к конкретному человеку, персекуторная оценка единственного события
и т.п.). Аффективный фон все пациенты оценивали как «обычный», «привычный» для них, «неизмененный».
Исходно средний балл по шкале PANSS составил 94,7±2,7 и 90,9±3,8 в 1 и 2-й группах (p<0,05), по подшкале негативных расстройств – 28,5±8,1 и 27,3±4,9 балла соответственно (p<0,05). Средний исходный балл по шкале SANS достигал 86,1±6,3 и 82,5±4,7 балла соответственно. Таким образом, сходство пациентов обеих групп по основным социодемографическим и клинико-динамическим показателям позволяет рассчитывать на валидность полученных данных.
Эффективность терапии
Положительная динамика в состоянии пациентов отмечалась в обеих группах (рис. 1). Улучшение состояния по шкале PANSS при приеме арипипразола (Амдоала)
достигало 25,4%, оланзапина (Парнасана) – 25,2% (разница недостоверна).
При оценке влияния терапии на клиническую картину двух клинических вариантов дефекта установлены следующие общие для обоих препаратов эффекты. Так, положительная динамика состояния у больных с неполной ремиссией без остаточной продуктивной симптоматики при приеме и арипипразола (Амдоала) и оланзапина (Парнасана) реализовалась уменьшением интенсивности психической и физической утомляемости, «анергии», трудности сосредоточения, когнитивных расстройств. Постепенно увеличивалась эмоциональная вовлеченность больных в общение с близкими, в события не только собственной, но и общественной жизни, расширялся круг общения и интересов. Пациенты задумывались о возможности трудоустройства. Однако к концу исследования у больных сохранялись мотивационные и волевые расстройства, не позволившие ни одному из неработающих пациентов устроиться на работу.
При терапии дефицитарных состояний с остаточными продуктивными симптомами, помимо описанного выше положительного влияния на астено-когнитивные и эмоциональные расстройства, удалось достичь некоторого снижения выраженности бредовых ретроспекций. Так, в части (29 из 39 пациентов) случаев больные начинали подвергать сомнению свою прежнюю патологическую интерпретацию событий, менее болезненно реагировали на упоминания или воспоминания о них и даже пытались сами инициировать обсуждение их с врачом и членами семьи.
В то же время следует отметить, что у 10 пациентов с остаточными продуктивными симптомами из 1-й группы на фоне оживления эмоциональности и побуждений отмечалось увеличение реактивной лабильности, тревожно-ипохондрических фобий без усиления психотической симптоматики (рис. 2).

При дифференцированной оценке влияния терапии арипипразолом (Амдоалом) и оланзапином (Парнасаном) на негативные расстройства по шкале SANS также установлено, что достоверные отличия (p<0,001) в спектре действия препаратов касаются таких симптомов, как моторное обеднение, бедность словарного запаса, способность к самообслуживанию и активность в свободное время – для арипипразола, взаимопонимание и доверие с родными, снижение рабочей продуктивности – для оланзапина (рис. 3).
Согласно когнитивным тестам среднее улучшение состояния больных было сопоставимо и составляло 19,1% от исходного в 1-й группе и 18,3% – во 2-й группе. Однако динамика результатов тестов в 2 группах носила не единообразный характер (представлена на примере теста Струпа); табл. 3. Так, в 1-й группе улучшение фиксировалось уже на визите М1 и постепенно увеличивалось к концу исследования. Во 2-й группе выраженность когнитивных расстройств в первые 2 мес (М1 и М2) незначительно увеличивалась, а затем начала прогрессивно снижаться.

С большой долей вероятности речь идет о проявлениях седативного эффекта оланзапина [19–21].
Отдельной оценки заслуживает влияние терапии на негативные и когнитивные расстройства у пациентов, переведенных с терапии типичными (галоперидол) и атипичными антипсихотиками на препараты исследования.
В случаях предшествующего приема галоперидола в первые 2 мес выраженность негативных и когнитивных расстройств существенно уменьшалась, затем скорость нарастания терапевтического эффекта снижалась и вновь нарастала к концу 6-го месяца лечения. При смене терапии с других атипичных антипсихотиков на арипипразол
(Амдоал) и оланзапин (Парнасан) нивелирование негативных расстройств носило плавно-поступательный характер на всем протяжении исследования (рис. 4).
Данный эффект при отмене галоперидола может быть отчасти объяснен редукцией в первые месяцы «вторичных» негативных расстройств (что подтверждается соответствующей динамикой средних баллов по шкалам HADS и Симпсона–Ангуса) и нарастанием положительного влияния арипипразола и оланзапина на «первичные» дефицитарные расстройства с течением времени. Такое объяснение находит подтверждение в результатах других клинических исследований [18, 22, 23].
Переносимость терапии
Переносимость терапии в используемых дозировках была хорошей. На это косвенно указывает тот факт, что ни один пациент не выбыл из исследования до его завершения. Возникавшие НЯ носили дозозависимый и/или транзиторный характер и разрешались самостоятельно или при уменьшении дозы препарата. Достоверно чаще НЯ развивались в 1-й месяц приема препаратов при первичном назначении препаратов в максимальной дозировке. В то же время спектр НЯ у арипипразола и оланзапина отличался, что, очевидно, объясняется рецепторными профилями препаратов (табл. 4).В 1-й группе НЯ отмечены у 19 (47,5%) пациентов, во 2-й группе – у 25 (62,5%). Наиболее частыми НЯ арипипразола являлись усиление тревоги, возбуждение, уменьшение продолжительности сна, оланзапина – гиперсомния, снижение либидо и ЭПР. При этом в 1-й группе дополнительное временное назначение корректоров ЭПР не потребовалось ни разу, во 2-й группе – у 17 (42,5%) пациентов.
По показателю изменения массы тела пациенты обеих групп существенно отличались: за 6 мес терапии в 1-й группе в целом отмечена тенденция к снижению массы тела (-1,9 кг), увеличение (+2,9 кг) зарегистрировано у 3 пациентов. Во 2-й группе, напротив, средняя масса тела увеличивалась, превышая на визите М6 7% от исходной у 12 больных.
Статистически значимых отличий между группами по основным гемодинамическим показателям, уровню липидов и глюкозы в крови не выявлено. Все изменения исходных значений уровня холестерина, липопротеидов низкой и высокой плотности, глюкозы не выходили за рамки установленных физиологических норм.
Качество жизни
Эффективность и безопасность психофармакотерапии оказывают существенное влияние на качество повседневного функционирования больного. Повседневное функционирование пациентов (шкала GAF; рис. 5) в 1-й группе улучшилось на 55,6% от исходного vs 42,8% в группе сравнения (р<0,001). Основываясь на жалобах пациентов, можно предположить, что разница между показателями обусловлена преимущественно частотой возникновения и выраженности НЯ оланзапина.
Заключение
В ходе натуралистического открытого сравнительного перекрестного фармакотерапевтического исследования подтверждена эффективность среднесрочной (24 нед) терапии атипичными антипсихотиками больных шизофренией с клинически отличающимися вариантами неполной лекарственной ремиссии. Установлено, что клиническими предикторами наибольшей эффективности применения арипипразола (Амдоала) является отсутствие резидуальной продуктивной симптоматики, в то время как для оланзапина, наоборот, наличие остаточных продуктивных симптомов в структуре дефекта.Скорость и динамика развития антинегативного (в отношении «первичных» и «вторичных» негативных расстройств) и прокогнитивного эффекта атипичных нейролептиков определяются не только механизмами рецепторного взаимодействия, но и характером предшествующей терапии и ее переносимости. Так, частичный агонист
D2-дофаминовых рецепторов арипипразол (Амдоал) может рассматриваться в качестве альтернативы нейролептикам, лечение которыми ассоциировано с жалобами на седацию и гиперсомнию, а также у пациентов с избыточной массой тела и/или тенденцией к ее увеличению, сахарным диабетом, сердечно-сосудистыми заболеваниями при наличии склонности к развитию ЭПР.
Полученные данные в практическом плане позволяют осуществлять более дифференцированный подход к назначению современных антипсихотиков с целью повышения эффективности и приверженности длительной терапии, сокращения финансовых затрат (на смену терапии, повторные госпитализации), повышения ресоциализации хронических больных шизофренией. Положительный субъективный опыт и отношение к антипсихотику сильно коррелируют с комплаентностью и благоприятным долговременным прогнозом.
Сведения об авторах
Медведев Владимир Эрнстович – канд. мед. наук, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПК МР ФГБОУ ВПО РУДН. E-mail: melkorcord@mail.ruФролова Вероника Игоревна – канд. мед. наук, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПК МР ФГБОУ ВПО РУДН
Тер-Исраелян Алексей Юрьевич – канд. мед. наук, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПК МР ФГБОУ ВПО РУДН, глав. врач МБУЗ ГПБ №13 г. Москвы
Гушанская Екатерина Владимировна – канд. мед. наук, доц. каф. психиатрии, психотерапии и психосоматической патологии ФПК МР ФГБОУ ВПО РУДН, зав. отд-нием МБУЗ ГПБ №13 г. Москвы
Список исп. литературыСкрыть список1. Jindal RD, Keshavan MS. Classifying antipsychotic agents. Need for new terminology. CNS Drugs 2008; 12: 1047–59.
2. Leught S et al. Second-generation vs first-generation antipsychotic drugs for schizophrenia: a meta-analysis. The Lancet 2009; 373: 31–41.
3. Sung-Wan Kim et al. Эффективность перехода на арипипразол с других атипичных антипсихотиков при лечении шизофрении. Психиатр. и психофармакотер. им. П.Б.Ганнушкина. 2010; 5: 30–4.
4. Иванов С.В. Клинические характеристики атипичных антипсихотиков: результаты сравнительных исследований при шизофрении. Психиатр. и психофармакотер. им. П.Б.Ганнушкина. 2012; 2: 9–19.
5. Комосса К., Румель-Клюге К., Гунгер Х. и др. Оланзапин в сравнении с другими атипичными антипсихотиками при лечении шизофрении. Соц. и клин. психиатрия. 2011; 3: 106–9.
6. Davis JM et al. A meta-analysis of the efficacy of second-generation antipsychotics. Arch Gen Psichiat 2003; 60 (6): 553–64.
7. Haro JM et al. SOHO Study Group. Three-year antipsychotic effectiveness in outpatient care of schizophrenia: observational vs randomized studies results. Eur Neuropsychopharmacol 2007; 17 (4): 235–44.
8. Цыганков Б.Д., Агасарян Э.Т. Анализ эффективности и
безопасности современных и классических антипсихотических препаратов. Журн. неврол. и психиатр. им. С.С.Корсакова. 2010; 9: 64–70.
9. Haslemo T et al. The effect of variable cigarette consumption on the interaction with clozapine and olanzapine. Eur J Clin Farmacol 2006; 62: 1049–53.
10. Бобров А.Е., Мутных Е.М., Краснослободцева Л.А. Сравнение антипсихотиков (кветиапина, арипипразола и галоперидола): терапевтическая динамика психопатологической и нейрокогнитивной симптоматики у больных шизоаффективными расстройствами. Психиатр. и психофармакотер.
им. П.Б.Ганнушкина. 2014; 1: 39–43.
11. Медведев В.Э. Лечение шизофрении современными атипичными антипсихотическими препаратами (уч.-метод. пособие). М.: Конти-Принт, 2014.
12. Lieberman JA et al. Effectiveness of antipsychotic drugs in patients with chronic schizophrenia. N Engl J Med 2005; 353: 1209–23.
13. Данилов Д.С. Современные классификации антипсихотических средств и их значение для клинической практики (современное состояние вопроса и его перспективы). Обозрение психиатрии и мед. психологии. 2010; 3: 36–42.
14. Дробижев М.Ю., Овчинников А.А. Антипсихотики: меняем старые поколения на новую классификацию? Соц. и клин. психиатрия. 2010; 2: 80–6.
15. Jody D, McQuade R, Kujawa M et al. Long-term weight effects of Aripiprazole vs olanzapine. Schizophrenia Research 2004; 1: 187.
16. Stahl S. Essenctial psychopharmacology. Cambridge 2013.
17. Kapur S et al. 5-HT2- and D2-receptor occupancy of olanzapine in schizophrenia: a PET investigation. Am J Psychiat 1998; 155: 921–8.
18. Морозова М.А., Бениашвили А.Г., Рубашкина В.В. Шизофренический дефект в качестве терапевтической мишени (исследование терапевтической динамики неполной ремиссии у больных приступообразно-прогредиентной шизофренией). Психиатр. и психофармакотер. им. П.Б.Ганнушкина. 2006; 4: 59–64.
19. Ястребов Д.В. Терапия современными антипсихотическими препаратами. Особенности применения оланзапина. Психиатр. и психофармакотер. им. П.Б.Ганнушкина. 2012; 5: 24–8.
20. Beasley CM Jr et al. All-cause treatment discontinuation in schizophrenia during treatment with olanzapine relative to other antipsychotics: an integrated analysis. J Clin Psychopharmacol 2007; 27 (3): 252–8.
21. Hindmarch I. Оценка негативного влияния психофармакологических лекарственных средств на когнитивные функции. Психиатр. и психофармакотер. им. П.Б.Ганнушкина. 2008; 5: 32–8.
22. Данилов Д.С., Магомедова Д.О. Опыт перевода с клозапина на арипипразол больных приступообразными формами шизофрении в период лекарственной ремиссии. Психиатр. и психофармакотер. им. П.Б.Ганнушкина. 2013; 6: 23–9.
23. Медведев В.Э., Фролова В.И., Гушанская Е.В., Тер-Исраелян А.Ю. Оценка эффективности и переносимости купирующей терапии атипичными и типичными нейролептиками при шизофрении. Психиатр. и психофармакотер. им. П.Б.Ганнушкина. 2014; 1: 25–35.
24. Медведев В.Э. Возможность и оправданность перевода на атипичные антипсихотики больных шизофренией. Психиатр. и психофармакотер. им. П.Б.Ганнушкина. 2013; 5: 23–8.
7 ноября 2014
Количество просмотров: 2883


