Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№03 2015
Терапевтическая «ниша» Афобазола в психиатрической практике: обоснование №03 2015
Номера страниц в выпуске:39-48
Проведен обзор литературы, обобщающий имеющиеся данные о механизмах действия Афобазола и его фармакологических свойствах, установленных в экспериментальных и доказательных клинических исследованиях. Определена характеристика психопатологических состояний, при которых применение препарата является оптимальным.
Ключевые слова: анксиолитик, Афобазол, фабомотизол, фармакодинамика, тревожные расстройства, s1-рецепторы, терапевтическая эффективность.
sjunja@bk.ru
Проведен обзор литературы, обобщающий имеющиеся данные о механизмах действия Афобазола и его фармакологических свойствах, установленных в экспериментальных и доказательных клинических исследованиях. Определена характеристика психопатологических состояний, при которых применение препарата является оптимальным.
Ключевые слова: анксиолитик, Афобазол, фабомотизол, фармакодинамика, тревожные расстройства, s1-рецепторы, терапевтическая эффективность.
sjunja@bk.ru
Для цитирования: Сюняков Т.С., Сюняков С.А., Незнамов Г.Г. Терапевтическая «ниша» Афобазола в психиатрической практике:
обоснование. Психиатрия и психофармакотерапия. 2015; 17(3): 39–48.
Afobazole therapeutic niche: the reasoning
T.S.Syunyakov, S.A.Syunyakov, G.G.Neznamov
V.V.Zakusov Institute of Pharmacology. 125315, Russian Federation, Moscow, ul. Baltiiskaia, d. 8, str. 1
This paper is the review of the literature on fabomotizole pharmacodynamics and pharmacological action in experimental and clinical studies. The characteristics of target psychiatric conditions is given in which the effectiveness of drug is optimal.
Key words: anxiolytic, Afobazole, fabomotizolum, pharmacodynamics, anxiety disorders, s1-receptors, effectiveness.
sjunja@bk.ru
For citation: Syunyakov T.S., Syunyakov S.A., Neznamov G.G. Afobazole therapeutic niche: the reasoning. Psychiatry and psychopharmacotherapy. 2015; 17(3): 39–48.
Анксиолитик Афобазол, производное 2-меркаптобензимидазола, является одним из наиболее востребованных и успешных современных отечественных препаратов, объемы продаж которого увеличиваются в последние годы. Подобная популярность де-факто связана с тем, что он одним из первых применяется среди пациентов, нуждающихся в коррекции эмоционального состояния. Однако такое широкое применение неизбежно приводит к возникновению вариабельности результатов терапии и поляризации отношения к препарату. Вместе с тем разброс мнений в плане общей оценки Афобазола как эффективного препарата и в отношении его места в терапии тревожных расстройств отмечается и в профессиональной среде. Так, существует множество публикаций относительно высокой эффективности Афобазола при тревожных расстройствах в психиатрии и психосоматике [1–12], но имеются и критические позиции [13, 14]. Наконец, в одних работах Афобазол рекомендуется в качестве средства выбора при определенных тревожных расстройствах [15], тогда как в других ему отводятся второстепенные роли [16]. Наряду с этим Афобазол включен в реестры Всемирной организации здравоохранения (ВОЗ) под международным непатентованным названием фабомотизол, а также в Анатомо-терапевтическо-химическую классификацию ВОЗ в группу анксиолитических средств под собственным кодом N05BX04, и относится к числу немногих отечественных препаратов с установленными нейрорецепторными механизмами действия.
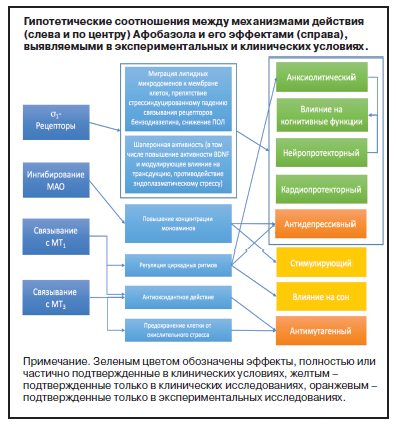
Задачей данной публикации явилась необходимость обобщить доказательные данные с тем, чтобы продемонстрировать соотношения между механизмами действия Афобазола и его основными эффектами, выявляющимися в экспериментальных и клинических исследованиях, и показать принципиальные терапевтические возможности применения препарата при разных психопатологических состояниях, при которых в терапевтических дозах его позитивное действие проявляется наиболее оптимально.
Механизмы действия Афобазола
В работе М.В.Воронина и С.Б.Середенина [17] обобщены результаты проведенного в лаборатории «Cerep» изучения взаимодействия Афобазола с широким кругом рецепторов и его экспериментальных исследований, которые вместе свидетельствуют о том, что препарат является агонистом s1-рецепторов, мелатониновых МТ1- и МТ3-рецепторов и обладает обратимым ингибирующим действием на моноаминоксидазу типа А (МАО-А).
Активированные s1-рецепторы за счет шаперонной активности1 противодействуют нарушениям правильной укладки белковых молекул при эндоплазматическом стрессе (ER-стрессе), вызванном ишемией или усилением перекисного окисления липидов (ПОЛ), влияют на внутриклеточное содержание ионов кальция, способствуют миграции липидных микродоменов к мембране клеток, противодействуя ее повреждениям в результате процессов перекисного окисления, и модулируют процессы передачи сигнала, в том числе за счет препятствия стресс-индуцированному падению связывания в бензодиазепиновом участке ГАМК-А-рецепторов [17–26]. Эти уникальные свойства s1-рецепторов обусловливают широкий круг свойств их агонистов, проявляющихся в отношении органов с их максимальной экспрессией, – головного мозга и миокарда. В экспериментальных и клинических условиях у агонистов s1-рецепторов выявляются анксиолитические [27], нейропротекторные [23, 24], кардиопротекторные [28, 29], прокогнитивные [30–32] и антидепрессивные [22, 30] свойства. Механизм анксиолитического действия Афобазола авторами препарата объясняется прежде всего его способностью предотвращать стресс-индуцированное падение связывающей способности бензодиазепинового участка ГАМК-А-рецептора [17].
Стимуляция МТ1-рецепторов сопряжена с регуляцией синхронизации циркадных ритмов [33], а у их лигандов выявляется антидепрессивное [34, 35], анксиолитическое [36, 37] и хронобиологическое [35, 38] действие. Рецепторы МТ3 представляют собой фермент хинонредуктазу 2-го типа и предохраняют клетки от окислительного стресса [39], а у их агонистов выявлены антимутагенные и антидепрессивные свойства [40]. Ингибиторы МАО повышают концентрацию моноаминов в синаптической щели и обладают антидепрессивным и стимулирующим эффектами [41–43]. Вместе с тем имеются экспериментальные данные о наличии у них и анксиолитических свойств [44, 45].
Таким образом, при проведении сопоставления первичных механизмов действия Афобазола (см. рисунок) и потенциально ассоциирующихся с ними фармакологических эффектов принципиальное значение имеет тот факт, что обнаруженные рецепторные «мишени» фабомотизола потенциально могут, и это неоднократно подчеркивалось исследователями, обусловливать основные эффекты препарата, выявляемые в экспериментальных и клинических условиях. При этом необходимо отметить, что в реализации отдельных фармакологических эффектов Афобазола гипотетически имеет место взаимодействие нескольких механизмов.
Ниже будет приведена доказательная база существования параллелизма между эффектами Афобазола, выявляемыми в экспериментальных работах и при его клиническом применении.
Экспериментальные данные о фармакологических свойствах Афобазола

В исследованиях на животных подтверждены адекватные профилю нейрорецепторных взаимодействий анксиолитические, нейро- и кардиопротекторные, антидепрессивные и антимутагенные свойства фабомотизола (см. рисунок).
Анксиолитическое действие Афобазола продемонстрировано на моделях «конфликтной ситуации», «открытого поля», «приподнятого крестообразного лабиринта». Оно характеризуется выраженной избирательностью (седативный и миорелаксантный эффекты не реализуются даже при введении препарата внутрь в дозе, в 20 раз превышающей среднюю терапевтическую) и реализуется селективно у экспериментальных животных с «пассивным» фенотипом эмоционально-стрессовой реакции [46–49].
Нейропротекторные свойства Афобазола доказаны в условиях ишемического и геморрагического повреждения головного мозга и на модели спинальной травмы: препарат уменьшает объем поражения головного мозга [50] и смертность животных [51, 52], восстанавливает возбудимость и деятельность рефлекторных центров спинного мозга [53]. При его введении снижаются содержание продуктов свободно-радикального окисления и активность каталазы [54] и повышается содержание стресс-белка HSP70 [55], нейротрофинов BDNF и NGF [56, 57]. Афобазол оказывает положительное цереброваскулярное действие [58–60], повышает выживаемость нейронов в условиях оксидативного стресса и глутаматергической эксайтотоксичности [61], улучшает обучаемость и неврологические функции, нарушенные в постинсультном периоде [51].
Афобазол повышает адаптационные способности сердечной мышцы после инфаркта [62], проявляет выраженное противофибрилляторное действие на моделях электрической фибрилляции сердца [63], аритмии, вызванной высокими дозами хлорида кальция [64], и при реперфузионном повреждении [65], уменьшает площадь ишемического повреждения сердца, стимулирует репаративные процессы в миокарде и препятствует постинфарктному ремоделированию левого желудочка [66].
У беспородных крыс Афобазол оказывал антидепрессивное действие в тестах Porsolt и Nomura, о чем свидетельствует сокращение под его действием периодов неподвижности животных, связанных с выученной беспомощностью [67].
Наконец, Афобазол при однократном и 5-дневном (совместном и предварительном) введении предупреждает или значимо снижает мутагенные и тератогенные эффекты диоксидина и циклофосфамида у мышей и крыс [68].
Фармакологические эффекты Афобазола, выявляемые в клинических условиях
Основные психофармакологические эффекты Афобазола, выявляемые у больных с тревожными расстройствами
Спектральные характеристики психотропного действия Афобазола были изучены уже в ранних клинических исследованиях2 с применением специального подхода, позволяющего оценивать особенности психотропного действия препарата3. Представляется важным, что в рамках этого подхода использовался дизайн исследований с приемом плацебо в течение 7 дней до назначения Афобазола для элиминации плацебо-чувствительных больных. В первом, проводимом в рамках II фазы клинико-фармакологическом исследовании Афобазола [69], основываясь на полученных в эксперименте данных о реализации анксиолитического эффекта препарата у стресс-неустойчивых особей, в качестве фармакологической «мишени» были выбраны больные с ситуационно обусловленными тревожными и тревожно-астеническими расстройствами в рамках диагностических рубрик по МКБ-10 «Генерализованное тревожное расстройство» – F41.1 (10 больных) и «Неврастения» – F48.0 (20 больных), с наличием преморбидных особенностей личности астенического круга. Впервые полученные на клиническом материале данные свидетельствовали о том, что у больных с «простыми» по структуре тревожными и тревожно-астеническими расстройствами и преморбидными личностными чертами астенического полюса препарат проявляет анксиолитическое действие. При этом анализ показателей шкалы оценки тревоги Гамильтона свидетельствует о совокупной обратной динамике как компонента психической, так и соматизированной тревоги. Также было установлено, что спектр клинико-фармакологического действия Афобазола не исчерпывается анксиолитическим эффектом, сочетаясь в том же дозовом диапазоне со стимулирующим действием, реализующимся в виде влияния на повышенную истощаемость, сонливость, апатию и пониженное настроение. При этом были показаны наличие у препарата вегетонормализующего действия и отсутствие собственно гипнотического эффекта при регистрируемой у изученных больных нормализации ночного сна, вероятно, вследствие положительных изменений других показателей состояния больных.
При последующем изучении [7, 71] было показано, что анксиолитический, стимулирующий и вегетонормализующий эффекты, а также позитивное влияние на нарушения ночного сна у больных с тревожными расстройствами проявляются с первых дней курсового применения Афобазола вне зависимости от преморбидных особенностей личности. Однако у больных с чертами личности стенического полюса был выявлен относительно более выраженный активирующий эффект, проявляющийся и при однократном приеме тестовой дозы, и при курсовом применении. То есть в клинических условиях у больных со стеническими преморбидными особенностями более отчетливо проявляется стимулирующий компонент действия препарата. Эта закономерность отличает препарат от бензодиазепинов, она более характерна для препаратов со стимулирующим действием [70].
Необходимо отметить, что в этих исследованиях наличие анксиолитического и активирующего компонентов действия Афобазола было объективизировано при помощи анализа изменений электроэнцефалограммы (ЭЭГ) при действии тестовой дозы Афобазола, однако у больных с преморбидными личностными чертами астенического, стенического полюсов и смешанными характеристиками выявлены различия этих изменений, наиболее четко вырисовывающиеся в сравнении с эффектами плацебо и выраженные в диапазоне частот d- и a-ритмов. У больных с астеническими личностными чертами отмечалось повышение энергии частот d-ритма 3–3,5 Гц и представленности низких частот a-ритма, тогда как при наличии стенических черт выявлялись снижение энергии d-ритма 0,5–1,5 Гц и увеличение представленности высоких частот a-ритма. Полученные результаты свидетельствуют о связи изменений ЭЭГ при действии тестовой дозы Афобазола с исследуемыми личностными чертами больных. Эти данные сопоставимы с проявлениями анксиолитического и активирующего эффектов анксиолитиков и стимуляторов соответственно. У больных с астеническими личностными чертами отмечалась ЭЭГ-реакция транквилизирующего типа без признаков неспецифической седации или активации, а у больных с чертами стеничности – отражение в изменениях ЭЭГ-стимулирующего эффекта с признаками неспецифической активации.
Таким образом, при изучении спектральных характеристик у Афобазола выявлены анксиолитический, стимулирующий (проявляющийся во влиянии на астеническую симптоматику, уровень бодрствования/дневной сонливости и настроение), вегетостабилизирующий эффекты и положительное влияние на расстройства ночного сна, которые были подтверждены и в последующих исследованиях [72]. Кроме того, во всех исследованиях, в которых использовалась шкала оценки тревоги Гамильтона, были подтверждены данные о совокупном влиянии Афобазола как на психические, так и соматические проявления тревоги [1–6, 9, 73].
Вегетостабилизирующее действие
В дополнение к приведенным данным о наличии вегетостабилизирующего действия в спектре психотропной активности Афобазола оно было подтверждено и при специальном изучении: у больных гипертонической болезнью, протекающей коморбидно с паническим расстройством, при анализе вариабельности артериального давления (АД). По результатам применения препарата у пациентов с исходно повышенной вариабельностью АД наблюдалось ее снижение, что, по данным авторов, свидетельствует о нормализации вегетативных механизмов в поддержании гомеостаза и регуляции АД и в свою очередь способствует уменьшению риска поражения органов-мишеней у пациентов с гипертонией [74]. Кроме того, при сравнительном изучении Афобазола и тофизопама (по 30 пациентов в каждой группе) [75] терапия обоими препаратами ассоциировалась с улучшением функционирования вегетативной нервной системы по показателям, оцениваемым при помощи методики исследования резервных функциональных возможностей организма с помощью спектрального анализа ритма сердца и показателей АД и частоты сердечных сокращений в покое и при проведении активной ортопробы с оценкой деятельности сегментарных и надсегментарных структур вегетативной регуляции. Вместе с тем, при применении Афобазола достоверное снижение симпатикотонии и повышение парасимпатических влияний происходили в более ранние сроки, чем при применении тофизопама (через 2 и 4 нед соответственно).
В дополнение к этому, в еще одной работе [76] были получены данные о том, что длительное применение Афобазола в составе комплексной кардиотропной терапии при гипертонической болезни приводило к существенному увеличению в сравнении с контрольной группой (только кардиотропная терапия) доли больных с редкой частотой возникновения кризов (1 раз в год или реже). При этом в основной группе наблюдалось 2-кратное сокращение частоты госпитализаций в долгосрочной перспективе (в течение 1 года после начала исследования).
Влияние на нарушения сна
Влияние Афобазола на нарушения сна стало предметом специального исследования [77]. В этой работе показано, что применение монотерапии Афобазолом в однократной суточной дозе 20 мг, применяемой за 30–40 мин до сна, у больных с инсомнией неорганической природы (n=30) положительно влияло на все параметры сна, оцениваемые валидными методиками. Так, через 10 дней терапии доля больных с «большой» или «очень большой» продолжительностью засыпания сократилась с 81% до примерно4 7%, с «минимальной» или «небольшой» продолжительностью сна – с 77 до 46%, с «частой» и «очень частой» частотой пробуждений – с 87 до примерно 7%. При этом доля пациентов с «высоким» или «очень высоким» качеством сна увеличилась с 0% до примерно 72%, продолжительность сна увеличилась с примерно 4,3 ч почти до 7 ч, а соотношение между общей продолжительностью нахождения в постели и общим временем сна существенно возросло. При этом авторы указывают, что добавление второго приема Афобазола или его заблаговременный (за 1–3 ч до сна) прием не приводили к столь выраженному улучшению качества ночного сна.
Данная работа представляет интерес тем, что она гипотетически позволяет предполагать возможность связи положительного влияния Афобазола на нарушения ночного сна как агониста МТ1-рецепторов с его хронобиологическим действием, проявляющимся, несмотря на отсутствие у препарата гипноседативных свойств и наличие стимулирующего компонента действия.
Влияние на пониженное настроение
Обнаружено несколько работ, в которых Афобазол применялся при тревожно-депрессивных состояниях, однако представленный материал не позволяет сделать каких-либо определенных выводов о наличии в спектре психотропной активности значимого антидепрессивного действия, так как верифицированного качественного изучения Афобазола при клинически очерченных депрессивных или тревожно-депрессивных состояниях не проводилось. Но как было указано выше, у Афобазола выявлено положительное влияние на вторичные расстройства настроения (гипотимию) в структуре тревожного синдрома.
Нейропротекторное действие Афобазола и его влияние на когнитивные функции у пациентов и здоровых добровольцев
Изучение влияния Афобазола на когнитивные функции проводилось на здоровых добровольцах и выборках больных с разными тревожными расстройствами с применением методик психофизиологического тестирования и методики для оценки интеллекта Векслера [78, 79]. Кроме того, изучалось влияние Афобазола на показатели Краткой шкалы исследования психического статуса (MMSE) у больных, перенесших ишемический инсульт [11, 80]. При этом целенаправленное изучение влияния на когнитивное функционирование проводилось лишь у здоровых добровольцев, у которых применение Афобазола в течение нескольких последовательных дней приводило к достоверному улучшению психофизиологических параметров скорости простой зрительно-моторной реакции и распределения внимания [79]. У больных с тревожными расстройствами по результатам курсовой 2-недельной терапии было выявлено позитивное влияние препарата на психофизиологические показатели объема, распределения и устойчивости внимания [71]. Исследование влияния 14-дневного применения Афобазола на результативность когнитивного функционирования по методике Векслера у больных со структурно «простыми» тревожными расстройствами (генерализованное тревожное расстройство) продемонстрировало статистически достоверное улучшение показателей по субтестам «Шифровка» и «Недостающие детали», что указывает на повышение продуктивности процессов концентрации и распределения внимания, увеличение объема кратковременной памяти, позитивные изменения скорости и точности зрительно-моторной координации, улучшение результатов дифференцировки существенного от второстепенного [78]. Вместе с тем при «сложных» тревожных расстройствах (тревожно-фобические и тревожно-ипохондрические расстройства), при которых Афобазол оказался неэффективен, достоверных изменений показателей продуктивности когнитивной деятельности в процессе терапии обнаружено не было. Эти данные свидетельствуют о том, что улучшение неглубоких нарушений когнитивного функционирования при применении Афобазола является скорее вторичным по отношению к реализации основных терапевтических эффектов у данного контингента больных (анксиолитического и стимулирующего).
Наряду с этим применение Афобазола в дозе 30 мг в день длительностью 30 дней изучалось у 30 больных пожилого возраста (средний возраст 67,4±2,9 года), перенесших (до 1 года после окончания острого периода) ишемический инсульт в каротидном бассейне [11]. У этих больных отмечалось значимое улучшение показателей ориентации, восприятия, внимания и памяти, оцениваемых при помощи MMSE. Данные изменения оказались сопряжены с увеличением линейной средней скорости кровотока в отдельных интракраниальных сосудах пораженного каротидного бассейна, а также с положительной динамикой частотно-амплитудных показателей ЭЭГ в виде уменьшения интенсивности в диапазоне медленных ритмов (d- и θ-) и увеличения в диапазоне a-ритма. Вместе с тем результаты данного исследования демонстрируют скорее вторичное по отношению к нейропротективному «прокогнитивное» действие Афобазола. На это же указывают результаты другого исследования [80], в рамках которого препарат применялся в течение 12 нед в дозе 30 мг в день у 30 больных, перенесших инсульт. Демонстрацией нейропротективного действия Афобазола в данной работе стало достижение качественной ремиссии у всех пациентов, получавших стандартную терапию и Афобазол, в сравнении с 46,7% в контрольной группе (только стандартная терапия, также 30 пациентов).
В качестве комментария следует отметить, что когнитивные нарушения у больных с тревожными и органическими нарушениями носят качественно различный характер, однако в обоих случаях их нарушения складываются из влияния собственно психического состояния (т.е. искажения когнитивного функционирования – так называемая «горячая» дисфункция когнитивного функционирования), с другой – из влияния физического нарушения активности нейрональных систем (очаг некроза, снижение нейрональной пластичности в результате активации перекисного окисления, нейродегенерации и других причин). Таким образом, вне зависимости от генеза когнитивных нарушений улучшение когнитивного функционирования и психоневрологического статуса больных под влиянием Афобазола является сложносоставным эффектом в результате его собственно нейропротекторного действия и положительных изменений эмоционального состояния.
Кардиопротекторное действие
Действие Афобазола в суточной дозе 30 мг было изучено у больных кардиологического профиля [10]. Положительное влияние на тяжесть сердечно-сосудистых расстройств зарегистрировано у больных (n=21) с пароксизмальной формой фибрилляции предсердий без выраженных структурных изменений. В сравнении с контрольной группой (n=20) применение Афобазола у них сопровождалось уменьшением частоты пароксизмов, длительности эпизодов аритмии, их более легкой переносимостью и тенденцией к трансформации в бессимптомную форму. В другом исследовании у больных с ишемической болезнью сердца и коморбидными тревожно-депрессивными расстройствами при применении препарата выявлено улучшение показателей по шкалам стабильности стенокардии на 44,3 и 38,4% у женщин и мужчин соответственно [81].
В рандомизированном исследовании [82] краткосрочное применение Афобазола (n=75) у больных с сердечно-сосудистыми заболеваниями (стабильная стенокардия напряжения, сердечные аритмии, гипертоническая болезнь) и повышенной тревожностью в условиях кардиологического стационара ассоциировалось с потенцированием скорости наступления и выраженности основных эффектов кардиотропной терапии (антиангинальной, антиаритмической, антигипертензивной), что отразилось в достоверном улучшении результатов мониторирования по Холтеру в сравнении с контрольной группой (n=70; кардиотропная терапия и однократные дозы феназепама либо валокордина/корвалола по требованию).
В остальных работах приводятся косвенные указания на кардиотропную эффективность Афобазола: в одном исследовании установлен кардиологически благоприятный профиль безопасности препарата без возникновения жизнеопасных аритмий и/или внутрисердечных блокад [9], в другом показана возможность путем присоединения Афобазола оптимизировать режим применения антигипертензивной терапии [83], в третьем – краткосрочный (10-дневный) прием Афобазола улучшил некоторые связанные со здоровьем параметры качества жизни у пациентов с гипертонической болезнью, но не с ишемической болезнью сердца [84]. В четвертом исследовании [85] изучалась эффективность добавления Афобазола к стандартной терапии у 19 больных, находящихся в остром периоде инфаркта миокарда (Афобазол добавлен 9 больным на 3–5-е сутки). У больных опытной группы в сравнении с контрольной (только стандартная терапия; n=10) через 30 дней терапии отмечались более высокие показатели удовлетворенности своим эмоциональным и социальным функционированием, активности и выносливости при выполнении физических нагрузок, меньшая тяжесть болевых ощущений. Вместе с тем в этих 4 публикациях не приведены данные о влиянии Афобазола на кардиологические показатели.
Исследования эффективности Афобазола
В 2012 г. был опубликован исчерпывающий систематический обзор клинических исследований Афобазола при разных тревожных расстройствах5 и протекающих коморбидно с тревогой соматических заболеваниях6 [15]. Основным выводом, который можно сделать по приведенным в обзоре данным, является то, что применение Афобазола эффективно и безопасно при купировании проявлений тревоги вне зависимости от их первичности или коморбидной взаимосвязи с соматической патологией. При этом следует учитывать, что купирующая эффективность терапии Афобазолом существенно варьирует в зависимости от структуры синдрома, достигая максимума при генерализованном тревожном расстройстве (вплоть до 89%) и снижаясь по мере усложнения психопатологического состояния. Эти данные принципиально соответствуют представлениям о терапевтической нише препарата, сформулированным по результатам как ранних [4, 71], так и более поздних исследований Афобазола [72], о его преимущественной эффективности при структурно простых тревожных и тревожно-астенических расстройствах, особенно при неврастении (F48.0), а также при аффективно-насыщенных чувственных фобиях, лишенных идеаторной переработки и метакогнитивных надстроек. При этих состояниях спектральные характеристики фармакологической активности препарата комплементарны основным проявлениям психопатологического синдрома. Недостаточная эффективность Афобазола выявляется при более комплексной структуре состояния, когда тревога сопряжена с расстройствами более глубоких психопатологических регистров: идеаторными (в том числе фобическими и/или ипохондрическими) расстройствами сверхценного или обсессивного круга. Другим важным наблюдением является то, что продолжительность психопатологического состояния является значимым предиктором результативности терапии Афобазолом: чем меньше длительность заболевания, тем выше вероятность высокой эффективности.
Это соотносится с данными о взаимосвязи длительности заболевания с содержанием малонового диальдегида (МДА) – маркера активности ПОЛ – в плазме крови больных разными тревожными расстройствами [72]. В свою очередь, содержание МДА достоверно коррелировало с выраженностью редукции психопатологических расстройств под влиянием терапии Афобазолом. При этом необходимо учитывать, что клеточное повреждение в результате ПОЛ является одним из важнейших механизмов прогрессирования и хронификации психических болезней [86, 87]. При этом Афобазол вызывал снижение концентрации МДА в плазме крови больных тревожными расстройствами [72], что соответствует экспериментальным данным о влиянии препарата на ПОЛ при моделировании ишемии головного мозга [54].
Заключение
Появление современных данных о нейрорецепторных взаимодействиях Афобазола инициировало целенаправленное изучение новых свойств препарата и в клинических, и в экспериментальных условиях. На рисунке в обобщенном виде отражены гипотетические представления о взаимосвязях между его механизмами действия и данными, полученными в экспериментальных и клинических исследованиях. Как видно, в отношении большей части фармакологических эффектов прослеживается параллелизм. Особенно важно подчеркнуть аналогию в особенностях реализации анксиолитического действия, которое наиболее полно реализуется у животных с пассивным фенотипом эмоционально-стрессовой реакции и пациентов с астеническими преморбидными личностными чертами [46–49, 69]. Вместе с тем в клинических условиях анксиолитическое действие в сочетании с выраженным стимулирующим наблюдалось и у больных с преморбидно стеническими личностными особенностями [7, 71], тогда как в экспериментальных условиях в тестах («приподнятый крестообразный лабиринт», «открытое поле» и «конфликтная ситуация») у животных с активным фенотипом эмоционально-стрессовой реакции оно не проявлялось [46–49]. Вероятно, это объясняется тем, что в указанных тестах у животных с активным фенотипом эмоционально-стрессовой реакции не развивались проявления эмоционального стресса. Однако в последующих исследованиях у мышей в более жестких условиях моделирования стресса при предъявлении хищника было выявлено падение связывающей способности бензодиазепинового участка ГАМК-А-рецептора вне зависимости от фенотипа эмоционально-стрессовой реакции. Афобазол препятствовал развитию нарушений функциональной активности бензодиазепиновых рецепторов и снижал поведенческие проявления стресса как у пассивных, так и активных в этом отношении линий животных [18]. Следует отметить, что данный эффект сопоставим с представлениями о свойствах агонистов s1-рецепторов. Таким образом, при наличии адекватных нейрорецепторным механизмам действия Афобазола нарушений анксиолитическое действие препарата проявлялось в равной степени и у животных, и у людей с тревожными расстройствами вне зависимости от стенической/астенической преморбидной структуры и устойчивости к эмоциональному стрессу.
Практически полное соответствие результатов экспериментальных и клинических исследований выявлено также в отношении нейро- и кардиопротекторного действия Афобазола, а также влияния Афобазола на повышенную при тревоге активность ПОЛ, в основе которых, как предполагается, также лежит агонизм препарата в отношении s1-рецепторов. Кроме того, взаимодействие потенциально связанных с данным механизмом нейропротекторного и анксиолитического эффектов гипотетически может лежать в основе реализации выявляемого в клинических условиях комплексного положительного влияния препарата на когнитивные функции.
Таким образом, в отношении анксиолитического, нейро- и кардиопротекторного эффектов Афобазола (а также комплексного положительного влияния на когнитивные функции) выявляется полное соответствие между данными о его рецепторном связывании и результатами экспериментальных и клинических исследований.
Вместе с тем у препарата имеется ряд свойств, которые выявлены либо только в экспериментальных, либо только в клинических условиях. Так, реализующееся у больных с простыми по структуре тревожными и тревожно-астеническими расстройствами стимулирующее действие [69, 71], гипотетически ассоциирующееся с ингибированием активности МАО типа А [43], не было напрямую продемонстрировано в исследованиях на животных. Наблюдаемое в тестах «приподнятый крестообразный лабиринт» и «открытое поле» повышение локомоторной активности животных [46–49], по мнению исследователей, является отражением анксиолитического, а не психостимулирующего эффекта препарата. Вместе с тем аналогичный эффект Афобазола в тестах Porsolt и Nomura [67] является экспериментальным подтверждением антидепрессивного действия, которое не было достаточно полно изучено в клинических условиях. Кроме того, выявленное влияние точного по времени назначения Афобазола на нарушения сна у больных с инсомниями неорганической природы [77] не нашло отражения в специальных экспериментальных исследованиях, однако оно гипотетически соотносится с хронобиологическими эффектами агонистов МТ1-рецепторов. Наконец, в клинических условиях не было изучено выявленное в работах на животных антимутагенное действие Афобазола [68].
Таким образом, в отношении большинства эффектов Афобазола, выявленных в экспериментальных и клинических условиях, установлен параллелизм, отражающий возможность трансляции механизмов действия и фармакологических эффектов из эксперимента в клинику. Более того, все выявленные к настоящему времени эффекты препарата соответствуют и могут быть объяснены его фармакодинамическими характеристиками. Эти данные подкрепляют и без того солидную доказательную базу терапевтических возможностей Афобазола. Вместе с тем во многих публикациях о проведенных исследованиях (в первую очередь это касается применения Афобазола при коморбидных с соматическими заболеваниями тревожных расстройствах) даются слишком размытые границы диагностических категорий, при которых Афобазол оказался эффективен. Это потенциально может порождать иллюзию того, что препарат эффективен при любых проявлениях тревоги. Так, по данным обзора С.В. Иванова (2012 г.) [15], в 13 из 19 проанализированных исследований не дается диагностических указаний в отношении состояния больных. При этом слишком широкое представление о противотревожном действии расширяет применение препарата на случаи, где он заведомо малоэффективен, а это может искажать представления о его терапевтических возможностях. В этой связи не лишним будет еще раз указать на то, что большинство исследователей единодушны в выводах относительно того, что Афобазол эффективен при простых по структуре тревожных и тревожно-астенических расстройствах и аффективно-насыщенных чувственных фобиях в рамках генерализованного тревожного расстройства, неврастении, расстройств адаптации, нозогенных реакций, когда тревога носит характер эмоции и лишена идеаторного компонента [15]. Включение в структуру тревожного синдрома обсессивных, ипохондрических и сверхценных расстройств, формирование устойчивой концепции болезни и прочих метакогнитивных надстроек сопряжено со снижением эффективности Афобазола.
1 Способствуют правильной пространственной укладке синтезируемых белков и образованию активных центров белковых молекул.
2 Исследования проводились в ФГБНУ НИИ фармакологии им. В.В.Закусова.
3 Подход основан на применении оригинальной методики группировки симптомов Шкалы оценки выраженности симптоматики и отражающих отдельные психотропные эффекты препаратов [4, 5].
4 Оценка производилась по приведенным в публикации графикам.
5 В обзор вошли исследования Афобазола при генерализованном тревожном расстройстве, расстройствах адаптации, тревожно-фобическом, ипохондрическом, соматоформном, паническом, посттравматическом стрессовом расстройствах, нозогенных реакциях и др.
6 В обзор вошли исследования Афобазола при ишемическом инсульте, инфаркте миокарда, гипертонической болезни, пароксизмальной форме фибрилляции предсердий, хроническом гастрите, хронической ишемии головного мозга, хроническом панкреатите, язвенной болезни двенадцатиперстной кишки, травмах опорно-двигательного аппарата.
Сведения об авторах
Сюняков Тимур Сергеевич – канд. мед. наук, ст. науч. сотр. лаб. фармакологической генетики ФГБНУ НИИ фармакологии им. В.В.Закусова. E-mail: sjunja@bk.ru
Сюняков Сергей Александрович – канд. мед. наук, вед. науч. сотр. лаб. клин. психофармакологии ФГБНУ НИИ фармакологии им. В.В.Закусова
Незнамов Григорий Георгиевич – д-р мед. наук, проф., зам. дир. по науч. работе, зав. лаб. клин. психофармакологии ФГБНУ НИИ фармакологии им. В.В.Закусова
Список исп. литературыСкрыть список1. Аведисова А.С., Чахава В.О., Лесс Ю.Э., Малыгин Я.В. Новый анксиолитик «афобазол» при терапии генерализованного тревожного расстройства (результаты сравнительного исследования с диазепамом). Психиатрия и психофармакотерапия им. П.Б.Ганнушкина. 2006; 8 (3): 16–9. / Avedisova A.S., Chakhava V.O., Less Iu.E., Malygin Ia.V. Novyi anksiolitik «afobazol» pri terapii generalizovannogo trevozhnogo rasstroistva (rezul'taty sravnitel'nogo issledovaniia s diazepamom). Psychiatry and psichopharmacotherapy. 2006; 8 (3): 16–9. [in Russian]
2. Бабюк И.А., Шульц О.Е. Исследование эффективности и переносимости афобазола у больных генерализованным тревожным расстройством. Журн. психиатрии и мед. психологии. 2007; 17 (1): 21–5. / Babiuk I.A., Shul'ts O.E. Issledovanie effektivnosti i perenosimosti afobazola u bol'nykh generalizovannym trevozhnym rasstroistvom. Zhurnal psikhiatrii i med. psikhologii. 2007; 17 (1): 21–5. [in Russian]
3. Краснов В.Н., Вельтищев Д.Ю., Немцов А.В., Ивушкин А.А. Новые подходы к лечению стрессовых и тревожных расстройств: результаты многоцентрового исследования эффективности афобазола в психиатрической практике. Психиатрия и психофармакотерапия. 2007; 9 (4): 16–20. / Krasnov V.N., Vel'tishchev D.Iu., Nemtsov A.V., Ivushkin A.A. Novye podkhody k lecheniiu stressovykh i trevozhnykh rasstroistv: rezul'taty mnogotsentrovogo issledovaniia effektivnosti afobazola v psikhiatricheskoi praktike. Psychiatry and psichopharmacotherapy. 2007; 9 (4): 16–20. [in Russian]
4. Незнамов Г.Г., Сюняков С.А., Чумаков Д.В., Маметова Л.Э. Новый селективный анксиолитик афобазол. Журн. неврологии и психиатрии им. С.С.Корсакова. 2005; 105 (4): 48–54. / Neznamov G.G., Siuniakov S.A., Chumakov D.V., Mametova L.E. Novyi selektivnyi anksiolitik afobazol. Zhurn. nevrologii i psikhiatrii im. S.S.Korsakova. 2005; 105 (4): 48–54. [in Russian]
5. Незнамов Г.Г., Сюняков С.А., Чумаков Д.В., Телешова Е.С. и др. Новый анксиолитик афобазол: результаты сравнительного клинического исследования с диазепамом при генерализованном тревожном расстройстве. Психиатрия и психофармакотерапия. 2006; 8 (4): 8–13. / Neznamov G.G., Siuniakov S.A., Chumakov D.V i dr. Novyi anksiolitik afobazol: rezul'taty sravnitel'nogo klinicheskogo issledovaniia s diazepamom pri generalizovannom trevozhnom rasstroistve. Psychiatry and psichopharmacotherapy. 2006; 8 (4): 8–13. [in Russian]
6. Смулевич А.Б., Андрющенко А.В., Романов Д.В. Психофармакотерапия тревожных расстройств пограничного уровня (сравнительное исследование анксиолитического эффекта Афобазола и оксазепама у больных с расстройствами адаптации и генерализованным тревожным расстройством). Рус. мед. журн. 2006; 14 (9): 725–29. / Smulevich A.B., Andriushchenko A.V., Romanov D.V. Psikhofarmakoterapiia trevozhnykh rasstroistv pogranichnogo urovnia (sravnitel'noe issledovanie anksioliticheskogo effekta Afobazola i oksazepama u bol'nykh s rasstroistvami adaptatsii i generalizovannym trevozhnym rasstroistvom). Rus. med. zhurn. 2006; 14 (9): 725–29. [in Russian]
7. Сюняков С.А., Чумаков Д.В., Бочкарев В.К. и др. Особенности действия анксиолитика афобазола у больных с различными индивидуально-типологическими чертами. Соц. и клин. психиатрия. 2006; 16 (1): 38–45. / Siuniakov S.A., Chumakov D.V., Bochkarev V.K. i dr. Osobennosti deistviia anksiolitika afobazola u bol'nykh s razlichnymi individual'no-tipologicheskimi chertami. Sots. i klin. psikhiatriia. 2006; 16 (1): 38–45. [in Russian]
8. Шоломов И.И., Лутошкина Е.Б., Салина Е.А. Эффективность Афобазола при тревожных расстройствах у пациентов с хронической цереброваскулярной недостаточностью. Журн. неврологии и психиатрии им. С.С.Корсакова. 2008; 6: 75–7. / Sholomov I.I., Lutoshkina E.B., Salina E.A. Effektivnost' Afobazola pri trevozhnykh rasstroistvakh u patsientov s khronicheskoi
tserebrovaskuliarnoi nedostatochnost'iu. Zhurn. nevrologii i psikhiatrii im. S.S.Korsakova. 2008; 108 (6): 75–7. [in Russian]
9. Медведев В.Э., Троснова А.П., Добровольский А.В. Психофармакотерапия тревожных расстройств у больных с сердечно-сосудистыми заболеваниями: применение Афобазола. Журн. неврологии и психиатрии им. С.С.Корсакова. 2007; 107 (7): 25–7. / Medvedev V.E., Trosnova A.P., Dobrovol'skii A.V. Psikhofarmakoterapiia trevozhnykh rasstroistv u bol'nykh s serdechno-sosudistymi zabolevaniiami: primenenie Afobazola. Zhurn. nevrologii i psikhiatrii im. S.S.Korsakova. 2007; 107 (7): 25–7. [in Russian]
10. Татарский Б.А., Бисерова И.Н. Использование Афобазола при лечении пароксизмальной формы фибрилляции предсердий. / Рус. мед. журн. 2007; 15 (9): 760–4. / Tatarskii B.A., Biserova I.N. Ispol'zovanie Afobazola pri lechenii paroksizmal'noi formy fibrilliatsii predserdii. Rus. med. zhurn. 2007; 15 (9): 760–4. [in Russian]
11. Кузнецова С.М. Применение Афобазола в системе реабилитации больных пожилого возраста, перенесших ишемический инсульт. Новости медицины и фармации. 2008; 20: 18–20. / Kuznetsova S.M. Primenenie Afobazola v sisteme reabilitatsii bol'nykh pozhilogo vozrasta, perenesshikh ishemicheskii insul't. Novosti meditsiny i farmatsii. 2008; 20: 18–20. [in Russian]
12. Давыдов А.Т., Литвинцев С.В., Бутко Д.Ю. и др. Опыт диагностики и лечения тревожного расстройства в постинсультном периоде у больных, перенесших ишемический инсульт. Рус. мед. журн. 2008; 5: 266–9. / Davydov A.T., Litvintsev S.V., Butko D.Iu. i dr. Opyt diagnostiki i lecheniia trevozhnogo rasstroistva v postinsul'tnom periode u bol'nykh, perenesshikh ishemicheskii insul't. Rus. med. zhurn. 2008; 5: 266–9. [in Russian]
13. Дробижев М.Ю., Овчинников А.А. Патогенетическая терапия тревожных расстройств. Соц. и клин. психиатрия. 2010; 4: 112–6. / Drobizhev M.Iu., Ovchinnikov A.A. Patogeneticheskaia terapiia trevozhnykh rasstroistv. Sots. i klin. psikhiatriia. 2010; 4: 112–6. [in Russian]
14. Дробижев М.Ю., Федотова А.В., Кикта С.В. Патогенетическая фармакотерапия фобических тревожных расстройств и состояний, обусловленных стрессом. Профилактическая медицина. 2013; 4: 34–9. / Drobizhev M.Iu., Fedotova A.V., Kikta S.V. Patogeneticheskaia farmakoterapiia fobicheskikh trevozhnykh rasstroistv i sostoianii, obuslovlennykh stressom. Profilakticheskaia meditsina. 2013; 4: 34–9. [in Russian]
15. Иванов С.В. Спектр применения современных анксиолитиков в психиатрии и общей медицине (систематический обзор клинических исследований селективного анксиолитика Афобазола). Эффективная фармакотерапия. Неврология и психиатрия. 2012; 3: 1–8. / Ivanov S.V. Spektr primeneniia sovremennykh anksiolitikov v psikhiatrii i obshchei meditsine (sistematicheskii obzor klinicheskikh issledovanii selektivnogo anksiolitika Afobazola). Effektivnaia farmakoterapiia. Nevrologiia i psikhiatriia. 2012; 3: 1–8. [in Russian]
16. Городничев А.В. Современные тенденции в терапии тревожных расстройств: от научных данных к клиническим рекомендациям. Биологические методы терапии психических расстройств. Доказательная медицина – клинической практике. Под ред. С.Н.Мосолова. М.: Социально-политическая мысль, 2012; с. 643–68. / Gorodnichev A.V. Sovremennye tendentsii v terapii trevozhnykh rasstroistv: ot nauchnykh dannykh k klinicheskim rekomendatsiiam. Biologicheskie metody terapii psikhicheskikh rasstroistv. Dokazatel'naia meditsina – klinicheskoi praktike. Pod red. S.N.Mosolova. M.: Sotsial'no-politicheskaia mysl', 2012; s. 643–68. [in Russian]
17. Середенин С.Б., Воронин М.В. Нейрорецепторные механизмы действия Афобазола. Эксперим. и клин. фармакология. 2009; 72 (1): 3–11. / Seredenin S.B., Voronin M.V. Neiroretseptornye mekhanizmy deistviia Afobazola. Eksperim. i klin. farmakologiia. 2009; 72 (1): 3–11. [in Russian]
18. Яркова М.А. Анализ связывающей способности бензодиазепинового участка ГАМКА-рецептора у мышей C57BL/6 и BALB/c при введении анксиолитиков. Эксперим. и клин. фармакология. 2011; 74 (8): 3–7. / Iarkova M.A. Analiz sviazyvaiushchei sposobnosti benzodiazepinovogo uchastka GAMKA-retseptora u myshei C57BL/6 i BALB/c pri vvedenii anksiolitikov. Eksperim. i klin. farmakologiia. 2011; 74 (8): 3–7. [in Russian]
19. Hayashi T. Sigma-1 receptor: the novel intracellular target of neuropsychotherapeutic drugs. J Pharmacol Sci 2015; 127 (1): 2–5.
20. Hashimoto K. Activation of sigma-1 receptor chaperone in the treatment of neuropsychiatric diseases and its clinical implication.
J Pharmacol Sci 2015; 127 (1): 6–9.
21. Hayashi T, Tsai S-Y, Mori T et al. Targeting ligand-operated chaperone sigma-1 receptors in the treatment of neuropsychiatric disorders. Exp Opin Ther Targets Informa 2011; 15 (5): 557–577.
22. Yagasaki Y, Numakawa T, Kumamaru E et al. Chronic antidepressants potentiate via sigma-1 receptors the brain-derived neurotrophic factor-induced signaling for glutamate release. J Biol Chem 2006; 281 (18): 12941–9.
23. Moriguchi S, Shinoda Y, Yamamoto Y et al. Stimulation of the sigma-1 receptor by DHEA enhances synaptic efficacy and neurogenesis in the hippocampal dentate gyrus of olfactory bulbectomized mice. PLoS One. Public Library of Science 2013; 84: e60863.
24. Maurice T, Lockhart BP. Neuroprotective and anti-amnesic potentials of sigma (σ) receptor ligands. Prog Neuro-Psychopharmacology Biol Psychiatry 1997; 21 (1): 69–102.
25. Fujimoto M, Hayashi T, Urfer R et al. Sigma-1 receptor chaperones regulate the secretion of brain-derived neurotrophic factor.
Synapse 2012; 66: 630–9.
26. Kikuchi-Utsumi K, Nakaki T. Chronic treatment with a selective ligand for the sigma-1 receptor chaperone, SA4503, up-regulates BDNF protein levels in the rat hippocampus. Neurosci Lett 2008; 440: 19–22.
27. Müller WE, Siebert B, Holoubek G, Gentsch C. Neuropharmacology of the anxiolytic drug opripramol, a sigma site ligand. Pharmacopsychiatry 2004; 37 (Suppl. 3).
28. Bhuiyan MS, Fukunaga K. Stimulation of sigma-1 receptor signaling by dehydroepiandrosterone ameliorates pressure overload-induced hypertrophy and dysfunctions in ovariectomized rats. Exp Opin Ther Targets 2009; 13 (11): 1253–65.
29. Bhuiyan MS, Fukunaga K, Tagashira H, Shioda N. Targeting sigma-1 receptor with fluvoxamine ameliorates pressure-overload-induced hypertrophy and dysfunctions. Exp Opin Ther Targets 2010; 14 (10): 1009–22.
30. Hindmarch I, Hashimoto K. Cognition and depression: the effects of fluvoxamine, a sigma-1 receptor agonist, reconsidered. Hum Psychopharmacol 2010; 25 (3): 193–200.
31. Iyo M, Shirayama Y, Watanabe H et al. Fluvoxamine as a sigma-1 receptor agonist improved cognitive impairments in a patient with schizophrenia. Prog Neuropsychopharmacol Biol Psychiatry 2008; 32 (4): 1072–3.
32. Niitsu T, Shirayama Y, Fujisaki M et al. Fluvoxamine improved cognitive impairments in a patient with schizophrenia. Prog Neuropsychopharmacol Biol Psychiatry 2010; 34 (7): 1345–6.
33. Berra B, Rizzo AM. Melatonin: circadian rhythm regulator, chronobiotic, antioxidant and beyond. Clin Dermatol 2009; 27 (2): 202–9.
34. Boyce P, Hopwood M. Manipulating melatonin in managing mood. Acta Psychiatr Scand Suppl 2013; 128: 16–23.
35. Rahman SA, Kayumov L, Shapiro CM. Antidepressant action of melatonin in the treatment of Delayed Sleep Phase Syndrome.
Sleep Med 2010; 11 (2): 131–6.
36. Papp M, Litwa E, Gruca P, Mocaër E. Anxiolytic-like activity of agomelatine and melatonin in three animal models of anxiety. Behav Pharmacol 2006; 17 (1): 9–18.
37. Stein DJ, Ahokas AA, de Bodinat C. Efficacy of agomelatine in generalized anxiety disorder: a randomized, double-blind, placebo-controlled study. J Clin Psychopharmacol 2008; 28 (5): 561–6.
38. Arendt J, Skene DJ. Melatonin as a chronobiotic. Sleep Med Rev 2005; 9 (1): 25–39.
39. Chen S, Wu K, Knox R. Free Rad Biol Med 2000; 29 (3–4): 276–84.
40. Oxenkrug GF, Bachurin SO, Prakhie IV, Zefirov NS. Quinone reductase 2 and antidepressant effect of melatonin derivatives. Ann N Y Acad Sci 2010; 1199: 121–4.
41. Riederer P, Lachenmayer L, Laux G. Clinical applications of MAO-inhibitors. Curr Med Chem 2004; 11 (15): 2033–43.
42. Krishnan RR, Davidson J, Miller R. MAO inhibitor therapy in trichotillomania associated with depression: Case report. J Clin Psychiatry 1984; 45 (6): 267–8.
43. Мосолов С.Н. Основы психофармакотерапии. М.: Восток, 1996. / Mosolov S.N. Osnovy psikhofarmakoterapii. M.: Vostok, 1996. [in Russian]
44. De Angelis L, Furlan C. The anxiolytic-like properties of two selective MAOIs, moclobemide and selegiline, in a standard and an enhanced light/dark aversion test. Pharmacol Biochem Behav 2000; 65 (4): 649–53.
45. Jindal A, Mahesh R, Kumar B. Anxiolytic-like effect of linezolid in experimental mouse models of anxiety. Prog Neuro-Psychopharmacology Biol Psychiatry 2013; 40 (1): 47–53.
46. Середенин С.Б., Воронина Т.А., Незнамов Г.Г. и др. Фармакогенетическая концепция анксиоселективного эффекта. Вестник РАМН. 1998; 11: 3–9. / Seredenin S.B., Voronina T.A., Neznamov G.G. i dr. Farmakogeneticheskaia kontseptsiia anksioselektivnogo effekta. Vestnik RAMN. 1998; 11: 3–9. [in Russian]
47. Яркова М.А. Изучение анксиолитических свойств производных 2-меркаптобензимидазола. Автореф. дис….канд. мед. наук. М., 1996. / Iarkova M.A. Izuchenie anksioliticheskikh svoistv proizvodnykh 2-merkaptobenzimidazola. Avtoref. dis….kand. med. nauk. M., 1996. [in Russian]
48. Seredenin SB, Blednov YA. A pharmacogenetic approach to the design of new selective, anxiolytic drugs – in book: Biological Basis of Individual Sensitivity to Psychotropic. Drugs 1994; p. 25–38.
49. Середенин С.Б. Лекции по фармакогенетике. М.: Медицинское информационное агентство, 2004. / Seredenin S.B. Lektsii po farmakogenetike. M.: Meditsinskoe informatsionnoe agentstvo, 2004. [in Russian]
50. Середенин С.Б., Поварова О.В., Медведев О.С. и др. Доказательство нейропротекторных свойств афобазола на экспериментальной модели фокальной ишемии головного мозга. Эксперим. и клин. фармакология. 2006; 69 (4): 3–5. / Seredenin S.B., Povarova O.V., Medvedev O.S. i dr. Dokazatel'stvo neiroprotektornykh svoistv afobazola na eksperimental'noi modeli fokal'noi ishemii golovnogo mozga. Eksperim. i klin. farmakologiia. 2006; 69 (4): 3–5. [in Russian]
51. Середенин С.Б., Крайнева В.А. Нейропротекторные свойства афобазола при экспериментальном моделировании геморрагического инсульта. Эксперим. и клин. фармакология. 2009; 72 (1): 24–8. / Seredenin S.B., Kraineva V.A. Neiroprotektornye svoistva afobazola pri eksperimental'nom modelirovanii gemorragicheskogo insul'ta. Eksperim. i klin. farmakologiia. 2009; 72 (1): 24–8. [in Russian]
52. Крайнева В.А., Середенин С.Б. Нейропротективные свойства афобазола при повторном моделировании геморрагического инсульта у старых крыс. Бюл. эксперим. биологии и медицины. 2010; 2: 165–8. / Kraineva V.A., Seredenin S.B. Neiroprotektivnye svoistva afobazola pri povtornom modelirovanii gemorragicheskogo insul'ta u starykh krys. Biul. eksperim. biologii i meditsiny. 2010; 2: 165–8. [in Russian]
53. Тумакаев Р.Ф., Баширов Ф.В., Середенин С.Б. Перспективность использования афобазола в лечении осложненной спинальной травмы. IV съезд фармакологов России «Инновации в современной фармакологии». Материалы съезда 18–21 сентября 2012 года. 2012. / Tumakaev R.F., Bashirov F.V., Seredenin S.B. Perspektivnost' ispol'zovaniia afobazola v lechenie oslozhnennoi spinal'noi travmy. IV s"ezd farmakologov Rossii «Innovatsii v sovremennoi farmakologii». Materialy s"ezda 18–21 sentiabria 2012 goda. 2012. [in Russian]
54. Силкина И.В., Зенина Т.А., Середенин С.Б., Мирзоян Р.С. Влияние афобазола на содержание продуктов свободнорадикального окисления и активность каталазы в условиях ишемии головного мозга. Эксперим. и клин. фармакология. 2006; 69 (4): 47–50. / Silkina I.V., Zenina T.A., Seredenin S.B., Mirzoian R.S. Vliianie afobazola na soderzhanie produktov svobodnoradikal'nogo okisleniia i aktivnost' katalazy v usloviiakh ishemii golovnogo mozga. Eksperim. i klin. farmakologiia. 2006; 69 (4): 47–50. [in Russian]
55. Антипова Т.А., Логвинов И.О., Курдюмов И.Н. и др. Влияние афобазола на содержание стресс-белка HSс70 в ткани мозга крыс при глобальной преходящей ишемии Эксперим. и клин. фармакология. 2009; 72 (1): 29–32. / Antipova T.A., Logvinov I.O., Kurdiumov I.N. i dr. Vliianie afobazola na soderzhanie stress-belka HSs70 v tkani mozga krys pri global'noi prekhodiashchei ishemii Eksperim. i klin. farmakologiia. 2009; 72 (1): 29–32. [in Russian]
56. Середенин С.Б., Мелкумян Д.С., Вальдман Е.А. и др. Влияние афобазола на содержание BDNF в структурах мозга инбредных мышей с различным фенотипом эмоционально-стрессовой реакции. Эксперим. и клин. фармакология. 2006; 69 (3): 3–6. / Seredenin S.B., Melkumian D.S., Val'dman E.A. i dr. Vliianie afobazola na soderzhanie BDNF v strukturakh mozga inbrednykh myshei s razlichnym fenotipom emotsional'no-stressovoi reaktsii. Eksperim. i klin. farmakologiia. 2006; 69 (3): 3–6. [in Russian]
57. Антипова Т.А., Сапожникова Д.С., Бахтина Л.Ю., Середенин С.Б. Селективный анксиолитик афобазол увеличивает содержание BDNF и NGF в культуре гиппокампальных нейронов линии НТ-22. Эксперим. и клин. фармакология. 2009; 72 (1): 12–4. / Antipova T.A., Sapozhnikova D.S., Bakhtina L.Iu., Seredenin S.B. Selektivnyi anksiolitik afobazol uvelichivaet soderzhanie BDNF i NGF v kul'ture gippokampal'nykh neironov linii NT-22. Eksperim. i klin. farmakologiia. 2009; 72 (1): 12–4. [in Russian]
58. Силкина И.В., Александрин В.В., Ганьшина Т.С. и др. Усиление кровоснабжения ишемизированного мозга под влиянием афобазола. Эксперим. и клин. фармакология. 2004; 67 (5): 9–12. / Silkina I.V., Aleksandrin V.V., Gan'shina T.S. i dr. Usilenie krovosnabzheniia ishemizirovannogo mozga pod vliianiem afobazola. Eksperim. i klin. farmakologiia. 2004; 67 (5): 9–12. [in Russian]
59. Мирзоян Р.С., Хайлов Н.А., Ганьшина Т.С. Цереброваскулярные эффекты афобазола при сочетанной сосудистой патологии мозга и сердца. Эксперим. и клин. фармакология. 2010; 73 (5): 2–7. / Mirzoian R.S., Khailov N.A., Gan'shina T.S. Tserebrovaskuliarnye effekty afobazola pri sochetannoi sosudistoi patologii mozga i serdtsa. Eksperim. i klin. farmakologiia. 2010; 73 (5): 2–7. [in Russian]
60. Мирзоян Р.С., Ганьшина Т.С., Хайлов Н.А. и др. Цереброваскулярная фармакология раздельной и сочетанной сосудистой патологии мозга и сердца. Эксперим. и клин. фармакология. 2014; 77 (3): 3–8. / Mirzoian R.S., Gan'shina T.S., Khailov N.A. i dr. Tserebrovaskuliarnaia farmakologiia razdel'noi i sochetannoi sosudistoi patologii mozga i serdtsa. Eksperim. i klin. farmakologiia. 2014; 77 (3): 3–8. [in Russian]
61. Zenina TA, Gavrish IV, Melkumyan DS, Seredenina TS et al. Neuroprotective Properties of Afobazol in Vitro. Bull Exp Biol Med 2005; 140 (2): 194–6.
62. Цорин И.Б., Палка И.П., Чичканов Г.Г. Особенности действия селективного анксиолитика афобазола на сердечно-сосудистую систему. Эксперим. и клин. фармакология. 2009; 72 (1): 41–5. / Tsorin I.B., Palka I.P., Chichkanov G.G. Osobennosti deistviia selektivnogo anksiolitika afobazola na serdechno-sosudistuiu sistemu. Eksperim. i klin. farmakologiia. 2009; 72 (1): 41–5. [in Russian]
63. Цорин И.Б., Крыжановский С.А., Вититнова М.Б., Столярук В.Н. Изучение противофибрилляторной активности Афобазола у животных с интактным и денервированным миокардом. Вестн. Российской академии медицинских наук. 2010; 4: 45–8. / Tsorin I.B., Kryzhanovskii S.A., Vititnova M.B., Stoliaruk V.N. Izuchenie protivofibrilliatornoi aktivnosti Afobazola u zhivotnykh s intaktnym i denervirovannym miokardom. Vestn. Rossiiskoi akademii meditsinskikh nauk. 2010; 4: 45–8. [in Russian]
64. Турилова А.И., Можаева Т.Я. Антиаритмические свойства афобазола и других производных 2-меркаптобензимидазола. Эксперим. и клин. фармакология. 2010; 73 (5): 8–11. / Turilova A.I., Mozhaeva T.Ia. Antiaritmicheskie svoistva afobazola i drugikh proizvodnykh 2-merkaptobenzimidazola. Eksperim. i klin. farmakologiia. 2010; 73 (5): 8–11. [in Russian]
65. Столярук В.Н., Вититнова М.Б., Крыжановский С.А. Изучение эффектов афобазола на модели реперфузионных аритмий. Вестн. Российской академии медицинских наук. 2010; 4: 41–5. / Stoliaruk V.N., Vititnova M.B., Kryzhanovskii S.A. Izuchenie effektov afobazola na modeli reperfuzionnykh aritmii. Vestn. Rossiiskoi akademii meditsinskikh nauk. 2010; 4: 41–5. [in Russian]
66. Середенин С.Б., Цорин И.Б., Дурнев А.Д. и др. Изучение антиишемического действия Афобазола в условиях экспериментального инфаркта миокарда. Бюл. эксперим. биологии и медицины. 2010; 9: 284–7. / Seredenin S.B., Tsorin I.B., Durnev A.D. i dr. Izuchenie antiishemicheskogo deistviia Afobazola v usloviiakh eksperimental'nogo infarkta miokarda. Biul. eksperim. biologii i meditsiny. 2010; 9: 284–7. [in Russian]
67. Середенин С.Б., Молодавкин Г.М., Воронин М.В., Воронина Т.А. Антидепрессивное действие афобазола в тестах сorsolt и Nomura. Эксперим. и клин. фармакология. 2009; 72 (1): 19–21. / Seredenin S.B., Molodavkin G.M., Voronin M.V., Voronina T.A. Antidepressivnoe deistvie afobazola v testakh sorsolt i Nomura. Eksperim. i klin. farmakologiia. 2009; 72 (1): 19–21. [in Russian]
68. Дурнев А.Д., Жанатаев А.К., Шредер О.В., Середенин С.Б. Антимутагенные и антитератогенные свойства афобазола. Эксперим. и клин. фармакология. 2009; 72 (1): 46–51. / Durnev A.D., Zhanataev A.K., Shreder O.V., Seredenin S.B. Antimutagennye i antiteratogennye svoistva afobazola. Eksperim. i klin. farmakologiia. 2009; 72 (1): 46–51. [in Russian]
69. Незнамов Г.Г., Сюняков С.А., Чумаков Д.В. и др. Результаты клинического изучения селективного анксиолитика афобазол. Эксперим. и клин. фармакология. 2001; 64 (2): 15–9. / Neznamov G.G., Siuniakov S.A., Chumakov D.V. i dr. Rezul'taty klinicheskogo izucheniia selektivnogo anksiolitika afobazol. Eksperim. i klin. farmakologiia. 2001; 64 (2): 15–9. [in Russian]
70. Середенин С.Б., Ведерников А.А. Влияние психотропных препаратов на поведение инбредных мышей в условиях открытого поля. Бюл. эксп. биол. мед. 1979; 88; 7: 38–40. / Seredenin S.B., Vedernikov A.A. Vliianie psikhotropnykh preparatov na povedenie inbrednykh myshei v usloviiakh otkrytogo polia. Biul. eksp. biol. med. 1979; 88; 7: 38–40. [in Russian]
71. Чумаков Д.В. Клинико-фармакологическая характеристика селективного анксиолитика афобазола. Автореф. дисс….канд. мед. наук. М., 2004. / Chumakov D.V. Kliniko-farmakologicheskaia kharakteristika selektivnogo anksiolitika afobazola. Avtoref. diss….kand. med. nauk. M., 2004. [in Russian]
72. Незнамов Г.Г., Сюняков Т.С., Золотов Н.Н. и др. Терапевтическое влияние анксиолитиков Феназепама и Афобазола на содержание малонового диальдегида в плазме крови и психическое состояние больных с тревожными расстройствами. Психические расстройства в общей медицине. 2014; 2: 40–7. / Neznamov G.G., Syunyakov T.S., Zolotov N.N. et al. Effects of anxiolytics Phenazepam and Afobazole on malondialdehyde plasma levels and clinical state in patients with anxiety disorders. Mental disorders in General medicine. 2014; 2: 40–7. [in Russian]
73. Аведисова А.С. Афобазол – безопасный препарат для лечения тревоги в общей практике. Рус. мед. журн. 2006; 14 (22): 1–3. / Avedisova A.S. Afobazol – bezopasnyi preparat dlia lecheniia trevogi v obshchei praktike. Rus. med. zhurn. 2006; 14 (22): 1–3. [in Russian]
74. Свищенко Е.П., Гулкевич О.В. Опыт применения препарата Афобазол® у пациентов с гипертонической болезнью и тревожными расстройствами (расширенный реферат)/ Психические расстройства в общей медицине. 2014; 1: 56–60. / Svischenko E.P., Gulkevich O.V. Experience with the Afobazol® in patients with hypertension. Mental disorders in General medicine. 2014; 1: 56–60. [in Russian]
75. Акарачкова Е.С., Шварков С.Б., Мамий В.И. Афобазол в терапии вегетативных проявлений тревоги и дезадаптации у больных неврологической и общесоматической практики. Рус. мед. журн. 2007; 15 (1): 1–6. / Akarachkova E.S., Shvarkov S.B., Mamii V.I. Afobazol v terapii vegetativnykh proiavlenii trevogi i dezadaptatsii u bol'nykh nevrologicheskoi i obshchesomaticheskoi praktiki. Rus. med. zhurn. 2007; 15 (1): 1–6. [in Russian]
76. Чумакова Е.А., Гапонова Н.И., Березина Т.Н. Оценка эффективности применения терапии афобазолом в комплексном лечении больных артериальной гипертензией. Рос. кардиол. журн. 2014; 2 (106): 71–7. / Chumakova E.A., Gaponova N.I., Berezina T.N. Otsenka effektivnosti primeneniia terapii afobazolom v kompleksnom lechenii bol'nykh arterial'noi gipertenziei. Ros. kardiol. zhurn. 2014; 2 (106): 71–7. [in Russian]
77. Ястребов Д.В., Михайлова О.И., Костычева Е.А. Применение препарата Афобазол при нарушениях сна у больных с тревожными расстройствами. Психиатрия и психофармакотерапия им. П.Б.Ганнушкина. 2013; 5: 32–5. / Yastrebov D.V., Mikhailova O.I., Kostycheva E.A. Afobazol administration in patients with sleep disorders comorbid with anxiety disorders. Psychiatry and Psychopharmacotherapy. 2013; 5: 32–5. [in Russian]
78. Сюняков Т.С., Шабанова А.А. Характеристика нарушений когнитивных функций у больных с тревожными расстройствами при терапии анксиолитиком афобазолом. Теоретические и прикладные проблемы медицинской психологии. Материалы Всероссийской научно-практической конференции 14–15 февраля 2013 года. Научный центр психического здоровья РАМН, 2013: с. 108–9. / Siuniakov T.S., Shabanova A.A. Kharakteristika narushenii kognitivnykh funktsii u bol'nykh s trevozhnymi rasstroistvami pri terapii anksiolitikom afobazolom. Teoreticheskie i prikladnye problemy meditsinskoi psikhologii. Materialy Vserossiiskoi nauchno-prakticheskoi konferentsii 14–15 fevralia 2013 goda. Nauchnyi tsentr psikhicheskogo zdorov'ia RAMN, 2013: s. 108–9. [in Russian]
79. Богдан Н.Г., Колотилинская Н.В., Надоров С.А. и др. Влияние афобазола на психофизиологические показатели здоровых добровольцев. Эксперим. и клин. фармакология. 2011; 74 (8): 8–12. / Bogdan N.G., Kolotilinskaia N.V., Nadorov S.A. i dr. Vliianie afobazola na psikhofiziologicheskie pokazateli zdorovykh dobrovol'tsev. Eksperim. i klin. farmakologiia. 2011; 74 (8): 8–12. [in Russian]
80. Давыдов А.Т., Литвинцев С.В., Бутко Д.Ю. и др. Опыт диагностики и лечения тревожного расстройства в постинсультном периоде у больных, перенесших ишемический инсульт. РМЖ (Человек и лекарство). 2008; 16 (5): 266–70. / Davydov A.T., Litvintsev S.V., Butko D.Iu. i dr. Opyt diagnostiki i lecheniia trevozhnogo rasstroistva v postinsul'tnom periode u bol'nykh, perenesshikh ishemicheskii insul't. RMZh (Chelovek i lekarstvo). 2008; 16 (5): 266–70. [in Russian]
81. Кудашова Е.А., Минаков Э.В. Комплексный подход к терапии пациентов с ишемической болезнью сердца и коморбидными тревожно-депрессивными расстройствами. Тульский государственный университет, 2008; 15: 4: 49. / Kudashova E.A., Minakov E.V. Kompleksnyi podkhod k terapii patsientov s ishemicheskoi bolezn'iu serdtsa i komorbidnymi trevozhno-depressivnymi rasstroistvami. Vestnik novykh meditsinskikh tekhnologii. Tul'skii gosudarstvennyi universitet, 2008; 15: 4: 49. [in Russian]
82. Мельник М.Г., Канорский С.Г., Богочанова О.А., Трубчанинова С.А. Оценка краткосрочных эффектов Афобазола у гериатрических больных с сочетанными психосоматическими заболеваниями. Психиатрия и психофармакотерапия им. П.Б.Ганнушкина. 2014; 4: 46–51. / Melnik M.G., Kanorsky S.G., Bogochanova O.A., Trubchaninova S.A. Evaluation of short-term effects Afobazol in geriatric patients with combined psychosomatic diseases. Psychiatry and Psychopharmacotherapy. 2014; 4: 46–51. [in Russian]
83. Калинина С.Ю., Жилина Н.И., Белова А.Н., Суворов А.В. Влияние анксиолитика Афобазола на эффективность лечения гипертонической болезни у пожилых женщин. Обозрение психиатрии и медицинской психологии им. В.М.Бехтерева. 2009; 4: 37–42. / Kalinina S.Iu., Zhilina N.I., Belova A.N., Suvorov A.V. Vliianie anksiolitika Afobazola na effektivnost' lecheniia gipertonicheskoi bolezni u pozhilykh zhenshchin. Obozrenie psikhiatrii i meditsinskoi psikhologii im. V.M.Bekhtereva. 2009; 4: 37–42. [in Russian]
84. Жидких Б.Д., Колесникова О.Е., Барбашина Т.А. и др. Влияние Афобазола на качество жизни кардиологических больных в процессе стационарного лечения. Рус. мед. журн. 2007; 15 (16): 1–4. / Zhidkikh B.D., Kolesnikova O.E., Barbashina T.A. i dr. Vliianie Afobazola na kachestvo zhizni kardiologicheskikh bol'nykh v protsesse statsionarnogo lecheniia. Rus. med. zhurn. 2007; 15 (16): 1–4. [in Russian]
85. Петрова Н., Кутузова А., Бобровская Е. Медикаментозная коррекция тревожных расстройств у больных острым инфарктом миокарда. Врач. 2010; 7: 53–6. / Petrova N., Kutuzova A., Bobrovskaia E. Medikamentoznaia korrektsiia trevozhnykh rasstroistv u bol'nykh ostrym infarktom miokarda. Vrach. 2010; 7: 53–6. [in Russian]
86. McGorry P, Keshavan M, Goldstone S et al. Biomarkers and clinical staging in psychiatry. World Psychiatry 2014; 13 (3): 211–23.
87. Александровский Ю.А., Поюровский М.В., Незнамов Г.Г. Неврозы и перекисное окисление липидов. М.: Наука, 1991. / Aleksandrovskii Iu.A., Poiurovskii M.V., Neznamov G.G. Nevrozy i perekisnoe okislenie lipidov. M.: Nauka, 1991. [in Russian]
17 сентября 2015
Количество просмотров: 4541


