Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Методы
Результаты




Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№01 2016
Место флувоксамина в лечении депрессии в России: открытое неконтролируемое рандомизированное многоцентровое обсервационное исследование №01 2016
Номера страниц в выпуске:4-10
Флувоксамин, селективный ингибитор обратного захвата серотонина, широко применяется для лечения депрессивных состояний, относящихся к числу наиболее распространенных как в мире, так и на территории России. Однако эффективность и безопасность применения этого препарата в условиях общемедицинской практики изучены недостаточно.
Методы: проспективное неконтролируемое открытое исследование было проведено в 11 центрах на территории Российской Федерации; 293 пациента (18 лет и старше), соответствующие критериям Diagnostic and Statistical Manual of mental disorders (DSM-IV) для депрессии и с оценками 17 и более по 17-пунктовой шкале оценки депрессии Гамильтона (HAMD-17) принимали флувоксамин по 50–300 мг в течение 6 нед. Первичной мерой эффективности было изменение баллов HAMD-17 и CGI (Clinical global impression scale – Шкала общего клинического впечатления) относительно стартовых значений. Вторичной мерой эффективности стала динамика качества сна, оцениваемая по специальной подшкале HAMD-17. Безопасность определялась по частоте и характеру сообщаемых нежелательных лекарственных явлений (НЛЯ).
Результаты: средний возраст пациентов 42,7 года, большинство женщины (72%). К концу лечения (42-й день) наблюдали клинически значимую редукцию средних оценок HAMD-17, CGI (тяжесть заболевания) и HAMD-17 (подшкала для оценки сна): стартовые баллы 23,1; 4,5 и 3,9 соответственно; изменение относительно стартовых баллов (D): 17,3 (95% доверительный интервал – ДИ -18,0; -16,7), 2,1 и 3,4 (95% ДИ -3,53; -3,20) соответственно. Судя по оценкам тяжести CGI и оценкам качества жизни, на 42-й день состояние 20,8% пациентов было нормальным (отсутствие заболевания), состояние 85% больных «намного улучшилось» или «очень заметно улучшилось». Чаще всего пациенты жаловались на тошноту (12,6%) и сонливость (5,1%). Не сообщалось о летальных исходах или серьезных НЛЯ, лишь 8 больных прекратили лечение из-за НЛЯ.
Вывод: применение флувоксамина в условиях общемедицинской практики привело к заметному улучшению состояния у пациентов с депрессией (оценки по шкалам HAMD-17 и CGI), т.е. обладало хорошим профилем эффективности, безопасности и переносимости.
Ключевые слова: флувоксамин, депрессия, шкала Гамильтона для оценки депрессии, повседневная клиническая практика.
Флувоксамин, селективный ингибитор обратного захвата серотонина, широко применяется для лечения депрессивных состояний, относящихся к числу наиболее распространенных как в мире, так и на территории России. Однако эффективность и безопасность применения этого препарата в условиях общемедицинской практики изучены недостаточно.
Методы: проспективное неконтролируемое открытое исследование было проведено в 11 центрах на территории Российской Федерации; 293 пациента (18 лет и старше), соответствующие критериям Diagnostic and Statistical Manual of mental disorders (DSM-IV) для депрессии и с оценками 17 и более по 17-пунктовой шкале оценки депрессии Гамильтона (HAMD-17) принимали флувоксамин по 50–300 мг в течение 6 нед. Первичной мерой эффективности было изменение баллов HAMD-17 и CGI (Clinical global impression scale – Шкала общего клинического впечатления) относительно стартовых значений. Вторичной мерой эффективности стала динамика качества сна, оцениваемая по специальной подшкале HAMD-17. Безопасность определялась по частоте и характеру сообщаемых нежелательных лекарственных явлений (НЛЯ).
Результаты: средний возраст пациентов 42,7 года, большинство женщины (72%). К концу лечения (42-й день) наблюдали клинически значимую редукцию средних оценок HAMD-17, CGI (тяжесть заболевания) и HAMD-17 (подшкала для оценки сна): стартовые баллы 23,1; 4,5 и 3,9 соответственно; изменение относительно стартовых баллов (D): 17,3 (95% доверительный интервал – ДИ -18,0; -16,7), 2,1 и 3,4 (95% ДИ -3,53; -3,20) соответственно. Судя по оценкам тяжести CGI и оценкам качества жизни, на 42-й день состояние 20,8% пациентов было нормальным (отсутствие заболевания), состояние 85% больных «намного улучшилось» или «очень заметно улучшилось». Чаще всего пациенты жаловались на тошноту (12,6%) и сонливость (5,1%). Не сообщалось о летальных исходах или серьезных НЛЯ, лишь 8 больных прекратили лечение из-за НЛЯ.
Вывод: применение флувоксамина в условиях общемедицинской практики привело к заметному улучшению состояния у пациентов с депрессией (оценки по шкалам HAMD-17 и CGI), т.е. обладало хорошим профилем эффективности, безопасности и переносимости.
Ключевые слова: флувоксамин, депрессия, шкала Гамильтона для оценки депрессии, повседневная клиническая практика.
zoigrek@mail.ru
Для цитирования: Смулевич А.Б., Ильина Н.А., Читлова В.В. Место флувоксамина в лечении депрессии в России: открытое неконтролируемое рандомизированное многоцентровое обсервационное исследование. Психиатрия и психофармакотерапия. 2016;
18 (1): 4–10.
Fluvoxamine in Treatment of Depression in Russian Patients: An Open-Label Uncontrolled and Randomized Multicenter Observational Study
A.B.Smulevich1,2, N.A.Ilyina1, V.V.Chitlova1,2
1Mental Health Research Center. 115522, Russian Federation, Moscow, Kashirskoe sh., d. 34;
2I.M.Sechenov First Moscow Medical State University of the Ministry of Health of the Russian Federation. 119991, Russian Federation, Moscow, ul. Trubetskaia, d. 8, str. 2
Fluvoxamine, a selective serotonin reuptake inhibitor is widely used in the treatment of depression, one of the most common disorders prevalent in Russia. However, studies demonstrating its efficacy and safety in routine settings in Russia are scarce.
Methods: this prospective uncontrolled open-label study was conducted at 11 centers in Russia. Total 293 patients (aged ≥18 years), meeting Diagnostic and Statistical Manual of mental disorders (DSM-IV) criteria for depression and scoring ≥17 on 17-item Hamilton Rating Scale of Depression (HAMD-17) received fluvoxamine 50–300 mg for 6 weeks. Primary efficacy measures included change from baseline in the HAMD-17 and Clinical Global Impression (CGI) scores. Secondary efficacy measure was evaluation of sleep quality changes on HAMD-17 subscale. Safety was assessed by monitoring of adverse drug reactions (ADRs).
Results: mean age of patients was 42.7 years and the majority of them were women (72%). At the end of treatment (day 42), clinically significant reduction was observed in mean HAMD-17, CGI-severity of illness and HAMD-17 sleep sub-score from 23.1, 4.5 and 3.9 at baseline to day 42; change from baseline (D) was: 17.3 (95% CI -18.0; -16.7), 2.1 and 3.4 (95% CI -3.53; -3.20), respectively. At day 42, 20.8% patients reported as normal (not at all ill) on the CGI-severity scale and 85% patients reported as “much improved” or “very much improved” on the CGI-change in severity and quality of life scores. Nausea (12.6%) and somnolence (5.1%) were the most frequently reported ADRs. No deaths or serious ADRs were reported but eight patients discontinued treatment due to ADRs.
Conclusion: treatment with fluvoxamine under routine settings showed marked improvement in Russian patients with depression as measured by HAMD-17 and CGI ratings and was thus efficacious as well as safe and well-tolerated.
Key words: fluvoxamine, depression, Hamilton Rating Scale of Depression, routine settings.
zoigrek@mail.ru
For citation: Smulevich A.B., Ilyina N.A., Chitlova V.V. Fluvoxamine in Treatment of Depression in Russian Patients: An Open-Label Uncontrolled and Randomized Multicenter Observational Study. Psychiatry and Psychopharmacotherapy. 2016; 18 (1): 4–10.
Введение
Депрессия – комплексное психическое расстройство, негативно влияющее на здоровье и экономическое положение не только пациентов, но и общества в целом. Ежегодно депрессивные состояния регистрируются более чем у 350 млн человек [1], при этом в общей популяции их распространенность в течение жизни варьирует от 10 до 15% [2]. По прогнозам специалистов, к 2020 г. депрессия займет 2-е место по показателю DALY (количество утраченных лет жизни с поправкой на длительность инвалидизации) для всех возрастных групп [3]. Аналогичный сценарий прогнозируется и для России, где распространенность депрессивной патологии в течение жизни и на текущий момент оценивается в недавних исследованиях в 30 и 20,7%, соответственно [4], с высокими показателями заболеваемости как среди женщин (44%), так и мужчин (23%) [5]. Известны биохимические, эндокринные, нейрофизиологические, психологические и социально-экономические факторы, способствующие развитию депрессии. В частности, значимое влияние на развитие депрессивных симптомов оказывают социальные условия [6]. Это особенно наглядно проявляется в нашем государстве, где социальные сдвиги последних десятилетий стали причиной значительного психологического неблагополучия и повысили частоту возникновения гипотимических состояний и других психических нарушений [5]. Депрессивные расстройства в общей популяции требуют пристального внимания, так как они ухудшают социальное функционирование и работоспособность индивидуума, заметно сказываются на его физическом здоровье и качестве жизни (КЖ) [7]. Более того, депрессия как сопутствующее расстройство [8] на фоне такой распространенной нозологической формы, как шизофрения [9], нередко реализуется в виде психогенных нарушений и ухудшает течение первичного заболевания [10]. Очевидно, что заболеваемость, обусловленная этим распространенным состоянием, должна быть сведена к минимуму прежде всего за счет высокого качества первичной медицинской помощи.
В настоящее время для лечения депрессивных расстройств применяют разные антидепрессанты, например, трициклические антидепрессанты, ингибиторы моноаминоксидазы и т.д., но во всем мире для более широкого применения рекомендованы селективные ингибиторы обратного захвата серотонина (СИОЗС) [11, 12]. Механизм действия СИОЗС основан на селективном подавлении обратного захвата нейротрансмиттера серотонина, который улучшает проведение нервных сигналов, таким образом редуцируя симптомы депрессии и улучшая психическое состояние [12]. С точки зрения эффективности, эти препараты равноценны трициклическим антидепрессантам, но предпочтительны в терминах безопасности и переносимости [13]. Национальный институт здоровья и клинического совершенства (National Institute for Health and Clinical Excellence – NICE, Великобритания) рекомендует применять генерические формы СИОЗС с учетом возможных побочных эффектов и предпочтений пациента [14].
Один из СИОЗС – флувоксамин – утвержден во многих странах для лечения депрессии [15]. Препарат отличается оптимальными фармакокинетическими свойствами, благодаря которым его можно принимать в течение дня однократно [16]; установлено, что по терапевтической эффективности флувоксамин превосходит имипрамин у больных с тяжелой депрессией [17, 18]. Терапия флувоксамином также связана с улучшением качества сна [19] и в меньшей мере влияет на массу тела [20].
Хотя флувоксамин давно закрепился на российском рынке и широко используется для лечения депрессивных состояний, его эффективность при применении в контролируемых условиях у тщательно отобранных пациентов [4, 21–23] исследована недостаточно. Также мало информации об эффективности и безопасности флувоксамина при лечении депрессии в неконтролируемых условиях общемедицинской практики.
Проведенное в рамках постмаркетингового надзора настоящее неконтролируемое многоцентровое обсервационное исследование позволяет оценить эффективность и безопасность применения флувоксамина у пациентов с депрессией в повседневной клинической практике на территории Российской Федерации.
Методы
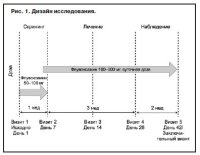
Дизайн исследования

Открытое обсервационное исследование проведено в 11 общеклинических центрах России с ноября 2006 г. по май 2007 г. Пациенты принимали флувоксамин по 50–300 мг 1 раз в день в течение 6 нед, выполняя плановые визиты в дни 1, 7, 14, 28 и 42 (рис. 1).
Рекомендованная начальная доза составила 50–100 мг 1 раз в день, при необходимости дозу увеличивали на 50 мг в неделю до максимальной 300 мг в день в зависимости от клинического ответа на терапию; дозы более 150 мг в день делили на несколько приемов.
Исследование проведено в соответствии с этическими принципами Хельсинкской Декларации и Европейскими рекомендациями Надлежащей клинической практики, применимыми регуляторными требованиями и утвержденным протоколом.
Пациенты
В исследование включены амбулаторные пациенты – взрослые мужчины и женщины не моложе 18 лет с диагнозом депрессии по Diagnostic and Statistical Manual of mental disorders – DSM-IV (4-е издание) и оценками 17 и более по 17-пунктовой Шкале депрессии Гамильтона (HAMD-17).
Из исследования исключали больных с подтвержденной недостаточностью печени или почек и гиперчувствительностью к препарату. Также критерием исключения были применение тизанидина или необратимых ингибиторов моноаминоксидазы в течение 2 нед до первоначального визита, а также беременность и лактация. В период наблюдения не допускался прием других антидепрессантов (кроме флувоксамина), седативных препаратов, транквилизаторов, нейролептиков, антипсихотических препаратов, наркотиков, противосудорожных препаратов, антикоагулянтов и таких препаратов, как цизаприд, пропранолол, теофиллин, циклоспорин, метадон, мексилетин, такрин, метопролол, терфенадин и астемизол. Все пациенты могли в любое время отказаться от участия в исследовании.
Оценка эффективности
За первичные конечные точки эффективности было принято изменение стартового общего балла HAMD-17 и оценки Clinical Global Impression Scale (CGI). Общие баллы HAMD-17 оценивали исходно и в дни исследования 7, 14, 28 и 42-й (или при досрочном выбывании из исследования), а оценки CGI исходно и на 42-й день.
Вторичной конечной точкой эффективности было изменение качества сна по оценкам в пунктах 4, 5 и 6 шкалы HAMD-17 за 6 нед.
Оценка безопасности

Переносимость и безопасность оценивали по спонтанно сообщаемым нежелательным лекарственным явлениям (НЛЯ), серьезным НЛЯ и антропометрическим показателям (индекс массы тела – ИМТ). Также учитывали прием всей сопутствующей лекарственной терапии и измеряли систолическое артериальное давление, диастолическое артериальное давление и частоту сердечных сокращений исходно и на 42-й день.
Статистический анализ
Размер выборки в рамках протокола формально не рассчитывался, но, исходя из соображений выполнимости исследования, было запланировано включить 300 пациентов. Анализ безопасности был проведен на всех пациентах, которые приняли хотя бы одну дозу исследуемого препарата (популяция безопасности), а анализ эффективности – на всех пациентах популяции безопасности, которым измерение эффективности после исходного (популяция ITT) проводилось хотя бы однократно.
Для обобщения демографических переменных использовали дескриптивные статистики. Изменения всех показателей эффективности относительно исходных были представлены дескриптивными статистиками, включая 95% доверительные интервалы и t-тест для одной выборки. Конечная точка относилась к последнему измерению, осуществленному на визите после исходного.
Безопасность оценивали в первую очередь по НЛЯ. Все возникшие во время лечения НЛЯ регистрировались, кодировались по MedDRA и представлялись в итоговых таблицах с количеством и процентом больных, сообщивших о данном НЛЯ.
Результаты
Распределение пациентов, исходные демографические и клинические характеристики
Всего были отобраны 293 пациента, которым было проведено лечение исследуемым препаратом – флувоксамином. До окончания срока исследования [(6 нед) 15 больных выбыли по следующим причинам: НЛЯ (n=8; чаще всего тошнота (n=3)], отсутствие эффективности (n=3), потеря для наблюдения (n=2) и отзыв согласия (n=2). За время исследования не было отмечено ни одного клинически значимого нарушения протокола.
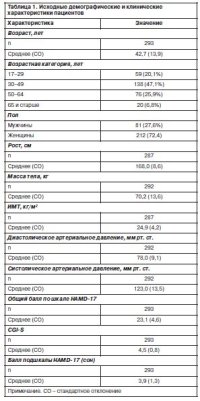
Исходные характеристики пациентов приведены в табл. 1.
Средний возраст 42,7 года, ИМТ 24,9 кг/м2, большинство пациентов – женщины (72%). Из сопутствующих медицинских состояний чаще всего упоминались сердечно-сосудистые заболевания (15%), травмы черепа (13,0%) и другие психические заболевания, кроме депрессии (9,9%). У 9 больных отмечено злоупотребление психоактивными препаратами/алкоголем (3,1%).
Из сопутствующих препаратов чаще всего упоминались седативные (23,9%), сердечно-сосудистые средства (12,6%), противосудорожные (9,6%) и антипсихотичекие препараты (9,6%). Комбинированная терапия антидепрессантами была назначена 7 (2,4%) пациентам.
Переменные эффективности – общий балл HAMD-17

На рис. 2 приводится среднее изменение общего балла HAMD-17 по визитам. Средний (±СО) общий балл HAMD-17 на старте исследования – 23,1±4,6 – устойчиво снижался до 5,8±4,3 на заключительном визите 42-го дня [D; 95% ДИ -17,3(-18,0; -16,7)].
В общем за время от первоначального до заключительного визита на 42-й день произошла редукция среднего балла HAMD-17 на 74,89%.
Подшкала HAMD-17 (сон)
Средняя (±СО) оценка качества сна по подшкале HAMD-17 снизилась с исходной 3,9±1,3 до 0,6±0,8 на заключительном визите на 42-й день [D; 95% ДИ -3,4 (-3,53; -3,20)]. В конечной точке средний балл составлял 0,7±1,0 (рис. 3).
Оценки CGI

Средняя оценка тяжести по шкале CGI снизилась от исходной 4,5 (средней тяжести/тяжелое заболевание) до 2,4 (пограничное состояние или легкое заболевание) на 42-й день. В общем к концу лечения (42-й день) средние баллы по CGI уменьшились на 46,67%. Судя по оценкам тяжести состояния по шкале CGI и оценкам КЖ, к 42-му дню состояние более 85% пациентов «намного улучшилось» или «очень заметно улучшилось» (рис. 4).
К концу лечения (42-й день) состояние (по шкале CGI) 20,8% пациентов (n=58) было нормальным (отсутствие заболевания). Клиническое состояние, классифицируемое как «пограничное», значительно улучшилось по сравнению с исходным в этой категории (40,9% vs 0,7%); табл. 2.
Большинство больных и исследователей оценили лечение как хорошее (66,67%) или отличное (20–21%).
Безопасность и переносимость

За 6 нед хотя бы одна НЛЯ возникла у 72 (24,6%) пациентов; табл. 3.
Большинство НЛЯ были легкими или умеренными по тяжести. Чаще всего пациенты жаловались на тошноту (37; 12,6%) и сонливость (15; 5,1%). Не было сообщений о летальных исходах или серьезных НЛЯ, но 8 больных прекратили лечение из-за НЛЯ. Единственными тяжелыми НЛЯ были тошнота (у 2 пациентов), сонливость и диарея (по 1 пациенту). Клинически значимых изменений витальных признаков, массы тела, ИМТ, частоты сердечных сокращений, систолического и диастолического артериального давления обнаружено не было.
Обсуждение
Несмотря на то что бремя депрессивных расстройств на территории РФ достаточно велико, исследования, посвященные рутинной терапии этого заболевания, малочисленны. Предпочтительным препаратом для лечения депрессии считается флувоксамин, но его эффективность в условиях повседневной клинической практики в России не исследована. Данное обсервационное исследование позволило установить эффективность терапии флувоксамином, о чем свидетельствует значительное улучшение общих баллов HAMD-17 и оценок CGI. Предпринятое исследование стало первым открытым обсервационным анализом эффективности и безопасности терапии на основе флувоксамина у российских пациентов с депрессией в неконтролируемых условиях.
Высокая доля женщин среди пациентов с депрессией (72%) в данном исследовании согласуется с данными других публикаций [24, 25] о более высокой распространенности депрессии среди женщин, чем мужчин, по отечественным данным; сходное соотношение наблюдается и в других странах мира.
Показатели эффективности в этом исследовании сопоставимы с результатами других исследований того же препарата, проведенных в Европе и других регионах
[19, 26–28]. Наблюдаемая редукция балла HAMD-17 на 75% при приеме флувоксамина близка к клинически значимому изменению на 71%, зафиксированному в одном из зарубежных исследований [29]. В отличие от остальных антидепрессантов флувоксамин быстро начинает действовать, что имеет большое значение, так как при отсутствии лечения на ранних стадиях заболевания пациентов велик риск аутоагрессивного поведения. Благодаря быстрому началу антидепрессивного действия препарата (снижение балла HAMD-17 уже через 7 дней от начала терапии) повышается приверженность больных лечению и сокращается частота отказа от терапии ввиду отсутствия эффекта. Этот факт подтвержден результатами зарубежного исследования [30]. Полученные данные коррелируют с таковыми, полученными при двойном слепом исследовании, в котором показано, что терапевтическое действие флувоксамина наступало раньше, чем при приеме других СИОЗС [19].
Как и общий балл HAMD-17, динамика баллов по шкале CGI также была положительной. В конечной точке зафиксирована редукция средней оценки по тяжести состояния на 46,67%, состояние 20,8% пациентов квалифицировалось на основании оценок по шкале CGI как «нормальное» и «отсутствие заболевания». В более ранних исследованиях сообщалось о значительно большем количестве ответов и большей редукции тяжести по показателям CGI при лечении флувоксамином по сравнению с другими СИОЗС на 2-й неделе, но не через 4 и 6 нед [19]. Мы оценивали состояние пациентов по шкале CGI исходно и на 6-й неделе (42-й день) и подтвердили благоприятный ответ на флувоксамин также и на 6-й неделе.

Факт о снижении КЖ при депрессии общеизвестен [31]. Это исследование продемонстрировало улучшение КЖ больных за 6 нед лечения, что коррелирует с результатами других исследований [26, 32]. Также отмечено улучшение качества сна (оценки по подшкале HAMD-17), что, соответственно, согласуется с данными исследований предыдущих лет [19, 33], в которых скорость редукции депрессивной симптоматики и оптимизации качества ночного сна под действием флувоксамина наступали значимо быстрее, чем при применении других СИОЗС. В этом исследовании флувоксамин продемонстрировал хорошую безопасность и благоприятный профиль переносимости. Из нежелательных реакций пациенты чаще всего сообщали о тошноте и сонливости. Эти результаты совпадают с данными предыдущих работ [20, 34–36]. В нашем исследовании терапия флувоксамином не привела к заметным изменениям массы тела или ИМТ, что особо благоприятно сказывается на приверженности лечению контингента пациентов, нуждающегося в долгосрочном приеме антидепрессанта [20].
Хотя открытые, неконтролируемые исследования имеют свои ограничения, рутинные условия проведения терапии в большей степени приближают ее к реальной клинической практике, чем двойное слепое исследование. Ограничением исследования была его короткая продолжительность, что не позволило собрать информацию о рецидивах и продолжительности ремиссии у пациентов с депрессией.
Выводы
Терапия флувоксамином в стандартных условиях приводила к заметной положительной динамике по шкалам HAMD-17 и CGI в изученной выборке пациентов с депрессией, обладала хорошим профилем эффективности, безопасности и переносимости.
Конфликт интересов
Данное исследование профинансировано компанией «Solvay Pharmaceuticals» в России.
Сведения об авторах
Смулевич Анатолий Болеславович – д-р мед. наук, проф., акад. РАН, засл. деят. науки РФ, рук. отд. по изучению пограничной психической патологии и психосоматических расстройств ФГБНУ НЦПЗ, зав. каф. психиатрии и психосоматики ИПО ГБОУ ВПО Первый МГМУ им. И.М. Сеченова, рук. межклинического психосоматического отд-ния Клинического центра ГБОУ ВПО Первый МГМУ им. И.М.Сеченова
Ильина Наталья Алексеевна – д-р мед. наук, вед. науч. сотр. отд. по изучению пограничной психической патологии и психосоматических расстройств ФГБНУ НЦПЗ
Читлова Виктория Валентиновна – канд. мед. наук, ст. науч. сотр. отд. по изучению пограничной психической патологии и психосоматических расстройств ФГБНУ НЦПЗ, доц. отд. по подготовке специалистов в области психиатрии, ассистент каф. психиатрии и психосоматики ИПО ГБОУ ВПО Первый МГМУ им. И.М.Сеченова. E-mail: zoigrek@mail.ru
Список исп. литературыСкрыть список1. Depression: a Global Public Health Concern. World Health Organization 2012.
2. Lépine JP, Briley M. The Increasing Burden of Depression. J Neuropsychiatr Disease Treat 2011; 7: 3–7.
3. Reddy MS. Depression: The Disorder and the Burden. Indian J Psychol Med 2010; 32: 1–2.
4. Pakriev S, Kovalev J, Mozhaev M. Prevalence of Depression in a General Hospital in Izhevsk, Russia. Nordic J Psychiatry 2009; 63: 469–74.
5. Bobak M, Pikhart H, Pajak A et al. Depressive Symptoms in Urban Population Samples in Russia, Poland and the Czech Republic. Br J Psychiatry 2006; 188: 359–65.
6. Nicholson A, Pikhart H, Pajak A et al. Socio-economic Status over the Life-Course and Depressive Symptoms in Men and Women in Eastern Europe. J Affect Disord 2008; 105: 125–36.
7. Patel D. Depression is the Most Common Mental Disorder in Community Settings, and Is a Major Cause of Disability. Occupat Medicine (London) 2008; 58: 453.
8. Гурович И.Я., Шмуклер А.Б., Сторожакова Я.А. и др. Частота выявления депрессивных нарушений и их терапия при шизофрении и расстройствах шизофренического спектра в клинической практике в России. Журн. неврологии и психиатрии им. С.С.Корсакова. 2013; 113 (11–2): 28–33. / Gurovich I.Ia., Shmukler A.B., Storozhakova Ia.A. i dr. Chastota vyiavleniia depressivnykh narushenii i ikh terapiia pri shizofrenii i rasstroistvakh shizofrenicheskogo spektra v klinicheskoi praktike v Rossii. Zhurn. nevrologii i psikhiatrii im. S.S.Korsakova. 2013; 113 (11–2): 28–33. [in Russian]
9. Смулевич А.Б., Дробижев М.А., Иванов С.В. Шизофрения и расстройства шизофренического спектра в соматическом стационаре. Журн. неврологии и психиатрии им. С.С.Корсакова. 2002; 7: 9–13. / Smulevich A.B., Drobizhev M.A., Ivanov S.V. Shizofreniia i rasstroistva shizofrenicheskogo spektra v somaticheskom statsionare. Zhurn. nevrologii i psikhiatrii im. S.S.Korsakova. 2002; 7: 9–13. [in Russian]
10. Смулевич А.Б. Депрессии и шизофрения. Журн. неврологии и психиатрии им. С.С.Корсакова. 2003; 103: 4–13. / Smulevich A.B. Depressii i shizofreniia. Zhurn. nevrologii i psikhiatrii im. S.S.Korsakova. 2003; 103: 4–13. [in Russian]
11. Козырев В.Н., Смулевич А.Б., Дробижев М.Ю. и др. Психотропные средства, применяемые в психиатрическом стационаре (фармакоэпидемиологические аспекты). Журн. неврологии и психиатрии им. С.С.Корсакова. 2003; 103: 25–32. / Kozyrev V.N., Smulevich A.B., Drobizhev M.Iu. i dr. Psikhotropnye sredstva, primeniaemye v psikhiatricheskom statsionare (farmakoepidemiologicheskie aspekty). Zhurn. nevrologii i psikhiatrii im. S.S.Korsakova. 2003; 103: 25–32. [in Russian]
12. Comparative Effectiveness of Second-Generation Antidepressants in the Pharmacologic Treatment of Adult Depression. Eds. G.Gartlehner, R.A.Hansen, P.Thieda et al. Agency for Healthcare Research and Quality, Rockville 2007.
13. Von Wolff A, Hölzel LP, Westphal A et al. Selective Serotonin Reuptake Inhibitors and Tricyclic Antidepressants in the Acute Treatment of Chronic Depression and Dysthymia: A Systematic Review and Meta-Analysis. J Affect Disord 2013; 144: 7–15.
14. National Institute for Health and Clinical Excellence Depression: The Treatment and Management of Depression in Adults (Update). National Clinical Practice Guideline [CG90] 2009.
15. Hachisu M, Ichimaru Y. Pharmacological and Clinical Aspects of Fluvoxamine (Depromel): The First Selective Serotonin Reuptake Inhibitor Approved for Clinical Use Employed in Japan. Folia Pharmac Japonica 2000; 115: 271–9.
16. Hrdina PD. Pharmacology of Serotonin Uptake Inhibitors: Focus on Fluvoxamine. J Psychiat Neurosci 1991; 16: 10–8.
17. Fabre L, Birkhimer LJ, Zaborny BA et al. Fluvoxamine versus Imipramine and Placebo: A Double-Blind Comparison in Depressed Patients. Int Clin Psychopharmacol 1996; 11: 119–27.
18. Kasper S, Möller HJ, Montgomery SA, Zondag E. Antidepressant Efficacy in Relation to Item Analysis and Severity of Depression: A Placebo-Controlled Trial of Fluvoxamine versus Imipramine. Int Clin Psychopharmacol 1995; 9: 3–12.
19. Dalery J, Honig A. Fluvoxamine versus Fluoxetine in Major Depressive Episode: A Double-Blind Randomized Comparison. Human Psychopharmacol 2003; 18: 379–84.
20. Westenberg HG, Sandner C. Tolerability and Safety of Fluvoxamine and Other Antidepressants. Int J Clin Practice 2006; 60: 482–91.
21. Пантелеева Г.П., Абрамова Л.И., Коренев А.Н. Ингибиторы обратного захвата серотонина в лечении разных типов эндогенных депрессий. Журн. неврологии и психиатрии им. С.С.Корсакова. 2000; 100: 36–41. / Panteleeva G.P., Abramova L.I., Korenev A.N. Ingibitory obratnogo zakhvata serotonina v lechenii raznykh tipov endogennykh depressii. Zhurn. Nevrologii i psikhiatrii im. S.S.Korsakova. 2000; 100: 36–41. [in Russian]
22. Шейфер М.С., Цыбина М.И., Давыденко М.В. Флувоксамин (феварин) в терапии депрессии. Журн. неврологии и психиатрии им. С.С.Корсакова. 2000; 100: 64–7. / Sheifer M.S., Tsybina M.I., Davydenko M.V. Fluvoksamin (fevarin) v terapii depressii. Zhurn. nevrologii i psikhiatrii im. S.S.Korsakova. 2000; 100: 64–7. [in Russian]
23. Незнамов Г.Г., Сюняков С.А., Телешова Е.С. и др. Терапевтическое действие и эффективность феварина (флувоксамина) у больных с непсихотическими тревожными апатоадинамическими депрессиями. Журн. неврологии и психиатрии им. С.С.Корсакова. 2001; 101: 19–24. / Neznamov G.G., Siuniakov S.A., Teleshova E.S. i dr. Terapevticheskoe deistvie i effektivnost' fevarina (fluvoksamina) u bol'nykh s nepsikhoticheskimi trevozhnymi apatoadinamicheskimi depressiiami. Zhurn. nevrologii i psikhiatrii im. S.S.Korsakova. 2001; 101: 19–24. [in Russian]
24. Averina M, Nilssen O, Brenn T et al. Social and Lifestyle Determinants of Depression, Anxiety, Sleeping Disorders and Self-Evaluated Quality of Life in Russia – A Population-Based Study in Arkhangelsk. Soc Psychiatry Psychiatr Epidemiol 2005; 40: 511–8.
25. Gafarov VV, Panov DO, Gromova EA et al. The Influence of Depression on Risk Development of Acute Cardiovascular Diseases in the Female Population Aged 25–64 in Russia. Int J Circumpolar Health 2013.
26. Sonawalla SB, Spillmann MK, Kolsky AR et al. Efficacy of Fluvoxamine in the Treatment of Major Depression with Comorbid Anxiety Disorders. J Clin Psychiatry 1999; 60: 580–3.
27. Furuse T, Hashimoto K. Fluvoxamine Monotherapy for Psychotic Depression: The Potential Role of Sigma-1 Receptors. Ann General Psychiatry 2009; 8: 26.
28. Kishimoto A, Todani A, Miura J et al. The Opposite Effects of Fluvoxamine and Sertraline in the Treatment of Psychotic Major Depression: A Case Report. Ann General Psychiatry 2010; 9: 23.
29. Zohar J, Keegstra H, Barrelet L. Fluvoxamine as Effective as Clomipramine against Symptoms of Severe Depression: Results from a Multicentre, Double-Blind Study. Hum Psychopharmacol 2003; 18: 113–9.
30. Katoh Y, Uchida S, Kawai M et al. Onset of Clinical Effects and Plasma Concentration of Fluvoxamine in Japanese Patients. Biol & Pharmaceut Bull 2010; 33: 1999–2002.
31. Rapaport MH, Clary C, Fayyad R, Endicott J. Quality-of-Life Impairment in Depressive and Anxiety Disorders. Am J Psychiatry 2005; 162: 1171–8.
32. Stein M, Fyer A, Davidson J et al. Fluvoxamine Treatment of Social Phobia (Social Anxiety Disorder): A Double-Blind, Placebo-Controlled Study. Am J Psychiatry 1999; 156: 756–60.
33. Wilson SJ, Bell C, Coupland NJ, Nutt DJ. Sleep Changes During Long-Term Treatment of Depression with Fluvoxamine – A Home-Based Study. Psychopharmacology 2000; 149: 360–5.
34. Irons J. Fluvoxamine in the Treatment of Anxiety Disorders. Neuropsych Dis Treat 2005; 1: 289–99.
35. Horii A, Uno A, Kitahara T et al. Effects of Fluvoxamine on Anxiety, Depression, and Subjective Handicaps of Chronic Dizziness Patients with or Without Neuro-Otologic Diseases. J Vestibul Res 2007; 17: 1–8.
36. Omori IM, Watanabe N, Nakagawa A et al. Fluvoxamine versus Other Anti-Depressive Agents for Depression. Cochrane Database Syst Rev 2010; 17 (3); Article ID: CD006114.
10 февраля 2016
Количество просмотров: 2450


