Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
RUDN
Abstract
The main goals of the treatment of schizophrenia, along with the relief of exacerbation, are to improve the functioning, readaptation and resocialization of the patient at all stages of the disease. The most effective method of achieving improved functioning and readaptation of patients is an integrated approach to therapy, including a combination of pharmacotherapy with psychosocial interventions.
An important medical task should be considered to establish the mutual influence of factors that potentially determine the effectiveness of complex therapy on functional outcomes in patients. The links between the effectiveness factors (psychopathological, personal, social, therapy-related) of complex therapy and functional outcomes are very diverse and nonlinear.
Various forms and combinations of psychosocial interventions (psychoeducation, cognitive behavioral therapy, cognitive remediation, social skills training, supported employment programs) along with effective antipsychotic pharmacotherapy can meet the individual needs of patients, including correction of negative symptoms and cognitive disorders, reintegration into society, assistance to recovery, assistance to patients and their families, which, in particular ultimately, it improves the quality of life and the level of functioning of the patient.
The inclusion in the complex therapy of schizophrenia of the atypical third-generation antipsychotic сariprazine (Reagilа), whose pharmacokinetic and pharmacodynamic characteristics, along with its high effectiveness against acute and chronic negative, cognitive, affective symptoms of schizophrenia, allow us to solve many problems of leveling the influence of such factors of incompetence as low criticism of one's condition, severity of symptoms, neurocognitive disorders, lack of positive dynamics, ineffectiveness of therapy, NYA, complexity of the treatment regimen, polyprogmasia and increased influence on the outcomes of complex therapy of schizophrenia.
Keywords: schizophrenia, complex therapy, psychosocial interventions, antipsychotics, сariprazine (Reagila).
For citation: V.E. Medvedev. Complex therapy of schizophrenia: problems and solutions. Psychiatry and psychopharmacotherapy. 2023; 5: 29–42.
Шизофрения – это хроническое психическое расстройство с тяжелым течением. Шизофрения входит в 15 ведущих причин инвалидности во всем мире [1]: продолжительность жизни больных шизофренией короче, чем в среднем по популяции; они более подвержены риску суицида и соматических заболеваний (включая сердечно-сосудистые, пульмонологические, онкологические заболевания и ожирение). Качество жизни пациентов снижено, а функциональные исходы, как правило, неблагоприятны [2-8]. Только 15% больных достигают соответствия критериям клинического выздоровления [9-11].
Клинические фенотипы шизофрении обусловлены взаимодействием генетических, биологических, психологических, социальных и средовых факторов и психопатологически гетерогенны, а также отличаются по факторам риска сопутствующих заболеваний, ответа на лечение и индивидуальных особенностей течения [12-21].
Основными целями лечения шизофрении наряду с купированием обострения являются улучшение функционирования («функциональные исходы») и реадаптация пациента в социуме на всех стадиях заболевания. Нарушения функционирования проявляются неудовлетворительным уровнем самообслуживания, межличностных отношений, бытовых навыков и трудоспособности даже в периоды ремиссии и отсутствия острого психоза [4, 6, 15, 22-23].
Наиболее эффективным методом достижения улучшения функционирования и реадаптации пациентов является комплексный подход в терапии, включающий сочетание фармакотерапии с психосоциальными вмешательствами. Подобный подход позволяет успешнее решать сложные клинические задачи, такие как коррекция негативных симптомов и когнитивных расстройств, которые лежат в основе большей части функциональных нарушений у больных шизофренией и плохо поддаются лечению как типичными антипсихотиками первого поколения, так и многими атипичными антипсихотиками второго поколения.
Повышение уровня знаний о факторах, влияющих на эффективность комплексной терапии, – важный шаг на пути к эффективному лечению шизофрении.
Цель настоящего обзора – установление взаимного влияния факторов (Табл. 1), которые потенциально определяют эффективность комплексной терапии в отношении функциональных исходов у пациентов.
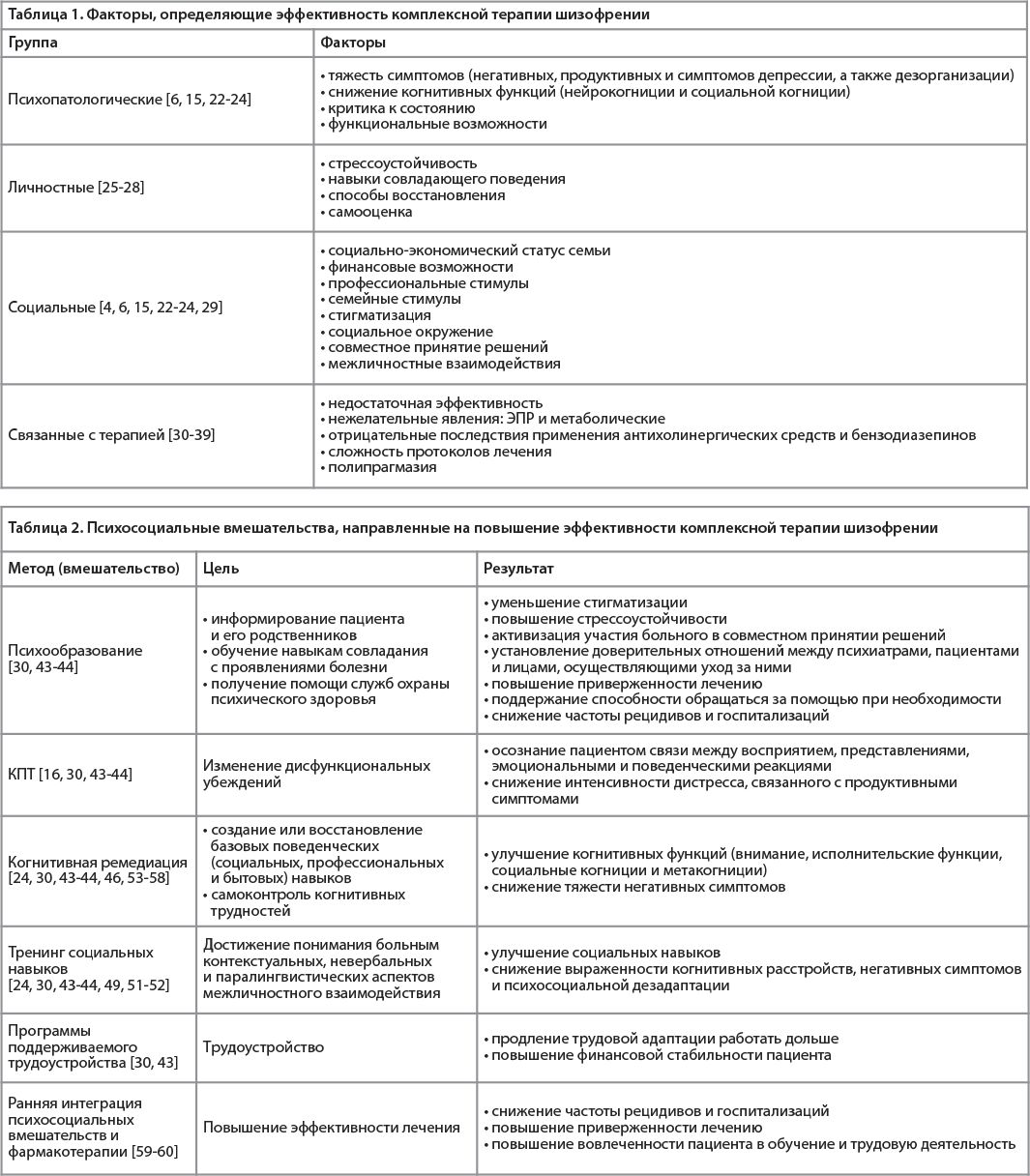
Связи между факторами эффективности комплексной терапии и функциональными исходами весьма разнообразны и нелинейны [6, 15, 23, 40-41]. Например, нейрокогниция влияет на показатели бытовых и трудовых навыков посредством изменения функциональных возможностей, социальной когниции, медико-социальной помощи и интернализованной стигмы, которая, в свою очередь, косвенно связана с функциональным исходом через стрессоустойчивость [6, 40]. Негативные симптомы, относящиеся к домену «опыта» (абулия, ангедония и асоциальность), влияют на функциональный исход, особенно на сферу межличностных отношений, как прямо, так и косвенно, через интернализованную стигму, стрессоустойчивость и использование медико-социальной помощи [6, 40] и т.д.
Таким образом, понимание сложных взаимосвязей между перечисленными факторами и функциональными исходами может способствовать внедрению комплексных программ лечения (психосоциальных вмешательств и фармакотерапии), нацеленных на восстановление больного шизофренией. Такие программы могут быть подобраны индивидуально в соответствии с потребностями больных. Они позволят снизить тяжесть симптомов и улучшить функциональные исходы, что повысит вероятность функционального восстановления [30, 43-44].
К настоящему моменту разработаны различные формы и комбинации психосоциальных вмешательств, которые позволяют удовлетворить индивидуальные потребности пациентов [30, 42-44], включая коррекцию негативных симптомов и когнитивных расстройств [30, 42-43, 45], реинтеграцию в общество, содействие восстановлению, помощь больным и их семьям [30, 42-43] (Табл. 2), что в конечном итоге повышает качество жизни и уровень функционирования больного.
Психообразование – это вмешательство, нацеленное на информирование пациента и его родственников о психическом расстройстве и возможном лечении.
Когнитивно-поведенческая терапия (КПТ) – вмешательство, направленное на осознание пациентом связи между восприятием, представлениями, эмоциональными и поведенческими реакциями [46-48].
Когнитивная ремедиация – вмешательство, основанное на формировании поведенческих навыков и нацеленное на улучшение когнитивных функций [46].
Тренинг социальных навыков – метод психосоциальной терапии, основанный на обсуждении контекстуальных (связанных с обстановкой), невербальных (связанных с языком тела) и паралингвистических (связанных с модуляциями голоса) аспектов межличностного взаимодействия [49-50].
Программы поддерживаемого трудоустройства помогают пациентам в рамках конкурентной занятости [30, 43].
Несмотря на признание преимущества комплексных, ранних и персонализированных методов терапии шизофрении, до сих пор недостаточно изучены предикторы ответа на такую терапию. В ряде работ подчеркивается, что при назначении комплексной терапии необходимо учитывать возможное неблагоприятное влияние различных антипсихотиков или сопутствующих препаратов на когнитивные функции, а также на вторичные негативные симптомы [30-31, 33]. Когнитивные нарушения могут усугубляться экстрапирамидными [34-35] или метаболическими нежелательными явлениями (НЯ) антипсихотических средств [36], а также сопутствующим применением антихолинергических препаратов или бензодиазепинов [37-39]. НЯ в виде экстрапирамидных симптомов (ЭПР), седация, продуктивные симптомы или нелеченая депрессия могут стать причиной развития вторичных негативных симптомов и низкой приверженности лечению [30-31] (Табл. 3).
Антипсихотическая терапия при расстройствах шизофренического спектра обеспечивает существенное снижение выраженности симптомов и является обязательным условием клинической стабилизации – состояния, при котором психотические симптомы отсутствуют или характеризуются легкой/средней степенью тяжести и не требуют коррекции терапии и (или) госпитализации [61].
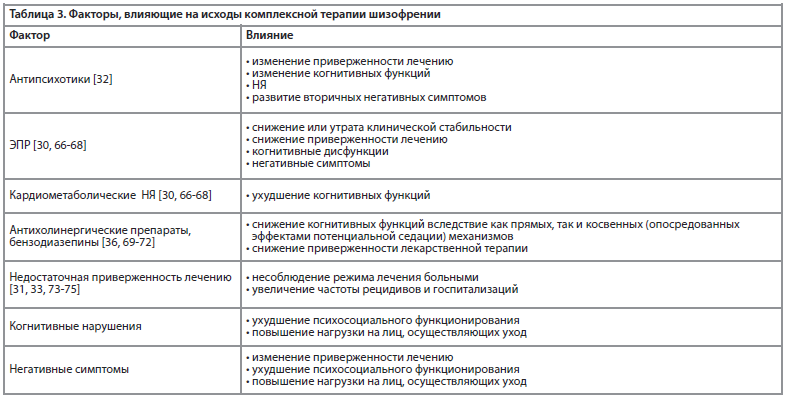
В реальной клинической практике постоянная антипсихотическая терапия необходима для предотвращения обострений и рецидивов [62], а также для применения методов нелекарственной терапии, улучшающих исходы лечения [63-65]. Антипсихотическая терапия включает антипсихотические препараты первого (АПП), второго (АВП) и третьего (АТП, парциальные/частичные агонисты дофаминовых рецепторов) поколений.
Согласно результатам метаанализов, АВП более эффективны, чем АПП [76-78]. Помимо типа антипсихотического препарата, на функциональные исходы у больных шизофренией влияет их доза [36]: при снижении дозы наблюдается улучшение различных когнитивных функций (памяти, зрительно-пространственного восприятия, речи, внимания и долговременной памяти) [36]. Это позволяет предположить, что пациенты с более тяжелым течением заболевания (которым обычно назначают высокие дозы антипсихотиков) получают меньшую пользу от когнитивной ремедиации, либо высокие дозы антипсихотиков ограничивают эффективность вмешательства вследствие развития ЭПС [79-80].
Нежелательные явления могут уменьшать приверженность лечению, что, в свою очередь, сопровождается снижением или утратой клинической стабильности и, как следствие, влияет на результаты комплексной терапии [30, 66-68].
Наиболее частые НЯ АПП связаны с неврологическими побочными эффектами, а антипсихотиков второго поколения (АВП) – с увеличением массы тела и метаболическими нарушениями [35, 81-85]. АТП значительно реже влияют на массу тела или вызывают двигательные НЯ [24, 35, 86-87].
Более высокая частота развития ЭПС при терапии АПП по сравнению с АВП и АТП может стать причиной неудовлетворительной приверженности лечению и усугублять когнитивные нарушения, приводить к развитию вторичных негативных симптомов, что оказывает опосредованное влияние на результаты комплексной терапии [24, 35, 86-87].
Метаболический синдром встречается примерно у 33,5% пациентов с шизофренией [88]. Развитие этого синдрома сопряжено с различными факторами риска: образом жизни (курением, неправильным питанием, низкой физической активностью, применением антипсихотических препаратов), а также с генетическими факторами, которые имеют отношение к шизофрении и/или ответу на лечение и взаимодействуют с генами, связанными с метаболическими функциями [88].
Кардиометаболические эффекты (увеличение массы тела и метаболический синдром) могут оказывать неблагоприятное влияние на когнитивные функции (скорость обработки информации, память, внимание, логическое мышление и решение задач) у пациентов с шизофренией [89-91], тем самым ухудшая результаты комплексной терапии.
Другие НЯ, которые в разной степени присущи всем антипсихотическим препаратам, включают изменения электрической активности сердца, гиперпролактинемию, антихолинергические эффекты, седацию, снижение порога судорожной готовности, сиалорею, нейтропению и агранулоцитоз, а также злокачественный нейролептический синдром [92-95].
Помимо антипсихотиков, многим пациентам с шизофренией назначаются и другие типы лекарственных средств, такие как антихолинергические препараты, бензодиазепины, антидепрессанты и стабилизаторы настроения. При этом длительное комбинированное применение бензодиазепинов с антипсихотиками приводит к снижению когнитивных функций вследствие как прямых, так и косвенных механизмов (опосредованных эффектами потенциальной седации) [36, 69-72].
Длительное применение антихолинергических препаратов, часто используемых для снижения тяжести ЭПР, связано с низкой приверженностью лекарственной терапии [72] и усугублением уже существующих когнитивных нарушений (например, скорости обработки информации, внимания, речи, решения задач и психомоторной активности) [38-39, 69, 96-102].
Длительное применение бензодиазепинов отрицательно влияет на познавательные процессы, причем неблагоприятным изменениям подвержены такие специфические когнитивные функции, как внимание и кратковременная память [37].
Низкая приверженность лечению наблюдается примерно у 50% больных [31] и существенно осложняет оказание медикаментозной помощи [30, 57]. Недостаточная приверженность лечению увеличивает частоту рецидивов и госпитализаций [103]. Однако является ли несоблюдение режима терапии причиной рецидивов и госпитализаций или это показатель прогрессирования заболевания – остается вопросом [30, 104].
На приверженность терапии антипсихотиками влияет несколько факторов: социальных, связанных с самим пациентом и с лекарственной терапией (Табл. 4) [31, 33, 105].
Когнитивные нарушения, определяемые как дефицит различных когнитивных функций (скорости обработки информации, внимания и вигильности, кратковременной памяти, вербальных обучения и памяти, зрительно-пространственных обучения и памяти, логического мышления и решения задач, социальных когниций) [126, 127], представляют собой важнейший аспект, который требует коррекции в рамках комплексного подхода к лечению.
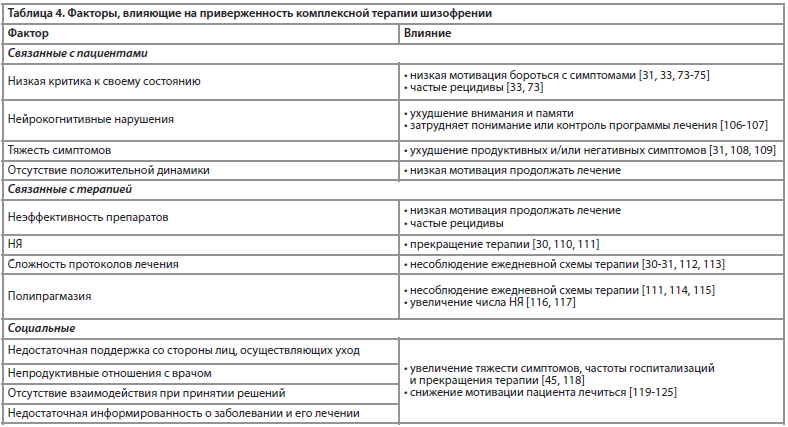
Когнитивные нарушения наблюдаются уже при дебюте и на ранних этапах шизофрении, зачастую предшествуют ему, связаны с неудовлетворительным функционированием в преморбидном периоде и характеризуются повышенной устойчивостью к терапии на всем протяжении болезни [26, 128].
При назначении комплексной терапии, нацеленной на восстановление познавательной деятельности, клиницисты должны учитывать ряд факторов, способных влиять на когнитивные функции: например, тип и дозу применяемых препаратов, приверженность лечению и НЯ фармакотерапии. Во избежание неблагоприятного влияния на когнитивную деятельность практикующие врачи должны отдавать предпочтение препаратам, которые оказывают незначительное влияние на эти функции, и ограничивать применение антихолинергических средств и бензодиазепинов, особенно при длительном лечении [37-39].
В различных обзорах и метаанализах сообщается, что когнитивная ремедиация, тренинг навыков и физические упражнения могут быть эффективными методами лечения и использоваться в составе комплексной терапии для улучшения когнитивных функций у больных шизофренией [52, 54-57, 129-131].
Негативные симптомы, как и когнитивные расстройства, наблюдаются уже при дебюте и на ранних этапах заболевания, могут предшествовать ему, связаны с неудовлетворительным функционированием в преморбидном периоде и отличаются повышенной устойчивостью на всем протяжении заболевания [24, 25, 132].
Негативные симптомы включают абулию, ангедонию и асоциальность, которые относятся к домену «опыта», а также притупленный аффект и алогию, которые составляют домен «дефицита экспрессии» [86, 87, 133-136]. Эти два домена негативных симптомов характеризуются различными патофизиологическими особенностями и разными взаимосвязями с функционированием пациента, что указывает на потенциальные различия в тактике их лечения [6, 15, 40, 136-142].
Важным клиническим вопросом с точки зрения как терапии, так и прогноза остается дифференциация первичных и вторичных негативных симптомов. Действительно, если первичные негативные симптомы зачастую носят стойкий характер и резистентны к лечению [143-144], то вторичные негативные симптомы можно эффективно лечить, воздействуя на факторы, составляющие их основу (например, паркинсонизм, продуктивные симптомы или депрессию) [86, 87].
В клинической практике дифференциация первичных и вторичных негативных симптомов может быть сложной задачей и должна рассматриваться как часть диагностического процесса.
Для оценки вторичного характера негативных симптомов практикующим врачам следует обращать внимание на то, усугубляются ли негативные симптомы в периоды обострения психоза или в результате изменения фармакотерапии, снижается ли их тяжесть по мере купирования галлюцинаций и бреда под действием антипсихотических препаратов. При наличии негативных симптомов, вторичных по отношению к продуктивным, рекомендуется пересмотреть дозу или тип антипсихотического препарата [24, 136, 145, 146].
В отношении антипсихотических препаратов установлено, что у больных шизофренией различные типы антипсихотиков по-разному влияют на негативные симптомы [24, 147]. Выявлено, что среди АВП амисульприд, клозапин, оланзапин, кветиапин и рисперидон более эффективно снижают тяжесть негативных симптомов, чем АПП [148, 149]. При применении атипичных антипсихотиков наблюдаются благоприятные эффекты в отношении преобладающих негативных симптомов [150-152]. Однако клинические данные, включенные в эти метаанализы, очень неоднородны, а подробная информация о характеристиках негативных симптомов (например, о разделении первичных и вторичных негативных симптомов) отсутствует [24, 136, 149].
Согласно выводам нескольких обзоров и метаанализов, эффективной тактикой лечения, используемой в рамках комплексной терапии для снижения тяжести негативных симптомов, может считаться антипсихотическая терапия и ряд психосоциальных вмешательств, таких как когнитивное обучение и тренинг навыков [24, 51-53].
Таким образом, в целях улучшения приверженности терапии больных с расстройствами шизофренического спектра необходимо: 1) снизить тяжесть симптомов; 2) улучшить когнитивные функции; 3) повысить у пациентов критику к своему состоянию; 4) сформировать более терпимое отношение к лекарственным препаратам; 5) по возможности исключить применение полифармакотерапии или сложных схем лечения; 6) привлекать пациентов к процессу принятия решений посредством прочного терапевтического альянса [24, 51-53].
В рамках подхода, ориентированного на функциональное восстановление больных шизофренией, для достижения указанных целей практически единодушно признается необходимость комплексной терапии, включающей психосоциальные вмешательства и фармакологическое лечение [30, 43, 136].
Психосоциальные вмешательства играют важную роль в удовлетворении сложных индивидуальных потребностей пациентов [30, 43, 45, 136], снижении тяжести негативных симптомов и когнитивных нарушений и улучшении реинтеграции в общество. Все это способствует трудоустройству больных, поддержке их и их семей и в конечном итоге функциональному восстановлению [30, 42, 43, 153]. Кроме того, благодаря терапевтическому альянсу психосоциальные вмешательства улучшают понимание пациентом своего заболевания, способствуют соблюдению режима лечения и тем самым снижают риск прекращения терапии и рецидивов.
Эффективные психосоциальные вмешательства, такие как когнитивное обучение и тренинг навыков, должны быть доступны пациентам с нарушением когнитивных функций, низкой социальной адаптацией и негативными симптомами. Кроме того, в клиническую практику необходимо внедрять психообразование и КПТ. Эти методы повышают приверженность лечению, а также уменьшают количество рецидивов и дистресс, связанный с продуктивными симптомами.
Применение антипсихотических препаратов составляет основу лечения, обеспечивающего надежный контроль симптомов и клиническую стабильность [30, 42, 43]. Постоянная антипсихотическая терапия необходима для предотвращения обострений и рецидивов [62]. В свою очередь, клиническая стабильность способствует более продуктивному участию пациента в нефармакологических вмешательствах и повышает вероятность благоприятного исхода [63-65].
В то же время антипсихотическая и сопутствующая терапия, которые обеспечивают эффективный контроль симптомов, нередко вызывают НЯ, способные серьезно влиять на общее состояние здоровья пациента, формировать негативное отношение к лекарственным препаратам и, как следствие, снижать приверженность лечению и эффективность комплексной терапии [30, 36-39, 67]. Учитывая различия индивидуального ответа на доступные препараты и их переносимость, при выборе антипсихотика следует руководствоваться особенностями конкретного пациента, которые включают психопатологические синдромы, физическое здоровье и сопутствующие заболевания [16, 154, 155].
В практическом плане, согласно результатам метаанализов, АВП и АТП эффективнее АПП по критерию улучшения негативных расстройств и когнитивных функций [76-78].
В качестве наиболее отвечающего основным задачам комплексного подхода к терапии пациентов с шизофренией и хорошо переносимого АТП можно рассматривать частичный агонист дофаминовых рецепторов – карипразин (Реагила®).
Карипразин – парциальный агонист дофаминовых D3/D2-рецепторов, с преимущественным связыванием с D3-рецепторами [156-158]. Воздействие карипразина именно на D3-рецепторы в сочетании с его парциальным агонизмом обусловливает выраженный терапевтический эффект карипразина при негативной, когнитивной и аффективной (депрессивной) симптоматике шизофрении [159].
Карипразин также обладает высокой аффинностью к серотониновым рецепторам 5-HT2B (Ki = 0,58 нМ) [160], меньшей – к рецепторам 5-HT1A (Ki = 3 нМ) (действует как частичный агонист для данного рецептора, в то же время являясь антагонистом 5-HT2B). Клинически данные свойства реализуются благоприятным эффектом воздействия на негативные симптомы и когнитивную дисфункцию, что подтверждается результатами доклинических и клинических исследований [161].
Аффинность карипразина в отношении других рецепторов менее выражена. В литературе в этой связи упоминаются 5-HT2A (Ki = 19 нМ), гистаминовый рецептор H1 (Ki = 23 нМ), 5-HT7 (Ki = 111 нМ) и рецепторы человека 5-HT2C (Ki = 134 нМ). В отношении всех изученных адренергических рецепторов карипразин обладает низкой активностью [159].
Метаболизируется карипразин системой цитохрома P450 (CYP3A4) и в меньшей степени – CYP2D6 [162]. В организме образуются два основных активных метаболита карипразина – дезметилкарипразин и дидезметилкарипразин (диноркарипразин). После многократного приема наблюдается кумуляция карипразина и его метаболитов (дезметилкарипразин и дидезметилкарипразин) в плазме. Оба метаболита фармакологически активны и обладают сходным с карипразином рецепторным и фармакологическим профилем. Равновесная концентрация для карипразина и дезметилкарипразина (но не для дидезметилкарипразина) достигается по прошествии 1 недели терапии [163].
Период полувыведения препарата составляет от 2 до 6 суток [163, 164], период полувыведения его активного метаболита дидезметилкарипразина – 2–3 недели [164]. Такой длительный период полувыведения может обеспечивать сохранение эффекта препарата в течение определенного времени после прекращения приема, предотвращая быстрое развитие рецидива в случае несоблюдения режима терапии. Это дает препарату терапевтические преимущества при его применении у больных с пониженной комплаентностью и отказом от приема пролонгированных инъекционных форм антипсихотиков либо с их непереносимостью, а также у пациентов с пониженным уровнем критичности к своему состоянию или с выраженными когнитивными расстройствами, обусловливающими забывчивость при приеме лекарств [159].
Согласно данным многочисленных исследований [165-169] и отечественной практики применения, карипразин в стандартных дозировках 1,5–6,0 мг/сут эффективен на всех этапах лечения шизофрении у больных с гетерогенными проявлениями заболевания: депрессивно-бредовой, апато-абулической, кататонической, неврозоподобной, обсессивно-компульсивной симптоматикой, в том числе резистентной и коморбидной с аддиктивными расстройствами [168-169].
При купировании обострения шизофрении в исследованиях II фазы, а также в плацебо-контролируемых исследованиях III фазы у пациентов с обострением шизофрении фиксируются высокая эффективность и хорошая переносимость карипразина во всех используемых дозах (1,5–6,0 мг/сут) [170, 171]. В исследованиях статистически значимые различия (p<0,001) с плацебо также отмечают на фоне лечения карипразином, уже начиная с первой (карипразин в дозе 6–9 мг/сут) или со второй недели терапии (карипразин в дозе 3–6 мг/сут) и до конца наблюдения [170-172]. Уменьшая продуктивные симптомы шизофрении, карипразин способствует стабилизации состояния пациентов и достижению устойчивой ремиссии.
В клиническом аспекте, как подчеркивается в серии метаанализов исследований купирующей терапии шизофрении карипразином [173-175], применение препарата ассоциируется в первую очередь со статистически достоверным уменьшением агрессивности и других проявлений обострения.
Антинегативный эффект карипразина по шкале PANSS-Factor Score for Negative Symptoms (FSNS), фиксируемый в исследованиях продолжительностью 26 и более недель, наблюдается у большего числа пациентов, чем при терапии рисперидоном (p=0,0022). Кроме того, начиная с десятой недели лечение карипразином по сравнению с терапией рисперидоном характеризуется более выраженным изменением средней исходной общей оценки по шкале PSP (p<0,0001): у пациентов наблюдается более выраженное улучшение по таким субдоменам шкалы, как «самообслуживание», «личностное и социальное функционирование» и «социально полезная деятельность» [176, 177].
В опубликованном метаанализе M. Krause с соавт. (2018), обобщающем данные 21 исследования, авторы приходят к заключению, что из всех атипичных антипсихотиков на сегодняшний день только для карипразина убедительно и методологически корректно доказано преимущество перед рисперидоном в устранении негативной и когнитивной симптоматики шизофрении, протекающей с выраженными или преимущественными негативными и когнитивными расстройствами [178].
Аналогичным образом в недавней публикации I. Laszlovszky с соавт. (2021) указывается, что изменения в сравнении с исходным уровнем по PANSS-FSNS за 6 недель значительно превосходят плацебо для карипразина (1,5-3 мг/день, p=0,0322; 4,5-6 мг/сут, p=0,0038), но не рисперидона (p=0,2204) и арипипразола (p=0,3265). В дальнейшем преимущество в нивелировании персистирующих и доминирующих негативных расстройств карипразина перед рисперидоном подтверждено и через 26 недель этого проспективного исследования [179]. Таким образом, карипразин обладает клинически доказанной эффективностью при терапии негативных симптомов шизофрении и улучшает социальное функционирование пациентов, что способствует их дальнейшему восстановлению.
Положительное влияние на когнитивные функции по каждому пункту когнитивной подшкалы PANSS (p<0,001) констатируется в сравнительных с плацебо и АВП (рисперидон, арипипразол) исследованиях, проводившихся как краткосрочно (6 недель, карипразин 1,5-9 мг/день [180]), так и длительно (26 недель, карипразин 4,5 мг/день, рисперидон 4,0 мг/день [181]). Обладая прокогнитивным эффектом, карипразин может улучшать приверженность пациентов к проводимой терапии шизофрении, что также может способствовать их восстановлению.
Профилактика рецидивов — один из важнейших компонентов комплексного лечения шизофрении. Длительное антипсихотическое лечение может существенно снижать риск развития рецидива в фазе стабилизации заболевания [172].
Результаты многоцентрового двойного слепого плацебо-контролируемого исследования S. Durgam и соавт. (2016), посвященного изучению эффективности, безопасности и переносимости карипразина при долгосрочной (до 72 недель) поддерживающей (противорецидивной) терапии шизофрении у взрослых, свидетельствуют о высокой противорецидивной эффективности препарата. Время до наступления рецидива оказывается значительно дольше в подгруппе карипразина, чем в подгруппе плацебо (p=0,001). Рецидив за время наблюдения наблюдается у 24,8% пациентов, получавших карипразин, и у 47,5%, получавших плацебо (отношение риска [95% ДИ] = 0,45 [0,28, 0,73]). Таким образом, лечение карипразином более чем вдвое снижает вероятность рецидива обострения шизофрении [182].
В другом долгосрочном исследовании подтверждаются как эффективность и безопасность карипразина при длительной противорецидивной терапии шизофрении, так и отдельно его эффективность в устранении негативной, когнитивной и аффективной симптоматики, а также влияние на общее качество жизни больных хронической шизофренией с преобладанием негативной симптоматики в сопоставлении с рисперидоном [176, 177].
Редукция острой психопатологической симптоматики, нивелирование негативных симптомов и улучшение когнитивных процессов у больных шизофренией при применении карипразина во всех исследованиях положительно коррелируют с повышением повседневного социального функционирования, приверженности к терапии и качества жизни [183-185].
В объединенном анализе данных по двум краткосрочным исследованиям пациентов, проходивших лечение острого обострения шизофрении карипразином, качество жизни по опроснику качества жизни SQLS-R4 при оценке общего балла и оценке «жизненных сил» и «психосоциальных факторов» статистически достоверно превосходит плацебо (p<0,0001) к 6-й неделе лечения [139, 186].
При длительном лечении карипразином показатели функционального улучшения (общий балл PSP, параметры: «уход за собой», «общественно полезная деятельность», «личные и социальные отношения», «агрессивное поведение») претерпевают положительную динамику (p<0,01) и сохраняют устойчивость при продолжении терапии препаратом по сравнению с группой больных, у которых препарат замещался плацебо [187, 188].
В сравнении с рисперидоном карипразин также демонстрирует статистически значимую разницу по общему баллу шкалы PSP и в каждом отдельном ее субдомене («уход за собой», «общественно полезная деятельность», «личные и социальные отношения») [189].
Согласно данным E. Rancans с соавт. (2021), у 70% у пациентов перевод на карипразин способствует преодолению терапевтической резистентности или недостаточной эффективности предшествующей антипсихотической (кветиапин, оланзапин, арипипразол, рисперидон, амисульприд и клозапин) терапии шизофрении.
Переносимость карипразина по результатам исследований может быть признана хорошей. Доля больных, выбывающих из исследований в связи с плохой переносимостью препарата, составляет 6-10,8% [173, 186].
Наиболее частыми (частота ≥ 10%) нежелательными явлениями (НЯ), возникающими на фоне приема любой дозировки препарата, являются акатизия, бессонница и головная боль. Не менее чем у 5% пациентов или с частотой, в 2 раза превышающей частоту в группе плацебо, могут развиваться экстрапирамидные расстройства и тремор. Большинство указанных НЯ характеризуется легкой или средней степенью тяжести [172].
Важно особо подчеркнуть, что клинически значимые метаболические изменения в уровне глюкозы крови натощак, липидов крови и пролактина, а также удлинение интервала QTc (>500 мс), изменение уровня артериального давления, офтальмологических нарушений на фоне приема карипразина по данным исследователей не наблюдаются [190-193].
При длительной терапии (48 и более недель) карипразином дисфункции печени не выявляется [190, 191]. Средний уровень пролактина снижается по сравнению с исходным значением. Значимые изменения массы тела (более 7% от исходного) носят разнонаправленный характер: у 33% пациентов отмечается увеличение веса, у 8% – уменьшение. Увеличение массы тела более 7% от исходного на фоне приема карипразина достоверно меньше, чем при приеме рисперидона [189-191].
В ряде краткосрочных и долгосрочных исследований обнаруживается, что карипразин приводит к снижению уровня пролактина на 276,5–362,0 мМЕ/л по сравнению с исходными значениями [190-193]. В открытом исследовании пациентов с шизофренией, принимающих карипразин в дозах от 3 мг/сут в течение двенадцати месяцев, уровень пролактина у пациентов снижается в среднем на 361,7 мМЕ/л по сравнению с исходными [189]. Аналогичным образом регистрируется снижение уровня пролактина при замене ранее назначенного антипсихотика, вызывающего гиперпролактинемию, терапией карипразином [194].
По сравнению с другими современными антипсихотиками (рисперидон, азенапин, луразидон, брекспипразол, арипипразол) карипразин имеет в среднем менее выраженные метаболические НЯ [149, 168]. В частности, он в меньшей степени влияет на массу тела, гиперлипидемию, гипертриглицеридемию, гиперхолестеринемию или гипергликемию, реже вызывает развитие сахарного диабета II типа и метаболического синдрома. Фармакогенная прибавка массы тела больше связана с рисперидоном, чем с карипразином [149, 159, 168]. Очевидно, что карипразин подходит для пациентов с шизофренией и неудовлетворительной переносимостью психофармакотерапии, поскольку хорошо переносится и улучшает приверженность к терапии.
Таким образом, карипразин (Реагила®) может являться фармакологической основой комплексной терапии пациентов с шизофренией. Включение в комплексную терапию шизофрении карипразина, фармакокинетические и фармкодинамические характеристики которого, высокая эффективность в отношении острой и хронической негативной, когнитивной, аффективной симптоматики шизофрении, позволяют решать многие задачи по нивелированию влияния таких факторов приверженности комплексной терапии, как низкая критика к своему состоянию, тяжесть симптомов, нейрокогнитивные нарушения, отсутствие положительной динамики, неэффективность терапии, НЯ, сложность схемы лечения, полипрогмазия и повышению влияния на исходы комплексной терапии шизофрении.
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№05 2023
Комплексная терапия шизофрении: проблемы и решения №05 2023
Номера страниц в выпуске:29-42
Резюме
Основными целями лечения шизофрении наряду с купированием обострения являются улучшение функционирования, реадаптация и ресоциализация пациента на всех стадиях заболевания. Наиболее эффективным методом достижения улучшения функционирования и реадаптации пациентов является комплексный подход в терапии, включающий сочетание фармакотерапии с психосоциальными вмешательствами.
Важной медицинской задачей следует считать установление взаимного влияния факторов, которые потенциально определяют эффективность комплексной терапии на функциональные исходы у пациентов. Связи между факторами эффективности (психопатологические, личностные, социальные, связанные с терапией) комплексной терапии и функциональными исходами весьма разнообразны и нелинейны.
Различные формы и комбинации психосоциальных вмешательств (психообразование, когнитивно-поведенческая терапия, когнитивная ремедиация, тренинг социальных навыков, программы поддерживаемого трудоустройства) наряду с эффективной антипсихотической фармакотерапией позволяют удовлетворить индивидуальные потребности пациентов, включая коррекцию негативных симптомов и когнитивных расстройств, реинтеграцию в общество, содействие восстановлению, помощь больным и их семьям, что в конечном итоге повышает качество жизни и уровень функционирования больного.
Включение в комплексную терапию шизофрении атипичного антипсихотика третьего поколения карипразина (Реагила), фармакокинетические и фармкодинамические характеристики которого наряду с высокой эффективность в отношении острой и хронической негативной, когнитивной, аффективной симптоматики шизофрении, позволяют решать многие задачи по нивелированию влияния таких факторов некомплаентности, как низкая критика к своему состоянию, тяжесть симптомов, нейрокогнитивные нарушения, отсутствие положительной динамики, неэффективность терапии, НЯ, сложность схемы лечения, полипрогмазия и повышению влияния на исходы комплексной терапии шизофрении.
Ключевые слова: шизофрения, комплексная терапия, психосоциальные вмешательства, антипсихотики, карипразин (Реагила®).
Для цитирования: В.Э. Медведев. Комплексная терапия шизофрении: проблемы и решения. Психиатрия и психофармакотерапия. 2023; 5: 29–42.
Основными целями лечения шизофрении наряду с купированием обострения являются улучшение функционирования, реадаптация и ресоциализация пациента на всех стадиях заболевания. Наиболее эффективным методом достижения улучшения функционирования и реадаптации пациентов является комплексный подход в терапии, включающий сочетание фармакотерапии с психосоциальными вмешательствами.
Важной медицинской задачей следует считать установление взаимного влияния факторов, которые потенциально определяют эффективность комплексной терапии на функциональные исходы у пациентов. Связи между факторами эффективности (психопатологические, личностные, социальные, связанные с терапией) комплексной терапии и функциональными исходами весьма разнообразны и нелинейны.
Различные формы и комбинации психосоциальных вмешательств (психообразование, когнитивно-поведенческая терапия, когнитивная ремедиация, тренинг социальных навыков, программы поддерживаемого трудоустройства) наряду с эффективной антипсихотической фармакотерапией позволяют удовлетворить индивидуальные потребности пациентов, включая коррекцию негативных симптомов и когнитивных расстройств, реинтеграцию в общество, содействие восстановлению, помощь больным и их семьям, что в конечном итоге повышает качество жизни и уровень функционирования больного.
Включение в комплексную терапию шизофрении атипичного антипсихотика третьего поколения карипразина (Реагила), фармакокинетические и фармкодинамические характеристики которого наряду с высокой эффективность в отношении острой и хронической негативной, когнитивной, аффективной симптоматики шизофрении, позволяют решать многие задачи по нивелированию влияния таких факторов некомплаентности, как низкая критика к своему состоянию, тяжесть симптомов, нейрокогнитивные нарушения, отсутствие положительной динамики, неэффективность терапии, НЯ, сложность схемы лечения, полипрогмазия и повышению влияния на исходы комплексной терапии шизофрении.
Ключевые слова: шизофрения, комплексная терапия, психосоциальные вмешательства, антипсихотики, карипразин (Реагила®).
Для цитирования: В.Э. Медведев. Комплексная терапия шизофрении: проблемы и решения. Психиатрия и психофармакотерапия. 2023; 5: 29–42.
Complex therapy of schizophrenia: problems and solutions
V.E. MedvedevRUDN
Abstract
The main goals of the treatment of schizophrenia, along with the relief of exacerbation, are to improve the functioning, readaptation and resocialization of the patient at all stages of the disease. The most effective method of achieving improved functioning and readaptation of patients is an integrated approach to therapy, including a combination of pharmacotherapy with psychosocial interventions.
An important medical task should be considered to establish the mutual influence of factors that potentially determine the effectiveness of complex therapy on functional outcomes in patients. The links between the effectiveness factors (psychopathological, personal, social, therapy-related) of complex therapy and functional outcomes are very diverse and nonlinear.
Various forms and combinations of psychosocial interventions (psychoeducation, cognitive behavioral therapy, cognitive remediation, social skills training, supported employment programs) along with effective antipsychotic pharmacotherapy can meet the individual needs of patients, including correction of negative symptoms and cognitive disorders, reintegration into society, assistance to recovery, assistance to patients and their families, which, in particular ultimately, it improves the quality of life and the level of functioning of the patient.
The inclusion in the complex therapy of schizophrenia of the atypical third-generation antipsychotic сariprazine (Reagilа), whose pharmacokinetic and pharmacodynamic characteristics, along with its high effectiveness against acute and chronic negative, cognitive, affective symptoms of schizophrenia, allow us to solve many problems of leveling the influence of such factors of incompetence as low criticism of one's condition, severity of symptoms, neurocognitive disorders, lack of positive dynamics, ineffectiveness of therapy, NYA, complexity of the treatment regimen, polyprogmasia and increased influence on the outcomes of complex therapy of schizophrenia.
Keywords: schizophrenia, complex therapy, psychosocial interventions, antipsychotics, сariprazine (Reagila).
For citation: V.E. Medvedev. Complex therapy of schizophrenia: problems and solutions. Psychiatry and psychopharmacotherapy. 2023; 5: 29–42.
Шизофрения – это хроническое психическое расстройство с тяжелым течением. Шизофрения входит в 15 ведущих причин инвалидности во всем мире [1]: продолжительность жизни больных шизофренией короче, чем в среднем по популяции; они более подвержены риску суицида и соматических заболеваний (включая сердечно-сосудистые, пульмонологические, онкологические заболевания и ожирение). Качество жизни пациентов снижено, а функциональные исходы, как правило, неблагоприятны [2-8]. Только 15% больных достигают соответствия критериям клинического выздоровления [9-11].
Клинические фенотипы шизофрении обусловлены взаимодействием генетических, биологических, психологических, социальных и средовых факторов и психопатологически гетерогенны, а также отличаются по факторам риска сопутствующих заболеваний, ответа на лечение и индивидуальных особенностей течения [12-21].
Основными целями лечения шизофрении наряду с купированием обострения являются улучшение функционирования («функциональные исходы») и реадаптация пациента в социуме на всех стадиях заболевания. Нарушения функционирования проявляются неудовлетворительным уровнем самообслуживания, межличностных отношений, бытовых навыков и трудоспособности даже в периоды ремиссии и отсутствия острого психоза [4, 6, 15, 22-23].
Наиболее эффективным методом достижения улучшения функционирования и реадаптации пациентов является комплексный подход в терапии, включающий сочетание фармакотерапии с психосоциальными вмешательствами. Подобный подход позволяет успешнее решать сложные клинические задачи, такие как коррекция негативных симптомов и когнитивных расстройств, которые лежат в основе большей части функциональных нарушений у больных шизофренией и плохо поддаются лечению как типичными антипсихотиками первого поколения, так и многими атипичными антипсихотиками второго поколения.
Повышение уровня знаний о факторах, влияющих на эффективность комплексной терапии, – важный шаг на пути к эффективному лечению шизофрении.
Цель настоящего обзора – установление взаимного влияния факторов (Табл. 1), которые потенциально определяют эффективность комплексной терапии в отношении функциональных исходов у пациентов.

Связи между факторами эффективности комплексной терапии и функциональными исходами весьма разнообразны и нелинейны [6, 15, 23, 40-41]. Например, нейрокогниция влияет на показатели бытовых и трудовых навыков посредством изменения функциональных возможностей, социальной когниции, медико-социальной помощи и интернализованной стигмы, которая, в свою очередь, косвенно связана с функциональным исходом через стрессоустойчивость [6, 40]. Негативные симптомы, относящиеся к домену «опыта» (абулия, ангедония и асоциальность), влияют на функциональный исход, особенно на сферу межличностных отношений, как прямо, так и косвенно, через интернализованную стигму, стрессоустойчивость и использование медико-социальной помощи [6, 40] и т.д.
Таким образом, понимание сложных взаимосвязей между перечисленными факторами и функциональными исходами может способствовать внедрению комплексных программ лечения (психосоциальных вмешательств и фармакотерапии), нацеленных на восстановление больного шизофренией. Такие программы могут быть подобраны индивидуально в соответствии с потребностями больных. Они позволят снизить тяжесть симптомов и улучшить функциональные исходы, что повысит вероятность функционального восстановления [30, 43-44].
К настоящему моменту разработаны различные формы и комбинации психосоциальных вмешательств, которые позволяют удовлетворить индивидуальные потребности пациентов [30, 42-44], включая коррекцию негативных симптомов и когнитивных расстройств [30, 42-43, 45], реинтеграцию в общество, содействие восстановлению, помощь больным и их семьям [30, 42-43] (Табл. 2), что в конечном итоге повышает качество жизни и уровень функционирования больного.
Психообразование – это вмешательство, нацеленное на информирование пациента и его родственников о психическом расстройстве и возможном лечении.
Когнитивно-поведенческая терапия (КПТ) – вмешательство, направленное на осознание пациентом связи между восприятием, представлениями, эмоциональными и поведенческими реакциями [46-48].
Когнитивная ремедиация – вмешательство, основанное на формировании поведенческих навыков и нацеленное на улучшение когнитивных функций [46].
Тренинг социальных навыков – метод психосоциальной терапии, основанный на обсуждении контекстуальных (связанных с обстановкой), невербальных (связанных с языком тела) и паралингвистических (связанных с модуляциями голоса) аспектов межличностного взаимодействия [49-50].
Программы поддерживаемого трудоустройства помогают пациентам в рамках конкурентной занятости [30, 43].
Несмотря на признание преимущества комплексных, ранних и персонализированных методов терапии шизофрении, до сих пор недостаточно изучены предикторы ответа на такую терапию. В ряде работ подчеркивается, что при назначении комплексной терапии необходимо учитывать возможное неблагоприятное влияние различных антипсихотиков или сопутствующих препаратов на когнитивные функции, а также на вторичные негативные симптомы [30-31, 33]. Когнитивные нарушения могут усугубляться экстрапирамидными [34-35] или метаболическими нежелательными явлениями (НЯ) антипсихотических средств [36], а также сопутствующим применением антихолинергических препаратов или бензодиазепинов [37-39]. НЯ в виде экстрапирамидных симптомов (ЭПР), седация, продуктивные симптомы или нелеченая депрессия могут стать причиной развития вторичных негативных симптомов и низкой приверженности лечению [30-31] (Табл. 3).
Антипсихотическая терапия при расстройствах шизофренического спектра обеспечивает существенное снижение выраженности симптомов и является обязательным условием клинической стабилизации – состояния, при котором психотические симптомы отсутствуют или характеризуются легкой/средней степенью тяжести и не требуют коррекции терапии и (или) госпитализации [61].

В реальной клинической практике постоянная антипсихотическая терапия необходима для предотвращения обострений и рецидивов [62], а также для применения методов нелекарственной терапии, улучшающих исходы лечения [63-65]. Антипсихотическая терапия включает антипсихотические препараты первого (АПП), второго (АВП) и третьего (АТП, парциальные/частичные агонисты дофаминовых рецепторов) поколений.
Согласно результатам метаанализов, АВП более эффективны, чем АПП [76-78]. Помимо типа антипсихотического препарата, на функциональные исходы у больных шизофренией влияет их доза [36]: при снижении дозы наблюдается улучшение различных когнитивных функций (памяти, зрительно-пространственного восприятия, речи, внимания и долговременной памяти) [36]. Это позволяет предположить, что пациенты с более тяжелым течением заболевания (которым обычно назначают высокие дозы антипсихотиков) получают меньшую пользу от когнитивной ремедиации, либо высокие дозы антипсихотиков ограничивают эффективность вмешательства вследствие развития ЭПС [79-80].
Нежелательные явления могут уменьшать приверженность лечению, что, в свою очередь, сопровождается снижением или утратой клинической стабильности и, как следствие, влияет на результаты комплексной терапии [30, 66-68].
Наиболее частые НЯ АПП связаны с неврологическими побочными эффектами, а антипсихотиков второго поколения (АВП) – с увеличением массы тела и метаболическими нарушениями [35, 81-85]. АТП значительно реже влияют на массу тела или вызывают двигательные НЯ [24, 35, 86-87].
Более высокая частота развития ЭПС при терапии АПП по сравнению с АВП и АТП может стать причиной неудовлетворительной приверженности лечению и усугублять когнитивные нарушения, приводить к развитию вторичных негативных симптомов, что оказывает опосредованное влияние на результаты комплексной терапии [24, 35, 86-87].
Метаболический синдром встречается примерно у 33,5% пациентов с шизофренией [88]. Развитие этого синдрома сопряжено с различными факторами риска: образом жизни (курением, неправильным питанием, низкой физической активностью, применением антипсихотических препаратов), а также с генетическими факторами, которые имеют отношение к шизофрении и/или ответу на лечение и взаимодействуют с генами, связанными с метаболическими функциями [88].
Кардиометаболические эффекты (увеличение массы тела и метаболический синдром) могут оказывать неблагоприятное влияние на когнитивные функции (скорость обработки информации, память, внимание, логическое мышление и решение задач) у пациентов с шизофренией [89-91], тем самым ухудшая результаты комплексной терапии.
Другие НЯ, которые в разной степени присущи всем антипсихотическим препаратам, включают изменения электрической активности сердца, гиперпролактинемию, антихолинергические эффекты, седацию, снижение порога судорожной готовности, сиалорею, нейтропению и агранулоцитоз, а также злокачественный нейролептический синдром [92-95].
Помимо антипсихотиков, многим пациентам с шизофренией назначаются и другие типы лекарственных средств, такие как антихолинергические препараты, бензодиазепины, антидепрессанты и стабилизаторы настроения. При этом длительное комбинированное применение бензодиазепинов с антипсихотиками приводит к снижению когнитивных функций вследствие как прямых, так и косвенных механизмов (опосредованных эффектами потенциальной седации) [36, 69-72].
Длительное применение антихолинергических препаратов, часто используемых для снижения тяжести ЭПР, связано с низкой приверженностью лекарственной терапии [72] и усугублением уже существующих когнитивных нарушений (например, скорости обработки информации, внимания, речи, решения задач и психомоторной активности) [38-39, 69, 96-102].
Длительное применение бензодиазепинов отрицательно влияет на познавательные процессы, причем неблагоприятным изменениям подвержены такие специфические когнитивные функции, как внимание и кратковременная память [37].
Низкая приверженность лечению наблюдается примерно у 50% больных [31] и существенно осложняет оказание медикаментозной помощи [30, 57]. Недостаточная приверженность лечению увеличивает частоту рецидивов и госпитализаций [103]. Однако является ли несоблюдение режима терапии причиной рецидивов и госпитализаций или это показатель прогрессирования заболевания – остается вопросом [30, 104].
На приверженность терапии антипсихотиками влияет несколько факторов: социальных, связанных с самим пациентом и с лекарственной терапией (Табл. 4) [31, 33, 105].
Когнитивные нарушения, определяемые как дефицит различных когнитивных функций (скорости обработки информации, внимания и вигильности, кратковременной памяти, вербальных обучения и памяти, зрительно-пространственных обучения и памяти, логического мышления и решения задач, социальных когниций) [126, 127], представляют собой важнейший аспект, который требует коррекции в рамках комплексного подхода к лечению.

Когнитивные нарушения наблюдаются уже при дебюте и на ранних этапах шизофрении, зачастую предшествуют ему, связаны с неудовлетворительным функционированием в преморбидном периоде и характеризуются повышенной устойчивостью к терапии на всем протяжении болезни [26, 128].
При назначении комплексной терапии, нацеленной на восстановление познавательной деятельности, клиницисты должны учитывать ряд факторов, способных влиять на когнитивные функции: например, тип и дозу применяемых препаратов, приверженность лечению и НЯ фармакотерапии. Во избежание неблагоприятного влияния на когнитивную деятельность практикующие врачи должны отдавать предпочтение препаратам, которые оказывают незначительное влияние на эти функции, и ограничивать применение антихолинергических средств и бензодиазепинов, особенно при длительном лечении [37-39].
В различных обзорах и метаанализах сообщается, что когнитивная ремедиация, тренинг навыков и физические упражнения могут быть эффективными методами лечения и использоваться в составе комплексной терапии для улучшения когнитивных функций у больных шизофренией [52, 54-57, 129-131].
Негативные симптомы, как и когнитивные расстройства, наблюдаются уже при дебюте и на ранних этапах заболевания, могут предшествовать ему, связаны с неудовлетворительным функционированием в преморбидном периоде и отличаются повышенной устойчивостью на всем протяжении заболевания [24, 25, 132].
Негативные симптомы включают абулию, ангедонию и асоциальность, которые относятся к домену «опыта», а также притупленный аффект и алогию, которые составляют домен «дефицита экспрессии» [86, 87, 133-136]. Эти два домена негативных симптомов характеризуются различными патофизиологическими особенностями и разными взаимосвязями с функционированием пациента, что указывает на потенциальные различия в тактике их лечения [6, 15, 40, 136-142].
Важным клиническим вопросом с точки зрения как терапии, так и прогноза остается дифференциация первичных и вторичных негативных симптомов. Действительно, если первичные негативные симптомы зачастую носят стойкий характер и резистентны к лечению [143-144], то вторичные негативные симптомы можно эффективно лечить, воздействуя на факторы, составляющие их основу (например, паркинсонизм, продуктивные симптомы или депрессию) [86, 87].
В клинической практике дифференциация первичных и вторичных негативных симптомов может быть сложной задачей и должна рассматриваться как часть диагностического процесса.
Для оценки вторичного характера негативных симптомов практикующим врачам следует обращать внимание на то, усугубляются ли негативные симптомы в периоды обострения психоза или в результате изменения фармакотерапии, снижается ли их тяжесть по мере купирования галлюцинаций и бреда под действием антипсихотических препаратов. При наличии негативных симптомов, вторичных по отношению к продуктивным, рекомендуется пересмотреть дозу или тип антипсихотического препарата [24, 136, 145, 146].
В отношении антипсихотических препаратов установлено, что у больных шизофренией различные типы антипсихотиков по-разному влияют на негативные симптомы [24, 147]. Выявлено, что среди АВП амисульприд, клозапин, оланзапин, кветиапин и рисперидон более эффективно снижают тяжесть негативных симптомов, чем АПП [148, 149]. При применении атипичных антипсихотиков наблюдаются благоприятные эффекты в отношении преобладающих негативных симптомов [150-152]. Однако клинические данные, включенные в эти метаанализы, очень неоднородны, а подробная информация о характеристиках негативных симптомов (например, о разделении первичных и вторичных негативных симптомов) отсутствует [24, 136, 149].
Согласно выводам нескольких обзоров и метаанализов, эффективной тактикой лечения, используемой в рамках комплексной терапии для снижения тяжести негативных симптомов, может считаться антипсихотическая терапия и ряд психосоциальных вмешательств, таких как когнитивное обучение и тренинг навыков [24, 51-53].
Таким образом, в целях улучшения приверженности терапии больных с расстройствами шизофренического спектра необходимо: 1) снизить тяжесть симптомов; 2) улучшить когнитивные функции; 3) повысить у пациентов критику к своему состоянию; 4) сформировать более терпимое отношение к лекарственным препаратам; 5) по возможности исключить применение полифармакотерапии или сложных схем лечения; 6) привлекать пациентов к процессу принятия решений посредством прочного терапевтического альянса [24, 51-53].
В рамках подхода, ориентированного на функциональное восстановление больных шизофренией, для достижения указанных целей практически единодушно признается необходимость комплексной терапии, включающей психосоциальные вмешательства и фармакологическое лечение [30, 43, 136].
Психосоциальные вмешательства играют важную роль в удовлетворении сложных индивидуальных потребностей пациентов [30, 43, 45, 136], снижении тяжести негативных симптомов и когнитивных нарушений и улучшении реинтеграции в общество. Все это способствует трудоустройству больных, поддержке их и их семей и в конечном итоге функциональному восстановлению [30, 42, 43, 153]. Кроме того, благодаря терапевтическому альянсу психосоциальные вмешательства улучшают понимание пациентом своего заболевания, способствуют соблюдению режима лечения и тем самым снижают риск прекращения терапии и рецидивов.
Эффективные психосоциальные вмешательства, такие как когнитивное обучение и тренинг навыков, должны быть доступны пациентам с нарушением когнитивных функций, низкой социальной адаптацией и негативными симптомами. Кроме того, в клиническую практику необходимо внедрять психообразование и КПТ. Эти методы повышают приверженность лечению, а также уменьшают количество рецидивов и дистресс, связанный с продуктивными симптомами.
Применение антипсихотических препаратов составляет основу лечения, обеспечивающего надежный контроль симптомов и клиническую стабильность [30, 42, 43]. Постоянная антипсихотическая терапия необходима для предотвращения обострений и рецидивов [62]. В свою очередь, клиническая стабильность способствует более продуктивному участию пациента в нефармакологических вмешательствах и повышает вероятность благоприятного исхода [63-65].
В то же время антипсихотическая и сопутствующая терапия, которые обеспечивают эффективный контроль симптомов, нередко вызывают НЯ, способные серьезно влиять на общее состояние здоровья пациента, формировать негативное отношение к лекарственным препаратам и, как следствие, снижать приверженность лечению и эффективность комплексной терапии [30, 36-39, 67]. Учитывая различия индивидуального ответа на доступные препараты и их переносимость, при выборе антипсихотика следует руководствоваться особенностями конкретного пациента, которые включают психопатологические синдромы, физическое здоровье и сопутствующие заболевания [16, 154, 155].
В практическом плане, согласно результатам метаанализов, АВП и АТП эффективнее АПП по критерию улучшения негативных расстройств и когнитивных функций [76-78].
В качестве наиболее отвечающего основным задачам комплексного подхода к терапии пациентов с шизофренией и хорошо переносимого АТП можно рассматривать частичный агонист дофаминовых рецепторов – карипразин (Реагила®).
Карипразин – парциальный агонист дофаминовых D3/D2-рецепторов, с преимущественным связыванием с D3-рецепторами [156-158]. Воздействие карипразина именно на D3-рецепторы в сочетании с его парциальным агонизмом обусловливает выраженный терапевтический эффект карипразина при негативной, когнитивной и аффективной (депрессивной) симптоматике шизофрении [159].
Карипразин также обладает высокой аффинностью к серотониновым рецепторам 5-HT2B (Ki = 0,58 нМ) [160], меньшей – к рецепторам 5-HT1A (Ki = 3 нМ) (действует как частичный агонист для данного рецептора, в то же время являясь антагонистом 5-HT2B). Клинически данные свойства реализуются благоприятным эффектом воздействия на негативные симптомы и когнитивную дисфункцию, что подтверждается результатами доклинических и клинических исследований [161].
Аффинность карипразина в отношении других рецепторов менее выражена. В литературе в этой связи упоминаются 5-HT2A (Ki = 19 нМ), гистаминовый рецептор H1 (Ki = 23 нМ), 5-HT7 (Ki = 111 нМ) и рецепторы человека 5-HT2C (Ki = 134 нМ). В отношении всех изученных адренергических рецепторов карипразин обладает низкой активностью [159].
Метаболизируется карипразин системой цитохрома P450 (CYP3A4) и в меньшей степени – CYP2D6 [162]. В организме образуются два основных активных метаболита карипразина – дезметилкарипразин и дидезметилкарипразин (диноркарипразин). После многократного приема наблюдается кумуляция карипразина и его метаболитов (дезметилкарипразин и дидезметилкарипразин) в плазме. Оба метаболита фармакологически активны и обладают сходным с карипразином рецепторным и фармакологическим профилем. Равновесная концентрация для карипразина и дезметилкарипразина (но не для дидезметилкарипразина) достигается по прошествии 1 недели терапии [163].
Период полувыведения препарата составляет от 2 до 6 суток [163, 164], период полувыведения его активного метаболита дидезметилкарипразина – 2–3 недели [164]. Такой длительный период полувыведения может обеспечивать сохранение эффекта препарата в течение определенного времени после прекращения приема, предотвращая быстрое развитие рецидива в случае несоблюдения режима терапии. Это дает препарату терапевтические преимущества при его применении у больных с пониженной комплаентностью и отказом от приема пролонгированных инъекционных форм антипсихотиков либо с их непереносимостью, а также у пациентов с пониженным уровнем критичности к своему состоянию или с выраженными когнитивными расстройствами, обусловливающими забывчивость при приеме лекарств [159].
Согласно данным многочисленных исследований [165-169] и отечественной практики применения, карипразин в стандартных дозировках 1,5–6,0 мг/сут эффективен на всех этапах лечения шизофрении у больных с гетерогенными проявлениями заболевания: депрессивно-бредовой, апато-абулической, кататонической, неврозоподобной, обсессивно-компульсивной симптоматикой, в том числе резистентной и коморбидной с аддиктивными расстройствами [168-169].
При купировании обострения шизофрении в исследованиях II фазы, а также в плацебо-контролируемых исследованиях III фазы у пациентов с обострением шизофрении фиксируются высокая эффективность и хорошая переносимость карипразина во всех используемых дозах (1,5–6,0 мг/сут) [170, 171]. В исследованиях статистически значимые различия (p<0,001) с плацебо также отмечают на фоне лечения карипразином, уже начиная с первой (карипразин в дозе 6–9 мг/сут) или со второй недели терапии (карипразин в дозе 3–6 мг/сут) и до конца наблюдения [170-172]. Уменьшая продуктивные симптомы шизофрении, карипразин способствует стабилизации состояния пациентов и достижению устойчивой ремиссии.
В клиническом аспекте, как подчеркивается в серии метаанализов исследований купирующей терапии шизофрении карипразином [173-175], применение препарата ассоциируется в первую очередь со статистически достоверным уменьшением агрессивности и других проявлений обострения.
Антинегативный эффект карипразина по шкале PANSS-Factor Score for Negative Symptoms (FSNS), фиксируемый в исследованиях продолжительностью 26 и более недель, наблюдается у большего числа пациентов, чем при терапии рисперидоном (p=0,0022). Кроме того, начиная с десятой недели лечение карипразином по сравнению с терапией рисперидоном характеризуется более выраженным изменением средней исходной общей оценки по шкале PSP (p<0,0001): у пациентов наблюдается более выраженное улучшение по таким субдоменам шкалы, как «самообслуживание», «личностное и социальное функционирование» и «социально полезная деятельность» [176, 177].
В опубликованном метаанализе M. Krause с соавт. (2018), обобщающем данные 21 исследования, авторы приходят к заключению, что из всех атипичных антипсихотиков на сегодняшний день только для карипразина убедительно и методологически корректно доказано преимущество перед рисперидоном в устранении негативной и когнитивной симптоматики шизофрении, протекающей с выраженными или преимущественными негативными и когнитивными расстройствами [178].
Аналогичным образом в недавней публикации I. Laszlovszky с соавт. (2021) указывается, что изменения в сравнении с исходным уровнем по PANSS-FSNS за 6 недель значительно превосходят плацебо для карипразина (1,5-3 мг/день, p=0,0322; 4,5-6 мг/сут, p=0,0038), но не рисперидона (p=0,2204) и арипипразола (p=0,3265). В дальнейшем преимущество в нивелировании персистирующих и доминирующих негативных расстройств карипразина перед рисперидоном подтверждено и через 26 недель этого проспективного исследования [179]. Таким образом, карипразин обладает клинически доказанной эффективностью при терапии негативных симптомов шизофрении и улучшает социальное функционирование пациентов, что способствует их дальнейшему восстановлению.
Положительное влияние на когнитивные функции по каждому пункту когнитивной подшкалы PANSS (p<0,001) констатируется в сравнительных с плацебо и АВП (рисперидон, арипипразол) исследованиях, проводившихся как краткосрочно (6 недель, карипразин 1,5-9 мг/день [180]), так и длительно (26 недель, карипразин 4,5 мг/день, рисперидон 4,0 мг/день [181]). Обладая прокогнитивным эффектом, карипразин может улучшать приверженность пациентов к проводимой терапии шизофрении, что также может способствовать их восстановлению.
Профилактика рецидивов — один из важнейших компонентов комплексного лечения шизофрении. Длительное антипсихотическое лечение может существенно снижать риск развития рецидива в фазе стабилизации заболевания [172].
Результаты многоцентрового двойного слепого плацебо-контролируемого исследования S. Durgam и соавт. (2016), посвященного изучению эффективности, безопасности и переносимости карипразина при долгосрочной (до 72 недель) поддерживающей (противорецидивной) терапии шизофрении у взрослых, свидетельствуют о высокой противорецидивной эффективности препарата. Время до наступления рецидива оказывается значительно дольше в подгруппе карипразина, чем в подгруппе плацебо (p=0,001). Рецидив за время наблюдения наблюдается у 24,8% пациентов, получавших карипразин, и у 47,5%, получавших плацебо (отношение риска [95% ДИ] = 0,45 [0,28, 0,73]). Таким образом, лечение карипразином более чем вдвое снижает вероятность рецидива обострения шизофрении [182].
В другом долгосрочном исследовании подтверждаются как эффективность и безопасность карипразина при длительной противорецидивной терапии шизофрении, так и отдельно его эффективность в устранении негативной, когнитивной и аффективной симптоматики, а также влияние на общее качество жизни больных хронической шизофренией с преобладанием негативной симптоматики в сопоставлении с рисперидоном [176, 177].
Редукция острой психопатологической симптоматики, нивелирование негативных симптомов и улучшение когнитивных процессов у больных шизофренией при применении карипразина во всех исследованиях положительно коррелируют с повышением повседневного социального функционирования, приверженности к терапии и качества жизни [183-185].
В объединенном анализе данных по двум краткосрочным исследованиям пациентов, проходивших лечение острого обострения шизофрении карипразином, качество жизни по опроснику качества жизни SQLS-R4 при оценке общего балла и оценке «жизненных сил» и «психосоциальных факторов» статистически достоверно превосходит плацебо (p<0,0001) к 6-й неделе лечения [139, 186].
При длительном лечении карипразином показатели функционального улучшения (общий балл PSP, параметры: «уход за собой», «общественно полезная деятельность», «личные и социальные отношения», «агрессивное поведение») претерпевают положительную динамику (p<0,01) и сохраняют устойчивость при продолжении терапии препаратом по сравнению с группой больных, у которых препарат замещался плацебо [187, 188].
В сравнении с рисперидоном карипразин также демонстрирует статистически значимую разницу по общему баллу шкалы PSP и в каждом отдельном ее субдомене («уход за собой», «общественно полезная деятельность», «личные и социальные отношения») [189].
Согласно данным E. Rancans с соавт. (2021), у 70% у пациентов перевод на карипразин способствует преодолению терапевтической резистентности или недостаточной эффективности предшествующей антипсихотической (кветиапин, оланзапин, арипипразол, рисперидон, амисульприд и клозапин) терапии шизофрении.
Переносимость карипразина по результатам исследований может быть признана хорошей. Доля больных, выбывающих из исследований в связи с плохой переносимостью препарата, составляет 6-10,8% [173, 186].
Наиболее частыми (частота ≥ 10%) нежелательными явлениями (НЯ), возникающими на фоне приема любой дозировки препарата, являются акатизия, бессонница и головная боль. Не менее чем у 5% пациентов или с частотой, в 2 раза превышающей частоту в группе плацебо, могут развиваться экстрапирамидные расстройства и тремор. Большинство указанных НЯ характеризуется легкой или средней степенью тяжести [172].
Важно особо подчеркнуть, что клинически значимые метаболические изменения в уровне глюкозы крови натощак, липидов крови и пролактина, а также удлинение интервала QTc (>500 мс), изменение уровня артериального давления, офтальмологических нарушений на фоне приема карипразина по данным исследователей не наблюдаются [190-193].
При длительной терапии (48 и более недель) карипразином дисфункции печени не выявляется [190, 191]. Средний уровень пролактина снижается по сравнению с исходным значением. Значимые изменения массы тела (более 7% от исходного) носят разнонаправленный характер: у 33% пациентов отмечается увеличение веса, у 8% – уменьшение. Увеличение массы тела более 7% от исходного на фоне приема карипразина достоверно меньше, чем при приеме рисперидона [189-191].
В ряде краткосрочных и долгосрочных исследований обнаруживается, что карипразин приводит к снижению уровня пролактина на 276,5–362,0 мМЕ/л по сравнению с исходными значениями [190-193]. В открытом исследовании пациентов с шизофренией, принимающих карипразин в дозах от 3 мг/сут в течение двенадцати месяцев, уровень пролактина у пациентов снижается в среднем на 361,7 мМЕ/л по сравнению с исходными [189]. Аналогичным образом регистрируется снижение уровня пролактина при замене ранее назначенного антипсихотика, вызывающего гиперпролактинемию, терапией карипразином [194].
По сравнению с другими современными антипсихотиками (рисперидон, азенапин, луразидон, брекспипразол, арипипразол) карипразин имеет в среднем менее выраженные метаболические НЯ [149, 168]. В частности, он в меньшей степени влияет на массу тела, гиперлипидемию, гипертриглицеридемию, гиперхолестеринемию или гипергликемию, реже вызывает развитие сахарного диабета II типа и метаболического синдрома. Фармакогенная прибавка массы тела больше связана с рисперидоном, чем с карипразином [149, 159, 168]. Очевидно, что карипразин подходит для пациентов с шизофренией и неудовлетворительной переносимостью психофармакотерапии, поскольку хорошо переносится и улучшает приверженность к терапии.
Таким образом, карипразин (Реагила®) может являться фармакологической основой комплексной терапии пациентов с шизофренией. Включение в комплексную терапию шизофрении карипразина, фармакокинетические и фармкодинамические характеристики которого, высокая эффективность в отношении острой и хронической негативной, когнитивной, аффективной симптоматики шизофрении, позволяют решать многие задачи по нивелированию влияния таких факторов приверженности комплексной терапии, как низкая критика к своему состоянию, тяжесть симптомов, нейрокогнитивные нарушения, отсутствие положительной динамики, неэффективность терапии, НЯ, сложность схемы лечения, полипрогмазия и повышению влияния на исходы комплексной терапии шизофрении.
Список исп. литературыСкрыть список1. GBD 2016 Disease and Injury Incidence and Prevalence Collaborators. Global, regional, and national incidence, prevalence, and years lived with disability for 328 diseases and injuries for 195 countries, 1990–2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet. 2017. 390:1211–1259. doi: 10.1016/S0140-6736(17)32154-2
2. Howes O.D., McCutcheon R., Agid O., de Bartolomeis A., van Beveren N.J., Birnbaum M.L. et al. Treatment-resistant schizophrenia: treatment response and resistance in psychosis (TRRIP) working group consensus guidelines on diagnosis and terminology. Am J Psychiatry. 2017.174:216–229. doi: 10.1176/appi.ajp.2016.16050503
3. Leucht S., Corves C., Arbter D., Engel R.R., Li C., Davis J.M. Second-generation versus first-generation antipsychotic drugs for schizophrenia: a meta-analysis. Lancet. 2009.373:31–41. doi: 10.1016/S0140-6736(08)61764-X
4. Harvey P.D., Strassnig M. Predicting the severity of everyday functional disability in people with schizophrenia: cognitive deficits, functional capacity, symptoms, and health status. World Psychiatry. 2012.11:73–79. doi: 10.1016/j.wpsyc.2012.05.004
5. Fleischhacker W.W., Arango C., Arteel P., Barnes T.R., Carpenter W., Duckworth K. et al. Schizophrenia–time to commit to policy change. Schizophr Bull. 2014. 40(Suppl. 3):S165–194. doi: 10.1093/schbul/sbu006
6. Galderisi S., Rossi A., Rocca P., Bertolino A., Mucci A., Bucci P. et al. The influence of illness-related variables, personal resources and context-related factors on real-life functioning of people with schizophrenia. World Psychiatry. 2014. 13:275–287. doi: 10.1002/wps.20167
7. Green M.F., Horan W.P., Lee J., McCleery A., Reddy L.F., Wynn J.K. Social disconnection in schizophrenia and the general community. Schizophr Bull. 2018. 44:242–249. doi: 10.1093/schbul/sbx082
8. Harvey P.D., Strassnig M.T., Silberstein J. Prediction of disability in schizophrenia: symptoms, cognition, and self-assessment. J Exp Psychopathol. 2019. 10:2043808719865693. doi: 10.1177/2043808719865693
9. Jääskeläinen E., Juola P., Hirvonen N., McGrath J.J., Saha S., Isohanni M. et al. A systematic review and meta-analysis of recovery in schizophrenia. Schizophr Bull. 2013. 39:1296–1306. doi: 10.1093/schbul/sbs130
10. Zipursky R.B., Agid O. Recovery, not progressive deterioration, should be the expectation in schizophrenia. World Psychiatry. 2015. 14:94–96. doi: 10.1002/wps.20194
11. Vita A., Barlati S. Recovery from schizophrenia: is it possible? Curr Opin Psychiatry. 2018. 31:246–55. doi: 10.1097/YCO.0000000000000407
12. Owen M.J., Sawa A., Mortensen P.B. Schizophrenia. Lancet. 2016. 388:86–97. doi: 10.1016/S0140-6736(15)01121-6
13. Stilo S.A., Murray R.M. Non-genetic factors in schizophrenia. Curr Psychiatry Rep. 2019. 21:100. doi: 10.1007/s11920-019-1091-3
14. Correll C.U., Schooler N.R. Negative symptoms in schizophrenia: a review and clinical guide for recognition, assessment, and treatment. Neuropsychiatr Dis Treat. 2020. 16:519–34. doi: 10.2147/NDT.S225643
15. Galderisi S., Rucci P., Mucci A., Rossi A., Rocca P., Bertolino A. et al. The interplay among psychopathology, personal resources, context-related factors and real-life functioning in schizophrenia: stability in relationships after 4 years and differences in network structure between recovered and non-recovered patients. World Psychiatry. 2020. 19:81–91. doi: 10.1002/wps.20700
16. Maj M., van Os J., De Hert M,. Gaebel W., Galderisi S., Green M.F. et al. The clinical characterization of the patient with primary psychosis aimed at personalization of management. World Psychiatry. 2021. 20:4–33. doi: 10.1002/wps.20809
17. Santo-Angles A., Salvador R., Gomar J.J., Guerrero-Pedraza A., Ramiro N., Tristany J. et al. Interindividual variability of functional connectome in schizophrenia. Schizophr Res. 2021. 235:65–73. doi: 10.1016/j.schres.2021.07.010
18. Gaebel W., Zielasek J. Schizophrenia in 2020: trends in diagnosis and therapy. Psychiatry Clin Neurosci. 2015. 69:661–673. doi: 10.1111/pcn.12322
19. Gaebel W., Riesbeck M., Larach V.W., Falkai P., Zielasek J. Trends in schizophrenia diagnosis and treatment. In: Javed A, Fountoulakis KN, editors. Advances in Psychiatry. Cham: Springer International Publishing.2019. p. 603–619.
20. McCutcheon R.A., Krystal J.H., Howes O.D. Dopamine and glutamate in schizophrenia: biology, symptoms and treatment. World Psychiatry. 2020. 19:15– 33. doi: 10.1002/wps.20693
21. Perrottelli A., Giordano G.M., Brando F., Giuliani L., Mucci A. EEG-based measures in at-risk mental state and early stages of schizophrenia: a systematic review. Front Psychiatry. 2021.12:653642. doi: 10.3389/fpsyt.2021. 653642
22. Galderisi S., Rossi A., Rocca P., Bertolino A., Mucci A., Bucci P. et al. Pathways to functional outcome in subjects with schizophrenia living in the community and their unaffected first-degree relatives. Schizophr Res. 2016.175:154–160. doi: 10.1016/j.schres.2016.04.043
23. Galderisi S., Rucci P., Kirkpatrick B., Mucci A., Gibertoni D., Rocca P. et al. Interplay among psychopathologic variables, personal resources, context-related factors, and real-life functioning in individuals with schizophrenia: a network analysis. JAMA Psychiatry. 2018. 75:396–404. doi: 10.1001/jamapsychiatry.2017.4607
24. Galderisi S., Kaiser S., Bitter I., Nordentoft M., Mucci A., Sabe M. et al. EPA guidance on treatment of negative symptoms in schizophrenia. Eur Psychiatry. 2021. 64:e21. doi: 10.1192/j.eurpsy.2021.13
25. Austin S.F., Mors O., Budtz-Jørgensen E., Secher R.G., Hjorthøj C.R., Bertelsen M. et al. Long-term trajectories of positive and negative symptoms in first episode psychosis: a 10 year follow-up study in the OPUS cohort. Schizophr Res. 2015. 168:84–91. doi: 10.1016/j.schres.2015.07.021
26. Tripathi A., Kar S.K., Shukla R. Cognitive deficits in schizophrenia: understanding the biological correlates and remediation strategies. Clin Psychopharmacol Neurosci. 2018.16:7–17. doi: 10.9758/cpn.2018.16.1.7
27. Harvey P.D., Isner E.C. Cognition, social cognition, and functional capacity in early-onset schizophrenia. Child Adolesc Psychiatr Clin N Am. 2020. 29:171–182. doi: 10.1016/j.chc.2019.08.008
28. Vesterager L., Christensen T., Olsen B.B., Krarup G., Melau M., Forchhammer H.B. et al. Cognitive and clinical predictors of functional capacity in patients with first episode schizophrenia. Schizophr Res. 2012. 141:251–256. doi: 10.1016/j.schres.2012.08.023
29. Feldman R. What is resilience: an affiliative neuroscience approach. World Psychiatry. 2020. 19:132–150. doi: 10.1002/wps.20729
30. Altamura A., Fagiolini A., Galderisi S., Rocca P., Rossi A. Integrated treatment of schizophrenia. 2015. 21:168–193.
31. Acosta F.J., Hernandez J.L., Pereira J., Herrera J., Rodriguez C.J. Medication adherence in schizophrenia. World J Psychiatry. 2012. 2:74–82. doi: 10.5498/wjp.v2.i5.74
32. Morrison A.P., Law H., Carter L., Sellers R., Emsley R., Pyle M. et al. Antipsychotic drugs versus cognitive behavioural therapy versus a combination of both in people with psychosis: a randomised controlled pilot and feasibility study. Lancet Psychiatry. 2018. 5:411–423. doi: 10.1016/S2215-0366(18)30096-8
33. Higashi K., Medic G., Littlewood K.J., Diez T., Granström O., De Hert M. Medication adherence in schizophrenia: factors influencing adherence and consequences of nonadherence, a systematic literature review. Therap Adv Psychopharmacol. 2013. 3:200–218. doi: 10.1177/2045125312474019
34. Fervaha G., Agid O., Takeuchi H., Lee J., Foussias G., Zakzanis K.K. et al. Extrapyramidal symptoms and cognitive test performance in patients with schizophrenia. Schizophr Res. 2015. 161:351–356. doi: 10.1016/j.schres.2014.11.018
35. Monteleone P., Cascino G., Monteleone A.M., Rocca P., Rossi A., Bertolino A. et al. Prevalence of antipsychotic-induced extrapyramidal symptoms and their association with neurocognition and social cognition in outpatients with schizophrenia in the “real-life”. Prog Neuropsychopharmacol Biol Psychiatry. 2021. 109:110250. doi: 10.1016/j.pnpbp.2021.110250
36. MacKenzie N.E., Kowalchuk C., Agarwal S.M., Costa-Dookhan K.A., Caravaggio F., Gerretsen P. et al. Antipsychotics, metabolic adverse effects, and cognitive function in schizophrenia. Front Psychiatry. 2018. 9:622. doi: 10.3389/fpsyt.2018.00622
37. Fond G., Berna F., Boyer L., Godin O., Brunel L., Andrianarisoa M. et al. Benzodiazepine long-term administration is associated with impaired attention/working memory in schizophrenia: results from the national multicentre FACE-SZ data set. Eur Arch Psychiatry Clin Neurosci. 2018. 268:17–26. doi: 10.1007/s00406-017-0787-9
38. Joshi Y.B., Thomas M.L., Braff D.L., Green M.F., Gur R.C., Gur R.E. et al. Anticholinergic Medication Burden-Associated Cognitive Impairment in Schizophrenia. Am J Psychiatry. 2021. 178:838–847. doi: 10.1176/appi.ajp. 2020.20081212
39. Khan W.U., Ghazala Z., Brooks H.J., Subramaniam P., Mulsant B.H., Kumar S. et al. The impact of anticholinergic burden on functional capacity in persons with schizophrenia across the adult life span. Schizophr Bull. 2021. 47:249–257. doi: 10.1093/schbul/sbaa093
40. Mucci A., Galderisi S., Gibertoni D., Rossi A., Rocca P., Bertolino A. et al. Factors associated with real-life functioning in persons with schizophrenia in a 4-year follow-up study of the Italian network for research on psychoses. JAMA Psychiatry. 2021. 78:550–559. doi: 10.1192/j.eurpsy.2021.135
41. Moura B.M., Isvoranu A.M., Kovacs V., van Rooijen G., van Amelsvoort T., Simons C.J.P. et al. The puzzle of functional recovery in schizophrenia-spectrum disorders-replicating a network analysis study. Schizophr Bull. 2022. 48:871–880. doi: 10.1093/schbul/sbac018
42. Chien W.T., Leung S.F., Yeung F.K., Wong W.K. Current approaches to treatments for schizophrenia spectrum disorders, part II: psychosocial interventions and patient-focused perspectives in psychiatric care. Neuropsychiatr Dis Treat. 2013. 9:1463–1481. doi: 10.2147/NDT.S49263
43. Chien W.T., Yip A.L. Current approaches to treatments for schizophrenia spectrum disorders, part I: an overview and medical treatments. Neuropsychiatr Dis Treat. 2013. 9:1311–1332. doi: 10.2147/NDT.S37485
44. Morin L., Franck N. Rehabilitation interventions to promote recovery from schizophrenia: a systematic review. Front Psychiatry. 2017. 8:100. doi: 10.3389/fpsyt.2017.00100
45. Barlati S., Deste G., Galluzzo A., Perin A.P., Valsecchi P., Turrina C. et al. Factors associated with response and resistance to cognitive remediation in schizophrenia: a critical review. Front Pharmacol. 2018. 9:1542. doi: 10.3389/fphar.2018.01542
46. Sarin F., Wallin L. Cognitive model and cognitive behavior therapy for schizophrenia: an overview. Nord J Psychiatry. 2014. 68:145–153. doi: 10.3109/08039488.2013.789074
47. Nowak I., Sabariego C., Switaj P., Anczewska M. Disability and recovery in schizophrenia: a systematic review of cognitive behavioral therapy interventions. BMC Psychiatry. 2016. 16:228. doi: 10.1186/s12888-016-0912-8
48. Laws K.R., Darlington N., Kondel T.K., McKenna P.J., Jauhar S. Cognitive behavioural therapy for schizophrenia - outcomes for functioning, distress and quality of life: a meta-analysis. BMC Psychology. 2018. 6:32. doi: 10.1186/s40359-018-0243-2
49. Turner D.T., McGlanaghy E., Cuijpers P., van der Gaag M., Karyotaki E., MacBeth A. A Meta-analysis of social skills training and related interventions for psychosis. Schizophr Bull. 2018. 44:475–491. doi: 10.1093/ schbul/sbx146
50. Browne J., Mueser K.T., Pratt S.I. Chapter 17 - social skills training for persons with schizophrenia. In: Nangle D.W., Erdley C.A., Schwartz-Mette R.A., editors. Social Skills Across the Life Span. Academic Press. 2020. p. 329–342.
51. Lutgens D., Gariepy G., Malla A. Psychological and psychosocial interventions for negative symptoms in psychosis: systematic review and meta-analysis. Br J Psychiatry. 2017. 210:324–332. doi: 10.1192/bjp.bp.116.197103
52. Yeo H., Yoon S., Lee J., Kurtz M.M., Choi K. A meta-analysis of the effects of social-cognitive training in schizophrenia: the role of treatment characteristics and study quality. BrJ Clin Psychol. 2022. 61:37–57. doi: 10.1111/bjc.12320
53. Wykes T. Cognitive remediation – where are we now and what should we do next? The Journal of Psychopathol. 2018. 24:57–61.
54. Cella M., Price T., Corboy H., Onwumere J., Shergill S., Preti A. Cognitive remediation for inpatients with psychosis: a systematic review and meta-analysis. Psychol Med. 2020. 50:1062–1076. doi: 10.1017/ S0033291720000872
55. Kambeitz-Ilankovic L., Betz L.T., Dominke C., Haas S.S., Subramaniam K., Fisher M. et al. Multi-outcome meta-analysis (MOMA) of cognitive remediation in schizophrenia: revisiting the relevance of human coaching and elucidating interplay between multiple outcomes. Neurosci Biobehav Rev. 2019. 107:828–845. doi: 10.1016/j.neubiorev.2019.09.031
56. Vita A., Barlati S., Ceraso A., Deste G., Nibbio G., Wykes T. Acceptability of cognitive remediation for schizophrenia: a systematic review and meta-analysis of randomized controlled trials. Psychol Med. 2022.1–11. doi: 10.1017/S0033291722000319
57. Vita A., Barlati S., Ceraso A., Nibbio G., Ariu C., Deste G. et al. Effectiveness, core elements, and moderators of response of cognitive remediation for schizophrenia a systematic review and meta-analysis of randomized clinical trials. JAMA Psychiatry. (2021) 78:848–858. doi: 10.1001/jamapsychiatry.20 21.0620
58. Glenthøj L.B., Mariegaard L.S., Fagerlund B., Jepsen J.R.M., Kristensen T.D., Wenneberg C. et al. Effectiveness of cognitive remediation in the ultra-high risk state for psychosis. World Psychiatry. 2020. 19:401–402. doi: 10.1002/wps.20760
59. Correll C.U., Galling B., Pawar A., Krivko A., Bonetto C., Ruggeri M. et al. Comparison of early intervention services vs treatment as usual for early- phase psychosis: a systematic review, meta-analysis, and meta-regression. JAMA Psychiatry. 2018. 75:555–565. doi: 10.1001/jamapsychiatry.2018.0623
60. Singh S.P., Javed A. Early intervention in psychosis in low- and middle-income countries: a WPA initiative. World Psychiatry. 2020. 19:122. doi: 10.1002/wps.20708
61. Keshavan M.S., Eack S. Cognitive Enhancement in Schizophrenia and Related Disorders. Cambridge University Press.2019. https://doi.org/10.1017/ 9781108163682
62. Leucht S., Tardy M., Komossa K., Heres S., Kissling W., Salanti G. et al. Antipsychotic drugs versus placebo for relapse prevention in schizophrenia: a systematic review and meta-analysis. Lancet. 2012. 379:2063–2071. doi: 10.1016/S0140-6736(12)60239-6
63. DeRosse P., Nitzburg G.C., Blair M., Malhotra A.K. Dimensional symptom severity and global cognitive function predict subjective quality of life in patients with schizophrenia and healthy adults. Schizophr Res. 2018. 195:385–390. doi: 10.1016/j.schres.2017.10.018
64. Cullen B.A., McGinty E.E., Zhang Y., dosReis S.C., Steinwachs D.M., Guallar E. et al. Guideline-concordant antipsychotic use and mortality in schizophrenia. Schizophr Bull. 2012. 39:1159–1168. doi: 10.1093/schbul/sbs097
65. Liu N.H., Daumit G.L., Dua T., Aquila R., Charlson F., Cuijpers P. et al. Excess mortality in persons with severe mental disorders: a multilevel intervention framework and priorities for clinical practice, policy and research agendas. World Psychiatry. 2017. 16:30–40. doi: 10.1002/wps.20384
66. Pringsheim T., Gardner D., Addington D., Martino D., Morgante F., Ricciardi L. et al. The assessment and treatment of antipsychotic-induced Akathisia. Can J Psychiatry. 2018. 63:719–729. doi: 10.1177/0706743718760288
67. Verdoux H., Quiles C., Bon L., Chéreau-Boudet I., Dubreucq J., Legros-Lafarge E. et al. Characteristics associated with self-reported medication adherence in persons with psychosis referred to psychosocial rehabilitation centers. Eur Arch Psychiatry Clin Neurosci. 2021. 271:1415–1424. doi: 10.1007/s00406-020-01207-x
68. Taipale H., Tanskanen A., Mehtälä J., Vattulainen P., Correll C.U., Tiihonen J. 20-year follow-up study of physical morbidity and mortality in relationship to antipsychotic treatment in a nationwide cohort of 62,250 patients with schizophrenia (FIN20). World psychiatry. 2020. 19:61–68. doi: 10.1002/wps. 20699
69. Tsoutsoulas C., Mulsant B.H., Kalache S.M., Kumar S., Ghazala Z., Voineskos A.N. et al. The influence of medical burden severity and cognition on functional competence in older community-dwelling individuals with schizophrenia. Schizophr Res. 2016. 170:330–335. doi: 10.1016/j.schres.2015.12.009
70. Baandrup L., Fagerlund B., Glenthoj B. Neurocognitive performance, subjective well-being, and psychosocial functioning after benzodiazepine withdrawal in patients with schizophrenia or bipolar disorder: a randomized clinical trial of add-on melatonin versus placebo. Eur Arch Psychiatry Clin Neurosci. (2017) 267:163–171. doi: 10.1007/s00406-016-0711-8
71. de la Iglesia-Larrad J.I., Barral C., Casado-Espada N.M., de Alarcón R., Maciá- Casas A., Vicente Hernandez B. et al. Benzodiazepine abuse, misuse, dependence, and withdrawal among schizophrenic patients: a review of the literature. Psychiatry Res. 2020. 284:112660. doi: 10.1016/j.psychres.2019.112660
72. Verdoux H., Quiles C., Bon L., Chereau-Boudet I., Dubreucq J., Fiegi L. et al. Impact of anticholinergic load on functioning and cognitive performances of persons with psychosis referred to psychosocial rehabilitation centers. Psychol Med. 2020. 51:1–9. doi: 10.1017/S0033291720001403
73. Beck E.M., Cavelti M., Kvrgic S., Kleim B., Vauth R. Are we addressing the ’right stuff’ to enhance adherence in schizophrenia? Understanding the role of insight and attitudes towards medication. Schizophr Res. 2011. 132:42–49. doi: 10.1016/j.schres.2011.07.019
74. Kao Y.C., Liu Y.P. Compliance and schizophrenia: the predictive potential of insight into illness, symptoms, and side effects. Compr Psychiatry. 2010. 51:557–565. doi: 10.1016/j.comppsych.2010.03.007
75. Velligan D.I., Sajatovic M., Hatch A., Kramata P., Docherty J.P. Why do psychiatric patients stop antipsychotic medication? A systematic review of reasons for nonadherence to medication in patients with serious mental illness. Patient Prefer Adherence. 2017. 11:449–468. doi: 10.2147/PPA.S124658
76. Nielsen R.E., Levander S., Kjaersdam Telléus G., Jensen S.O., Østergaard Christensen T., Leucht S. Second-generation antipsychotic effect on cognition in patients with schizophrenia–a meta-analysis of randomized clinical trials. Acta Psychiatr Scand. 2015. 131:185–196. doi: 10.1111/acps.12374
77. Gabay A.S., Kempton M.J., Mehta M.A. Facial affect processing deficits in schizophrenia: a meta-analysis of antipsychotic treatment effects. J Psychopharmacol. 2015. 29:224–229. doi: 10.1177/0269881114560184
78. Zhang J.P., Gallego J.A., Robinson D.G., Malhotra A.K., Kane J.M., Correll C.U. Efficacy and safety of individual second-generation vs. first-generation antipsychotics in first-episode psychosis: a systematic review and meta-analysis. Int J Neuropsychopharmacol. 2013. 16:1205–1218. doi: 10.1017/ S1461145712001277
79. Rodewald K., Holt D.V., Rentrop M., Roesch-Ely D., Liebrenz M., Funke J. et al. Predictors for improvement of problem-solving during cognitive remediation for patients with Schizophrenia. J Int Neuropsychol Soc. 2014. 20:455–460. doi: 10.1017/S1355617714000162
80. Vita A., Deste G., De Peri L., Barlati S., Poli R., Cesana B.M. et al. Predictors of cognitive and functional improvement and normalization after cognitive remediation in patients with schizophrenia. Schizophr Res. 2013. 150:51–57. doi: 10.1016/j.schres.2013.08.011
81. Leong I. Side effects of olanzapine worsened by metabolic dysfunction. Nat Rev Endocrinol. 2018. 14:129. doi: 10.1038/nrendo.2017.183
82. Galderisi S., De Hert M., Del Prato S., Fagiolini A., Gorwood P., Leucht S. et al. Identification and management of cardiometabolic risk in subjects with schizophrenia spectrum disorders: a Delphi expert consensus study. Eur Psychiatry. 2021. 64:e7. doi: 10.1192/j.eurpsy.2020.115
83. Sykes D.A., Moore H., Stott L., Holliday N., Javitch J.A., Lane J.R. et al. Extrapyramidal side effects of antipsychotics are linked to their association kinetics at dopamine D(2) receptors. Nat Commun. 2017. 8:763. doi: 10.1038/s41467-017-00716-z
84. Ames D., Carr-Lopez S.M., Gutierrez M.A., Pierre J.M., Rosen J.A., Shakib S. et al. Detecting and managing adverse effects of antipsychotic medications: current state of play. Psychiatr Clin North Am. 2016. 39:275–311. doi: 10.1016/j.psc.2016.01.008
85. Fabrazzo M., Monteleone P., Prisco V., Perris F., Catapano F., Tortorella A. et al. Olanzapine is faster than haloperidol in inducing metabolic abnormalities in schizophrenic and bipolar patients. Neuropsychobiology. 2015. 72:29–36. doi: 10.1159/000437430
86. Galderisi S., Mucci A., Dollfus S., Nordentoft M., Falkai P., Kaiser S. et al. EPA guidance on assessment of negative symptoms in schizophrenia. Eur Psychiatry. 2021. 64:e23. doi: 10.1192/j.eurpsy. 2021.11
87. Galderisi S., Mucci A., Buchanan R.W., Arango C. Negative symptoms of schizophrenia: new developments and unanswered research questions. Lancet Psychiatry. 2018. 5:664–677. doi: 10.1016/S2215-0366(18)30050-6
88. De Hert M., Schreurs V., Vancampfort D., Van Winkel R. Metabolic syndrome in people with schizophrenia: a review. World Psychiatry. 2009. 8:15– 22. doi: 10.1002/j.2051-5545.2009.tb00199.x
89. Lindenmayer J.P., Khan A., Kaushik S., Thanju A., Praveen R., Hoffman L. et al. Relationship between metabolic syndrome and cognition in patients with schizophrenia. Schizophr Res. 2012. 142:171–176. doi: 10.1016/j.schres.2012.09.019
90. Li C., Zhan G., Rao S., Zhang H. Metabolic syndrome and its factors affect cognitive function in chronic schizophrenia complicated by metabolic syndrome. J Nerv Ment Dis. 2014. 202:313–318. doi: 10.1097/NMD. 0000000000000124
91. Bora E., Akdede B.B., Alptekin K. The relationship between cognitive impairment in schizophrenia and metabolic syndrome: a systematic review and meta-analysis. Psychol Med. 2017. 47:1030–1040. doi: 10.1017/S0033291716003366
92. Papola D., Ostuzzi G., Gastaldon C., Morgano G.P., Dragioti E., Carvalho A.F. et al. Antipsychotic use and risk of life-threatening medical events: umbrella review of observational studies. Acta Psychiatr Scand. 2019. 140:227–243. doi: 10.1111/acps.13066
93. Stroup T.S., Gray N. Management of common adverse effects of antipsychotic medications. World Psychiatry. 2018. 17:341–356. doi: 10.1002/wps.20567
94. Gupta S., Lakshmanan D.A.M., Khastgir U., Nair R. Management of antipsychotic-induced hyperprolactinaemia. BJPsych Advances. 2017. 23:278–286. doi: 10.1192/apt.bp.115.014928
95. Fabrazzo M., Prisco V., Sampogna G., Perris F., Catapano F., Monteleone A. et al. Clozapine versus other antipsychotics during the first 18 weeks of treatment: a retrospective study on risk factor increase of blood dyscrasias. Psychiatry Res. 2017. 256:275–282. doi: 10.1016/j.psychres.2017.06.068
96. Ogino S., Miyamoto S., Miyake N., Yamaguchi N. Benefits and limits of anticholinergic use in schizophrenia: focusing on its effect on cognitive function. Psychiatry Clin Neurosci. 2014. 68:37–49. doi: 10.1111/pcn.12088
97. O’Reilly K., O’Connell P., Donohoe G., Coyle C., O’Sullivan D., Azvee Z. et al. Anticholinergic burden in schizophrenia and ability to benefit from psychosocial treatment programmes: a 3-year prospective cohort study. Psychol Med. 2016. 46:3199–3211. doi: 10.1017/S00332917160 02154
98. Kim S.J., Jung D., Shim J.C., Moon J.J., Jeon D.W., Kim Y.N. et al. The effect of anticholinergic burden on cognitive and daily living functions in patients with schizophrenia. Asian J Psychiatr. 2019. 46:111–117. doi: 10.1016/j.ajp. 2019.10.013
99. Ang M.S., Abdul Rashid N.A., Lam M., Rapisarda A., Kraus M., Keefe R.S.E. et al. The impact of medication anticholinergic burden on cognitive performance in people with schizophrenia. J Clin Psychopharmacol. 2017. 37:651–65 6. doi: 10.1097/JCP.0000000000000790
100. Frydecka D., Beszłej J.A., Go´scimski P., Kiejna A., Misiak B. Profiling cognitive impairment in treatment-resistant schizophrenia patients. Psychiatry Res. (2016) 235:133–138. doi: 10.1016/j.psychres.2015.11.028
101. Eum S., Hill S.K., Rubin L.H., Carnahan R.M., Reilly J.L., Ivleva E.I. et al. Cognitive burden of anticholinergic medications in psychotic disorders. Schizophr Res. 2017. 190:129–135. doi: 10.1016/j.schres.2017.03.034
102. Fond G., Godin O., Dumontaud M., Faget C., Schürhoff F., Berna F. et al. Sexual dysfunctions are associated with major depression, chronic inflammation and anticholinergic consumption in the real-world schizophrenia FACE-SZ national cohort. Prog Neuro-Psychopharmacol Biol Psychiatry. 2019. 94:109654. doi: 10.1016/j.pnpbp.2019.109654
103. Morken G., Widen J.H., Grawe R.W. Non-adherence to antipsychotic medication, relapse and rehospitalisation in recent-onset schizophrenia. BMC Psychiatry. 2008. 8:32. doi: 10.1186/1471-244X-8-32
104. Kane J.M., Garcia-Ribera C. Clinical guideline recommendations for antipsychotic long-acting injections. Br J Psychiatry Suppl. 2009. 52:S63–67. doi: 10.1192/bjp.195.52.s63
105. Amore M., Murri M.B., Calcagno P., Rocca P., Rossi A., Aguglia E. et al. The association between insight and depressive symptoms in schizophrenia: undirected and Bayesian network analyses. European Psychiatry. 2020. 63:e46. doi: 10.1192/j.eurpsy.2020.45
106. Jeste S.D., Patterson T.L., Palmer B.W., Dolder C.R., Goldman S., Jeste D.V. Cognitive predictors of medication adherence among middle-aged and older outpatients with schizophrenia. Schizophr Res. 2003. 63:49–58. doi: 10.1016/S0920-9964(02)00314-6
107. Keith S.J., Kane J.M. Partial compliance and patient consequences in schizophrenia: our patients can do better. J Clin Psychiatry. 2003. 64:1308–1315. doi: 10.4088/JCP.v64n1105
108. Hudson T.J., Owen R.R., Thrush C.R., Han X., Pyne J.M., Thapa P. et al. A pilot study of barriers to medication adherence in schizophrenia. J Clin Psychiatry. 2004. 65:211–216. doi: 10.4088/JCP.v65n0211
109. Tattan T.M., Creed F.H. Negative symptoms of schizophrenia and compliance with medication. Schizophr Bull. 2001. 27:149–155. doi: 10.1093/oxfordjournals.schbul.a006853
110. Hasan A., Falkai P., Wobrock T., Lieberman J., Glenthoj B., Gattaz W.F. et al. World Federation of Societies of Biological Psychiatry (WFSBP) Guidelines for Biological Treatment of Schizophrenia, part 1: update 2012 on the acute treatment of schizophrenia and the management of treatment resistance. World J Biol Psychiatry. 2012. 3:318–378. doi: 10.3109/15622975.2012.696143
111. Leporini C., De Sarro G., Russo E. Adherence to therapy and adverse drug reactions: is there a link? Expert Opin Drug Saf. 2014. 13(Suppl. 1):S41–55. doi: 10.1517/14740338.2014.947260
112. Lähteenvuo M., Tiihonen J. Antipsychotic polypharmacy for the management of schizophrenia: evidence and recommendations. Drugs. 2021. 81:1273–1284. doi: 10.1007/s40265-021-01556-4
113. Remington G., Kwon J., Collins A., Laporte D., Mann S., Christensen B. The use of electronic monitoring (MEMS) to evaluate antipsychotic compliance in outpatients with schizophrenia. Schizophr Res. 2007. 90:229–237. doi: 10.1016/j.schres.2006.11.015
114. Marcum Z.A., Gellad W.F. Medication adherence to multidrug regimens. Clin Geriatr Med. 2012. 28:287–300. doi: 10.1016/j.cger.2012.01.008
115. Zelko E., Klemenc-Ketis Z., Tusek-Bunc K. Medication adherence in elderly with polypharmacy living at home. a systematic review of existing studies. Mater Sociomed. 2016. 28:129–132. doi: 10.5455/msm.2016.28.129-132
116. Hashimoto Y., Uno J., Miwa T., Kurihara M., Tanifuji H., Tensho M. Effects of antipsychotic polypharmacy on side-effects and concurrent use of medications in schizophrenic outpatients. Psychiatry Clin Neurosci. 2012. 66:405– 410. doi: 10.1111/j.1440-1819.2012.02376.x
117. Chapman S.C., Horne R. Medication nonadherence and psychiatry. Curr Opin Psychiatry. 2013. 26:446–452. doi: 10.1097/YCO.0b013e3283642da4
118. Johansen R., Iversen V.C., Melle I., Hestad K.A. Therapeutic alliance in early schizophrenia spectrum disorders: a cross-sectional study. Ann Gen Psychiatry. 2013. 12:14. doi: 10.1186/1744-859X-12-14
119. Ishii M., Okumura Y., Sugiyama N., Hasegawa H., Noda T., Hirayasu Y. et al. Efficacy of shared decision making on treatment satisfaction for patients with first- admission schizophrenia: study protocol for a randomised controlled trial. BMC Psychiatry. 2014. 14:111. doi: 10.1186/1471-244X-14-111
120. Fiorillo A., Barlati S., Bellomo A., Corrivetti G., Nicolò G., Sampogna G. et al. The role of shared decision-making in improving adherence to pharmacological treatments in patients with schizophrenia: a clinical review. Ann Gen Psychiatry. 2020. 19:43. doi: 10.1186/s12991-020-00293-4
121. Ishii M., Okumura Y., Sugiyama N., Hasegawa H., Noda T., Hirayasu Y. et al. Feasibility and efficacy of shared decision making for first-admission schizophrenia: a randomized clinical trial. BMC Psychiatry. 2017. 17:52. doi: 10.1186/s12888-017-1218-1
122. Mucci A., Kawohl W., Maria C., Wooller A. Treating schizophrenia: open conversations and stronger relationships through psychoeducation and shared decision-making. Front Psychiatry. 2020. 11:761. doi: 10.3389/fpsyt.2020.00761
123. Huang C., Lam L., Zhong Y., Plummer V., Cross W.. Chinese mental health professionals’ perceptions of shared decision-making regarding people diagnosed with schizophrenia: a qualitative study. Int J Ment Health Nurs. 2021. 30:189–199. doi: 10.1111/inm.12771_1
124. Vega D., Acosta F.J., Saavedra P. Testing the hypothesis of subtypes of nonadherence in schizophrenia and schizoaffective disorder: a prospective study. World J Psychiatry. 2020. 10:260–271. doi: 10.5498/wjp.v10.i11.260
125. Harris B.A., Panozzo G. Therapeutic alliance, relationship building, and communication strategies-for the schizophrenia population: an integrative review. Arch Psychiatr Nurs. 2019. 33:104–111. doi: 10.1016/j.apnu .2018.08.003
126. Green M.F., Lee J., Wynn J.K. Experimental approaches to social disconnection in the general community: can we learn from schizophrenia research? World Psychiatry. 2020. 19:177–178. doi: 10.1002/wps.20734
127. Lysaker P.H., Hasson-Ohayon I. Metacognition in psychosis: a renewed path to understanding of core disturbances and recovery-oriented treatment. World Psychiatry. 2021. 20:359–361. doi: 10.1002/wps.20914
128. Harvey P.D. When does cognitive decline occur in the period prior to the first episode of schizophrenia? Psychiatry. 2009. 6:12–14.
129. Dauwan M., Begemann M.J.H., Slot M.I.E., Lee E.H.M., Scheltens P., Sommer I.E.C. Physical exercise improves quality of life, depressive symptoms, and cognition across chronic brain disorders: a transdiagnostic systematic review and meta-analysis of randomized controlled trials. J Neurol. 2021. 268:1222–1246. doi: 10.1007/s00415-019-09493-9
130. Fernández-Abascal B., Suárez-Pinilla P., Cobo-Corrales C., Crespo-Facorro B., Suárez-Pinilla M. In- and outpatient lifestyle interventions on diet and exercise and their effect on physical and psychological health: a systematic review and metaanalysis of randomised controlled trials in patients with schizophrenia spectrum disorders and first episode of psychosis. Neurosci Biobehav Rev. 2021. 125:535–168. doi: 10.1016/j.neubiorev.2021.01.005
131. Millman L.S.M., Terhune D.B., Hunter E.C.M., Orgs G. Towards a neurocognitive approach to dance movement therapy for mental health: a systematic review. Clin Psychol Psychother. 2021. 28:24–38. doi: 10.1002/ cpp.2490
132. Bucci P., Mucci A., van Rossum I.W., Aiello C., Arango C., Baandrup L. et al. Persistent negative symptoms in recent-onset psychosis: relationship to treatment response and psychosocial functioning. Eur Neuropsychopharmacol. 2020. 34:76– 86. doi: 10.1016/j.euroneuro.2020.03.010
133. Moritz S., Silverstein S.M., Dietrichkeit M., Gallinat J. Neurocognitive deficits in schizophrenia are likely to be less severe and less related to the disorder than previously thought. World Psychiatry. 2020. 19:254–255. doi: 10.1002/wps.20759
134. Gaebel W., Falkai P., Hasan A. The revised German evidence- and consensus-based schizophrenia guideline. World Psychiatry. 2020. 19:117–119. doi: 10.1002/wps.20706
135. Sanislow C.A. RDoC at 10: changing the discourse for psychopathology. World Psychiatry. 2020. 19:311–312. doi: 10.1002/wps.20800
136. Giordano G.M., Brando F., Pezzella P., De Angelis M., Mucci A., Galderisi S. Factors influencing the outcome of integrated therapy approach in schizophrenia: A narrative review of the literature Frontiers in Psychiatry. 2022. Volume 13; 1-17. 10.3389/fpsyt.2022.970210
137. Kotov R., Jonas K.G., Carpenter W.T., Dretsch M.N., Eaton N.R., Forbes M.K. et al. Validity and utility of hierarchical taxonomy of psychopathology (HiTOP): I. Psychosis superspectrum. World Psychiatry. 2020. 19:151–172. doi: 10.1002/wps.20730
138. First M.B., Gaebel W., Maj M., Stein D.J., Kogan C.S., Saunders J.B. et al. An organization- and category-level comparison of diagnostic requirements for mental disorders in ICD-11 and DSM-5. World Psychiatry. 2021 .20:34–51. doi: 10.1002/wps.20825
139. Lahey B.B., Moore T.M., Kaczkurkin A.N., Zald D.H. Hierarchical models of psychopathology: empirical support, implications, and remaining issues. World Psychiatry. 2021. 20:57–63. doi: 10.1002/wps.20824
140. Krueger R.F., Hobbs K.A., Conway C.C., Dick D.M., Dretsch M.N., Eaton N.R. et al. Validity and utility of hierarchical taxonomy of psychopathology (HiTOP): II. Externalizing superspectrum. World Psychiatry. 2021. 20:171–193. doi: 10.1002/wps.20844
141. Giordano G.M., Bucci P., Mucci A., Pezzella P., Galderisi S. Gender differences in clinical and psychosocial features among persons with schizophrenia: a mini review. Front Psychiatry. 2021. 12:789179. doi: 10.3389/fpsyt.2021. 789179
142. Giordano G.M., Stanziano M., Papa M., Mucci A., Prinster A., Soricelli A. et al. Functional connectivity of the ventral tegmental area and avolition in subjects with schizophrenia: a resting state functional MRI study. Eur Neuropsychopharmacol. 2018. 28:589–602. doi: 10.1016/j.euroneuro.2018.03.013
143. Mucci A., Merlotti E., Üçok A., Aleman A., Galderisi S. Primary and persistent negative symptoms: concepts, assessments and neurobiological bases. Schizophr Res. 2017. 186:19–28. doi: 10.1016/j.schres.2016.05.014
144. Kirkpatrick B., Mucci A., Galderisi S. Primary, enduring negative symptoms: an update on research. Schizophr Bull. 2017. 43:730–736. doi: 10.1093/schbul/sbx064
145. Huhn M., Nikolakopoulou A., Schneider-Thoma J., Krause M., Samara M., Peter N. et al. Comparative efficacy and tolerability of 32 oral antipsychotics for the acute treatment of adults with multi-episode schizophrenia: a systematic review and network meta-analysis. Lancet. 2019. 394:939–951. doi: 10.1016/S0140-6736(19)31135-3
146. Krause M., Huhn M., Schneider-Thoma J., Bighelli I., Gutsmiedl K., Leucht S. Efficacy, acceptability and tolerability of antipsychotics in patients with schizophrenia and comorbid substance use. A systematic review and meta-analysis. Eur Neuropsychopharmacol. 2019. 29:32–45. doi: 10.1016/j.euroneuro.2018.11.1105
147. Fusar-Poli P., Papanastasiou E., Stahl D., Rocchetti M., Carpenter W., Shergill S. et al. Treatments of negative symptoms in schizophrenia: meta-analysis of 168 randomized placebo-controlled trials. Schizophr Bull. 2015. 41:892–899. doi: 10.1093/schbul/sbu170
148. Leucht S., Corves C., Arbter D., Engel R.R., Li C., Davis J.M. Second-generation versus first-generation antipsychotic drugs for schizophrenia: a meta-analysis. Lancet. 2009. 373:31–41. doi: 10.1016/S0140-6736(08) 61764-X
149. Медведев В.Э. Лечение шизофрении современными атипичными антипсихотическими препаратами” (учебно-методическое пособие). - М.: ОАО “Конти-Принт”, 2014. – 72 с.
150. Fleischhacker W., Galderisi S., Laszlovszky I., Szatmári B., Barabássy Á., Acsai K. et al. The efficacy of cariprazine in negative symptoms of schizophrenia: post hoc analyses of PANSS individual items and PANSS-derived factors. Eur Psychiatry. 2019. 58:1–9. doi: 10.1016/j.eurpsy.2019.01.015
151. Krause M., Zhu Y., Huhn M., Schneider-Thoma J., Bighelli I., Nikolakopoulou A. et al. Antipsychotic drugs for patients with schizophrenia and predominant or prominent negative symptoms: a systematic review and meta-analysis. Eur Arch Psychiatry Clin Neurosci. 2018. 268:625–639. doi: 10.1007/s00406-018-0869-3
152. Németh G., Laszlovszky I., Czobor P., Szalai E., Szatmári B., Harsányi J. et al. Cariprazine versus risperidone monotherapy for treatment of predominant negative symptoms in patients with schizophrenia: a randomised, doubleblind, controlled trial. Lancet. 2017. 389:1103–1113. doi: 10.1016/ S0140-6736(17) 30060-0
153. Pharoah F., Mari J., Rathbone J., Wong W. Family intervention for schizophrenia. Cochrane Database Syst Rev. 2010. 12:Cd000088. doi: 10.1002/14651858.CD000088.pub3
154. Carpenter W.T. Primary psychosis: more to know, much more to do. World Psychiatry. 2021. 20:1–2. doi: 10.1002/wps.20807
155. Galderisi S., Giordano G.M. We are not ready to abandon the current schizophrenia construct, but should be prepared to do so. Schizophr Res. 2022. 242:30–34. doi: 10.1016/j.schres.2021.12.007
156. Kiss B., Horváth A., Némethy Z. et al. Cariprazine (RGH-188), a dopamine D(3) receptor-preferring, D(3)/D(2) dopamine receptor antagonist-partial agonist antipsychotic candidate: in vitro and neurochemical profile // J PharmacolExpTher. 2010. 333; 328–340.
157. Медведев В.Э. Карипразин – новый антипсихотик для лечения шизофрении. Современная терапия психических расстройств. 2019. 2; 22-29.
158. Шмуклер А.Б. Карипразин (реагила) - новый атипичный антипсихотик с уникальным спектром психотропной активности. Социальная и клиническая психиатрия. 2020. 30(1);.110.
159. Stahl S.M. Mechanism of action of cariprazine. CNS Spectrums. 2016. 21; 123–127. doi:10.1017/S1092852916000043
160. Keator D.B., Mukherjee J., Preda A., et al. Dopamine D2 and D3 receptor occupancy of cariprazine in schizophrenic patients. Schizophr Bull. 2009. 35(Suppl. 1);154.
161. Newman-Tancredi A. The importance of 5-HT1A receptor agonism in antipsychotic drug action: rationale and perspectives. CurrOpinInvestig Drugs. 2010. 11;802–812.
162. Kirschner N., Gemesi L.I., Vastag M. et al. In vitro metabolism of RGH-188. Drug Metab Rev. 2008. 40(Suppl. 1); 128–129.
163. Kapas M., Meszaros G.P., Yu B. et al. Comparison of the pharmacokinetic behaviour of RGH-188 in schizophrenic patients and healthy volunteers. EurNeuropsychopharmacol. 2008. 18(Suppl. 4); 433.
164. Meszaros G.P., Kapas M., Borsos M., et al. Pharmacokinetics of RGH-188, a new dopamine D3/D2 antagonist/partial agonist atypical antipsychotic, in healthy subjects. EurNeuropsychopharmacol. 2007. 217(Suppl. 4);451–452.
165. Горобец Л.Н., Литвинов А.В. Карипразин: нейроэндокринные и метаболические аспекты переносимости у больных с психическими расстройствами. Современная терапия психических расстройств. 2020. 3; 19-27. DOI: 10.21265/PSYPH.2020.79.49.003
166. Доровских И.В., Павлова Т.А., Шайдеггер Ю.М. Карипразин – современный антипсихотик с благоприятным нейроэндокринным профилем. Формулы Фармации. 2020:2(3).; 58-63. doi: 10.17816/phf46072
167. Абриталин Е.Ю., Медведев В.Э., Морозов П.В. Опыт применения карипразина в стационарной и амбулаторной психиатрической практике. Психиатрия и психофармакотерапия им. П.Б. Ганнушкина. 2020: 6; 25-30.
168. Карипразин: от теории к практике (Специальность «Психиатрия» 31.08.20) : Пособие для врачей / Под ред. В. Э. Медведева. — М.: ООО «СИНАПС», 2021. — 114 с..
169. Медведев В.Э. Карипразин — современный препарат для лечения шизофрении и биполярного расстройства. Современная терапия психических расстройств. 2022;3:51-57.
170. Durgam S., Bose A., Starace A., et al. An evaluation of the safety and efficacy of cariprazine in patients with acute exacerbation of schizophrenia: a phase II, randomized clinical trial. Schizophr Res. 2014. 152; 450-457.
171. Lieberman J.A., Cutler A.J., Wan S. et al. Cariprazine in acute exacerbation of schizophrenia: a fixed-dose, randomised, double-blind, placebo- and active-controlled trial. EurNeuropsychopharmacol. 2013. 23(suppl 2); 477–478.
172. Kane J.M., Zukin S., Wang Y., Lu K., Ruth A., Nagy K. Efficacy and Safety of Cariprazine in Acute Exacerbation of Schizophrenia. Results From an International, Phase III Clinical Trial. J ClinPsychopharmacol. 2015. 35; 367–373.
173. Citrome L., Durgam S., Lu K. et al. The effect of cariprazine on hostility associated with schizophrenia: post hoc analyses from 3 randomized controlled trials. J Clin Psychiatry. 2016. 77 (1); 109–115.
174. Earley W., Durgam S., Lu K. et al. Safety and tolerability of cariprazine in patients with acute exacerbation of schizophrenia: a pooled analysis of four phase II/III randomized, double-blind, placebo-controlled studies. IntClinPsychopharmacol. 2017. 32 (6); 319–328.
175. Zhao M.J., Qin B., Wang J.B. et al. Efficacy and Acceptability of Cariprazine in Acute Exacerbation of Schizophrenia: Meta-Analysis of Randomized Placebo-Controlled Trials. J ClinPsychopharmacol. 2018.38 (1); 55–59.
176. Németh G., Laszlovszky I., Czobor P. et al. Cariprazine versus risperidone monotherapy for treatment of predominant negative symptoms in patients with schizophrenia: a randomised, double-blind, controlled trial. Lancet. 2017. 389 (10074); 1103–1113. http://dx.doi.org/10.1016/S0140-6736(17)30060-0
177. Németh B., Molnár A., Akehurst R. et al. Quality-adjusted life year difference in patients with predominant negative symptoms of schizophrenia treated with cariprazine and risperidone. J Comp Eff Res. 2017. 6 (8); 639–648.
178. Krause M., Zhu Y., Huhn M. et al. Antipsychotic drugs for patients with schizophrenia and predominant or prominent negative symptoms: a systematic review and meta-analysis. Eur Arch Psychiatry ClinNeurosci. 2018. 268(7); 625-639. doi: 10.1007/s00406-018-0869-3.
179. Laszlovszky I., Barabássy, Á. & Németh, G. Cariprazine, A Broad-Spectrum Antipsychotic for the Treatment of Schizophrenia: Pharmacology, Efficacy, and Safety. Adv Ther. 2021. 38; 3652–3673. https://doi.org/10. 1007/s12325-021-01797-5
180. Fleischhacker W.W., Marder S., Lu K. et al. Efficacy of cariprazine versus placebo across schizophrenia symptom domains: pooled analyses from 3 phase II/III trials. Poster presented at the annual meeting of the American Society of Clinical Psychopharmacology; Miami, Florida; June 22–25, 2015.
181. Fleischhacker W., Galderisi S., Laszlovszky I. et al. The efficacy of cariprazine in negative symptoms of schizophrenia: post hoc analyses of PANSS individual items and PANSS-derived factors. Eur Psychiatry. 2019;58:1–9.
182. Durgam S., Earley W., Li R. et al. Long-term cariprazine treatment for the prevention of relapse in patients with schizophrenia: A randomized, double-blind, placebo-controlled trial. Schizophr Res. 2016. 176 (2–3); 264–271.
183. Neill J.C., Grayson B., Kiss B., Gyertyán I., Ferguson P., Adham N. Effects of cariprazine, a novel antipsychotic, on cognitive deficit and negative symptoms in a rodent model of schizophrenia symptomatology. Eur Neuropsychopharmacol. 2016 Jan; 26(1): 3-14. doi: 10.1016/j.euroneuro.2015.11.016.
184. Marder S., Fleischhacker W.W., Earley W., Lu K., Zhong Y., Németh G., Laszlovszky I., Szalai E., Durgam S. Efficacy of cariprazine across symptom domains in patients with acute exacerbation of schizophrenia: Pooled analyses from 3 phase II/III studies. Eur Neuropsychopharmacol. 2019 Jan;29(1):127-136. doi: 10.1016/j.euroneuro.2018.10.008.
185. Csehi R., Dombi Z.B., Sebe B., Molnár M.J. Real-Life Clinical Experience With Cariprazine: A Systematic Review of Case Studies. Front Psychiatry. 2022 Mar 17;13:827744. doi: 10.3389/fpsyt.2022.827744.
186. Citrome L. Cariprazine in Schizophrenia: Clinical Efficacy, Tolerability, and Place in Therapy. AdvTher. 2013. Published online: January 28, DOI 10.1007/s12325-013-0006-7
187. Durgam S., Starace A., Li D. et al. An evaluation of the safety and efficacy of cariprazine in patients with acute exacerbation of schizophrenia: a phase II, randomized clinical trial. Schizophr Res. 2014. 152 ; 450–457.
188. Nasrallah H.A., Earley W., Cutler A.J. et al. The safety and tolerability of cariprazine in long-term treatment of schizophrenia: a post hoc pooled analysis. BMC Psychiatry. 2017. 17 (1); 305.
189. Cutler A.J., Durgam S., Wang Y. et al. Evaluation of the long-term safety and tolerability of cariprazine in patients with schizophrenia: results from a 1-year open-label study. CNS Spectrums. 2018. 23 (1); 39-50. DOI: 10.1017/S1092852917000220.
190. Citrome L. Cariprazine in Schizophrenia: Clinical Efficacy, Tolerability, and Place in Therapy. AdvTher. 2013. Published online: January 28, DOI 10.1007/s12325-013-0006-7
191. Citrome L., Durgam S., Lu K. et al. The effect of cariprazine on hostility associated with schizophrenia: post hoc analyses from 3 randomized controlled trials. J Clin Psychiatry. 2016. 77 (1); 109–115.
192. Earley W., Durgam S., Lu K. et al. Safety and tolerability of cariprazine in patients with acute exacerbation of schizophrenia: a pooled analysis of four phase II/III randomized, double-blind, placebo-controlled studies. IntClinPsychopharmacol. 2017. 32 (6);319–328.
193. Zhao M.J., Qin B., Wang J.B. et al. Efficacy and Acceptability of Cariprazine in Acute Exacerbation of Schizophrenia: Meta-Analysis of Randomized Placebo-Controlled Trials. J ClinPsychopharmacol. 2018. 38 (1); 55–59.
194. Reagila (cariprazine): assessment report. European Medicines Agency, 2017. Available from: http://www.ema.europa.eu
195. Rancans E., Dombi Z.B., Mátrai P., Barabássy Á., Sebe B., Skrivele I., Németh G. The effectiveness and safety of cariprazine in schizophrenia patients with negative symptoms and insufficient effectiveness of previous antipsychotic therapy: an observational study. Int Clin Psychopharmacol. 2021 May 1;36(3):154-161. doi: 10.1097/YIC.0000000000000351.
29 ноября 2023
Количество просмотров: 1134


