Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
K.R. Evgrafov Mental Hospital.
440026, Russian Federation, Penza, ul. Lermontova, d. 28. skrembler@mail.ru
Abstract
An article summarizing the clinical aspects of the practice of using basic psychopharmacological drugs in pregnant women in Russia at the present time. Topical issues of the applied use of drugs, their features, and prescription tactics are covered.
Keywords: psychopharmacotherapy in pregnacy, psychopharmacotherapy and pregnancy, antidepressants in pregnancy, antipsychotics in pregnancy, anxiolytics in pregnancy, tranquilizers in pregnancy, mood stabilizers in pregnancy, correctors in pregnancy.
For citation: Maslov K.A. Psychopharmacotherapy in pregnacy in Russia, in modern clinical practice of the psychiatrist. Questions of applied practical application. Psychiatry and psychopharmacotherapy. 2024; 3: 19–32. DOI: 10.62202/2075-1761-2024-26-3-19-32
Выделяют несколько типов потенциальных нежелательных эффектов психофармакотерапевтических препаратов на плод и новорожденного [18]:
1. Структурные нарушения (врожденные аномалии);
2. Острые неонатальные эффекты, проявляющиеся интоксикацией и синдромом отмены;
3. Внутриутробную смерть;
4. Замедление внутриутробного роста;
5. Нейроповеденческую тератогенность.
Основным общепризнанным принципом фармакотерапии беременных является принятие решения о применении фармакотерапии только в случае, когда возможный риск осложнений для матери или плода при неиспользовании медикаментов превышает риск их побочного действия, что имеет отражение в действующих инструкциях к лекарственным препаратам [19]. Вторым принципом, или т.н. условным «золотым правилом», является подход максимального (по возможности) отказа матери от какой-либо фармакотерапии в I триместре беременности (в период закладки нервной трубки и других жизненно важных органов).
Прием лекарственных средств, получаемых отцом, малоизучен, но есть мнение, что прием фармакотерапии отцом до зачатия не приводит к значимому риску развития серьезных врожденных аномалий.
При выборе психофармакологического средства отдается предпочтение препаратам с меньшим количеством метаболитов, более высоким связыванием с белками (снижают плацентарный проход) и меньшим количеством взаимодействий с другими лекарствами [20]. По данным доступных исследований, прием поддерживающей фармакотерапии во время беременности у женщин с различными психическими расстройствами значительно снижает риск рецидива [21]. Принимая во внимание, что качественные рандомизированные плацебо-контролируемые клинические испытания применения психофармакотерапевтических препаратов у беременных недоступны по этическим соображениям, поскольку беременные женщины с различными психопатологическими расстройствами нуждаются в лечении, мы располагаем натуралистическими данными, таким образом большая часть существующих исследований психофармакологии менее качественные, чем другие современные рандомизированные клинические испытания [22]. Достаточно сложно оценить влияние именно приема именно психотропных препаратов на плод у беременных, в сравнении с незатронутой популяцией, поскольку невозможно достоверно оценить влияние психопатологических расстройств (генетической предрасположенности или психиатрических расстройств родителей), а не приема психофармакотерапии, связанной с данной патологией [23].
С 1979 по 2015 год Агентством по контролю безопасности пищевых продуктов и лекарственных средств (Food and Drug Administration – FDA) в США для определения степени риска неблагоприятного воздействия лекарственных средств на плод была введена и применялась система категорий оценки риска применения лекарственных средств во время беременности, в которой лекарственные средства были распределены на 4 категории от А (безопасные) до Х (противопоказанные), которая представлена в табл. 1 [24, 25].

С 2015 года и по сегодняшний день FDA в США введены новые правила маркировки лекарственных при беременности и в период лактации для рецептурных препаратов (Pregnancy and Lactation Labeling Rule – PLLR or final rule), где вместо категорий A, B, C, D, X к каждому препарату прилагается индивидуальное резюме, включающее риски использования препарата во время беременности и в период лактации, с ссылкой на доклинические и клинические исследования, указанием проникновения препарата в грудное молоко, рисков для женщин и мужчин репродуктивного возраста, необходимости тестирования на беременность, контрацепции и риска бесплодия от препарата [24].
В Австралии существует похожая на американскую система категорий оценки риска применения лекарственных средств во время беременности – Австралийская система классификации лекарств для назначения во время беременности (Australian The Therapeutic Goods Administration – AU TGA), представлена в табл. 2 [26].
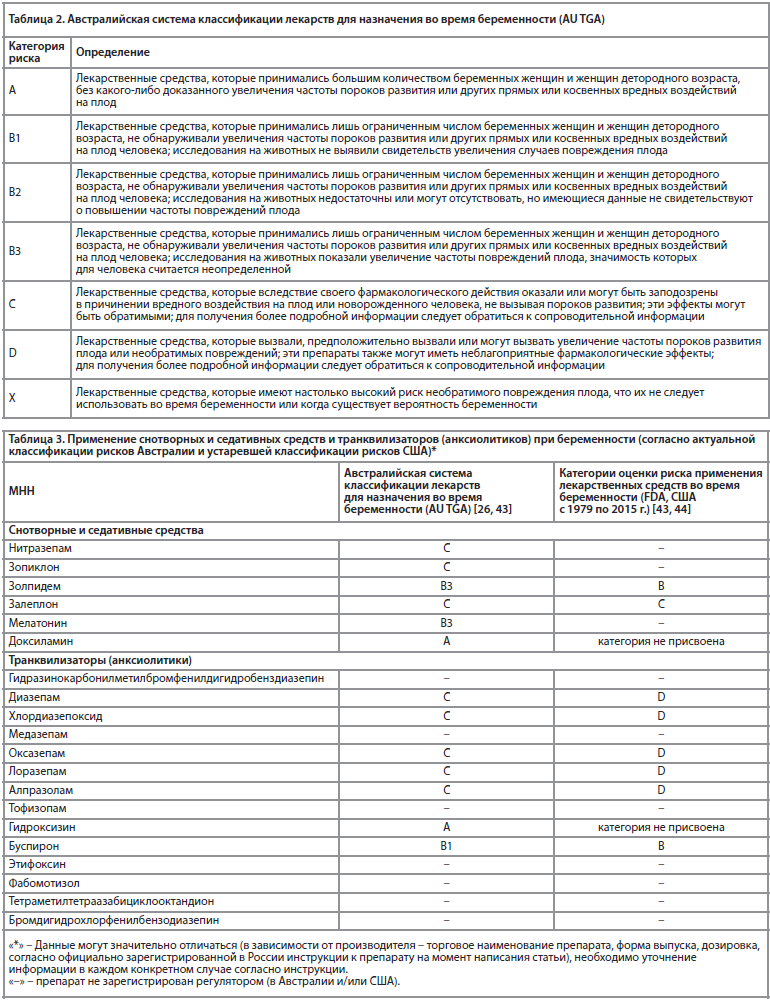
Причем австралийская система категоризации не является иерархической и отличается от американской, несмотря на некоторую схожесть.
Особенности Австралийской системы категоризации [26]:
1. Данные о людях отсутствуют или недостаточны для препаратов категорий B1, B2 и B3;
2. Подкатегории категории B основаны на данных о животных;
3. Присвоение категории В не означает большей безопасности, чем категория С;
4. Лекарственные средства категории D не являются абсолютно противопоказанными во время беременности (например, противосудорожные средства).
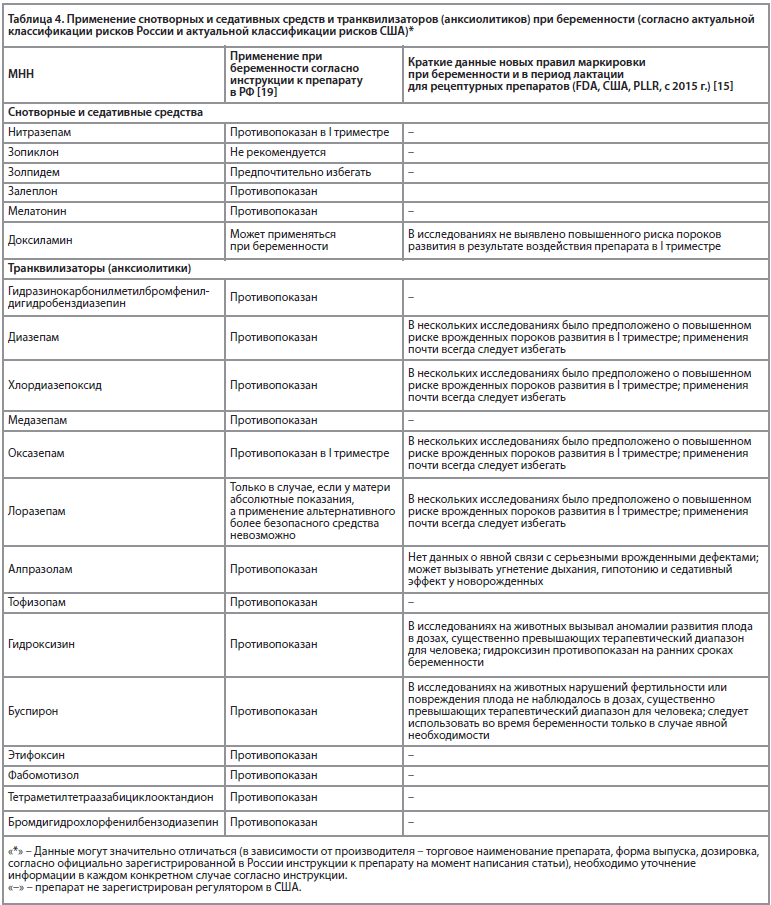
Особенности применения снотворных и седативных средств и транквилизаторов при беременности в России и за рубежом представлены в табл. 3 и 4.
По данным современных качественных исследований, наибольший профиль безопасности из группы антидепрессантов имеют сертралин и циталопрам [49].
По трициклическим антидепрессантам (далее – ТЦА) имеются исследования, которые предполагали, что их воздействие может быть связано с аномалиями конечностей, однако в последующем не были подтверждены последующими исследованиями, о неонатальных нейроповеденческих эффектах воздействия на плод не сообщалось [50-52].
Можно предположить, что антидепрессанты (возможно, за исключением пароксетина и флуоксетина) следует использовать в качестве лечения второй линии во время беременности (после психотерапии), без значительного повышения риска серьезных врожденных пороков развития [53].
Исследования антидепрессантов других групп, не относящихся к селективным ингибиторам обратного захвата серотонина (далее – СИОЗС) и ТЦА, а именно: бупропион, дулоксетин, миртазапин, нефазодон и венлафаксин не обнаружили повышенного риска аномалий развития плода или неблагоприятных событий во время беременности [54-59].
В различных странах (США, Великобритания, Германия, Норвегия, Нидерланды, Канада, Австралия, Новая Зеландия) сообществами специалистов, в большинстве случаев, при беременности, наряду с психотерапией рекомендуется назначение антидепрессантов [42].
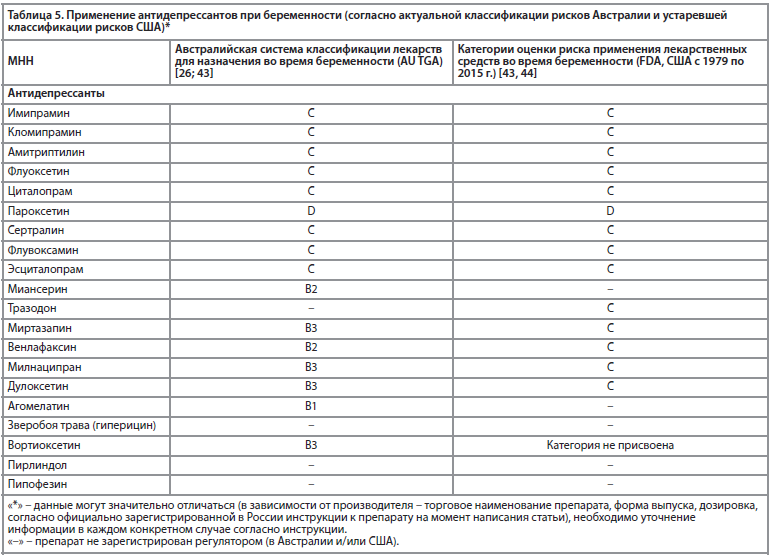
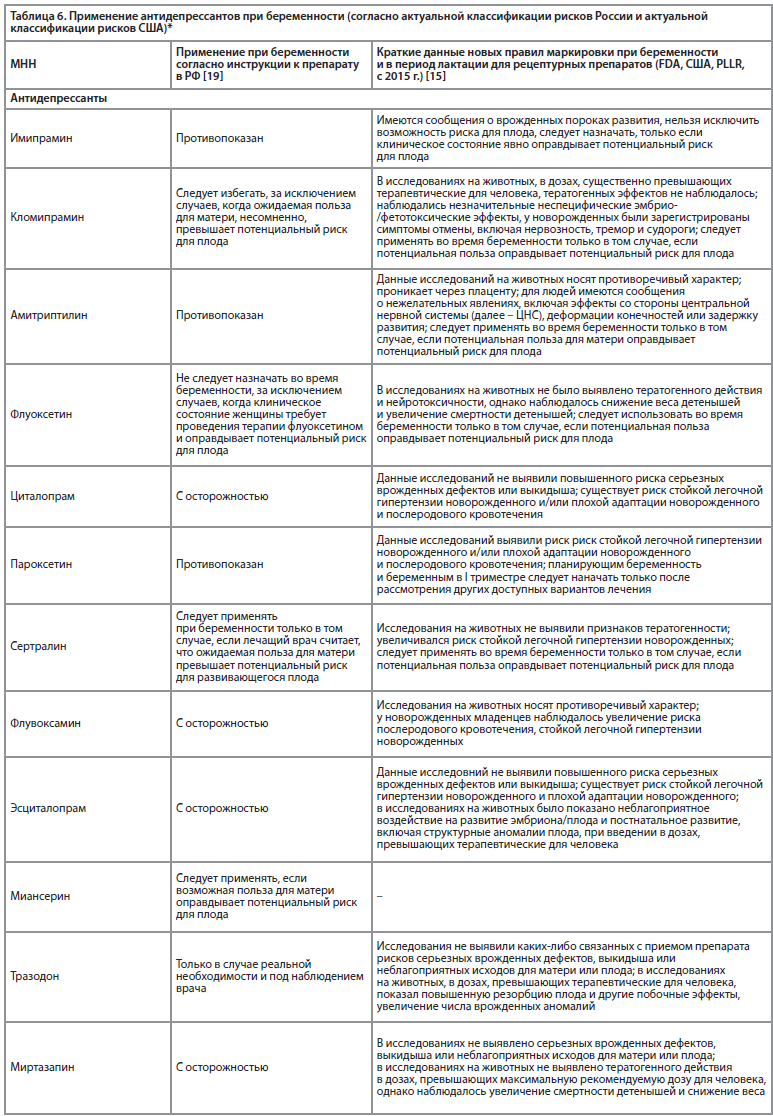
Особенности применения антидепрессантов при беременности в России и за рубежом представлены в табл. 5 и 6.
При применении препаратов лития во время беременности уровень аномалий сердечно-сосудистой системы, включая аномалию Эбштейна, у детей значительно выше, чем в общей популяции [63]. Прием лития матерями, во время беременности, по данным исследований, связан с повышенным риском снижения концентрационной способности мочи, гипотиреоза, гиперпаратиреоза и увеличения веса у новорожденных [64], а также многоводия, преэклампсии, респираторного дистресс-синдрома, гипотонии, преждевременных родов и риска развития дефекта сердечной перегородки [45].
При применении ламотриджина в период беременности был выявлен риск тератогенных эффектов [65], однако метаанализ исходов беременности у женщин, принимавших ламотриджин, и последующие исследования не обнаружили связи между приемом ламотриджина беременной и увеличением частоты врожденных дефектов плода и других неблагоприятных исходов [66, 67].
Имеются исследования карбамазепина, где его прием во время беременности были связан с риском развития т.н. «карбамазепинового синдрома» (дисморфические черты лица и легкая умственная отсталость), причем его распространенность, по-видимому, не связана с дозой или наличием судорог у матери [68].
Есть ограниченные доказательства того, что некоторые стабилизаторы настроения (из группы противоэпилептических препаратов) влияют на метаболизм фолиевой кислоты и что риск пороков развития может быть снижен, если в течение одного месяца перед зачатием, а также в течение I триместра беременности принимать до 4-5 мг фолиевой кислоты в сутки [20, 69-71].
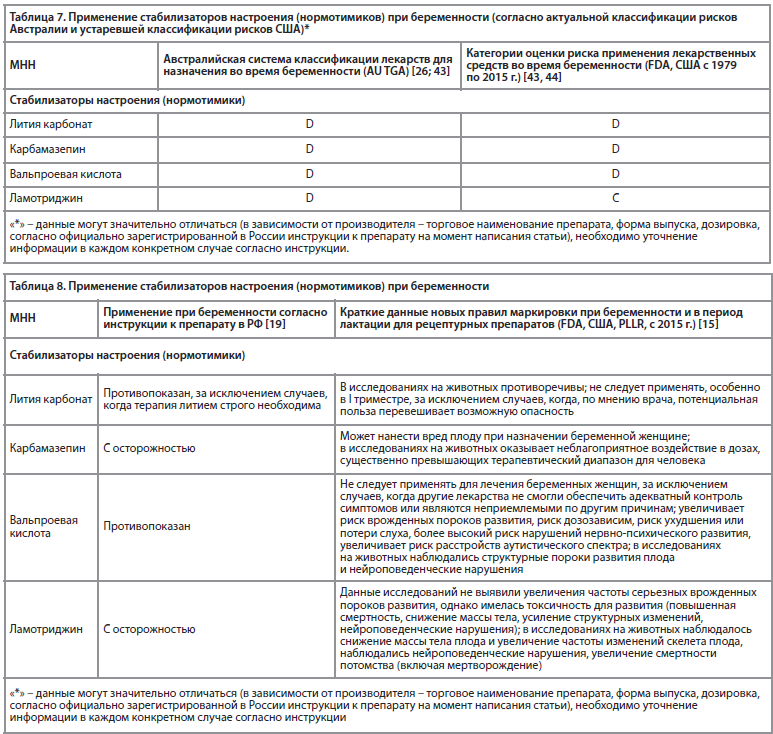
Особенности применения стабилизаторов настроения (нормотимиков) при беременности в России и за рубежом представлены в табл. 7 и 8.
По данным крупных исследований, прием беременными женщинами АП связан с увеличением гестационной массы тела и диабетом, а также с повышенным риском преждевременных родов [45].
Исследования показали, что АПП и антипсихотические препараты второго поколения (далее – АВП), вероятно, связаны с повышенным риском неонатальных осложнений, большинство АВП повышают риск гестационных метаболических осложнений (масса тела детей, родившихся у матерей, которые принимали во время беременности АВП, значительно больше по сравнению с детьми, родившимися от матерей, подвергшихся воздействию АПП), таким образом, вероятно, выбор менее вредного варианта во время беременности должен быть ограничен АПП у пациентов, ранее не принимавших лекарства, если же во время лечения АП наступает беременность, предпочтение следует отдавать продолжению той терапии, которую беременная получала ранее и на которой был эффект [79].
Хотя есть и иные исследования, в которых не подтверждается связь межу приемом АП и риском развития гестационного сахарного диабета, включая АП как первого, так и второго поколения [80, 81].
Результаты большинства существующих на данный момент исследований показывают, что лечение АП во время беременности, по-видимому, безопасно с точки зрения тератогенности во время беременности, по крайней мере при монотерапии [82, 83].
Данные исследований, на данный момент, не подтверждают тератогенное действие клозапина, увеличение риска мертворождения, аборта, преждевременных родов, нарушений развития плода или увеличение риска осложнений при родах, при приеме беременными женщинами [84].
Исследование показывает, что, вероятно, прием оланзапина в I триместре беременности не связан с повышенным риском врожденных пороков развития, прием кветиапина и рисперидона также не дают существенного увеличения риска [85]. Одним из наиболее безопасных АП является клозапин [86].
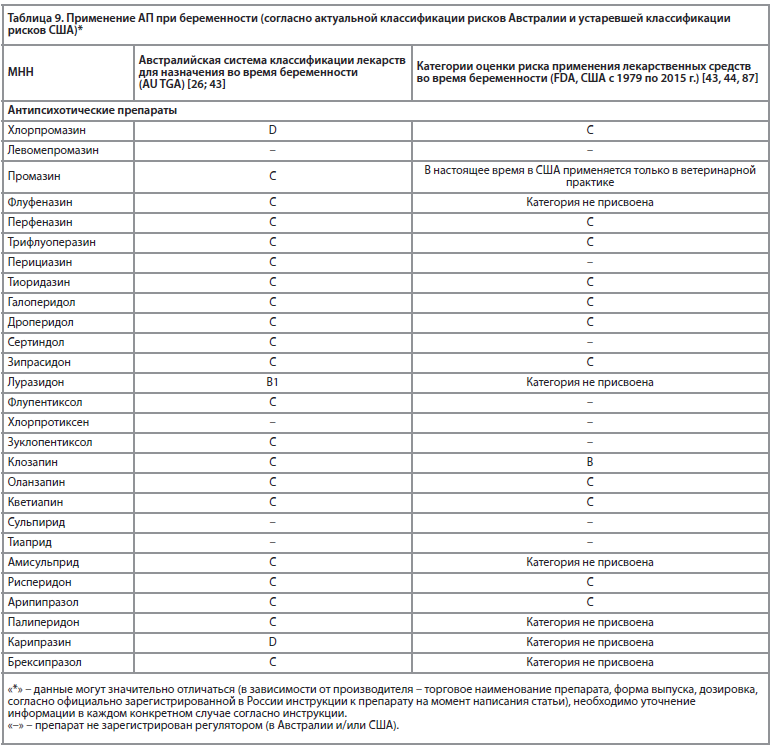
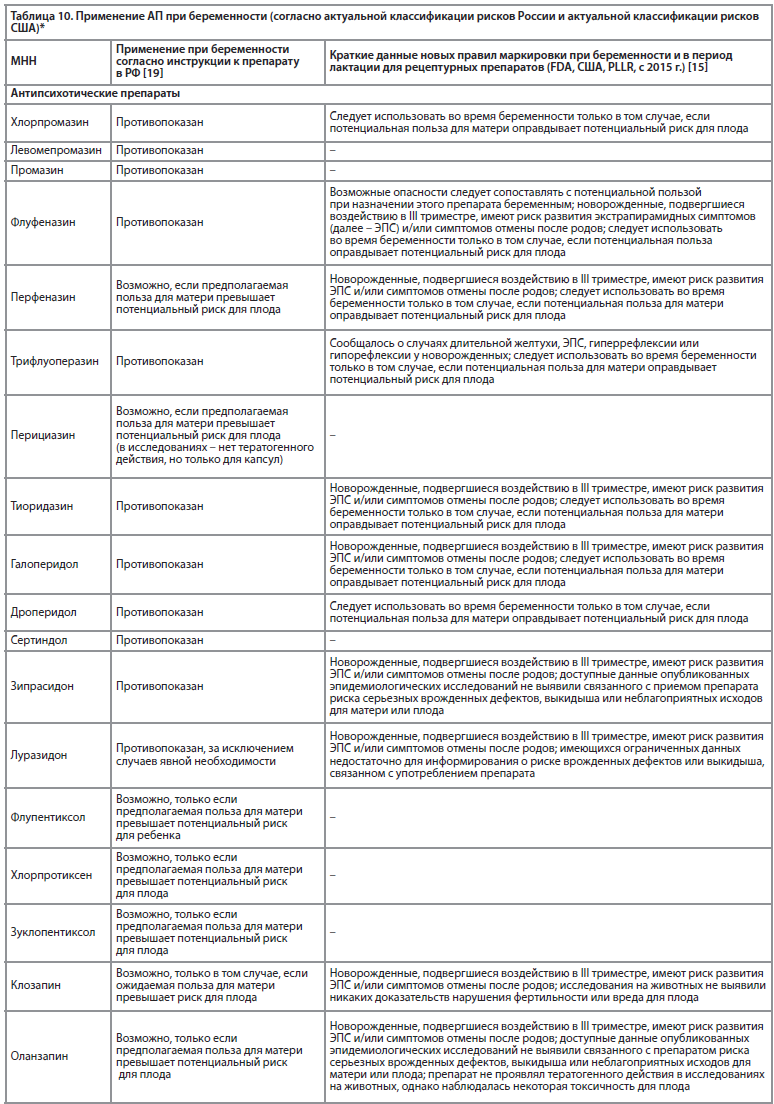
Особенности применения АП при беременности в России и за рубежом представлены в табл. 9 и 10.
Корректоры лекарственно-индуцированных экстрапирамидных расстройств
Препаратом выбора для лечения ЭПС у матери является дифенгидрамин, бета-блокаторы, при коррекции акатизии, также не приводят к учащению случаев врожденных пороков развития и уродств, а вот применение тригексифенидила и амантадина, вероятно, ассоциируется с повышенным риском развития мальформации [89, 90].
Имеются сообщения о беременных женщинах без болезни Паркинсона, принимавших тригексифенидил, у которых родились здоровые дети (серьезных врожденных дефектов не наблюдалось, но увеличилось количество мелких) [91, 92].
Прием амантадина был связан с тератогенным действием при исследованиях, как на животных, так и на людях, его прием беременными повышает риски неблагоприятных исходов для плода, поэтому во время беременности его применение не рекомендуется [93-95].
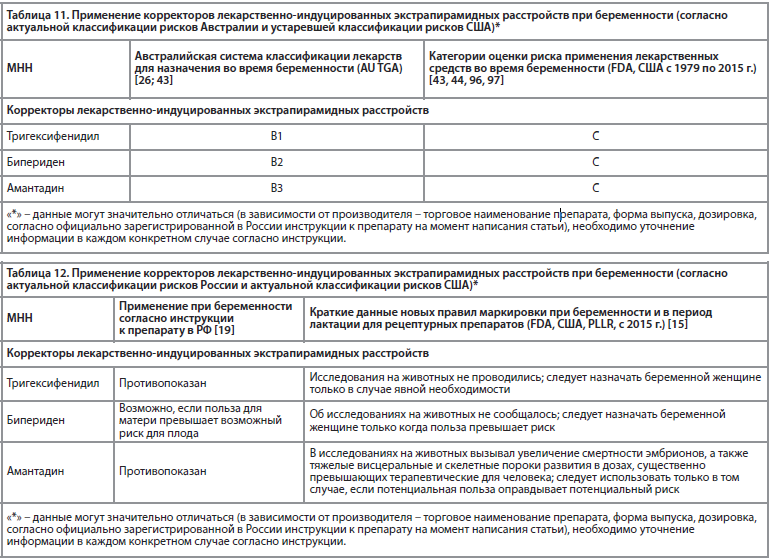
Особенности применения корректоров лекарственно-индуцированных экстрапирамидных расстройств в России и за рубежом представлены в табл. 11 и 12.
В настоящее время общие принципы ведения беременных или планирующих беременность женщин с психическим расстройством выглядят следующим образом:
1. Приоритет планирования беременности на период стойкой ремиссии;
2. Информирование женщин о влиянии психофармакотерапии на саму женщину и плод;
3. Получение согласия на психофармакотерапию в период беременности;
4. При наличии возможности (продолжительная стабильная ремиссия), избегание применения препаратов в период зачатья и в I триместре беременности;
5. При назначении препаратов рассмотрение наиболее безопасных при беременности;
6. Избегание полипрагмазии, приоритет монотерапии;
7. Рассмотрение немедикаментозных подходов к терапии (при наличии показаний и отсутствии противопоказаний) – психотерапия, медицинская реабилитация;
8. Предупреждение о важности постепенной отмены препаратов в случае принятия решения об их отмене, а также о рекомендации частых визитов к психиатру в период беременности;
9. Взаимодействие между психиатром и акушером-гинекологом, который ведет беременную;
10. Продолжение наблюдения у психиатра после родов.
Сведения об авторе
Маслов Константин Андреевич, врач-психиатр ГБУЗ ОПБ
им. К.Р. Евграфова (г. Пенза,), skrembler@mail.ru
Дата поступления: 19.03.2024
Received: 19.03.2024
Принята к печати: 20.05.2024
Accepted: 20.05.2024
Автор заявляет об отсутствии конфликта интересов.
Author declares no conflicts of interest.
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№03 2024
Психофармакотерапия у беременных в России, в современной клинической практике врача-психиатра. Вопросы прикладного практического применения №03 2024
Номера страниц в выпуске:19-32
Резюме
Статья, обобщающая клинические аспекты практики применения основных психофармакологических препаратов у беременных в России в настоящее время. Освещены актуальные вопросы прикладного применения препаратов, их особенностей, тактик назначения.
Ключевые слова: психофармакотерапия у беременных, психофармакотерапия и беременность, антидепрессанты при беременности, антипсихотики при беременности, анксиолитики при беременности, транквилизаторы при беременности, стабилизаторы настроения при беременности, корректоры при беременности.
Для цитирования: Маслов К.А. Психофармакотерапия у беременных в России, в современной клинической практике врача-психиатра. Вопросы прикладного практического применения. Психиатрия и психофармакотерапия. 2024; 3: 19–32. DOI: 10.62202/2075-1761-2024-26-3-19-32
Статья, обобщающая клинические аспекты практики применения основных психофармакологических препаратов у беременных в России в настоящее время. Освещены актуальные вопросы прикладного применения препаратов, их особенностей, тактик назначения.
Ключевые слова: психофармакотерапия у беременных, психофармакотерапия и беременность, антидепрессанты при беременности, антипсихотики при беременности, анксиолитики при беременности, транквилизаторы при беременности, стабилизаторы настроения при беременности, корректоры при беременности.
Для цитирования: Маслов К.А. Психофармакотерапия у беременных в России, в современной клинической практике врача-психиатра. Вопросы прикладного практического применения. Психиатрия и психофармакотерапия. 2024; 3: 19–32. DOI: 10.62202/2075-1761-2024-26-3-19-32
Psychopharmacotherapy in pregnacy in Russia, in modern clinical practice of the psychiatrist. Questions of applied practical application
K.A. MaslovK.R. Evgrafov Mental Hospital.
440026, Russian Federation, Penza, ul. Lermontova, d. 28. skrembler@mail.ru
Abstract
An article summarizing the clinical aspects of the practice of using basic psychopharmacological drugs in pregnant women in Russia at the present time. Topical issues of the applied use of drugs, their features, and prescription tactics are covered.
Keywords: psychopharmacotherapy in pregnacy, psychopharmacotherapy and pregnancy, antidepressants in pregnancy, antipsychotics in pregnancy, anxiolytics in pregnancy, tranquilizers in pregnancy, mood stabilizers in pregnancy, correctors in pregnancy.
For citation: Maslov K.A. Psychopharmacotherapy in pregnacy in Russia, in modern clinical practice of the psychiatrist. Questions of applied practical application. Psychiatry and psychopharmacotherapy. 2024; 3: 19–32. DOI: 10.62202/2075-1761-2024-26-3-19-32
Введение
Важным вопросом клинической практики психиатрии является применение психофармакотерапии у беременных. Период беременности характеризуются значительными биологическими, психологическими и социальными изменениями, которые влияют на мать и плод. Гормональная и биологическая перестройка организма женщины при беременности могут влиять на патологию течения беременности и увеличивать риски развития и обострения психических расстройств [1]. По сведениям ВОЗ, более 90% женщин в мире во время беременности принимают какие-либо лекарственные средства, а также алкоголь, никотин и даже наркотики [2], в России наблюдается примерно аналогичная картина [3]. Нередко при беременности имеются определенные предубеждения против лекарственных препаратов, особенно в пользу препаратов растительного происхождения и биологически активных добавок к пище, однако по данным исследований их прием увеличивает риск врожденных аномалий [4] и перинатальной смертности [5]. По некоторым сведениям, у женщин с психическими расстройствами риск осложнений во время беременности и родов в 6 и более раз выше, чем в общей популяции [6]. Во время беременности женщины, при наличии показаний, также нуждаются в фармакотерапии психических расстройств. В силу этических вопросов влияние терапии на течение и исходы беременности является одной из наименее изученных областей медицины [7]. По данным разных исследователей, от 10% до 30% женщин используют психотропные препараты в период беременности [8-11]. По некоторым оценкам, более чем для 80% существующих лекарственных средств сведения о безопасности при беременности недостаточны [12]. В целом в популяции риск врожденных аномалий встречается в 1-3% случаев [13], по другим данным предполагаемый фоновый риск серьезных врожденных дефектов и крупных пороков развити, при клинически подтвержденной беременности, составляет 2-4%, а малых пороков и невынашивания до 15-20% [14-17]. Таким образом, вопрос возможности назначения психофармакотерапии у беременных для практического врача имеет важное значение.Общие принципы ведения беременности у пациенток, требующих назначения психофармакотерапии
Ключевым вопросом применения психофармакотерапии, как и лекарственных средств вообще, при беременности является проблема безопасности для плода.Выделяют несколько типов потенциальных нежелательных эффектов психофармакотерапевтических препаратов на плод и новорожденного [18]:
1. Структурные нарушения (врожденные аномалии);
2. Острые неонатальные эффекты, проявляющиеся интоксикацией и синдромом отмены;
3. Внутриутробную смерть;
4. Замедление внутриутробного роста;
5. Нейроповеденческую тератогенность.
Основным общепризнанным принципом фармакотерапии беременных является принятие решения о применении фармакотерапии только в случае, когда возможный риск осложнений для матери или плода при неиспользовании медикаментов превышает риск их побочного действия, что имеет отражение в действующих инструкциях к лекарственным препаратам [19]. Вторым принципом, или т.н. условным «золотым правилом», является подход максимального (по возможности) отказа матери от какой-либо фармакотерапии в I триместре беременности (в период закладки нервной трубки и других жизненно важных органов).
Прием лекарственных средств, получаемых отцом, малоизучен, но есть мнение, что прием фармакотерапии отцом до зачатия не приводит к значимому риску развития серьезных врожденных аномалий.
При выборе психофармакологического средства отдается предпочтение препаратам с меньшим количеством метаболитов, более высоким связыванием с белками (снижают плацентарный проход) и меньшим количеством взаимодействий с другими лекарствами [20]. По данным доступных исследований, прием поддерживающей фармакотерапии во время беременности у женщин с различными психическими расстройствами значительно снижает риск рецидива [21]. Принимая во внимание, что качественные рандомизированные плацебо-контролируемые клинические испытания применения психофармакотерапевтических препаратов у беременных недоступны по этическим соображениям, поскольку беременные женщины с различными психопатологическими расстройствами нуждаются в лечении, мы располагаем натуралистическими данными, таким образом большая часть существующих исследований психофармакологии менее качественные, чем другие современные рандомизированные клинические испытания [22]. Достаточно сложно оценить влияние именно приема именно психотропных препаратов на плод у беременных, в сравнении с незатронутой популяцией, поскольку невозможно достоверно оценить влияние психопатологических расстройств (генетической предрасположенности или психиатрических расстройств родителей), а не приема психофармакотерапии, связанной с данной патологией [23].
Некоторые современные классификации рисков
В отечественной клинической практике в настоящее время используется указание на особенности применения при беременности в инструкции к лекарственному препарату, где есть либо указание на то, противопоказан или нет конкретный препарат во время беременности, либо имеется отдельный раздел, посвященный беременности и лактации, где описаны особенности назначения препарата при беременности. В случае, если применение препарата не противопоказано, обычно оно разрешено только в случае, если предполагаемая польза для матери превышает потенциальный риск для плода [19].С 1979 по 2015 год Агентством по контролю безопасности пищевых продуктов и лекарственных средств (Food and Drug Administration – FDA) в США для определения степени риска неблагоприятного воздействия лекарственных средств на плод была введена и применялась система категорий оценки риска применения лекарственных средств во время беременности, в которой лекарственные средства были распределены на 4 категории от А (безопасные) до Х (противопоказанные), которая представлена в табл. 1 [24, 25].

С 2015 года и по сегодняшний день FDA в США введены новые правила маркировки лекарственных при беременности и в период лактации для рецептурных препаратов (Pregnancy and Lactation Labeling Rule – PLLR or final rule), где вместо категорий A, B, C, D, X к каждому препарату прилагается индивидуальное резюме, включающее риски использования препарата во время беременности и в период лактации, с ссылкой на доклинические и клинические исследования, указанием проникновения препарата в грудное молоко, рисков для женщин и мужчин репродуктивного возраста, необходимости тестирования на беременность, контрацепции и риска бесплодия от препарата [24].
В Австралии существует похожая на американскую система категорий оценки риска применения лекарственных средств во время беременности – Австралийская система классификации лекарств для назначения во время беременности (Australian The Therapeutic Goods Administration – AU TGA), представлена в табл. 2 [26].

Причем австралийская система категоризации не является иерархической и отличается от американской, несмотря на некоторую схожесть.
Особенности Австралийской системы категоризации [26]:
1. Данные о людях отсутствуют или недостаточны для препаратов категорий B1, B2 и B3;
2. Подкатегории категории B основаны на данных о животных;
3. Присвоение категории В не означает большей безопасности, чем категория С;
4. Лекарственные средства категории D не являются абсолютно противопоказанными во время беременности (например, противосудорожные средства).
Снотворные и седативные средства и транквилизаторы (анксиолитики) при беременности
В исследованиях на животных не было выявлено тератогенного действия транквилизаторов [27, 28]. Многочисленные экспериментальные исследования на животных свидетельствуют о «поведенческой тератогенности» бензодиазепинов, в то же время данных о влиянии транквилизаторов на поведение детей при их пренатальном применении не получено [29, 30]. Относительно людей, с одной стороны выявлено, что при применении бензодиазепиновых транквилизаторов в I триместре беременности возрастают риски их тератогенного действия [31-36], с другой стороны, ряд исследователей не выявили отчетливой связи между использованием во время беременности транквилизаторов и развитием врожденных аномалий у детей [37-39]. По сведениям сравнительно крупных исследований, воздействие снотворных средств и бензодиазепиновых транквилизаторов во время беременности не было связано с более высоким риском врожденных пороков развития, но было связано с повышенным риском преждевременных родов, низкой массой тела при рождении, по сравнению с теми младенцами, матери которых не принимали психофармакотерапию [40]. Есть сведения метаанализа миллиона беременностей при применении бензодиазепинов и бензодиазепиноподобных лекарственных препаратов, который не выявил повышенных тератогенных рисков, таких как сердечно-сосудистые пороки развития и расщелина неба, в исследованиях типа «случай-контроль» [41]. В настоящее время исследователи склоняются к мнению, что использование бензодиазепинов, по-видимому, не несет значительного риска соматического тератогенеза [20]. Если во время беременности рассматривается возможность прекращения применения бензодиазепинов, то не следует резко отменять бензодиазепины [20]. Для лечения тревожных симптомов и кратковременного лечения нарушений сна во время беременности можно назначать бензодиазепины, но с целью минимизации фармакологического воздействия препарата на плод предпочтительно применять препараты с коротким периодом полувыведения (например, лоразепам, оксазепам) [42].Особенности применения снотворных и седативных средств и транквилизаторов при беременности в России и за рубежом представлены в табл. 3 и 4.

Антидепрессанты при беременности
По данным крупных исследований, прием беременными женщинами антидепрессантов связан с повышенным риском самопроизвольных абортов, мертворождения, преждевременных родов, дыхательной недостаточности, эндокринных и метаболических нарушений, синдрома отмены, пороков сердца [45], однако другие исследования показывают отсутствие доказательств повышенного риска прибавки веса при гестации, гестационного диабета и задержки увеличения веса после родов, у новорожденных, рожденных женщинами с психическими расстройствами, принимавшими антидепрессанты, по сравнению с женщинами с психическими расстройствами, не получавшими лекарств [46]. Крупные исследования разных лет показали, что у женщин, получавших антидепрессанты в период беременности, не было выявлено каких-либо значительных аномалий развития у потомства [47, 48].По данным современных качественных исследований, наибольший профиль безопасности из группы антидепрессантов имеют сертралин и циталопрам [49].
По трициклическим антидепрессантам (далее – ТЦА) имеются исследования, которые предполагали, что их воздействие может быть связано с аномалиями конечностей, однако в последующем не были подтверждены последующими исследованиями, о неонатальных нейроповеденческих эффектах воздействия на плод не сообщалось [50-52].
Можно предположить, что антидепрессанты (возможно, за исключением пароксетина и флуоксетина) следует использовать в качестве лечения второй линии во время беременности (после психотерапии), без значительного повышения риска серьезных врожденных пороков развития [53].
Исследования антидепрессантов других групп, не относящихся к селективным ингибиторам обратного захвата серотонина (далее – СИОЗС) и ТЦА, а именно: бупропион, дулоксетин, миртазапин, нефазодон и венлафаксин не обнаружили повышенного риска аномалий развития плода или неблагоприятных событий во время беременности [54-59].
В различных странах (США, Великобритания, Германия, Норвегия, Нидерланды, Канада, Австралия, Новая Зеландия) сообществами специалистов, в большинстве случаев, при беременности, наряду с психотерапией рекомендуется назначение антидепрессантов [42].
Особенности применения антидепрессантов при беременности в России и за рубежом представлены в табл. 5 и 6.


Стабилизаторы настроения (нормотимики)
Обзор исследований стабилизаторов настроения показал, что воздействие всех четырех широко используемых стабилизаторов настроения (вальпроаты, препараты лития, ламотриджин, карбамазепин) во время беременности увеличивает риски тератогенного воздействия на плод (дефекты нервной трубки, сердечные и черепно-лицевые дефекты), частоту осложнений беременности и неонатальных осложнений, из всех стабилизаторов настроения прием вальпроатов может быть связан с увеличением риска негативных последствий для развития нервной системы детей в долгосрочной перспективе [60, 61]. Вальпроаты оказывают значительное тератогенное действие, включая дефекты нервной трубки [62].При применении препаратов лития во время беременности уровень аномалий сердечно-сосудистой системы, включая аномалию Эбштейна, у детей значительно выше, чем в общей популяции [63]. Прием лития матерями, во время беременности, по данным исследований, связан с повышенным риском снижения концентрационной способности мочи, гипотиреоза, гиперпаратиреоза и увеличения веса у новорожденных [64], а также многоводия, преэклампсии, респираторного дистресс-синдрома, гипотонии, преждевременных родов и риска развития дефекта сердечной перегородки [45].
При применении ламотриджина в период беременности был выявлен риск тератогенных эффектов [65], однако метаанализ исходов беременности у женщин, принимавших ламотриджин, и последующие исследования не обнаружили связи между приемом ламотриджина беременной и увеличением частоты врожденных дефектов плода и других неблагоприятных исходов [66, 67].
Имеются исследования карбамазепина, где его прием во время беременности были связан с риском развития т.н. «карбамазепинового синдрома» (дисморфические черты лица и легкая умственная отсталость), причем его распространенность, по-видимому, не связана с дозой или наличием судорог у матери [68].
Есть ограниченные доказательства того, что некоторые стабилизаторы настроения (из группы противоэпилептических препаратов) влияют на метаболизм фолиевой кислоты и что риск пороков развития может быть снижен, если в течение одного месяца перед зачатием, а также в течение I триместра беременности принимать до 4-5 мг фолиевой кислоты в сутки [20, 69-71].
Особенности применения стабилизаторов настроения (нормотимиков) при беременности в России и за рубежом представлены в табл. 7 и 8.

Антипсихотические препараты при беременности
По данным ряда исследований считается, что тератогенный риск для группы антипсихотических препаратов (далее – АП) в целом не превышает таковой в общей популяции [72-75], также не наблюдалось увеличение риска нарушений развития и побочных эффектов у новорожденных [76]. По данным исследований, многолетний катамнез детей, матери которых принимали антипсихотические препараты первого поколения (далее – АПП) во время беременности, не было выявлено каких-либо отклонений в их поведении [77]. Крупное когортное исследование детей с наблюдением за ними до 14-летнего возраста показало, что повышенный риск расстройств психического развития (таких как расстройства аутистического спектра, синдром дефицита внимания с гиперактивностью, задержка психического развития, речевые расстройства, умственная отсталость и поведенческие нарушения), наблюдаемый у детей, рожденных от женщин, принимавших АП на поздних сроках беременности, по-видимому, объясняется характеристиками матери и не связан причинно-следственной связью с пренатальным воздействием АП [78].По данным крупных исследований, прием беременными женщинами АП связан с увеличением гестационной массы тела и диабетом, а также с повышенным риском преждевременных родов [45].
Исследования показали, что АПП и антипсихотические препараты второго поколения (далее – АВП), вероятно, связаны с повышенным риском неонатальных осложнений, большинство АВП повышают риск гестационных метаболических осложнений (масса тела детей, родившихся у матерей, которые принимали во время беременности АВП, значительно больше по сравнению с детьми, родившимися от матерей, подвергшихся воздействию АПП), таким образом, вероятно, выбор менее вредного варианта во время беременности должен быть ограничен АПП у пациентов, ранее не принимавших лекарства, если же во время лечения АП наступает беременность, предпочтение следует отдавать продолжению той терапии, которую беременная получала ранее и на которой был эффект [79].
Хотя есть и иные исследования, в которых не подтверждается связь межу приемом АП и риском развития гестационного сахарного диабета, включая АП как первого, так и второго поколения [80, 81].
Результаты большинства существующих на данный момент исследований показывают, что лечение АП во время беременности, по-видимому, безопасно с точки зрения тератогенности во время беременности, по крайней мере при монотерапии [82, 83].
Данные исследований, на данный момент, не подтверждают тератогенное действие клозапина, увеличение риска мертворождения, аборта, преждевременных родов, нарушений развития плода или увеличение риска осложнений при родах, при приеме беременными женщинами [84].
Исследование показывает, что, вероятно, прием оланзапина в I триместре беременности не связан с повышенным риском врожденных пороков развития, прием кветиапина и рисперидона также не дают существенного увеличения риска [85]. Одним из наиболее безопасных АП является клозапин [86].
Особенности применения АП при беременности в России и за рубежом представлены в табл. 9 и 10.


Инъекционные лекарственные формы АП пролонгированного действия
В настоящее время в литературе отсутствуют обобщающие данные относительно применения инъекционных АП пролонгированного действия (long-acting injectable antipsychotic – LAI) во время беременности, по сравнению с пероральными препаратами, однако эксперты считают, что в настоящее время, для принятия клинических решений, возможно опираться на имеющуюся информацию по пероральным формам АП и по клиническим показаниям использовать приемущества прологированных форм АП в терапии психотических расстройств у беременных [88], см. табл. 9 и 10.Корректоры лекарственно-индуцированных экстрапирамидных расстройств
Препаратом выбора для лечения ЭПС у матери является дифенгидрамин, бета-блокаторы, при коррекции акатизии, также не приводят к учащению случаев врожденных пороков развития и уродств, а вот применение тригексифенидила и амантадина, вероятно, ассоциируется с повышенным риском развития мальформации [89, 90].
Имеются сообщения о беременных женщинах без болезни Паркинсона, принимавших тригексифенидил, у которых родились здоровые дети (серьезных врожденных дефектов не наблюдалось, но увеличилось количество мелких) [91, 92].
Прием амантадина был связан с тератогенным действием при исследованиях, как на животных, так и на людях, его прием беременными повышает риски неблагоприятных исходов для плода, поэтому во время беременности его применение не рекомендуется [93-95].
Особенности применения корректоров лекарственно-индуцированных экстрапирамидных расстройств в России и за рубежом представлены в табл. 11 и 12.

Заключение
Применение психофармакотерапевтических препаратов у беременных подразумевает необходимость оценки врачом-психиатром соотношения пользы для матери и риска для плода, в каждом конкретном случае, что зачастую является непростой задачей. Особенности психофармакотерапии беременных, сопутствующие проблемы, а также пути их преодоления изучены в многочисленных научных исследованиях, однако эффективное и научно обоснованное назначение фармакотерапии там, где она необходима, и отказ от нее там, где в ней нет нужды, в частности требует более подробной проработки данного вопроса и включения его в национальные клинические рекомендации, в соответствии с требованиями доказательной медицины.В настоящее время общие принципы ведения беременных или планирующих беременность женщин с психическим расстройством выглядят следующим образом:
1. Приоритет планирования беременности на период стойкой ремиссии;
2. Информирование женщин о влиянии психофармакотерапии на саму женщину и плод;
3. Получение согласия на психофармакотерапию в период беременности;
4. При наличии возможности (продолжительная стабильная ремиссия), избегание применения препаратов в период зачатья и в I триместре беременности;
5. При назначении препаратов рассмотрение наиболее безопасных при беременности;
6. Избегание полипрагмазии, приоритет монотерапии;
7. Рассмотрение немедикаментозных подходов к терапии (при наличии показаний и отсутствии противопоказаний) – психотерапия, медицинская реабилитация;
8. Предупреждение о важности постепенной отмены препаратов в случае принятия решения об их отмене, а также о рекомендации частых визитов к психиатру в период беременности;
9. Взаимодействие между психиатром и акушером-гинекологом, который ведет беременную;
10. Продолжение наблюдения у психиатра после родов.
Сведения об авторе
Маслов Константин Андреевич, врач-психиатр ГБУЗ ОПБ
им. К.Р. Евграфова (г. Пенза,), skrembler@mail.ru
Дата поступления: 19.03.2024
Received: 19.03.2024
Принята к печати: 20.05.2024
Accepted: 20.05.2024
Автор заявляет об отсутствии конфликта интересов.
Author declares no conflicts of interest.
Список исп. литературыСкрыть список1. Hallberg P, Sjöblom V. The use of selective serotonin reuptake inhibitors during pregnancy and breast-feeding: a review and clinical aspects. J Clin Psychopharmacol. 2005 Feb;25(1):59-73.
2. Jacobs LR. Prescription to over-the-counter drug reclassification. Am Fam Physician. 1998 May 1;57(9):2209-14.
3. Стриженок Е.А., Гудков И.В., Страчунский Л.С. Применение лекарственных средств при беременности: результаты многоцентрового фармакоэпидемиологического исследования. Клиническая Микробиология и Антимикробная Химиотерапия. 2007; 9(2):162-175. / Strizhenok E.A., Gudkov I.V., Strachunskij L.S. Primenenie lekarstvenny`x sredstv pri beremennosti: rezul`taty` mnogocentrovogo farmakoe`pidemiologicheskogo issledovaniya. Klinicheskaya Mikrobiologiya i Antimikrobnaya Ximioterapiya. 2007; 9(2):162-175. [in Russian].
4. Chuang CH, Doyle P, Wang JD et al. Herbal medicines used during the first trimester and major congenital malformations: an analysis of data from a pregnancy cohort study. Drug Saf. 2006;29(6):537-48.
5. Ab Rahman A, Ahmad Z, Naing L et al. The use of herbal medicines during pregnancy and perinatal mortality in Tumpat District, Kelantan, Malaysia. Southeast Asian J Trop Med Public Health. 2007 Nov;38(6):1150-7.
6. Dally A. Motherhood and Mental Illness. Edited by I. F. Brockington and R. Kumar London: Academic Press. 1982. Pp 265.
7. Ушкалова Е. А., Ткачева О. Н., Чухарева Н. А. Проблемы безопасности применения лекарственных средств во время беременности и кормления грудью. Акушерство и гинекология. 2011. №2. С.4–7. / Ushkalova E. A., Tkacheva O. N., Chuxareva N. A. Problemy` bezopasnosti primeneniya lekarstvenny`x sredstv vo vremya beremennosti i kormleniya grud`yu. Akusherstvo i ginekologiya. 2011. №2. S.4–7. [in Russian].
8. Christopher LJ. Taking drugs during pregnancy. Dev Med Child Neurol. 1978 Jun;20(3):380-3.
9. Forfar JO, Nelson MM. Epidemiology of drugs taken by pregnant women: drugs that may affect the fetus adversely. Clin Pharmacol Ther. 1973 Jul-Aug;14(4):632-42.
10. Paton C. Prescribing in pregnancy. Br J Psychiatry. 2008 May;192(5):321-2.
11. Rayburn W, Wible-Kant J, Bledsoe P. Changing trends in drug use during pregnancy. J Reprod Med. 1982 Sep;27(9):569-75.
12. Lo WY, Friedman JM. Teratogenicity of recently introduced medications in human pregnancy. Obstet Gynecol. 2002 Sep;100(3):465-73.
13. Portnoi G, Chng LA, Karimi-Tabesh L et al. Prospective comparative study of the safety and effectiveness of ginger for the treatment of nausea and vomiting in pregnancy. Am J Obstet Gynecol. 2003 Nov;189(5):1374-7.
14, The DailyMed database [Electronic resource]. URL: http://dailymed.nlm. nih.gov/. (access date: 17.03.2024).
15. Centers for Disease Control and Prevention (CDC). Update on overall prevalence of major birth defects--Atlanta, Georgia, 1978-2005. MMWR Morb Mortal Wkly Rep. 2008 Jan 11;57(1):1-5.
16. Rasmussen SA, Hernandez-Diaz S, Abdul-Rahman OA et al. Assessment of congenital anomalies in infants born to pregnant women enrolled in clinical trials. Clin Infect Dis. 2014 Dec 15;59 Suppl 7(Suppl 7):S428-36.
17. Feldkamp ML, Carey JC, Byrne JLB et al. Etiology and clinical presentation of birth defects: population based study. BMJ. 2017 May 30;357:j2249.
18. Ушкалова, А. В. Лечение психических заболеваний в период беременности. Ушкалова А. В., Ушкалова Е. А. Фарматека. 2013. № 10(263). С. 76-85. / Ushkalova, A. V. Lechenie psixicheskix zabolevanij v period beremennosti. Ushkalova A. V., Ushkalova E. A. Farmateka. 2013. № 10(263). S. 76-85. [in Russian].
19. Государственный реестр лекарственных средств [Электронный ресурс]. URL: http://grls.rosminzdrav.ru. (Дата обращения: 17.03.2024). / Gosudarstvennyj reestr lekarstvennyh sredstv [Elektronnyj resurs]. URL: http://grls.rosminzdrav.ru. (Data obrashcheniya: 17.03.2024). [in Russian].
20. Rostin P, Balke S, Sroka D et al. The CHANGED Score-A New Tool for the Prediction of Insulin Dependency in Gestational Diabetes. J Clin Med. 2023 Nov 18;12(22):7169.
21. Stevens AWMM, Goossens PJJ, Knoppert-van der Klein EAM et al. Risk of recurrence of mood disorders during pregnancy and the impact of medication: A systematic review. J Affect Disord. 2019 Apr 15;249:96-103.
22. El Marroun H, White T, Verhulst FC et al. Maternal use of antidepressant or anxiolytic medication during pregnancy and childhood neurodevelopmental outcomes: a systematic review. Eur Child Adolesc Psychiatry. 2014 Oct;23(10):973-92.
23. Poels EMP, Schrijver L, Kamperman AM et al. Long-term neurodevelopmental consequences of intrauterine exposure to lithium and antipsychotics: a systematic review and meta-analysis. Eur Child Adolesc Psychiatry. 2018 Sep;27(9):1209-1230.
24. The Food and Drug Administration (FDA) website. Pregnancy and Lactation Labeling (Drugs) Final Rule [Electronic resource]. URL: http://www.fda.gov/drugs/labeling-information-drug-products/pregnancy-and-lactation-labeling-drugs-f.... (access date: 17.03.2024).
25. Лызикова Ю. А., Эйныш Е. А. Применение лекарственных средств во время беременности. Проблемы здоровья и экологии. 2012. №3(33). С.88-95. / Ly`zikova Yu. A., E`jny`sh E. A. Primenenie lekarstvenny`x sredstv vo vremya beremennosti. Problemy` zdorov`ya i e`kologii. 2012. №3(33). S.88-95. [in Russian].
26. The Therapeutic Goods Administration (TGA) is Australia's regulatory authority for therapeutic goods. Australian categorisation system for prescribing medicines in pregnancy [Electronic resource]. URL: http://www.tga.gov.au/australian-categorisation-system-prescribing-medicines-pregnancy. (access date: 17.03.2024).
27. Кирющенков А. П., Тараховский М. Л. Влияние лекарственных средств на плод. – М.: Медицина, 1990. – 271 с. / Kiryushhenkov A. P., Taraxovskij M. L. Vliyanie lekarstvenny`x sredstv na plod. – M.: Medicina, 1990. 271s. [in Russian].
28. Tuchmann-Duplessis H. Drugs and other xenobiotics as teratogens. Pharmacol Ther. 1984;26(3):273-344.
29. Pascuzzi Jackson V, DeMyer W, Hingtgen J. Delayed maze-learning in rats after prenatal exposure to clorazepate. Arch Neurol. 1980 Jun;37(6):350-1.
30. Maderdrut JL, Oppenheim RW, Reitzel JL. Behavioral analysis of benzodiazepine-mediated inhibition in the early chick embryo. Brain Res. 1983 Dec 19;289(1-2):385-90.
31. Aarskog D. Letter: Association between maternal intake of diazepam and oral clefts. Lancet. 1975 Nov 8;2(7941):921.
32. Laegreid L, Olegård R, Wahlström J et al. Abnormalities in children exposed to benzodiazepines in utero. Lancet. 1987 Jan 10;1(8524):108-9.
33. Safra MJ, Oakley GP Jr. Association between cleft lip with or without cleft palate and prenatal exposure to diazepam. Lancet. 1975 Sep 13;2(7933):
478-80.
34. Saxén I, Saxén L. Letter: Association between maternal intake of diazepam and oral clefts. Lancet. 1975 Sep 13;2(7933):498.
35. Crombie DL, Pinsent RJ, Fleming DM et al. Letter: Fetal effects of tranquilizers in pregnancy. N Engl J Med. 1975 Jul 24;293(4):198-9.
36. Milkovich L, van den Berg BJ. Effects of prenatal meprobamate and chlordiazepoxide hydrochloride on human embryonic and fetal development. N Engl J Med. 1974 Dec 12;291(24):1268-71.
37. Hartz SC, Heinonen OP, Shapiro S et al. Antenatal exposure to meprobamate and chlordiazepoxide in relation to malformations, mental development, and childhood mortality. N Engl J Med. 1975 Apr 3;292(14):726-8.
38. Jick H, Holmes LB, Hunter JR et al. First-trimester drug use and congenital disorders. JAMA. 1981 Jul 24-31;246(4):343-6.
39. Rosenberg L, Mitchell AA, Parsells JL et al. Lack of relation of oral clefts to diazepam use during pregnancy. N Engl J Med. 1983 Nov 24;309(21):1282-5.
40. Grigoriadis S, Alibrahim A, Mansfield JK et al. Hypnotic benzodiazepine receptor agonist exposure during pregnancy and the risk of congenital malformations and other adverse pregnancy outcomes: A systematic review and meta-analysis. Acta Psychiatr Scand. 2022 Oct;146(4):312-324.
41. Bais B, Molenaar NM, Bijma HH et al. Prevalence of benzodiazepines and benzodiazepine-related drugs exposure before, during and after pregnancy: A systematic review and meta-analysis. J Affect Disord. 2020 May 15;269:18-27.
42. Eleftheriou G, Zandonella Callegher R, Butera R et al. Consensus Panel Recommendations for the Pharmacological Management of Pregnant Women with Depressive Disorders. Int J Environ Res Public Health. 2023 Aug 11;20(16):6565.
43. The Drugs.com Drug Information Database Website [Electronic resource]. URL: http://www.drugs.com/. (access date: 17.03.2024).
44. American Family Physician (AFP) Website. ACOG Guidelines on Psychiatric Medication Use During Pregnancy and Lactation [Electronic resource]. URL: http://www.aafp.org/pubs/afp/issues/2008/0915/p772.html. (access date: 17.03.2024).
45. Oyebode F, Rastogi A, Berrisford G et al. Psychotropics in pregnancy: safety and other considerations. Pharmacol Ther. 2012 Jul;135(1):71-7.
46. Lopez-Yarto M, Ruiz-Mirazo E, Holloway AC et al. Do psychiatric medications, especially antidepressants, adversely impact maternal metabolic outcomes? J Affect Disord. 2012 Dec 10;141(2-3):120-9.
47. Rowe IL. Prescriptions of psychotropic drugs by general practitioners. 2. Antidepressants. Med J Aust. 1973 Mar 31;1(13):642-4.
48. Pedersen LH, Henriksen TB, Vestergaard M et al. Selective serotonin reuptake inhibitors in pregnancy and congenital malformations: population based cohort study. BMJ. 2009 Sep 23;339:b3569.
49. Koren G, Nordeng H. Antidepressant use during pregnancy: the benefit-risk ratio. Am J Obstet Gynecol. 2012 Sep;207(3):157-63.
50. Altshuler LL, Cohen L, Szuba MP et al. Pharmacologic management of psychiatric illness during pregnancy: dilemmas and guidelines. Am J Psychiatry. 1996 May;153(5):592-606.
51. McElhatton PR, Garbis HM, Eléfant E et al. The outcome of pregnancy in 689 women exposed to therapeutic doses of antidepressants. A collaborative study of the European Network of Teratology Information Services (ENTIS). Reprod Toxicol. 1996 Jul-Aug;10(4):285-94.
52. Nulman I, Rovet J, Stewart DE et al. Neurodevelopment of children exposed in utero to antidepressant drugs. N Engl J Med. 1997 Jan 23;336(4):258-62.
53. Desaunay P, Eude LG, Dreyfus M et al. Benefits and Risks of Antidepressant Drugs During Pregnancy: A Systematic Review of Meta-analyses. Paediatr Drugs. 2023 May;25(3):247-265.
54. Källén B. Neonate characteristics after maternal use of antidepressants in late pregnancy. Arch Pediatr Adolesc Med. 2004 Apr;158(4):312-6.
55. Yaris F, Kadioglu M, Kesim M et al. Newer antidepressants in pregnancy: prospective outcome of a case series. Reprod Toxicol. 2004 Dec;19(2):
235-8.
56. Yaris F, Ulku C, Kesim M et al. Psychotropic drugs in pregnancy: a case-control study. Prog Neuropsychopharmacol Biol Psychiatry. 2005 Feb;29(2):333-8.
57. Kesim M, Yaris F, Kadioglu M et al. Mirtazapine use in two pregnant women: is it safe? Teratology. 2002 Nov;66(5):204.
58. Rohde A, Dembinski J, Dorn C. Mirtazapine (Remergil) for treatment resistant hyperemesis gravidarum: rescue of a twin pregnancy. Arch Gynecol Obstet. 2003 Aug;268(3):219-21.
59. Einarson A, Bonari L, Voyer-Lavigne S et al. A multicentre prospective controlled study to determine the safety of trazodone and nefazodone use during pregnancy. Can J Psychiatry. 2003 Mar;48(2):106-10.
60. Galbally M, Roberts M, Buist A; Perinatal Psychotropic Review Group. Mood stabilizers in pregnancy: a systematic review. Aust N Z J Psychiatry. 2010 Nov;44(11):967-77.
61. Haskey C, Galbally M. Mood stabilizers in pregnancy and child developmental outcomes: A systematic review. Aust N Z J Psychiatry. 2017 Nov;51(11):1087-1097.
62. Smith J, Whitehall J. Sodium valproate and the fetus: a case study and review of the literature. Neonatal Netw. 2009 Nov-Dec;28(6):363-7.
63. Weinstein MR, Goldfield M. Cardiovascular malformations with lithium use during pregnancy. Am J Psychiatry. 1975 May;132(5):529-31.
64. McKnight RF, Adida M, Budge K et al. Lithium toxicity profile: a systematic review and meta-analysis. Lancet. 2012 Feb 25;379(9817):721-8.
65. Berwaerts K, Sienaert P, De Fruyt J. Teratogene effecten van lamotrigine bij vrouwen met een bipolaire stoornis [Teratogenic effects of lamotrigine in women with bipolar disorder]. Tijdschr Psychiatr. 2009;51(10):741-50.
66. Pariente G, Leibson T, Shulman T et al. Pregnancy Outcomes Following In Utero Exposure to Lamotrigine: A Systematic Review and Meta-Analysis. CNS Drugs. 2017 Jun;31(6):439-450.
67. Veroniki AA, Cogo E, Rios P et al. Comparative safety of anti-epileptic drugs during pregnancy: a systematic review and network meta-analysis of congenital malformations and prenatal outcomes. BMC Med. 2017 May 5;15(1):95.
68. Ornoy A, Cohen E. Outcome of children born to epileptic mothers treated with carbamazepine during pregnancy. Arch Dis Child. 1996 Dec;75(6):517-20.
69. Walker SP, Permezel M, Berkovic SF. The management of epilepsy in pregnancy. BJOG. 2009 May;116(6):758-67.
70. Kjaer D, Horvath-Puhó E, Christensen J et al. Antiepileptic drug use, folic acid supplementation, and congenital abnormalities: a population-based case-control study. BJOG. 2008 Jan;115(1):98-103.
71. Galbally M, Snellen M, Walker S et al. Management of antipsychotic and mood stabilizer medication in pregnancy: recommendations for antenatal care. Aust N Z J Psychiatry. 2010 Feb;44(2):99-108.
72. Slone D, Siskind V, Heinonen OP et al. Antenatal exposure to the phenothiazines in relation to congenital malformations, perinatal mortality rate, birth weight, and intelligence quotient score. Am J Obstet Gynecol. 1977 Jul 1;128(5):486-8.
73. Gentile S. Antipsychotic therapy during early and late pregnancy. A systematic review. Schizophr Bull. 2010 May;36(3):518-44.
74. Milkovich L, van den Berg BJ. An evaluation of the teratogenicity of certain antinauseant drugs. Am J Obstet Gynecol. 1976 May 15;125(2):244-8.
75. Van Waes A, Van de Velde F. Safety evaluation of haloperidol in the treatment of hyperemesis gravidarum. J. Clin. Pharm. 1969;9(4):224–227.
76. Einarson A, Boskovic R. Use and safety of antipsychotic drugs during pregnancy. J Psychiatr Pract. 2009 May;15(3):183-92.
77. Stika L, Elisová K, Honzáková L et al. Effects of drug administration in pregnancy on children's school behaviour. Pharm Weekbl Sci. 1990 Dec 14;12(6):252-5.
78. Straub L, Hernández-Díaz S, Bateman BT et al. Association of Antipsychotic Drug Exposure in Pregnancy With Risk of Neurodevelopmental Disorders: A National Birth Cohort Study. JAMA Intern Med. 2022 May 1;182(5):522-533.
79. Gentile S. Antipsychotic therapy during early and late pregnancy. A systematic review. Schizophr Bull. 2010 May;36(3):518-44.
80. Uguz F. Antipsychotic Use During Pregnancy and the Risk of Gestational Diabetes Mellitus: A Systematic Review. J Clin Psychopharmacol. 2019 Mar/Apr;39(2):162-167.
81. Wang Z, Man KKC, Ma T et al. Association between antipsychotic use in pregnancy and the risk of gestational diabetes: Population-based cohort studies from the United Kingdom and Hong Kong and an updated meta-analysis. Schizophr Res. 2021 Mar;229:55-62.
82. Hillemacher T, Simen S, Rehme MK et al. Antipsychotika in der Schwangerschaft: eine systematische Übersichtsarbeit [Antipsychotics during pregnancy: a systematic review]. Nervenarzt. 2021 May;92(5):494-500. German.
83. Wang Z, Brauer R, Man KKC et al. Prenatal exposure to antipsychotic agents and the risk of congenital malformations in children: A systematic review and meta-analysis. Br J Clin Pharmacol. 2021 Nov;87(11):4101-4123.
84. Beex-Oosterhuis MM, Van Gool AR, Heerdink ER et al. Clozapine Treatment During Pregnancy and the Postpartum Period: A Systematic Literature Review. J Clin Psychiatry. 2021 Dec 14;83(1):21r13952.
85. Ennis ZN, Damkier P. Pregnancy exposure to olanzapine, quetiapine, risperidone, aripiprazole and risk of congenital malformations. A systematic review. Basic Clin Pharmacol Toxicol. 2015 Apr;116(4):315-20.
86. Шмуклер А.Б. Психофармакотерапия в период беременности. Доктор.Ру. 2010. №4(55). С. 71-77. / Shmukler A.B. Psixofarmakoterapiya v period beremennosti. Doktor.Ru. 2010. №4(55). S.71-77. [in Russian].
87. Davis C (2007). "Promazine". In Enna SJ, Bylund DB (eds.). X Pharm: The Comprehensive Pharmacology Reference. Elsevier. pp. 1–6.
88. Orsolini L, Sceusa F, Pompili S et al. Severe and persistent mental illness (SPMI) in pregnancy and breastfeeding: focus on second-generation long acting injectable antipsychotics. Expert Opin Drug Saf. 2021 Oct;20(10):1207-1224.
89. Рациональная фармакотерапия в психиатрической практике : Руководство для практикующих врачей. – Москва : Литтерра, 2014. – 1080 с. – (Рациональная фармакотерапия). / Racional`naya farmakoterapiya v psixiatricheskoj praktike : Rukovodstvo dlya praktikuyushhix vrachej. – Moskva : Litterra, 2014. – 1080 s. – (Racional`naya farmakoterapiya). [in Russian].
90. Петрюк П.Т. Шизофрения и беременность: состояние вопроса и пути решения. Психічне здоров’я. 2009. №2. С. 108–118. / Petryuk P.T. Shizofreniya i beremennost`: sostoyanie voprosa i puti resheniya. Psixіchne zdorov’ya. 2009. №2. S. 108–118. [in Russian].
91. Robottom BJ, Reich SG. Exposure to high dosage trihexyphenidyl during pregnancy for treatment of generalized dystonia: case report and literature review. Neurologist. 2011 Nov;17(6):340-1.
92. Mendhekar DN, Andrade C. Uneventful use of haloperidol and trihehexyphenidyl during three consecutive pregnancies. Arch Womens Ment Health. 2011 Feb;14(1):83-4.
93. Kranick SM, Mowry EM, Colcher A et al. Movement disorders and pregnancy: a review of the literature. Mov Disord. 2010 Apr 30;25(6):665-71.
94. Lamichhane D, Narayanan NS, Gonzalez-Alegre P. Two cases of pregnancy in Parkinson's disease. Parkinsonism Relat Disord. 2014 Feb;20(2):239-40.
95. Scott M, Chowdhury M. Pregnancy in Parkinson's disease: unique case report and review of the literature. Mov Disord. 2005 Aug;20(8):1078-9.
96. Robottom BJ, Reich SG. Exposure to high dosage trihexyphenidyl during pregnancy for treatment of generalized dystonia: case report and literature review. Neurologist. 2011 Nov;17(6):340-1.
97. Smith MS, Evatt ML. Movement disorders in pregnancy. Neurol Clin. 2004 Nov;22(4):783-98.


