Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№05 2012
Генетика и эпигенетика шизофрении (лекция) №05 2012
Номера страниц в выпуске:34-44
Шизофрения – тяжелое хроническое инвалидизирующее мозговое заболевание, поражающее около 1% популяции земного шара. Гетерогенность симптоматики, лежащая в основе современного выделения форм и вариантов течения данной патологии, может быть частично обусловлена разнообразием генетической природы заболевания, а также сложными взаимодействиями генетических механизмов и средовых влияний. Ввиду сложной и недостаточно исследованной генетики шизофрении затруднено понимание механизмов, посредством которых генетическая вариабельность переформируется в фенотипы страдания. Настоящий обзор посвящен современным исследованиям в области генетики и эпигенетики шизофрении.
The genetics and epigenetics of schizophrenia (a lecture)
A.V.Trailin, O.A.Levada
Zaporozhye Medical Academy of Postgraduate Education, Ministry of Health of Ukraine
Шизофрения – тяжелое хроническое инвалидизирующее мозговое заболевание, поражающее около 1% популяции земного шара [155]. Гетерогенность симптоматики, лежащая в основе современного выделения форм и вариантов течения данной патологии, может быть частично обусловлена разнообразием генетической природы заболевания, а также сложными взаимодействиями генетических механизмов и средовых влияний. Ввиду сложной и недостаточно исследованной генетики шизофрении затруднено понимание механизмов, посредством которых генетическая вариабельность переформируется в фенотипы страдания. Настоящий обзор посвящен современным исследованиям в области генетики и эпигенетики шизофрении.
Современные генетические методы исследования шизофрении
Для раскрытия роли генетики в этиологии шизофрении принято использовать несколько дизайнов исследования [150].
Исследование сцепления
Исследование сцепления (linkage study) дает ответ на вопрос: «Имеется ли связь между участками или отдельным участком ДНК и определенным фенотипическим признаком?» Анализ сцепления применяется для картирования генетических локусов путем изучения распределения определенного признака внутри семей. Он является наиболее надежным методом для выявления регионов генома, содержащих локусы «больших эффектов» или региональных кластеров редких локусов повышенного риска [28, 60, 144]. Однако разрешение этого метода невелико: выявленный участок хромосомы может содержать несколько миллионов пар оснований, а значит, тысячи генов.
Исследование ассоциаций
Исследования ассоциаций между фенотипами, фенотипами и генетическими полиморфизмами или двумя генетическими полиморфизмами отвечают на вопрос: «Чем обусловлено различное проявление признака среди разных людей в популяции?» Если частота присутствия определенного гена-кандидата или его аллеля в группе лиц с конкретным заболеванием достоверно выше, чем в группе контроля, данный аллель рассматривается как ассоциированный с заболеванием и становится маркером области генома человека, в которой локализуется ген-кандидат. Разработаны следующие дизайны исследований для выявления генетических ассоциаций: случай-контроль, семейный дизайн, ассоциация количественных признаков.
Если изучение сцепления генов позволяет определить и локализовать ген-кандидат, то ассоциативные исследования определяют потенциальную этиологическую роль аллелей этого гена в развитии заболевания.
Исследования генетического сцепления и генетических ассоциаций могут носить общегеномный характер: genome-wide linkage studies (GWLS) и genome-wide association studies (GWAS) соответственно, и позволяют одновременно выявлять сотни тысяч маркеров предрасположенности к заболеванию [144]. Имеющиеся GWAS оптимально обнаруживают варианты, ответственные за повышение относительного риска заболевания в степени выше чем 1,1 [62]. Когда относительный риск составляет 3 и более или имеется много независимых вариантов риска, анализ сцепления становится более мощным, чем анализ ассоциаций [15].
Новые стандарты
В области генетических исследований существует общая тенденция ухода от изучения отдельных генов и белков. Новый стандарт исследований – это анализ коэкспрессированных генных сетей (карты всех активных генов в ЦНС в настоящее время) или генных продуктов (proteoms), анализ метаболических путей, исследования общегеномных эпигенетических моделей, таких как модели связывания факторов транскрипции (transcriptomes), модели метилирования (methylomes), изучение специфических условий среды с их специфическими патогенными и защитными эффектами (enviromics). Принимая во внимание, что экспрессия генов управляется не только спецификой унаследованных аллелей, но и эпигенетическими факторами, не кодирующими РНК, взаимодействием с продуктами генов, также вовлеченных в данный процесс и т.д., правильный подход к изучению молекулярного патогенеза шизофрении и связанных с нею психических расстройств должен включать одновременный анализ всех этих эффектов [16, 97].
Исследование эндофенотипов
Очевидно, что гены могут действовать на нескольких уровнях, начиная от самого генного продукта, через клеточный, системный и поведенческий, вплоть до комплексных фенотипов, таких как терапевтический эффект или нарушения социальных взаимодействий, причем эффект гена не обязательно одинаков на каждом из уровней [102].
Одной из стратегий, которая нашла много последователей в психиатрии, является отход от болезни как сущности к более конкретным биологическим уровням, таким как клеточный, системный, или данным нейрокогнитивных исследований, в надежде, что эффект генов будет более заметным на этих уровнях и легче будет обнаружить новые генетические варианты, повышающие риск заболевания. Эта стратегия получила название концепции эндофенотипов, и ее правомочность особенно убедительно подтверждается, когда в качестве метода количественной оценки структуры и функционирования мозга используется нейровизуализация [102].
Неинвазивная оценка статуса ЦНС
Одной из самых сложных задач в будущем будет решение проблемы тканевой и клеточной специфичности эпигенетических изменений ЦНС. Косвенная (периферийная) оценка с применением мононуклеарных лейкоцитов периферической крови дала обнадеживающие результаты [50]. Однако эти периферийные корреляты позволяют провести лишь грубую оценку изменений в ЦНС [98].
Экспериментальные модели
Современные экспериментальные модели заключаются в «имплантации» животному гипотетического биологического фактора, например вариации количества повторов (CNV), содержании его в различных условиях высокого риска и контроле за развитием структурных и функциональных последствий [91, 98]. Кроме того, возможно применение межвидового генетического картирования, которое сравнивает результаты картирования генов пациентов с функциональными данными, полученными путем картирования рекомбинантных инбредных линий мышей. При этом для выявления генетических вариантов, которые влияют на развитие мозга у людей, используется свойство эволюционного консерватизма, присущего генам, которые участвуют в формировании ЦНС [120].
Структура генетического риска шизофрении
Генетическая склонность к шизофрении, возможно, определяется сотнями и даже тысячами генов [98, 105].
Применение метода генетических ассоциаций позволило собрать базу данных генов шизофрении, объединившую однонуклеотидные генетические полиморфизмы (SNP), ассоциация которых с шизофренией имеет серьезное научное обоснование (табл. 1) [13, 23, 41]. Общегеномные ассоциативные исследования путем изучения до 1% нормальных и патологических геномов идентифицировали лишь малую часть генов, вовлеченных в этиопатогенез шизофрении, но при этом показали, что за повышение риска шизофрении ответственно очень большое количество генов, однако общепопуляционный риск каждой из генетических поломок невелик [77, 126].
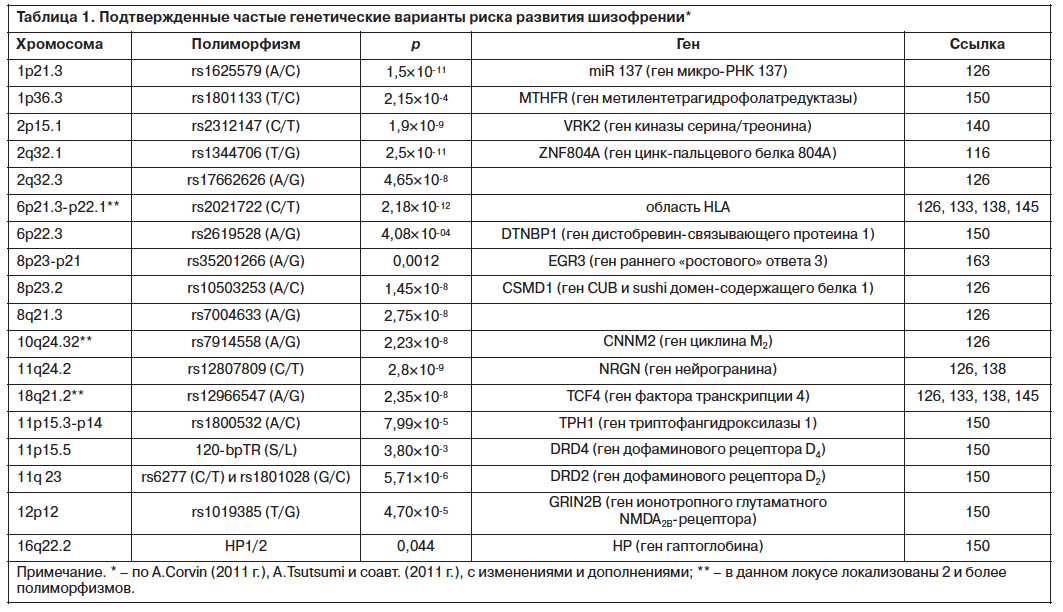
Многие из выявленных аллелей являются рецессивными [86]. Это дает основание думать, что при эволюции человека происходил отбор аллелей, которые увеличивают риск развития шизофрении [77].
Общегеномные исследования сцепления выявили редкие мутации/варианты, которые повышают восприимчивость к семейной шизофрении почти на каждой хромосоме, но лишь некоторые регионы показали воспроизводимость в других исследованиях. Один из таких регионов находится вблизи теломер хромосомы 13q. Эти регионы также были связаны с биполярным расстройством (БПР) [127].
В метаанализе Lewis и соавт. (2003 г.) систематизированы данные 20 исследований по изучению сцепления определенных хромосомных регионов и шизофрении [89]. Показано, что только одна область на длинном плече хромосомы 2 (2q22.1) с высокой степенью достоверности (р<0,000417) фигурировала во всех 20 исследованиях [89, 90]. Других локусов, тесно связанных с заболеванием, выявить не удалось, хотя еще 9 хромосом (5q, 3p, 11q, 6p, 1q, 22q, 8p, 20q, 4р) были идентифицированы как носители номинально значимых регионов с пограничной (р<0,05) достоверностью [42].
Данное исследование практически положило конец поиску одного гена, повышающего риск шизофрении. Кроме того, были определены участки генома, повышающие восприимчивость к шизофрении, и выявлено их совпадение с нестабильными сегментами генома, характеризующимися высокой частотой CNV, неоднократно упоминавшимися в связи с шизофренией [98, 132].
Генетические причины шизофрении
Частота SNP – мутации одной пары оснований в определенном локусе – в популяции составляет более 1%, а у каждого человека их насчитывается более 1 млн. Недавний доклад Международного консорциума по шизофрении показал, что сотни и тысячи частых аллелей, каждая с малым эффектом, в совокупности могут объяснить примерно 30% генетического риска заболевания [145, 146]. В дополнение к SNP в качестве этиологических факторов шизофрении были предложены CNV.
В отличие от SNP CNV встречаются в популяции редко (менее 1%). Они включают дупликации и делеции по меньшей мере 1 тыс. пар оснований, что представляет собой большие (протяженные) генетические повреждения (до 12% генома), которые затрагивают обычно несколько генов (по некоторым данным, от нескольких тысяч до нескольких миллионов пар нуклеотидов) [34, 125]. Вследствие этого индивидуальные геномы могут отличаться по количеству копий сегментов ДНК и определенных генов, т.е. меняется «доза гена». В случае дупликации может появиться лишняя копия гена, а при делеции, наоборот, одной копией гена может стать меньше, и, следовательно, понижается или повышается экспрессия продукта гена – белка или не кодирующей РНК [2]. Дупликации и делеции фрагментов ДНК также могут встраиваться в нуклеотидную последовательность гена или выпадать из нее, вызывая разрыв, что нарушает нормальную экспрессию гена. Ввиду большого масштаба поломок вклад CNV в вариативность генома сопоставим с вкладом однонуклеотидных полиморфизмов или даже превышает его [2].
CNV ответственны за 2–4% генетической предрасположенности к шизофрении. Использование более тонких технологий может увеличить этот показатель до 10–20% [136]. При шизофрении повышена частота CNV, которые затрагивают гены, участвующие в развитии ЦНС, особенно нейрегулин- и глутаматергических путей [157].
Индивидуальные CNV достоверно повышают риск шизофрении по сравнению с менее масштабными генетическими вариациями (табл. 2), но поскольку CNV наблюдаются и у здоровых лиц, а также увеличивают риск других психических расстройств (например, аутизма), они не могут в полной мере объяснить генетический риск шизофрении [30]. С другой стороны, работы по изучению роли CNV при шизофрении отличает хорошая воспроизводимость результатов [127].
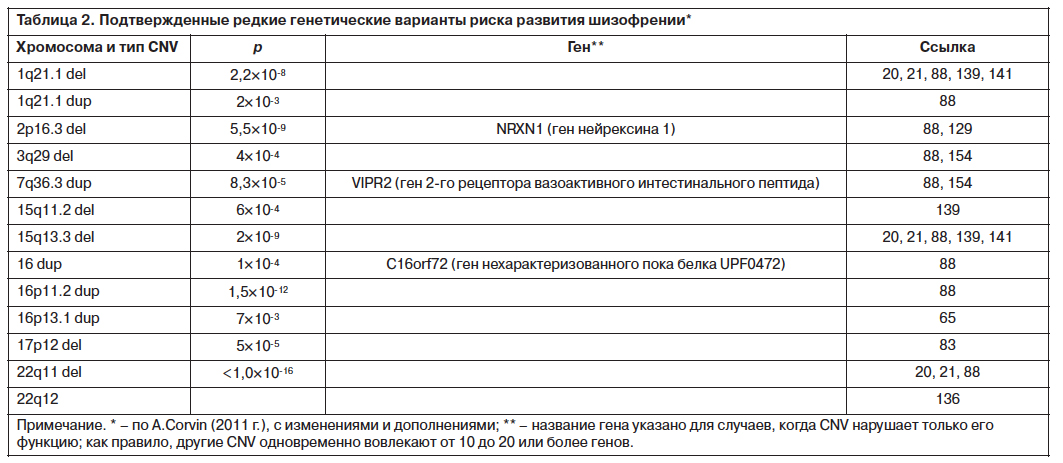
Большинство CNV не унаследованы, а являются результатом спонтанных мутаций ДНК в момент зачатия или развития, которые могут быть ответственны за спорадические случаи шизофрении [161]. Так, у пациентов с шизофренией без семейного анамнеза заболевания обнаружено в
8 раз больше редких спонтанных мутаций, чем в контрольной группе. Данные мутации в основном затрагивали пути формирования мозга. Эта находка может также объяснить, почему шизофрения персистирует в популяции, а не подчиняется естественному отбору. Так, у 27 из 53 пациентов со спорадическими случаями шизофрении выявлено 40 мутаций de novo, затрагивающих 40 генов [160].
Имеется несколько групп доказательств, подтверждающих роль мутаций de novo в качестве механизма возникновения шизофрении. Во-первых, мутации de novo генерируются с высокой частотой в популяции. Очень высокая конкордантность монозиготных близнецов и очень низкая – дизиготных также поддерживает гипотезу о том, что значительная часть случаев шизофрении может возникнуть в результате новых мутаций [73]. Кроме того, несмотря на снижение репродуктивной функции и чрезвычайно разнообразные факторы риска окружающей среды, распространение шизофрении сохраняется во всем мире на относительно высоком и стабильном уровне – около 1%. Рост риска данного заболевания с повышением возраста отца также может быть объяснен увеличением у него количества мутаций de novo [96].
Сообщается, что у больных шизофренией инсерции чаще встречаются на хромосоме Xq23 (52%), а делеции – в основном на хромосоме 3q13.12 (32%) [107]. В последнее время в ряде крупных статей сообщали об ассоциации целого ряда CNV с шизофренией (см. табл. 2). Носителями делеций в регионах 22q11.2, 1q21.1 и 15q13.3 могут быть до 2% лиц с данной патологией [20, 21].
Среди генов, функция которых нарушается путем CNV, – ген нейрексина 1 (NRXN1), последовательность нуклеотидов которого разрывается делецией в участке 2p16, и ген белка А2, связывающего предшественник амилоида (APBA2), в котором происходит дупликация [84]. Оба гена необходимы для образования и функционирования синапсов.
Помимо модификации гена, пол родителя, у которого произошла CNV, также имеет значение, особенно если затронут проксимальный сегмент длинного плеча хромосомы 15 [19]. Распространенность психотических нарушений значительно выше у пациентов, унаследовавших 2 копии материнской хромосомы 15, чем в случае делеции региона 15q11-q13 отцовской хромосомы [59]. У части пациентов с шизофренией также выявлены дупликации в регионе хромосомы 15q11-q13 материнского происхождения [65]. Этот локус содержит регион управления импринтингом, с различным способом метилирования материнских и отцовских аллелей, что влияет на экспрессию нескольких генов, необходимых для развития нервной системы [59].
Эти исследования достоверно показывают, что некоторые носители de novo и унаследованных CNV, особенно при условии, что они нарушают функции генов, подвергаются высокому риску развития шизофрении. В большинстве случаев у носителей этих генетических вариантов развивается типичная шизофрения, однако может возникнуть и синдром шизофрении в виде неспособности к обучению [136].
Для обнаружения редких CNV необходимы выборки больших объемов, которые удалось сформировать, объединив усилия многих научных коллективов в консорциуме по шизофрении. При полногеномном исследовании редких вариантов CNV у 3391 пациента с шизофренией и 3181 человека из контрольной группы у 1% всех обследованных обнаружены участки CNV длиной более 100 тыс. пар оснований. При этом у больных они встречались чаще, чем в контроле [2, 141].
Эпигенетические механизмы: взаимодействия среды и генома
Эпигенетику можно определить как процесс взаимодействия генотипа организма со средой при формировании фенотипа. Она изучает механизмы, при помощи которых на основе генетической информации, заключенной в одной клетке (зиготе), за счет различной экспрессии генов в разных типах клеток может осуществляться развитие многоклеточного организма, состоящего из дифференцированных клеток [1, 12]. Благодаря эпигенетическим механизмам патогены среды способны достичь ядер клеток и изменить геном, потенцируя существующие или создавая новые генетические риски развития заболевания. Эпигенетические нарушения были предложены в качестве патогенетического механизма шизофрении [117].
Геномная восприимчивость к воздействиям окружающей среды продолжается в течение всей жизни: от гаметогенеза до стадии зрелых, дифференцированных соматических клеток [98]. Основными механизмами эпигенетического контроля считаются:
Метилирование ДНК заключается в присоединении метильной группы к цитозину в составе CpG-динуклеотида в позиции С5 цитозинового кольца. У человека метилировано около 1% геномной ДНК. В то время как упорядоченное метилирование ДНК необходимо для определения уникальных свойств клетки, аберрантное метилирование ДНК может коррелировать с шизофренией и другими заболеваниями [5].
Анализ посмертных образцов мозга пациентов с шизофренией предоставил доказательства гиперметилирования промотора генов реелина (RELN), факторов транскрипции SOX10 и FOXP2, серотонинового рецептора 2А (HTR2A), в результате чего снижалась экспрессия этих генов [4, 6, 68, 148]. Гипометилирование промотора гена мембраносвязанной катехол-О-метилтрансферазы (MB-COMT), напротив, ведет к его гиперэкспрессии [3].
Недавние исследования показали повышение базального уровня диметилированного лизина в 9-м положении
3-го гистона (H3K9 мет2), маркера репрессивного хроматина в лимфоцитах пациентов с шизофренией по сравнению с нормальным контролем. Более высокий уровень H3K9 мет2 также ассоциируется с более ранним дебютом заболевания [5]. Повышенный уровень H3-(метил)-аргинина 17 ассоциируется со снижением экспрессии некоторых метаболических генов, таких как CRYM, кодирующий синтез регулируемого НАДФ белка, связывающего тиреоидные гормоны, генов цитохрома С1 (CYTOC/CYC1), малатдегидрогеназы и орнитинаминотрансферазы в префронтальной коре у пациентов с шизофренией [5, 11].
В то время как с возрастом у здоровых усиливается метилирование H3K4 в промоторе гена глутаматдекарбоксилазы (GAD1), ГАМКергического гена, как правило, у пациентов с шизофренией в префронтальной коре отмечается его гипометилирование. Последующие исследования на мышах показали, что клозапин, но не галоперидол, может увеличить метилирование H3K4 [5, 63].
На этом фоне недавние сообщения об обнаружении в ДНК, полученной из слюны лиц с шизофренией, гипометилирования первого экзона гена HTR2A и промотора гена MB-COMT показывают, что эпигенетические изменения могут служить периферическими диагностическими биомаркерами шизофрении и потенциальными мишенями для терапии [5, 51, 114].
Посттрансляционное динамическое ремоделирование хроматина путем ковалентной модификации хвостов гистонов в нуклеосомах, вокруг которых обернута молекула ДНК, также считается эпигенетическим механизмом регуляции экспрессии генов. Хвосты гистонов являются предметом динамической ковалентной модификации в виде ацетилирования, метилирования и фосфорилирования, которые определяют, будет ли ДНК доступной для регуляторных и транскрипционных факторов.
Например, ацетилирование лизина в хвосте гистона, 9-м положении гистона H3 (H3K9 ац), создает отрицательно заряженные амидные группы, которые отталкивают отрицательно заряженные фосфатные группы ДНК, что разрыхляет структуру хроматина и облегчает транскрипцию генов за счет увеличения доступности молекул ДНК для транскрипционных факторов и РНК-полимераз, тогда как ацетилирование гистона и метилирование лизина в 9-м положении гистона H3 (H3K9 мет), напротив, являются доминирующими чертами конденсированного хроматина, где экспрессия генов подавлена [98]. В этом контексте ингибиторы гистондеацетилазы, такие как вальпроат натрия, который индуцирует экспрессию молчащих генов, уже давно рассматриваются как важные препараты в психиатрической практике [5, 7].
Накапливаются доказательства того, что связь между средовыми воздействиями, с одной стороны, активностью и экспрессией генов, с другой, реализуется через динамические конформации хроматина [36, 98, 142, 143]. Это справедливо не только для патогенов химической или биологической природы, но и для негативных психосоциальных воздействий [113, 143, 158].
Одним из первых доказательств аберрантной регуляции модификации гистонов при шизофрении было изменение ультраструктуры хроматина нейтрофилов, что может служить периферическим суррогатным маркером, который отражает эпигенетические нарушения в мозге, и может быть использовано для эффективной ранней диагностики и терапии шизофрении [5, 67]. Пимозид (типичный антипсихотик) может ослаблять увеличение количества богатых аргинином гистонов у лиц с шизофренией [5, 137].
В целом эти исследования наглядно демонстрируют, что выбор эпигенетических изменений в качестве мишени может стать основной стратегией разработки терапии шизофрении.
В последнее время большое внимание привлечено к
изучению роли в процессах регуляции генетической активности малых интерферирующих РНК и микро-РНК [100]. Интерферирующие РНК могут изменять стабильность и трансляцию мРНК путем моделирования функций полисом и структуры хроматина [1].
Микро-РНК – это малые некодирующие РНК длиной 21–25 оснований, которые либо ингибируют трансляцию мРНК, либо участвуют в деградации целевых мРНК. Посмертный анализ 260 микро-РНК из лобных долей пациентов с шизофренией и шизоаффективным расстройством выявил повышение экспрессии miR-106b и снижение экспрессии 16 других микро-РНК, среди которых miR-24, miR-26b, miR-30e and miR-92 [5].
При шизофрении обнаружено увеличение биогенеза микро-РНК в дорсолатеральной префронтальной коре и верхней височной извилине, причиной чего является увеличение количества РНК-связывающего белка Dgcr8, необходимого для созревания первичных микро-РНК [5, 24].
Показано, что при шизофрении увеличивается содержание в постсмертном мозге miR-181b, miR-15a, miR-15b, miR-195, и miR-107, среди генов-мишеней которых гены рецепторов глутумата: GRM5, GRM7, GRIK2, GRIN1 и GRID, серотонина (HTR1B, HTR2C и HTR4), ГАМК (GABR1, GABRA1), дофамина (DRD1), М-холинорецептора 1, и другие гены-кандидаты, вовлеченные в патогенез заболевания: мозгового нейтротрофического фактора (BDNF), нейрегулина 1 (NRG1), RELN, атаксина 2 [5, 24].
В целом, несмотря на противоречивые данные ряда исследований, одни из которых показали снижение, а дру-гие – повышение содержания микро-РНК при развитии шизофрении, последнее исследование 453 микро-РНК в постсмертном мозге установило, что содержание 19% исследуемых микро-РНК снижено при шизофрении, тогда как изменений в сторону увеличения экспрессии не было вовсе [5, 108].
Эпигенетические нарушения могут быть одной из причин половых различий в восприимчивости к шизофрении. Так, общегеномный анализ в постсмертном мозге пациентов, умерших от шизофрении или БПР, обнаружил более 12 тыс. CpG-островков наряду с большим количеством специфичных для пола метилированных генов [5, 105]. Среди последних – гиперметилирование ДНК гена WDR18 у мужчин, больных шизофренией, и ненормальное метилирование ДНК ГАМК- и глутаматергических генов при шизофрении и БПР. В других исследованиях было продемонстрировано ослабление экспрессии, чувствительной к эстрогену miR-30b, в мозге женщин с шизофренией [5, 101].
Несмотря на возрастающее количество доказательств роли эпигенетических аберраций в патогенезе шизофрении, существует точка зрения, что лишь некоторые из них могут быть этиологическими факторами заболевания, в то время как большинство из эпигенетических модификаций вторичны и обусловлены болезнью, эффектами препаратов или ненормальным образом жизни пациентов. Следовательно, для того чтобы выявить ген-кандидат (а не вторично измененный ген), необходим поиск факторов, вызывающих эпигенетические нарушения и раскрытие механизмов их действия.
Нарушение эпигенетической регуляции при шизофрении
Причиной нарушения эпигенетической регуляции при шизофрении являются средовые эффекты и/или эпимутации, т.е. ошибки в запрограммированном метилировании ДНК. Эпимутации происходят в течение гамето- и эмбриогенеза, когда появляются эпигенетические маркеры, чтобы запрограммировать время- и тканеспецифические события в процессе развития [75, 98]. Точность передачи модели метилирования ДНК ниже, чем таковая последовательности ДНК [98, 153]. Поэтому эпимутации de novo возникают на один или два порядка чаще, чем мутации ДНК в соматических клетках [61]. Это подразумевает их значительный вклад в заболевания человека [43]. Они могут возникать как случайно, так и специфическим образом в ответ на определенные изменения среды.
Каким бы ни было их происхождение, эпигенетические маркеры передаются путем митоза дочерним соматическим клеткам во время морфогенеза и роста [36, 98]. Это обеспечивает механизм, с помощью которого эпигенетические последствия ранних экологических патогенных воздействий продолжают действовать на протяжении всего развития, особенно в постмитотических клетках (нейронах и др.). Они могут выступать в качестве молекулярных предшественников развивающихся при шизофрении структурных и функциональных нарушений [1, 44]. Эпигенетические метки в некоторых случаях сохраняются в процессе гаметогенеза и могут быть перенесены от предков к потомкам [1, 39, 71].
Возможные мишени нарушений эпигенетической регуляции
Унаследованные полиморфные гены. По аналогии с гипотезой «двойного удара» в канцерогенезе генетический дефект (рецессивная мутация) не приведет к болезни, если только не будет сочетаться с другим генетическим (соматическая мутация) или средовым фактором [эпигенетическое подавление второй (нормальной) аллели], что приводит к проявлению мутации.
К примеру, имеется SNP, повышающий активность пролиндегидрогеназы и увеличивающий риск шизофрении. Он может сочетаться с двумя другими SNP, снижающими активность пролиндегидрогеназы и, соответственно, риск шизофрении [78]. В этом случае наличие мутации или эпигенетического воздействия повысит риск шизофрении, если они снизят активность протективного аллеля [98].
Нормальные гены. Нарушение эпигенетической регуляции нормальных генов, вовлеченных в развитие ЦНС (например, DISC1, NRG1, рецептора подсемейства эпидермального фактора роста ErbB4, COMT, BDNF, DTNP1 и др.), может привести к ряду генетических аномалий, таких как аберрантная моноаллельная экспрессия, неадекватная доза гена и рассинхронизация геномной активности [98].
Гены-протекторы. Так можно обозначить гены, обладающие положительными эффектами на когнитивные способности, мотивации, эмоции и развитие ЦНС. Например, Met/Met-вариант гена COMT ассоциируется со снижением риска шизофрении, имеет благоприятное влияние на оперативную память и предотвращает развитие психоза у наркоманов, употребляющих каннабис [35, 45]. Если гомозиготность Met/Met будет нарушена эпигенетически, это, вероятно, увеличит и риск шизофрении, и тяжесть ее симптомов [98].
Патологическая активация генов. «Патологичность» генома шизофрении характеризуется не только гипер-, но и гипометилированием нуклеотидов [105]. Хотя модифицирование активности генов нервной ткани путем гипометилирования не настолько эффективно, как в случае гиперметилирования, оно может проявляться некоторой активацией генов [105]. Например, при шизофрении не происходит возраст-зависимого подавления экспрессии генов, участвующих в развитии ЦНС, но имеет место продолжающаяся их экспрессия, по-видимому, вследствие гипометилирования промоторов [98, 149].
Условно патологические гены. Термин относится к нормальным генам глии и других соматических клеток, регулирующих межклеточные взаимодействия и иммунный ответ (например, гены, кодирующие цитокины).
Индуцированная инфекцией активация этих генов во время критических периодов внутриутробного развития нарушает нормальное формирование ЦНС [146].
Метастабильные эпиаллели. Пока идентифицированы лишь несколько генов с метастабильными эпиаллелями [70]. Они представляют собой локусы, которые могут претерпевать разнообразные эпигенетические модификации обратимого характера. В результате генетически идентичные организмы могут иметь широкий ряд фенотипов (здоровых и больных лиц). Метастабильные эпиаллели особенно чувствительны к средовым факторам в период внутриутробного развития [98].
Средовые факторы риска при шизофрении
Нарушения эпигенетической регуляции и пренатальные факторы риска «первого удара»
Экологические факторы являются неотъемлемой частью патогенеза шизофрении [32, 98, 156]. В ряде исследований установлена взаимосвязь данного заболевания с рождением зимой или ранней весной, рождением в городе, возрастом отца, голодом, нарушениями питания и перинатальными осложнениями [5].
В зависимости от срока беременности, с которым совпадает воздействие средового фактора, повреждаются различные нейробиологические мишени, вовлекаются разные патогенетические механизмы и возможны различные фенотипические проявления. Пренатальные факторы в основном влияют на геном и/или развивающиеся ткани головного мозга. Их можно обозначить как факторы риска «первого удара» [98].
В основном это факторы биологической природы (вирусы, бактерии, токсины), влияющие на беременную с генетической предрасположенностью к психозу, особенно в 1 и 2-м триместрах [32]. Поскольку большинство вирусов не проникает через плаценту, предполагается непрямое влияние на плод, вероятно, связанное с противовирусным ответом иммунной системы матери, например путем секреции провоспалительных цитокинов [47]. Действительно, высокий уровень интерлейкина-8 в крови женщины во время беременности увеличивает риск шизофрении у ребенка и приводит к структурным изменениям в структурах ЦНС, вовлеченных в патогенез шизофрении [33, 47].
В настоящее время раскрыты три различных механизма реализации эффекта пренатальной инфекции [98].
Эпигенетическое подавление генов плаценты/ плода. В эксперименте на мышах Y.Bobetsis и соавт.
(2010 г.) выявили 74 гена, регуляция которых была эпигенетически нарушена вследствие бактериальной инфекции во время беременности [27]. Большинство генов, участвующих в развитии плода, были подавлены. Среди них внимание обращали 3 гена, вовлеченных в развитие ЦНС, – синаптотагмин X (SYT10), нейропептид галанин (GAL) и его рецептор (GALR3). SYT10 регулирует секрецию нейротрансмиттеров и, соответственно, сигнализацию между нейронами, в то время как мутации гена галанина лежат в основе распространенных нарушений в ЦНС, включающих, например, меньшее количество сенсорных нейронов и снижение способности к регенерации нервов.
Патологическая активация микроглии. Исследования in vitro продемонстрировали активацию микроглии провоспалительными цитокинами. Фетальный мозг богат микроглией, и в случае активации она способна вырабатывать хемокины и цитокины, которые могут быть токсичными для ЦНС. При бактериальной инфекции липополисахарид эндотоксина проникает через плаценту и индуцирует выработку цитокинов в головном мозге плода [72].
Нарушение функции фетоплацентарного комплекса. Провоспалительные цитокины играют важную роль в сохранении фетоплацентарного комплекса, и повышение их уровня может привести к повреждению плода. У людей интерлейкин-6 способствует развитию у матери реакции «хозяин против графта», вплоть до развития спонтанного аборта. В более легких случаях целостность фетоплацентарного барьера нарушается лишь частично, что достаточно для повышения риска шизофрении либо через нейротоксическое повреждение (вероятно, с участием механизмов гипоксии или мальнутриции), либо эпигенетическое нарушение регуляции генома [98].
Среди неинфекционных факторов риска первого удара выделяют ассоциированные с повышенным риском шизофрении социальные факторы, реализующиеся через тяжелый материнский стресс в 1-м триместре беременности, депрессию, гипоксию плода вследствие акушерских осложнений, дефицит питательных веществ, особенно необходимых для формирования S-аденозилметионина, например фолиевой кислоты, холина, витамина В12 [82, 95, 98, 112, 130].
Нарушение эпигенетической регуляции уже предрасположенного к развитию заболевания генома, вероятно, является основным механизмом эффектов пренатальных или ранних послеродовых воздействий окружающей среды. Эпигеном особенно чувствителен к нарушению в пренатальный период, во время быстрой репликации клеток и точной установки эпигенетических маркеров для управления развитием [44, 98].
Предполагается и другой механизм патогенетических эффектов пренатальных средовых факторов. Они часто вызывают прямое повреждение мозга (например, этанол, отравление свинцом и т.д.). Последовавшее за этим аберрантное развитие ЦНС формирует ранние аберрантные нейронные структуры и функции («продромальная ЦНС») с повышенной чувствительностью к воздействиям окружающей среды. Этот продромальный мозг становится независимым фактором риска шизофрении, субстратом для взаимодействия с окружающей средой, которое в отдельных случаях может привести к фенотипу шизофрении [98].
Факторы риска постнатального «второго удара»
После рождения изначально генетически предрасположенная к развитию заболевания ЦНС, скомпрометированная пренатальными нарушениями, может подвергаться различным средовым воздействиям, достоверно увеличивающим риск шизофрении [98, 130, 156]. Период, в котором реализуются эффекты средовых факторов риска «второго удара», простирается от раннего послеродового периода через детство до поздней юности или даже позже. Доказанные факторы риска «второго удара» включают в себя воздействия социальной среды (проживание в городах, а не в сельской местности, международная миграция), психологических патогенов (стресс), химических веществ (употребление каннабиса) и др. [98, 130].
Точные механизмы реализации эффектов постнатальных средовых факторов в значительной степени неизвестны, но, по-видимому, неоднородны. Известно, например, что динамическое регулирование метилирования ДНК продолжается и в дифференцированных нейронах коры под влиянием различных социальных факторов, алкоголя и метамфетаминов [98, 115, 122, 124, 134].
В дополнение к нарушению эпигенетической регуляции генома (как описано выше) факторы окружающей среды могут нарушить развитие ЦНС посредством потенцирования биологических путей, вовлеченных в патогенез шизофрении [98]. Например, употребление каннабиса подростками увеличивает риск данного заболевания во время чувствительных периодов кортикогенеза. В частности, носители аллеля COMT Val (этот вариант связан с быстрым метаболизмом дофамина, низким содержанием дофамина в коре и высоким – в среднем мозге) были более склонны к развитию психоза, если они употребляли каннабис, по сравнению с носителями аллеля COMT Met или взрослыми наркоманами – носителями полиморфизма COMT Val [35]. Провоцирующий эффект каннабиса объясняется тем, что конопля вызывает значительное снижение коркового содержания дофамина и увеличение его содержания в среднем мозге [98]. Данный пример демонстрирует, как уже существующая наследственная дисфункция дофаминергической системы мозга, усиленная средовыми воздействиями, приводит к повышению риска психоза. Он также свидетельствует в пользу смешанной модели генетического риска шизофрении: эпигенетические воздействия потенцируют предсуществующую полигенно обусловленную уязвимость [98].
Острый психосоциальный стресс повышает риск шизофрении через взаимодействие «геном–среда», возможно, с участием цитокинов [98, 130, 162]. Кроме того, стресс также приводит к увеличению содержания дофамина в стриатуме – хорошо известный фактор развития позитивной симптоматики шизофрении, особенно в контексте имеющейся предрасположенности [93, 98, 121].
Миграция и ассоциированный с нею низкий социально-экономический статус могут создать так называемый стресс «социального фиаско» или «нестабильной социальной иерархии», в развитии которых участвуют ядра ЦНС и кортикальные пути, вовлеченные в патогенез шизофрении [98, 164].
Хотя кортикогенезом в первую очередь управляет генетическая информация, эффективность ее реализации зависит также от интенсивности и способа использования [74, 98]. Генетический и «пользовательский» механизмы сосуществуют в определенной пропорции вплоть до конечной стадии развития мозга [98]. Другими словами, в некоторых случаях экологические патогены увеличивают риск за счет активации биологических путей, вовлеченных в патогенез шизофрении.
Комплексное нелинейное развитие шизофрении
Комплексная структура генетической предрасположенности к шизофрении является необходимым условием для последующего развертывания нейропатологических процессов, а также субстратом для эпигенетической модуляции патогенами среды [98]. В некоторых случаях для фенотипических проявлений достаточно только генетических факторов (например, CNV или точечные мутации).
В других случаях эпигенетические факторы накладываются на фон, представляющий собой несколько генетических отклонений, каждое с малой величиной эффекта. Так как в каждом отдельном случае сочетание генетических и экологических факторов варьирует, клинические проявления и эволюция заболевания также вариабельны.
Влияние экологических факторов может меняться в зависимости от ряда обстоятельств, таких как: тип экологического патогена; интенсивность его влияния; острое или хроническое воздействие; этап развития ЦНС; чувствительность эпигенетических процессов, активных во время экспозиции; сосуществование защитных факторов, таких как корректирующие эффекты среды и защитные генетические варианты [98].
Смешанная модель генетического риска в структуре шизофрении
Эмпирические данные поддерживают существование при шизофрении аллелей риска обоих типов: частых (SNP) и редких (CNV), но предполагают, что ни один из них не играет специфической роли в патогенезе болезни [118].
Несмотря на доказательства высокой наследуемости, большинство случаев шизофрении производит впечатление спорадических, поскольку родители около 90% больных шизофренией сами не страдают этим заболеванием, а у 60% лиц с данной патологией отсутствуют больные родственники 1 и 2-й степени родства [98].
Их причиной могут быть CNV de novo. Действительно, в некоторых случаях редкие и масштабные генетические повреждения, такие как CNV, достаточны, чтобы вызвать шизофрению [147]. Эти редкие мутации, как правило, имеют высокую, но неполную пенетрантность, тем самым объясняя впечатление спорадичности возникновения заболевания [106]. Как показали Xu и соавт. (2011 г.), примерно в половине изученных случаев шизофрении идентифицированные CNV были не унаследованы, а возникли de novo в первом поколении [160].
Этим же, возможно, объясняется более высокий риск развития шизофрении у детей пациентов, чем у их братьев и сестер [136]. При генетическом консультировании в случае, если установлено, что в основе заболевания пробанда лежит CNV de novo, риск развития заболевания у сиблингов будет значительно ниже.
Определение точного характера CNV и тех генетических/эпигенетических и средовых факторов, которые влияют на их пенетрантность и экспрессивность, в совокупности приводя к повышению риска широкого диапазона нарушений развития, будет захватывающим вызовом для психоневрологических исследований в ближайшем будущем [136].
Редкие CNV могут нарушать структуру различных хромосомных регионов, но обычно за развитие шизофрении отвечает какой-то один из них [106]. В соответствии со «смешанной моделью» в случае CNV средовые воздействия не обязательны, но могут утяжелять фенотипические проявления [106]. С другой стороны, редкого CNV не всегда достаточно, чтобы вызвать шизофрению, в таком случае необходимо наличие «генетического фона», состоящего из других нормальных и/или полиморфных генов, эпистатически усиливающих эффект CNV.
Экологические факторы способны синергически увеличить риск шизофрении, но только при наличии генетической предрасположенности, а не как независимые факторы риска [95, 98]. При этом низкая пенетрантность полигенной склонности к заболеванию, субстратом которой являются вариабельные редкие и/или частые структурные повреждения генома, синергетически потенцируется через взаимодействие «геном–среда».
Такой синергизм может быть опосредован эпигенетической модуляцией унаследованной генетической предрасположенности (т.е. увеличением ее пенетрантности); путем повышения восприимчивости к шизофрении с помощью специальных эффектов (например, активное использование уязвимого биологического пути); через неспецифические эффекты (например, прямая травма мозга); всеми механизмами в некоторой пропорции [98].
Этот сценарий объясняет аномальный, значительный эффект эпигенетических воздействий, которые накладываются на многофакторный фон, в котором каждый фактор в малой степени повышает предрасположенность к заболеванию. Также в эту модель вписываются описанные выше случаи, когда одна структурная аномалия с большим эффектом накладывается на многофакторный фон [98].
Таким образом, создается впечатление, что шизофрения у разных людей может быть обусловлена как большим количеством частых генетических вариаций с малыми эффектами, так и редкими генетическими вариантами с большими эффектами [98]. Каждый клинический случай шизофрении может быть специфическим с генетической точки зрения и представлять интерактивное сочетание широкого, но в конечном счете ограниченного спектра патологических генетических вариантов [98].
В самом деле, симуляционные исследования на основе компьютерного моделирования показывают, что в основе наследования шизофрении могут лежать тысячи аллелей [145]. Это означает, что взаимодействие между генами, эпистаз, может играть важную роль в патогенезе, а также способствовать взаимодействию генома со средой [102]. В результате один и тот же генотип может реализоваться в нескольких различных фенотипах, и наоборот, различные генотипы могут иметь сходные фенотипические проявления.
Шизофрения как патология формирования ЦНС
Все больше авторов осмысливают шизофрению как расстройство развития ЦНС в отличие от статического поражения головного мозга или несостоятельности созревания мозга на окончательной стадии его развития [66, 80, 98].
Эта гипотеза получила новый импульс в результате недавно сделанных открытий в области эпидемиологии, развития и нейровизуализации. Так, нейровизуализационные исследования выявили структурные аномалии головного мозга уже на момент начала заболевания. Во-вторых, часто у пациентов, которым с возрастом был выставлен диагноз шизофрении, еще в молодом возрасте встречались когнитивные и моторные нарушения. Наконец, экспериментальное повреждение мозга у приматов в неонатальный период имеет отсроченные эффекты на их поведение [118].
Несколько генов, вовлеченных в формирование ЦНС, локализованы в хромосомных локусах, в которых также идентифицированы гены-кандидаты повышенного риска шизофрении, которые характеризуются полиморфным статусом и меняют свою экспрессию в эмбриогенезе [91]. Например, у детей с ранним началом заболевания, гипофункцией фронтальной коры и сниженным объемом серого вещества коры при МРТ, выявлены 3 SNP в гене GAD1, который кодирует белок GAD67 [8].
Более важно то, что большинство ассоциированных с риском шизофрении специфических генов, включая DISC1, NRG1, DTNP1, ген NCAM – молекулы адгезии нервных клеток, а также RELN, BDNF, NR1-субъединицы NMDA-рецепторов, играют важную роль в формировании мозга, нейротрансмиссии и синаптической пластичности [91].
При шизофрении хорошо известны анатомические нарушения, такие как расширение желудочков, сокращение объема префронтальной коры и гиппокампа, уменьшение мозга в целом [53, 91]. При этом заболевании выявляют существенные изменения размеров и морфологии нейронов, а также синаптических связей [56, 91].
Исследования корковой и лимбической области мозга показывают, что структурная и молекулярная целостности синаптических комплексов, глутаматергических рецепторов и путей трансдукции сигнала играют критически важную роль в мозге в процессе его формирования, синаптогенеза и синаптической пластичности [17, 91].
Требуется время, для того чтобы первоначальная предрасположенность к шизофрении материализовалась в аберрантные структуры, связи и функции ЦНС. Иными словами, развивающаяся ЦНС, так сказать, «не готова» для шизофрении, потому что ее полная функциональность еще не установлена. В момент полового созревания функции мозга становятся более уязвимыми для имеющихся биодефектов.
Фактически имеются четыре подтвержденные стадии шизофрении: повышенного риска, продромального периода, психоза и хронической инвалидности [66, 98].
Недавно было показано, что прогрессирование от продрома к манифестной шизофрении у пациентов ультравысокого риска может быть значительно замедлено с помощью нейропротекторных соединений, таких как w-3 полиненасыщенные жирные кислоты [14]. Эти данные в очередной раз указывают на нелинейность патогенеза шизофрении, и что продром является скорее независимым фактором риска шизофрении, а не обязательной стадией ее развития. В рамках этой концепции манифестация психоза может рассматриваться не как начало, а как поздняя стадия заболевания [66].
В подтверждение концепции шизофрении как патологии развития ЦНС можно привести факт выявленного генетического сходства между шизофренией и синдромами, при которых психопатология проявляется в детском возрасте и которые часто группируются как расстройства формирования ЦНС [118, 131]. Так, конкретные вариации количества копий, которые в значительной степени связаны с шизофренией, также ассоциированы с такими расстройствами, как аутизм, умственная отсталость, синдром дефицита внимания и гиперактивности (СДВГ), генерализованная эпилепсия [118, 159].
Важно, что все эти расстройства ассоциированы с нарушениями познания, чаще встречаются у мужчин и в основном ассоциируются с задержкой развития различной степени, мягкими неврологическими симптомами и двигательными нарушениями. Кроме того, между этими синдромами есть достоверная коморбидность, что также указывает на их возможную принадлежность к одной группе [118].
Это дает возможность ряду исследователей предполагать, что данные нарушения представляют собой континуум генетических и экологически индуцированных нарушений в развитии ЦНС, а не набор дискретных этиологических единиц. При этом главный клинический синдром частично отражает тяжесть и преобладающий тип аномального развития мозга и, как следствие, функциональных нарушений, а также модифицирующие эффекты других генетических и экологических факторов. Таким образом, аутизм может быть диагностирован, когда нарушения мозговых проводящих путей приводят к явным расстройствам коммуникации в социуме, СДВГ – когда преобладают нарушения тормозного контроля и умственная отсталость – когда доминируют когнитивные нарушения [118].
Если классифицировать тяжелые психические заболевания по убыванию тяжести нарушений развития ЦНС, то они расположатся следующим образом: интеллектуальная инвалидность, аутизм, СДВГ, шизофрения, БПР [118].
Гипотеза «разобщения»
Согласно гипотезе «разобщения», впервые предложенной Friston и соавт. в 1990-х годах, первопричиной шизофрении является патологическая синаптическая пластичность вследствие дисрегуляции NMDA-рецепторов дофамином.
В поддержку роли NMDA-рецепторов при шизофрении свидетельствуют результаты нескольких исследований. Во-первых, препараты, блокирующие NMDA-рецепторы, такие как кетамин и фенциклидин, могут вызывать психотические симптомы у здоровых людей [69]. Кроме того, введение кетамина вызывает дефицит обработки сенсорной информации в контрольной группе, аналогичный таковому при шизофрении, что свидетельствует о роли
NMDA-рецепторов для этих дефицитов [152]. Активность дофаминергических нейронов среднего мозга частично регулируется глутаматергическими проекциями из префронтальной коры, которые действуют через NMDA-рецепторы, и их блокада повышает амфетамин-индуцированное увеличение содержания дофамина в стриатуме в контрольной группе, похожее на увеличение у пациентов с шизофренией [76]. Наконец, генетические варианты, которые играют роль в NMDA-сигнализации, были связаны с повышением риска шизофрении при исследованиях генов-кандидатов (например, DAOA – ген активатора оксидазы D-аминокислот, GRM3 и белок, регулирующий сигнальную активность G-белков) [57, 110].
Использование визуализационной генетики для исследования нервных связей. В двух метаанализах, посвященных изучению степени влияния генетического полиморфизма на функцию мозга, показана большая величина эффекта полиморфизмов 5HTTLPR (гена белка-транспортера обратного захвата серотонина) и COMT Val158Met на активацию нейронов миндалины и префронтальной коры [104, 110, 111].
Роль COMT заключается в деградации катехоламинов, в том числе и дофамина [22, 54, 102]. Ген COMT состоит из двух промоторов и шести экзонов, которые кодируют и мембранную (MB-COMT), и растворимую (S-COMT) формы COMT, и расположен на хромосоме 22q11.22-23. Путем изучения генетического сцепления доказана связь этого региона с шизофренией [102, 119].
MB-COMT-изоформа преимущественно экспрессируется в дендритах нейронов всех отделов коры, мозжечка, миндалины, скорлупы, таламуса, гиппокампа и спинного мозга [99, 102]. Посмертные исследования показали, что наиболее высокое содержание COMT характерно для внесинаптических пространств префронтальной коры и гиппокампа [92, 102]. Поскольку в префронтальной коре содержание транспортеров дофамина невелико, COMT, как полагают, играет ключевую роль в его деградации в этой области мозга [52, 102].
Результатом эволюционно нового SNP в гене COMT является замена аминокислоты валина (Val) на метионин в 158-м кодоне MB-COMT. Эта замена приводит к значительному (38%) снижению ферментативной активности в головном мозге и лимфоцитах [37, 102]. Следовательно, носители аллеля met имеют более высокую концентрацию внеклеточного дофамина в префронтальной коре [26, 102].
В метаанализах функциональных нейровизуализационных исследований показана достоверная связь между генотипом COMT и активацией префронтальной коры [102, 104].
Структурные связи и шизофрения. Нарушение целостности белого вещества мозга изучалось при шизофрении [46, 110]. Существуют два основных постулата о природе дефицита белого вещества при шизофрении. Согласно «глобальной теории» белое вещество разрушается равномерно по всему мозгу. Теория «макроцепей» предполагает, что страдают специфические проводящие тракты белого вещества, что может быть причиной или следствием нарушений в областях серого вещества, которые эти тракты соединяют [85, 110].
В последнее время среди генов – кандидатов высокого риска шизофрении внимание обращено на гены, которые влияют на организацию олигодендроцитов. Установлено, что уровень экспрессии шести генов миелина, экспрессируемых олигодендроцитами, значительно снижен у больных шизофренией в сравнении с контрольной группой. Среди них: ген гликопротеина, ассоциированного с миелином, фосфодиэстеразы циклических нуклеотидов, миелинового и лимфоцитарного белка, ErbB3 и трансферрина [55, 110].
Наибольшей величиной эффекта, о которой сообщалось на сегодняшний день, характеризуется влияние SNP NRG1 на целостность белого вещества в переднем таламическом пути [110, 135]. Похожим эффектом обладают полиморфизмы генов ErbB4, MTHFR, серотонина (5HTT) [110].
Функциональные связи. Изменение функциональных связей представляет собой ключевой элемент патогенеза шизофрении, о чем свидетельствуют данные исследований с применением ЭЭГ, ПЭТ и фМРТ, выявивших нарушение префронтально-височных связей у лиц с данным заболеванием при выполнении когнитивных заданий [31, 87, 103, 110].
Эффект полиморфизмов может реализоваться в фенотипе посредством нарушения функциональных связей между отделами мозга. Наибольшей величиной эффекта характеризуется влияние SNP в гене цинк-пальцевого белка 804A (ZNF804A) на функциональные связи в правой префронтальной коре у пациентов с шизофренией [133]. Полиморфизм 5HTTLPR-системы, ассоциированный с тревожностью и депрессией, реализуется через нарушение функциональных связей между миндалиной и поясной корой. В среднем гены риска шизофрении оказывают значительный эффект на функциональные и структурные связи.
Аномалии интернейронов. Согласно одной из гипотез в основе различных нарушений развития ЦНС у людей, в том числе эпилепсии, аутизма и шизофрении, лежат аномалии интернейронов [9, 128]. Эта гипотеза вытекала из наблюдения снижения экспрессии GAD67 в дорсолатеральной префронтальной коре при этих страданиях [10, 128].
Причем имеет место селективное снижение содержания GAD67 в парвальбумин-позитивных нейронах мозга шизофреников [58, 128]. Позже генетические исследования также поддержали эту гипотезу, выявив SNP в области промотора гена GAD1 (2q31.1), кодирующего белок GAD67 у лиц, заболевших шизофренией в детстве, или больных БПР [8, 94, 128].
Шизофрения – модульное расстройство мозга
Мозг человека состоит из функциональных сетей, которые отвечают за обработку разномодальной информации [48]. Последние научные и технологические достижения сформировали наше понимание шизофрении как модульного заболевания.
Патофизиология шизофрении включает в себя нарушения связей между отдаленными и локальными нейронными ансамблями. На основании имеющихся данных шизофрения представляет распространенные нарушения во многих корковых и подкорковых районах и скорее всего вовлекает нарушение работы всех нейромедиаторных систем мозга (ГАМК, дофамин, глутамат, ацетилхолин и др.).
ЭЭГ-нарушения у пациентов с шизофренией (нарушение синхронизации b-ритма при выполнении заданий и отсроченная синхронизация g-ритма) иллюстрируют прерывание связи между отделами коры/мозга и их модульную природу [98, 151]. Эти находки объясняют также, почему подростковый возраст, когда временной профиль мозговой активности должен достичь «взрослого» уровня, является критическим периодом для манифестации имеющихся аномалий при шизофрении.
Нейробиология шизофрении не соответствует ее клинической классификации
Каждый из трех групп главных симптомов шизофрении (позитивные, негативные и когнитивные) может развиться через несколько различных нейробиологических путей. Эти пути могут развиваться одновременно или последовательно как независимые либо как взаимозависимые [98]. Нелинейность этиопатогенетического процесса при шизофрении означает, что окончательный фенотипический результат не может быть предсказан исходя из начальных условий. Другими словами, нелинейность патогенеза обеспечивает возможность любого финала: один и более этиологические факторы взаимодействуют, чтобы создать один клинический подтип, либо один этиопатогенетический фактор и/или аберрантный путь (например, дефицит ГАМК) лежит в основе различных фенотипических результатов (например, параноидная, дезорганизованная или недифференцированная шизофрения) [98].
В таких сложных биологических системах фенотипические различия возникают, когда несколько вариабельных генетических факторов нелинейно взаимодействуют между собой и с несколькими вариабельными факторами окружающей среды, которые отличаются по срокам, продолжительности и степени тяжести.
Нелинейность процесса также указывает, что генетическая предрасположенность к шизофрении не транслируется просто в фенотип, а скорее предполагает возможность целого спектра проявлений: от легких до самых тяжелых случаев [81]. Есть убедительные доказательства того, что шизофрения может быть самым тяжелым результатом семейной полигенной предрасположенности к аберрантной архитектуре и функциям ЦНС [98].
Выводы
Шизофрения представляет собой сложное многофакторное заболевание с чрезвычайно вариабельным течением и клиническими проявлениями, что обусловливается динамическим взаимодействием между многими патогенными и протекторными факторами.
Воздействие средовых факторов является неотъемлемым компонентом патогенеза шизофрении. Одним из доказанных молекулярных механизмов реализации средовых воздействий самой разной модальности является эпигенетическая модуляция генной активности.
В настоящее время необходима трансляция накопленных результатов генетических и эпигенетических исследований шизофрении в практику психиатрической генетики.
Сведения об авторах
Траилин Андрей Вячеславович – д-р мед. наук, доц., зав. каф. лабораторной диагностики и общей патологии ГУ ЗМАПО Минздрава Украины. E-mail: antral@list.ru
Левада Олег Анатольевич – канд. мед. наук, доц., зав. курсом психиатрии каф. семейной медицины ГУ ЗМАПО Минздрава Украины. E-mail: oleg_levada@ukr.net
Статья была опубликована в журнале НЕЙРОNEWS© (Украина) и воспроизводится с любезного разрешения редакции.
www.neuro.health-ua.com
A.V.Trailin, O.A.Levada
Zaporozhye Medical Academy of Postgraduate Education, Ministry of Health of Ukraine
Шизофрения – тяжелое хроническое инвалидизирующее мозговое заболевание, поражающее около 1% популяции земного шара [155]. Гетерогенность симптоматики, лежащая в основе современного выделения форм и вариантов течения данной патологии, может быть частично обусловлена разнообразием генетической природы заболевания, а также сложными взаимодействиями генетических механизмов и средовых влияний. Ввиду сложной и недостаточно исследованной генетики шизофрении затруднено понимание механизмов, посредством которых генетическая вариабельность переформируется в фенотипы страдания. Настоящий обзор посвящен современным исследованиям в области генетики и эпигенетики шизофрении.
Современные генетические методы исследования шизофрении
Для раскрытия роли генетики в этиологии шизофрении принято использовать несколько дизайнов исследования [150].
Исследование сцепления
Исследование сцепления (linkage study) дает ответ на вопрос: «Имеется ли связь между участками или отдельным участком ДНК и определенным фенотипическим признаком?» Анализ сцепления применяется для картирования генетических локусов путем изучения распределения определенного признака внутри семей. Он является наиболее надежным методом для выявления регионов генома, содержащих локусы «больших эффектов» или региональных кластеров редких локусов повышенного риска [28, 60, 144]. Однако разрешение этого метода невелико: выявленный участок хромосомы может содержать несколько миллионов пар оснований, а значит, тысячи генов.
Исследование ассоциаций
Исследования ассоциаций между фенотипами, фенотипами и генетическими полиморфизмами или двумя генетическими полиморфизмами отвечают на вопрос: «Чем обусловлено различное проявление признака среди разных людей в популяции?» Если частота присутствия определенного гена-кандидата или его аллеля в группе лиц с конкретным заболеванием достоверно выше, чем в группе контроля, данный аллель рассматривается как ассоциированный с заболеванием и становится маркером области генома человека, в которой локализуется ген-кандидат. Разработаны следующие дизайны исследований для выявления генетических ассоциаций: случай-контроль, семейный дизайн, ассоциация количественных признаков.
Если изучение сцепления генов позволяет определить и локализовать ген-кандидат, то ассоциативные исследования определяют потенциальную этиологическую роль аллелей этого гена в развитии заболевания.
Исследования генетического сцепления и генетических ассоциаций могут носить общегеномный характер: genome-wide linkage studies (GWLS) и genome-wide association studies (GWAS) соответственно, и позволяют одновременно выявлять сотни тысяч маркеров предрасположенности к заболеванию [144]. Имеющиеся GWAS оптимально обнаруживают варианты, ответственные за повышение относительного риска заболевания в степени выше чем 1,1 [62]. Когда относительный риск составляет 3 и более или имеется много независимых вариантов риска, анализ сцепления становится более мощным, чем анализ ассоциаций [15].
Новые стандарты
В области генетических исследований существует общая тенденция ухода от изучения отдельных генов и белков. Новый стандарт исследований – это анализ коэкспрессированных генных сетей (карты всех активных генов в ЦНС в настоящее время) или генных продуктов (proteoms), анализ метаболических путей, исследования общегеномных эпигенетических моделей, таких как модели связывания факторов транскрипции (transcriptomes), модели метилирования (methylomes), изучение специфических условий среды с их специфическими патогенными и защитными эффектами (enviromics). Принимая во внимание, что экспрессия генов управляется не только спецификой унаследованных аллелей, но и эпигенетическими факторами, не кодирующими РНК, взаимодействием с продуктами генов, также вовлеченных в данный процесс и т.д., правильный подход к изучению молекулярного патогенеза шизофрении и связанных с нею психических расстройств должен включать одновременный анализ всех этих эффектов [16, 97].
Исследование эндофенотипов
Очевидно, что гены могут действовать на нескольких уровнях, начиная от самого генного продукта, через клеточный, системный и поведенческий, вплоть до комплексных фенотипов, таких как терапевтический эффект или нарушения социальных взаимодействий, причем эффект гена не обязательно одинаков на каждом из уровней [102].
Одной из стратегий, которая нашла много последователей в психиатрии, является отход от болезни как сущности к более конкретным биологическим уровням, таким как клеточный, системный, или данным нейрокогнитивных исследований, в надежде, что эффект генов будет более заметным на этих уровнях и легче будет обнаружить новые генетические варианты, повышающие риск заболевания. Эта стратегия получила название концепции эндофенотипов, и ее правомочность особенно убедительно подтверждается, когда в качестве метода количественной оценки структуры и функционирования мозга используется нейровизуализация [102].
Неинвазивная оценка статуса ЦНС
Одной из самых сложных задач в будущем будет решение проблемы тканевой и клеточной специфичности эпигенетических изменений ЦНС. Косвенная (периферийная) оценка с применением мононуклеарных лейкоцитов периферической крови дала обнадеживающие результаты [50]. Однако эти периферийные корреляты позволяют провести лишь грубую оценку изменений в ЦНС [98].
Экспериментальные модели
Современные экспериментальные модели заключаются в «имплантации» животному гипотетического биологического фактора, например вариации количества повторов (CNV), содержании его в различных условиях высокого риска и контроле за развитием структурных и функциональных последствий [91, 98]. Кроме того, возможно применение межвидового генетического картирования, которое сравнивает результаты картирования генов пациентов с функциональными данными, полученными путем картирования рекомбинантных инбредных линий мышей. При этом для выявления генетических вариантов, которые влияют на развитие мозга у людей, используется свойство эволюционного консерватизма, присущего генам, которые участвуют в формировании ЦНС [120].
Структура генетического риска шизофрении
Генетическая склонность к шизофрении, возможно, определяется сотнями и даже тысячами генов [98, 105].
Применение метода генетических ассоциаций позволило собрать базу данных генов шизофрении, объединившую однонуклеотидные генетические полиморфизмы (SNP), ассоциация которых с шизофренией имеет серьезное научное обоснование (табл. 1) [13, 23, 41]. Общегеномные ассоциативные исследования путем изучения до 1% нормальных и патологических геномов идентифицировали лишь малую часть генов, вовлеченных в этиопатогенез шизофрении, но при этом показали, что за повышение риска шизофрении ответственно очень большое количество генов, однако общепопуляционный риск каждой из генетических поломок невелик [77, 126].

Многие из выявленных аллелей являются рецессивными [86]. Это дает основание думать, что при эволюции человека происходил отбор аллелей, которые увеличивают риск развития шизофрении [77].
Общегеномные исследования сцепления выявили редкие мутации/варианты, которые повышают восприимчивость к семейной шизофрении почти на каждой хромосоме, но лишь некоторые регионы показали воспроизводимость в других исследованиях. Один из таких регионов находится вблизи теломер хромосомы 13q. Эти регионы также были связаны с биполярным расстройством (БПР) [127].
В метаанализе Lewis и соавт. (2003 г.) систематизированы данные 20 исследований по изучению сцепления определенных хромосомных регионов и шизофрении [89]. Показано, что только одна область на длинном плече хромосомы 2 (2q22.1) с высокой степенью достоверности (р<0,000417) фигурировала во всех 20 исследованиях [89, 90]. Других локусов, тесно связанных с заболеванием, выявить не удалось, хотя еще 9 хромосом (5q, 3p, 11q, 6p, 1q, 22q, 8p, 20q, 4р) были идентифицированы как носители номинально значимых регионов с пограничной (р<0,05) достоверностью [42].
Данное исследование практически положило конец поиску одного гена, повышающего риск шизофрении. Кроме того, были определены участки генома, повышающие восприимчивость к шизофрении, и выявлено их совпадение с нестабильными сегментами генома, характеризующимися высокой частотой CNV, неоднократно упоминавшимися в связи с шизофренией [98, 132].
Генетические причины шизофрении
Частота SNP – мутации одной пары оснований в определенном локусе – в популяции составляет более 1%, а у каждого человека их насчитывается более 1 млн. Недавний доклад Международного консорциума по шизофрении показал, что сотни и тысячи частых аллелей, каждая с малым эффектом, в совокупности могут объяснить примерно 30% генетического риска заболевания [145, 146]. В дополнение к SNP в качестве этиологических факторов шизофрении были предложены CNV.
В отличие от SNP CNV встречаются в популяции редко (менее 1%). Они включают дупликации и делеции по меньшей мере 1 тыс. пар оснований, что представляет собой большие (протяженные) генетические повреждения (до 12% генома), которые затрагивают обычно несколько генов (по некоторым данным, от нескольких тысяч до нескольких миллионов пар нуклеотидов) [34, 125]. Вследствие этого индивидуальные геномы могут отличаться по количеству копий сегментов ДНК и определенных генов, т.е. меняется «доза гена». В случае дупликации может появиться лишняя копия гена, а при делеции, наоборот, одной копией гена может стать меньше, и, следовательно, понижается или повышается экспрессия продукта гена – белка или не кодирующей РНК [2]. Дупликации и делеции фрагментов ДНК также могут встраиваться в нуклеотидную последовательность гена или выпадать из нее, вызывая разрыв, что нарушает нормальную экспрессию гена. Ввиду большого масштаба поломок вклад CNV в вариативность генома сопоставим с вкладом однонуклеотидных полиморфизмов или даже превышает его [2].
CNV ответственны за 2–4% генетической предрасположенности к шизофрении. Использование более тонких технологий может увеличить этот показатель до 10–20% [136]. При шизофрении повышена частота CNV, которые затрагивают гены, участвующие в развитии ЦНС, особенно нейрегулин- и глутаматергических путей [157].
Индивидуальные CNV достоверно повышают риск шизофрении по сравнению с менее масштабными генетическими вариациями (табл. 2), но поскольку CNV наблюдаются и у здоровых лиц, а также увеличивают риск других психических расстройств (например, аутизма), они не могут в полной мере объяснить генетический риск шизофрении [30]. С другой стороны, работы по изучению роли CNV при шизофрении отличает хорошая воспроизводимость результатов [127].

Большинство CNV не унаследованы, а являются результатом спонтанных мутаций ДНК в момент зачатия или развития, которые могут быть ответственны за спорадические случаи шизофрении [161]. Так, у пациентов с шизофренией без семейного анамнеза заболевания обнаружено в
8 раз больше редких спонтанных мутаций, чем в контрольной группе. Данные мутации в основном затрагивали пути формирования мозга. Эта находка может также объяснить, почему шизофрения персистирует в популяции, а не подчиняется естественному отбору. Так, у 27 из 53 пациентов со спорадическими случаями шизофрении выявлено 40 мутаций de novo, затрагивающих 40 генов [160].
Имеется несколько групп доказательств, подтверждающих роль мутаций de novo в качестве механизма возникновения шизофрении. Во-первых, мутации de novo генерируются с высокой частотой в популяции. Очень высокая конкордантность монозиготных близнецов и очень низкая – дизиготных также поддерживает гипотезу о том, что значительная часть случаев шизофрении может возникнуть в результате новых мутаций [73]. Кроме того, несмотря на снижение репродуктивной функции и чрезвычайно разнообразные факторы риска окружающей среды, распространение шизофрении сохраняется во всем мире на относительно высоком и стабильном уровне – около 1%. Рост риска данного заболевания с повышением возраста отца также может быть объяснен увеличением у него количества мутаций de novo [96].
Сообщается, что у больных шизофренией инсерции чаще встречаются на хромосоме Xq23 (52%), а делеции – в основном на хромосоме 3q13.12 (32%) [107]. В последнее время в ряде крупных статей сообщали об ассоциации целого ряда CNV с шизофренией (см. табл. 2). Носителями делеций в регионах 22q11.2, 1q21.1 и 15q13.3 могут быть до 2% лиц с данной патологией [20, 21].
Среди генов, функция которых нарушается путем CNV, – ген нейрексина 1 (NRXN1), последовательность нуклеотидов которого разрывается делецией в участке 2p16, и ген белка А2, связывающего предшественник амилоида (APBA2), в котором происходит дупликация [84]. Оба гена необходимы для образования и функционирования синапсов.
Помимо модификации гена, пол родителя, у которого произошла CNV, также имеет значение, особенно если затронут проксимальный сегмент длинного плеча хромосомы 15 [19]. Распространенность психотических нарушений значительно выше у пациентов, унаследовавших 2 копии материнской хромосомы 15, чем в случае делеции региона 15q11-q13 отцовской хромосомы [59]. У части пациентов с шизофренией также выявлены дупликации в регионе хромосомы 15q11-q13 материнского происхождения [65]. Этот локус содержит регион управления импринтингом, с различным способом метилирования материнских и отцовских аллелей, что влияет на экспрессию нескольких генов, необходимых для развития нервной системы [59].
Эти исследования достоверно показывают, что некоторые носители de novo и унаследованных CNV, особенно при условии, что они нарушают функции генов, подвергаются высокому риску развития шизофрении. В большинстве случаев у носителей этих генетических вариантов развивается типичная шизофрения, однако может возникнуть и синдром шизофрении в виде неспособности к обучению [136].
Для обнаружения редких CNV необходимы выборки больших объемов, которые удалось сформировать, объединив усилия многих научных коллективов в консорциуме по шизофрении. При полногеномном исследовании редких вариантов CNV у 3391 пациента с шизофренией и 3181 человека из контрольной группы у 1% всех обследованных обнаружены участки CNV длиной более 100 тыс. пар оснований. При этом у больных они встречались чаще, чем в контроле [2, 141].
Эпигенетические механизмы: взаимодействия среды и генома
Эпигенетику можно определить как процесс взаимодействия генотипа организма со средой при формировании фенотипа. Она изучает механизмы, при помощи которых на основе генетической информации, заключенной в одной клетке (зиготе), за счет различной экспрессии генов в разных типах клеток может осуществляться развитие многоклеточного организма, состоящего из дифференцированных клеток [1, 12]. Благодаря эпигенетическим механизмам патогены среды способны достичь ядер клеток и изменить геном, потенцируя существующие или создавая новые генетические риски развития заболевания. Эпигенетические нарушения были предложены в качестве патогенетического механизма шизофрении [117].
Геномная восприимчивость к воздействиям окружающей среды продолжается в течение всей жизни: от гаметогенеза до стадии зрелых, дифференцированных соматических клеток [98]. Основными механизмами эпигенетического контроля считаются:
- метилирование ДНК;
- ремоделирование хроматина;
- регуляция на уровне РНК (в частности, РНК-интерференция);
- прионизация белков;
- инактивация X-хромосом [1, 38, 109].
Метилирование ДНК заключается в присоединении метильной группы к цитозину в составе CpG-динуклеотида в позиции С5 цитозинового кольца. У человека метилировано около 1% геномной ДНК. В то время как упорядоченное метилирование ДНК необходимо для определения уникальных свойств клетки, аберрантное метилирование ДНК может коррелировать с шизофренией и другими заболеваниями [5].
Анализ посмертных образцов мозга пациентов с шизофренией предоставил доказательства гиперметилирования промотора генов реелина (RELN), факторов транскрипции SOX10 и FOXP2, серотонинового рецептора 2А (HTR2A), в результате чего снижалась экспрессия этих генов [4, 6, 68, 148]. Гипометилирование промотора гена мембраносвязанной катехол-О-метилтрансферазы (MB-COMT), напротив, ведет к его гиперэкспрессии [3].
Недавние исследования показали повышение базального уровня диметилированного лизина в 9-м положении
3-го гистона (H3K9 мет2), маркера репрессивного хроматина в лимфоцитах пациентов с шизофренией по сравнению с нормальным контролем. Более высокий уровень H3K9 мет2 также ассоциируется с более ранним дебютом заболевания [5]. Повышенный уровень H3-(метил)-аргинина 17 ассоциируется со снижением экспрессии некоторых метаболических генов, таких как CRYM, кодирующий синтез регулируемого НАДФ белка, связывающего тиреоидные гормоны, генов цитохрома С1 (CYTOC/CYC1), малатдегидрогеназы и орнитинаминотрансферазы в префронтальной коре у пациентов с шизофренией [5, 11].
В то время как с возрастом у здоровых усиливается метилирование H3K4 в промоторе гена глутаматдекарбоксилазы (GAD1), ГАМКергического гена, как правило, у пациентов с шизофренией в префронтальной коре отмечается его гипометилирование. Последующие исследования на мышах показали, что клозапин, но не галоперидол, может увеличить метилирование H3K4 [5, 63].
На этом фоне недавние сообщения об обнаружении в ДНК, полученной из слюны лиц с шизофренией, гипометилирования первого экзона гена HTR2A и промотора гена MB-COMT показывают, что эпигенетические изменения могут служить периферическими диагностическими биомаркерами шизофрении и потенциальными мишенями для терапии [5, 51, 114].
Посттрансляционное динамическое ремоделирование хроматина путем ковалентной модификации хвостов гистонов в нуклеосомах, вокруг которых обернута молекула ДНК, также считается эпигенетическим механизмом регуляции экспрессии генов. Хвосты гистонов являются предметом динамической ковалентной модификации в виде ацетилирования, метилирования и фосфорилирования, которые определяют, будет ли ДНК доступной для регуляторных и транскрипционных факторов.
Например, ацетилирование лизина в хвосте гистона, 9-м положении гистона H3 (H3K9 ац), создает отрицательно заряженные амидные группы, которые отталкивают отрицательно заряженные фосфатные группы ДНК, что разрыхляет структуру хроматина и облегчает транскрипцию генов за счет увеличения доступности молекул ДНК для транскрипционных факторов и РНК-полимераз, тогда как ацетилирование гистона и метилирование лизина в 9-м положении гистона H3 (H3K9 мет), напротив, являются доминирующими чертами конденсированного хроматина, где экспрессия генов подавлена [98]. В этом контексте ингибиторы гистондеацетилазы, такие как вальпроат натрия, который индуцирует экспрессию молчащих генов, уже давно рассматриваются как важные препараты в психиатрической практике [5, 7].
Накапливаются доказательства того, что связь между средовыми воздействиями, с одной стороны, активностью и экспрессией генов, с другой, реализуется через динамические конформации хроматина [36, 98, 142, 143]. Это справедливо не только для патогенов химической или биологической природы, но и для негативных психосоциальных воздействий [113, 143, 158].
Одним из первых доказательств аберрантной регуляции модификации гистонов при шизофрении было изменение ультраструктуры хроматина нейтрофилов, что может служить периферическим суррогатным маркером, который отражает эпигенетические нарушения в мозге, и может быть использовано для эффективной ранней диагностики и терапии шизофрении [5, 67]. Пимозид (типичный антипсихотик) может ослаблять увеличение количества богатых аргинином гистонов у лиц с шизофренией [5, 137].
В целом эти исследования наглядно демонстрируют, что выбор эпигенетических изменений в качестве мишени может стать основной стратегией разработки терапии шизофрении.
В последнее время большое внимание привлечено к
изучению роли в процессах регуляции генетической активности малых интерферирующих РНК и микро-РНК [100]. Интерферирующие РНК могут изменять стабильность и трансляцию мРНК путем моделирования функций полисом и структуры хроматина [1].
Микро-РНК – это малые некодирующие РНК длиной 21–25 оснований, которые либо ингибируют трансляцию мРНК, либо участвуют в деградации целевых мРНК. Посмертный анализ 260 микро-РНК из лобных долей пациентов с шизофренией и шизоаффективным расстройством выявил повышение экспрессии miR-106b и снижение экспрессии 16 других микро-РНК, среди которых miR-24, miR-26b, miR-30e and miR-92 [5].
При шизофрении обнаружено увеличение биогенеза микро-РНК в дорсолатеральной префронтальной коре и верхней височной извилине, причиной чего является увеличение количества РНК-связывающего белка Dgcr8, необходимого для созревания первичных микро-РНК [5, 24].
Показано, что при шизофрении увеличивается содержание в постсмертном мозге miR-181b, miR-15a, miR-15b, miR-195, и miR-107, среди генов-мишеней которых гены рецепторов глутумата: GRM5, GRM7, GRIK2, GRIN1 и GRID, серотонина (HTR1B, HTR2C и HTR4), ГАМК (GABR1, GABRA1), дофамина (DRD1), М-холинорецептора 1, и другие гены-кандидаты, вовлеченные в патогенез заболевания: мозгового нейтротрофического фактора (BDNF), нейрегулина 1 (NRG1), RELN, атаксина 2 [5, 24].
В целом, несмотря на противоречивые данные ряда исследований, одни из которых показали снижение, а дру-гие – повышение содержания микро-РНК при развитии шизофрении, последнее исследование 453 микро-РНК в постсмертном мозге установило, что содержание 19% исследуемых микро-РНК снижено при шизофрении, тогда как изменений в сторону увеличения экспрессии не было вовсе [5, 108].
Эпигенетические нарушения могут быть одной из причин половых различий в восприимчивости к шизофрении. Так, общегеномный анализ в постсмертном мозге пациентов, умерших от шизофрении или БПР, обнаружил более 12 тыс. CpG-островков наряду с большим количеством специфичных для пола метилированных генов [5, 105]. Среди последних – гиперметилирование ДНК гена WDR18 у мужчин, больных шизофренией, и ненормальное метилирование ДНК ГАМК- и глутаматергических генов при шизофрении и БПР. В других исследованиях было продемонстрировано ослабление экспрессии, чувствительной к эстрогену miR-30b, в мозге женщин с шизофренией [5, 101].
Несмотря на возрастающее количество доказательств роли эпигенетических аберраций в патогенезе шизофрении, существует точка зрения, что лишь некоторые из них могут быть этиологическими факторами заболевания, в то время как большинство из эпигенетических модификаций вторичны и обусловлены болезнью, эффектами препаратов или ненормальным образом жизни пациентов. Следовательно, для того чтобы выявить ген-кандидат (а не вторично измененный ген), необходим поиск факторов, вызывающих эпигенетические нарушения и раскрытие механизмов их действия.
Нарушение эпигенетической регуляции при шизофрении
Причиной нарушения эпигенетической регуляции при шизофрении являются средовые эффекты и/или эпимутации, т.е. ошибки в запрограммированном метилировании ДНК. Эпимутации происходят в течение гамето- и эмбриогенеза, когда появляются эпигенетические маркеры, чтобы запрограммировать время- и тканеспецифические события в процессе развития [75, 98]. Точность передачи модели метилирования ДНК ниже, чем таковая последовательности ДНК [98, 153]. Поэтому эпимутации de novo возникают на один или два порядка чаще, чем мутации ДНК в соматических клетках [61]. Это подразумевает их значительный вклад в заболевания человека [43]. Они могут возникать как случайно, так и специфическим образом в ответ на определенные изменения среды.
Каким бы ни было их происхождение, эпигенетические маркеры передаются путем митоза дочерним соматическим клеткам во время морфогенеза и роста [36, 98]. Это обеспечивает механизм, с помощью которого эпигенетические последствия ранних экологических патогенных воздействий продолжают действовать на протяжении всего развития, особенно в постмитотических клетках (нейронах и др.). Они могут выступать в качестве молекулярных предшественников развивающихся при шизофрении структурных и функциональных нарушений [1, 44]. Эпигенетические метки в некоторых случаях сохраняются в процессе гаметогенеза и могут быть перенесены от предков к потомкам [1, 39, 71].
Возможные мишени нарушений эпигенетической регуляции
Унаследованные полиморфные гены. По аналогии с гипотезой «двойного удара» в канцерогенезе генетический дефект (рецессивная мутация) не приведет к болезни, если только не будет сочетаться с другим генетическим (соматическая мутация) или средовым фактором [эпигенетическое подавление второй (нормальной) аллели], что приводит к проявлению мутации.
К примеру, имеется SNP, повышающий активность пролиндегидрогеназы и увеличивающий риск шизофрении. Он может сочетаться с двумя другими SNP, снижающими активность пролиндегидрогеназы и, соответственно, риск шизофрении [78]. В этом случае наличие мутации или эпигенетического воздействия повысит риск шизофрении, если они снизят активность протективного аллеля [98].
Нормальные гены. Нарушение эпигенетической регуляции нормальных генов, вовлеченных в развитие ЦНС (например, DISC1, NRG1, рецептора подсемейства эпидермального фактора роста ErbB4, COMT, BDNF, DTNP1 и др.), может привести к ряду генетических аномалий, таких как аберрантная моноаллельная экспрессия, неадекватная доза гена и рассинхронизация геномной активности [98].
Гены-протекторы. Так можно обозначить гены, обладающие положительными эффектами на когнитивные способности, мотивации, эмоции и развитие ЦНС. Например, Met/Met-вариант гена COMT ассоциируется со снижением риска шизофрении, имеет благоприятное влияние на оперативную память и предотвращает развитие психоза у наркоманов, употребляющих каннабис [35, 45]. Если гомозиготность Met/Met будет нарушена эпигенетически, это, вероятно, увеличит и риск шизофрении, и тяжесть ее симптомов [98].
Патологическая активация генов. «Патологичность» генома шизофрении характеризуется не только гипер-, но и гипометилированием нуклеотидов [105]. Хотя модифицирование активности генов нервной ткани путем гипометилирования не настолько эффективно, как в случае гиперметилирования, оно может проявляться некоторой активацией генов [105]. Например, при шизофрении не происходит возраст-зависимого подавления экспрессии генов, участвующих в развитии ЦНС, но имеет место продолжающаяся их экспрессия, по-видимому, вследствие гипометилирования промоторов [98, 149].
Условно патологические гены. Термин относится к нормальным генам глии и других соматических клеток, регулирующих межклеточные взаимодействия и иммунный ответ (например, гены, кодирующие цитокины).
Индуцированная инфекцией активация этих генов во время критических периодов внутриутробного развития нарушает нормальное формирование ЦНС [146].
Метастабильные эпиаллели. Пока идентифицированы лишь несколько генов с метастабильными эпиаллелями [70]. Они представляют собой локусы, которые могут претерпевать разнообразные эпигенетические модификации обратимого характера. В результате генетически идентичные организмы могут иметь широкий ряд фенотипов (здоровых и больных лиц). Метастабильные эпиаллели особенно чувствительны к средовым факторам в период внутриутробного развития [98].
Средовые факторы риска при шизофрении
Нарушения эпигенетической регуляции и пренатальные факторы риска «первого удара»
Экологические факторы являются неотъемлемой частью патогенеза шизофрении [32, 98, 156]. В ряде исследований установлена взаимосвязь данного заболевания с рождением зимой или ранней весной, рождением в городе, возрастом отца, голодом, нарушениями питания и перинатальными осложнениями [5].
В зависимости от срока беременности, с которым совпадает воздействие средового фактора, повреждаются различные нейробиологические мишени, вовлекаются разные патогенетические механизмы и возможны различные фенотипические проявления. Пренатальные факторы в основном влияют на геном и/или развивающиеся ткани головного мозга. Их можно обозначить как факторы риска «первого удара» [98].
В основном это факторы биологической природы (вирусы, бактерии, токсины), влияющие на беременную с генетической предрасположенностью к психозу, особенно в 1 и 2-м триместрах [32]. Поскольку большинство вирусов не проникает через плаценту, предполагается непрямое влияние на плод, вероятно, связанное с противовирусным ответом иммунной системы матери, например путем секреции провоспалительных цитокинов [47]. Действительно, высокий уровень интерлейкина-8 в крови женщины во время беременности увеличивает риск шизофрении у ребенка и приводит к структурным изменениям в структурах ЦНС, вовлеченных в патогенез шизофрении [33, 47].
В настоящее время раскрыты три различных механизма реализации эффекта пренатальной инфекции [98].
Эпигенетическое подавление генов плаценты/ плода. В эксперименте на мышах Y.Bobetsis и соавт.
(2010 г.) выявили 74 гена, регуляция которых была эпигенетически нарушена вследствие бактериальной инфекции во время беременности [27]. Большинство генов, участвующих в развитии плода, были подавлены. Среди них внимание обращали 3 гена, вовлеченных в развитие ЦНС, – синаптотагмин X (SYT10), нейропептид галанин (GAL) и его рецептор (GALR3). SYT10 регулирует секрецию нейротрансмиттеров и, соответственно, сигнализацию между нейронами, в то время как мутации гена галанина лежат в основе распространенных нарушений в ЦНС, включающих, например, меньшее количество сенсорных нейронов и снижение способности к регенерации нервов.
Патологическая активация микроглии. Исследования in vitro продемонстрировали активацию микроглии провоспалительными цитокинами. Фетальный мозг богат микроглией, и в случае активации она способна вырабатывать хемокины и цитокины, которые могут быть токсичными для ЦНС. При бактериальной инфекции липополисахарид эндотоксина проникает через плаценту и индуцирует выработку цитокинов в головном мозге плода [72].
Нарушение функции фетоплацентарного комплекса. Провоспалительные цитокины играют важную роль в сохранении фетоплацентарного комплекса, и повышение их уровня может привести к повреждению плода. У людей интерлейкин-6 способствует развитию у матери реакции «хозяин против графта», вплоть до развития спонтанного аборта. В более легких случаях целостность фетоплацентарного барьера нарушается лишь частично, что достаточно для повышения риска шизофрении либо через нейротоксическое повреждение (вероятно, с участием механизмов гипоксии или мальнутриции), либо эпигенетическое нарушение регуляции генома [98].
Среди неинфекционных факторов риска первого удара выделяют ассоциированные с повышенным риском шизофрении социальные факторы, реализующиеся через тяжелый материнский стресс в 1-м триместре беременности, депрессию, гипоксию плода вследствие акушерских осложнений, дефицит питательных веществ, особенно необходимых для формирования S-аденозилметионина, например фолиевой кислоты, холина, витамина В12 [82, 95, 98, 112, 130].
Нарушение эпигенетической регуляции уже предрасположенного к развитию заболевания генома, вероятно, является основным механизмом эффектов пренатальных или ранних послеродовых воздействий окружающей среды. Эпигеном особенно чувствителен к нарушению в пренатальный период, во время быстрой репликации клеток и точной установки эпигенетических маркеров для управления развитием [44, 98].
Предполагается и другой механизм патогенетических эффектов пренатальных средовых факторов. Они часто вызывают прямое повреждение мозга (например, этанол, отравление свинцом и т.д.). Последовавшее за этим аберрантное развитие ЦНС формирует ранние аберрантные нейронные структуры и функции («продромальная ЦНС») с повышенной чувствительностью к воздействиям окружающей среды. Этот продромальный мозг становится независимым фактором риска шизофрении, субстратом для взаимодействия с окружающей средой, которое в отдельных случаях может привести к фенотипу шизофрении [98].
Факторы риска постнатального «второго удара»
После рождения изначально генетически предрасположенная к развитию заболевания ЦНС, скомпрометированная пренатальными нарушениями, может подвергаться различным средовым воздействиям, достоверно увеличивающим риск шизофрении [98, 130, 156]. Период, в котором реализуются эффекты средовых факторов риска «второго удара», простирается от раннего послеродового периода через детство до поздней юности или даже позже. Доказанные факторы риска «второго удара» включают в себя воздействия социальной среды (проживание в городах, а не в сельской местности, международная миграция), психологических патогенов (стресс), химических веществ (употребление каннабиса) и др. [98, 130].
Точные механизмы реализации эффектов постнатальных средовых факторов в значительной степени неизвестны, но, по-видимому, неоднородны. Известно, например, что динамическое регулирование метилирования ДНК продолжается и в дифференцированных нейронах коры под влиянием различных социальных факторов, алкоголя и метамфетаминов [98, 115, 122, 124, 134].
В дополнение к нарушению эпигенетической регуляции генома (как описано выше) факторы окружающей среды могут нарушить развитие ЦНС посредством потенцирования биологических путей, вовлеченных в патогенез шизофрении [98]. Например, употребление каннабиса подростками увеличивает риск данного заболевания во время чувствительных периодов кортикогенеза. В частности, носители аллеля COMT Val (этот вариант связан с быстрым метаболизмом дофамина, низким содержанием дофамина в коре и высоким – в среднем мозге) были более склонны к развитию психоза, если они употребляли каннабис, по сравнению с носителями аллеля COMT Met или взрослыми наркоманами – носителями полиморфизма COMT Val [35]. Провоцирующий эффект каннабиса объясняется тем, что конопля вызывает значительное снижение коркового содержания дофамина и увеличение его содержания в среднем мозге [98]. Данный пример демонстрирует, как уже существующая наследственная дисфункция дофаминергической системы мозга, усиленная средовыми воздействиями, приводит к повышению риска психоза. Он также свидетельствует в пользу смешанной модели генетического риска шизофрении: эпигенетические воздействия потенцируют предсуществующую полигенно обусловленную уязвимость [98].
Острый психосоциальный стресс повышает риск шизофрении через взаимодействие «геном–среда», возможно, с участием цитокинов [98, 130, 162]. Кроме того, стресс также приводит к увеличению содержания дофамина в стриатуме – хорошо известный фактор развития позитивной симптоматики шизофрении, особенно в контексте имеющейся предрасположенности [93, 98, 121].
Миграция и ассоциированный с нею низкий социально-экономический статус могут создать так называемый стресс «социального фиаско» или «нестабильной социальной иерархии», в развитии которых участвуют ядра ЦНС и кортикальные пути, вовлеченные в патогенез шизофрении [98, 164].
Хотя кортикогенезом в первую очередь управляет генетическая информация, эффективность ее реализации зависит также от интенсивности и способа использования [74, 98]. Генетический и «пользовательский» механизмы сосуществуют в определенной пропорции вплоть до конечной стадии развития мозга [98]. Другими словами, в некоторых случаях экологические патогены увеличивают риск за счет активации биологических путей, вовлеченных в патогенез шизофрении.
Комплексное нелинейное развитие шизофрении
Комплексная структура генетической предрасположенности к шизофрении является необходимым условием для последующего развертывания нейропатологических процессов, а также субстратом для эпигенетической модуляции патогенами среды [98]. В некоторых случаях для фенотипических проявлений достаточно только генетических факторов (например, CNV или точечные мутации).
В других случаях эпигенетические факторы накладываются на фон, представляющий собой несколько генетических отклонений, каждое с малой величиной эффекта. Так как в каждом отдельном случае сочетание генетических и экологических факторов варьирует, клинические проявления и эволюция заболевания также вариабельны.
Влияние экологических факторов может меняться в зависимости от ряда обстоятельств, таких как: тип экологического патогена; интенсивность его влияния; острое или хроническое воздействие; этап развития ЦНС; чувствительность эпигенетических процессов, активных во время экспозиции; сосуществование защитных факторов, таких как корректирующие эффекты среды и защитные генетические варианты [98].
Смешанная модель генетического риска в структуре шизофрении
Эмпирические данные поддерживают существование при шизофрении аллелей риска обоих типов: частых (SNP) и редких (CNV), но предполагают, что ни один из них не играет специфической роли в патогенезе болезни [118].
Несмотря на доказательства высокой наследуемости, большинство случаев шизофрении производит впечатление спорадических, поскольку родители около 90% больных шизофренией сами не страдают этим заболеванием, а у 60% лиц с данной патологией отсутствуют больные родственники 1 и 2-й степени родства [98].
Их причиной могут быть CNV de novo. Действительно, в некоторых случаях редкие и масштабные генетические повреждения, такие как CNV, достаточны, чтобы вызвать шизофрению [147]. Эти редкие мутации, как правило, имеют высокую, но неполную пенетрантность, тем самым объясняя впечатление спорадичности возникновения заболевания [106]. Как показали Xu и соавт. (2011 г.), примерно в половине изученных случаев шизофрении идентифицированные CNV были не унаследованы, а возникли de novo в первом поколении [160].
Этим же, возможно, объясняется более высокий риск развития шизофрении у детей пациентов, чем у их братьев и сестер [136]. При генетическом консультировании в случае, если установлено, что в основе заболевания пробанда лежит CNV de novo, риск развития заболевания у сиблингов будет значительно ниже.
Определение точного характера CNV и тех генетических/эпигенетических и средовых факторов, которые влияют на их пенетрантность и экспрессивность, в совокупности приводя к повышению риска широкого диапазона нарушений развития, будет захватывающим вызовом для психоневрологических исследований в ближайшем будущем [136].
Редкие CNV могут нарушать структуру различных хромосомных регионов, но обычно за развитие шизофрении отвечает какой-то один из них [106]. В соответствии со «смешанной моделью» в случае CNV средовые воздействия не обязательны, но могут утяжелять фенотипические проявления [106]. С другой стороны, редкого CNV не всегда достаточно, чтобы вызвать шизофрению, в таком случае необходимо наличие «генетического фона», состоящего из других нормальных и/или полиморфных генов, эпистатически усиливающих эффект CNV.
Экологические факторы способны синергически увеличить риск шизофрении, но только при наличии генетической предрасположенности, а не как независимые факторы риска [95, 98]. При этом низкая пенетрантность полигенной склонности к заболеванию, субстратом которой являются вариабельные редкие и/или частые структурные повреждения генома, синергетически потенцируется через взаимодействие «геном–среда».
Такой синергизм может быть опосредован эпигенетической модуляцией унаследованной генетической предрасположенности (т.е. увеличением ее пенетрантности); путем повышения восприимчивости к шизофрении с помощью специальных эффектов (например, активное использование уязвимого биологического пути); через неспецифические эффекты (например, прямая травма мозга); всеми механизмами в некоторой пропорции [98].
Этот сценарий объясняет аномальный, значительный эффект эпигенетических воздействий, которые накладываются на многофакторный фон, в котором каждый фактор в малой степени повышает предрасположенность к заболеванию. Также в эту модель вписываются описанные выше случаи, когда одна структурная аномалия с большим эффектом накладывается на многофакторный фон [98].
Таким образом, создается впечатление, что шизофрения у разных людей может быть обусловлена как большим количеством частых генетических вариаций с малыми эффектами, так и редкими генетическими вариантами с большими эффектами [98]. Каждый клинический случай шизофрении может быть специфическим с генетической точки зрения и представлять интерактивное сочетание широкого, но в конечном счете ограниченного спектра патологических генетических вариантов [98].
В самом деле, симуляционные исследования на основе компьютерного моделирования показывают, что в основе наследования шизофрении могут лежать тысячи аллелей [145]. Это означает, что взаимодействие между генами, эпистаз, может играть важную роль в патогенезе, а также способствовать взаимодействию генома со средой [102]. В результате один и тот же генотип может реализоваться в нескольких различных фенотипах, и наоборот, различные генотипы могут иметь сходные фенотипические проявления.
Шизофрения как патология формирования ЦНС
Все больше авторов осмысливают шизофрению как расстройство развития ЦНС в отличие от статического поражения головного мозга или несостоятельности созревания мозга на окончательной стадии его развития [66, 80, 98].
Эта гипотеза получила новый импульс в результате недавно сделанных открытий в области эпидемиологии, развития и нейровизуализации. Так, нейровизуализационные исследования выявили структурные аномалии головного мозга уже на момент начала заболевания. Во-вторых, часто у пациентов, которым с возрастом был выставлен диагноз шизофрении, еще в молодом возрасте встречались когнитивные и моторные нарушения. Наконец, экспериментальное повреждение мозга у приматов в неонатальный период имеет отсроченные эффекты на их поведение [118].
Несколько генов, вовлеченных в формирование ЦНС, локализованы в хромосомных локусах, в которых также идентифицированы гены-кандидаты повышенного риска шизофрении, которые характеризуются полиморфным статусом и меняют свою экспрессию в эмбриогенезе [91]. Например, у детей с ранним началом заболевания, гипофункцией фронтальной коры и сниженным объемом серого вещества коры при МРТ, выявлены 3 SNP в гене GAD1, который кодирует белок GAD67 [8].
Более важно то, что большинство ассоциированных с риском шизофрении специфических генов, включая DISC1, NRG1, DTNP1, ген NCAM – молекулы адгезии нервных клеток, а также RELN, BDNF, NR1-субъединицы NMDA-рецепторов, играют важную роль в формировании мозга, нейротрансмиссии и синаптической пластичности [91].
При шизофрении хорошо известны анатомические нарушения, такие как расширение желудочков, сокращение объема префронтальной коры и гиппокампа, уменьшение мозга в целом [53, 91]. При этом заболевании выявляют существенные изменения размеров и морфологии нейронов, а также синаптических связей [56, 91].
Исследования корковой и лимбической области мозга показывают, что структурная и молекулярная целостности синаптических комплексов, глутаматергических рецепторов и путей трансдукции сигнала играют критически важную роль в мозге в процессе его формирования, синаптогенеза и синаптической пластичности [17, 91].
Требуется время, для того чтобы первоначальная предрасположенность к шизофрении материализовалась в аберрантные структуры, связи и функции ЦНС. Иными словами, развивающаяся ЦНС, так сказать, «не готова» для шизофрении, потому что ее полная функциональность еще не установлена. В момент полового созревания функции мозга становятся более уязвимыми для имеющихся биодефектов.
Фактически имеются четыре подтвержденные стадии шизофрении: повышенного риска, продромального периода, психоза и хронической инвалидности [66, 98].
Недавно было показано, что прогрессирование от продрома к манифестной шизофрении у пациентов ультравысокого риска может быть значительно замедлено с помощью нейропротекторных соединений, таких как w-3 полиненасыщенные жирные кислоты [14]. Эти данные в очередной раз указывают на нелинейность патогенеза шизофрении, и что продром является скорее независимым фактором риска шизофрении, а не обязательной стадией ее развития. В рамках этой концепции манифестация психоза может рассматриваться не как начало, а как поздняя стадия заболевания [66].
В подтверждение концепции шизофрении как патологии развития ЦНС можно привести факт выявленного генетического сходства между шизофренией и синдромами, при которых психопатология проявляется в детском возрасте и которые часто группируются как расстройства формирования ЦНС [118, 131]. Так, конкретные вариации количества копий, которые в значительной степени связаны с шизофренией, также ассоциированы с такими расстройствами, как аутизм, умственная отсталость, синдром дефицита внимания и гиперактивности (СДВГ), генерализованная эпилепсия [118, 159].
Важно, что все эти расстройства ассоциированы с нарушениями познания, чаще встречаются у мужчин и в основном ассоциируются с задержкой развития различной степени, мягкими неврологическими симптомами и двигательными нарушениями. Кроме того, между этими синдромами есть достоверная коморбидность, что также указывает на их возможную принадлежность к одной группе [118].
Это дает возможность ряду исследователей предполагать, что данные нарушения представляют собой континуум генетических и экологически индуцированных нарушений в развитии ЦНС, а не набор дискретных этиологических единиц. При этом главный клинический синдром частично отражает тяжесть и преобладающий тип аномального развития мозга и, как следствие, функциональных нарушений, а также модифицирующие эффекты других генетических и экологических факторов. Таким образом, аутизм может быть диагностирован, когда нарушения мозговых проводящих путей приводят к явным расстройствам коммуникации в социуме, СДВГ – когда преобладают нарушения тормозного контроля и умственная отсталость – когда доминируют когнитивные нарушения [118].
Если классифицировать тяжелые психические заболевания по убыванию тяжести нарушений развития ЦНС, то они расположатся следующим образом: интеллектуальная инвалидность, аутизм, СДВГ, шизофрения, БПР [118].
Гипотеза «разобщения»
Согласно гипотезе «разобщения», впервые предложенной Friston и соавт. в 1990-х годах, первопричиной шизофрении является патологическая синаптическая пластичность вследствие дисрегуляции NMDA-рецепторов дофамином.
В поддержку роли NMDA-рецепторов при шизофрении свидетельствуют результаты нескольких исследований. Во-первых, препараты, блокирующие NMDA-рецепторы, такие как кетамин и фенциклидин, могут вызывать психотические симптомы у здоровых людей [69]. Кроме того, введение кетамина вызывает дефицит обработки сенсорной информации в контрольной группе, аналогичный таковому при шизофрении, что свидетельствует о роли
NMDA-рецепторов для этих дефицитов [152]. Активность дофаминергических нейронов среднего мозга частично регулируется глутаматергическими проекциями из префронтальной коры, которые действуют через NMDA-рецепторы, и их блокада повышает амфетамин-индуцированное увеличение содержания дофамина в стриатуме в контрольной группе, похожее на увеличение у пациентов с шизофренией [76]. Наконец, генетические варианты, которые играют роль в NMDA-сигнализации, были связаны с повышением риска шизофрении при исследованиях генов-кандидатов (например, DAOA – ген активатора оксидазы D-аминокислот, GRM3 и белок, регулирующий сигнальную активность G-белков) [57, 110].
Использование визуализационной генетики для исследования нервных связей. В двух метаанализах, посвященных изучению степени влияния генетического полиморфизма на функцию мозга, показана большая величина эффекта полиморфизмов 5HTTLPR (гена белка-транспортера обратного захвата серотонина) и COMT Val158Met на активацию нейронов миндалины и префронтальной коры [104, 110, 111].
Роль COMT заключается в деградации катехоламинов, в том числе и дофамина [22, 54, 102]. Ген COMT состоит из двух промоторов и шести экзонов, которые кодируют и мембранную (MB-COMT), и растворимую (S-COMT) формы COMT, и расположен на хромосоме 22q11.22-23. Путем изучения генетического сцепления доказана связь этого региона с шизофренией [102, 119].
MB-COMT-изоформа преимущественно экспрессируется в дендритах нейронов всех отделов коры, мозжечка, миндалины, скорлупы, таламуса, гиппокампа и спинного мозга [99, 102]. Посмертные исследования показали, что наиболее высокое содержание COMT характерно для внесинаптических пространств префронтальной коры и гиппокампа [92, 102]. Поскольку в префронтальной коре содержание транспортеров дофамина невелико, COMT, как полагают, играет ключевую роль в его деградации в этой области мозга [52, 102].
Результатом эволюционно нового SNP в гене COMT является замена аминокислоты валина (Val) на метионин в 158-м кодоне MB-COMT. Эта замена приводит к значительному (38%) снижению ферментативной активности в головном мозге и лимфоцитах [37, 102]. Следовательно, носители аллеля met имеют более высокую концентрацию внеклеточного дофамина в префронтальной коре [26, 102].
В метаанализах функциональных нейровизуализационных исследований показана достоверная связь между генотипом COMT и активацией префронтальной коры [102, 104].
Структурные связи и шизофрения. Нарушение целостности белого вещества мозга изучалось при шизофрении [46, 110]. Существуют два основных постулата о природе дефицита белого вещества при шизофрении. Согласно «глобальной теории» белое вещество разрушается равномерно по всему мозгу. Теория «макроцепей» предполагает, что страдают специфические проводящие тракты белого вещества, что может быть причиной или следствием нарушений в областях серого вещества, которые эти тракты соединяют [85, 110].
В последнее время среди генов – кандидатов высокого риска шизофрении внимание обращено на гены, которые влияют на организацию олигодендроцитов. Установлено, что уровень экспрессии шести генов миелина, экспрессируемых олигодендроцитами, значительно снижен у больных шизофренией в сравнении с контрольной группой. Среди них: ген гликопротеина, ассоциированного с миелином, фосфодиэстеразы циклических нуклеотидов, миелинового и лимфоцитарного белка, ErbB3 и трансферрина [55, 110].
Наибольшей величиной эффекта, о которой сообщалось на сегодняшний день, характеризуется влияние SNP NRG1 на целостность белого вещества в переднем таламическом пути [110, 135]. Похожим эффектом обладают полиморфизмы генов ErbB4, MTHFR, серотонина (5HTT) [110].
Функциональные связи. Изменение функциональных связей представляет собой ключевой элемент патогенеза шизофрении, о чем свидетельствуют данные исследований с применением ЭЭГ, ПЭТ и фМРТ, выявивших нарушение префронтально-височных связей у лиц с данным заболеванием при выполнении когнитивных заданий [31, 87, 103, 110].
Эффект полиморфизмов может реализоваться в фенотипе посредством нарушения функциональных связей между отделами мозга. Наибольшей величиной эффекта характеризуется влияние SNP в гене цинк-пальцевого белка 804A (ZNF804A) на функциональные связи в правой префронтальной коре у пациентов с шизофренией [133]. Полиморфизм 5HTTLPR-системы, ассоциированный с тревожностью и депрессией, реализуется через нарушение функциональных связей между миндалиной и поясной корой. В среднем гены риска шизофрении оказывают значительный эффект на функциональные и структурные связи.
Аномалии интернейронов. Согласно одной из гипотез в основе различных нарушений развития ЦНС у людей, в том числе эпилепсии, аутизма и шизофрении, лежат аномалии интернейронов [9, 128]. Эта гипотеза вытекала из наблюдения снижения экспрессии GAD67 в дорсолатеральной префронтальной коре при этих страданиях [10, 128].
Причем имеет место селективное снижение содержания GAD67 в парвальбумин-позитивных нейронах мозга шизофреников [58, 128]. Позже генетические исследования также поддержали эту гипотезу, выявив SNP в области промотора гена GAD1 (2q31.1), кодирующего белок GAD67 у лиц, заболевших шизофренией в детстве, или больных БПР [8, 94, 128].
Шизофрения – модульное расстройство мозга
Мозг человека состоит из функциональных сетей, которые отвечают за обработку разномодальной информации [48]. Последние научные и технологические достижения сформировали наше понимание шизофрении как модульного заболевания.
Патофизиология шизофрении включает в себя нарушения связей между отдаленными и локальными нейронными ансамблями. На основании имеющихся данных шизофрения представляет распространенные нарушения во многих корковых и подкорковых районах и скорее всего вовлекает нарушение работы всех нейромедиаторных систем мозга (ГАМК, дофамин, глутамат, ацетилхолин и др.).
ЭЭГ-нарушения у пациентов с шизофренией (нарушение синхронизации b-ритма при выполнении заданий и отсроченная синхронизация g-ритма) иллюстрируют прерывание связи между отделами коры/мозга и их модульную природу [98, 151]. Эти находки объясняют также, почему подростковый возраст, когда временной профиль мозговой активности должен достичь «взрослого» уровня, является критическим периодом для манифестации имеющихся аномалий при шизофрении.
Нейробиология шизофрении не соответствует ее клинической классификации
Каждый из трех групп главных симптомов шизофрении (позитивные, негативные и когнитивные) может развиться через несколько различных нейробиологических путей. Эти пути могут развиваться одновременно или последовательно как независимые либо как взаимозависимые [98]. Нелинейность этиопатогенетического процесса при шизофрении означает, что окончательный фенотипический результат не может быть предсказан исходя из начальных условий. Другими словами, нелинейность патогенеза обеспечивает возможность любого финала: один и более этиологические факторы взаимодействуют, чтобы создать один клинический подтип, либо один этиопатогенетический фактор и/или аберрантный путь (например, дефицит ГАМК) лежит в основе различных фенотипических результатов (например, параноидная, дезорганизованная или недифференцированная шизофрения) [98].
В таких сложных биологических системах фенотипические различия возникают, когда несколько вариабельных генетических факторов нелинейно взаимодействуют между собой и с несколькими вариабельными факторами окружающей среды, которые отличаются по срокам, продолжительности и степени тяжести.
Нелинейность процесса также указывает, что генетическая предрасположенность к шизофрении не транслируется просто в фенотип, а скорее предполагает возможность целого спектра проявлений: от легких до самых тяжелых случаев [81]. Есть убедительные доказательства того, что шизофрения может быть самым тяжелым результатом семейной полигенной предрасположенности к аберрантной архитектуре и функциям ЦНС [98].
Выводы
Шизофрения представляет собой сложное многофакторное заболевание с чрезвычайно вариабельным течением и клиническими проявлениями, что обусловливается динамическим взаимодействием между многими патогенными и протекторными факторами.
Воздействие средовых факторов является неотъемлемым компонентом патогенеза шизофрении. Одним из доказанных молекулярных механизмов реализации средовых воздействий самой разной модальности является эпигенетическая модуляция генной активности.
В настоящее время необходима трансляция накопленных результатов генетических и эпигенетических исследований шизофрении в практику психиатрической генетики.
Сведения об авторах
Траилин Андрей Вячеславович – д-р мед. наук, доц., зав. каф. лабораторной диагностики и общей патологии ГУ ЗМАПО Минздрава Украины. E-mail: antral@list.ru
Левада Олег Анатольевич – канд. мед. наук, доц., зав. курсом психиатрии каф. семейной медицины ГУ ЗМАПО Минздрава Украины. E-mail: oleg_levada@ukr.net
Статья была опубликована в журнале НЕЙРОNEWS© (Украина) и воспроизводится с любезного разрешения редакции.
www.neuro.health-ua.com
Список исп. литературыСкрыть список1. Вайсерман А.М., Войтенко В.П., Мехова Л.В. Эпигенетическая эпидемиология возрастзависимых заболеваний. Онтогенез. 2011; 42 (1): 30–50.
2. Голимбет В.Е., Корень Е.В. Вариации числа копий в геноме – новая страница в генетических исследованиях в области психиатрии: международный проект PsychCNVs. Журн. неврол. и психиатр. 2010; 1: 107–9.
3. Abdolmaleky HM, Cheng KH, Faraone SV et al. Hypomethylation of MB-COMT promoter is a major risk factor for schizophrenia and bipolar disorder. Hum Mol Gen 2006; 15: 3132–45.
4. Abdolmaleky HM, Cheng KH, Russo A et al. Hypermethylation of the reelin (RELN) promoter in the brain of schizophreniс patients: a preliminary report. Am J Med Gen. Neuropsychiat Gen 2005; 134 (1): 60–6.
5. Abdolmaleky HM, Thiagalingam S. Can the schizophrenia epigenome provide clues for the molecular basis of pathogenesis? Epigenom 2011; 3 (6): 679–83.
6. Abdolmaleky HM, Yaqubi S, Papageorgis P et al. Epigenetic dysregulation of HTR2A in the brain of patients with schizophrenia andbipolar disorder. Schizophr Res 2011; 129 (2–3): 183–90.
7. Abdolmaleky HM, Zhou JR, Thiagalingam S et al. Epigenetic and pharmacoepigenomic studies of major psychoses and potentials for therapeutics. Pharmacogenomics 2008; 9 (12): 1809–23.
8. Addington M, Gornick M, Duckworthetal J. GAD1 (2q31.1), which encodes glutamic acid decarboxylase (GAD67), is associated with childhood-onset schizophrenia and cortical graymatter volume loss. Mol Psychiat 2005; 10 (6): 581–8.
9. Akbarian S, Huang HS. Molecular and cellular mechanisms of altered GAD1/GAD67 expression in schizophrenia and related disorders. Brain Research Rev 2006; 52 (2): 293–304.
10. Akbarian S, Kim JJ, Potkin SG et al. Gene expression for glutamic acid decarboxylase is reduced without loss of neurons in prefrontal cortex of schizophrenics. Archiv Gen Psychiat 1995; 52 (4): 258–78.
11. Akbarian S, Ruehl MG, Bliven E et al. Chromatin alterations associated with down-regulated metabolic gene expression in the prefrontal cortex of subjects with schizophrenia. Arch Gen Psychiat 2005; 62 (8): 829–40.
12. Akhtar A, Cavalli G. The epigenome network of excellence. PloS Biol 2005; 3 (5): е177.
13. Allen NC, Bagade S, McQueen MB et al. Systematic meta-analyses and field synopsis of genetic association studies in schizophrenia: the SzGene database. Nat Gen 2008; 40: 827–34.
14. Amminger PG, Schäfer MR, Papageorgiou P et al. Long-chain omega-3 fatty acids for indicated prevention of psychotic disorders. A randomized, placebo-controlled trial. Arch Gen Psychiat 2010; 67: 146–54.
15. Anderson CA, Soranzo N, Zeggini E, Barrett JC. Synthetic associations are unlikely to account for many common disease genome-wide association signals. PLoS Biol 2011; 9: e1000580.
16. Anthony JC. The promise of psychiatric enviromics. Brit J Psychiat 2001; 178 (40): s8–11.
17. Arnold SE, Talbot K, Hahn CG. Neurodevelopment, neuroplasticity, and new genes for schizophrenia. Prog Brain Res 2005; 147: 319–45.
18. Badner JA, Gershon ES. Meta-analysis of whole-genome linkage scans of bipolar disorder and schizophrenia. Mol Psychiat 2002; 7: 405–11.
19. Bassett AS. Parental origin, DNA structure, and the schizophrenia spectrum. Am J Psychiat 2011; 168 (4): 350–3.
20. Bassett AS, Costain G, Fung WL et al. Clinically detectable copy number variations in a Canadian catchment population of schizophrenia. J Psychiat Res 2010; 44: 1005–9.
21. Bassett AS, Scherer SW, Brzustowicz LM. Copy number variations in schizophrenia: critical review and new perspectives on concepts of genetics and disease. Am J Psychiat 2010; 167: 899–14.
22. Bertocci B, Miggiano V, Da Prada M et al. Human catechol-O-methyltransferase: cloning and expression of themembrane-associated form. Proc Natl Acad Sci USA 1991; 88: 1416–20.
23. Bertram L. Genetic research in schizophrenia: new tools and future perspectives. Schizophr Bull 2008; 34: 806–12.
24. Beveridge NJ, Gardiner E, Carroll AP et al. Schizophrenia is associated with an increase in cortical microRNA biogenesis. Mol Psychiat 2010; 15 (12): 1176–89.
25. Beveridge NJ, Tooney PA, Carroll AP et al. Dysregulation of miRNA 181b in the temporal cortex in schizophrenia. Hum Mol Gen 2008; 17 (8): 1156–68.
26. Bilder RM, Volavka J, Lachman HM, Grace AA. The catechol-O-methyltransferase polymorphism: relations to the tonic-phasic dopamine hypothesis and neuropsychiatric phenotypes. Neuropsychopharmacol 2004; 29: 1943–61.
27. Bobetsis YA, Barros SP, Lin DM et al. Altered gene expression in murine placentas in aninfection-induced intrauterine growth restriction model: a microarray analysis. J Repr Immun 2010; 85: 140–8.
28. Borecki IB, Province MA. Linkage and association: basic concepts. Adv Gen 2008; 60: 51–74.
29. Bornovalova MA, Hicks BM, Iacono WG, McGue M. Familial transmission and heritability of childhood disruptive disorders. Am J Psychiat 2010; 167: 1066–74.
30. Bray NJ, Markus Leweke F, Kapur S, Meyer-Lindenberg A. The neurobiology of schizophrenia: new leads and avenues for treatment. Cur Opin in Neurobiol 2010; 20: 810–5.
1 мая 2012
Количество просмотров: 5803


