Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
1 Saint Petersburg State University. 199034, Russian Federation, Saint Petersburg, Universitetskaia nab., d. 7/9. petrova_nn@mail.ru
2 N.I.Pirogov Russian National Research Medical University of the Ministry of Health of the Russian Federation. 117997, Russian Federation, Moscow, ul. Ostrovitianova, d. 1;
3 «Sotex Pharmacological Company»;
4 David Ben-Gurion University in Negev.8410501, Israel, Be'er Sheva;
5 Stavropol State Medical University of the Ministry of Health of the Russian Federation. 355017, Russian Federation, Stavropol, ul. Mira, d. 310.
Abstract
The COVID-19 pandemic that has raged around the world over the past year has led to a sharp deterioration in the mental health and psychological well-being of the entire human population. This is facilitated by many factors: both the pronounced neuroinvasive and neurotoxic properties of the SARS-CoV-2 virus itself, and, to an even greater extent, the pronounced distress that many people experience both as a result of the pandemic itself and as a result of governmental measures to combat it, leading to profound economic recession, mass unemployment and poverty.
These factors, acting together, have sharply raised the incidence of depressive, anxiety and stress-related disorders in the population, especially among some risk groups, such as the elderly people, patients with chronic somatic and / or mental illnesses, and healthcare professionals. In addition, the current lack of effective specific treatments for COVID-19 has posed a challenge for doctors and researchers to search for potentially effective drugs against this infection among drugs which were already approved for clinical use for other indications (so-called repositioning of drugs).
In this article, we show the reader, why various approaches based on immunomodulation, including immunomodulation through sigma-1 cellular receptors, are of great interest to both scientists and practitioners working in the field of COVID-19 treatment. Then we present to the reader the results of the first pilot randomized clinical trial devoted to the study of the possible efficacy and safety of the use of fluvoxamine (which in Russia is known as Rocona) in the prevention of severe complications and unfavorable outcome of COVID-19 infection. We also discuss possible alternative (non sigma-1 receptor related) mechanisms of fluvoxamine’s efficacy in the prevention of COVID-19 complications.
Keywords: COVID-19, SARS-CoV-2, pandemic, coronavirus, distress, mental health, depression, anxiety, fluvoxamine, Rocona, sigma-1 receptor, autophagy, acidic sphingomyelinase, melatonin
For citation: Petrova N.N., Morozov P.V., Markin A.V., Bekker R.A., Bykov Yu.V. The COVID-19 pandemic: challenges of our times, with discussion on the latest data regarding an issue of rational psychopharmacotherapy choices in patients with SARS-CoV-2 infection. Psychiatry and psychopharmacotherapy. 2020; 6: 8–24.
Не менее хорошо известно, что разные вирусы обладают различной способностью вызывать подобного рода психические осложнения. Это во многом связано с наличием или отсутствием у конкретного вируса нейротропных свойств (то есть способности непосредственно поражать нервные или глиальные клетки, вызывая тем самым вирусный энцефалит), или способности провоцировать выраженную системную воспалительную реакцию организма и связанный с ней «цитокиновый шторм», либо служить триггером для развития разнообразных аутоиммунных реакций на мозговую ткань. В частности, такого рода психические осложнения часто описываются после перенесенного гриппа, других острых респираторных вирусных инфекций (ОРВИ), в том числе — вызванных различными коронавирусами, а также после перенесенной кори, опоясывающего лишая, инфекционного мононуклеоза, острого гепатита А, эпидемического паротита, у пациентов с хроническим носительством вируса иммунодефицита человека (ВИЧ) или вирусов гепатита В и/или С, и так далее [Gale SD et al, 2018].
Более того, показано, что внутриутробно перенесенная вирусная инфекция, причем даже не из числа явно тератогенных, таких как краснуха (например, заболевание матери гриппом или банальным ОРВИ в период беременности, причем необязательно в первом триместре), — может в дальнейшем создавать у ребенка предрасположенность к развитию депрессивных и тревожных расстройств в более старшем, подростковом или уже взрослом возрасте [Schnittker J, 2020].
Ассоциация депрессивных расстройств, независимо от их генеза или от первоначального их триггера, с выраженной реактивацией латентных вирусов герпес-группы (вирусов простого герпеса различных подтипов, цитомегаловируса, вируса Эпштейна-Барр), носителями которых являются до 90% популяции, а также с реактивацией так называемых «эндогенных ретровирусов» или ретротранспозонов, встроенных в наш геном, даже побудила турецкого исследователя Турхана Канли выдвинуть спорную и дискуссионную гипотезу о том, что клиническая депрессия, возможно, является своеобразным «герпетическим энцефалитом низкой интенсивности» [Canli T, 2014; 2019].
Не является исключением из общего правила о высокой частоте психических осложнений (прежде всего — депрессивных и тревожных состояний), после перенесенных вирусных инфекций, и новая коронавирусная инфекция, впервые обнаруженная в 2019 году, получившая название COVID-19 (сам же вирус, вызывающий эту болезнь, получил название SARS-CoV-2) [Ahorsu DK et al, 2020; Le HT et al, 2020; Wadoo O et al, 2020].
Более того, сегодня имеются основания утверждать, что вредное влияние нынешней пандемии COVID-19 на психическое здоровье популяции — существенно больше, чем у многих других упомянутых выше вирусных инфекций. Причины этого мы рассмотрим ниже.
Одной из важных причин, обуславливающих столь высокую частоту неблагоприятных психических и неврологических последствий перенесенного COVID-19, является весьма выраженная нейротропность вируса SARS-CoV-2 (более выраженная, чем у других ранее известных коронавирусов, включая его ближайшего родственника SARS-CoV-1, или «вирус атипичной пневмонии»). Этот новый коронавирус способен непосредственно проникать в нейроны и клетки глии в ЦНС, заражать их и активно размножаться в них, вызывая их апоптотическую гибель и запуская каскад реактивного воспаления в мозге [Yesilkaya UH et al, 2020].
Особенно интересно отметить, что, помимо своего основного и уже хорошо известного механизма проникновения в клетки самых различных тканей — связывания с мембранным белком ангиотензин-превращающего фермента изотипа 2 (белком ACE2), который обильно экспрессируется не только в легочной ткани, но и в сосудах, в миокарде, в нервной системе, в ЖКТ, почках, надпочечниках и других тканях, вирус SARS-CoV-2 способен использовать и другой механизм проникновения в мозг — связывание с некоторыми белками-шаперонами нейронов и глиальных клеток, а именно — с так называемыми «сигма-1» и «сигма-2» рецепторами [Yesilkaya UH et al, 2020].
Еще один возможный (если исходить из результатов экспериментов на животных — весьма частый) путь проникновения SARS-CoV-2 в головной мозг — это через его способность связываться с белком нейропилин-1, обильно экспрессируемым как на поверхности клеток обонятельного эпителия слизистой носа, так и на поверхности нервных клеток, особенно в тех областях мозга, которые имеют отношение к функциям обоняния и вкуса. При этом может наблюдаться восходящее инфицирование, благодаря близости носовых раковин, обонятельной луковицы и головного мозга. Этот механизм проникновения вируса хорошо объясняет такой частый симптом COVID-19, как гипосмия или полная аносмия (снижение или полная утрата обоняния) и иногда также гипогевзия или полная агевзия (снижение или полная утрата вкусовой чувствительности) [Davies J et al, 2020].
Последствия инфицирования головного мозга вирусом SARS-CoV-2 порой бывают весьма тяжелыми, и отнюдь не ограничиваются вышеописанным «постковидным синдромом». Так, в частности, в литературе описаны случаи возникновения синдрома Гийена-Барре на фоне заболевания COVID-19, а также случаи манифестации болезни Паркинсона после перенесенного COVID-19 [Chaná-Cuevas P et al, 2020; Nanda S et al, 2020].
В литературе также описаны множественные случаи COVID-ассоциированной энцефалопатии, в том числе тяжелого течения (вплоть до развития коматозных состояний и до летальных исходов именно по причине тяжелой энцефалопатии, а не по причине респираторного дистресса или полиорганной недостаточности), случаи развития отека мозга на фоне COVID-19, случаи развития на фоне COVID-19 острого некротизирующего геморрагического энцефалита, вирусных энцефалитов и менингитов, стойких когнитивных и/или двигательных нарушений, нарушений зрения и слуха, напоминающих проявления первичных нейродегенеративных заболеваний [Mishra R, Banerjea AC, 2020].
Другими важными причинами поражений ЦНС при тяжелом течении COVID-19, помимо прямого нейротропного (нейроинвазивного) и нейротоксического действия самого вируса SARS-CoV-2, являются гипоксия мозга, связанная с острой дыхательной недостаточностью (ОДН) или с острым респираторным дистресс-синдромом (ОРДС), интоксикация, связанная с метаболическими нарушениями и нередким развитием острой полиорганной недостаточности (печеночной, почечной, надпочечниковой) на фоне тяжелого течения COVID-19, влияние цитокинового шторма, провоцирующего нейровоспаление даже в отсутствие прямой инвазии вируса в мозг, а также нарушение кровоснабжения мозга при развитии острой сердечно-сосудистой недостаточности или коллаптоидных состояний на фоне тяжелого COVID-19 [Mishra R, Banerjea AC, 2020].
Кроме того, хорошо известно, что COVID-19 часто сопровождается развитием выраженной гиперкоагуляции и наклонностью к тромбозам сосудов и к тромбоэмболическим осложнениям, особенно у лежачих или малоподвижных пациентов, и в первую очередь — у пациентов, находящихся в коматозном состоянии или на искусственной вентиляции легких (ИВЛ) [Bikdeli B et al, 2020].
Иногда на фоне COVID-19 могут наблюдаться, напротив, повышенная кровоточивость и связанные с нею геморрагические осложнения. Они обусловлены как COVID-ассоциированным поражением эндотелия сосудов, особенно мелких капилляров (эндотелиальной дисфункцией), повышением ломкости и проницаемости сосудов (COVID-ассоциированной макро- и микроангиопатией, капилляротоксикозом), так и коагулопатией потребления на фоне диссеминированного внутрисосудистого свертывания (ДВС-синдрома), или же передозировкой антикоагулянтов либо антиагрегантов, часто применяемых в комплексном лечении пациентов с COVID-19 как раз для профилактики гиперкоагуляционных и тромботических осложнений [Al-Samkari H et al, 2020; Amraei R, Rahimi N, 2020].
Все это значительно повышает риск развития на фоне COVID-19 различных сердечно-сосудистых и неврологических катастроф, в частности, ишемических или, напротив, геморрагических инсультов острых инфарктов миокарда [Marshall M, 2020]. А это, в свою очередь, может в ближайшее время значительно повысить количество пациентов, страдающих постинсультными и/или постинфарктными депрессиями и тревожными состояниями.
Показано, что наиболее частыми последствиями перенесенного COVID-19 для психики среди выписанных из стационара пациентов являются: посттравматическое стрессовое расстройство (ПТСР) — оно наблюдается у каждого третьего такого пациента. Вторыми по частоте в этой популяции являются депрессивные расстройства, которые наблюдаются у каждого шестого такого пациента, и различные тревожные расстройства, также наблюдаемые примерно у каждого шестого пациента, перенесшего COVID-19 в достаточно тяжелой форме, которая потребовала госпитализации [Rogers JP et al, 2020].
Однако, помимо вредного прямого и косвенного нейротропного действия самого вируса SARS-CoV-2, на психическое здоровье населения в период пандемии COVID-19 неблагоприятно влияет целый ряд других факторов, которые мы рассмотрим ниже.
Именно эти необычные биологические свойства нового коронавируса SARS-CoV-2 привели к тому, что его распространение, в отличие от распространения менее контагиозных SARS-CoV-1 или MERS-CoV, не удалось быстро ограничить или остановить. Поэтому оно быстро приняло характер сначала эпидемии, а затем и пандемии. С другой же стороны, высокая летальность новой коронавирусной инфекции и нередко тяжелый характер ее течения, особенно у пожилых пациентов или у пациентов, отягощенных хроническими заболеваниями, — вынудили правительства разных стран мира отнестись к COVID-19 гораздо серьезнее, чем принято относиться к сезонным эпидемиям гриппа или ОРВИ, и предпринять жесткие карантинные меры [Aleebrahim-Dehkordi E et al, 2020].
Неблагоприятное влияние пандемии COVID-19 на состояние общего психического здоровья популяции отмечается в самых разных странах и регионах мира, вне зависимости от сложности эпидемиологической обстановки в конкретной стране, в конкретном регионе или области, от жесткости предпринимаемых правительством страны или региона/области карантинных мер, от количества выделяемых на социальную поддержку населения средств и от других подобных факторов. Так, об этом синхронно пишут исследователи из таких разных и весьма географически удаленных друг от друга стран с разными подходами к обеспечению карантина, как Швеция, Иран, Гонконг, Вьетнам, Тайвань, Катар [Ahorsu DK et al, 2020; Le HT et al, 2020; Wadoo O et al, 2020].
Показано, что пандемия COVID-19 ассоциируется с ухудшением психического здоровья населения не только и не столько по причине заболеваемости и смертности, связанных с самой этой болезнью, но и по причине того, что значительная часть населения (особенно пожилые люди и люди из групп риска) испытывает сильный и продолжительный хронический стресс, связанный со страхом заразиться этой болезнью, страхом ее тяжелого протекания, страхом смерти, а также по причине того, что меры по сдерживанию или замедлению распространения пандемии, такие как социальное дистанцирование и самоизоляция, сами по себе порождают дополнительный стресс. Кроме того, на фоне карантинных ограничений и экономического спада часть людей потеряла работу, у другой части существенно ухудшилось материальное положение, и это тоже служит дополнительным источником стресса для них [Ahorsu DK et al, 2020; Le HT et al, 2020; Wadoo O et al, 2020].
В период пандемии COVID-19, которая свирепствует в мире уже более полугода, огромное количество людей во всем мире постоянно находится в быстро меняющихся условиях, связанных с реальной угрозой для жизни. Неспособность каждого отдельно взятого индивидуума как-то повлиять на ситуацию с пандемией и карантином или хотя бы как-то контролировать ее — создаeт классическую ситуацию «выученной беспомощности» (которая, как известно, служит хорошей экспериментальной моделью депрессии на животных). Длительное нахождение в такой обстановке закономерно порождает страх, тревогу, отчаяние, чувство безнадежности или беспомощности, и может приводить к развитию депрессивных состояний [Stein MB, 2020].
Следует еще раз подчеркнуть, что как сама пандемия COVID-19, так и карантинные меры, предпринимаемые для замедления ее распространения (в частности, ограничение социальных контактов и самоизоляция), могут оказать — и уже оказывают — выраженное негативное влияние на психическое здоровье популяции. В связи с этим ряд авторов призывает к тому, чтобы специалисты в области психического здоровья давали публичные рекомендации населению о том, как справляться со стрессом, вызванным пандемией и карантином, и как предотвратить или уменьшить негативные последствия их для своего психического здоровья [Stein MB, 2020].
Интересно отметить, что, по данным британских исследователей, наибольший психологический дистресс в условиях пандемии COVID-19 переживают вовсе не лица пожилого возраста или принадлежащие к группам риска (как можно было бы ожидать, исходя из логики вещей), а женщины, лица молодого возраста и родители детей дошкольного возраста [Pierce M et al, 2020].
 Между тем, большое количество исследований, проведенных задолго до нынешней пандемии COVID-19, указывают на тесную связь между такими неблагоприятными факторами, как хронический стресс, социальная изоляция, одиночество, безработица или бедность, ограничение физической активности, недоступность квалифицированной общемедицинской и психиатрической помощи, — и ухудшением психического и соматического здоровья в популяции [Отчет KFF…, 2020].
Между тем, большое количество исследований, проведенных задолго до нынешней пандемии COVID-19, указывают на тесную связь между такими неблагоприятными факторами, как хронический стресс, социальная изоляция, одиночество, безработица или бедность, ограничение физической активности, недоступность квалифицированной общемедицинской и психиатрической помощи, — и ухудшением психического и соматического здоровья в популяции [Отчет KFF…, 2020].
Так, в частности, в США по состоянию на март 2020 года 32% опрошенных взрослых сообщили интервьюерам, что их психическое здоровье и психологическое благополучие подверглись значительному негативному влиянию из-за дистресса, вызванного пандемией COVID-19. А в августе 2020 года в тех же США количество тех людей, кто сообщил интервьюерам о значительном негативном влиянии на них хронического стресса, связанного с пандемией COVID-19, среди опрашиваемых взрослых выросло уже до 53% [Отчет KFF…, 2020].
Среди симптомов дистресса, описываемых опрошенными, часто отмечались нарушения сна, изменения в пищевом поведении, увеличение потребления алкоголя и/или других психоактивных веществ (ПАВ), включая никотин и кофеин, обострения различных хронических психических и соматических заболеваний [Отчет KFF…, 2020].
Кроме того, согласно тому же отчету, в США за период с мая по июль 2020 года наблюдался устойчивый рост количества людей, сообщающих о наличии у них симптомов тревоги и/или депрессии (рис. 1) [Отчет KFF…, 2020].
В ухудшении общего психического здоровья популяции в период пандемии COVID-19 значительную роль играет вынужденная социальная изоляция или самоизоляция, связанная с карантинными мерами. Так, в частности, в США данные на конец марта 2020 года показывают, что среди тех опрошенных, которые пребывали в вынужденной изоляции или самоизоляции, значительно бóльший процент (47%) сообщал о негативных последствиях хронического стресса и беспокойства, связанных с пандемией COVID-19, для их психического здоровья и/или душевного комфорта, чем среди тех, кто не был в вынужденной изоляции или самоизоляции (37%) [Отчет KFF…, 2020].
Кроме того, те из опрошенных, которые находились в вынужденной изоляции или самоизоляции, гораздо чаще (в 21% случаев) сообщали не просто о последствиях, но именно о выраженных (тяжелых) последствиях хронического стресса, связанного с пандемией COVID-19, для их психического здоровья и/или душевного комфорта, чем те, кто не подвергался вынужденной изоляции и не прибегал к самоизоляции (среди них сообщили о тяжелых последствиях всего 13%) [Отчет KFF…, 2020].
Социальная изоляция или самоизоляция и одиночество, а также ограничение передвижений и физической активности могут представлять особую опасность для психического здоровья и душевного комфорта подростков и пожилых людей, по сравнению с молодыми взрослыми. Так, в США среди лиц в возрасте 65 лет и старше доля тех, кто сообщил интервьюерам о негативных последствиях пандемии COVID-19 для их психического здоровья, увеличилась с марта по июль 2020 года с 27% до 47% [Отчет KFF…, 2020].
Другим хорошо известным фактором, негативно влияющим на психическое здоровье в популяции, является безработица и/или бедность (низкий уровень доходов, низкий социально-экономический статус). Так, в США среди тех людей, которые на фоне пандемии COVID-19 потеряли работу или испытали ухудшение материального положения, о негативных последствиях этой пандемии и связанного с ней хронического стресса и беспокойства, для их психического здоровья сообщили 58% опрошенных [Отчет KFF…, 2020].
Кроме того, было также показано, что лица с более низким уровнем доходов и/или с более низким социально-экономическим статусом (например, с более низким уровнем образования и квалификации и/или живущие в районах с более низким качеством жилья и инфраструктуры) значительно чаще людей с более высоким уровнем доходов и/или с более высоким социально-экономическим статусом (уровнем образования, качеством жилья) сообщают о серьезных негативных последствиях пандемии COVID-19 для их психического здоровья и душевного благополучия [Отчет KFF…, 2020].
 Третьим важным фактором, который может обуславливать ухудшение психического здоровья, как сам по себе, так и в особенности на фоне воздействия хронического стресса, является наличие коморбидных соматических расстройств. Показано, что этот фактор играет роль и на фоне бушующей ныне пандемии COVID-19. Так, в США среди опрошенных взрослых, имеющих те или иные проблемы соматического здоровья, 62% сообщили о негативных последствиях пандемии COVID-19 и связанного с ней хронического стресса и беспокойства для их психического здоровья или психологического благополучия. В то же время среди лиц с хорошим соматическим здоровьем таких было меньше — 51%. Люди с проблемами соматического здоровья также чаще (в 38% случаев) сообщали о значительно выраженном негативном влиянии пандемии на их психическое здоровье и психологический комфорт, чем люди с хорошим соматическим здоровьем (в 23% случаев) [Отчет KFF…, 2020].
Третьим важным фактором, который может обуславливать ухудшение психического здоровья, как сам по себе, так и в особенности на фоне воздействия хронического стресса, является наличие коморбидных соматических расстройств. Показано, что этот фактор играет роль и на фоне бушующей ныне пандемии COVID-19. Так, в США среди опрошенных взрослых, имеющих те или иные проблемы соматического здоровья, 62% сообщили о негативных последствиях пандемии COVID-19 и связанного с ней хронического стресса и беспокойства для их психического здоровья или психологического благополучия. В то же время среди лиц с хорошим соматическим здоровьем таких было меньше — 51%. Люди с проблемами соматического здоровья также чаще (в 38% случаев) сообщали о значительно выраженном негативном влиянии пандемии на их психическое здоровье и психологический комфорт, чем люди с хорошим соматическим здоровьем (в 23% случаев) [Отчет KFF…, 2020].
Ограничение доступности или несвоевременность оказания общемедицинской и психиатрической помощи в период пандемии COVID-19, из-за перераспределения ресурсов медицинской системы на борьбу с пандемией, также играет существенную роль в ухудшении психического здоровья в популяции. Так, в США 4% опрошенных заявили о том, что в период пандемии они столкнулись со снижением доступности экстренной медицинской помощи, не связанной с COVID-19, и/или с пропусками, задержками или переносами на более поздний срок планового общемедицинского и/или психиатрического обслуживания. Большинство из них утверждают, что в результате этого их психическое состояние и душевное благополучие ухудшились (у некоторых — значительно) [Отчет KFF…, 2020].
Влияют на переносимость хронического стресса, связанного с пандемией COVID-19, также гендерные различия и различия в семейном положении. Наличие детей, порождая тревогу и беспокойство за их здоровье на фоне пандемии, является дополнительным фактором риска развития психических проблем. Другим установленным фактором риска является принадлежность к женскому полу. Так, в США более половины опрошенных женщин, имеющих детей в возрасте до 18 лет (57% в марте и 59% в июле 2020 года), сообщили о серьезных отрицательных последствиях стресса, связанного с пандемией COVID-19, для их психического здоровья. Это заметно выше соответствующих показателей как для бездетных женщин, так и для мужчин (в том числе — для одиноких мужчин с детьми). Так, среди мужчин, имеющих детей до 18 лет, в марте 2020 года сообщали о серьезных негативных последствиях стресса, связанного с пандемией COVID-19, 32% опрошенных, а в июле 2020 года — 49% опрошенных [Отчет KFF…, 2020].
Еще до пандемии было известно, что потеря работы или снижение уровня доходов либо социально-экономического статуса (например, вынужденный переезд в район с худшими жилищными условиями и худшей инфраструктурой) — тесно ассоциируются с повышением риска развития депрессивных и тревожных расстройств, с повышенным уровнем стресса, тревоги, беспокойства, со снижением самооценки, а также с повышением частоты самоубийств, и с повышением потребления алкоголя и ПАВ [Отчет KFF…, 2020].
Экстраполяция имеющихся данных о влиянии предыдущих экономических потрясений на нынешнюю ситуацию, предпринятая фондом Well Being Trust и Центром политических исследований Роберта Грэма, показывает, что экономический спад на фоне пандемии COVID-19 и карантинных мер, и связанные с этим безработица и ухудшение материального положения населения, могут к 2029 году привести к дополнительным 75 000 смертей от суицидов, а также от злоупотребления алкоголем или ПАВ, включая никотин, в одних только США [Отчет KFF…, 2020].
Еще одна группа исследователей из США также предприняла попытку оценить влияние пандемии COVID-19 на психическое здоровье, частоту употребления ПАВ и распространенность суицидальных тенденций среди взрослого населения США (≥ 18 лет). С этой целью они в период с 24 по 30 июня 2020 года провели репрезентативные групповые обследования жителей различных городов и поселков в каждом из штатов США [Czeisler ME et al, 2020].
В выборке из этого исследования 40,9% опрошенных сообщили о появлении у них в период пандемии COVID-19 симптомов как минимум одного психического или поведенческого расстройства. В частности, 30,9% опрошенных сообщили о развитии у них симптомов депрессивного или тревожного расстройства на фоне стресса, связанного с пандемией COVID-19, 26,3% сообщили о развитии у них симптомов ПТСР в связи с психологической травмой, нанесенной им либо самой пандемией COVID-19 как таковой, либо фактом перенесения этой болезни либо ими самими, либо кем-то из близких, родственников или друзей, а 13,3% признались в том, что начали употреблять или увеличили потребление алкоголя и/или ПАВ, включая никотин, для того, чтобы справиться со стрессом, вызванным пандемией COVID-19 [Czeisler ME et al, 2020].
Кроме того, 10,7% респондентов этого исследования сообщили о том, что в течение 30 дней, предшествовавших опросу, они серьезно задумывались о самоубийстве. Этот процент был значительно выше среди молодежи в возрасте от 18 до 24 лет (25,5%), среди представителей расовых и этнических меньшинств, которые ощущают себя дискриминированными (например, среди респондентов латиноамериканского происхождения он составил 18,6%), а также среди лиц трудоспособного возраста, вынужденных ухаживать за пожилыми или больными родственниками (30,7%) [Czeisler ME et al, 2020].
Интересные данные опубликованы южнокорейскими исследователями. Они одними из первых в мире поставили вопрос о том, что связь между пандемией COVID-19 и психическими расстройствами может иметь двусторонний характер: не только COVID-19 может вызывать психические расстройства de novo или обострения и рецидивы уже имеющихся психических расстройств, но и наоборот — имеющееся психическое расстройство может повышать риск заражения SARS-CoV-2, риск заболевания COVID-19 или риск тяжелого его течения. Для проверки этого предположения они предприняли масштабное когортное исследование [Lee SW et al, 2020].
Задача южнокорейских исследователей по получению большой выборки значительно облегчалась тем, что Южная Корея оказалась одной из немногих стран мира, в которых на SARS-CoV-2 был протестирован значительный процент популяции. В период с 1 января по 15 мая 2020 года тестирование на SARS-CoV-2 в этой стране прошли 216 418 человек. Из них у 7160 человек (у 3,3% всех протестированных) тест оказался положительным. В исследуемую когорту авторы включили всех тех лиц в возрасте старше 20 лет, которые были протестированы на SARS-CoV-2 в указанный период времени, независимо от результатов теста (положительный или отрицательный) [Lee SW et al, 2020].
Тяжелое течение и неблагоприятные клинические исходы COVID-19 среди тех, у кого тест на SARS-CoV-2 был положительным, в этом исследовании определялись как потребность в кислородной поддержке, вынужденная госпитализация в отделение интенсивной терапии или в отделение реанимации, необходимость в ИВЛ, а также летальный исход [Lee SW et al, 2020].
Анализ влияния наличия психических расстройств на риск заражения SARS-CoV-2 или заболевания COVID-19 в этой когорте показал, что сам по себе диагноз психического заболевания не коррелирует с повышенной вероятностью положительного результата теста на SARS-CoV-2 или с повышенной вероятностью проявления клинических симптомов COVID-19. Однако при этом также обнаружилось, что пациенты с тяжелыми, особенно психотическими, формами аффективных и неаффективных расстройств имеют более высокий риск тяжелого течения и неблагоприятных клинических исходов COVID-19, чем пациенты без психических расстройств в анамнезе или пациенты с легкими и среднетяжелыми психическими расстройствами [Lee SW et al, 2020].
В Австралии в апреле 2020 года был проведен онлайн-опрос о влиянии пандемии COVID-19 на психическое здоровье популяции. В нем принял участие 1491 взрослый. Средний возраст участников опроса составил 50,5±14,9 года. Среди них было 67% женщин. Участниками опроса было отмечено негативное влияние пандемии COVID-19 на уровень их физической активности (об этом сообщили 48,9% всех опрошенных), на качество сна (40,7% всех опрошенных), на частоту употребления алкоголя и/или на среднее количество употребляемого спиртного (26,6% всех опрошенных) и на уровень потребления табака (6,9% всех опрошенных) [Stanton R et al, 2020].
Все эти неблагоприятные изменения на фоне пандемии COVID-19 тесно ассоциировались с наличием симптомов депрессии и/или тревоги. Они были более выраженными и чаще отмечались у женщин, а также у тех лиц, которые находились в вынужденной изоляции или самоизоляции, были безработными или имели низкий уровень доходов, низкий социально-экономический статус (низкий уровень образования, неблагоприятные условия проживания), и у имеющих хронические соматические или психические заболевания [Stanton R et al, 2020].
Интересно отметить, что среди сравнительно молодых лиц (в возрасте от 18 до 45 лет) уровень дистресса, связанного с пандемией COVID-19, был выше, а неблагоприятные последствия для психического здоровья отмечались чаще, чем среди лиц более старшего возраста. Возможно, это связано с тем, что молодые люди психологически хуже переносят карантинные ограничения, социальную изоляцию или самоизоляцию и вынужденное уменьшение свободы перемещения, чем люди пенсионного возраста, более склонные к «домоседству» [Stanton R et al, 2020].
Испанские исследователи также попытались оценить влияние пандемии COVID-19 на психическое здоровье популяции, опросив 976 взрослых по Шкале тревоги и стресса (DASS). Хотя уровни дистресса, тревоги и депрессии в испанской популяции в начале пандемии были достаточно низкими, они постепенно повышались по мере развертывания пандемии и ужесточения карантинных мер. Лица с хроническими психическими или соматическими заболеваниями сообщали о большем количестве и большей выраженности симптомов дистресса, тревоги и депрессии, чем лица без таковой отягощенности, а молодые, опять-таки, сообщали об этом чаще, чем пожилые [Ozamiz-Etxebarria N et al, 2020].
Кроме того, более выраженная тревожная и депрессивная симптоматика отмечалась у тех лиц, которым была предписана изоляция (пребывание на дому) в связи с наличием симптомов COVID-19, положительным результатом теста на вирус SARS-CoV-2 или контактным статусом. Авторы этого исследования констатировали, что по мере продолжения или ужесточения карантинных мер и социальной изоляции можно ожидать дальнейшего увеличения распространенности симптомов дистресса, тревоги и депрессии в испанской популяции [Ozamiz-Etxebarria N et al, 2020].
Исследователи из Гонконга через 3 месяца после появления в этом городе первого подтвержденного случая заболевания COVID-19 провели опрос 500 респондентов с помощью Опросника о здоровье пациента, состоящего из 9 вопросов (Patient Health Questionnaire-9, PHQ-9), и Шкалы оценки генерализованной тревоги из 7 вопросов (Generalized Anxiety Disorder-7, GAD-7). При этом у 19% от общего числа опрошенных обнаружились клинически значимые симптомы депрессии, а у 14% от общего числа опрошенных — клинически значимые симптомы тревоги. Кроме того, 25,4% всех респондентов заявили о том, что их психическое здоровье и психологическое благополучие ухудшились именно из-за пандемии COVID-19 и связанного с ней стресса [Choi EH et al, 2020].
Авторы этого исследования отметили, что среди значимых причин ухудшения психического состояния респонденты чаще всего называли ограничение доступности плановой медицинской помощи, в том числе плановых хирургических вмешательств, необходимость постоянно носить маски на улице и в общественных местах и связанные с этим неудобства и дискомфорт, необходимость соблюдать социальную дистанцию и ограничивать контакты с другими людьми, отсутствие возможности работать на дому, потерю работы или ухудшение материального положения [Choi EH et al, 2020].
Влияние пандемии COVID-19 и связанного с ней стресса на общее психическое здоровье популяции, и в частности — на распространенность в популяции симптомов депрессии, тревоги и ипохондрии (чрезмерной обеспокоенности своим здоровьем), изучали также турецкие исследователи. Применявшиеся ими методики включали в себя опрос респондентов по Госпитальной шкале тревоги и депрессии (Hospital Anxiety and Depression Scale, HADS) и по Опроснику тревоги за здоровье (Health Anxiety Inventory, HAI) [Özdin S, Özdin SB, 2020].
Кроме того, авторы этого исследования также попытались выяснить, какие факторы влияют на индивидуальную переносимость стресса, связанного с пандемией, и на риск развития неблагоприятных последствий этого стресса для психического здоровья индивидуума. Они учитывали такие факторы, как место проживания (город или деревня), профессия, социальный статус, возраст, пол, семейное положение, наличие несовершеннолетних детей, совместное проживание с человеком старше 60 лет или с человеком, принадлежащим к группе риска тяжелого течения COVID-19, наличие лиц с подтвержденным заражением SARS-CoV-2 или с симптомами COVID-19 среди знакомых, друзей или родственников, наличие в анамнезе или на данный момент какого-либо психического расстройства, наличие хронических соматических заболеваний или избыточной массы тела [Özdin S, Özdin SB, 2020].
В общей сложности у 23,6% опрошенных жителей Турции были выявлены клинически значимые симптомы депрессии, а у 45,1% опрошенных — клинически значимые симптомы тревоги и/или ипохондрии (чрезмерной обеспокоенности своим здоровьем) [Özdin S, Özdin SB, 2020].
В этом исследовании факторами повышенного риска ухудшения психического состояния или развития психосоциальной дезадаптации на фоне пандемии COVID-19 оказались проживание в городе, принадлежность к женскому полу, наличие хронических соматических заболеваний, наличие психических расстройств в анамнезе или на текущий момент [Özdin S, Özdin SB, 2020].
Пандемия COVID-19 также спровоцировала у значительного числа психиатрических пациентов рецидивы или обострения, или ухудшение течения некоторых ранее имевшихся у них психических расстройств. К числу тех психиатрических пациентов, которые наиболее подвержены неблагоприятному влиянию стресса, связанного с пандемией COVID-19, относят страдающих обсессивно-компульсивным расстройством (ОКР) [Lee SA et al, 2020].
С чрезмерным, патологическим страхом заразиться SARS-CoV-2 или заболеть COVID-19, развившимся на фоне пандемии и связанного с нею дистресса, ассоциирована новая психопатологическая конструкция — так называемая коронафобия [Lee SA et al, 2020].
В ответ на очевидное усиление нужды в психиатрической помощи у пациентов с ОКР на фоне пандемии COVID-19 и на поступающие от пациентских организаций настойчивые призывы о помощи мировое психиатрическое сообщество создало специальную рабочую экспертную группу для разработки рекомендаций по оказанию помощи пациентам с ОКР в период пандемии. В нее вошли эксперты по ОКР из таких авторитетных международных психиатрических организаций, как Международный колледж расстройств обсессивно-компульсивного спектра (ICOCS), Исследовательская сеть обсессивно-компульсивных расстройств (OCRN) и Европейский колледж нейропсихофармакологии [Морозов ПВ, Петрова НН, 2020].
Результатом работы этой экспертной группы явился документ, который может служить основой для разработки практических рекомендаций по оказанию психиатрической помощи пациентам с ОКР в период пандемии COVID-19 [Морозов ПВ, Петрова НН, 2020].
Ряд экспертов высказывает опасение о том, что предпринимаемые правительствами разных стран мира с целью ограничения скорости распространения пандемии COVID-19 карантинные меры, в частности меры по социальному дистанцированию, изоляции и самоизоляции, — могут привести не только к неблагоприятным последствиям для психического здоровья и психологического комфорта популяции, но и к повышению риска самоубийств. К этому могут привести и вызванные пандемией COVID-19 неблагоприятные изменения в различных экономических, психосоциальных и связанных со здоровьем факторах риска суицидальности, таких как распространенность безработицы и бедности, снижение доступности и своевременности общемедицинской и психиатрической помощи, разрушение традиционных социальных связей и др. [Reger MA et al, 2020].
Неблагоприятные последствия пандемии COVID-19 для психического здоровья и психологического комфорта человеческой популяции в ближайшем будущем, скорее всего, будут только увеличиваться в связи с повседневной доступностью информации о росте количества зараженных и заболевших, об увеличении количества умерших от COVID-19, а также в связи с прогрессированием экономического спада, ростом уровня безработицы и бедности, снижением доступности и качества медицинской помощи из-за перераспределения ресурсов медицинской системы на борьбу с пандемией, а также в связи со снижением доступности социальной, психологической и религиозной поддержки, ограничением или разрушением традиционных социальных связей и контактов [Reger MA et al, 2020].
Также возможно, что круглосуточное освещение в средствах массовой информации всего мира беспрецедентных событий, связанных с пандемией COVID-19 и мерами борьбы с ней, принявшее в последние полгода характер настоящего «информационного шторма», — может служить дополнительным стрессовым фактором, или даже может непосредственно выступать триггером для развития психических расстройств или для проявления суицидальных тенденций, особенно у лиц с ранее имевшимися психическими проблемами или с предрасположенностью к их развитию [Reger MA et al, 2020].
Между тем все ведущие суицидологические теории подчеркивают ту ключевую роль, которую играет наличие работы, поддержание устойчивых социальных связей, возможность получения морально-психологической поддержки, в профилактике самоубийств [Reger MA et al, 2020].
В свете всего вышесказанного, в условиях пандемии COVID-19 и связанного с ней роста влияния таких факторов риска суицидальности, как безработица и бедность, одиночество, разрушение или ограничение социальных связей и контактов, необходима разработка активных мер по профилактике роста количества самоубийств. Эти меры должны учитывать определенные ограничения доступа к психиатрической и психотерапевтической помощи, накладываемые пандемией [Reger MA et al, 2020].
Несмотря на все те трудности, которые накладывают такие ограничения, пандемия COVID-19 открывает перед нами также уникальные возможности по совершенствованию системы оказания психиатрической, суицидологической и психотерапевтической помощи населению, по широкому внедрению телепсихиатрии. В полном соответствии с этим в США наблюдается тенденция к расширению использования телемедицины, и в частности телепсихиатрии, в ответ на трудности, связанные с пандемией COVID-19 и карантинными ограничениями [Reger MA et al, 2020].
Следует особо подчеркнуть, что официальный термин «социальное дистанцирование», несмотря на свое звучание, в действительности требует лишь поддержания определенного минимального физического расстояния между людьми для затруднения передачи вируса, а не социального или психоэмоционального дистанцирования между ними. В связи с этим людям рекомендуется предпринимать активные усилия для того, чтобы оставаться на связи с родственниками, друзьями, близкими и значимыми людьми и поддерживать личностно значимые для них отношения с помощью телефона, Интернета или видеоконференций. Особенно важно это для людей с психическими расстройствами или с повышенным риском самоубийства [Reger MA et al, 2020].
Уже давно существуют научно обоснованные, имеющие надежную доказательную базу мероприятия по профилактике самоубийств, которые могут осуществляться дистанционно (или даже разрабатывались именно таким образом, чтобы их можно было осуществлять дистанционно). Например, в рандомизированных клинических испытаниях (РКИ) было показано, что даже кратковременное контактное вмешательство, кратковременное проявление заботы, внимания и участия, такое как участливый телефонный звонок (телефонная аутрич-работа), SMS-сообщение или заботливое письмо от бывшего лечащего врача (например, токсиколога, интенсивиста или анестезиолога-реаниматолога) пациенту, выписанному из соответствующего отделения стационара после неудавшейся попытки самоубийства, с вопросом о том, как он себя чувствует и как у него дела, — существенно снижает вероятность повторных суицидальных попыток в ближайшие недели [Reger MA et al, 2020].
Аналогичным эффектом обладают телефонные звонки, SMS-сообщения и письма с проявлениями заботы, внимания и интереса к положению дел у пациента, склонного к суицидальным тенденциям и проявлениям, от семейного врача (участкового терапевта), от лечащего психиатра или психотерапевта и даже просто от близких, друзей, родственников [Reger MA et al, 2020].
С другой же стороны, наряду с тем очевидным негативным влиянием, которое оказывают сама пандемия COVID-19, экономический спад, рост безработицы и бедности, социальная изоляция и самоизоляция, снижение доступности общемедицинской и психиатрической помощи и связанный со всем этим дистресс на психическое здоровье популяции и на распространенность в ней суицидальных тенденций, — можно предположить и влияние противоположно направленного эффекта — так называемого эффекта «тянем лямку вместе» [Reger MA et al, 2020].
Этот эффект описывается так — члены некоего сообщества или популяции, совместно переживающие общий для них всех негативный социальный или психоэмоциональный опыт, могут оказывать более сильную, чем до того, социальную и психоэмоциональную поддержку, и могут формировать более тесные, чем до того, социальные связи. Так, в США показатели частоты самоубийств, согласно предыдущему историческому опыту, почти всегда снижались в ранние периоды после крупных национальных катастроф, таких как крушение башен-близнецов в Нью-Йорке 11 сентября 2001 года [Reger MA et al, 2020].
Поэтому можно предполагать, что бушующая ныне в мире пандемия COVID-19 может изменить по крайней мере у части людей сложившиеся ранее взгляды на ценность человеческой жизни и здоровья и на смерть, сделать для них сохранение собственной или чьей-то еще жизни и здоровья, а также поддержание прочных социальных связей более ценным, чем ранее, и тем самым может предотвратить некоторое количество самоубийств [Reger MA et al, 2020].
Истинные масштабы пандемии нового коронавируса SARS-CoV-2 и ее возможное долгосрочное влияние на психическое здоровье и психологическое благополучие населения Земли еще только предстоит оценить, поскольку пандемия еще далеко не закончилась [Figueroa CA, Aguilera A, 2020].
Тем не менее уже сейчас имеются данные, позволяющие связать как перенесенный тем или иным отдельно взятым индивидуумом COVID‐19, так и общий дистресс, связанный с обстановкой пандемии, карантинными ограничениями, экономическим спадом, безработицей или ухудшением материального положения огромного множества людей — с долгосрочными неблагоприятными последствиями для психического здоровья и психологического благополучия как популяции в целом, так и каждого отдельно взятого индивидуума, особенно лиц из числа исходно предрасположенных к развитию психических и психологических проблем [Figueroa CA, Aguilera A, 2020].
Все вышесказанное делает особенно актуальной в эпоху пандемии COVID-19 проблему оказания своевременной психиатрической, психологической и социальной помощи лицам с психическими расстройствами или с проблемами психосоциальной адаптации [Figueroa CA, Aguilera A, 2020].
Это обусловлено целым рядом факторов — как повышенной частотой контакта с носителями SARS-CoV-2 или больными COVID-19 и повышенной угрозой жизни и здоровью этих категорий работников, так и влиянием общего психического и психологического стресса, связанного с пандемией, влиянием информационных перегрузок, вынужденных переработок из-за нехватки врачей и персонала, дополнительных смен, в том числе ночных, вынужденной работы не по основной врачебной или сестринской специальности, а также влиянием психологической нагрузки, связанной с необходимостью принимать тяжелые и ответственные решения, например, проводить триаж (распределение пациентов на тех, кто нуждается в экстренной помощи и получит ее, тех, кто пока может подождать, и тех, кто мог бы получить помощь в более благоприятных условиях, но не получит ее из-за ограниченности доступных медицинских и технических ресурсов, и фактически может быть при этом обречен на смерть) [Zhang WR et al, 2020].
Анализ тех неблагоприятных последствий для психического здоровья и психологического здоровья медицинских работников, которые принесли с собой предыдущие эпидемические вспышки опасных коронавирусов SARS-CoV-1 и MERS, показал, что нежелательные последствия психического и психологического стресса, перенесенного этими людьми в период эпидемической вспышки, могут сохраняться в этой субпопуляции до трех лет после собственно вспышки, а возможно, и дольше [Zhang WR et al, 2020].
На основании этих данных, группа китайских исследователей, возглавляемая W. Zhang, предприняла масштабное исследование того, как повлияла сегодняшняя пандемия COVID-19 на состояние психического здоровья и внутреннего психологического комфорта работников сферы здравоохранения Китайской Народной Республики.
В этом исследовании приняли участие в общей сложности 2182 человека. Для опроса участников исследования использовались следующие шкалы и опросники: Шкала оценки тяжести бессонницы (Insomnia Severity Index, ISI), краткий вариант Опросника Здоровья Пациента, состоящий всего из 4 вопросов (Patient Health Questionnaire-4, PHQ-4), и обновленная ревизия Структурированного Списка Симптомов, состоящего из 90 вопросов (Structured symptom CheckList-90, Revised, SCL-90-R) [Zhang WR et al, 2020].
Авторы этого исследования сумели показать, что, по сравнению с немедицинскими работниками сферы здравоохранения (например, техническим и административным персоналом, в общей сложности 1255 человек), у медицинских работников (в общей сложности 927 человек) отмечается более высокая распространенность нарушений сна (38,4%, против 30,5% среди немедиков, p<0,01), симптомов тревоги (13%, против 8,5% среди немедиков, p<0,01), симптомов депрессии (12,2%, против 9,5% среди немедиков, p<0,04), симптомов соматизации (1,6%, против 0,4% среди немедиков, p<0,01), обсессивно-компульсивных симптомов (5,3%, против 2,2% среди немедиков, p<0,01) [Zhang WR et al, 2020].
Они также показали, что группами повышенного риска развития психических расстройств на фоне пандемии COVID-19 среди всех медработников оказались сотрудники женского пола, сотрудники, проживающие в сельской местности, особенно те из них, которые по причине транспортной и логистической удаленности их места проживания не имеют возможности быстрого доступа к близлежащим крупным центрам оказания высококвалифицированной медицинской помощи пациентам с COVID-19, или по причине плохого качества связи не имеют возможности быстро организовать получение квалифицированной дистанционной консультации от коллег, а также сотрудники с повышенным риском контакта с пациентами, инфицированными SARS-CoV-2 либо страдающими COVID-19 [Zhang WR et al, 2020].
 Другая международная группа исследователей, в которую вошли специалисты из Великобритании и Греции, недавно опубликовала подробный систематический обзор и метаанализ, также посвященный изучению вопроса о влиянии пандемии COVID-19 на психическое здоровье и психологическое благополучие сотрудников сферы здравоохранения. Они сумели идентифицировать в доступной им мировой научной литературе 13 качественных исследований, удовлетворяющих критериям отбора для включения в этот метаанализ, с общим числом опрошенных участников 33 062 человека [Pappa S et al, 2020].
Другая международная группа исследователей, в которую вошли специалисты из Великобритании и Греции, недавно опубликовала подробный систематический обзор и метаанализ, также посвященный изучению вопроса о влиянии пандемии COVID-19 на психическое здоровье и психологическое благополучие сотрудников сферы здравоохранения. Они сумели идентифицировать в доступной им мировой научной литературе 13 качественных исследований, удовлетворяющих критериям отбора для включения в этот метаанализ, с общим числом опрошенных участников 33 062 человека [Pappa S et al, 2020].
Распространенность симптомов тревоги среди медицинских работников оценивалась в 12 из 13 включенных в данный метаанализ исследований. Медианное значение распространенности тревожных симптомов по всему пулу участников этих исследований составило 23,2%. Распространенность симптомов депрессии среди медицинских работников изучалась в 10 из 13 исследований. При этом медианная распространенность депрессивных симптомов по всей выборке составила 22,8%. Распространенность нарушений сна среди медработников оценивалась в 5 из 13 исследований, медианное значение по всей выборке составило 38,9% [Pappa S et al, 2020].
В этом метаанализе также были выявлены значительные гендерные и профессиональные различия как в общей распространенности, так и в степени выраженности аффективных и тревожных симптомов среди медработников. А именно авторы показали, что среди медработников женского пола и общая распространенность, и степень выраженности аффективных и тревожных нарушений выше, чем среди медработников мужского пола, а у среднего медперсонала — выше, чем у врачей (см. таблицу 1) [Pappa S et al, 2020].
Кроме того, авторы также отметили высокий уровень синдрома профессионального выгорания (СПВ) у медработников на фоне пандемии COVID-19 и связанных с ней перегрузок, и выраженное негативное влияние СПВ на состояние психического здоровья медработников и на их внутренний психологический комфорт и качество жизни [Pappa S et al, 2020].
С другой же стороны, карбамазепин, вальпроаты, некоторые АП (например, клозапин, хлорпромазин) и некоторые АД (например, миртазапин, миансерин) могут проявлять миелотоксические свойства (в диапазоне от лейкопении и тромбоцитопении до жизнеопасного агранулоцитоза). Некоторые АП и АД, а также карбамазепин могут усиливать гиповолемию и имеющиеся электролитные нарушения, артериальную гипотензию, вызывать синдром неадекватной секреции антидиуретического гормона и т. д. Некоторые АП (например, сертиндол, зипрасидон, амисульприд, тиоридазин, трифлуоперазин) и некоторые АД (например, тразодон, трициклические антидепрессанты — ТЦА) способны изменять интервал QT на электрокардиограмме (ЭКГ) и повышать вероятность развития жизнеопасных сердечных аритмий, в том числе пируэтной желудочковой тахикардии (ЖТ) и фибрилляции желудочков (ФЖ) [Мосолов СН, 2020; Информация о взаимодействии…, 2020].
Далее, бензодиазепины и барбитураты могут снижать тонус скелетных мышц и угнетать активность дыхательного центра мозга, повышая тем самым риск развития пневмонии. Центральные антихолинергические препараты, такие как тригексифенидил, бипериден, неблагоприятно влияют на секрецию бронхиальной слизи и ее вязкость. Показано, что у пожилых пациентов эти препараты в 1,6–2,5 раза повышают риск развития пневмонии [Мосолов СН, 2020; Информация о взаимодействии…, 2020].
Согласно данным о лекарственных взаимодействиях психотропных препаратов со средствами терапии коронавирусной инфекции (COVID‐19), адаптированным С. Н. Мосоловым для РФ с сайта отделения клинической фармакологии Ливерпульского университета, к АД с низким риском или отсутствием риска взаимодействия с противовирусными препаратами относятся СИОЗС флувоксамин и флуоксетин, а также СИОЗСиН милнаципран и дулоксетин [Мосолов СН, 2020; Информация о взаимодействии…, 2020].
Вполне логично, что в условиях отсутствия в настоящее время клинически доступных противовирусных лекарств, которые бы обладали специфической эффективностью именно против нового коронавируса SARS-CoV-2, взгляды как ученых-исследователей, так и практикующих врачей обратились к исследованию эффективности и безопасности при COVID-19 уже доступных на мировом фармацевтическом рынке противовирусных лекарств, изначально создававшихся для борьбы с совсем другими вирусными инфекциями [Homolak J, Kodvanj I, 2020].
Таковы, например, комбинация ритонавир/лопинавир, изначально предназначавшаяся для лечения ВИЧ-инфекции, ацикловир, который эффективен против вирусов простого герпеса, или озельтамивир, который эффективен против вирусов гриппа типа А подтипа H1N1. Однако результаты клинических испытаний эффективности этих лекарств при лечении COVID-19 предсказуемо оказались достаточно разочаровывающими, поскольку в структуре белков и РНК вируса SARS-CoV-2 попросту нет тех молекулярных мишеней, на которые нацелено действие каждого из вышеупомянутых противовирусных средств [Homolak J, Kodvanj I, 2020].
Неудачи в клиническом применении уже существующих противовирусных лекарств для лечения COVID-19 закономерно вызвали необходимость в поиске принципиально иных подходов к лечению этой инфекции, в ожидании, пока появятся противовирусные лекарства, специфически эффективные именно против вируса SARS-CoV-2 [Homolak J, Kodvanj I, 2020].
Одним из методов, который изначально представлялся исследователям и практическим врачам весьма перспективным и многообещающим в лечении инфекции COVID-19, является иммуномодуляция. Действительно, уже достаточно давно было показано, что чрезмерно интенсивная воспалительная реакция организма на инфицирование вирусом SARS-CoV-2 и связанный с ней «цитокиновый шторм» — часто представляют даже бóльшую угрозу для жизни и здоровья пациента, чем собственно вирусное поражение клеток [Schön MP et al, 2020; Lenze EJ et al, 2020].
В рамках этого подхода, для лечения COVID-19 пытались и пытаются с различной степенью успешности применять различные иммуномодулирующие и противовоспалительные средства, например, синтетические глюкокортикоиды (дексаметазон, преднизолон, метилпреднизолон) [Mattos-Silva P et al, 2020; Tomazini BM et al, 2020], хлорохин или гидроксихлорохин [Gautam SS et al, 2020; Gautret P et al, 2020; Choudhary R, Sharma AK, 2020; Arshad S et al, 2020], индометацин [Marinella MA, 2020; Gomeni R et al, 2020], аспирин [Chow JH et al, 2020], колхицин [Altschuler EL, Kast RE, 2020; Lenze EJ et al, 2020], лефлуномид [Tsai YC, Tsai TF, 2020; Hu K et al, 2020; Wang M et al, 2020], микофенолат мофетил [Tsai YC, Tsai TF, 2020], талидомид [Tsai YC, Tsai TF, 2020], дапсон [Farouk A, Salman S, 2020; Altschuler EL, Kast RE, 2020], некоторые антигельминтные препараты с иммуномодулирующими свойствами, такие как левамизол или ивермектин [Choudhary R, Sharma AK, 2020; Uyaroğlu OA et al, 2020], некоторые антибиотики, тоже обладающие иммуномодулирующими свойствами, прежде всего азитромицин и некоторые другие макролиды [Gautret P et al, 2020; Choudhary R, Sharma AK, 2020; Arshad S et al, 2020], но также миноциклин и доксициклин [Farouk A, Salman S, 2020; Singh H et al, 2020; Gautam SS et al, 2020], некоторые фторхинолоны [Karampela I, Dalamaga M, 2020; Marciniec K et al, 2020], ингибиторы кальциневрина (циклоспорин, такролимус и др.) [Rudnicka L et al, 2020; Guisado-Vasco P et al, 2020; Liu С et al, 2020], различные антицитокиновые препараты (антагонист фактора некроза опухолей-альфа (ФНО-α) инфликсимаб, антагонист интерлейкина-6 (ИЛ-6) тоцилизумаб, антагонист интерлейкина-1 (ИЛ-1) анакинра и другие) [Schön MP et al, 2020], и даже препараты цитостатического ряда, такие как метотрексат [Caruso A et al, 2020; Seif F et al, 2020; Frohman EM et al, 2020], азатиоприн или его активный метаболит — 6-меркаптопурин [Schön MP et al, 2020], циклофосфамид [Revannasiddaiah S et al, 2020], флударабин [Ugurel OM et al, 2020], гидроксимочевина [Tsai YC, Tsai TF, 2020].
При этом довольно быстро было обнаружено, что некоторые из вышеупомянутых препаратов, помимо своего основного — противовоспалительного и иммуномодулирующего — эффекта, также оказывают угнетающее воздействие на репликацию самого вируса SARS-CoV-2, причем не только in vitro, но и in vivo. В частности, такой эффект был показан у хлорохина и гидроксихлорохина, а также у индометацина, азитромицина и некоторых других антибиотиков-макролидов [Homolak J, Kodvanj I, 2020; Schloer S et al, 2020].
Позднее было показано, что эффект угнетения репликации SARS-CoV-2 у таких препаратов, как хлорохин, гидроксихлорохин, индометацин, азитромицин и некоторые другие антибиотики группы макролидов, — по крайней мере частично опосредуется их способностью легко проникать внутрь лизосом в клетках (так называемым лизосомотропным действием), способностью их при этом изменять pH внутренней среды лизосом, а также функциональным ингибированием этими препаратами активности кислой сфингомиелиназы, фермента, который активен в основном в лизосомах [Homolak J, Kodvanj I, 2020; Schloer S et al, 2020].
Между тем некоторые АД, в том числе такие препараты группы селективных ингибиторов обратного захвата серотонина (СИОЗС), как флуоксетин и флувоксамин, — тоже обладают и выраженными лизосомотропными свойствами, и способностью сильно ингибировать функциональную активность кислой сфингомиелиназы. Эти их свойства были известны задолго до пандемии COVID-19, но привлекли внимание исследователей в плане изучения их пригодности для лечения этой болезни лишь совсем недавно [Kornhuber J et al, 2011; Homolak J, Kodvanj I, 2020; Schloer S et al, 2020].
Другим важным теоретическим обоснованием для изучения потенциальной пригодности именно флувоксамина для лечения инфекции COVID-19 является то, что, как мы уже упоминали ранее, вирус SARS-CoV-2 способен проникать в различные клетки организма, особенно в нейроны и глиальные клетки ЦНС, при помощи связывания с поверхностными сигма-1 рецепторами (механизма, альтернативного связыванию с его «обычным» сайтом проникновения — белком ангиотензин-превращающего фермента изотипа 2, ACE2) [Yesilkaya UH et al, 2020].
Между тем давно и хорошо известно, что флувоксамин является самым мощным из клинически доступных агонистов сигма-1 рецепторов (не только среди АД), с Ki всего 36 nM [Narita N et al, 1996; Cobos EJ et al, 2008; Albayrak Y, Hashimoto K, 2017; Беккер РА, Быков ЮВ, 2019 (a), (b)].
Как известно, информация о том, что вирус SARS-CoV-2 использует в качестве основного механизма своего проникновения в клетки организма человека связывание с поверхностным белком ACE2, первоначально послужила основанием для подозрений в том, что ингибиторы ангиотензин-превращающего фермента (ИАПФ) и блокаторы рецепторов ангиотензина 1-го типа (БРА1), вызывая контррегуляторное усиление экспрессии белка ACE2, потенциально могут ухудшать клиническое течение инфекции COVID-19, повышать вероятность развития тяжелых долгосрочных неблагоприятных последствий этой инфекции для здоровья (например, пневмосклероза), или даже могут повышать вероятность летального исхода, или же что они могут повышать вероятность заражения вирусом SARS-CoV-2 [McFee RB, 2020].
Эти опасения даже послужили в то время основанием для некоторых специалистов рекомендовать, по возможности, отменять ИАПФ или БРА1 у пациентов, получающих эти препараты по какому-либо поводу (например, по поводу гипертонической болезни или хронической сердечной недостаточности) в случае заражения этого пациента вирусом SARS-CoV-2 [McFee RB, 2020].
Однако в дальнейшем было показано, что эти опасения на самом деле беспочвенны, и что ни ИАПФ, ни БРА1 на самом деле не ухудшают течения COVID-19, не повышают вероятность развития тяжелых осложнений и долгосрочных неблагоприятных последствий этой инфекции для здоровья, и не оказывают отрицательного влияния на частоту летальных исходов при ней. Рекомендация отменять ИАПФ или БРА1 у пациентов, получающих эти препараты и заразившихся вирусом SARS-CoV-2 или заболевших COVID-19, была названа преждевременной (базирующейся либо на спекулятивных, умозрительных рассуждениях, либо на неполных и противоречивых предварительных клинических данных), ошибочной, научно необоснованной, вредной или даже опасной для здоровья и жизни пациентов [Flacco ME et al, 2020; Hippisley-Cox J et al, 2020; Rossi GP et al, 2020].
Более того, было показано, что на самом деле прием ИАПФ или БРА1 во время лечения от инфекции COVID-19, или продолжение их приема у тех пациентов, которые их уже принимали до заражения, может оказывать защитное влияние в отношении риска развития острого респираторного дистресс-синдрома (ОРДС), а также в отношении риска развития тяжелых сердечно-сосудистых и почечных осложнений COVID-19, и способно уменьшать интенсивность системного и местного (в легочной ткани) воспаления и выраженность «цитокинового шторма». Кроме того, обнаружилось также, что прием ИАПФ или БРА1 может оказывать защитное влияние в отношении собственно риска заражения вирусом SARS-CoV-2 при контакте [South AM et al, 2020; Zhang X et al, 2020; Javanmard SH et al, 2020; Seif F et al, 2020].
Рассуждая по аналогии, легко прийти к мысли о том, что если ИАПФ и БРА1, то есть прямые лиганды или индукторы экспрессии основного клеточного рецептора, через который вирус SARS-CoV-2 способен проникать в организм — белка ACE2, — оказались полезными в лечении инфекции COVID-19, то и агонисты сигма-1 рецепторов, такие как флувоксамин (то есть лиганды «второстепенных ворот» для этого вируса), тоже могут оказаться потенциально полезными в лечении этой инфекции, и заслуживают изучения в этом качестве [Lenze EJ et al, 2020].
Кроме того, показано, что в экспериментах на животных сигма-1 агонисты, и в первую очередь самый мощный из них — флувоксамин, — эффективно уменьшают системное и местное воспаление, ограничивают секрецию воспалительных цитокинов и предотвращают развитие «цитокинового шторма», уменьшая тем самым вероятность неблагоприятного исхода при экспериментальном сепсисе. Этот эффект опосредуется взаимодействием активированных сигма-1 рецепторов с различными внутриклеточными мишенями, в том числе с одним из важных датчиков внутриклеточного стресса в эндоплазматическом ретикулуме — так называемым «инозитол-опосредованным ферментом 1α» (IRE1) [Rosen DA et al, 2019].
Еще одним теоретическим обоснованием для прицельного изучения потенциальной эффективности именно флувоксамина в лечении инфекции COVID-19 является то, что он, в отличие от всех других СИОЗС и прочих АД, клинически значимо ингибирует катаболизм в печени как эндогенного, так и экзогенного (принимаемого перорально) мелатонина, и значительно повышает концентрацию мелатонина в плазме крови [Demisch K, 1987; von Bahr С et al, 2000; Härtter S et al, 2000; 2001; Беккер РА, Быков ЮВ, 2019 (a), (b)].
Между тем положительное влияние экзогенного (перорально назначаемого) мелатонина на течение как новейшей инфекции COVID-19, так и ряда других, давно известных человечеству, вирусных инфекций, типа гриппа, которое связывают с мощными антиоксидантными, анти-свободнорадикальными, противовоспалительными и иммуномодулирующими свойствами этого гормона — хорошо известно. Ныне пероральный мелатонин входит во многие национальные протоколы и рекомендации по лечению COVID-19 [Anderson G, Reiter RJ, 2020; Zhang R et al, 2020; Giménez VM et al, 2020].
Существует даже предположение о том, что бóльшая в среднем тяжесть течения инфекции COVID-19 и более высокий риск тяжелых осложнений и летальных исходов при этой болезни у лиц пожилого и старческого возраста, по сравнению с более молодыми пациентами, — могут быть в значительной степени обусловлены именно выраженным снижением секреции эндогенного мелатонина с возрастом, наряду с влиянием других неблагоприятных факторов старения [Öztürk G et al, 2020].
В свете этого способность флувоксамина значительно повышать концентрацию эндогенного мелатонина в плазме крови и увеличивать биодоступность экзогенного (перорально принимаемого) мелатонина — может быть очень выгодным свойством именно этого АД при лечении пациентов с инфекцией COVID-19 [Lenze EJ et al, 2020; García IG et al, 2020].
Кроме того, флувоксамин обладает выраженными нейропротективными и кардиопротективными свойствами, проявляющимися в разных клинических ситуациях и в разных экспериментальных моделях (например, в модели ишемии и последующей реперфузии мозга или миокарда, в модели экспериментального аутоиммунного воспаления ЦНС, в модели нейротоксичности, обусловленной воздействием МДМА, кетамина, фенциклидина, бета-амилоида и др.) [Беккер РА, Быков ЮВ, 2019 (a)].
С учетом выраженных нейротропных (нейроинвазивных), кардиотоксических и нейротоксических свойств вируса SARS-CoV-2, выраженная нейропротективная и кардиопротективная активность флувоксамина также может иметь значение при лечении пациентов с COVID-19 этим препаратом.
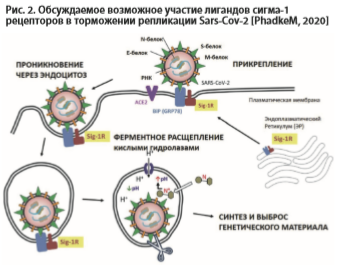
Репликация коронавирусов происходит в модифицированном мембранном комплексе, полученном из эндоплазматического ретикулума. Соответственно, влияние на ремоделирование эндоплазматического ретикулума вирусом может иметь решающее значение для выяснения новых терапевтических противовирусных подходов. Рецептор sigma-1 (Sig-1R) — это управляемый лигандом мембранный белок-шаперон — действует как модулятор стресса в эндоплазматическоме ретикулуме. Многие перепрофилированные лекарства, включенные в схемы терапии пациентов с COVID-19, часто идентифицируются как Лиганды Sig-1R in vitro. Sig-1R регулирует ключевые механизмы адаптивного стрессового ответа клеток-хозяев и принимает участие в ранних стадиях репликации вируса. Таргетирование Sig-1R, как ожидается, не приведет к резкому снижению установленной вирусной репликации, но оно может помешать ранним этапам индуцированного вирусом перепрограммирования клеток-хозяев, помочь замедлить течение инфекции, предотвратить обострение заболевания и/или создать временное окно для созревания защитного иммунного ответа. Препараты на основе Sig-1R могут принести пользу не только в качестве раннего вмешательства, профилактики, но и в качестве адъювантной терапии [Phadke M. 2020].
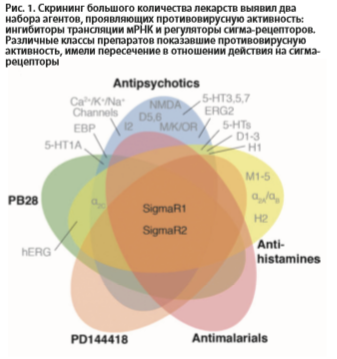
Основная проблема лигандов сигма-рецепторов в том, что противовирусный эффект у них развивается в токсичных или близким к токсичным для клеток человека концентрациях.
В то же время известен агент, обладающий высоким сродством к сигма-рецепторам Ki(nM)=17 и одновременно высоким терапевтическим индексом, разрешающим прием его в высоких (до 300 мг/сут) дозах. Речь идет о флувоксамине [S.B. Smith, 2017].
 Протокол исследования
Протокол исследования
Детально описанные нами в предыдущем разделе теоретические предпосылки для возникновения интереса к изучению потенциальной эффективности флувоксамина в лечении COVID-19 послужили мотивацией для группы авторов из Вашингтона, США, предпринять первое пилотное исследование эффективности и безопасности флувоксамина в лечении этой новой инфекции [Lenze EJ et al, 2020].
Авторы этого исследования поставили своей задачей выяснить, может ли флувоксамин, назначаемый в качестве раннего средства лечения пациентам с легким течением инфекции COVID-19, уменьшить вероятность перехода этого заболевания в более тяжелую форму или полностью предотвратить такое развитие событий [Lenze EJ et al, 2020].
Цитируемое нами исследование являлось по своему дизайну двойным слепым плацебо-контролируемым, рандомизированным клиническим исследованием (РКИ). В нем сравнивалась эффективность и безопасность флувоксамина и плацебо в предотвращении неблагоприятных исходов и осложнений COVID-19 у взрослых амбулаторных пациентов с лабораторно (методом полимеразной цепной реакции — ПЦР) подтвержденной инфекцией вирусом SARS-CoV-2. Оно получило одобрение этической комиссии и институционального Наблюдательного совета Вашингтонского университета и проводилось в строгом соответствии с Хельсинкской декларацией [Lenze EJ et al, 2020].
Набор пациентов-добровольцев для участия в этом РКИ осуществлялся с апреля по август 2020 года. Для того, чтобы не подвергать как участников исследования, так и персонал клиники дополнительному риску заражения вирусом SARS-CoV-2, для этого исследования был разработан инновационный, полностью дистанционный (бесконтактный) телемедицинский протокол [Lenze EJ et al, 2020].
В это РКИ включались взрослые амбулаторные пациенты обоего пола (от 18 лет, без ограничения сверху по возрасту) с подтвержденной методом ПЦР инфекцией вирусом SARS-CoV-2, у которых наблюдались легкие симптомы COVID-19 в течение как минимум 7 дней, предшествующих рандомизации. Критерии исключения из исследования включали среднетяжелое или тяжелое течение инфекции COVID-19, при котором требовалась госпитализация, амбулаторное назначение кислородной поддержки, либо при котором насыщение артериальной крови пациента кислородом составляло менее 92% при дыхании атмосферным воздухом, на момент рандомизации, а также, наоборот, бессимптомное течение инфекции SARS-CoV-2 [Lenze EJ et al, 2020].
Другими критериями исключения из исследования были наличие у кандидата предсуществующих тяжелых бронхолегочных заболеваний (хронической обструктивной болезни легких — ХОБЛ, легочного фиброза, легочной гипертензии), декомпенсированного цирроза печени, тяжелой хронической сердечной недостаточности (ХСН) III или IV функционального класса, а также наличие у кандидата выраженной иммуносупрессии (получение химиотерапии по поводу злокачественных новообразований, получение иммуносупрессивной терапии по поводу трансплантации органов, трансплантации костного мозга или по поводу аутоиммунных и ревматических заболеваний, прием высоких доз глюкокортикоидов по любой причине) [Lenze EJ et al, 2020].
В конечном итоге в этом РКИ приняли участие 152 взрослых амбулаторных пациента обоего пола с лабораторно подтвержденной инфекцией SARS-CoV-2 и с легкими симптомами COVID-19. Средний возраст участников составлял 46 лет. Все пациенты были стратифицированы на четыре возрастные когорты (от 18 до 44 лет, от 45 до 54 лет, от 55 до 64 лет и старше 65 лет). Рандомизация проводилась раздельно в каждой из возрастных когорт. В общей сложности 80 пациентов попали в группу флувоксамина, и 72 пациента — в группу плацебо. При этом авторы исследования тщательно следили за максимально возможным совпадением всех демографических и клинических характеристик пациентов как в группе плацебо, так и в группе флувоксамина [Lenze EJ et al, 2020].
В частности, средний уровень насыщения артериальной крови кислородом при дыхании атмосферным воздухом (важнейший показатель степени поражения легких при COVID-19) на момент рандомизации не отличался в группах плацебо и флувоксамина, и в обеих группах составлял 97% [Lenze EJ et al, 2020].
Затем в течение 2 последующих дней доза флувоксамина в группе активного лечения постепенно увеличивалась до 100 мг 2 раза в сутки (200 мг/сут), если позволяла переносимость. После 2 дней приема этой дозы — дозу флувоксамина в группе активного лечения снова увеличивали до 100 мг 3 раза в сутки (300 мг/сут), если позволяла переносимость. В группе плацебо, для обеспечения адекватного ослепления, аналогичным образом проводилось поэтапное увеличение дозы и кратности приема плацебо [Lenze EJ et al, 2020].
Желаемая конечная доза флувоксамина 300 мг/сут была выбрана авторами этого РКИ, исходя из доступных в литературе данных об аффинности флувоксамина in vitro к человеческим сигма-1 рецепторам и о степени занятости этих рецепторов in vivo при приеме различных доз флувоксамина, по данным позитронно-эмиссионной томографии (ПЭТ) [Lenze EJ et al, 2020].
Эту дозу флувоксамина или плацебо пациенты должны были продолжать принимать в двойном слепом режиме на протяжении 15 дней, после чего пациентам из группы активного лечения предоставлялась возможность либо прекратить дальнейший прием флувоксамина, либо продолжить его уже в открытом режиме на протяжении еще 6 дней. Стоит отметить, что введение 6-дневной открытой фазы исследования после завершения основной фазы РКИ не предусматривалось первоначальным протоколом исследования [Lenze EJ et al, 2020].
Первичной конечной точкой в этом РКИ служило наличие или отсутствие ухудшения клинической картины COVID-19 за период приема, соответственно, флувоксамина или плацебо. Клиническое ухудшение определялось авторами этого РКИ как проявление одышки, или вынужденная госпитализация пациента по поводу одышки или по поводу развития пневмонии, или снижение насыщения артериальной крови кислородом при дыхании атмосферным воздухом ниже 92%, или появление необходимости в дополнительной кислородной поддержке для обеспечения насыщения крови кислородом на уровне 92% и выше [Lenze EJ et al, 2020].
Авторы данного РКИ показали, что ухудшение клинического течения COVID-19 не наблюдалось ни у одного из 80 пациентов в группе флувоксамина (0%). В то же время оно наблюдалось у 6 из 72 (8,3%) пациентов в группе плацебо. Абсолютная разница шансов клинического ухудшения между группами, по данным статистического анализа, составила 8,7% (доверительный интервал 95%, диапазон от 1,8% до 16,4%, p=0,009) [Lenze EJ et al, 2020].
В группе плацебо момент начала клинического ухудшения отмечался в период от 1 до 7 дней после рандомизации, или от 3 до 12 дней после появления первых симптомов COVID-19. Это в целом совпадает с тем, что мы сегодня знаем о типичном течении инфекции COVID-19 (необходимость в госпитализации или клиническое ухудшение обычно наступает после 8–10 дней первоначально легких или среднетяжелых симптомов болезни) [Lenze EJ et al, 2020].
Четырем из шести пациентов в группе плацебо, у которых наступило ухудшение клинического течения COVID-19, потребовалась госпитализация. Продолжительность пребывания в больнице в этих случаях колебалась от 4 дней до 21 дня. Одному из этих пациентов потребовалась ИВЛ в течение 10 суток [Lenze EJ et al, 2020].
В группе плацебо также чаще отмечалось развитие пневмонии (6 человек, против 3 человек в группе флувоксамина), развитие одышки или затруднения дыхания (4 человека, против 2 человек в группе флувоксамина) [Lenze EJ et al, 2020].
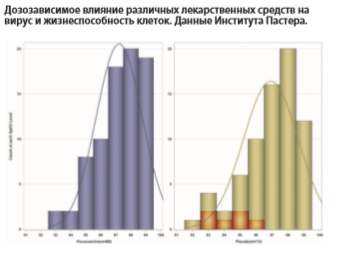
Ниже мы приводим колоколообразный график распределения исходной (до начала исследования) величины насыщения артериальной крови кислородом при дыхании атмосферным воздухом в обеих группах — флувоксамина и плацебо. Как можно видеть из этого графика, медианная величина исходного насыщения артериальной крови кислородом достоверно не различалась в обеих группах (97% в группе флувоксамина, 97% в группе плацебо). Также на этом графике видно, что все шесть случаев клинического ухудшения течения COVID-19 в группе плацебо (отмечены на графике оранжевым цветом) — приходятся на левую часть кривой, то есть — на тех пациентов, у которых исходное насыщение крови кислородом хотя и было выше допустимой для отбора в данное РКИ границы (92%), но было ниже или равно 96%, — иначе говоря, на исходно более тяжелых пациентов [Lenze EJ et al, 2020].
В то же время в группе, получавшей плацебо (72 человека), было зарегистрировано 6 ПЭ, которые были расценены авторами данного РКИ как серьезные (в частности, один эпизод сильной головной боли, потребовавший визита пациента в отделение экстренной помощи стационара), и 12 ПЭ, расцененных авторами данного РКИ как легкие [Lenze EJ et al, 2020].
Интересно отметить, что ПЭ со стороны ЖКТ, такие как тошнота, рвота, диарея, развивались в группе плацебо чаще, чем в группе флувоксамина (5 человек, против 1 человека в группе флувоксамина) [Lenze EJ et al, 2020].
При этом флувоксамин, в отличие от многих других упоминавшихся нами в данной статье иммуномодулирующих и противовоспалительных препаратов, ранее изучавшихся или изучаемых в настоящее время как перспективные средства для лечения COVID-19, весьма безопасен и хорошо переносится, и имеет низкий уровень ПЭ. В частности, ПЭ со стороны ЖКТ в описываемом нами РКИ отмечались в группе плацебо вдвое чаще, чем в группе флувоксамина.
Вместе с тем следует иметь в виду, что данное РКИ является пилотным. Оно имеет определенные ограничения, связанные, в частности, с тем, что в нем участвовало сравнительно небольшое количество участников (всего 152 человека) и только из одной географической области (федеральный округ Вашингтон в США). Сами авторы цитируемого нами РКИ подчеркивают, что выводы их исследования о возможной эффективности флувоксамина в качестве средства предотвращения тяжелого течения или средства смягчения течения COVID-19 следует воспринимать как предварительные, и что они нуждаются в воспроизведении на более крупных и более гетерогенных (и по географическому местоположению, и по этническому составу, и по тяжести течения и т.д.) выборках пациентов с COVID-19.
В то же время, учитывая ограниченность имеющихся сегодня терапевтических опций для лечения COVID-19, плохую переносимость многих из них, а также резкое повышение актуальности проблемы депрессий, тревожных состояний, ПТСР и ОКР в популяции, страдающей от пандемии COVID-19 (то есть повышение актуальности основных показаний к назначению флувоксамина, согласно его инструкции по применению), эти выводы, сколь бы предварительными они ни были, заслуживают особого внимания — и клинического применения уже сегодня.
Авторы цитируемого нами РКИ также указывают, что их собственное исследование мотивировалось гипотезой о том, что флувоксамин может быть эффективен в лечении COVID-19 вследствие своего агонизма к сигма-1 рецепторам (S1R) и угнетающего влияния на секрецию воспалительных цитокинов через внутриклеточный сигнальный каскад S1R-IRE1. Если эта гипотеза верна, то положительное действие флувоксамина на клиническое течение COVID-19 подобно действию при этой патологии других антицитокиновых и противовоспалительных препаратов, таких как колхицин или гидроксихлорохин.
Возможные альтернативные или дополнительные механизмы полезного действия флувоксамина на клиническое течение COVID-19 включают в себя его прямое противовирусное действие (угнетение проникновения вируса SARS-CoV-2 в клетку) за счет прямого связывания с «альтернативными воротами проникновения вируса», каковыми являются сигма-1 рецепторы (S1R), а также за счет лизосомотропного действия флувоксамина и функционального угнетения им активности кислой сфингомиелиназы, за счет его влияния на pH внутри лизосом, за счет модулирующего влияния флувоксамина на процессы аутофагии через сигнальный путь S1R-IRE1, или за счет угнетения им агрегации тромбоцитов и предотвращения свойственной COVID-19 гиперкоагуляции, или за счет повышения содержания эндогенного мелатонина в плазме крови и повышения биодоступности экзогенного мелатонина (полезность мелатонина при COVID-19 уже показана), а также, возможно, за счет каких-то других его эффектов, например нейро- и кардиопротективного.
Нельзя при этом сбрасывать со счетов и основное клиническое действие флувоксамина — антистрессовое, антидепрессивное и противотревожное, поскольку показано, что депрессия, тревога и хронический стресс сами по себе являются независимыми факторами риска тяжелого течения инфекции COVID-19.
Важными потенциальными преимуществами применения флувоксамина как средства амбулаторного лечения COVID-19 являются его высокая безопасность, хорошая переносимость, низкий уровень ПЭ (особенно по сравнению с такими препаратами, как, например, гидроксихлорохин или азитромицин), широкая доступность этого препарата на рынке, его низкая стоимость (особенно по сравнению с такими, например, препаратами, как инфликсимаб или анакинра), возможность его перорального приема (в отличие от многих антицитокиновых препаратов, которые требуют исключительно внутривенного введения).
В отличие от многих других альтернативных иммуномодуляторов, предлагавшихся для лечения COVID-19, таких как хлорохин, гидроксихлорохин, азитромицин, а также в отличие от ТЦА и от некоторых других СИОЗС (например, от эсциталопрама и циталопрама) — флувоксамин не способствует удлинению интервала QT на ЭКГ. Поэтому он не обладает аритмогенным или кардиотоксическим действием. Это особенно важно при лечении пожилых пациентов или пациентов с предсуществующими заболеваниями сердца.
Вместе с тем при сочетанном применении флувоксамина с другими лекарственными препаратами следует всегда помнить и учитывать, что флувоксамин является мощным ингибитором изоферментов цитохрома печени P450 1А2 и 2С19. Поэтому он способен значительно повышать концентрации в плазме крови тех лекарств, которые метаболизируются всецело или в значительной степени при помощи этих изоферментов (например, теофиллина и аминофиллина). Однако большинство применяемых сегодня в медицине лекарственных препаратов метаболизируются всецело или в основном при помощи изофермента P450 2D6.
В свете представленных данных, на сегодняшний день представляется оправданным использовать флувоксамин как антидепрессант первого выбора для терапии депрессии и ОКР у пациентов с риском заражения COVID-19. Ожидания от терапии включают: улучшение психического состояния этих пациентов, уменьшение тревоги, депрессии, нарушений сна, проявления ОКР, а также снижение рисков развития осложнений при COVID-19.
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№06 2020
Пандемия COVID-19: актуальные вызовы времени, а также новейшие данные к вопросу рационального выбора психофармакотерапии у пациентов с SARS-CoV-2 №06 2020
Номера страниц в выпуске:8-24
Резюме
Бушующая в последний год во всем мире пандемия COVID-19 привела к резкому ухудшению психического здоровья и психологического благополучия всей человеческой популяции. Этому способствует множество факторов: как выраженные нейроинвазивные и нейротоксические свойства самого вируса SARS-CoV-2, так и, в еще большей степени, выраженный дистресс, который испытывают многие люди и вследствие самой пандемии, и вследствие мер борьбы с ней, экономического спада, роста безработицы и бедности.
Это резко актуализировало в последний год проблему депрессивных, тревожных и связанных со стрессом расстройств в популяции, в том числе среди таких групп риска, как пожилые люди, пациенты с хроническими соматическими и/или психическими заболеваниями, медицинские работники. Кроме того, отсутствие в настоящее время эффективных специфических средств лечения COVID-19 поставило перед врачами и исследователями проблему поиска потенциально эффективных против этой инфекции лекарств среди уже утвержденных к клиническому применению по другим показаниям препаратов (так называемого репозиционирования лекарств).
В данной статье мы показываем, почему большой интерес и ученых, и практиков при лечении COVID-19 вызывают подходы, основанные на иммуномодуляции, в том числе — на иммуномодуляции через сигма-1 рецепторы клеток. Затем мы представляем читателю результаты первого пилотного рандомизированного клинического исследования (РКИ), посвященного изучению возможной эффективности и безопасности применения флувоксамина (в России известного как препарат Рокона) в профилактике тяжелого течения и неблагоприятного исхода инфекции COVID-19, а также обсуждаем возможные альтернативные механизмы его положительного действия при этой патологии.
Ключевые слова: COVID-19, SARS-CoV-2, пандемия, коронавирус, дистресс, психическое здоровье, депрессия, тревога, флувоксамин, Рокона, сигма-1 рецептор, аутофагия, кислая сфингомиелиназа, мелатонин.
Для цитирования: Н.Н. Петрова, П.В. Морозов, А.В. Маркин, Р.А. Беккер, Ю.В. Быков. Пандемия COVID-19: актуальные вызовы времени, а также новейшие данные к вопросу рационального выбора психофармакотерапии у пациентов с SARS-CoV-2. Психиатрия и психофармакотерапия. 2020; 6: 8–24.
Бушующая в последний год во всем мире пандемия COVID-19 привела к резкому ухудшению психического здоровья и психологического благополучия всей человеческой популяции. Этому способствует множество факторов: как выраженные нейроинвазивные и нейротоксические свойства самого вируса SARS-CoV-2, так и, в еще большей степени, выраженный дистресс, который испытывают многие люди и вследствие самой пандемии, и вследствие мер борьбы с ней, экономического спада, роста безработицы и бедности.
Это резко актуализировало в последний год проблему депрессивных, тревожных и связанных со стрессом расстройств в популяции, в том числе среди таких групп риска, как пожилые люди, пациенты с хроническими соматическими и/или психическими заболеваниями, медицинские работники. Кроме того, отсутствие в настоящее время эффективных специфических средств лечения COVID-19 поставило перед врачами и исследователями проблему поиска потенциально эффективных против этой инфекции лекарств среди уже утвержденных к клиническому применению по другим показаниям препаратов (так называемого репозиционирования лекарств).
В данной статье мы показываем, почему большой интерес и ученых, и практиков при лечении COVID-19 вызывают подходы, основанные на иммуномодуляции, в том числе — на иммуномодуляции через сигма-1 рецепторы клеток. Затем мы представляем читателю результаты первого пилотного рандомизированного клинического исследования (РКИ), посвященного изучению возможной эффективности и безопасности применения флувоксамина (в России известного как препарат Рокона) в профилактике тяжелого течения и неблагоприятного исхода инфекции COVID-19, а также обсуждаем возможные альтернативные механизмы его положительного действия при этой патологии.
Ключевые слова: COVID-19, SARS-CoV-2, пандемия, коронавирус, дистресс, психическое здоровье, депрессия, тревога, флувоксамин, Рокона, сигма-1 рецептор, аутофагия, кислая сфингомиелиназа, мелатонин.
Для цитирования: Н.Н. Петрова, П.В. Морозов, А.В. Маркин, Р.А. Беккер, Ю.В. Быков. Пандемия COVID-19: актуальные вызовы времени, а также новейшие данные к вопросу рационального выбора психофармакотерапии у пациентов с SARS-CoV-2. Психиатрия и психофармакотерапия. 2020; 6: 8–24.
The COVID-19 pandemic: challenges of our times, with discussion on the latest data regarding an issue of rational psychopharmacotherapy choices in patients with SARS-CoV-2 infection
N.N. Petrova1, P.V. Morozov2, A.V. Markin3, R.A. Bekker4, Yu.V. Bykov51 Saint Petersburg State University. 199034, Russian Federation, Saint Petersburg, Universitetskaia nab., d. 7/9. petrova_nn@mail.ru
2 N.I.Pirogov Russian National Research Medical University of the Ministry of Health of the Russian Federation. 117997, Russian Federation, Moscow, ul. Ostrovitianova, d. 1;
3 «Sotex Pharmacological Company»;
4 David Ben-Gurion University in Negev.8410501, Israel, Be'er Sheva;
5 Stavropol State Medical University of the Ministry of Health of the Russian Federation. 355017, Russian Federation, Stavropol, ul. Mira, d. 310.
Abstract
The COVID-19 pandemic that has raged around the world over the past year has led to a sharp deterioration in the mental health and psychological well-being of the entire human population. This is facilitated by many factors: both the pronounced neuroinvasive and neurotoxic properties of the SARS-CoV-2 virus itself, and, to an even greater extent, the pronounced distress that many people experience both as a result of the pandemic itself and as a result of governmental measures to combat it, leading to profound economic recession, mass unemployment and poverty.
These factors, acting together, have sharply raised the incidence of depressive, anxiety and stress-related disorders in the population, especially among some risk groups, such as the elderly people, patients with chronic somatic and / or mental illnesses, and healthcare professionals. In addition, the current lack of effective specific treatments for COVID-19 has posed a challenge for doctors and researchers to search for potentially effective drugs against this infection among drugs which were already approved for clinical use for other indications (so-called repositioning of drugs).
In this article, we show the reader, why various approaches based on immunomodulation, including immunomodulation through sigma-1 cellular receptors, are of great interest to both scientists and practitioners working in the field of COVID-19 treatment. Then we present to the reader the results of the first pilot randomized clinical trial devoted to the study of the possible efficacy and safety of the use of fluvoxamine (which in Russia is known as Rocona) in the prevention of severe complications and unfavorable outcome of COVID-19 infection. We also discuss possible alternative (non sigma-1 receptor related) mechanisms of fluvoxamine’s efficacy in the prevention of COVID-19 complications.
Keywords: COVID-19, SARS-CoV-2, pandemic, coronavirus, distress, mental health, depression, anxiety, fluvoxamine, Rocona, sigma-1 receptor, autophagy, acidic sphingomyelinase, melatonin
For citation: Petrova N.N., Morozov P.V., Markin A.V., Bekker R.A., Bykov Yu.V. The COVID-19 pandemic: challenges of our times, with discussion on the latest data regarding an issue of rational psychopharmacotherapy choices in patients with SARS-CoV-2 infection. Psychiatry and psychopharmacotherapy. 2020; 6: 8–24.
Введение. Актуальность проблемы
Ассоциация перенесенных вирусных инфекций с рецидивами или с манифестациями de novo различных психических заболеваний, прежде всего — с депрессивными и тревожными расстройствами — известна давно [Gale SD et al, 2018].Не менее хорошо известно, что разные вирусы обладают различной способностью вызывать подобного рода психические осложнения. Это во многом связано с наличием или отсутствием у конкретного вируса нейротропных свойств (то есть способности непосредственно поражать нервные или глиальные клетки, вызывая тем самым вирусный энцефалит), или способности провоцировать выраженную системную воспалительную реакцию организма и связанный с ней «цитокиновый шторм», либо служить триггером для развития разнообразных аутоиммунных реакций на мозговую ткань. В частности, такого рода психические осложнения часто описываются после перенесенного гриппа, других острых респираторных вирусных инфекций (ОРВИ), в том числе — вызванных различными коронавирусами, а также после перенесенной кори, опоясывающего лишая, инфекционного мононуклеоза, острого гепатита А, эпидемического паротита, у пациентов с хроническим носительством вируса иммунодефицита человека (ВИЧ) или вирусов гепатита В и/или С, и так далее [Gale SD et al, 2018].
Более того, показано, что внутриутробно перенесенная вирусная инфекция, причем даже не из числа явно тератогенных, таких как краснуха (например, заболевание матери гриппом или банальным ОРВИ в период беременности, причем необязательно в первом триместре), — может в дальнейшем создавать у ребенка предрасположенность к развитию депрессивных и тревожных расстройств в более старшем, подростковом или уже взрослом возрасте [Schnittker J, 2020].
Ассоциация депрессивных расстройств, независимо от их генеза или от первоначального их триггера, с выраженной реактивацией латентных вирусов герпес-группы (вирусов простого герпеса различных подтипов, цитомегаловируса, вируса Эпштейна-Барр), носителями которых являются до 90% популяции, а также с реактивацией так называемых «эндогенных ретровирусов» или ретротранспозонов, встроенных в наш геном, даже побудила турецкого исследователя Турхана Канли выдвинуть спорную и дискуссионную гипотезу о том, что клиническая депрессия, возможно, является своеобразным «герпетическим энцефалитом низкой интенсивности» [Canli T, 2014; 2019].
Не является исключением из общего правила о высокой частоте психических осложнений (прежде всего — депрессивных и тревожных состояний), после перенесенных вирусных инфекций, и новая коронавирусная инфекция, впервые обнаруженная в 2019 году, получившая название COVID-19 (сам же вирус, вызывающий эту болезнь, получил название SARS-CoV-2) [Ahorsu DK et al, 2020; Le HT et al, 2020; Wadoo O et al, 2020].
Более того, сегодня имеются основания утверждать, что вредное влияние нынешней пандемии COVID-19 на психическое здоровье популяции — существенно больше, чем у многих других упомянутых выше вирусных инфекций. Причины этого мы рассмотрим ниже.
Вирус SARS-CoV-2 как высоконейротропный вирус
Перенесенный COVID-19, даже в том случае, если болезнь протекала в легкой ОРЗ-подобной форме, без присоединения пневмонии и других органных осложнений, часто оставляет после себя целый ряд психических и неврологических симптомов, таких как длительно сохраняющаяся постинфекционная астения, слабость, вялость, утомляемость, нарушения сна, депрессивные и тревожные состояния. Это явление даже получило в научной литературе специальное наименование — «пост-ковидный синдром» [Yesilkaya UH et al, 2020].Одной из важных причин, обуславливающих столь высокую частоту неблагоприятных психических и неврологических последствий перенесенного COVID-19, является весьма выраженная нейротропность вируса SARS-CoV-2 (более выраженная, чем у других ранее известных коронавирусов, включая его ближайшего родственника SARS-CoV-1, или «вирус атипичной пневмонии»). Этот новый коронавирус способен непосредственно проникать в нейроны и клетки глии в ЦНС, заражать их и активно размножаться в них, вызывая их апоптотическую гибель и запуская каскад реактивного воспаления в мозге [Yesilkaya UH et al, 2020].
Особенно интересно отметить, что, помимо своего основного и уже хорошо известного механизма проникновения в клетки самых различных тканей — связывания с мембранным белком ангиотензин-превращающего фермента изотипа 2 (белком ACE2), который обильно экспрессируется не только в легочной ткани, но и в сосудах, в миокарде, в нервной системе, в ЖКТ, почках, надпочечниках и других тканях, вирус SARS-CoV-2 способен использовать и другой механизм проникновения в мозг — связывание с некоторыми белками-шаперонами нейронов и глиальных клеток, а именно — с так называемыми «сигма-1» и «сигма-2» рецепторами [Yesilkaya UH et al, 2020].
Еще один возможный (если исходить из результатов экспериментов на животных — весьма частый) путь проникновения SARS-CoV-2 в головной мозг — это через его способность связываться с белком нейропилин-1, обильно экспрессируемым как на поверхности клеток обонятельного эпителия слизистой носа, так и на поверхности нервных клеток, особенно в тех областях мозга, которые имеют отношение к функциям обоняния и вкуса. При этом может наблюдаться восходящее инфицирование, благодаря близости носовых раковин, обонятельной луковицы и головного мозга. Этот механизм проникновения вируса хорошо объясняет такой частый симптом COVID-19, как гипосмия или полная аносмия (снижение или полная утрата обоняния) и иногда также гипогевзия или полная агевзия (снижение или полная утрата вкусовой чувствительности) [Davies J et al, 2020].
Последствия инфицирования головного мозга вирусом SARS-CoV-2 порой бывают весьма тяжелыми, и отнюдь не ограничиваются вышеописанным «постковидным синдромом». Так, в частности, в литературе описаны случаи возникновения синдрома Гийена-Барре на фоне заболевания COVID-19, а также случаи манифестации болезни Паркинсона после перенесенного COVID-19 [Chaná-Cuevas P et al, 2020; Nanda S et al, 2020].
В литературе также описаны множественные случаи COVID-ассоциированной энцефалопатии, в том числе тяжелого течения (вплоть до развития коматозных состояний и до летальных исходов именно по причине тяжелой энцефалопатии, а не по причине респираторного дистресса или полиорганной недостаточности), случаи развития отека мозга на фоне COVID-19, случаи развития на фоне COVID-19 острого некротизирующего геморрагического энцефалита, вирусных энцефалитов и менингитов, стойких когнитивных и/или двигательных нарушений, нарушений зрения и слуха, напоминающих проявления первичных нейродегенеративных заболеваний [Mishra R, Banerjea AC, 2020].
Другими важными причинами поражений ЦНС при тяжелом течении COVID-19, помимо прямого нейротропного (нейроинвазивного) и нейротоксического действия самого вируса SARS-CoV-2, являются гипоксия мозга, связанная с острой дыхательной недостаточностью (ОДН) или с острым респираторным дистресс-синдромом (ОРДС), интоксикация, связанная с метаболическими нарушениями и нередким развитием острой полиорганной недостаточности (печеночной, почечной, надпочечниковой) на фоне тяжелого течения COVID-19, влияние цитокинового шторма, провоцирующего нейровоспаление даже в отсутствие прямой инвазии вируса в мозг, а также нарушение кровоснабжения мозга при развитии острой сердечно-сосудистой недостаточности или коллаптоидных состояний на фоне тяжелого COVID-19 [Mishra R, Banerjea AC, 2020].
Кроме того, хорошо известно, что COVID-19 часто сопровождается развитием выраженной гиперкоагуляции и наклонностью к тромбозам сосудов и к тромбоэмболическим осложнениям, особенно у лежачих или малоподвижных пациентов, и в первую очередь — у пациентов, находящихся в коматозном состоянии или на искусственной вентиляции легких (ИВЛ) [Bikdeli B et al, 2020].
Иногда на фоне COVID-19 могут наблюдаться, напротив, повышенная кровоточивость и связанные с нею геморрагические осложнения. Они обусловлены как COVID-ассоциированным поражением эндотелия сосудов, особенно мелких капилляров (эндотелиальной дисфункцией), повышением ломкости и проницаемости сосудов (COVID-ассоциированной макро- и микроангиопатией, капилляротоксикозом), так и коагулопатией потребления на фоне диссеминированного внутрисосудистого свертывания (ДВС-синдрома), или же передозировкой антикоагулянтов либо антиагрегантов, часто применяемых в комплексном лечении пациентов с COVID-19 как раз для профилактики гиперкоагуляционных и тромботических осложнений [Al-Samkari H et al, 2020; Amraei R, Rahimi N, 2020].
Все это значительно повышает риск развития на фоне COVID-19 различных сердечно-сосудистых и неврологических катастроф, в частности, ишемических или, напротив, геморрагических инсультов острых инфарктов миокарда [Marshall M, 2020]. А это, в свою очередь, может в ближайшее время значительно повысить количество пациентов, страдающих постинсультными и/или постинфарктными депрессиями и тревожными состояниями.
Показано, что наиболее частыми последствиями перенесенного COVID-19 для психики среди выписанных из стационара пациентов являются: посттравматическое стрессовое расстройство (ПТСР) — оно наблюдается у каждого третьего такого пациента. Вторыми по частоте в этой популяции являются депрессивные расстройства, которые наблюдаются у каждого шестого такого пациента, и различные тревожные расстройства, также наблюдаемые примерно у каждого шестого пациента, перенесшего COVID-19 в достаточно тяжелой форме, которая потребовала госпитализации [Rogers JP et al, 2020].
Однако, помимо вредного прямого и косвенного нейротропного действия самого вируса SARS-CoV-2, на психическое здоровье населения в период пандемии COVID-19 неблагоприятно влияет целый ряд других факторов, которые мы рассмотрим ниже.
Другие факторы, неблагоприятно влияющие на психическое здоровье населения в период пандемии COVID-19 Особые биологические свойства вируса SARS-CoV-2, обусловившие пандемический характер его распространения и вызвавшие необходимость в карантинных мерах
Инфекция, вызываемая вирусом SARS-CoV-2, отличается от всех ранее известных человечеству коронавирусных инфекций не только значительно большей тяжестью течения и более высокой смертностью по сравнению с «обычными», повсеместно распространенными в человеческой популяции коронавирусами, регулярно вызывающими сезонные ОРВИ сравнительно легкого течения, но также значительно более высокой контагиозностью по сравнению с двумя другими, ранее обнаруженными, «проблематичными» и опасными коронавирусами — вирусом атипичной пневмонии (SARS-CoV-1) и вирусом так называемой «ближневосточной пневмонии» (MERS-CoV) [Aleebrahim-Dehkordi E et al, 2020].Именно эти необычные биологические свойства нового коронавируса SARS-CoV-2 привели к тому, что его распространение, в отличие от распространения менее контагиозных SARS-CoV-1 или MERS-CoV, не удалось быстро ограничить или остановить. Поэтому оно быстро приняло характер сначала эпидемии, а затем и пандемии. С другой же стороны, высокая летальность новой коронавирусной инфекции и нередко тяжелый характер ее течения, особенно у пожилых пациентов или у пациентов, отягощенных хроническими заболеваниями, — вынудили правительства разных стран мира отнестись к COVID-19 гораздо серьезнее, чем принято относиться к сезонным эпидемиям гриппа или ОРВИ, и предпринять жесткие карантинные меры [Aleebrahim-Dehkordi E et al, 2020].
Неблагоприятное влияние экономических, психологических и социальных факторов, связанных с пандемией COVID-19 и принимаемыми карантинными мерами, на психическое здоровье популяции
Нанесенный и самой пандемией COVID-19, и принятыми в борьбе с ней жесткими карантинными мерами прямой и косвенный экономический ущерб, а также порожденный как самой пандемией, так и карантинными ограничениями масштабный социальный и психологический дистресс, в сочетании со значительным ограничением доступности плановой и экстренной медицинской помощи, не связанной с оказанием помощи больным COVID-19, из-за ограниченности ресурсов медицинской системы и перераспределения их на борьбу с пандемией — оказали выраженное негативное влияние не только на соматическое, но и на психическое здоровье и психологическое благополучие всего населения Земли — отнюдь не только на тех, кто непосредственно заразился SARS-CoV-2 или заболел COVID-19, и тем самым испытал на себе вредное нейротропное действие этого нового вируса [Ahorsu DK et al, 2020; Le HT et al, 2020; Wadoo O et al, 2020].Неблагоприятное влияние пандемии COVID-19 на состояние общего психического здоровья популяции отмечается в самых разных странах и регионах мира, вне зависимости от сложности эпидемиологической обстановки в конкретной стране, в конкретном регионе или области, от жесткости предпринимаемых правительством страны или региона/области карантинных мер, от количества выделяемых на социальную поддержку населения средств и от других подобных факторов. Так, об этом синхронно пишут исследователи из таких разных и весьма географически удаленных друг от друга стран с разными подходами к обеспечению карантина, как Швеция, Иран, Гонконг, Вьетнам, Тайвань, Катар [Ahorsu DK et al, 2020; Le HT et al, 2020; Wadoo O et al, 2020].
Показано, что пандемия COVID-19 ассоциируется с ухудшением психического здоровья населения не только и не столько по причине заболеваемости и смертности, связанных с самой этой болезнью, но и по причине того, что значительная часть населения (особенно пожилые люди и люди из групп риска) испытывает сильный и продолжительный хронический стресс, связанный со страхом заразиться этой болезнью, страхом ее тяжелого протекания, страхом смерти, а также по причине того, что меры по сдерживанию или замедлению распространения пандемии, такие как социальное дистанцирование и самоизоляция, сами по себе порождают дополнительный стресс. Кроме того, на фоне карантинных ограничений и экономического спада часть людей потеряла работу, у другой части существенно ухудшилось материальное положение, и это тоже служит дополнительным источником стресса для них [Ahorsu DK et al, 2020; Le HT et al, 2020; Wadoo O et al, 2020].
В период пандемии COVID-19, которая свирепствует в мире уже более полугода, огромное количество людей во всем мире постоянно находится в быстро меняющихся условиях, связанных с реальной угрозой для жизни. Неспособность каждого отдельно взятого индивидуума как-то повлиять на ситуацию с пандемией и карантином или хотя бы как-то контролировать ее — создаeт классическую ситуацию «выученной беспомощности» (которая, как известно, служит хорошей экспериментальной моделью депрессии на животных). Длительное нахождение в такой обстановке закономерно порождает страх, тревогу, отчаяние, чувство безнадежности или беспомощности, и может приводить к развитию депрессивных состояний [Stein MB, 2020].
Следует еще раз подчеркнуть, что как сама пандемия COVID-19, так и карантинные меры, предпринимаемые для замедления ее распространения (в частности, ограничение социальных контактов и самоизоляция), могут оказать — и уже оказывают — выраженное негативное влияние на психическое здоровье популяции. В связи с этим ряд авторов призывает к тому, чтобы специалисты в области психического здоровья давали публичные рекомендации населению о том, как справляться со стрессом, вызванным пандемией и карантином, и как предотвратить или уменьшить негативные последствия их для своего психического здоровья [Stein MB, 2020].
Интересно отметить, что, по данным британских исследователей, наибольший психологический дистресс в условиях пандемии COVID-19 переживают вовсе не лица пожилого возраста или принадлежащие к группам риска (как можно было бы ожидать, исходя из логики вещей), а женщины, лица молодого возраста и родители детей дошкольного возраста [Pierce M et al, 2020].
Текущие масштабы проблемы
Вынужденное продолжение или ужесточение карантинных мер и других изменений в сфере общественного здравоохранения, таких как перераспределение ресурсов всей медицинской системы на борьбу с COVID-19 в ущерб всем остальным областям медицины, связанное с разрастанием масштабов пандемии COVID-19 во всем мире, — неизбежно приводит к тому, что все большее количество людей по всему миру оказывается в таких ситуациях, которые потенциально могут привести (и уже приводят!) к значительному ухудшению их психического и соматического здоровья — в частности, в ситуации хронического стресса, вынужденной социальной изоляции и одиночества, ограничения передвижений и в целом ограничения физической активности, в ситуации потери работы или ухудшения материального положения семьи, и/или в ситуации ограничения доступности психиатрической и общемедицинской помощи, не связанной с COVID-19 [Отчет KFF…, 2020]. Между тем, большое количество исследований, проведенных задолго до нынешней пандемии COVID-19, указывают на тесную связь между такими неблагоприятными факторами, как хронический стресс, социальная изоляция, одиночество, безработица или бедность, ограничение физической активности, недоступность квалифицированной общемедицинской и психиатрической помощи, — и ухудшением психического и соматического здоровья в популяции [Отчет KFF…, 2020].
Между тем, большое количество исследований, проведенных задолго до нынешней пандемии COVID-19, указывают на тесную связь между такими неблагоприятными факторами, как хронический стресс, социальная изоляция, одиночество, безработица или бедность, ограничение физической активности, недоступность квалифицированной общемедицинской и психиатрической помощи, — и ухудшением психического и соматического здоровья в популяции [Отчет KFF…, 2020].Так, в частности, в США по состоянию на март 2020 года 32% опрошенных взрослых сообщили интервьюерам, что их психическое здоровье и психологическое благополучие подверглись значительному негативному влиянию из-за дистресса, вызванного пандемией COVID-19. А в августе 2020 года в тех же США количество тех людей, кто сообщил интервьюерам о значительном негативном влиянии на них хронического стресса, связанного с пандемией COVID-19, среди опрашиваемых взрослых выросло уже до 53% [Отчет KFF…, 2020].
Среди симптомов дистресса, описываемых опрошенными, часто отмечались нарушения сна, изменения в пищевом поведении, увеличение потребления алкоголя и/или других психоактивных веществ (ПАВ), включая никотин и кофеин, обострения различных хронических психических и соматических заболеваний [Отчет KFF…, 2020].
Кроме того, согласно тому же отчету, в США за период с мая по июль 2020 года наблюдался устойчивый рост количества людей, сообщающих о наличии у них симптомов тревоги и/или депрессии (рис. 1) [Отчет KFF…, 2020].
В ухудшении общего психического здоровья популяции в период пандемии COVID-19 значительную роль играет вынужденная социальная изоляция или самоизоляция, связанная с карантинными мерами. Так, в частности, в США данные на конец марта 2020 года показывают, что среди тех опрошенных, которые пребывали в вынужденной изоляции или самоизоляции, значительно бóльший процент (47%) сообщал о негативных последствиях хронического стресса и беспокойства, связанных с пандемией COVID-19, для их психического здоровья и/или душевного комфорта, чем среди тех, кто не был в вынужденной изоляции или самоизоляции (37%) [Отчет KFF…, 2020].
Кроме того, те из опрошенных, которые находились в вынужденной изоляции или самоизоляции, гораздо чаще (в 21% случаев) сообщали не просто о последствиях, но именно о выраженных (тяжелых) последствиях хронического стресса, связанного с пандемией COVID-19, для их психического здоровья и/или душевного комфорта, чем те, кто не подвергался вынужденной изоляции и не прибегал к самоизоляции (среди них сообщили о тяжелых последствиях всего 13%) [Отчет KFF…, 2020].
Социальная изоляция или самоизоляция и одиночество, а также ограничение передвижений и физической активности могут представлять особую опасность для психического здоровья и душевного комфорта подростков и пожилых людей, по сравнению с молодыми взрослыми. Так, в США среди лиц в возрасте 65 лет и старше доля тех, кто сообщил интервьюерам о негативных последствиях пандемии COVID-19 для их психического здоровья, увеличилась с марта по июль 2020 года с 27% до 47% [Отчет KFF…, 2020].
Другим хорошо известным фактором, негативно влияющим на психическое здоровье в популяции, является безработица и/или бедность (низкий уровень доходов, низкий социально-экономический статус). Так, в США среди тех людей, которые на фоне пандемии COVID-19 потеряли работу или испытали ухудшение материального положения, о негативных последствиях этой пандемии и связанного с ней хронического стресса и беспокойства, для их психического здоровья сообщили 58% опрошенных [Отчет KFF…, 2020].
Кроме того, было также показано, что лица с более низким уровнем доходов и/или с более низким социально-экономическим статусом (например, с более низким уровнем образования и квалификации и/или живущие в районах с более низким качеством жилья и инфраструктуры) значительно чаще людей с более высоким уровнем доходов и/или с более высоким социально-экономическим статусом (уровнем образования, качеством жилья) сообщают о серьезных негативных последствиях пандемии COVID-19 для их психического здоровья и душевного благополучия [Отчет KFF…, 2020].
 Третьим важным фактором, который может обуславливать ухудшение психического здоровья, как сам по себе, так и в особенности на фоне воздействия хронического стресса, является наличие коморбидных соматических расстройств. Показано, что этот фактор играет роль и на фоне бушующей ныне пандемии COVID-19. Так, в США среди опрошенных взрослых, имеющих те или иные проблемы соматического здоровья, 62% сообщили о негативных последствиях пандемии COVID-19 и связанного с ней хронического стресса и беспокойства для их психического здоровья или психологического благополучия. В то же время среди лиц с хорошим соматическим здоровьем таких было меньше — 51%. Люди с проблемами соматического здоровья также чаще (в 38% случаев) сообщали о значительно выраженном негативном влиянии пандемии на их психическое здоровье и психологический комфорт, чем люди с хорошим соматическим здоровьем (в 23% случаев) [Отчет KFF…, 2020].
Третьим важным фактором, который может обуславливать ухудшение психического здоровья, как сам по себе, так и в особенности на фоне воздействия хронического стресса, является наличие коморбидных соматических расстройств. Показано, что этот фактор играет роль и на фоне бушующей ныне пандемии COVID-19. Так, в США среди опрошенных взрослых, имеющих те или иные проблемы соматического здоровья, 62% сообщили о негативных последствиях пандемии COVID-19 и связанного с ней хронического стресса и беспокойства для их психического здоровья или психологического благополучия. В то же время среди лиц с хорошим соматическим здоровьем таких было меньше — 51%. Люди с проблемами соматического здоровья также чаще (в 38% случаев) сообщали о значительно выраженном негативном влиянии пандемии на их психическое здоровье и психологический комфорт, чем люди с хорошим соматическим здоровьем (в 23% случаев) [Отчет KFF…, 2020].Ограничение доступности или несвоевременность оказания общемедицинской и психиатрической помощи в период пандемии COVID-19, из-за перераспределения ресурсов медицинской системы на борьбу с пандемией, также играет существенную роль в ухудшении психического здоровья в популяции. Так, в США 4% опрошенных заявили о том, что в период пандемии они столкнулись со снижением доступности экстренной медицинской помощи, не связанной с COVID-19, и/или с пропусками, задержками или переносами на более поздний срок планового общемедицинского и/или психиатрического обслуживания. Большинство из них утверждают, что в результате этого их психическое состояние и душевное благополучие ухудшились (у некоторых — значительно) [Отчет KFF…, 2020].
Влияют на переносимость хронического стресса, связанного с пандемией COVID-19, также гендерные различия и различия в семейном положении. Наличие детей, порождая тревогу и беспокойство за их здоровье на фоне пандемии, является дополнительным фактором риска развития психических проблем. Другим установленным фактором риска является принадлежность к женскому полу. Так, в США более половины опрошенных женщин, имеющих детей в возрасте до 18 лет (57% в марте и 59% в июле 2020 года), сообщили о серьезных отрицательных последствиях стресса, связанного с пандемией COVID-19, для их психического здоровья. Это заметно выше соответствующих показателей как для бездетных женщин, так и для мужчин (в том числе — для одиноких мужчин с детьми). Так, среди мужчин, имеющих детей до 18 лет, в марте 2020 года сообщали о серьезных негативных последствиях стресса, связанного с пандемией COVID-19, 32% опрошенных, а в июле 2020 года — 49% опрошенных [Отчет KFF…, 2020].
Еще до пандемии было известно, что потеря работы или снижение уровня доходов либо социально-экономического статуса (например, вынужденный переезд в район с худшими жилищными условиями и худшей инфраструктурой) — тесно ассоциируются с повышением риска развития депрессивных и тревожных расстройств, с повышенным уровнем стресса, тревоги, беспокойства, со снижением самооценки, а также с повышением частоты самоубийств, и с повышением потребления алкоголя и ПАВ [Отчет KFF…, 2020].
Экстраполяция имеющихся данных о влиянии предыдущих экономических потрясений на нынешнюю ситуацию, предпринятая фондом Well Being Trust и Центром политических исследований Роберта Грэма, показывает, что экономический спад на фоне пандемии COVID-19 и карантинных мер, и связанные с этим безработица и ухудшение материального положения населения, могут к 2029 году привести к дополнительным 75 000 смертей от суицидов, а также от злоупотребления алкоголем или ПАВ, включая никотин, в одних только США [Отчет KFF…, 2020].
Еще одна группа исследователей из США также предприняла попытку оценить влияние пандемии COVID-19 на психическое здоровье, частоту употребления ПАВ и распространенность суицидальных тенденций среди взрослого населения США (≥ 18 лет). С этой целью они в период с 24 по 30 июня 2020 года провели репрезентативные групповые обследования жителей различных городов и поселков в каждом из штатов США [Czeisler ME et al, 2020].
В выборке из этого исследования 40,9% опрошенных сообщили о появлении у них в период пандемии COVID-19 симптомов как минимум одного психического или поведенческого расстройства. В частности, 30,9% опрошенных сообщили о развитии у них симптомов депрессивного или тревожного расстройства на фоне стресса, связанного с пандемией COVID-19, 26,3% сообщили о развитии у них симптомов ПТСР в связи с психологической травмой, нанесенной им либо самой пандемией COVID-19 как таковой, либо фактом перенесения этой болезни либо ими самими, либо кем-то из близких, родственников или друзей, а 13,3% признались в том, что начали употреблять или увеличили потребление алкоголя и/или ПАВ, включая никотин, для того, чтобы справиться со стрессом, вызванным пандемией COVID-19 [Czeisler ME et al, 2020].
Кроме того, 10,7% респондентов этого исследования сообщили о том, что в течение 30 дней, предшествовавших опросу, они серьезно задумывались о самоубийстве. Этот процент был значительно выше среди молодежи в возрасте от 18 до 24 лет (25,5%), среди представителей расовых и этнических меньшинств, которые ощущают себя дискриминированными (например, среди респондентов латиноамериканского происхождения он составил 18,6%), а также среди лиц трудоспособного возраста, вынужденных ухаживать за пожилыми или больными родственниками (30,7%) [Czeisler ME et al, 2020].
Интересные данные опубликованы южнокорейскими исследователями. Они одними из первых в мире поставили вопрос о том, что связь между пандемией COVID-19 и психическими расстройствами может иметь двусторонний характер: не только COVID-19 может вызывать психические расстройства de novo или обострения и рецидивы уже имеющихся психических расстройств, но и наоборот — имеющееся психическое расстройство может повышать риск заражения SARS-CoV-2, риск заболевания COVID-19 или риск тяжелого его течения. Для проверки этого предположения они предприняли масштабное когортное исследование [Lee SW et al, 2020].
Задача южнокорейских исследователей по получению большой выборки значительно облегчалась тем, что Южная Корея оказалась одной из немногих стран мира, в которых на SARS-CoV-2 был протестирован значительный процент популяции. В период с 1 января по 15 мая 2020 года тестирование на SARS-CoV-2 в этой стране прошли 216 418 человек. Из них у 7160 человек (у 3,3% всех протестированных) тест оказался положительным. В исследуемую когорту авторы включили всех тех лиц в возрасте старше 20 лет, которые были протестированы на SARS-CoV-2 в указанный период времени, независимо от результатов теста (положительный или отрицательный) [Lee SW et al, 2020].
Тяжелое течение и неблагоприятные клинические исходы COVID-19 среди тех, у кого тест на SARS-CoV-2 был положительным, в этом исследовании определялись как потребность в кислородной поддержке, вынужденная госпитализация в отделение интенсивной терапии или в отделение реанимации, необходимость в ИВЛ, а также летальный исход [Lee SW et al, 2020].
Анализ влияния наличия психических расстройств на риск заражения SARS-CoV-2 или заболевания COVID-19 в этой когорте показал, что сам по себе диагноз психического заболевания не коррелирует с повышенной вероятностью положительного результата теста на SARS-CoV-2 или с повышенной вероятностью проявления клинических симптомов COVID-19. Однако при этом также обнаружилось, что пациенты с тяжелыми, особенно психотическими, формами аффективных и неаффективных расстройств имеют более высокий риск тяжелого течения и неблагоприятных клинических исходов COVID-19, чем пациенты без психических расстройств в анамнезе или пациенты с легкими и среднетяжелыми психическими расстройствами [Lee SW et al, 2020].
В Австралии в апреле 2020 года был проведен онлайн-опрос о влиянии пандемии COVID-19 на психическое здоровье популяции. В нем принял участие 1491 взрослый. Средний возраст участников опроса составил 50,5±14,9 года. Среди них было 67% женщин. Участниками опроса было отмечено негативное влияние пандемии COVID-19 на уровень их физической активности (об этом сообщили 48,9% всех опрошенных), на качество сна (40,7% всех опрошенных), на частоту употребления алкоголя и/или на среднее количество употребляемого спиртного (26,6% всех опрошенных) и на уровень потребления табака (6,9% всех опрошенных) [Stanton R et al, 2020].
Все эти неблагоприятные изменения на фоне пандемии COVID-19 тесно ассоциировались с наличием симптомов депрессии и/или тревоги. Они были более выраженными и чаще отмечались у женщин, а также у тех лиц, которые находились в вынужденной изоляции или самоизоляции, были безработными или имели низкий уровень доходов, низкий социально-экономический статус (низкий уровень образования, неблагоприятные условия проживания), и у имеющих хронические соматические или психические заболевания [Stanton R et al, 2020].
Интересно отметить, что среди сравнительно молодых лиц (в возрасте от 18 до 45 лет) уровень дистресса, связанного с пандемией COVID-19, был выше, а неблагоприятные последствия для психического здоровья отмечались чаще, чем среди лиц более старшего возраста. Возможно, это связано с тем, что молодые люди психологически хуже переносят карантинные ограничения, социальную изоляцию или самоизоляцию и вынужденное уменьшение свободы перемещения, чем люди пенсионного возраста, более склонные к «домоседству» [Stanton R et al, 2020].
Испанские исследователи также попытались оценить влияние пандемии COVID-19 на психическое здоровье популяции, опросив 976 взрослых по Шкале тревоги и стресса (DASS). Хотя уровни дистресса, тревоги и депрессии в испанской популяции в начале пандемии были достаточно низкими, они постепенно повышались по мере развертывания пандемии и ужесточения карантинных мер. Лица с хроническими психическими или соматическими заболеваниями сообщали о большем количестве и большей выраженности симптомов дистресса, тревоги и депрессии, чем лица без таковой отягощенности, а молодые, опять-таки, сообщали об этом чаще, чем пожилые [Ozamiz-Etxebarria N et al, 2020].
Кроме того, более выраженная тревожная и депрессивная симптоматика отмечалась у тех лиц, которым была предписана изоляция (пребывание на дому) в связи с наличием симптомов COVID-19, положительным результатом теста на вирус SARS-CoV-2 или контактным статусом. Авторы этого исследования констатировали, что по мере продолжения или ужесточения карантинных мер и социальной изоляции можно ожидать дальнейшего увеличения распространенности симптомов дистресса, тревоги и депрессии в испанской популяции [Ozamiz-Etxebarria N et al, 2020].
Исследователи из Гонконга через 3 месяца после появления в этом городе первого подтвержденного случая заболевания COVID-19 провели опрос 500 респондентов с помощью Опросника о здоровье пациента, состоящего из 9 вопросов (Patient Health Questionnaire-9, PHQ-9), и Шкалы оценки генерализованной тревоги из 7 вопросов (Generalized Anxiety Disorder-7, GAD-7). При этом у 19% от общего числа опрошенных обнаружились клинически значимые симптомы депрессии, а у 14% от общего числа опрошенных — клинически значимые симптомы тревоги. Кроме того, 25,4% всех респондентов заявили о том, что их психическое здоровье и психологическое благополучие ухудшились именно из-за пандемии COVID-19 и связанного с ней стресса [Choi EH et al, 2020].
Авторы этого исследования отметили, что среди значимых причин ухудшения психического состояния респонденты чаще всего называли ограничение доступности плановой медицинской помощи, в том числе плановых хирургических вмешательств, необходимость постоянно носить маски на улице и в общественных местах и связанные с этим неудобства и дискомфорт, необходимость соблюдать социальную дистанцию и ограничивать контакты с другими людьми, отсутствие возможности работать на дому, потерю работы или ухудшение материального положения [Choi EH et al, 2020].
Влияние пандемии COVID-19 и связанного с ней стресса на общее психическое здоровье популяции, и в частности — на распространенность в популяции симптомов депрессии, тревоги и ипохондрии (чрезмерной обеспокоенности своим здоровьем), изучали также турецкие исследователи. Применявшиеся ими методики включали в себя опрос респондентов по Госпитальной шкале тревоги и депрессии (Hospital Anxiety and Depression Scale, HADS) и по Опроснику тревоги за здоровье (Health Anxiety Inventory, HAI) [Özdin S, Özdin SB, 2020].
Кроме того, авторы этого исследования также попытались выяснить, какие факторы влияют на индивидуальную переносимость стресса, связанного с пандемией, и на риск развития неблагоприятных последствий этого стресса для психического здоровья индивидуума. Они учитывали такие факторы, как место проживания (город или деревня), профессия, социальный статус, возраст, пол, семейное положение, наличие несовершеннолетних детей, совместное проживание с человеком старше 60 лет или с человеком, принадлежащим к группе риска тяжелого течения COVID-19, наличие лиц с подтвержденным заражением SARS-CoV-2 или с симптомами COVID-19 среди знакомых, друзей или родственников, наличие в анамнезе или на данный момент какого-либо психического расстройства, наличие хронических соматических заболеваний или избыточной массы тела [Özdin S, Özdin SB, 2020].
В общей сложности у 23,6% опрошенных жителей Турции были выявлены клинически значимые симптомы депрессии, а у 45,1% опрошенных — клинически значимые симптомы тревоги и/или ипохондрии (чрезмерной обеспокоенности своим здоровьем) [Özdin S, Özdin SB, 2020].
В этом исследовании факторами повышенного риска ухудшения психического состояния или развития психосоциальной дезадаптации на фоне пандемии COVID-19 оказались проживание в городе, принадлежность к женскому полу, наличие хронических соматических заболеваний, наличие психических расстройств в анамнезе или на текущий момент [Özdin S, Özdin SB, 2020].
Пандемия COVID-19 также спровоцировала у значительного числа психиатрических пациентов рецидивы или обострения, или ухудшение течения некоторых ранее имевшихся у них психических расстройств. К числу тех психиатрических пациентов, которые наиболее подвержены неблагоприятному влиянию стресса, связанного с пандемией COVID-19, относят страдающих обсессивно-компульсивным расстройством (ОКР) [Lee SA et al, 2020].
С чрезмерным, патологическим страхом заразиться SARS-CoV-2 или заболеть COVID-19, развившимся на фоне пандемии и связанного с нею дистресса, ассоциирована новая психопатологическая конструкция — так называемая коронафобия [Lee SA et al, 2020].
В ответ на очевидное усиление нужды в психиатрической помощи у пациентов с ОКР на фоне пандемии COVID-19 и на поступающие от пациентских организаций настойчивые призывы о помощи мировое психиатрическое сообщество создало специальную рабочую экспертную группу для разработки рекомендаций по оказанию помощи пациентам с ОКР в период пандемии. В нее вошли эксперты по ОКР из таких авторитетных международных психиатрических организаций, как Международный колледж расстройств обсессивно-компульсивного спектра (ICOCS), Исследовательская сеть обсессивно-компульсивных расстройств (OCRN) и Европейский колледж нейропсихофармакологии [Морозов ПВ, Петрова НН, 2020].
Результатом работы этой экспертной группы явился документ, который может служить основой для разработки практических рекомендаций по оказанию психиатрической помощи пациентам с ОКР в период пандемии COVID-19 [Морозов ПВ, Петрова НН, 2020].
Ряд экспертов высказывает опасение о том, что предпринимаемые правительствами разных стран мира с целью ограничения скорости распространения пандемии COVID-19 карантинные меры, в частности меры по социальному дистанцированию, изоляции и самоизоляции, — могут привести не только к неблагоприятным последствиям для психического здоровья и психологического комфорта популяции, но и к повышению риска самоубийств. К этому могут привести и вызванные пандемией COVID-19 неблагоприятные изменения в различных экономических, психосоциальных и связанных со здоровьем факторах риска суицидальности, таких как распространенность безработицы и бедности, снижение доступности и своевременности общемедицинской и психиатрической помощи, разрушение традиционных социальных связей и др. [Reger MA et al, 2020].
Неблагоприятные последствия пандемии COVID-19 для психического здоровья и психологического комфорта человеческой популяции в ближайшем будущем, скорее всего, будут только увеличиваться в связи с повседневной доступностью информации о росте количества зараженных и заболевших, об увеличении количества умерших от COVID-19, а также в связи с прогрессированием экономического спада, ростом уровня безработицы и бедности, снижением доступности и качества медицинской помощи из-за перераспределения ресурсов медицинской системы на борьбу с пандемией, а также в связи со снижением доступности социальной, психологической и религиозной поддержки, ограничением или разрушением традиционных социальных связей и контактов [Reger MA et al, 2020].
Также возможно, что круглосуточное освещение в средствах массовой информации всего мира беспрецедентных событий, связанных с пандемией COVID-19 и мерами борьбы с ней, принявшее в последние полгода характер настоящего «информационного шторма», — может служить дополнительным стрессовым фактором, или даже может непосредственно выступать триггером для развития психических расстройств или для проявления суицидальных тенденций, особенно у лиц с ранее имевшимися психическими проблемами или с предрасположенностью к их развитию [Reger MA et al, 2020].
Между тем все ведущие суицидологические теории подчеркивают ту ключевую роль, которую играет наличие работы, поддержание устойчивых социальных связей, возможность получения морально-психологической поддержки, в профилактике самоубийств [Reger MA et al, 2020].
В свете всего вышесказанного, в условиях пандемии COVID-19 и связанного с ней роста влияния таких факторов риска суицидальности, как безработица и бедность, одиночество, разрушение или ограничение социальных связей и контактов, необходима разработка активных мер по профилактике роста количества самоубийств. Эти меры должны учитывать определенные ограничения доступа к психиатрической и психотерапевтической помощи, накладываемые пандемией [Reger MA et al, 2020].
Несмотря на все те трудности, которые накладывают такие ограничения, пандемия COVID-19 открывает перед нами также уникальные возможности по совершенствованию системы оказания психиатрической, суицидологической и психотерапевтической помощи населению, по широкому внедрению телепсихиатрии. В полном соответствии с этим в США наблюдается тенденция к расширению использования телемедицины, и в частности телепсихиатрии, в ответ на трудности, связанные с пандемией COVID-19 и карантинными ограничениями [Reger MA et al, 2020].
Следует особо подчеркнуть, что официальный термин «социальное дистанцирование», несмотря на свое звучание, в действительности требует лишь поддержания определенного минимального физического расстояния между людьми для затруднения передачи вируса, а не социального или психоэмоционального дистанцирования между ними. В связи с этим людям рекомендуется предпринимать активные усилия для того, чтобы оставаться на связи с родственниками, друзьями, близкими и значимыми людьми и поддерживать личностно значимые для них отношения с помощью телефона, Интернета или видеоконференций. Особенно важно это для людей с психическими расстройствами или с повышенным риском самоубийства [Reger MA et al, 2020].
Уже давно существуют научно обоснованные, имеющие надежную доказательную базу мероприятия по профилактике самоубийств, которые могут осуществляться дистанционно (или даже разрабатывались именно таким образом, чтобы их можно было осуществлять дистанционно). Например, в рандомизированных клинических испытаниях (РКИ) было показано, что даже кратковременное контактное вмешательство, кратковременное проявление заботы, внимания и участия, такое как участливый телефонный звонок (телефонная аутрич-работа), SMS-сообщение или заботливое письмо от бывшего лечащего врача (например, токсиколога, интенсивиста или анестезиолога-реаниматолога) пациенту, выписанному из соответствующего отделения стационара после неудавшейся попытки самоубийства, с вопросом о том, как он себя чувствует и как у него дела, — существенно снижает вероятность повторных суицидальных попыток в ближайшие недели [Reger MA et al, 2020].
Аналогичным эффектом обладают телефонные звонки, SMS-сообщения и письма с проявлениями заботы, внимания и интереса к положению дел у пациента, склонного к суицидальным тенденциям и проявлениям, от семейного врача (участкового терапевта), от лечащего психиатра или психотерапевта и даже просто от близких, друзей, родственников [Reger MA et al, 2020].
С другой же стороны, наряду с тем очевидным негативным влиянием, которое оказывают сама пандемия COVID-19, экономический спад, рост безработицы и бедности, социальная изоляция и самоизоляция, снижение доступности общемедицинской и психиатрической помощи и связанный со всем этим дистресс на психическое здоровье популяции и на распространенность в ней суицидальных тенденций, — можно предположить и влияние противоположно направленного эффекта — так называемого эффекта «тянем лямку вместе» [Reger MA et al, 2020].
Этот эффект описывается так — члены некоего сообщества или популяции, совместно переживающие общий для них всех негативный социальный или психоэмоциональный опыт, могут оказывать более сильную, чем до того, социальную и психоэмоциональную поддержку, и могут формировать более тесные, чем до того, социальные связи. Так, в США показатели частоты самоубийств, согласно предыдущему историческому опыту, почти всегда снижались в ранние периоды после крупных национальных катастроф, таких как крушение башен-близнецов в Нью-Йорке 11 сентября 2001 года [Reger MA et al, 2020].
Поэтому можно предполагать, что бушующая ныне в мире пандемия COVID-19 может изменить по крайней мере у части людей сложившиеся ранее взгляды на ценность человеческой жизни и здоровья и на смерть, сделать для них сохранение собственной или чьей-то еще жизни и здоровья, а также поддержание прочных социальных связей более ценным, чем ранее, и тем самым может предотвратить некоторое количество самоубийств [Reger MA et al, 2020].
Истинные масштабы пандемии нового коронавируса SARS-CoV-2 и ее возможное долгосрочное влияние на психическое здоровье и психологическое благополучие населения Земли еще только предстоит оценить, поскольку пандемия еще далеко не закончилась [Figueroa CA, Aguilera A, 2020].
Тем не менее уже сейчас имеются данные, позволяющие связать как перенесенный тем или иным отдельно взятым индивидуумом COVID‐19, так и общий дистресс, связанный с обстановкой пандемии, карантинными ограничениями, экономическим спадом, безработицей или ухудшением материального положения огромного множества людей — с долгосрочными неблагоприятными последствиями для психического здоровья и психологического благополучия как популяции в целом, так и каждого отдельно взятого индивидуума, особенно лиц из числа исходно предрасположенных к развитию психических и психологических проблем [Figueroa CA, Aguilera A, 2020].
Все вышесказанное делает особенно актуальной в эпоху пандемии COVID-19 проблему оказания своевременной психиатрической, психологической и социальной помощи лицам с психическими расстройствами или с проблемами психосоциальной адаптации [Figueroa CA, Aguilera A, 2020].
Психические расстройства на фоне пандемии COVID-19 среди медицинских работников
Работники системы здравоохранения, прежде всего те, кто непосредственно работает с пациентами (врачи, средний и младший медицинский персонал), являются группой повышенного риска как в отношении заражения вирусом SARS-CoV-2 или заболевания COVID-19, так и в отношении риска развития некоторых видов психических расстройств на фоне пандемии COVID-19 [Zhang WR et al, 2020].Это обусловлено целым рядом факторов — как повышенной частотой контакта с носителями SARS-CoV-2 или больными COVID-19 и повышенной угрозой жизни и здоровью этих категорий работников, так и влиянием общего психического и психологического стресса, связанного с пандемией, влиянием информационных перегрузок, вынужденных переработок из-за нехватки врачей и персонала, дополнительных смен, в том числе ночных, вынужденной работы не по основной врачебной или сестринской специальности, а также влиянием психологической нагрузки, связанной с необходимостью принимать тяжелые и ответственные решения, например, проводить триаж (распределение пациентов на тех, кто нуждается в экстренной помощи и получит ее, тех, кто пока может подождать, и тех, кто мог бы получить помощь в более благоприятных условиях, но не получит ее из-за ограниченности доступных медицинских и технических ресурсов, и фактически может быть при этом обречен на смерть) [Zhang WR et al, 2020].
Анализ тех неблагоприятных последствий для психического здоровья и психологического здоровья медицинских работников, которые принесли с собой предыдущие эпидемические вспышки опасных коронавирусов SARS-CoV-1 и MERS, показал, что нежелательные последствия психического и психологического стресса, перенесенного этими людьми в период эпидемической вспышки, могут сохраняться в этой субпопуляции до трех лет после собственно вспышки, а возможно, и дольше [Zhang WR et al, 2020].
На основании этих данных, группа китайских исследователей, возглавляемая W. Zhang, предприняла масштабное исследование того, как повлияла сегодняшняя пандемия COVID-19 на состояние психического здоровья и внутреннего психологического комфорта работников сферы здравоохранения Китайской Народной Республики.
В этом исследовании приняли участие в общей сложности 2182 человека. Для опроса участников исследования использовались следующие шкалы и опросники: Шкала оценки тяжести бессонницы (Insomnia Severity Index, ISI), краткий вариант Опросника Здоровья Пациента, состоящий всего из 4 вопросов (Patient Health Questionnaire-4, PHQ-4), и обновленная ревизия Структурированного Списка Симптомов, состоящего из 90 вопросов (Structured symptom CheckList-90, Revised, SCL-90-R) [Zhang WR et al, 2020].
Авторы этого исследования сумели показать, что, по сравнению с немедицинскими работниками сферы здравоохранения (например, техническим и административным персоналом, в общей сложности 1255 человек), у медицинских работников (в общей сложности 927 человек) отмечается более высокая распространенность нарушений сна (38,4%, против 30,5% среди немедиков, p<0,01), симптомов тревоги (13%, против 8,5% среди немедиков, p<0,01), симптомов депрессии (12,2%, против 9,5% среди немедиков, p<0,04), симптомов соматизации (1,6%, против 0,4% среди немедиков, p<0,01), обсессивно-компульсивных симптомов (5,3%, против 2,2% среди немедиков, p<0,01) [Zhang WR et al, 2020].
Они также показали, что группами повышенного риска развития психических расстройств на фоне пандемии COVID-19 среди всех медработников оказались сотрудники женского пола, сотрудники, проживающие в сельской местности, особенно те из них, которые по причине транспортной и логистической удаленности их места проживания не имеют возможности быстрого доступа к близлежащим крупным центрам оказания высококвалифицированной медицинской помощи пациентам с COVID-19, или по причине плохого качества связи не имеют возможности быстро организовать получение квалифицированной дистанционной консультации от коллег, а также сотрудники с повышенным риском контакта с пациентами, инфицированными SARS-CoV-2 либо страдающими COVID-19 [Zhang WR et al, 2020].
 Другая международная группа исследователей, в которую вошли специалисты из Великобритании и Греции, недавно опубликовала подробный систематический обзор и метаанализ, также посвященный изучению вопроса о влиянии пандемии COVID-19 на психическое здоровье и психологическое благополучие сотрудников сферы здравоохранения. Они сумели идентифицировать в доступной им мировой научной литературе 13 качественных исследований, удовлетворяющих критериям отбора для включения в этот метаанализ, с общим числом опрошенных участников 33 062 человека [Pappa S et al, 2020].
Другая международная группа исследователей, в которую вошли специалисты из Великобритании и Греции, недавно опубликовала подробный систематический обзор и метаанализ, также посвященный изучению вопроса о влиянии пандемии COVID-19 на психическое здоровье и психологическое благополучие сотрудников сферы здравоохранения. Они сумели идентифицировать в доступной им мировой научной литературе 13 качественных исследований, удовлетворяющих критериям отбора для включения в этот метаанализ, с общим числом опрошенных участников 33 062 человека [Pappa S et al, 2020].Распространенность симптомов тревоги среди медицинских работников оценивалась в 12 из 13 включенных в данный метаанализ исследований. Медианное значение распространенности тревожных симптомов по всему пулу участников этих исследований составило 23,2%. Распространенность симптомов депрессии среди медицинских работников изучалась в 10 из 13 исследований. При этом медианная распространенность депрессивных симптомов по всей выборке составила 22,8%. Распространенность нарушений сна среди медработников оценивалась в 5 из 13 исследований, медианное значение по всей выборке составило 38,9% [Pappa S et al, 2020].
В этом метаанализе также были выявлены значительные гендерные и профессиональные различия как в общей распространенности, так и в степени выраженности аффективных и тревожных симптомов среди медработников. А именно авторы показали, что среди медработников женского пола и общая распространенность, и степень выраженности аффективных и тревожных нарушений выше, чем среди медработников мужского пола, а у среднего медперсонала — выше, чем у врачей (см. таблицу 1) [Pappa S et al, 2020].
Кроме того, авторы также отметили высокий уровень синдрома профессионального выгорания (СПВ) у медработников на фоне пандемии COVID-19 и связанных с ней перегрузок, и выраженное негативное влияние СПВ на состояние психического здоровья медработников и на их внутренний психологический комфорт и качество жизни [Pappa S et al, 2020].
Особенности психофармакотерапии психических расстройств на фоне COVID-19
Присоединение у пациента с тем или иным психическим расстройством интеркуррентного заболевания COVID-19, или же возникновение рецидива или манифестация психических расстройств de novo на фоне COVID-19 обуславливает некоторые особенности психофармакотерапии (ПФТ) при таком сочетании. Так, в частности, обусловленный выраженной воспалительной реакцией в легких «цитокиновый шторм» может оказывать гепатотоксическое влияние, а также может непосредственно угнетать систему цитохрома P450 и тормозить метаболизм некоторых антипсихотиков (АП) в печени. В частности, это показано для клозапина, оланзапина и рисперидона. Эти изменения могут потребовать снижения дозы данных АП в период болезни COVID-19 во избежание развития выраженных побочных эффектов (ПЭ) [Мосолов СН, 2020; Информация о взаимодействии…, 2020].С другой же стороны, карбамазепин, вальпроаты, некоторые АП (например, клозапин, хлорпромазин) и некоторые АД (например, миртазапин, миансерин) могут проявлять миелотоксические свойства (в диапазоне от лейкопении и тромбоцитопении до жизнеопасного агранулоцитоза). Некоторые АП и АД, а также карбамазепин могут усиливать гиповолемию и имеющиеся электролитные нарушения, артериальную гипотензию, вызывать синдром неадекватной секреции антидиуретического гормона и т. д. Некоторые АП (например, сертиндол, зипрасидон, амисульприд, тиоридазин, трифлуоперазин) и некоторые АД (например, тразодон, трициклические антидепрессанты — ТЦА) способны изменять интервал QT на электрокардиограмме (ЭКГ) и повышать вероятность развития жизнеопасных сердечных аритмий, в том числе пируэтной желудочковой тахикардии (ЖТ) и фибрилляции желудочков (ФЖ) [Мосолов СН, 2020; Информация о взаимодействии…, 2020].
Далее, бензодиазепины и барбитураты могут снижать тонус скелетных мышц и угнетать активность дыхательного центра мозга, повышая тем самым риск развития пневмонии. Центральные антихолинергические препараты, такие как тригексифенидил, бипериден, неблагоприятно влияют на секрецию бронхиальной слизи и ее вязкость. Показано, что у пожилых пациентов эти препараты в 1,6–2,5 раза повышают риск развития пневмонии [Мосолов СН, 2020; Информация о взаимодействии…, 2020].
Согласно данным о лекарственных взаимодействиях психотропных препаратов со средствами терапии коронавирусной инфекции (COVID‐19), адаптированным С. Н. Мосоловым для РФ с сайта отделения клинической фармакологии Ливерпульского университета, к АД с низким риском или отсутствием риска взаимодействия с противовирусными препаратами относятся СИОЗС флувоксамин и флуоксетин, а также СИОЗСиН милнаципран и дулоксетин [Мосолов СН, 2020; Информация о взаимодействии…, 2020].
Проблема лечения COVID-19 имеющимися средствами
Пандемия COVID-19, бушующая в мире уже более полугода, поставила перед практическими врачами очень острый вопрос о том, чем еще, кроме чисто симптоматического лечения (жаропонижающие, отхаркивающие и другие средства) и помощи в поддержании жизненно важных функций организма, прежде всего — функции внешнего дыхания (обогащенные кислородом или гелий-кислородные смеси, ИВЛ, а в особенно тяжелых случаях с тотальным поражением легких — даже ЭКМО), мы можем помочь пациентам с этой болезнью [Homolak J, Kodvanj I, 2020].Вполне логично, что в условиях отсутствия в настоящее время клинически доступных противовирусных лекарств, которые бы обладали специфической эффективностью именно против нового коронавируса SARS-CoV-2, взгляды как ученых-исследователей, так и практикующих врачей обратились к исследованию эффективности и безопасности при COVID-19 уже доступных на мировом фармацевтическом рынке противовирусных лекарств, изначально создававшихся для борьбы с совсем другими вирусными инфекциями [Homolak J, Kodvanj I, 2020].
Таковы, например, комбинация ритонавир/лопинавир, изначально предназначавшаяся для лечения ВИЧ-инфекции, ацикловир, который эффективен против вирусов простого герпеса, или озельтамивир, который эффективен против вирусов гриппа типа А подтипа H1N1. Однако результаты клинических испытаний эффективности этих лекарств при лечении COVID-19 предсказуемо оказались достаточно разочаровывающими, поскольку в структуре белков и РНК вируса SARS-CoV-2 попросту нет тех молекулярных мишеней, на которые нацелено действие каждого из вышеупомянутых противовирусных средств [Homolak J, Kodvanj I, 2020].
Неудачи в клиническом применении уже существующих противовирусных лекарств для лечения COVID-19 закономерно вызвали необходимость в поиске принципиально иных подходов к лечению этой инфекции, в ожидании, пока появятся противовирусные лекарства, специфически эффективные именно против вируса SARS-CoV-2 [Homolak J, Kodvanj I, 2020].
Одним из методов, который изначально представлялся исследователям и практическим врачам весьма перспективным и многообещающим в лечении инфекции COVID-19, является иммуномодуляция. Действительно, уже достаточно давно было показано, что чрезмерно интенсивная воспалительная реакция организма на инфицирование вирусом SARS-CoV-2 и связанный с ней «цитокиновый шторм» — часто представляют даже бóльшую угрозу для жизни и здоровья пациента, чем собственно вирусное поражение клеток [Schön MP et al, 2020; Lenze EJ et al, 2020].
В рамках этого подхода, для лечения COVID-19 пытались и пытаются с различной степенью успешности применять различные иммуномодулирующие и противовоспалительные средства, например, синтетические глюкокортикоиды (дексаметазон, преднизолон, метилпреднизолон) [Mattos-Silva P et al, 2020; Tomazini BM et al, 2020], хлорохин или гидроксихлорохин [Gautam SS et al, 2020; Gautret P et al, 2020; Choudhary R, Sharma AK, 2020; Arshad S et al, 2020], индометацин [Marinella MA, 2020; Gomeni R et al, 2020], аспирин [Chow JH et al, 2020], колхицин [Altschuler EL, Kast RE, 2020; Lenze EJ et al, 2020], лефлуномид [Tsai YC, Tsai TF, 2020; Hu K et al, 2020; Wang M et al, 2020], микофенолат мофетил [Tsai YC, Tsai TF, 2020], талидомид [Tsai YC, Tsai TF, 2020], дапсон [Farouk A, Salman S, 2020; Altschuler EL, Kast RE, 2020], некоторые антигельминтные препараты с иммуномодулирующими свойствами, такие как левамизол или ивермектин [Choudhary R, Sharma AK, 2020; Uyaroğlu OA et al, 2020], некоторые антибиотики, тоже обладающие иммуномодулирующими свойствами, прежде всего азитромицин и некоторые другие макролиды [Gautret P et al, 2020; Choudhary R, Sharma AK, 2020; Arshad S et al, 2020], но также миноциклин и доксициклин [Farouk A, Salman S, 2020; Singh H et al, 2020; Gautam SS et al, 2020], некоторые фторхинолоны [Karampela I, Dalamaga M, 2020; Marciniec K et al, 2020], ингибиторы кальциневрина (циклоспорин, такролимус и др.) [Rudnicka L et al, 2020; Guisado-Vasco P et al, 2020; Liu С et al, 2020], различные антицитокиновые препараты (антагонист фактора некроза опухолей-альфа (ФНО-α) инфликсимаб, антагонист интерлейкина-6 (ИЛ-6) тоцилизумаб, антагонист интерлейкина-1 (ИЛ-1) анакинра и другие) [Schön MP et al, 2020], и даже препараты цитостатического ряда, такие как метотрексат [Caruso A et al, 2020; Seif F et al, 2020; Frohman EM et al, 2020], азатиоприн или его активный метаболит — 6-меркаптопурин [Schön MP et al, 2020], циклофосфамид [Revannasiddaiah S et al, 2020], флударабин [Ugurel OM et al, 2020], гидроксимочевина [Tsai YC, Tsai TF, 2020].
При этом довольно быстро было обнаружено, что некоторые из вышеупомянутых препаратов, помимо своего основного — противовоспалительного и иммуномодулирующего — эффекта, также оказывают угнетающее воздействие на репликацию самого вируса SARS-CoV-2, причем не только in vitro, но и in vivo. В частности, такой эффект был показан у хлорохина и гидроксихлорохина, а также у индометацина, азитромицина и некоторых других антибиотиков-макролидов [Homolak J, Kodvanj I, 2020; Schloer S et al, 2020].
Позднее было показано, что эффект угнетения репликации SARS-CoV-2 у таких препаратов, как хлорохин, гидроксихлорохин, индометацин, азитромицин и некоторые другие антибиотики группы макролидов, — по крайней мере частично опосредуется их способностью легко проникать внутрь лизосом в клетках (так называемым лизосомотропным действием), способностью их при этом изменять pH внутренней среды лизосом, а также функциональным ингибированием этими препаратами активности кислой сфингомиелиназы, фермента, который активен в основном в лизосомах [Homolak J, Kodvanj I, 2020; Schloer S et al, 2020].
Теоретические предпосылки для изучения флувоксамина в качестве перспективного средства лечения инфекции COVID-19
Как мы уже упоминали выше, наличие у того или иного лекарственного препарата выраженной лизосомотропной активности, а также наличие у этого препарата способности сильно ингибировать функциональную активность кислой сфингомиелиназы признаются потенциально полезными для лечения инфекции COVID-19 свойствами. Считается, что именно эти свойства, наряду с прочими, по крайней мере частично определяют клиническую полезность при лечении COVID-19 таких упоминавшихся нами выше иммуномодулирующих и противовоспалительных агентов, как азитромицин, хлорохин и гидроксихлорохин, индометацин [Homolak J, Kodvanj I, 2020; Schloer S et al, 2020].Между тем некоторые АД, в том числе такие препараты группы селективных ингибиторов обратного захвата серотонина (СИОЗС), как флуоксетин и флувоксамин, — тоже обладают и выраженными лизосомотропными свойствами, и способностью сильно ингибировать функциональную активность кислой сфингомиелиназы. Эти их свойства были известны задолго до пандемии COVID-19, но привлекли внимание исследователей в плане изучения их пригодности для лечения этой болезни лишь совсем недавно [Kornhuber J et al, 2011; Homolak J, Kodvanj I, 2020; Schloer S et al, 2020].
Другим важным теоретическим обоснованием для изучения потенциальной пригодности именно флувоксамина для лечения инфекции COVID-19 является то, что, как мы уже упоминали ранее, вирус SARS-CoV-2 способен проникать в различные клетки организма, особенно в нейроны и глиальные клетки ЦНС, при помощи связывания с поверхностными сигма-1 рецепторами (механизма, альтернативного связыванию с его «обычным» сайтом проникновения — белком ангиотензин-превращающего фермента изотипа 2, ACE2) [Yesilkaya UH et al, 2020].
Между тем давно и хорошо известно, что флувоксамин является самым мощным из клинически доступных агонистов сигма-1 рецепторов (не только среди АД), с Ki всего 36 nM [Narita N et al, 1996; Cobos EJ et al, 2008; Albayrak Y, Hashimoto K, 2017; Беккер РА, Быков ЮВ, 2019 (a), (b)].
Как известно, информация о том, что вирус SARS-CoV-2 использует в качестве основного механизма своего проникновения в клетки организма человека связывание с поверхностным белком ACE2, первоначально послужила основанием для подозрений в том, что ингибиторы ангиотензин-превращающего фермента (ИАПФ) и блокаторы рецепторов ангиотензина 1-го типа (БРА1), вызывая контррегуляторное усиление экспрессии белка ACE2, потенциально могут ухудшать клиническое течение инфекции COVID-19, повышать вероятность развития тяжелых долгосрочных неблагоприятных последствий этой инфекции для здоровья (например, пневмосклероза), или даже могут повышать вероятность летального исхода, или же что они могут повышать вероятность заражения вирусом SARS-CoV-2 [McFee RB, 2020].
Эти опасения даже послужили в то время основанием для некоторых специалистов рекомендовать, по возможности, отменять ИАПФ или БРА1 у пациентов, получающих эти препараты по какому-либо поводу (например, по поводу гипертонической болезни или хронической сердечной недостаточности) в случае заражения этого пациента вирусом SARS-CoV-2 [McFee RB, 2020].
Однако в дальнейшем было показано, что эти опасения на самом деле беспочвенны, и что ни ИАПФ, ни БРА1 на самом деле не ухудшают течения COVID-19, не повышают вероятность развития тяжелых осложнений и долгосрочных неблагоприятных последствий этой инфекции для здоровья, и не оказывают отрицательного влияния на частоту летальных исходов при ней. Рекомендация отменять ИАПФ или БРА1 у пациентов, получающих эти препараты и заразившихся вирусом SARS-CoV-2 или заболевших COVID-19, была названа преждевременной (базирующейся либо на спекулятивных, умозрительных рассуждениях, либо на неполных и противоречивых предварительных клинических данных), ошибочной, научно необоснованной, вредной или даже опасной для здоровья и жизни пациентов [Flacco ME et al, 2020; Hippisley-Cox J et al, 2020; Rossi GP et al, 2020].
Более того, было показано, что на самом деле прием ИАПФ или БРА1 во время лечения от инфекции COVID-19, или продолжение их приема у тех пациентов, которые их уже принимали до заражения, может оказывать защитное влияние в отношении риска развития острого респираторного дистресс-синдрома (ОРДС), а также в отношении риска развития тяжелых сердечно-сосудистых и почечных осложнений COVID-19, и способно уменьшать интенсивность системного и местного (в легочной ткани) воспаления и выраженность «цитокинового шторма». Кроме того, обнаружилось также, что прием ИАПФ или БРА1 может оказывать защитное влияние в отношении собственно риска заражения вирусом SARS-CoV-2 при контакте [South AM et al, 2020; Zhang X et al, 2020; Javanmard SH et al, 2020; Seif F et al, 2020].
Рассуждая по аналогии, легко прийти к мысли о том, что если ИАПФ и БРА1, то есть прямые лиганды или индукторы экспрессии основного клеточного рецептора, через который вирус SARS-CoV-2 способен проникать в организм — белка ACE2, — оказались полезными в лечении инфекции COVID-19, то и агонисты сигма-1 рецепторов, такие как флувоксамин (то есть лиганды «второстепенных ворот» для этого вируса), тоже могут оказаться потенциально полезными в лечении этой инфекции, и заслуживают изучения в этом качестве [Lenze EJ et al, 2020].
Кроме того, показано, что в экспериментах на животных сигма-1 агонисты, и в первую очередь самый мощный из них — флувоксамин, — эффективно уменьшают системное и местное воспаление, ограничивают секрецию воспалительных цитокинов и предотвращают развитие «цитокинового шторма», уменьшая тем самым вероятность неблагоприятного исхода при экспериментальном сепсисе. Этот эффект опосредуется взаимодействием активированных сигма-1 рецепторов с различными внутриклеточными мишенями, в том числе с одним из важных датчиков внутриклеточного стресса в эндоплазматическом ретикулуме — так называемым «инозитол-опосредованным ферментом 1α» (IRE1) [Rosen DA et al, 2019].
Еще одним теоретическим обоснованием для прицельного изучения потенциальной эффективности именно флувоксамина в лечении инфекции COVID-19 является то, что он, в отличие от всех других СИОЗС и прочих АД, клинически значимо ингибирует катаболизм в печени как эндогенного, так и экзогенного (принимаемого перорально) мелатонина, и значительно повышает концентрацию мелатонина в плазме крови [Demisch K, 1987; von Bahr С et al, 2000; Härtter S et al, 2000; 2001; Беккер РА, Быков ЮВ, 2019 (a), (b)].
Между тем положительное влияние экзогенного (перорально назначаемого) мелатонина на течение как новейшей инфекции COVID-19, так и ряда других, давно известных человечеству, вирусных инфекций, типа гриппа, которое связывают с мощными антиоксидантными, анти-свободнорадикальными, противовоспалительными и иммуномодулирующими свойствами этого гормона — хорошо известно. Ныне пероральный мелатонин входит во многие национальные протоколы и рекомендации по лечению COVID-19 [Anderson G, Reiter RJ, 2020; Zhang R et al, 2020; Giménez VM et al, 2020].
Существует даже предположение о том, что бóльшая в среднем тяжесть течения инфекции COVID-19 и более высокий риск тяжелых осложнений и летальных исходов при этой болезни у лиц пожилого и старческого возраста, по сравнению с более молодыми пациентами, — могут быть в значительной степени обусловлены именно выраженным снижением секреции эндогенного мелатонина с возрастом, наряду с влиянием других неблагоприятных факторов старения [Öztürk G et al, 2020].
В свете этого способность флувоксамина значительно повышать концентрацию эндогенного мелатонина в плазме крови и увеличивать биодоступность экзогенного (перорально принимаемого) мелатонина — может быть очень выгодным свойством именно этого АД при лечении пациентов с инфекцией COVID-19 [Lenze EJ et al, 2020; García IG et al, 2020].
Кроме того, флувоксамин обладает выраженными нейропротективными и кардиопротективными свойствами, проявляющимися в разных клинических ситуациях и в разных экспериментальных моделях (например, в модели ишемии и последующей реперфузии мозга или миокарда, в модели экспериментального аутоиммунного воспаления ЦНС, в модели нейротоксичности, обусловленной воздействием МДМА, кетамина, фенциклидина, бета-амилоида и др.) [Беккер РА, Быков ЮВ, 2019 (a)].
С учетом выраженных нейротропных (нейроинвазивных), кардиотоксических и нейротоксических свойств вируса SARS-CoV-2, выраженная нейропротективная и кардиопротективная активность флувоксамина также может иметь значение при лечении пациентов с COVID-19 этим препаратом.
Противовирусные свойства лигандов сигма-рецепторов
В настоящее время нет противовирусных препаратов с доказанной в широкомасштабных РКИ клинической эффективностью для терапии инфекции SARS-CoV-2. Скрининг лекарств в ходе множественных вирусных анализов выявил два набора фармакологических агентов, проявляющих противовирусную активность: ингибиторы трансляции мРНК и регуляторы рецепторов Sigma1 и Sigma2 [Gordon DE, et al. 2020].Репликация коронавирусов происходит в модифицированном мембранном комплексе, полученном из эндоплазматического ретикулума. Соответственно, влияние на ремоделирование эндоплазматического ретикулума вирусом может иметь решающее значение для выяснения новых терапевтических противовирусных подходов. Рецептор sigma-1 (Sig-1R) — это управляемый лигандом мембранный белок-шаперон — действует как модулятор стресса в эндоплазматическоме ретикулуме. Многие перепрофилированные лекарства, включенные в схемы терапии пациентов с COVID-19, часто идентифицируются как Лиганды Sig-1R in vitro. Sig-1R регулирует ключевые механизмы адаптивного стрессового ответа клеток-хозяев и принимает участие в ранних стадиях репликации вируса. Таргетирование Sig-1R, как ожидается, не приведет к резкому снижению установленной вирусной репликации, но оно может помешать ранним этапам индуцированного вирусом перепрограммирования клеток-хозяев, помочь замедлить течение инфекции, предотвратить обострение заболевания и/или создать временное окно для созревания защитного иммунного ответа. Препараты на основе Sig-1R могут принести пользу не только в качестве раннего вмешательства, профилактики, но и в качестве адъювантной терапии [Phadke M. 2020].
Основная проблема лигандов сигма-рецепторов в том, что противовирусный эффект у них развивается в токсичных или близким к токсичным для клеток человека концентрациях.
В то же время известен агент, обладающий высоким сродством к сигма-рецепторам Ki(nM)=17 и одновременно высоким терапевтическим индексом, разрешающим прием его в высоких (до 300 мг/сут) дозах. Речь идет о флувоксамине [S.B. Smith, 2017].
Предварительные результаты пилотного клинического изучения эффективности и безопасности флувоксамина при лечении инфекции COVID-19
 Протокол исследования
Протокол исследованияДетально описанные нами в предыдущем разделе теоретические предпосылки для возникновения интереса к изучению потенциальной эффективности флувоксамина в лечении COVID-19 послужили мотивацией для группы авторов из Вашингтона, США, предпринять первое пилотное исследование эффективности и безопасности флувоксамина в лечении этой новой инфекции [Lenze EJ et al, 2020].
Авторы этого исследования поставили своей задачей выяснить, может ли флувоксамин, назначаемый в качестве раннего средства лечения пациентам с легким течением инфекции COVID-19, уменьшить вероятность перехода этого заболевания в более тяжелую форму или полностью предотвратить такое развитие событий [Lenze EJ et al, 2020].
Цитируемое нами исследование являлось по своему дизайну двойным слепым плацебо-контролируемым, рандомизированным клиническим исследованием (РКИ). В нем сравнивалась эффективность и безопасность флувоксамина и плацебо в предотвращении неблагоприятных исходов и осложнений COVID-19 у взрослых амбулаторных пациентов с лабораторно (методом полимеразной цепной реакции — ПЦР) подтвержденной инфекцией вирусом SARS-CoV-2. Оно получило одобрение этической комиссии и институционального Наблюдательного совета Вашингтонского университета и проводилось в строгом соответствии с Хельсинкской декларацией [Lenze EJ et al, 2020].
Набор пациентов-добровольцев для участия в этом РКИ осуществлялся с апреля по август 2020 года. Для того, чтобы не подвергать как участников исследования, так и персонал клиники дополнительному риску заражения вирусом SARS-CoV-2, для этого исследования был разработан инновационный, полностью дистанционный (бесконтактный) телемедицинский протокол [Lenze EJ et al, 2020].
В это РКИ включались взрослые амбулаторные пациенты обоего пола (от 18 лет, без ограничения сверху по возрасту) с подтвержденной методом ПЦР инфекцией вирусом SARS-CoV-2, у которых наблюдались легкие симптомы COVID-19 в течение как минимум 7 дней, предшествующих рандомизации. Критерии исключения из исследования включали среднетяжелое или тяжелое течение инфекции COVID-19, при котором требовалась госпитализация, амбулаторное назначение кислородной поддержки, либо при котором насыщение артериальной крови пациента кислородом составляло менее 92% при дыхании атмосферным воздухом, на момент рандомизации, а также, наоборот, бессимптомное течение инфекции SARS-CoV-2 [Lenze EJ et al, 2020].
Другими критериями исключения из исследования были наличие у кандидата предсуществующих тяжелых бронхолегочных заболеваний (хронической обструктивной болезни легких — ХОБЛ, легочного фиброза, легочной гипертензии), декомпенсированного цирроза печени, тяжелой хронической сердечной недостаточности (ХСН) III или IV функционального класса, а также наличие у кандидата выраженной иммуносупрессии (получение химиотерапии по поводу злокачественных новообразований, получение иммуносупрессивной терапии по поводу трансплантации органов, трансплантации костного мозга или по поводу аутоиммунных и ревматических заболеваний, прием высоких доз глюкокортикоидов по любой причине) [Lenze EJ et al, 2020].
В конечном итоге в этом РКИ приняли участие 152 взрослых амбулаторных пациента обоего пола с лабораторно подтвержденной инфекцией SARS-CoV-2 и с легкими симптомами COVID-19. Средний возраст участников составлял 46 лет. Все пациенты были стратифицированы на четыре возрастные когорты (от 18 до 44 лет, от 45 до 54 лет, от 55 до 64 лет и старше 65 лет). Рандомизация проводилась раздельно в каждой из возрастных когорт. В общей сложности 80 пациентов попали в группу флувоксамина, и 72 пациента — в группу плацебо. При этом авторы исследования тщательно следили за максимально возможным совпадением всех демографических и клинических характеристик пациентов как в группе плацебо, так и в группе флувоксамина [Lenze EJ et al, 2020].
В частности, средний уровень насыщения артериальной крови кислородом при дыхании атмосферным воздухом (важнейший показатель степени поражения легких при COVID-19) на момент рандомизации не отличался в группах плацебо и флувоксамина, и в обеих группах составлял 97% [Lenze EJ et al, 2020].
Описание самого вмешательства
Все участники этого РКИ получали первую дозу лекарства (50 мг флувоксамина или плацебо, в зависимости от того, в какую из двух групп попал участник после рандомизации) вечером сразу после предварительной (до начала исследования) оценки жизненно важных показателей (насыщения артериальной крови кислородом, частоты сердечных сокращений, величины артериального давления, температуры тела) и подтверждения пригодности участника в качестве кандидата в это РКИ [Lenze EJ et al, 2020].Затем в течение 2 последующих дней доза флувоксамина в группе активного лечения постепенно увеличивалась до 100 мг 2 раза в сутки (200 мг/сут), если позволяла переносимость. После 2 дней приема этой дозы — дозу флувоксамина в группе активного лечения снова увеличивали до 100 мг 3 раза в сутки (300 мг/сут), если позволяла переносимость. В группе плацебо, для обеспечения адекватного ослепления, аналогичным образом проводилось поэтапное увеличение дозы и кратности приема плацебо [Lenze EJ et al, 2020].
Желаемая конечная доза флувоксамина 300 мг/сут была выбрана авторами этого РКИ, исходя из доступных в литературе данных об аффинности флувоксамина in vitro к человеческим сигма-1 рецепторам и о степени занятости этих рецепторов in vivo при приеме различных доз флувоксамина, по данным позитронно-эмиссионной томографии (ПЭТ) [Lenze EJ et al, 2020].
Эту дозу флувоксамина или плацебо пациенты должны были продолжать принимать в двойном слепом режиме на протяжении 15 дней, после чего пациентам из группы активного лечения предоставлялась возможность либо прекратить дальнейший прием флувоксамина, либо продолжить его уже в открытом режиме на протяжении еще 6 дней. Стоит отметить, что введение 6-дневной открытой фазы исследования после завершения основной фазы РКИ не предусматривалось первоначальным протоколом исследования [Lenze EJ et al, 2020].
Первичной конечной точкой в этом РКИ служило наличие или отсутствие ухудшения клинической картины COVID-19 за период приема, соответственно, флувоксамина или плацебо. Клиническое ухудшение определялось авторами этого РКИ как проявление одышки, или вынужденная госпитализация пациента по поводу одышки или по поводу развития пневмонии, или снижение насыщения артериальной крови кислородом при дыхании атмосферным воздухом ниже 92%, или появление необходимости в дополнительной кислородной поддержке для обеспечения насыщения крови кислородом на уровне 92% и выше [Lenze EJ et al, 2020].
Результаты исследования
ЭффективностьАвторы данного РКИ показали, что ухудшение клинического течения COVID-19 не наблюдалось ни у одного из 80 пациентов в группе флувоксамина (0%). В то же время оно наблюдалось у 6 из 72 (8,3%) пациентов в группе плацебо. Абсолютная разница шансов клинического ухудшения между группами, по данным статистического анализа, составила 8,7% (доверительный интервал 95%, диапазон от 1,8% до 16,4%, p=0,009) [Lenze EJ et al, 2020].
В группе плацебо момент начала клинического ухудшения отмечался в период от 1 до 7 дней после рандомизации, или от 3 до 12 дней после появления первых симптомов COVID-19. Это в целом совпадает с тем, что мы сегодня знаем о типичном течении инфекции COVID-19 (необходимость в госпитализации или клиническое ухудшение обычно наступает после 8–10 дней первоначально легких или среднетяжелых симптомов болезни) [Lenze EJ et al, 2020].
Четырем из шести пациентов в группе плацебо, у которых наступило ухудшение клинического течения COVID-19, потребовалась госпитализация. Продолжительность пребывания в больнице в этих случаях колебалась от 4 дней до 21 дня. Одному из этих пациентов потребовалась ИВЛ в течение 10 суток [Lenze EJ et al, 2020].
В группе плацебо также чаще отмечалось развитие пневмонии (6 человек, против 3 человек в группе флувоксамина), развитие одышки или затруднения дыхания (4 человека, против 2 человек в группе флувоксамина) [Lenze EJ et al, 2020].
Ниже мы приводим колоколообразный график распределения исходной (до начала исследования) величины насыщения артериальной крови кислородом при дыхании атмосферным воздухом в обеих группах — флувоксамина и плацебо. Как можно видеть из этого графика, медианная величина исходного насыщения артериальной крови кислородом достоверно не различалась в обеих группах (97% в группе флувоксамина, 97% в группе плацебо). Также на этом графике видно, что все шесть случаев клинического ухудшения течения COVID-19 в группе плацебо (отмечены на графике оранжевым цветом) — приходятся на левую часть кривой, то есть — на тех пациентов, у которых исходное насыщение крови кислородом хотя и было выше допустимой для отбора в данное РКИ границы (92%), но было ниже или равно 96%, — иначе говоря, на исходно более тяжелых пациентов [Lenze EJ et al, 2020].
Безопасность и побочные эффекты
В группе, получавшей флувоксамин (80 человек), был зарегистрирован один ПЭ, расцененный авторами как серьезный (вазовагальный обморок), и 11 легких ПЭ, которые типичны для всей группы СИОЗС, в частности головная боль у 2 пациентов, тошнота, рвота и диарея у 1 пациента, болезненное мышечное напряжение — у 1 пациента, тризм челюстей или бруксизм (скрежетание зубов) — у 1 пациента [Lenze EJ et al, 2020].В то же время в группе, получавшей плацебо (72 человека), было зарегистрировано 6 ПЭ, которые были расценены авторами данного РКИ как серьезные (в частности, один эпизод сильной головной боли, потребовавший визита пациента в отделение экстренной помощи стационара), и 12 ПЭ, расцененных авторами данного РКИ как легкие [Lenze EJ et al, 2020].
Интересно отметить, что ПЭ со стороны ЖКТ, такие как тошнота, рвота, диарея, развивались в группе плацебо чаще, чем в группе флувоксамина (5 человек, против 1 человека в группе флувоксамина) [Lenze EJ et al, 2020].
Заключение
Как можно видеть из процитированных нами данных первого пилотного РКИ, посвященного исследованию эффективности и безопасности флувоксамина в лечении COVID-19, флувоксамин может быть эффективным средством предотвращения или снижения вероятности клинического ухудшения у взрослых амбулаторных пациентов с легкими формами этого заболевания.При этом флувоксамин, в отличие от многих других упоминавшихся нами в данной статье иммуномодулирующих и противовоспалительных препаратов, ранее изучавшихся или изучаемых в настоящее время как перспективные средства для лечения COVID-19, весьма безопасен и хорошо переносится, и имеет низкий уровень ПЭ. В частности, ПЭ со стороны ЖКТ в описываемом нами РКИ отмечались в группе плацебо вдвое чаще, чем в группе флувоксамина.
Вместе с тем следует иметь в виду, что данное РКИ является пилотным. Оно имеет определенные ограничения, связанные, в частности, с тем, что в нем участвовало сравнительно небольшое количество участников (всего 152 человека) и только из одной географической области (федеральный округ Вашингтон в США). Сами авторы цитируемого нами РКИ подчеркивают, что выводы их исследования о возможной эффективности флувоксамина в качестве средства предотвращения тяжелого течения или средства смягчения течения COVID-19 следует воспринимать как предварительные, и что они нуждаются в воспроизведении на более крупных и более гетерогенных (и по географическому местоположению, и по этническому составу, и по тяжести течения и т.д.) выборках пациентов с COVID-19.
В то же время, учитывая ограниченность имеющихся сегодня терапевтических опций для лечения COVID-19, плохую переносимость многих из них, а также резкое повышение актуальности проблемы депрессий, тревожных состояний, ПТСР и ОКР в популяции, страдающей от пандемии COVID-19 (то есть повышение актуальности основных показаний к назначению флувоксамина, согласно его инструкции по применению), эти выводы, сколь бы предварительными они ни были, заслуживают особого внимания — и клинического применения уже сегодня.
Авторы цитируемого нами РКИ также указывают, что их собственное исследование мотивировалось гипотезой о том, что флувоксамин может быть эффективен в лечении COVID-19 вследствие своего агонизма к сигма-1 рецепторам (S1R) и угнетающего влияния на секрецию воспалительных цитокинов через внутриклеточный сигнальный каскад S1R-IRE1. Если эта гипотеза верна, то положительное действие флувоксамина на клиническое течение COVID-19 подобно действию при этой патологии других антицитокиновых и противовоспалительных препаратов, таких как колхицин или гидроксихлорохин.
Возможные альтернативные или дополнительные механизмы полезного действия флувоксамина на клиническое течение COVID-19 включают в себя его прямое противовирусное действие (угнетение проникновения вируса SARS-CoV-2 в клетку) за счет прямого связывания с «альтернативными воротами проникновения вируса», каковыми являются сигма-1 рецепторы (S1R), а также за счет лизосомотропного действия флувоксамина и функционального угнетения им активности кислой сфингомиелиназы, за счет его влияния на pH внутри лизосом, за счет модулирующего влияния флувоксамина на процессы аутофагии через сигнальный путь S1R-IRE1, или за счет угнетения им агрегации тромбоцитов и предотвращения свойственной COVID-19 гиперкоагуляции, или за счет повышения содержания эндогенного мелатонина в плазме крови и повышения биодоступности экзогенного мелатонина (полезность мелатонина при COVID-19 уже показана), а также, возможно, за счет каких-то других его эффектов, например нейро- и кардиопротективного.
Нельзя при этом сбрасывать со счетов и основное клиническое действие флувоксамина — антистрессовое, антидепрессивное и противотревожное, поскольку показано, что депрессия, тревога и хронический стресс сами по себе являются независимыми факторами риска тяжелого течения инфекции COVID-19.
Важными потенциальными преимуществами применения флувоксамина как средства амбулаторного лечения COVID-19 являются его высокая безопасность, хорошая переносимость, низкий уровень ПЭ (особенно по сравнению с такими препаратами, как, например, гидроксихлорохин или азитромицин), широкая доступность этого препарата на рынке, его низкая стоимость (особенно по сравнению с такими, например, препаратами, как инфликсимаб или анакинра), возможность его перорального приема (в отличие от многих антицитокиновых препаратов, которые требуют исключительно внутривенного введения).
В отличие от многих других альтернативных иммуномодуляторов, предлагавшихся для лечения COVID-19, таких как хлорохин, гидроксихлорохин, азитромицин, а также в отличие от ТЦА и от некоторых других СИОЗС (например, от эсциталопрама и циталопрама) — флувоксамин не способствует удлинению интервала QT на ЭКГ. Поэтому он не обладает аритмогенным или кардиотоксическим действием. Это особенно важно при лечении пожилых пациентов или пациентов с предсуществующими заболеваниями сердца.
Вместе с тем при сочетанном применении флувоксамина с другими лекарственными препаратами следует всегда помнить и учитывать, что флувоксамин является мощным ингибитором изоферментов цитохрома печени P450 1А2 и 2С19. Поэтому он способен значительно повышать концентрации в плазме крови тех лекарств, которые метаболизируются всецело или в значительной степени при помощи этих изоферментов (например, теофиллина и аминофиллина). Однако большинство применяемых сегодня в медицине лекарственных препаратов метаболизируются всецело или в основном при помощи изофермента P450 2D6.
В свете представленных данных, на сегодняшний день представляется оправданным использовать флувоксамин как антидепрессант первого выбора для терапии депрессии и ОКР у пациентов с риском заражения COVID-19. Ожидания от терапии включают: улучшение психического состояния этих пациентов, уменьшение тревоги, депрессии, нарушений сна, проявления ОКР, а также снижение рисков развития осложнений при COVID-19.
Список исп. литературыСкрыть список1. Беккер Р.А., Быков Ю.В. Тревожные и диссомнические депрессии: клиника, диагностика, терапия и эффективность препарата Рокона® (флувоксамин). Психиатрия и психофармакотерапия им. П. Б. Ганнушкина.2019;21(3):17-23.
2. Беккер Р.А, Быков Ю.В. Флувоксамин: антидепрессант широкого спектра с рядом особенностей и преимуществ (обзор литературы). Психиатрия и психофармакотерапия им. П.Б. Ганнушкина. 2019;21(1):11-26.
3. Морозов П.В, Петрова Н.Н. О подходах к терапии и предупреждению обсессивно-компульсивных расстройств (ОКР) в период пандемии COVID-19 (обзор международных рекомендаций). Психиатрия и психофармакотерапия им. П.Б. Ганнушкина. 2020;02:37-40.
4. Мосолов С.Н. Проблемы психического здоровья в условиях пандемии COVID-19. Журнал неврологии и психиатрии им. С.С. Корсакова. 2020;120(5):7-15. DOI: 10.17116/jnevro20201200517.
5. Ahorsu DK, Lin CY, Pakpour AH. The Association Between Health Status and Insomnia, Mental Health, and Preventive Behaviors: The Mediating Role of Fear of COVID-19. Gerontol Geriatr Med. 2020;6: 2333721420966081. DOI: 10.1177/2333721420966081.
6. Albayrak Y, Hashimoto K. Sigma-1 Receptor Agonists and Their Clinical Implications in Neuropsychiatric Disorders. Adv Exp Med Biol. 2017;964:153-161. DOI: 10.1007/978-3-319-50174-1_11.
7. Aleebrahim-Dehkordi E, Soveyzi F, Deravi N et al. Human coronaviruses SARS-CoV, MERS-CoV, and SARS-CoV-2 in children. J Pediatr Nurs. 2020;56:70-79. DOI: 10.1016/j.pedn.2020.10.020.
8. Al-Samkari H, Leaf RK, Dzik WH et al. COVID-19 and coagulation: bleeding and thrombotic manifestations of SARS-CoV-2 infection. Blood. 2020;136(4):489-500. DOI: 10.1182/blood.2020006520.
9. Altschuler EL, Kast RE. Dapsone, colchicine and olanzapine as treatment adjuncts to prevent COVID-19 associated adult respiratory distress syndrome (ARDS). Med Hypotheses. 2020;141:109774. DOI: 10.1016/j.mehy.2020.109774.
10. Amraei R, Rahimi N. COVID-19, Renin-Angiotensin System and Endothelial Dysfunction. Cells. 2020;9(7):1652. DOI: 10.3390/cells9071652.
11. Anderson G, Reiter RJ. Melatonin: Roles in influenza, Covid-19, and other viral infections. Rev Med Virol. 2020;30(3):e2109. DOI: 10.1002/rmv.2109.
12. Arshad S, Kilgore P, Chaudhry ZS et al. Treatment with hydroxychloroquine, azithromycin, and combination in patients hospitalized with COVID-19. Int J Infect Dis. 2020;97:396-403. DOI: 10.1016/j.ijid.2020.06.099.
13. Bikdeli B, Madhavan MV, Jimenez D et al. COVID-19 and Thrombotic or Thromboembolic Disease: Implications for Prevention, Antithrombotic Therapy, and Follow-Up: JACC State-of-the-Art Review. J Am Coll Cardiol. 2020;75(23):2950-2973. doi: 10.1016/j.jacc.2020.04.031.
14. Canli T. A model of human endogenous retrovirus (HERV) activation in mental health and illness. Med Hypotheses. 2019;133:109404. DOI: 10.1016/j.mehy.2019.109404.
15. Canli T. Reconceptualizing major depressive disorder as an infectious disease. Biol Mood Anxiety Disord. 2014;4:10. DOI: 10.1186/2045-5380-4-10.
16. Caruso A, Caccuri F, Bugatti A et al. Methotrexate inhibits SARS-CoV-2 virus replication "in vitro". J Med Virol. 2020. DOI: 10.1002/jmv.26512.
17. Chaná-Cuevas P, Salles-Gándara P, Rojas-Fernandez A et al. The Potential Role of SARS-COV-2 in the Pathogenesis of Parkinson's Disease. Front Neurol. 2020;11:1044. DOI: 10.3389/fneur.2020.01044.
18. Choi EH, Hui BH, Wan EF. Depression and Anxiety in Hong Kong during COVID-19. Int J Environ Res Public Health. 2020;17(10):3740. DOI: 10.3390/ijerph17103740.
19. Choudhary R, Sharma AK. Potential use of hydroxychloroquine, ivermectin and azithromycin drugs in fighting COVID-19: trends, scope and relevance. New Microbes New Infect. 2020;35:100684. DOI: 10.1016/j.nmni. 2020.100684.
20. Chow JH, Khanna AK, Kethireddy S et al. Aspirin Use is Associated with Decreased Mechanical Ventilation, ICU Admission, and In-Hospital Mortality in Hospitalized Patients with COVID-19. Anesth Analg. 2020. DOI: 10.1213/ANE.0000000000005292.
21. Cobos EJ, Entrena JM, Nieto FR et al. Pharmacology and therapeutic potential of sigma(1) receptor ligands. Curr Neuropharmacol. 2008;6(4):344-366. DOI: 10.2174/157015908787386113.
22. Czeisler ME, Lane RI, Petrosky E et al. Mental Health, Substance Use, and Suicidal Ideation During the COVID-19 Pandemic - United States, June 24-30, 2020. MMWR Morb Mortal Wkly Rep. 2020;69(32):1049-1057. DOI: 10.15585/mmwr.mm6932a1.
23. Davies J, Randeva HS, Chatha K et al. Neuropilin‑1 as a new potential SARS‑CoV‑2 infection mediator implicated in the neurologic features and central nervous system involvement of COVID‑19. Mol Med Rep. 2020;22(5):4221-4226. DOI: 10.3892/mmr.2020.11510.
24. Demisch K, Demisch L, Nickelsen T et al. The influence of acute and subchronic administration of various antidepressants on early morning melatonin plasma levels in healthy subjects: increases following fluvoxamine. J Neural Transm. 1987;68(3-4):257-270. DOI: 10.1007/BF02098502.
25. Farouk A, Salman S. Dapsone and doxycycline could be potential treatment modalities for COVID-19. Med Hypotheses. 2020;140:109768. DOI: 10.1016/j.mehy.2020.109768.
26. Figueroa CA, Aguilera A. The Need for a Mental Health Technology Revolution in the COVID-19 Pandemic. Front Psychiatry. 2020;11:523. DOI: 10.3389/fpsyt.2020.00523.
27. Flacco ME, Martellucci CA, Bravi F et al. Treatment with ACE inhibitors or ARBs and risk of severe/lethal COVID-19: a meta-analysis. Heart. 2020;106(19):1519-1524. DOI: 10.1136/heartjnl-2020-317336.
28. Frohman EM, Villemarette-Pittman NR, Cruz RA et al. Part II. high-dose methotrexate with leucovorin rescue for severe COVID-19: An immune stabilization strategy for SARS-CoV-2 induced 'PANIC' attack. J Neurol Sci. 2020;415:116935. DOI: 10.1016/j.jns.2020.116935.
29. Gale SD, Berrett AN, Erickson LD et al. Association between virus exposure and depression in US adults. Psychiatry Res. 2018;261:73-79. DOI: 10.1016/j.psychres.2017.12.037.
30. García IG, Rodriguez-Rubio M, Mariblanca AR et al. A randomized multicenter clinical trial to evaluate the efficacy of melatonin in the prophylaxis of SARS-CoV-2 infection in high-risk contacts (MeCOVID Trial): A structured summary of a study protocol for a randomised controlled trial. Trials. 2020;21(1):466. DOI: 10.1186/s13063-020-04436-6.
31. Gautam SS, Gautam CS, Garg VK et al. Combining hydroxychloroquine and minocycline: potential role in moderate to severe COVID-19 infection. Expert Rev Clin Pharmacol. 2020;13(11):1183-1190. DOI: 10.1080/17512433.2020.1832889.
32. Gautret P, Lagier JC, Parola P et al. Clinical and microbiological effect of a combination of hydroxychloroquine and azithromycin in 80 COVID-19 patients with at least a six-day follow up: A pilot observational study. Travel Med Infect Dis. 2020;34:101663. DOI: 10.1016/j.tmaid.2020.101663.
33. Giménez VM, Inserra F, Tajer CD et al. Lungs as target of COVID-19 infection: Protective common molecular mechanisms of vitamin D and melatonin as a new potential synergistic treatment. Life Sci. 2020;254:117808. DOI: 10.1016/j.lfs.2020.117808.
34. Gomeni R, Xu T, Gao X et al. Model based approach for estimating the dosage regimen of indomethacin a potential antiviral treatment of patients infected with SARS CoV-2. J Pharmacokinet Pharmacodyn. 2020;47(3): 189-198. DOI: 10.1007/s10928-020-09690-4.
35. Gordon DE, Jang GM, Bouhaddou M, et al. A SARS-CoV-2 protein interaction map reveals targets for drug repurposing. Nature. 2020 Jul;583(7816):459-468. doi: 10.1038/s41586-020-2286-9.
36. Guisado-Vasco P, Valderas-Ortega S, Carralón-González MM et al. Clinical characteristics and outcomes among hospitalized adults with severe COVID-19 admitted to a tertiary medical center and receiving antiviral, antimalarials, glucocorticoids, or immunomodulation with tocilizumab or cyclosporine: A retrospective observational study (COQUIMA cohort). EClinicalMedicine. 2020;100591. DOI: 10.1016/j.eclinm.2020.100591.
37. Härtter S, Grözinger M, Weigmann H et al. Increased bioavailability of oral melatonin after fluvoxamine coadministration. Clin Pharmacol Ther. 2000;67(1):1-6. DOI: 10.1067/mcp.2000.104071.
38. Härtter S, Wang X, Weigmann H et al. Differential effects of fluvoxamine and other antidepressants on the biotransformation of melatonin. J Clin Psychopharmacol. 2001;21(2):167-74. DOI: 10.1097/00004714-200104 000-00008.
39. Hippisley-Cox J, Young D, Coupland С et al. Risk of severe COVID-19 disease with ACE inhibitors and angiotensin receptor blockers: cohort study including 8.3 million people. Heart. 2020;106(19):1503-1511. DOI: 10.1136/heartjnl-2020-317393.
40. Homolak J, Kodvanj I. Widely available lysosome targeting agents should be considered as potential therapy for COVID-19. Int J Antimicrob Agents. 2020;56(2):106044. DOI: 10.1016/j.ijantimicag.2020.106044.
41. https://www.covid19‐druginteractions.org Информация о взаимодействии противовирусных лекарств с психотропными и другими препаратами с сайта отделения клинической фармакологии Ливерпульского университета. Адаптировано С.Н. Мосоловым для РФ в 2020 г. Доступ проверен 18.11.2020 г.
42. https://www.kff.org/coronavirus-covid-19/issue-brief/the-implications-of-covid-19-for-mental-health-... Отчет KFF о последствиях COVID-19 для психического и наркологического здоровья популяции. Опубликовано 21.09.2020. Доступ проверен 18.11.2020.
43. Hu K, Wang M, Zhao Y et al. A Small-Scale Medication of Leflunomide as a Treatment of COVID-19 in an Open-Label Blank-Controlled Clinical Trial. Virol Sin. 2020;1-9. DOI: 10.1007/s12250-020-00258-7.
44. Javanmard SH, Heshmat-Ghahdarijani K, Vaseghi G. Angiotensin-converting-enzyme inhibitors (ACE inhibitors) and angiotensin II receptor blocker (ARB) use in COVID-19 prevention or treatment: A paradox. Infect Control Hosp Epidemiol. 2020;1-2. DOI: 10.1017/ice.2020.195.
45. Karampela I, Dalamaga M. Could Respiratory Fluoroquinolones, Levofloxacin and Moxifloxacin, Prove to be Beneficial as an Adjunct Treatment in COVID-19? Arch Med Res. 2020;51(7):741-742. DOI: 10.1016/j.arcmed.2020.06.004.
46. Kornhuber J, Muehlbacher M, Trapp S et al. Identification of novel functional inhibitors of acid sphingomyelinase. PLoS One. 2011;6(8):e23852. DOI: 10.1371/journal.pone.0023852.
47. Le HT, Lai AX, Sun J et al. Anxiety and Depression Among People Under the Nationwide Partial Lockdown in Vietnam. Front Public Health. 2020;8:589359. DOI: 10.3389/fpubh.2020.589359.
48. Lee SA, Jobe MC, Mathis AA et al. Incremental validity of coronaphobia: Coronavirus anxiety explains depression, generalized anxiety, and death anxiety. J Anxiety Disord. 2020;74:102268. DOI: 10.1016/j.janxdis.2020.102268.
49. Lee SW, Yang JM, Moon SY et al. Association between mental illness and COVID-19 susceptibility and clinical outcomes in South Korea: a nationwide cohort study. Lancet Psychiatry. 2020;S2215-0366(20)30421-1. DOI: 10.1016/S2215-0366(20)30421-1.
50. Lenze EJ, Mattar C, Zorumski CF et al. Fluvoxamine vs Placebo and Clinical Deterioration in Outpatients With Symptomatic COVID-19: A Randomized Clinical Trial. JAMA. 2020;e2022760. DOI: 10.1001/jama. 2020.22760.
51. Liu C, von Brunn A, Zhu D. Cyclophilin A and CD147: novel therapeutic targets for the treatment of COVID-19. Med Drug Discov. 2020;7:100056. DOI: 10.1016/j.medidd.2020.100056.
52. Marciniec K, Beberok A, Pęcak P et al. Ciprofloxacin and moxifloxacin could interact with SARS-CoV-2 protease: preliminary in silico analysis. Pharmacol Rep. 2020;1-9. DOI: 10.1007/s43440-020-00169-0.
53. Marinella MA. Indomethacin and resveratrol as potential treatment adjuncts for SARS-CoV-2/COVID-19. Int J Clin Pract. 2020;74(9):e13535. DOI: 10.1111/ijcp.13535.
54. Marshall M. How COVID-19 can damage the brain. Nature. 2020;585(7825):342-343. DOI: 10.1038/d41586-020-02599-5.
55. Mattos-Silva P, Felix NS, Silva PL et al. Pros and cons of corticosteroid therapy for COVID-19 patients. Respir Physiol Neurobiol. 2020;280:103492. DOI: 10.1016/j.resp.2020.103492.
56. McFee RB. COVID-19: Therapeutics and interventions currently under consideration. Dis Mon. 2020;101058. DOI: 10.1016/j.disamonth.2020. 101058.
57. Mishra R, Banerjea AC. Neurological Damage by Coronaviruses: A Catastrophe in the Queue! Front Immunol. 2020;11:565521. DOI: 10.3389/fimmu.2020.565521.
58. Nanda S, Handa R, Prasad A, Anand R et al. Covid-19 associated Guillain-Barre Syndrome: Contrasting tale of four patients from a tertiary care centre in India. Am J Emerg Med. 2020;S0735-6757(20)30823-8. DOI: 10.1016/j.ajem.2020.09.029.
59. Narita N, Hashimoto K, Tomitaka S et al. Interactions of selective serotonin reuptake inhibitors with subtypes of sigma receptors in rat brain. Eur J Pharmacol. 1996;307(1):117-119. DOI: 10.1016/0014-2999(96)00254-3.
60. Ozamiz-Etxebarria N, Dosil-Santamaria M, Picaza-Gorrochategui M et al. Stress, anxiety, and depression levels in the initial stage of the COVID-19 outbreak in a population sample in the northern Spain. Cad Saude Publica. 2020;36(4):e00054020. DOI: 10.1590/0102-311X00054020.
61. Özdin S, Özdin SB. Levels and predictors of anxiety, depression and health anxiety during COVID-19 pandemic in Turkish society: The importance of gender. Int J Soc Psychiatry. 2020;66(5):504-511. DOI: 10.1177/ 0020764020927051.
62. Öztürk G, Akbulut KG, Güney S. Melatonin, aging, and COVID-19: Could melatonin be beneficial for COVID-19 treatment in the elderly? Turk J Med Sci. 2020;50(6):1504-1512. DOI: 10.3906/sag-2005-356.
63. Pappa S, Ntella V, Giannakas T et al. Prevalence of depression, anxiety, and insomnia among healthcare workers during the COVID-19 pandemic: A systematic review and meta-analysis. Brain Behav Immun. 2020;88:901-907. DOI: 10.1016/j.bbi.2020.05.026.
64. Pierce M, Hope H, Ford T et al. Mental health before and during the COVID-19 pandemic: a longitudinal probability sample survey of the UK population. Lancet Psychiatry. 2020;7:883-892. DOI: 10.1016/S2215-0366(20)30308-4.
65. Phadke M, Saunik S. COVID-19 treatment by repurposing drugs until the vaccine is in sight. Drug Dev Res. 2020 Aug;81(5):541-543. doi: 10.1002/ddr.21666.
66. Reger MA, Stanley IH, Joiner TE. Suicide Mortality and Coronavirus Disease 2019-A Perfect Storm? JAMA Psychiatry. 2020. DOI: 10.1001/jamapsychiatry.2020.1060.
67. Revannasiddaiah S, Devadas SK, Palassery R et al. A potential role for cyclophosphamide in the mitigation of acute respiratory distress syndrome among patients with SARS-CoV-2. Med Hypotheses. 2020;144:109850. DOI: 10.1016/j.mehy.2020.109850.
68. Rogers JP, Chesney E, Oliver D et al. Psychiatric and neuropsychiatric presentations associated with severe coronavirus infections: a systematic review and meta-analysis with comparison to the COVID-19 pandemic. Lancet Psychiatry. 2020;7(7):611-627. DOI: 10.1016/S2215-0366(20)30203-0.
69. Rosen DA, Seki SM, Fernández-Castañeda A et al. Modulation of the sigma-1 receptor-IRE1 pathway is beneficial in preclinical models of inflammation and sepsis. Sci Transl Med. 2019;11(478):eaau5266. DOI: 10.1126/scitranslmed.aau5266.
70. Rossi GP, Sanga V, Barton M. Potential harmful effects of discontinuing ACE-inhibitors and ARBs in COVID-19 patients. Elife. 2020;9:e57278. DOI: 10.7554/eLife.57278.
71. Rudnicka L, Glowacka P, Goldust M et al. Cyclosporine therapy during the COVID-19 pandemic. J Am Acad Dermatol. 2020;83(2):e151-e152. DOI: 10.1016/j.jaad.2020.04.153.
72. Schloer S, Brunotte L, Goretzko J et al. Targeting the endolysosomal host-SARS-CoV-2 interface by clinically licensed functional inhibitors of acid sphingomyelinase (FIASMA) including the antidepressant fluoxetine. Emerg Microbes Infect. 2020;9(1):2245-2255. DOI: 10.1080/22221751. 2020.1829082.
73. Schnittker J. In-utero determinants of adult depression: evidence from the 1918 flu pandemic. Biodemography Soc Biol. 2020;65(3):227-244. DOI: 10.1080/19485565.2020.1744424.
74. Schön MP, Berking C, Biedermann T et al. COVID-19 and immunological regulations - from basic and translational aspects to clinical implications. J Dtsch Dermatol Ges. 2020;10.1111/ddg.14169. DOI: 10.1111/ddg.14169.
75. Seif F, Aazami H, Khoshmirsafa M et al. JAK Inhibition as a New Treatment Strategy for Patients with COVID-19. Int Arch Allergy Immunol. 2020;181(6):467-475. DOI: 10.1159/000508247.
76. Seif F, Pornour M, Mansouri D. Combination of JAKinibs with Methotrexate or Anti-Cytokine Biologics in Patients with Severe COVID-19. Int Arch Allergy Immunol. 2020;181(8):648-649. DOI: 10.1159/000509198.
77. Singh H, Kakkar AK, Chauhan P. Repurposing minocycline for COVID-19 management: mechanisms, opportunities, and challenges. Expert Rev Anti Infect Ther. 2020;18(10):997-1003. DOI: 10.1080/14787210. 2020.1782190.
78. S.B. Smith, T.-P. Su (eds.), Sigma Receptors: Their Role in Disease and as Therapeutic Targets, 2017, Advances in Experimental Medicine and Biology 964, DOI 10.1007/978-3-319-50174-1_11
79. South AM, Diz DI, Chappell MC. COVID-19, ACE2, and the cardiovascular consequences. Am J Physiol Heart Circ Physiol. 2020;318(5):H1084-H1090. DOI: 10.1152/ajpheart.00217.2020.
80. Stanton R, To QG, Khalesi S et al. Depression, Anxiety and Stress during COVID-19: Associations with Changes in Physical Activity, Sleep, Tobacco and Alcohol Use in Australian Adults. Int J Environ Res Public Health. 2020;17(11):4065. DOI: 10.3390/ijerph17114065.
81. Stein MB. COVID-19 and Anxiety and Depression in 2020. Depress Anxiety. 2020;37:302. DOI: 10.1002/da.22870.
82. Tomazini BM, Maia IS, Cavalcanti AB et al. Effect of Dexamethasone on Days Alive and Ventilator-Free in Patients With Moderate or Severe Acute Respiratory Distress Syndrome and COVID-19: The CoDEX Randomized Clinical Trial. JAMA. 2020;324(13):1307-1316. DOI: 10.1001/jama.2020.17021.
83. Tsai YC, Tsai TF. Oral disease-modifying antirheumatic drugs and immunosuppressants with antiviral potential, including SARS-CoV-2 infection: a review. Ther Adv Musculoskelet Dis. 2020;12:1759720X20947296. DOI: 10.1177/1759720X20947296.
84. Ugurel OM, Mutlu O, Sariyer E et al. Evaluation of the potency of FDA-approved drugs on wild type and mutant SARS-CoV-2 helicase (Nsp13). Int J Biol Macromol. 2020;163:1687-1696. DOI: 10.1016/j.ijbiomac.2020.09.138.
85. Uyaroğlu OA, Güven GS, Güllü I. Can Levamisole be used in the treatment of COVID-19 patients presenting with diarrhea? J Infect Dev Ctries. 2020;14(8):844-846. DOI: 10.3855/jidc.13101.
86. von Bahr C, Ursing C, Yasui N et al. Fluvoxamine but not citalopram increases serum melatonin in healthy subjects - an indication that cytochrome P450 CYP1A2 and CYP2C19 hydroxylate melatonin. Eur J Clin Pharmacol. 2000;56(2):123-127. DOI: 10.1007/s002280050729.
87. Wadoo O, Latoo J, Reagu SM et al. Mental health during COVID-19 in Qatar. Gen Psychiatr. 2020;33(6):e100313. DOI: 10.1136/gpsych-2020-100313.
88. Wang M, Zhao Y, Hu W et al. Treatment of COVID-19 Patients with Prolonged Post-Symptomatic Viral Shedding with Leflunomide - a Single-Center, Randomized, Controlled Clinical Trial. Clin Infect Dis. 2020;ciaa1417. DOI: 10.1093/cid/ciaa1417.
89. Yesilkaya UH, Balcioglu YH, Sahin S. Reissuing the sigma receptors for SARS-CoV-2. J Clin Neurosci. 2020;80:72-73. DOI: 10.1016/j.jocn. 2020.08.014.
90. Zhang R, Wang X, Ni L et al. COVID-19: Melatonin as a potential adjuvant treatment. Life Sci. 2020;250:117583. DOI: 10.1016/j.lfs.2020.117583.
91. Zhang WR, Wang KW, Yin L et al. Mental Health and Psychosocial Problems of Medical Health Workers during the COVID-19 Epidemic in China. Psychother Psychosom. 2020;89(4):242-250. DOI: 10.1159/000507639.
92. Zhang X, Li S, Niu S. ACE2 and COVID-19 and the resulting ARDS. Postgrad Med J. 2020;96(1137):403-407. DOI: 10.1136/postgradmedj-2020-137935.


