Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Абстракт
Как известно, многие пациенты с психическими расстройствами имеют те или иные сопутствующие (коморбидные) соматические заболевания. Такие пациенты часто оказываются вынуждены, по вышеуказанной причине, принимать много лекарств для одновременного лечения всех имеющихся у них заболеваний – как психических, так и соматических. Это, естественно, резко повышает вероятность нежелательных межлекарственных взаимодействий между назначенными пациенту препаратами – взаимодействий, потенциально способных привести (и часто на практике приводящих) либо к повышению вероятности проявления побочных эффектов (ПЭ) и даже токсичности того или иного препарата, либо, наоборот, к снижению или даже полной потере его эффективности. Острота проблемы усугубляется еще и тем, что препараты для лечения разных заболеваний одному и тому же пациенту обычно назначают разные специалисты, и не всегда они осведомлены о назначениях друг друга и о характере, степени вероятности и степени опасности возможных межлекарственных взаимодействий. Одним из типичных примеров потенциально опасных межлекарственных взаимодействий является резкое повышение концентрации в плазме крови многих антипсихотиков (АП) и антидепрессантов (АД) при одновременном их применении с одним из часто назначаемых при ВИЧ-инфекции компонентов активной антиретровирусной терапии (АРВТ) – ритонавиром. Между тем частота ВИЧ-инфицирования среди психиатрических пациентов значительно выше, чем в общей популяции (тому есть много причин, например повышенная частота рискованного сексуального поведения). В свете всего вышесказанного особое значение приобретает учет возможных межлекарственных взаимодействий при назначении психотропных препаратов и предпочтение тем из них, которые имеют минимальные риски нежелательных фармакокинетических взаимодействий. В данной статье мы показываем, что замещенные бензамиды, и в частности тиаприд, – особенно хорошо удовлетворяют этому требованию.
Ключевые слова: коморбидные соматические заболевания, фармакокинетика, изоферменты цитохрома, P450, генетические полиморфизмы, межлекарственные взаимодействия, антипсихотик, бензамиды, тиаприд, ВИЧ-инфекция, синдром приобретенного иммунодефицита, ритонавир.
Для цитирования: Р.А. Беккер, Ю.В. Быков. Проблема фармакокинетических взаимодействий в психиатрии: в фокусе – тиаприд. Психиатрия и психофармакотерапия. 2022; 1: 18–25.
The problem of pharmacokinetic interactions in psychiatry: focus on tiapride
Bekker R.A.1, Bykov Yu.V.2
AbstractIt is well known that many psychiatric patients have one or more comorbid somatic diseases. Such patients are often compelled, for the above reason, to take many drugs, in order to simultaneously treat all their illnesses, both mental and somatic. This, of course, dramatically increases the likelihood of unwanted drug-drug interactions between the drugs prescribed to the patient – interactions that can potentially lead either to an increase in the likelihood of side effects and even toxicity of a particular drug, or, conversely, to reduction or even complete loss of the drug’s effectiveness. The severity of the problem is aggravated by the fact that drugs for the treatment of different diseases are usually prescribed to the same patient by different specialists. Those specialists are not always aware of each other's prescriptions and the nature, degree of probability and degree of danger of possible drug interactions. One of the typical examples of potentially dangerous drug-drug interactions is a sharp increase in plasma concentrations of many antipsychotics and antidepressants when they are used simultaneously with one of the components of active antiretroviral therapy often prescribed for control of HIV infection – ritonavir. Meanwhile, the frequency of HIV infection among psychiatric patients is significantly higher than in the general population. This is for many reasons, for example, an increased frequency of risky sexual behavior among psychiatric patients. In light of this, it is of particular importance to take into account possible drug interactions when prescribing psychotropic drugs, and to prefer those that have minimal risks of unwanted pharmacokinetic interactions with other drugs. In this paper, we show that substituted benzamides, and in particular tiapride, meet this requirement particularly well.
Keywords: somatic comorbidity, HIV infection, acquired immunodeficiency syndrome, ritonavir, pharmacokinetic interactions, antipsychotic, benzamide, tiapride.
For citation: Bekker R.A., Bykov Yu.V. The problem of pharmacokinetic interactions in psychiatry: focus on tiapride. Psychiatry and psychopharma
Введение
(Обоснование актуальности проблемы)
Как известно, в связи с значительным повышением распространенности депрессий, тревожных расстройств, синдрома дефицита внимания (СДВГ) в человеческой популяции в последние десятилетия, а также в связи со снижением стигматизации психиатрии в целом и психофармакологического лечения в частности в этот исторический период, в связи с повышением обращаемости к врачам с жалобами на психические проблемы и выявляемости психических расстройств – все больший процент населения Земли в какие-то периоды своей жизни принимает те или иные психотропные препараты, и часто – в комбинациях [Ruiz P, 2017; Preskorn SH, 2018].
С другой же стороны, многие пациенты с хроническими психическими расстройствами также имеют одно или несколько коморбидных соматических заболеваний, как трансмиссивных (передающихся от человека человеку; такова, например, ВИЧ-инфекция), так и нетрансмиссивных (не способных передаваться от человека человеку). Верно, однако, и обратное: пациенты, страдающие определенными соматическими заболеваниями, с повышенной частотой имеют коморбидные или соматогенно обусловленные психические расстройства (например, тревожные и/или депрессивные, диссомнические расстройства, а порой даже психозы) [Ruiz P, 2017; Preskorn SH, 2018].
Причин для высокой частоты коморбидности психических расстройств с определенными соматическими заболеваниями существует множество, и не все эти причины на данный момент окончательно установлены. Среди таких причин называют, в частности, значительное пересечение генов, необходимых для создания предрасположенностей к таким психическим расстройствам, как шизофрения или депрессия, с генами, необходимыми для создания предрасположенностей к таким соматическим заболеваниям, как сахарный диабет (СД) 2-го типа, ожирение, метаболический синдром (МС), артериальная гипертензия (АГ), частичное пересечение патогенетических механизмов развития всех этих заболеваний (например, то, что и там и там играют роль воспаление, оксидативный стресс и др.), соматические побочные эффекты (ПЭ) ряда психотропных препаратов (диабетогенные, атерогенные, адипогенные и т. д.) и психиатрические ПЭ ряда препаратов для лечения соматических заболеваний (депрессогенные, анксиогенные, порой даже психотомиметические и др.), неблагоприятное психологическое влияние осознания факта тяжелой соматической болезни, рискованное сексуальное поведение многих психически больных, их пренебрежение к контролю своего состояния здоровья, плохое питание, употребление алкоголя, психоактивных веществ (ПАВ), курение и др. [Ruiz P, 2017; Preskorn SH, 2018].
Вследствие высокой частоты коморбидности психических и соматических расстройств, значительный процент психиатрических пациентов вынуждены принимать одновременно несколько (или даже много) лекарств для одновременного лечения всех имеющихся у них болезней. Это сильно повышает риск развития у них неблагоприятных межлекарственных взаимодействий [Ruiz P, 2017; Preskorn SH, 2018].
Проблема усугубляется еще и тем, что разные лекарства для лечения различных имеющихся у одного и того же пациента психических и соматических проблем чаще всего назначаются разными специалистами и в разное время. При этом далеко не всегда каждый из этих специалистов оказывается своевременно осведомлен о назначениях и рекомендациях всех остальных специалистов, участвующих в лечении данного конкретного пациента, и далеко не всегда каждый из них правильно осведомлен о возможном характере, степени вероятности и степени потенциальной опасности тех или иных межлекарственных взаимодействий назначенных пациенту препаратов и их сочетаний [Ruiz P, 2017; Preskorn SH, 2018].
По этой причине неблагоприятные межлекарственные взаимодействия могут возникать, но не распознаваться вообще, или распознаваться недостаточно своевременно, даже в тех случаях, когда эти взаимодействия имеют или могут иметь серьезные последствия для здоровья и благополучия пациента [Ruiz P, 2017; Preskorn SH, 2018].
Неблагоприятные последствия не распознанных вовремя нежелательных межлекарственных взаимодействий могут варьировать в диапазоне от снижения или полной потери эффективности того или иного препарата до резкого усиления как его основного фармакологического эффекта, так и его ПЭ, проявлений острой или хронической токсичности лекарства или даже летального исхода [Ruiz P, 2017; Preskorn SH, 2018].
Психиатру важно всегда помнить, что психотропные препараты могут неблагоприятно взаимодействовать не только друг с другом, но и с другими препаратами, назначенными другими специалистами по непсихиатрическим показаниям, и что не всегда он, психиатр, будет своевременно в курсе обо всех этих назначениях – и всегда учитывать этот факт при планировании психофармакологического лечения каждого конкретного пациента, при определении его стратегии и тактики [Ruiz P, 2017; Preskorn SH, 2018].
Статистика показывает, что пациенты с психическими расстройствами относятся к группе повышенного риска развития нежелательных межлекарственных взаимодействий [Prior PI, Baker GB, 2003; Hefner G et al, 2020].
Одна из причин этого заключается в том, что при обострении, рецидиве (повторном эпизоде) или прогрессировании основного психического расстройства такие пациенты нередко нуждаются в комбинированном психофармакологическом лечении, которое может включать в себя сразу несколько психотропных препаратов из разных фармакологических групп – например, антипсихотики (АП), антидепрессанты (АД), нормотимики (НТ), анксиолитики (АЛ), β-блокаторы (ББ) и др. Это, естественно, резко повышает вероятность развития у таких пациентов нежелательных межлекарственных взаимодействий, и может привести к сложным и трудно предсказуемым результатам подобного взаимодействия [Prior PI, Baker GB, 2003; Kennedy WK et al, 2013; Hefner G et al, 2020].
Многие пациенты с хроническими психическими расстройствами вынуждены постоянно или на протяжении длительного времени (месяцами или годами) принимать те или иные психотропные препараты, нередко – в комбинациях. Многие из них вынуждены также периодически или постоянно принимать дополнительные лекарства – например, при лечении обострения сопутствующего хронического соматического заболевания или заболевания, которое развилось de novo [Prior PI, Baker GB, 2003; Kennedy WK et al, 2013; Hefner G et al, 2020].
Несмотря на значительное повышение в последние десятилетия осведомленности психиатров о возможности нежелательных межлекарственных взаимодействий между психотропными и другими препаратами и о той роли, которую могут играть изоферменты системы цитохрома P450 печени (CYP), глюкуронидазы (UGT) и белок P-gp в этих взаимодействиях, уровень этой осведомленности все еще остается недопустимо низким. Именно это и предопределяет высокую актуальность данной темы на современном этапе [Prior PI, Baker GB, 2003; Kennedy WK et al, 2013; Hefner G et al, 2020].
Ниже мы кратко напомним читателю основные факты о путях и механизмах развития нежелательных межлекарственных взаимодействий.
Основные факты о межлекарственных взаимодействиях
Как известно, основным органом, в котором происходят окислительный метаболизм, обезвреживание и подготовка к экскреции с мочой и/или с желчью и затем с калом большинства лекарств (в том числе и психотропных), а также большинства ксенобиотиков, ядов и токсинов, – является печень. Другие органы и ткани, такие как почки, головной и спинной мозг, кожа, кровь, легкие и слизистая ЖКТ, – вносят гораздо менее значимый вклад в эти процессы [Krishna DR, Klotz U, 1994].
Для большинства психотропных препаратов, в том числе для большинства АП и АД, основным путем их выведения из организма является окислительный метаболизм в печени при участии тех или иных изоферментов системы цитохрома P450 печени. В дальнейшем окисленные, более водорастворимые, метаболиты лекарств нередко подвергаются второму этапу обезвреживания, еще больше повышающему их растворимость в воде, – конъюгации с серной, глюкуроновой или уксусной кислотой (сульфатированию, глюкуронизации или ацетилированию). Окисленные и/или конъюгированные метаболиты лекарств затем выводятся в основном с мочой и, в небольшой степени, также с желчью (то есть в конечном итоге – с калом). Следует иметь в виду, что у некоторых лекарств, в том числе у некоторых АП и АД, в результате окислительного этапа печеночного метаболизма образуются активные метаболиты – иногда даже более активные, чем родительское соединение [Javaid JI, 1994].
Поскольку большинство психотропных препаратов, включая и большинство АД, и большинство АП (как типичных – ТАП, так и атипичных – ААП) – подвергаются окислительному метаболизму в печени при участии изоферментов системы цитохрома P450 (CYP), а многие из них сами могут сильно влиять на активность CYP в ту или иную сторону, – то очень важно, чтобы и психиатры, и врачи других специальностей были хорошо осведомлены об особенностях совместного применения психотропных препаратов с препаратами других фармакологических групп, которые могут ингибировать или, напротив, индуцировать те или иные изоферменты CYP [Urichuk L et al, 2008].
Возможное добавление или, наоборот, отмена каких-либо других (не психотропных) препаратов может сильно повлиять на эффективность, безопасность и переносимость параллельно проводимой психотропной терапии на многих уровнях – например, изменяя всасывание, распределение, метаболизм или выведение тех или иных психотропных препаратов или их активных метаболитов [Kennedy WK, et al, 2013].
В повседневной клинической практике психиатра особенно большое значение имеют те межлекарственные взаимодействия, которые реализуются через разнонаправленные воздействия на активность тех или иных изоферментов системы цитохрома P450 печени, во вторую очередь – межлекарственные взаимодействия, реализующиеся через влияние на глюкуронилтрансферазы (UGT) или на активность белка P-gp [Kennedy WK, et al, 2013].
Поскольку большинство АП и АД метаболизируются теми или иными изоферментами CYP450, то ингибиторы этих изоферментов (например, такие как ритонавир, кетоконазол, флувоксамин, пароксетин, бупропион, ципрофлоксацин) – могут повышать их уровни в плазме крови и замедлять их обезвреживание и выведение. Это может привести к усилению как основного фармакологического действия данных препаратов, так и их ПЭ, а порой даже к проявлениям острой и/или хронической токсичности данных препаратов, к явлениям их передозировки и даже к летальным исходам. И наоборот, индукторы изоферментов CYP450 печени, такие как карбамазепин, фенитоин, фенобарбитал, рифампицин, никотин, алкоголь, – могут снижать уровни многих АП и АД в плазме крови и ускорять их обезвреживание и выведение. Это может привести к снижению или даже полной утрате терапевтической эффективности АП и/или АД, к рецидиву или обострению основного психического расстройства, и даже к совершению пациентом суицида на фоне внезапного рецидива психического расстройства [Spina E et al, 2003; Shafiekhani M et al, 2018; Kratz T, Diefenbacher A, 2019].
Такого рода межлекарственные взаимодействия особенно опасны в случае психотропных лекарств с узким терапевтическим диапазоном (то есть с легкостью достижения токсических уровней даже при сравнительно небольшой передозировке или небольшом повышении концентрации препарата в крови) и/или с критическим значением поддержания стабильного терапевтически эффективного уровня данного лекарства в крови для поддержания и сохранения психической стабильности больного (ввиду его полирезистентности к другим препаратам), как клозапин или трициклические антидепрессанты (ТЦА) [Spina E et al, 2003; Shafiekhani M et al, 2018; Kratz T, Diefenbacher A, 2019].
Кроме фармакокинетических взаимодействий, врачам следует учитывать также вероятность взаимодействий на уровне фармакодинамики. По этой причине следует по возможности избегать совместного назначения лекарств с частично или полностью взаимно перекрывающимися, суммирующимися или взаимно усиливающими друг друга ПЭ, такими как сердечно-сосудистые, седативные, М-холиноблокирующие, экстрапирамидные или кардиометаболические ПЭ, или риск серотонинового синдрома [Shafiekhani M et al, 2018].
Также следует по возможности избегать совместного назначения лекарств, полезные фармакологические эффекты которых взаимно аннигилируются с ПЭ других лекарств из данной комбинации (например, желательно избегать назначения при психотической форме депрессии АД совместно с потенциально депрессогенным ТАП – для этого следует выбрать ААП со «встроенными» антидепрессивными свойствами) [Shafiekhani M et al, 2018].
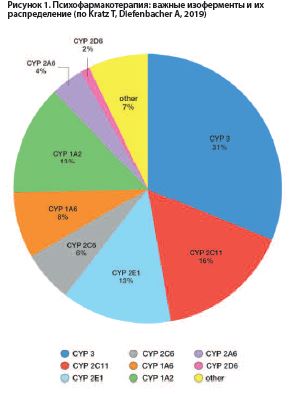
На рис. № 1 показано распределение важности роли тех или иных изоферментов системы цитохрома P450 печени в окислительном метаболизме и экскреции психотропных препаратов [Kratz T, Diefenbacher A, 2019].
Как можно видеть из круговой диаграммы на рисунке 1, изоферментами системы цитохрома P450 (CYP), особенно важными для окислительного катаболизма психотропных препаратов, являются (в порядке убывания значимости) CYP1A2, CYP3A4, CYP2D6, CYP2C19, CYP2B6 и CYP2C9 [Kratz T, Diefenbacher A, 2019].
 Как мы уже упоминали ранее, при одновременном совместном приеме нескольких препаратов, каждый из которых катаболизируется системой смешанных оксидаз (системой цитохрома P450) печени, уровни этих препаратов в плазме крови могут измениться в любую сторону – как повыситься, так и снизиться [Kratz T, Diefenbacher A, 2019].
Как мы уже упоминали ранее, при одновременном совместном приеме нескольких препаратов, каждый из которых катаболизируется системой смешанных оксидаз (системой цитохрома P450) печени, уровни этих препаратов в плазме крови могут измениться в любую сторону – как повыситься, так и снизиться [Kratz T, Diefenbacher A, 2019].
Комбинация двух лекарств может привести к фармакокинетическому взаимодействию, если одно из вводимых лекарств (лекарство № 1) ингибирует или индуцирует тот или иной изофермент системы P450 печени («препарат-хищник»), а другое лекарство в этой комбинации (лекарство № 2) – в значительной степени катаболизируется именно этим изоферментом, индуцируемым или ингибируемым лекарством № 1 («препарат-жертва») [Kratz T, Diefenbacher A, 2019].
Однако очень часто в повседневной клинической практике возникает ситуация, когда два лекарства конкурируют за один и тот же изофермент CYP, конкурентно ингибируя метаболизм друг друга и повышая концентрации друг друга в плазме крови. В таких случаях каждый из двух препаратов в комбинации – является одновременно и «хищником», и «жертвой» взаимодействия [Kratz T, Diefenbacher A, 2019].
Таким образом, для правильного расчета возможных межлекарственных взаимодействий у конкретного пациента очень важно знать, какими путями и с использованием каких изоферментов CYP катаболизируется каждое из лекарств, принимаемых пациентом, и каким образом, с какой силой и в какую сторону каждое из этих лекарств влияет на активность тех или иных изоферментов CYP – ингибирует, индуцирует или не оказывает клинически значимого влияния [Kratz T, Diefenbacher A, 2019].
Так, в частности, при назначении психотропных препаратов пожилым пациентам необходимо учитывать возможность ингибирования некоторыми из них изофермента CYP2D6, который играет важную роль в катаболизме многих лекарств, используемых в лечении типичных соматических болезней пожилого возраста (антигипертензивных, гиполипидемических препаратов и др.), а также в катаболизме ряда других психотропных препаратов [Kratz T, Diefenbacher A, 2019].
Другой характерный пример нежелательных межлекарственных взаимодействий – возможность резкого повышения концентрации в плазме крови некоторых ААП, метаболизируемых изоферментом CYP1A2, например оланзапина, при их совместном применении с ципрофлоксацином, который сильно ингибирует CYP1A2 [Benkert O, Hippius H, 2018].
Помимо взаимодействий лекарств друг с другом, важно учитывать и возможность их взаимодействия с некоторыми биологически активными добавками (БАДами) и даже с некоторыми компонентами пищи. Так, в частности, грейпфрутовый сок, а точнее некоторые содержащиеся в нем горькие полифенольные соединения (например, нарингенин), могут сильно ингибировать изоферменты цитохрома P450 печени, особенно CYP3A4. По этой причине грейпфрутовый сок может в 3-5 раз повысить биодоступность и уровень в плазме крови таких психотропных препаратов, метаболизируемых через CYP3A4, как кветиапин, кломипрамин, карбамазепин и буспирон. Пациенты должны быть проинформированы об этом и проинструктированы избегать употребления больших количеств грейпфрутового сока [Etheridge AS et al, 2007].
Важно отметить, что большинство АП и АД являются высоколипофильными соединениями. Это облегчает их проникновение в мозг, где они, собственно, и реализуют свое психотропное действие. Но это же их свойство облегчает и их экстракцию печенью из плазмы крови. В дальнейшем экстрагированное клетками печени из плазмы крови психотропное лекарство обычно подвергается экстенсивному окислительному метаболизму с помощью тех или иных изоферментов системы P450 (CYP) для повышения его растворимости в воде и облегчения его выведения из организма [Scordo MG, Spina E, 2002].
Существует очень широкая межиндивидуальная вариабельность скорости биотрансформации в печени тех или иных АП и АД у разных людей. Это приводит к значительным различиям в достигаемых при приеме фиксированных доз этих препаратов концентрациях в плазме крови у разных людей. А это, в свою очередь, приводит к значительным различиям как в терапевтической эффективности, так и в переносимости, уровне ПЭ и в токсичности одной и той же дозы одного и того же препарата у разных людей. Это диктует необходимость гибкого индивидуального подбора режима дозирования психотропной терапии для каждого конкретного пациента, с учетом индивидуальных особенностей его фармакогенетики, а также особенностей фармакокинетики и фармакодинамики разных психотропных препаратов именно у него [Scordo MG, Spina E, 2002].
Многие АД и АП (как ТАП, так и некоторые ААП) в значительной степени метаболизируются изоферментом CYP2D6. Между тем однонуклеотидные генетические полиморфизмы, сильно изменяющие степень его активности, очень широко распространены в популяции. Генетические полиморфизмы некоторых других изоферментов системы цитохрома P450, особенно CYP1A2 и CYP3A4, тоже очень распространены в популяции. Все это способствует большой межиндивидуальной вариабельности фармакокинетики многих АД и АП, и сильно осложняет врачу задачу учета и прогнозирования риска неблагоприятных межлекарственных взаимодействий [Scordo MG, Spina E, 2002].
Кроме взаимодействий через P450, важную роль играют также взаимодействия, связанные с P-гликопротеином
(P-gp), показанные на рис. 2. Этот белок, известный также как белок множественной лекарственной устойчивости, является АТФ-зависимым насосом оттока с широкой субстратной специфичностью [Schinkel AH, Jonker JW, 2003].
Белок P-gp в высокой степени экспрессируется в апикальной мембране кишечного эпителия, гепатоцитах, эпителии проксимальных канальцев почек, а также в эндотелии капилляров головного мозга. Он перекачивает различные ксенобиотики из плазмы крови обратно в просвет кишечника, в желчные протоки, почечные канальцы, а также из ткани мозга обратно в мозговые капилляры [Kim JE et al, 2014].
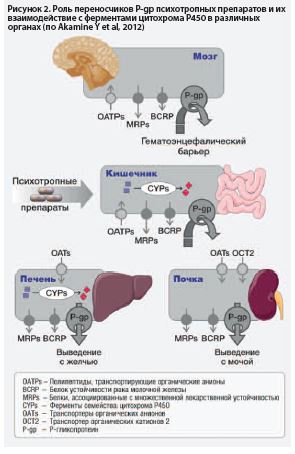 Белок P-gp играет важную роль в кишечной абсорбции, распределении в ЦНС и в выведении лекарств с желчью/мочой [Kim JE et al, 2013]. Следовательно, ингибирование или индукция P-gp при одновременном приеме тех или иных лекарств, одно из которых является высокоаффинным субстратом P-gp, а другое – его индуктором или ингибитором, – может привести к нежелательному фармакокинетическому взаимодействию, которое может либо усилить терапевтический эффект лекарства и его ПЭ за счет усиления его проникновения через гематоэнцефалический барьер (ГЭБ) или замедления его элиминации печенью и почками, либо ослабить эффект лекарства и даже привести к терапевтической неудаче [Marchetti S et al, 2007].
Белок P-gp играет важную роль в кишечной абсорбции, распределении в ЦНС и в выведении лекарств с желчью/мочой [Kim JE et al, 2013]. Следовательно, ингибирование или индукция P-gp при одновременном приеме тех или иных лекарств, одно из которых является высокоаффинным субстратом P-gp, а другое – его индуктором или ингибитором, – может привести к нежелательному фармакокинетическому взаимодействию, которое может либо усилить терапевтический эффект лекарства и его ПЭ за счет усиления его проникновения через гематоэнцефалический барьер (ГЭБ) или замедления его элиминации печенью и почками, либо ослабить эффект лекарства и даже привести к терапевтической неудаче [Marchetti S et al, 2007].
Примером взаимодействия через P-gp является резкое усиление ингибиторами P-gp – верапамилом или омепразолом – центрального дельта-опиоидного эффекта лоперамида, который в норме почти не проникает через ГЭБ, или усиление литием (также ингибитором P-gp) эффектов АД, АП, донепезила и др. [Marchetti S et al, 2007].
Фармакокинетические особенности и преимущества тиаприда
Тиаприд практически не метаболизируется цитохромами P450 печени, и выводится в основном в неизмененном виде, посредством почечной экскреции (с мочой) – до 80%. Еще до 20% неизмененного тиаприда – выводится посредством печеночной экскреции в желчь и последующего удаления с калом [Cudennec A et al, 1997; Rey E et al, 1982; Stahl SM, 2013; Ястребов ДВ, 2015].
Сам тиаприд также не влияет на активность каких-либо изоферментов системы цитохрома P450 печени или глюкуронидаз (UGT) – не индуцирует и не ингибирует ни один из них [Mizuchi A et al, 1983; Rey E et al, 1982; Stahl SM, 2013; Ястребов ДВ, 2015].
Кроме того, тиаприд также практически не связывается с белками плазмы крови, не подвергается конъюгации с глюкуронидом, сульфатом или ацетатом, не является высокоаффинным субстратом белка P450 [Точилов ВА, Протальская АГ, 1998; Roos RA et al, 1986].
Стоит отметить, что практически полное отсутствие печеночного метаболизма через систему цитохрома P450 – вообще характерная особенность всех сульфонил-замещенных бензамидов, кроме сульпирида, который все-таки в небольшой, клинически незначимой степени метаболизируется в печени [Ястребов ДВ, 2015].
Период полувыведения (T1/2) у всех сульфонил-замещенных бензамидов достаточно короткий. В случае тиаприда он варьирует от 2 до 4 часов [Peters DH, Faulds D, 1994; Ястребов ДВ, 2015].
Отсутствие у тиаприда печеночного метаболизма позволяет с успехом применять его у пожилых людей с возрастным снижением функции печени и у пациентов с поражениями печени, в том числе тяжелыми (например, с тяжелым алкогольным гепатитом и даже с алкогольным циррозом печени) [Минко АИ, 2019].
Все эти фармакокинетические особенности тиаприда обуславливают весьма низкий потенциал для развития нежелательных межлекарственных взаимодействий при сочетании тиаприда с другими лекарствами, включая мощные ингибиторы ряда изоферментов системы цитохрома P450 (например, ритонавир, флувоксамин, кетоконазол и др.), их мощные индукторы (например, карбамазепин или рифампицин), мощные блокаторы белка P-gp (верапамил, дилтиазем, циклоспорин, литий, омепразол и др.) [Peters DH, Faulds D, 1994].
Фармакодинамика тиаприда
Тиаприд – это ААП из группы сульфонил-замещенных бензамидов, близкий химический родственник сульпирида, амисульприда, сультоприда и метоклопрамида. Он является селективным антагонистом (точнее, весьма слабым парциальным агонистом) дофаминовых рецепторов подтипов D2 и D3, преимущественно в лимбических областях мозга и в голубоватом пятне [Karia S et al, 2013; Морозов ПВ с соавт, 2020; Fekete S et al, 2021].
В целом сравнение сульфонил-замещенных бензамидов, как подгруппы ААП, с ТАП показывает, что характерными для всей подгруппы замещенных бензамидов отличительными особенностями рецепторного профиля является высокая селективность их связывания с дофаминовыми рецепторами D2 и D3 подтипов, при минимальном их сродстве к дофаминовым рецепторам подтипа D1 (блокада которых неблагоприятно влияет на когнитивное функционирование пациентов), и практически полное отсутствие сродства к гистаминовым, холинергическим, адренергическим, ГАМК, бензодиазепиновым, опиоидным или каким-либо еще рецепторам головного мозга [Stahl SM, 2013; Ястребов ДВ, 2015; Коробов НВ, 2016].
Между тем связывание с гистаминовыми H1, мускариновыми холинергическими, α1 адренергическими рецепторами характерно для многих других АП, и обуславливает целый ряд нежелательных ПЭ, таких как чрезмерная седация и сонливость (H1), ортостатическая гипотензия и тахикардия (α1), запоры, задержка мочи, сухость во рту, парез аккомодации глаз, нарушения памяти, когнитивные нарушения (КН) (М-холинорецепторы) [Stahl SM, 2013; Ястребов ДВ, 2015].
Все семейство сульфонил-замещенных бензамидов, к которому относятся такие препараты, как тиаприд, сульпирид, амисульприд, сультоприд, – обладает гораздо большей тропностью к дофаминовым D2 рецепторам лимбических и гиппокампальных областей мозга, чем к D2 рецепторам в нигростриарной системе. Как полагают, именно этим свойством бензамидных ААП, а также их слабым парциальным агонизмом (а не «молчаливым антагонизмом» или даже инверсным агонизмом, как у многих других АП) по отношению к D2 подтипу дофаминовых рецепторов – может объясняться сравнительно малая выраженность проявлений ЭПС и акатизии при лечении ААП из группы бензамидов, даже при их использовании в достаточно высоких дозах [Stahl SM, 2013; Ястребов ДВ, 2015; Быков ЮВ, Беккер РА, 2019; Беккер РА, Быков ЮВ, 2019].
Все замещенные бензамиды, включая и тиаприд, в низких и средних дозах (например, 25-50 мг/сут амисульприда, 50-200 мг/сут сульпирида или 300–600 мг/сут тиаприда), наряду с противорвотной (антиэметической) активностью, свойственной и многим другим АП, демонстрируют также специфические антидиспептические, антидиарейные, спазмолитические и регулирующие моторику (прокинетические) свойства в желудочно-кишечном тракте (ЖКТ). Они способствуют открытию привратника желудка, ускорению пассажа пищевой кашицы по ЖКТ при запорах, одновременно предотвращая развитие диареи и болезненных спазмов. Эти свойства замещенных бензамидов связывают с их одновременным воздействием как на дофаминовые D2 рецепторы, так и на серотониновые 5-HT4 рецепторы в ЖКТ [Stahl SM, 2013; Ястребов ДВ, 2015; Быков ЮВ, Беккер РА, 2019; Беккер РА, Быков ЮВ, 2019].
Наличие у замещенных бензамидов (тиаприда, сульпирида) подобных свойств – делает их высокоэффективными и удобными в клинической практике средствами для лечения синдрома раздраженного кишечника (СРК) и функциональной диспепсии (ФД) [Emmanuel A, Quigley EM, 2013].
Антипсихотическое действие тиаприда, как полагают, обусловлено блокадой дофаминовых D2 рецепторов в мезолимбическом и мезокортикальном проводящих путях, седативное – блокадой α1 адренорецепторов и D2 дофаминовых рецепторов ретикулярной формации ствола мозга, противорвотное его действие – блокадой дофаминовых D2 рецепторов триггерной зоны и рвотного центра, гипотермическое действие – блокадой α1 адренорецепторов и дофаминовых D2 рецепторов центров терморегуляции гипоталамуса, антимигренозное его действие – блокадой дофаминовых D2 рецепторов ядра тройничного нерва [Басов АН, 2013; Stahl SM, 2013; Быков ЮВ, Беккер РА, 2016].
Блокада дофаминовых D2 рецепторов в нигростриарном пути, с одной стороны, предопределяет антидискинетическое и противотикозное действие тиаприда, его высокую клиническую эффективность при синдроме Туретта и при других тикозных расстройствах, а также при купировании острых дискинезий (ОД) от других АП, а с другой – иногда может вызывать нерезко выраженные проявления ЭПС и/или акатизии при лечении тиапридом, особенно при высоких его дозах. Блокада же дофаминовых D2 рецепторов тубероинфундибулярного пути может приводить к повышению уровня пролактина в плазме крови при лечении тиапридом [Басов АН, 2013; Stahl SM, 2013; Быков ЮВ, Беккер РА, 2016].
Важной особенностью тиаприда является то, что даже при максимальных, согласно инструкции по применению препарата, дозах – процент оккупации D2 дофаминовых рецепторов стриатума никогда не превышает 80%. Это обуславливает как сбалансированность и умеренность антипсихотического действия тиаприда, так и редкость возникновения при лечении им ПЭ, связанных с чрезмерной дофаминергической блокадой в нигростриарном и мезокортикальном путях, – проявлений ЭПС и/или акатизии, нейролептических депрессий, нейролептик-индуцированного дефицитарного синдрома (НИДС) [Ястребов ДВ, 2015].
В малых дозах (50-100 мг/сут) тиаприд, подобно другим замещенным бензамидам (сульпириду, амисульприду), применяемым в малых дозах, – преимущественно блокирует пресинаптические «тормозные» (ауторегуляторные) дофаминовые D2 рецепторы. Это приводит к усилению дофаминергической нейротрансмиссии в ЦНС и к проявлению антидепрессивного, растормаживающего, активирующе-энергизирующего действия тиаприда [Stahl SM, 2013; Быков ЮВ, Беккер РА, 2019; Беккер РА, Быков ЮВ, 2019].
Вместе с тем некоторые авторы отрицают наличие у тиаприда стимулирующего, активирующе-энергизирующего компонента действия при низких его дозах, и определяют тиаприд как «бензамид с седативными свойствами, проявляющимися уже начиная с малых его доз» [Dose M, Lange HW, 2000].
Антипсихотическое действие у тиаприда является самым слабым среди всех ААП подгруппы сульфонил-замещенных бензамидов. По этому параметру тиаприд уступает не только таким мощным ААП, как сультоприд и амисульприд, но и сравнительно слабому в этом отношении сульпириду. Тем не менее антипсихотической активности тиаприда часто оказывается вполне достаточно для купирования, например, психозов позднего возраста, развивающихся на фоне тех или иных деменций, или для лечения так называемых «органических психозов», развивающихся на фоне органических поражений ЦНС (например, на фоне ВИЧ-ассоциированной энцефалопатии), или для купирования психотических проявлений при психотической форме депрессии [Абриталин ЕЮ, Краснов АА, 2021].
С другой же стороны, важным преимуществом применения именно тиаприда в вышеуказанных клинических ситуациях является то, что он реже всех остальных сульфонил-замещенных производных бензамида вызывает проявления ЭПС и/или акатизию, при том что на фоне применения других бензамидов эти ПЭ и без того возникают крайне редко [Абриталин ЕЮ, Краснов АА, 2021].
В рецепторном профиле тиаприда присутствуют также свойства сильного парциального агониста 5-HT4 подтипа серотониновых рецепторов и блокатора 5-HT7 подтипа их. Эти рецепторные свойства тиаприда предопределяют его антидепрессивную, противотревожную, анальгетическую и антимигренозную активность, а также его способность нормализовывать сон и циркадные ритмы и положительно влиять на когнитивное функционирование больных [Быков ЮВ, Беккер РА, 2019; Беккер РА, Быков ЮВ, 2019; Морозов ПВ с соавт, 2020; Абриталин ЕЮ, Краснов АА, 2021].
Наличие у тиаприда таких свойств значительно расширяет сферу его клинического применения, позволяя применять его не только при тиках, психозах, агрессивности или нарушениях поведения, но и при депрессиях и тревожных расстройствах (в комбинации с АД), при мигрени, хронических головных болях напряжения (ХГБН) и различных других хронических болевых синдромах (ХБС), например при фибромиалгии (ФМА) и др. [Быков ЮВ, Беккер РА, 2019; Беккер РА, Быков ЮВ, 2019; Морозов ПВ с соавт, 2020; Абриталин ЕЮ, Краснов АА, 2021].
Заключение
Как убедительно показывают приведенные нами данные литературы, многие пациенты с психическими расстройствами имеют одно или несколько сопутствующих (коморбидных) соматических расстройств, тоже нуждающихся в специфическом фармакологическом лечении. Это вынуждает многих психиатрических пациентов принимать одновременно несколько (или даже много) лекарств, назначенных разными специалистами в разное время и по разным поводам, для лечения всех имеющихся у них расстройств – как психических, так и соматических. В свою очередь, высокая частота коморбидности психических расстройств с целым рядом серьезных соматических заболеваний, тоже нуждающихся в активном фармакологическом лечении, в сочетании со значительной распространенностью в человеческой популяции генетических полиморфизмов таких белков, играющих важную роль в катаболизме и экскреции лекарств, как изоферменты системы смешанных оксидаз печени (иначе говоря, изоферменты системы цитохрома P450 печени), глюкуронилтрансферазы (UGT), белки системы генов множественной лекарственной устойчивости (MDR), в частности, P-гликопротеин (P-gp), – предопределяют повышенную вероятность развития разнообразных нежелательных межлекарственных взаимодействий в субпопуляции психиатрических пациентов. Эти нежелательные межлекарственные взаимодействия могут приводить как к снижению или даже полной утрате эффективности тех или иных лекарств при сочетании их с некоторыми другими лекарствами, так и к неожиданно резкому усилению и основного фармакологического эффекта некоторых лекарств, и их ПЭ, вплоть до проявлений их острой или хронической токсичности, и даже до летальных исходов при определенных неблагоприятных лекарственных сочетаниях. В свете всего вышесказанного особое значение приобретает подбор у психиатрических пациентов, особенно у тех из них, у кого имеются известные соматические отягощенности (например, коморбидная ВИЧ-инфекция), – таких психотропных препаратов и таких режимов психотропной терапии, которые имеют по возможности меньший риск нежелательных межлекарственных взаимодействий.Тиаприд - ААП из группы сульфонил-замещенных бензамидов, который в полной мере соответствует этому требованию. Он сам практически не метаболизируется изоферментами цитохрома P450 или глюкуронилтрансферазами (UGT), и не влияет на их активность (не индуцирует и не ингибирует). Кроме того, тиаприд, в отличие, например, от рисперидона, не является высокоаффинным субстратом белка P-gp. Поэтому его эффективность или вероятность развития ПЭ при лечении им не подвержены значительным изменениям под влиянием приема таких мощных ингибиторов P-gp, как верапамил, циклоспорин, омепразол или литий. В то же время широкий спектр фармакологических свойств тиаприда, в котором, наряду с умеренной антипсихотической активностью (основным свойством любого ААП), присутствуют также антидискинетическая (противотикозная), противорвотная, умеренная седативная, антидепрессивная, антиагрессивная, антидисфорическая, анксиолитическая (противотревожная), сильная анальгетическая и сильная антимигренозная активности, а также способность, благодаря его 5-HT7 блокирующим свойствам, улучшать когнитивное функционирование больных, нормализовывать сон и циркадные ритмы, потенцировать антидепрессивное действие АД и анальгетическое действие НПВС, опиоидов, – значительно расширяет диапазон тех клинических ситуаций, в которых тиаприд может быть с успехом применен. Хорошая переносимость тиаприда, низкая вероятность развития ЭПС, акатизии, ортостатической гипотензии, чрезмерной седации при лечении им, отсутствие у него М-холиноблокирующих ПЭ – делают тиаприд особенно подходящим препаратом для лечения соматически отягощенных пациентов, пациентов пожилого и старческого возраста, а также пациентов с органическими поражениями ЦНС (например, с ВИЧ-ассоциированной энцефалопатией и психозами на почве ее). Многие такие пациенты как раз принимают лекарства, имеющие высокий риск нежелательных взаимодействий со многими другими психотропными средствами, но безопасные в комбинации с тиапридом. Резюмируя, мы считаем, что тиаприд заслуживает значительно более широкого применения в психиатрии, неврологии и наркологии, и особенно – в ряде вышеупомянутых клинических ситуаций.
.
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№01 2022
Проблема фармакокинетических взаимодействий в психиатрии: в фокусе – тиаприд №01 2022
Абстракт
Как известно, многие пациенты с психическими расстройствами имеют те или иные сопутствующие (коморбидные) соматические заболевания. Такие пациенты часто оказываются вынуждены, по вышеуказанной причине, принимать много лекарств для одновременного лечения всех имеющихся у них заболеваний – как психических, так и соматических. Это, естественно, резко повышает вероятность нежелательных межлекарственных взаимодействий между назначенными пациенту препаратами – взаимодействий, потенциально способных привести (и часто на практике приводящих) либо к повышению вероятности проявления побочных эффектов (ПЭ) и даже токсичности того или иного препарата, либо, наоборот, к снижению или даже полной потере его эффективности. Острота проблемы усугубляется еще и тем, что препараты для лечения разных заболеваний одному и тому же пациенту обычно назначают разные специалисты, и не всегда они осведомлены о назначениях друг друга и о характере, степени вероятности и степени опасности возможных межлекарственных взаимодействий. Одним из типичных примеров потенциально опасных межлекарственных взаимодействий является резкое повышение концентрации в плазме крови многих антипсихотиков (АП) и антидепрессантов (АД) при одновременном их применении с одним из часто назначаемых при ВИЧ-инфекции компонентов активной антиретровирусной терапии (АРВТ) – ритонавиром. Между тем частота ВИЧ-инфицирования среди психиатрических пациентов значительно выше, чем в общей популяции (тому есть много причин, например повышенная частота рискованного сексуального поведения). В свете всего вышесказанного особое значение приобретает учет возможных межлекарственных взаимодействий при назначении психотропных препаратов и предпочтение тем из них, которые имеют минимальные риски нежелательных фармакокинетических взаимодействий. В данной статье мы показываем, что замещенные бензамиды, и в частности тиаприд, – особенно хорошо удовлетворяют этому требованию.
Ключевые слова: коморбидные соматические заболевания, фармакокинетика, изоферменты цитохрома, P450, генетические полиморфизмы, межлекарственные взаимодействия, антипсихотик, бензамиды, тиаприд, ВИЧ-инфекция, синдром приобретенного иммунодефицита, ритонавир.
Для цитирования: Р.А. Беккер, Ю.В. Быков. Проблема фармакокинетических взаимодействий в психиатрии: в фокусе – тиаприд. Психиатрия и психофармакотерапия. 2022; 1: 18–25.
The problem of pharmacokinetic interactions in psychiatry: focus on tiapride
Bekker R.A.1, Bykov Yu.V.2
AbstractIt is well known that many psychiatric patients have one or more comorbid somatic diseases. Such patients are often compelled, for the above reason, to take many drugs, in order to simultaneously treat all their illnesses, both mental and somatic. This, of course, dramatically increases the likelihood of unwanted drug-drug interactions between the drugs prescribed to the patient – interactions that can potentially lead either to an increase in the likelihood of side effects and even toxicity of a particular drug, or, conversely, to reduction or even complete loss of the drug’s effectiveness. The severity of the problem is aggravated by the fact that drugs for the treatment of different diseases are usually prescribed to the same patient by different specialists. Those specialists are not always aware of each other's prescriptions and the nature, degree of probability and degree of danger of possible drug interactions. One of the typical examples of potentially dangerous drug-drug interactions is a sharp increase in plasma concentrations of many antipsychotics and antidepressants when they are used simultaneously with one of the components of active antiretroviral therapy often prescribed for control of HIV infection – ritonavir. Meanwhile, the frequency of HIV infection among psychiatric patients is significantly higher than in the general population. This is for many reasons, for example, an increased frequency of risky sexual behavior among psychiatric patients. In light of this, it is of particular importance to take into account possible drug interactions when prescribing psychotropic drugs, and to prefer those that have minimal risks of unwanted pharmacokinetic interactions with other drugs. In this paper, we show that substituted benzamides, and in particular tiapride, meet this requirement particularly well.
Keywords: somatic comorbidity, HIV infection, acquired immunodeficiency syndrome, ritonavir, pharmacokinetic interactions, antipsychotic, benzamide, tiapride.
For citation: Bekker R.A., Bykov Yu.V. The problem of pharmacokinetic interactions in psychiatry: focus on tiapride. Psychiatry and psychopharma
Введение
(Обоснование актуальности проблемы)
Как известно, в связи с значительным повышением распространенности депрессий, тревожных расстройств, синдрома дефицита внимания (СДВГ) в человеческой популяции в последние десятилетия, а также в связи со снижением стигматизации психиатрии в целом и психофармакологического лечения в частности в этот исторический период, в связи с повышением обращаемости к врачам с жалобами на психические проблемы и выявляемости психических расстройств – все больший процент населения Земли в какие-то периоды своей жизни принимает те или иные психотропные препараты, и часто – в комбинациях [Ruiz P, 2017; Preskorn SH, 2018].
С другой же стороны, многие пациенты с хроническими психическими расстройствами также имеют одно или несколько коморбидных соматических заболеваний, как трансмиссивных (передающихся от человека человеку; такова, например, ВИЧ-инфекция), так и нетрансмиссивных (не способных передаваться от человека человеку). Верно, однако, и обратное: пациенты, страдающие определенными соматическими заболеваниями, с повышенной частотой имеют коморбидные или соматогенно обусловленные психические расстройства (например, тревожные и/или депрессивные, диссомнические расстройства, а порой даже психозы) [Ruiz P, 2017; Preskorn SH, 2018].
Причин для высокой частоты коморбидности психических расстройств с определенными соматическими заболеваниями существует множество, и не все эти причины на данный момент окончательно установлены. Среди таких причин называют, в частности, значительное пересечение генов, необходимых для создания предрасположенностей к таким психическим расстройствам, как шизофрения или депрессия, с генами, необходимыми для создания предрасположенностей к таким соматическим заболеваниям, как сахарный диабет (СД) 2-го типа, ожирение, метаболический синдром (МС), артериальная гипертензия (АГ), частичное пересечение патогенетических механизмов развития всех этих заболеваний (например, то, что и там и там играют роль воспаление, оксидативный стресс и др.), соматические побочные эффекты (ПЭ) ряда психотропных препаратов (диабетогенные, атерогенные, адипогенные и т. д.) и психиатрические ПЭ ряда препаратов для лечения соматических заболеваний (депрессогенные, анксиогенные, порой даже психотомиметические и др.), неблагоприятное психологическое влияние осознания факта тяжелой соматической болезни, рискованное сексуальное поведение многих психически больных, их пренебрежение к контролю своего состояния здоровья, плохое питание, употребление алкоголя, психоактивных веществ (ПАВ), курение и др. [Ruiz P, 2017; Preskorn SH, 2018].
Вследствие высокой частоты коморбидности психических и соматических расстройств, значительный процент психиатрических пациентов вынуждены принимать одновременно несколько (или даже много) лекарств для одновременного лечения всех имеющихся у них болезней. Это сильно повышает риск развития у них неблагоприятных межлекарственных взаимодействий [Ruiz P, 2017; Preskorn SH, 2018].
Проблема усугубляется еще и тем, что разные лекарства для лечения различных имеющихся у одного и того же пациента психических и соматических проблем чаще всего назначаются разными специалистами и в разное время. При этом далеко не всегда каждый из этих специалистов оказывается своевременно осведомлен о назначениях и рекомендациях всех остальных специалистов, участвующих в лечении данного конкретного пациента, и далеко не всегда каждый из них правильно осведомлен о возможном характере, степени вероятности и степени потенциальной опасности тех или иных межлекарственных взаимодействий назначенных пациенту препаратов и их сочетаний [Ruiz P, 2017; Preskorn SH, 2018].
По этой причине неблагоприятные межлекарственные взаимодействия могут возникать, но не распознаваться вообще, или распознаваться недостаточно своевременно, даже в тех случаях, когда эти взаимодействия имеют или могут иметь серьезные последствия для здоровья и благополучия пациента [Ruiz P, 2017; Preskorn SH, 2018].
Неблагоприятные последствия не распознанных вовремя нежелательных межлекарственных взаимодействий могут варьировать в диапазоне от снижения или полной потери эффективности того или иного препарата до резкого усиления как его основного фармакологического эффекта, так и его ПЭ, проявлений острой или хронической токсичности лекарства или даже летального исхода [Ruiz P, 2017; Preskorn SH, 2018].
Психиатру важно всегда помнить, что психотропные препараты могут неблагоприятно взаимодействовать не только друг с другом, но и с другими препаратами, назначенными другими специалистами по непсихиатрическим показаниям, и что не всегда он, психиатр, будет своевременно в курсе обо всех этих назначениях – и всегда учитывать этот факт при планировании психофармакологического лечения каждого конкретного пациента, при определении его стратегии и тактики [Ruiz P, 2017; Preskorn SH, 2018].
Статистика показывает, что пациенты с психическими расстройствами относятся к группе повышенного риска развития нежелательных межлекарственных взаимодействий [Prior PI, Baker GB, 2003; Hefner G et al, 2020].
Одна из причин этого заключается в том, что при обострении, рецидиве (повторном эпизоде) или прогрессировании основного психического расстройства такие пациенты нередко нуждаются в комбинированном психофармакологическом лечении, которое может включать в себя сразу несколько психотропных препаратов из разных фармакологических групп – например, антипсихотики (АП), антидепрессанты (АД), нормотимики (НТ), анксиолитики (АЛ), β-блокаторы (ББ) и др. Это, естественно, резко повышает вероятность развития у таких пациентов нежелательных межлекарственных взаимодействий, и может привести к сложным и трудно предсказуемым результатам подобного взаимодействия [Prior PI, Baker GB, 2003; Kennedy WK et al, 2013; Hefner G et al, 2020].
Многие пациенты с хроническими психическими расстройствами вынуждены постоянно или на протяжении длительного времени (месяцами или годами) принимать те или иные психотропные препараты, нередко – в комбинациях. Многие из них вынуждены также периодически или постоянно принимать дополнительные лекарства – например, при лечении обострения сопутствующего хронического соматического заболевания или заболевания, которое развилось de novo [Prior PI, Baker GB, 2003; Kennedy WK et al, 2013; Hefner G et al, 2020].
Несмотря на значительное повышение в последние десятилетия осведомленности психиатров о возможности нежелательных межлекарственных взаимодействий между психотропными и другими препаратами и о той роли, которую могут играть изоферменты системы цитохрома P450 печени (CYP), глюкуронидазы (UGT) и белок P-gp в этих взаимодействиях, уровень этой осведомленности все еще остается недопустимо низким. Именно это и предопределяет высокую актуальность данной темы на современном этапе [Prior PI, Baker GB, 2003; Kennedy WK et al, 2013; Hefner G et al, 2020].
Ниже мы кратко напомним читателю основные факты о путях и механизмах развития нежелательных межлекарственных взаимодействий.
Основные факты о межлекарственных взаимодействиях
Как известно, основным органом, в котором происходят окислительный метаболизм, обезвреживание и подготовка к экскреции с мочой и/или с желчью и затем с калом большинства лекарств (в том числе и психотропных), а также большинства ксенобиотиков, ядов и токсинов, – является печень. Другие органы и ткани, такие как почки, головной и спинной мозг, кожа, кровь, легкие и слизистая ЖКТ, – вносят гораздо менее значимый вклад в эти процессы [Krishna DR, Klotz U, 1994].
Для большинства психотропных препаратов, в том числе для большинства АП и АД, основным путем их выведения из организма является окислительный метаболизм в печени при участии тех или иных изоферментов системы цитохрома P450 печени. В дальнейшем окисленные, более водорастворимые, метаболиты лекарств нередко подвергаются второму этапу обезвреживания, еще больше повышающему их растворимость в воде, – конъюгации с серной, глюкуроновой или уксусной кислотой (сульфатированию, глюкуронизации или ацетилированию). Окисленные и/или конъюгированные метаболиты лекарств затем выводятся в основном с мочой и, в небольшой степени, также с желчью (то есть в конечном итоге – с калом). Следует иметь в виду, что у некоторых лекарств, в том числе у некоторых АП и АД, в результате окислительного этапа печеночного метаболизма образуются активные метаболиты – иногда даже более активные, чем родительское соединение [Javaid JI, 1994].
Поскольку большинство психотропных препаратов, включая и большинство АД, и большинство АП (как типичных – ТАП, так и атипичных – ААП) – подвергаются окислительному метаболизму в печени при участии изоферментов системы цитохрома P450 (CYP), а многие из них сами могут сильно влиять на активность CYP в ту или иную сторону, – то очень важно, чтобы и психиатры, и врачи других специальностей были хорошо осведомлены об особенностях совместного применения психотропных препаратов с препаратами других фармакологических групп, которые могут ингибировать или, напротив, индуцировать те или иные изоферменты CYP [Urichuk L et al, 2008].
Возможное добавление или, наоборот, отмена каких-либо других (не психотропных) препаратов может сильно повлиять на эффективность, безопасность и переносимость параллельно проводимой психотропной терапии на многих уровнях – например, изменяя всасывание, распределение, метаболизм или выведение тех или иных психотропных препаратов или их активных метаболитов [Kennedy WK, et al, 2013].
В повседневной клинической практике психиатра особенно большое значение имеют те межлекарственные взаимодействия, которые реализуются через разнонаправленные воздействия на активность тех или иных изоферментов системы цитохрома P450 печени, во вторую очередь – межлекарственные взаимодействия, реализующиеся через влияние на глюкуронилтрансферазы (UGT) или на активность белка P-gp [Kennedy WK, et al, 2013].
Поскольку большинство АП и АД метаболизируются теми или иными изоферментами CYP450, то ингибиторы этих изоферментов (например, такие как ритонавир, кетоконазол, флувоксамин, пароксетин, бупропион, ципрофлоксацин) – могут повышать их уровни в плазме крови и замедлять их обезвреживание и выведение. Это может привести к усилению как основного фармакологического действия данных препаратов, так и их ПЭ, а порой даже к проявлениям острой и/или хронической токсичности данных препаратов, к явлениям их передозировки и даже к летальным исходам. И наоборот, индукторы изоферментов CYP450 печени, такие как карбамазепин, фенитоин, фенобарбитал, рифампицин, никотин, алкоголь, – могут снижать уровни многих АП и АД в плазме крови и ускорять их обезвреживание и выведение. Это может привести к снижению или даже полной утрате терапевтической эффективности АП и/или АД, к рецидиву или обострению основного психического расстройства, и даже к совершению пациентом суицида на фоне внезапного рецидива психического расстройства [Spina E et al, 2003; Shafiekhani M et al, 2018; Kratz T, Diefenbacher A, 2019].
Такого рода межлекарственные взаимодействия особенно опасны в случае психотропных лекарств с узким терапевтическим диапазоном (то есть с легкостью достижения токсических уровней даже при сравнительно небольшой передозировке или небольшом повышении концентрации препарата в крови) и/или с критическим значением поддержания стабильного терапевтически эффективного уровня данного лекарства в крови для поддержания и сохранения психической стабильности больного (ввиду его полирезистентности к другим препаратам), как клозапин или трициклические антидепрессанты (ТЦА) [Spina E et al, 2003; Shafiekhani M et al, 2018; Kratz T, Diefenbacher A, 2019].
Кроме фармакокинетических взаимодействий, врачам следует учитывать также вероятность взаимодействий на уровне фармакодинамики. По этой причине следует по возможности избегать совместного назначения лекарств с частично или полностью взаимно перекрывающимися, суммирующимися или взаимно усиливающими друг друга ПЭ, такими как сердечно-сосудистые, седативные, М-холиноблокирующие, экстрапирамидные или кардиометаболические ПЭ, или риск серотонинового синдрома [Shafiekhani M et al, 2018].
Также следует по возможности избегать совместного назначения лекарств, полезные фармакологические эффекты которых взаимно аннигилируются с ПЭ других лекарств из данной комбинации (например, желательно избегать назначения при психотической форме депрессии АД совместно с потенциально депрессогенным ТАП – для этого следует выбрать ААП со «встроенными» антидепрессивными свойствами) [Shafiekhani M et al, 2018].
На рис. № 1 показано распределение важности роли тех или иных изоферментов системы цитохрома P450 печени в окислительном метаболизме и экскреции психотропных препаратов [Kratz T, Diefenbacher A, 2019].
Как можно видеть из круговой диаграммы на рисунке 1, изоферментами системы цитохрома P450 (CYP), особенно важными для окислительного катаболизма психотропных препаратов, являются (в порядке убывания значимости) CYP1A2, CYP3A4, CYP2D6, CYP2C19, CYP2B6 и CYP2C9 [Kratz T, Diefenbacher A, 2019].
Комбинация двух лекарств может привести к фармакокинетическому взаимодействию, если одно из вводимых лекарств (лекарство № 1) ингибирует или индуцирует тот или иной изофермент системы P450 печени («препарат-хищник»), а другое лекарство в этой комбинации (лекарство № 2) – в значительной степени катаболизируется именно этим изоферментом, индуцируемым или ингибируемым лекарством № 1 («препарат-жертва») [Kratz T, Diefenbacher A, 2019].
Однако очень часто в повседневной клинической практике возникает ситуация, когда два лекарства конкурируют за один и тот же изофермент CYP, конкурентно ингибируя метаболизм друг друга и повышая концентрации друг друга в плазме крови. В таких случаях каждый из двух препаратов в комбинации – является одновременно и «хищником», и «жертвой» взаимодействия [Kratz T, Diefenbacher A, 2019].
Таким образом, для правильного расчета возможных межлекарственных взаимодействий у конкретного пациента очень важно знать, какими путями и с использованием каких изоферментов CYP катаболизируется каждое из лекарств, принимаемых пациентом, и каким образом, с какой силой и в какую сторону каждое из этих лекарств влияет на активность тех или иных изоферментов CYP – ингибирует, индуцирует или не оказывает клинически значимого влияния [Kratz T, Diefenbacher A, 2019].
Так, в частности, при назначении психотропных препаратов пожилым пациентам необходимо учитывать возможность ингибирования некоторыми из них изофермента CYP2D6, который играет важную роль в катаболизме многих лекарств, используемых в лечении типичных соматических болезней пожилого возраста (антигипертензивных, гиполипидемических препаратов и др.), а также в катаболизме ряда других психотропных препаратов [Kratz T, Diefenbacher A, 2019].
Другой характерный пример нежелательных межлекарственных взаимодействий – возможность резкого повышения концентрации в плазме крови некоторых ААП, метаболизируемых изоферментом CYP1A2, например оланзапина, при их совместном применении с ципрофлоксацином, который сильно ингибирует CYP1A2 [Benkert O, Hippius H, 2018].
Помимо взаимодействий лекарств друг с другом, важно учитывать и возможность их взаимодействия с некоторыми биологически активными добавками (БАДами) и даже с некоторыми компонентами пищи. Так, в частности, грейпфрутовый сок, а точнее некоторые содержащиеся в нем горькие полифенольные соединения (например, нарингенин), могут сильно ингибировать изоферменты цитохрома P450 печени, особенно CYP3A4. По этой причине грейпфрутовый сок может в 3-5 раз повысить биодоступность и уровень в плазме крови таких психотропных препаратов, метаболизируемых через CYP3A4, как кветиапин, кломипрамин, карбамазепин и буспирон. Пациенты должны быть проинформированы об этом и проинструктированы избегать употребления больших количеств грейпфрутового сока [Etheridge AS et al, 2007].
Важно отметить, что большинство АП и АД являются высоколипофильными соединениями. Это облегчает их проникновение в мозг, где они, собственно, и реализуют свое психотропное действие. Но это же их свойство облегчает и их экстракцию печенью из плазмы крови. В дальнейшем экстрагированное клетками печени из плазмы крови психотропное лекарство обычно подвергается экстенсивному окислительному метаболизму с помощью тех или иных изоферментов системы P450 (CYP) для повышения его растворимости в воде и облегчения его выведения из организма [Scordo MG, Spina E, 2002].
Существует очень широкая межиндивидуальная вариабельность скорости биотрансформации в печени тех или иных АП и АД у разных людей. Это приводит к значительным различиям в достигаемых при приеме фиксированных доз этих препаратов концентрациях в плазме крови у разных людей. А это, в свою очередь, приводит к значительным различиям как в терапевтической эффективности, так и в переносимости, уровне ПЭ и в токсичности одной и той же дозы одного и того же препарата у разных людей. Это диктует необходимость гибкого индивидуального подбора режима дозирования психотропной терапии для каждого конкретного пациента, с учетом индивидуальных особенностей его фармакогенетики, а также особенностей фармакокинетики и фармакодинамики разных психотропных препаратов именно у него [Scordo MG, Spina E, 2002].
Многие АД и АП (как ТАП, так и некоторые ААП) в значительной степени метаболизируются изоферментом CYP2D6. Между тем однонуклеотидные генетические полиморфизмы, сильно изменяющие степень его активности, очень широко распространены в популяции. Генетические полиморфизмы некоторых других изоферментов системы цитохрома P450, особенно CYP1A2 и CYP3A4, тоже очень распространены в популяции. Все это способствует большой межиндивидуальной вариабельности фармакокинетики многих АД и АП, и сильно осложняет врачу задачу учета и прогнозирования риска неблагоприятных межлекарственных взаимодействий [Scordo MG, Spina E, 2002].
Кроме взаимодействий через P450, важную роль играют также взаимодействия, связанные с P-гликопротеином
(P-gp), показанные на рис. 2. Этот белок, известный также как белок множественной лекарственной устойчивости, является АТФ-зависимым насосом оттока с широкой субстратной специфичностью [Schinkel AH, Jonker JW, 2003].
Белок P-gp в высокой степени экспрессируется в апикальной мембране кишечного эпителия, гепатоцитах, эпителии проксимальных канальцев почек, а также в эндотелии капилляров головного мозга. Он перекачивает различные ксенобиотики из плазмы крови обратно в просвет кишечника, в желчные протоки, почечные канальцы, а также из ткани мозга обратно в мозговые капилляры [Kim JE et al, 2014].
Примером взаимодействия через P-gp является резкое усиление ингибиторами P-gp – верапамилом или омепразолом – центрального дельта-опиоидного эффекта лоперамида, который в норме почти не проникает через ГЭБ, или усиление литием (также ингибитором P-gp) эффектов АД, АП, донепезила и др. [Marchetti S et al, 2007].
Фармакокинетические особенности и преимущества тиаприда
Тиаприд практически не метаболизируется цитохромами P450 печени, и выводится в основном в неизмененном виде, посредством почечной экскреции (с мочой) – до 80%. Еще до 20% неизмененного тиаприда – выводится посредством печеночной экскреции в желчь и последующего удаления с калом [Cudennec A et al, 1997; Rey E et al, 1982; Stahl SM, 2013; Ястребов ДВ, 2015].
Сам тиаприд также не влияет на активность каких-либо изоферментов системы цитохрома P450 печени или глюкуронидаз (UGT) – не индуцирует и не ингибирует ни один из них [Mizuchi A et al, 1983; Rey E et al, 1982; Stahl SM, 2013; Ястребов ДВ, 2015].
Кроме того, тиаприд также практически не связывается с белками плазмы крови, не подвергается конъюгации с глюкуронидом, сульфатом или ацетатом, не является высокоаффинным субстратом белка P450 [Точилов ВА, Протальская АГ, 1998; Roos RA et al, 1986].
Стоит отметить, что практически полное отсутствие печеночного метаболизма через систему цитохрома P450 – вообще характерная особенность всех сульфонил-замещенных бензамидов, кроме сульпирида, который все-таки в небольшой, клинически незначимой степени метаболизируется в печени [Ястребов ДВ, 2015].
Период полувыведения (T1/2) у всех сульфонил-замещенных бензамидов достаточно короткий. В случае тиаприда он варьирует от 2 до 4 часов [Peters DH, Faulds D, 1994; Ястребов ДВ, 2015].
Отсутствие у тиаприда печеночного метаболизма позволяет с успехом применять его у пожилых людей с возрастным снижением функции печени и у пациентов с поражениями печени, в том числе тяжелыми (например, с тяжелым алкогольным гепатитом и даже с алкогольным циррозом печени) [Минко АИ, 2019].
Все эти фармакокинетические особенности тиаприда обуславливают весьма низкий потенциал для развития нежелательных межлекарственных взаимодействий при сочетании тиаприда с другими лекарствами, включая мощные ингибиторы ряда изоферментов системы цитохрома P450 (например, ритонавир, флувоксамин, кетоконазол и др.), их мощные индукторы (например, карбамазепин или рифампицин), мощные блокаторы белка P-gp (верапамил, дилтиазем, циклоспорин, литий, омепразол и др.) [Peters DH, Faulds D, 1994].
Фармакодинамика тиаприда
Тиаприд – это ААП из группы сульфонил-замещенных бензамидов, близкий химический родственник сульпирида, амисульприда, сультоприда и метоклопрамида. Он является селективным антагонистом (точнее, весьма слабым парциальным агонистом) дофаминовых рецепторов подтипов D2 и D3, преимущественно в лимбических областях мозга и в голубоватом пятне [Karia S et al, 2013; Морозов ПВ с соавт, 2020; Fekete S et al, 2021].
В целом сравнение сульфонил-замещенных бензамидов, как подгруппы ААП, с ТАП показывает, что характерными для всей подгруппы замещенных бензамидов отличительными особенностями рецепторного профиля является высокая селективность их связывания с дофаминовыми рецепторами D2 и D3 подтипов, при минимальном их сродстве к дофаминовым рецепторам подтипа D1 (блокада которых неблагоприятно влияет на когнитивное функционирование пациентов), и практически полное отсутствие сродства к гистаминовым, холинергическим, адренергическим, ГАМК, бензодиазепиновым, опиоидным или каким-либо еще рецепторам головного мозга [Stahl SM, 2013; Ястребов ДВ, 2015; Коробов НВ, 2016].
Между тем связывание с гистаминовыми H1, мускариновыми холинергическими, α1 адренергическими рецепторами характерно для многих других АП, и обуславливает целый ряд нежелательных ПЭ, таких как чрезмерная седация и сонливость (H1), ортостатическая гипотензия и тахикардия (α1), запоры, задержка мочи, сухость во рту, парез аккомодации глаз, нарушения памяти, когнитивные нарушения (КН) (М-холинорецепторы) [Stahl SM, 2013; Ястребов ДВ, 2015].
Все семейство сульфонил-замещенных бензамидов, к которому относятся такие препараты, как тиаприд, сульпирид, амисульприд, сультоприд, – обладает гораздо большей тропностью к дофаминовым D2 рецепторам лимбических и гиппокампальных областей мозга, чем к D2 рецепторам в нигростриарной системе. Как полагают, именно этим свойством бензамидных ААП, а также их слабым парциальным агонизмом (а не «молчаливым антагонизмом» или даже инверсным агонизмом, как у многих других АП) по отношению к D2 подтипу дофаминовых рецепторов – может объясняться сравнительно малая выраженность проявлений ЭПС и акатизии при лечении ААП из группы бензамидов, даже при их использовании в достаточно высоких дозах [Stahl SM, 2013; Ястребов ДВ, 2015; Быков ЮВ, Беккер РА, 2019; Беккер РА, Быков ЮВ, 2019].
Все замещенные бензамиды, включая и тиаприд, в низких и средних дозах (например, 25-50 мг/сут амисульприда, 50-200 мг/сут сульпирида или 300–600 мг/сут тиаприда), наряду с противорвотной (антиэметической) активностью, свойственной и многим другим АП, демонстрируют также специфические антидиспептические, антидиарейные, спазмолитические и регулирующие моторику (прокинетические) свойства в желудочно-кишечном тракте (ЖКТ). Они способствуют открытию привратника желудка, ускорению пассажа пищевой кашицы по ЖКТ при запорах, одновременно предотвращая развитие диареи и болезненных спазмов. Эти свойства замещенных бензамидов связывают с их одновременным воздействием как на дофаминовые D2 рецепторы, так и на серотониновые 5-HT4 рецепторы в ЖКТ [Stahl SM, 2013; Ястребов ДВ, 2015; Быков ЮВ, Беккер РА, 2019; Беккер РА, Быков ЮВ, 2019].
Наличие у замещенных бензамидов (тиаприда, сульпирида) подобных свойств – делает их высокоэффективными и удобными в клинической практике средствами для лечения синдрома раздраженного кишечника (СРК) и функциональной диспепсии (ФД) [Emmanuel A, Quigley EM, 2013].
Антипсихотическое действие тиаприда, как полагают, обусловлено блокадой дофаминовых D2 рецепторов в мезолимбическом и мезокортикальном проводящих путях, седативное – блокадой α1 адренорецепторов и D2 дофаминовых рецепторов ретикулярной формации ствола мозга, противорвотное его действие – блокадой дофаминовых D2 рецепторов триггерной зоны и рвотного центра, гипотермическое действие – блокадой α1 адренорецепторов и дофаминовых D2 рецепторов центров терморегуляции гипоталамуса, антимигренозное его действие – блокадой дофаминовых D2 рецепторов ядра тройничного нерва [Басов АН, 2013; Stahl SM, 2013; Быков ЮВ, Беккер РА, 2016].
Блокада дофаминовых D2 рецепторов в нигростриарном пути, с одной стороны, предопределяет антидискинетическое и противотикозное действие тиаприда, его высокую клиническую эффективность при синдроме Туретта и при других тикозных расстройствах, а также при купировании острых дискинезий (ОД) от других АП, а с другой – иногда может вызывать нерезко выраженные проявления ЭПС и/или акатизии при лечении тиапридом, особенно при высоких его дозах. Блокада же дофаминовых D2 рецепторов тубероинфундибулярного пути может приводить к повышению уровня пролактина в плазме крови при лечении тиапридом [Басов АН, 2013; Stahl SM, 2013; Быков ЮВ, Беккер РА, 2016].
Важной особенностью тиаприда является то, что даже при максимальных, согласно инструкции по применению препарата, дозах – процент оккупации D2 дофаминовых рецепторов стриатума никогда не превышает 80%. Это обуславливает как сбалансированность и умеренность антипсихотического действия тиаприда, так и редкость возникновения при лечении им ПЭ, связанных с чрезмерной дофаминергической блокадой в нигростриарном и мезокортикальном путях, – проявлений ЭПС и/или акатизии, нейролептических депрессий, нейролептик-индуцированного дефицитарного синдрома (НИДС) [Ястребов ДВ, 2015].
В малых дозах (50-100 мг/сут) тиаприд, подобно другим замещенным бензамидам (сульпириду, амисульприду), применяемым в малых дозах, – преимущественно блокирует пресинаптические «тормозные» (ауторегуляторные) дофаминовые D2 рецепторы. Это приводит к усилению дофаминергической нейротрансмиссии в ЦНС и к проявлению антидепрессивного, растормаживающего, активирующе-энергизирующего действия тиаприда [Stahl SM, 2013; Быков ЮВ, Беккер РА, 2019; Беккер РА, Быков ЮВ, 2019].
Вместе с тем некоторые авторы отрицают наличие у тиаприда стимулирующего, активирующе-энергизирующего компонента действия при низких его дозах, и определяют тиаприд как «бензамид с седативными свойствами, проявляющимися уже начиная с малых его доз» [Dose M, Lange HW, 2000].
Антипсихотическое действие у тиаприда является самым слабым среди всех ААП подгруппы сульфонил-замещенных бензамидов. По этому параметру тиаприд уступает не только таким мощным ААП, как сультоприд и амисульприд, но и сравнительно слабому в этом отношении сульпириду. Тем не менее антипсихотической активности тиаприда часто оказывается вполне достаточно для купирования, например, психозов позднего возраста, развивающихся на фоне тех или иных деменций, или для лечения так называемых «органических психозов», развивающихся на фоне органических поражений ЦНС (например, на фоне ВИЧ-ассоциированной энцефалопатии), или для купирования психотических проявлений при психотической форме депрессии [Абриталин ЕЮ, Краснов АА, 2021].
С другой же стороны, важным преимуществом применения именно тиаприда в вышеуказанных клинических ситуациях является то, что он реже всех остальных сульфонил-замещенных производных бензамида вызывает проявления ЭПС и/или акатизию, при том что на фоне применения других бензамидов эти ПЭ и без того возникают крайне редко [Абриталин ЕЮ, Краснов АА, 2021].
В рецепторном профиле тиаприда присутствуют также свойства сильного парциального агониста 5-HT4 подтипа серотониновых рецепторов и блокатора 5-HT7 подтипа их. Эти рецепторные свойства тиаприда предопределяют его антидепрессивную, противотревожную, анальгетическую и антимигренозную активность, а также его способность нормализовывать сон и циркадные ритмы и положительно влиять на когнитивное функционирование больных [Быков ЮВ, Беккер РА, 2019; Беккер РА, Быков ЮВ, 2019; Морозов ПВ с соавт, 2020; Абриталин ЕЮ, Краснов АА, 2021].
Наличие у тиаприда таких свойств значительно расширяет сферу его клинического применения, позволяя применять его не только при тиках, психозах, агрессивности или нарушениях поведения, но и при депрессиях и тревожных расстройствах (в комбинации с АД), при мигрени, хронических головных болях напряжения (ХГБН) и различных других хронических болевых синдромах (ХБС), например при фибромиалгии (ФМА) и др. [Быков ЮВ, Беккер РА, 2019; Беккер РА, Быков ЮВ, 2019; Морозов ПВ с соавт, 2020; Абриталин ЕЮ, Краснов АА, 2021].
Заключение
Как убедительно показывают приведенные нами данные литературы, многие пациенты с психическими расстройствами имеют одно или несколько сопутствующих (коморбидных) соматических расстройств, тоже нуждающихся в специфическом фармакологическом лечении. Это вынуждает многих психиатрических пациентов принимать одновременно несколько (или даже много) лекарств, назначенных разными специалистами в разное время и по разным поводам, для лечения всех имеющихся у них расстройств – как психических, так и соматических. В свою очередь, высокая частота коморбидности психических расстройств с целым рядом серьезных соматических заболеваний, тоже нуждающихся в активном фармакологическом лечении, в сочетании со значительной распространенностью в человеческой популяции генетических полиморфизмов таких белков, играющих важную роль в катаболизме и экскреции лекарств, как изоферменты системы смешанных оксидаз печени (иначе говоря, изоферменты системы цитохрома P450 печени), глюкуронилтрансферазы (UGT), белки системы генов множественной лекарственной устойчивости (MDR), в частности, P-гликопротеин (P-gp), – предопределяют повышенную вероятность развития разнообразных нежелательных межлекарственных взаимодействий в субпопуляции психиатрических пациентов. Эти нежелательные межлекарственные взаимодействия могут приводить как к снижению или даже полной утрате эффективности тех или иных лекарств при сочетании их с некоторыми другими лекарствами, так и к неожиданно резкому усилению и основного фармакологического эффекта некоторых лекарств, и их ПЭ, вплоть до проявлений их острой или хронической токсичности, и даже до летальных исходов при определенных неблагоприятных лекарственных сочетаниях. В свете всего вышесказанного особое значение приобретает подбор у психиатрических пациентов, особенно у тех из них, у кого имеются известные соматические отягощенности (например, коморбидная ВИЧ-инфекция), – таких психотропных препаратов и таких режимов психотропной терапии, которые имеют по возможности меньший риск нежелательных межлекарственных взаимодействий.Тиаприд - ААП из группы сульфонил-замещенных бензамидов, который в полной мере соответствует этому требованию. Он сам практически не метаболизируется изоферментами цитохрома P450 или глюкуронилтрансферазами (UGT), и не влияет на их активность (не индуцирует и не ингибирует). Кроме того, тиаприд, в отличие, например, от рисперидона, не является высокоаффинным субстратом белка P-gp. Поэтому его эффективность или вероятность развития ПЭ при лечении им не подвержены значительным изменениям под влиянием приема таких мощных ингибиторов P-gp, как верапамил, циклоспорин, омепразол или литий. В то же время широкий спектр фармакологических свойств тиаприда, в котором, наряду с умеренной антипсихотической активностью (основным свойством любого ААП), присутствуют также антидискинетическая (противотикозная), противорвотная, умеренная седативная, антидепрессивная, антиагрессивная, антидисфорическая, анксиолитическая (противотревожная), сильная анальгетическая и сильная антимигренозная активности, а также способность, благодаря его 5-HT7 блокирующим свойствам, улучшать когнитивное функционирование больных, нормализовывать сон и циркадные ритмы, потенцировать антидепрессивное действие АД и анальгетическое действие НПВС, опиоидов, – значительно расширяет диапазон тех клинических ситуаций, в которых тиаприд может быть с успехом применен. Хорошая переносимость тиаприда, низкая вероятность развития ЭПС, акатизии, ортостатической гипотензии, чрезмерной седации при лечении им, отсутствие у него М-холиноблокирующих ПЭ – делают тиаприд особенно подходящим препаратом для лечения соматически отягощенных пациентов, пациентов пожилого и старческого возраста, а также пациентов с органическими поражениями ЦНС (например, с ВИЧ-ассоциированной энцефалопатией и психозами на почве ее). Многие такие пациенты как раз принимают лекарства, имеющие высокий риск нежелательных взаимодействий со многими другими психотропными средствами, но безопасные в комбинации с тиапридом. Резюмируя, мы считаем, что тиаприд заслуживает значительно более широкого применения в психиатрии, неврологии и наркологии, и особенно – в ряде вышеупомянутых клинических ситуаций.
.
2 февраля 2022
Количество просмотров: 1891


