Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№01 2009
Открытое сравнительное исследование терапевтической эквивалентности препарата Адепресс (пароксетин) и Паксил (пароксетин) при терапии больных депрессивными расстройствами №01 2009
Номера страниц в выпуске:30-33
На фоне постоянно меняющихся условий на рынке психотропных препаратов и достаточно высокой цены на оригинальные препараты неуклонно растет производство и продажа препаратов дженерического происхождения. При этом, по данным Всемирной организации здравоохранения, во многих развивающихся странах 10–20% лекарственных препаратов, отобранных для проведения исследований по контролю качества, не могли пройти такую проверку.
На фоне постоянно меняющихся условий на рынке психотропных препаратов и достаточно высокой цены на оригинальные препараты неуклонно растет производство и продажа препаратов дженерического происхождения. При этом, по данным Всемирной организации здравоохранения, во многих развивающихся странах 10–20% лекарственных препаратов, отобранных для проведения исследований по контролю качества, не могли пройти такую проверку [1].
Выпуском дженериков активно занимаются во всех странах мира, в том числе и в России. Дженерик, как и оригинал, – официально разрешенное лекарственное средство, необходимо производить по всем технологическим и санитарным стандартам [2]. Как правило, дженерики обладают теми же лечебными свойствами, поскольку в них содержатся те же активные вещества, что и в оригинале. Побочные действия дженериков и оригинальных препаратов должны совпадать [3]. По истечении срока патентной защиты фирма-оригинал продает другим производителям полуфабрикат своего бренда – формулу, но технологию изготовления не раскрывает, поэтому способ производства (наполнители, производственное оборудование или процессы, параметры линии производства) конечного продукта может различаться, что в итоге может отразиться на безопасности и эффективности лекарственного препарата. В связи с этим при регистрации дженерических препаратов представляется необходимым анализ не только биоэквивалентности, не дающий исчерпывающей информации о препарате, но и комплексный анализ его фармацевтической эквивалентности, включающий изучение профиля безопасности и эффективности.
Пароксетин широко известен отечественным психиатрам как препарат, обладающий высокой эффективностью при лечении не только депрессивных состояний, но и широкого круга аффективных расстройств, включая обсессивно-компульсивное, паническое, генерализованное тревожное, посттравматическое стрессовое и социальную фобию [4]. Кроме того, препарат с успехом используется при лечении предменструального дисфорического расстройства, соматоформных расстройств, хронических болевых синдромов, булимии, алкоголизма и других токсикоманий [5].
Известно, что пароксетин обладает высокой селективностью в своем классе антидепрессантов (СИОЗС), т.е. соотношением между обратным захватом норадреналина и серотонина (НА/5-HT). Обладая самым мощным эффектом ингибирования обратного захвата 5-НТ, в сравнении с другими антидепрессантами он оказывает слабое ингибирующее влияние на обратный захват НА, что в меньшей степени характерно для других препаратов класса СИОЗС. Кроме того, пароксетин обладает низким аффинитетом к м-холинорецепторам (слабым антихолинергическим действием), a1-, a2- и b-адренорецепторам, а также к допаминовым (D2), 5-HT1-подобным, 5-HT2-подобным и гистаминовым H1-рецепторам, что в свою очередь определяет редкость возникновения побочных явлений. Паксил имеет более благоприятный спектр взаимодействий с соматотропными медикаментозными средствами, так как его биотрансформация ассоциируется всего лишь с двумя цитохромными ферментами печени. Препарат характеризуется коротким по сравнению с сертралином и флуоксетином периодом полувыведения, что связано с отсутствием у него активных метаболитов.
Целью проведенного исследования являлась оценка терапевтической эквивалентности препарата Адепресс (пароксетин; ОАО «ВЕРОФАРМ», Россия) и Паксила (пароксетин; ГлаксоСмитКляйн, Великобритания) при терапии больных депрессивными расстройствами.
Исследование проводилось в Отделе пограничной психиатрии ФГУ социальной и судебной психиатрии им. В.П.Сербского на базе Московской городской психиатрической клинической больницы №12. Были изучены 50 больных, наблюдавшихся амбулаторно в ПКБ №12. Критериями включения в исследование являлись наличие депрессивного расстройства в виде депрессивного эпизода легкой (F32.0) или средней (F32.1) степени выраженности либо рекуррентного депрессивного расстройства с текущим эпизодом легкой (F33.1) или умеренной (F33.2) степени выраженности; общее количество баллов по шкале депрессии Гамильтона не менее 15 и не менее 3 баллов по шкале CGI-S; возраст пациентов – от 18 до 65 лет; использование контрацепции женщинами детородного возраста; отсутствие приема лекарственных средств, обладающих психотропной активностью на протяжении не менее 1 нед до начала испытаний и во время его проведения. Критериями исключения из исследования считались возраст моложе 18 и старше 65 лет; высокий суицидальный риск; беременность или период лактации; органическое поражение центральной нервной системы; шизофрения; биполярное расстройство; алкоголизм; отсутствие улучшения при предыдущей терапии пароксетином; аллергическая реакция на пароксетин в анамнезе; эпилепсия и судорожные состояния в анамнезе; алкоголизм и злоупотребление психоактивными препаратами, шизофрения; любые клинически значимые заболевания почек, печени, сердечно-сосудистой, дыхательной системы, цереброваскулярные расстройства в стадии декомпенсации или другие прогрессирующие соматические заболевания; участие в клинических исследованиях в течение последних 3 мес; высокая вероятность отказа от выполнения условий терапии; противопоказания к применению антидепрессантов.
В начале исследования путем рандомизации по методу случайных чисел были сформированы две группы пациентов: пациенты 1-й группы (25 человек) принимали Паксил в течение 2 нед, затем Адепресс в течение оставшихся 2 нед терапии; 2-й (25 человек) – сначала принимали Адепресс в течение 2 нед, затем Паксил (оставшиеся 2 нед).
Препараты назначали в дозе 20 мг/сут. Длительность исследования составила 4 нед. При выраженной тревоге, а также бессоннице в первые дни лечения допускалось использование небольших доз короткоживущих бензодиазепиновых транквилизаторов и снотворных (лоразепам, зопиклон).
Обследование проводили до начала лечения (фон), на 7, 14 и 28-й день приема пароксетина. Общая эффективность терапии оценивалась по шкале общего клинического впечатления (CGI). Критерием эффективности по CGI являлось достижение оценки «улучшение» и «значительное улучшение». Динамика депрессии также оценивалась с помощью HDRS. Редукция симптоматики до 9 баллов и менее оценивалась как уровень ремиссии; 50% и более редукция суммы баллов оценивалась как выраженное улучшение (респондеры), на 25–49% – как незначительное улучшение (парциальные респондеры), редукция менее 25% – как отсутствие эффекта (нонреспондеры).
Нежелательные явления регистрировались с помощью шкалы оценки побочной симптоматики (UKU). Также производилась оценка витальных функций (артериальное давление, пульс). Лабораторное исследование предусматривало общие клинические анализы крови и мочи, определение глюкозы крови (проводили до начала и в конце исследования).
В 65% случаев депрессии характеризовались легкой и в 35% – средней степенью тяжести. В клинической картине имели место элементы депрессивной самооценки, окружающего и перспективы, а также вялость, апатия, безынициативность, пассивность, симптомы раздражительной слабости, ежедневная усталость, состояние бессилия, бессонница.
Анализ результатов применения пароксетина показал, что на всем протяжении лечения эффективность терапии депрессии у больных, начавших лечение с Паксила и на 14-й день перешедших на прием Адепресса (1-я группа), не отличалась от эффективности в группе с «зеркальным» дизайном исследования, т.е. вначале получивших Адепресс и перешедших на прием Паксила на 2-й неделе терапии (2-я группа; табл. 1).
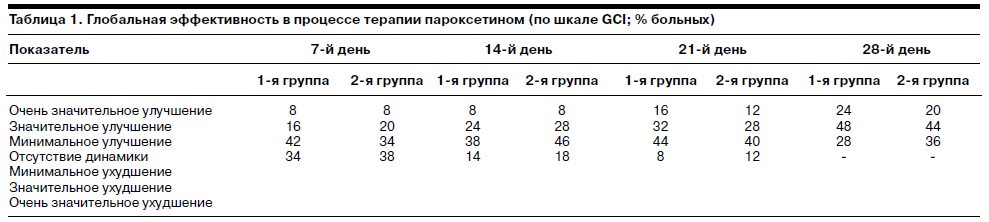
Данные табл. 1, характеризующие глобальную эффективность в процессе терапии пароксетином, свидетельствует о появлении значительного улучшения состояния уже к концу 1-й недели терапии как в 1-й (8%), так и во 2-й (8%) группе. Кроме того, в значительном количестве случаев (42 и 34% соответственно для 1 и 2-й групп) наблюдалось минимальное улучшение состояния. Более существенная положительная терапевтическая динамика отмечалась на 21-й день терапии, когда значительное улучшение наблюдалось у 16 и 12% больных (для 1 и 2-й групп соответственно). Наиболее отчетливая терапевтическая редукция депрессивной симптоматики отмечалась на 21 и 28-й день лечения: в эти дни обследования у 32 и 28% больных соответственно было достигнуто очень значительное, а у 48 и 44% – значительное улучшение состояния. Существенным является отсутствие пациентов, у которых в конце периода наблюдения не имелось хоть какой-нибудь положительной динамики или состояние ухудшилось.
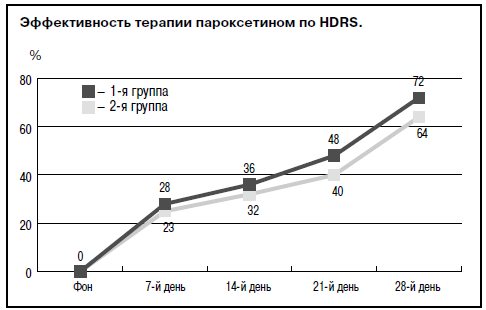
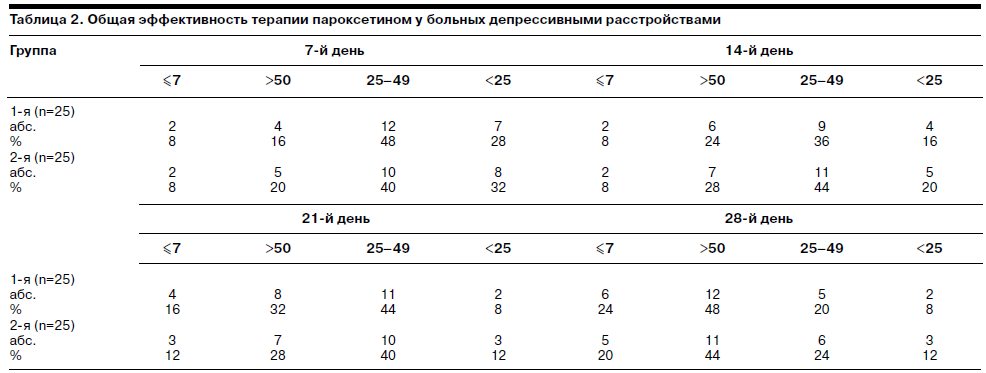
Так, начиная с 7-го дня приема пароксетина (табл. 2; см. рисунок) у больных 1 и 2-й групп уже в 8% случаев наблюдалась ремиссия, а у 16% пациентов 1-й группы и у 20% 2-й – респонс. В этот же период 48% (1-я группа) и 40% (2-я группа) пациентов характеризовались как частичные респондеры. На 2-й неделе терапии наблюдалось увеличение групп респондеров и частичных респондеров: в 1-й группе – 24 и 36% соответственно; во 2-й – 28 и 44%. Темп прироста терапевтического эффекта значительно увеличивался (почти в 2 раза) к 21-му дню терапии, когда состояние 16% больных 1-й группы и 12% – 2-й расценивалось как ремиссия, а респондерами являлись почти половина (32%) пациентов 1-й группы и половина (28%) – 2-й. К концу терапии у 24% больных 1-й группы наблюдался полный терапевтический эффект (ремиссия), а респондерами являлись 48% пациентов.
Эффективность терапии больных 2-й группы в конце лечения была практически сопоставимой с эффективностью в 1-й группе: ремиссия отмечалась в 20% случаев, респондерами являлись 44% пациентов. В остальных случаях в 1 и 2-й группах в конце лечения наблюдались случаи парциального эффекта (20 и 24% соответственно) или его отсутствие (8 и 12% соответственно).
Скорость наступления тимоаналептического эффекта, а также его выраженность практически не различались. В конце проведенного курса терапии в 1-й группе пациентов депрессивная симптоматика согласно оценке по подшкалам HDRS регрессировала на 64,3% (p<0,004), тревога/соматизация – на 42,9% (p<0,005), психомоторная ретардация – на 72,8%, расстройства сна – на 71,5% (p<0,005). Во 2-й группе общий балл значений депрессии снизился на 65,1% (p<0,005), по показателю тревога/соматизация – на 53,7% (p<0,005), психомоторная ретардация – на 71,5%, сон улучшился на 65,9% (p<0,004).
Отказов от терапии на всем протяжении лечения не было ни в одной из исследованных групп. Все нежелательные явления (НЯ), возникающие в процессе терапии антидепрессантами, относились к категории ожидаемых и проявлялись в психической, вегетативной и неврологической сферах. Качественный спектр НЯ представлен в табл. 4.
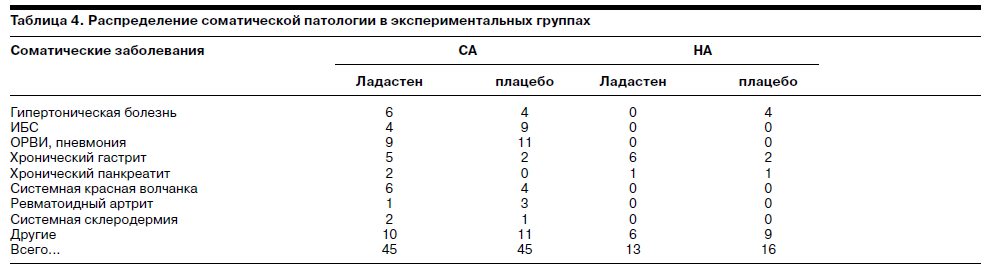
При отсутствии значимых различий в эффективности исследуемых антидепрессантов не наблюдалось различий в переносимости терапии между пациентами 1 и 2-й групп. При этом смена терапии на 2-й неделе не вызвала появления НЯ и не была заметна для пациентов обеих групп.

В целом переносимость терапии Адепрессом не имела значимых различий и соответствовала побочному профилю переносимости Паксила. Мужчины во время приема Паксила (7 человек) и во время приема Адепресса (5 человек) жаловались на задержку эякуляции и удлинение полового акта. У 3 пациентов, принимавших Паксил, и 2 – Адепресс, в течение первых 3 дней лечения транзиторно наблюдалось ухудшение состояния в форме усиления тревоги. Данное явление купировалось назначением лоразепама 2 мг/сут в течение 4 дней. Последующая отмена транквилизатора не вызывала обострения симптомов тревоги ни в одной из групп терапии. Снижение аппетита зарегистрировано у 6 человек, получавших Паксил, и у 8 – Адепресс, и оставалось актуальным на протяжении всего срока терапии. Тремор пальцев рук регистрировался только в течение 1-й недели терапии у 3 человек, принимавших Паксил, и 5 – принимавших Адепресс.
Таким образом, сравнительный анализ общей эффективности между 1 и 2-й группами показал сопоставимую эффективность лечения. По шкале CGI к моменту завершения лечения в 72% случаев для 1-й группы (p<0,001) и 63,3% – для 2-й (p<0,001) зафиксировано «значительное улучшение» и «улучшение». Достоверных различий (CGI) в динамике редукции депрессии не было вплоть до окончания периода наблюдения. Картина клинического улучшения в терапевтических группах в период смены препаратов не изменилась.
Полученные результаты свидетельствуют о высокой эффективности антидепрессивной терапии Адепрессом и Паксилом. Оба препарата имеют равнозначную тимоаналептическую активность у больных депрессивными расстройствами. Препараты одинаково эффективно воздействуют на весь симптомокомплекс депрессии, гармонично подвергая редукции тревожные, апатические, ипохондрические и инсомнические нарушения. Клиническая эквивалентность Адепресса подтверждается результатами специальных исследований, в которых показано, что он биоэквивалентен оригинальному препарату Паксил по всем фармакокинетическим параметрам. Применение Адепресса сопровождается хорошей переносимостью и редкостью возникновения НЯ. Таким образом, результаты исследования показали сопоставимость терапевтического и побочных профилей Адепресса, а значит, терапевтическую эквивалентность с оригинальным препаратом Паксил.
Выпуском дженериков активно занимаются во всех странах мира, в том числе и в России. Дженерик, как и оригинал, – официально разрешенное лекарственное средство, необходимо производить по всем технологическим и санитарным стандартам [2]. Как правило, дженерики обладают теми же лечебными свойствами, поскольку в них содержатся те же активные вещества, что и в оригинале. Побочные действия дженериков и оригинальных препаратов должны совпадать [3]. По истечении срока патентной защиты фирма-оригинал продает другим производителям полуфабрикат своего бренда – формулу, но технологию изготовления не раскрывает, поэтому способ производства (наполнители, производственное оборудование или процессы, параметры линии производства) конечного продукта может различаться, что в итоге может отразиться на безопасности и эффективности лекарственного препарата. В связи с этим при регистрации дженерических препаратов представляется необходимым анализ не только биоэквивалентности, не дающий исчерпывающей информации о препарате, но и комплексный анализ его фармацевтической эквивалентности, включающий изучение профиля безопасности и эффективности.
Пароксетин широко известен отечественным психиатрам как препарат, обладающий высокой эффективностью при лечении не только депрессивных состояний, но и широкого круга аффективных расстройств, включая обсессивно-компульсивное, паническое, генерализованное тревожное, посттравматическое стрессовое и социальную фобию [4]. Кроме того, препарат с успехом используется при лечении предменструального дисфорического расстройства, соматоформных расстройств, хронических болевых синдромов, булимии, алкоголизма и других токсикоманий [5].
Известно, что пароксетин обладает высокой селективностью в своем классе антидепрессантов (СИОЗС), т.е. соотношением между обратным захватом норадреналина и серотонина (НА/5-HT). Обладая самым мощным эффектом ингибирования обратного захвата 5-НТ, в сравнении с другими антидепрессантами он оказывает слабое ингибирующее влияние на обратный захват НА, что в меньшей степени характерно для других препаратов класса СИОЗС. Кроме того, пароксетин обладает низким аффинитетом к м-холинорецепторам (слабым антихолинергическим действием), a1-, a2- и b-адренорецепторам, а также к допаминовым (D2), 5-HT1-подобным, 5-HT2-подобным и гистаминовым H1-рецепторам, что в свою очередь определяет редкость возникновения побочных явлений. Паксил имеет более благоприятный спектр взаимодействий с соматотропными медикаментозными средствами, так как его биотрансформация ассоциируется всего лишь с двумя цитохромными ферментами печени. Препарат характеризуется коротким по сравнению с сертралином и флуоксетином периодом полувыведения, что связано с отсутствием у него активных метаболитов.
Целью проведенного исследования являлась оценка терапевтической эквивалентности препарата Адепресс (пароксетин; ОАО «ВЕРОФАРМ», Россия) и Паксила (пароксетин; ГлаксоСмитКляйн, Великобритания) при терапии больных депрессивными расстройствами.
Исследование проводилось в Отделе пограничной психиатрии ФГУ социальной и судебной психиатрии им. В.П.Сербского на базе Московской городской психиатрической клинической больницы №12. Были изучены 50 больных, наблюдавшихся амбулаторно в ПКБ №12. Критериями включения в исследование являлись наличие депрессивного расстройства в виде депрессивного эпизода легкой (F32.0) или средней (F32.1) степени выраженности либо рекуррентного депрессивного расстройства с текущим эпизодом легкой (F33.1) или умеренной (F33.2) степени выраженности; общее количество баллов по шкале депрессии Гамильтона не менее 15 и не менее 3 баллов по шкале CGI-S; возраст пациентов – от 18 до 65 лет; использование контрацепции женщинами детородного возраста; отсутствие приема лекарственных средств, обладающих психотропной активностью на протяжении не менее 1 нед до начала испытаний и во время его проведения. Критериями исключения из исследования считались возраст моложе 18 и старше 65 лет; высокий суицидальный риск; беременность или период лактации; органическое поражение центральной нервной системы; шизофрения; биполярное расстройство; алкоголизм; отсутствие улучшения при предыдущей терапии пароксетином; аллергическая реакция на пароксетин в анамнезе; эпилепсия и судорожные состояния в анамнезе; алкоголизм и злоупотребление психоактивными препаратами, шизофрения; любые клинически значимые заболевания почек, печени, сердечно-сосудистой, дыхательной системы, цереброваскулярные расстройства в стадии декомпенсации или другие прогрессирующие соматические заболевания; участие в клинических исследованиях в течение последних 3 мес; высокая вероятность отказа от выполнения условий терапии; противопоказания к применению антидепрессантов.
В начале исследования путем рандомизации по методу случайных чисел были сформированы две группы пациентов: пациенты 1-й группы (25 человек) принимали Паксил в течение 2 нед, затем Адепресс в течение оставшихся 2 нед терапии; 2-й (25 человек) – сначала принимали Адепресс в течение 2 нед, затем Паксил (оставшиеся 2 нед).
Препараты назначали в дозе 20 мг/сут. Длительность исследования составила 4 нед. При выраженной тревоге, а также бессоннице в первые дни лечения допускалось использование небольших доз короткоживущих бензодиазепиновых транквилизаторов и снотворных (лоразепам, зопиклон).
Обследование проводили до начала лечения (фон), на 7, 14 и 28-й день приема пароксетина. Общая эффективность терапии оценивалась по шкале общего клинического впечатления (CGI). Критерием эффективности по CGI являлось достижение оценки «улучшение» и «значительное улучшение». Динамика депрессии также оценивалась с помощью HDRS. Редукция симптоматики до 9 баллов и менее оценивалась как уровень ремиссии; 50% и более редукция суммы баллов оценивалась как выраженное улучшение (респондеры), на 25–49% – как незначительное улучшение (парциальные респондеры), редукция менее 25% – как отсутствие эффекта (нонреспондеры).
Нежелательные явления регистрировались с помощью шкалы оценки побочной симптоматики (UKU). Также производилась оценка витальных функций (артериальное давление, пульс). Лабораторное исследование предусматривало общие клинические анализы крови и мочи, определение глюкозы крови (проводили до начала и в конце исследования).
В 65% случаев депрессии характеризовались легкой и в 35% – средней степенью тяжести. В клинической картине имели место элементы депрессивной самооценки, окружающего и перспективы, а также вялость, апатия, безынициативность, пассивность, симптомы раздражительной слабости, ежедневная усталость, состояние бессилия, бессонница.
Анализ результатов применения пароксетина показал, что на всем протяжении лечения эффективность терапии депрессии у больных, начавших лечение с Паксила и на 14-й день перешедших на прием Адепресса (1-я группа), не отличалась от эффективности в группе с «зеркальным» дизайном исследования, т.е. вначале получивших Адепресс и перешедших на прием Паксила на 2-й неделе терапии (2-я группа; табл. 1).

Данные табл. 1, характеризующие глобальную эффективность в процессе терапии пароксетином, свидетельствует о появлении значительного улучшения состояния уже к концу 1-й недели терапии как в 1-й (8%), так и во 2-й (8%) группе. Кроме того, в значительном количестве случаев (42 и 34% соответственно для 1 и 2-й групп) наблюдалось минимальное улучшение состояния. Более существенная положительная терапевтическая динамика отмечалась на 21-й день терапии, когда значительное улучшение наблюдалось у 16 и 12% больных (для 1 и 2-й групп соответственно). Наиболее отчетливая терапевтическая редукция депрессивной симптоматики отмечалась на 21 и 28-й день лечения: в эти дни обследования у 32 и 28% больных соответственно было достигнуто очень значительное, а у 48 и 44% – значительное улучшение состояния. Существенным является отсутствие пациентов, у которых в конце периода наблюдения не имелось хоть какой-нибудь положительной динамики или состояние ухудшилось.

Так, начиная с 7-го дня приема пароксетина (табл. 2; см. рисунок) у больных 1 и 2-й групп уже в 8% случаев наблюдалась ремиссия, а у 16% пациентов 1-й группы и у 20% 2-й – респонс. В этот же период 48% (1-я группа) и 40% (2-я группа) пациентов характеризовались как частичные респондеры. На 2-й неделе терапии наблюдалось увеличение групп респондеров и частичных респондеров: в 1-й группе – 24 и 36% соответственно; во 2-й – 28 и 44%. Темп прироста терапевтического эффекта значительно увеличивался (почти в 2 раза) к 21-му дню терапии, когда состояние 16% больных 1-й группы и 12% – 2-й расценивалось как ремиссия, а респондерами являлись почти половина (32%) пациентов 1-й группы и половина (28%) – 2-й. К концу терапии у 24% больных 1-й группы наблюдался полный терапевтический эффект (ремиссия), а респондерами являлись 48% пациентов.

Эффективность терапии больных 2-й группы в конце лечения была практически сопоставимой с эффективностью в 1-й группе: ремиссия отмечалась в 20% случаев, респондерами являлись 44% пациентов. В остальных случаях в 1 и 2-й группах в конце лечения наблюдались случаи парциального эффекта (20 и 24% соответственно) или его отсутствие (8 и 12% соответственно).

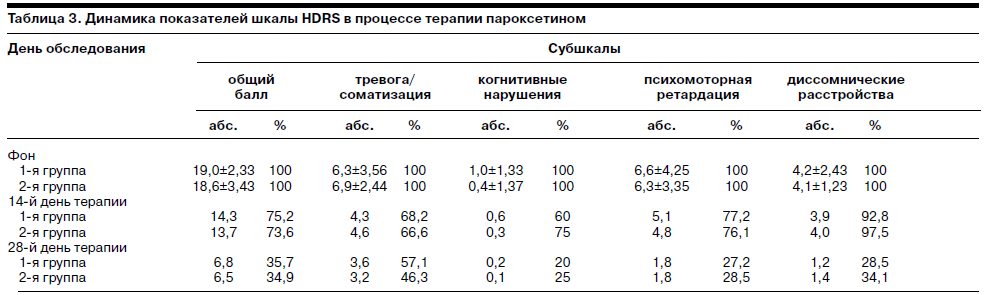
Скорость наступления тимоаналептического эффекта, а также его выраженность практически не различались. В конце проведенного курса терапии в 1-й группе пациентов депрессивная симптоматика согласно оценке по подшкалам HDRS регрессировала на 64,3% (p<0,004), тревога/соматизация – на 42,9% (p<0,005), психомоторная ретардация – на 72,8%, расстройства сна – на 71,5% (p<0,005). Во 2-й группе общий балл значений депрессии снизился на 65,1% (p<0,005), по показателю тревога/соматизация – на 53,7% (p<0,005), психомоторная ретардация – на 71,5%, сон улучшился на 65,9% (p<0,004).
Отказов от терапии на всем протяжении лечения не было ни в одной из исследованных групп. Все нежелательные явления (НЯ), возникающие в процессе терапии антидепрессантами, относились к категории ожидаемых и проявлялись в психической, вегетативной и неврологической сферах. Качественный спектр НЯ представлен в табл. 4.

При отсутствии значимых различий в эффективности исследуемых антидепрессантов не наблюдалось различий в переносимости терапии между пациентами 1 и 2-й групп. При этом смена терапии на 2-й неделе не вызвала появления НЯ и не была заметна для пациентов обеих групп.

В целом переносимость терапии Адепрессом не имела значимых различий и соответствовала побочному профилю переносимости Паксила. Мужчины во время приема Паксила (7 человек) и во время приема Адепресса (5 человек) жаловались на задержку эякуляции и удлинение полового акта. У 3 пациентов, принимавших Паксил, и 2 – Адепресс, в течение первых 3 дней лечения транзиторно наблюдалось ухудшение состояния в форме усиления тревоги. Данное явление купировалось назначением лоразепама 2 мг/сут в течение 4 дней. Последующая отмена транквилизатора не вызывала обострения симптомов тревоги ни в одной из групп терапии. Снижение аппетита зарегистрировано у 6 человек, получавших Паксил, и у 8 – Адепресс, и оставалось актуальным на протяжении всего срока терапии. Тремор пальцев рук регистрировался только в течение 1-й недели терапии у 3 человек, принимавших Паксил, и 5 – принимавших Адепресс.
Таким образом, сравнительный анализ общей эффективности между 1 и 2-й группами показал сопоставимую эффективность лечения. По шкале CGI к моменту завершения лечения в 72% случаев для 1-й группы (p<0,001) и 63,3% – для 2-й (p<0,001) зафиксировано «значительное улучшение» и «улучшение». Достоверных различий (CGI) в динамике редукции депрессии не было вплоть до окончания периода наблюдения. Картина клинического улучшения в терапевтических группах в период смены препаратов не изменилась.
Полученные результаты свидетельствуют о высокой эффективности антидепрессивной терапии Адепрессом и Паксилом. Оба препарата имеют равнозначную тимоаналептическую активность у больных депрессивными расстройствами. Препараты одинаково эффективно воздействуют на весь симптомокомплекс депрессии, гармонично подвергая редукции тревожные, апатические, ипохондрические и инсомнические нарушения. Клиническая эквивалентность Адепресса подтверждается результатами специальных исследований, в которых показано, что он биоэквивалентен оригинальному препарату Паксил по всем фармакокинетическим параметрам. Применение Адепресса сопровождается хорошей переносимостью и редкостью возникновения НЯ. Таким образом, результаты исследования показали сопоставимость терапевтического и побочных профилей Адепресса, а значит, терапевтическую эквивалентность с оригинальным препаратом Паксил.
Список исп. литературыСкрыть список1. Guberman A, Corman C. Generic substitution for brand name antiepileptic drugs: a survey. Can J Neurol Sci 2000; 27 (1): 37–43.
2. Brundtland JH. Global partnerships for health. WHO Drug Information, 1999; 13 (2): 61–2.
3. The rules governing medicinal products in the European Union. Investigation of Bioavailability and Bioequivalence, 1998; 3C: 231–44.
4. Мосолов С.Н. Клиническое применение современных антидепрессантов. СПб., 1995.
5. Ахапкин Р.В. Применение препарата Плизил (пароксетин) в психиатрической практике. Психиатр. и психофармакотер. 10 (3): 61–6.


