Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№04 2014
Проблемы терапии расстройств тревожно-депрессивного континуума №04 2014
Номера страниц в выпуске:58-60
Симпозиум, посвященный проблемам диагностики и терапии расстройств тревожно-депрессивного спектра, состоялся в рамках Конгресса ECNP-2013 (Барселона) 7 октября 2013 г. В приветственном слове профессор G.Racagni (Италия) анонсировал обсуждение изменений подходов к диагностике тревожных и депрессивных расстройств в DSM-V и биологических и фармакологических основ терапии депрессий в контексте новой классификации.
Резюме. В статье по материалам симпозиума на ЕCNP-2013 представлен обзор изменений критериев диагностики аффективных расстройств в DSM-V. Освещены аспекты современных подходов к терапии тревожных и депрессивных расстройств.
Ключевые слова: DSM-V, аффективные расстройства, агомелатин.
Treatment of anxiety-depressive continuum disorders
V.E.Medvedev
People’s Friendship University of Russia, Moscow
Summary. Article presents the review of DSM-V diagnostic criteria for affective disorders adapted from ECNP symposium. Contemporary aspects of treatment of anxiety and affective disorders are discussed.
Key words: DSM-V, affective disorders, agomelatine.
Симпозиум, посвященный проблемам диагностики и терапии расстройств тревожно-депрессивного спектра, состоялся в рамках Конгресса ECNP-2013 (Барселона) 7 октября 2013 г. В приветственном слове профессор G.Racagni (Италия) анонсировал обсуждение изменений подходов к диагностике тревожных и депрессивных расстройств в DSM-V и биологических и фармакологических основ терапии депрессий в контексте новой классификации.
Развернутый доклад «DSM-V: что нового в аффективных и тревожных расстройствах» один из главных координаторов и разработчиков DSM-V профессор D.Kupfer (США) начал с описания ключевых принципов формирования классификации. В частности, было акцентировано внимание на том, что в отличие от предшествующей версии в новой учтены: возможность коморбидности нескольких видов психических расстройств, наличие возрастной динамики и патоморфоза, а также межкультуральные отличия клинической картины психопатологических нарушений. Особо докладчик подчеркнул мобильность новой версии классификации: наличие ее электронного варианта должно позволить в будущем оперативнее вносить изменения в отдельные главы.
Описывая структуру DSM-V, D.Kupfer помимо базовой, содержащей определения психических расстройств, и второй части (критерии и коды) указал на особую роль третьей части в качестве сборника описаний наиболее дискутабельных психопатологических состояний (например, интернет-зависимость, латентная шизофрения, динамика расстройств личности и т.п.), требующих дальнейшего всестороннего изучения.
Раздел «Аффективные расстройства» претерпел значимые изменения. В частности, предпринята попытка улучшить диагностику биполярного аффективного расстройства (БАР) за счет добавления нового критерия А: «Активность или энергичность» для мании/гипомании. Данное предложение основано на исследованиях J.Angst, H.Akiskal и других ученых, свидетельствующих, что изменения энергичности и активности так же важны, как и изменения настроения. Более того, «активность или энергичность», определяемые как «период аномально повышенного настроения, раздражительности» и «аномально и постоянно повышенная энергия и активность», по мнению выступающего, могут даже рассматриваться в качестве ключевых симптомов мании/гипомании.
Переходя к обсуждению причин исключения из классификации «реакции тяжелой утраты», докладчик указал на то, что тяжелая утрата представляет собой скорее выраженный психологический дистресс, который может вызвать или усилить большой депрессивный эпизод (БДЭ) у предрасположенных пациентов. При этом подчеркивалось, что вероятность реакции тяжелой утраты и природа ее симптомов не отличаются от таковых при воздействии других тяжелых психологических стрессоров, приводящих к развитию БДЭ. Наличие БДЭ, так же как и реакции утраты, связано с высокой встречаемостью ощущения душевного неблагополучия, идей малоценности, «плохого самочувствия», суицидальных мыслей и нарушения социального и профессионального функционирования. Наконец, согласно диагностическим указаниям DSM-IV реакции тяжелой утраты длятся до 2 мес, хотя чаще всего, по утверждению D.Kupfer, их длительность составляет 1–2 года.
В то же время разработчики классификации предусмотрительно сохранили в разделе сноску о том, что БДЭ может диагностироваться наряду с (в дополнении к) нормальной реакцией на значимую утрату. Имеется также сноска, объясняющая разницу между реакцией тяжелой утраты и БДЭ.
Касаясь изменений в спецификаторах тяжести (легкий, умеренный, тяжелый, с психотическими симптомами, в частичной ремиссии, в полной ремиссии, неспецифицировано) аффективных расстройств, автор подчеркнул, что в DSM-IV отсутствовала возможность указать на наличие психотической симптоматики при отсутствии выраженной тяжести расстройства, в то время как результаты многих исследований доказывают, что не все тяжелые аффективные эпизоды являются психотическими и не все психотические аффективные эпизоды являются тяжелыми.
Особый раздел в обновленной DSM составили спецификаторы смешанных аффективных расстройств (смешанные эпизоды). В классификации представления о смешанных состояниях расширены за счет уменьшения числа симптоматических характеристик «противоположного полюса», требующихся для диагностики. Исключены перекрывающиеся симптомы «противоположного полюса» (например, симптом БДЭ «психомоторное возбуждение» не считается признаком смешанности для маниакального эпизода; маниакальная повышенная отвлекаемость не считается признаком смешанности для БДЭ). В качестве критерия смешанности рассматриваются при маниакальных и гипоманиакальных состояниях: три и более депрессивных симптома (депрессивное настроение, снижение интереса, усталость, психомоторная заторможенность, чувство бессмысленности жизни, суицидальные мысли) в течение большей части дней; при БДЭ: три и более симптомов мании (повышенный фон настроения, самоуверенность, болтливость, скачка идей, повышенная энергия или активность, участие в мероприятиях, доставляющих удовольствие, сниженная потребность во сне) в течение большинства дней.
Интересным и требующим дальнейшего обсуждения представляется включение в раздел аффективных расстройств критерия «Тревожный дистресс» (легкий, умеренный, умеренно-тяжелый, с ажитацией – тяжелый), относимого как к маниакальному эпизоду, БДЭ, гипоманиакальным эпизодам при БАР I и II типа, к большому депрессивному расстройству (БДР) и к персистирующему депрессивному расстройству (дистимия). Как минимум два симптома «тревожного дистресса» (чувство взвинченности, беспокойство, трудности сосредоточения, концентрации внимания, предчувствие надвигающихся неприятностей, страх потери контроля на протяжении большинства дней) должны присутствовать в течение большинства дней во время аффективного эпизода. Коморбидность с тревогой ассоциируется с худшим прогнозом (например, повышенным суицидальным риском, резистентностью к терапии).
Учитывая данные о том, что панические атаки могут возникать не только в рамках любого тревожного расстройства, но и при любом аффективном расстройстве, в раздел введен самостоятельный спецификатор «с паническими атаками» (например, ПТСР с ПА).
Наконец, в рубрике, посвященной генерализованному тревожному расстройству (ГТР), удалено исключение случаев, когда ГТР манифестирует во время БДЭ; теперь ГТР и БДЭ «могут быть коморбидными друг другу». В остальном прежние критерии ГТР не претерпели изменений.
Все перечисленные нововведения должны, по мнению докладчика, упростить и улучшить диагностику аффективных расстройств и расширить возможности подбора терапии в случаях коморбидности с тревожными расстройствами.
Профессор S.Stahl (США) в начале своего выступления, посвященного современным биологическим аспектам терапии расстройств «тревожно-депрессивного контину-ума», остановился на обсуждении возможности и значения перекрывания симптомов БДР и тревожных расстройств. Докладчик отметил, что несмотря на то что ключевые симптомы депрессии (депрессивный аффект, утрата интересов, ангедония, идеи малоценности, суицидальные мысли) отличаются от таковых при тревожных расстройствах (тревога, беспокойство, раздражительность, мышечное напряжение, компульсии, фобическое избегание, ПА), существует большая вероятность «перекрывания» симптомов (нарушения сна, концентрации внимания, утомляемость, психомоторное возбуждение), считающихся диагностическими и для БДЭ, и для нескольких видов тревожных расстройств. Таким образом, выявление или невыявление всего лишь нескольких симптомов может «превратить» БДЭ в тревожное расстройство и наоборот.
В то же время, по мнению S.Stahl, с терапевтической точки зрения точный диагноз в пределах этого спектра расстройств не имеет большого значения. То есть психофармакотерапия первого ряда может не сильно отличаться для пациента с БДЭ и симптомами тревоги по сравнению с пациентом с БДЭ и коморбидным тревожным расстройством с полным «набором» симптомов тревоги. Терапевтическая стратегия для пациентов с любым из этих расстройств состоит в следующем: разделение расстройства на определенные симптомы – соотнесение этих симптомов с определенными проводящими путями головного мозга (ГМ), функционирование которых нарушено, – рациональный выбор препарата с учетом специфических нейротрансмиттеров, влияющих на функционирование этих путей.
Каждый из диагностических симптомов депрессии гипотетически связан с нарушением передачи информации в определенных проводящих путях (цепях нейронов) ГМ; различные симптомы топографически локализованы в определенных участках ГМ. В частности, при депрессии регистрируется низкая активность в покое в дорсолатеральной префронтальной коре и высокая – в вентро-медиальной префронтальной коре и амигдале.
Кроме того, симптомы депрессии могут характеризоваться по их аффективной экспрессии, т.е. вызывают ли они снижение позитивного аффекта (гипотимия, отсутствие счастья, интереса, удовольствия, снижение энергии, энтузиазма, снижение бдительности и уверенности в себе) или увеличение негативного аффекта (чувство вины, одиночества, страха, тревоги, враждебность, раздражительность).
Редукция позитивного аффекта предположительно связана с дисфункцией дофаминергической и, возможно, норадренергической систем. Усиление негативной аффективности более вероятно сопряжено с дисфункцией серотонинерической и норадренергической систем.
В свою очередь развитие симптомов страха (паника, фобии) связано с патологией проводящих путей, ведущих к амигдале, и с ее повышенной активацией, а проявления тревожной обеспокоенности (дурные предчувствия, ожидания, обсессии) – с патологией в кортико-стриато-таламокортикальном пути. К нейротрансмиттерам, регулирующим нейрональные цепи, идущие к амигдале, относятся серотонин, ГАМК, глутамат, кортикотропин-рилизинг-фактор, норэпинефрин. Также в нейротрансмиссии в данных нейрональных цепях принимают участие потенциалзависимые ионные каналы. К нейромедиаторам тревожной обеспокоенности докладчик также отнес глутамат, ГАМК, серотонин, норэпинефрин и дофамин.
Еще один возможный общий механизм развития тревожной и депрессивной симптоматики – супрессия мозгового фактора некроза (brain derivate nekrosis factor, BDNF). BDNF играет заметную роль в правильном росте и формировании нейронов и межнейронных связей. Если ген, кодирующий BDNF, выключен, снижение концентрации BDNF может уменьшать способность мозга продуцировать нейроны и формировать нейрональные связи. Это ведет к уменьшению числа синапсов и даже нейронов. Также, по мнению автора, ген, кодирующий выработку BDNF, может выключаться при хроническом стрессе, что вносит свой вклад в формирование атрофии вещества ГМ.
В этой связи интересны представленные докладчиком данные, свидетельствующие, что антидепрессант агомелатин повышает уровень BDNF в префронтальной коре ГМ. Кроме того, уникальная синергия агомелатина необходима для ингибирования стресс-индуцированного высвобождения глутамата. Нейрональная активность дофамина и норэпинефрина также меняется в результате мелатонинергической активации на фоне назначения агомелатина.
В завершение своего сообщения S.Stahl подчеркнул, что проводящие пути ГМ, связанные с развитием симптомов депрессии и тревоги, в значительной степени перекрываются. Нейротрансмиттеры регулируют эффективность передачи информации в этих проводящих путях, и таким образом продукция симптомов связана как с тревогой, так и с депрессией. Таким образом, нейрофармакологические мишени для тревожных и депрессивных симптомов также перекрываются; что объясняет наличие анксиолитического эффекта у антидепрессантов (пример: агомелатин).
Имеющее важное практическое значение сообщение представил профессор K.Demyttenaere (Бельгия), критически оценивший результаты современных рандомизированных клинических исследований (РКИ) эффективности антидепрессивной терапии.
В предисловии к своему докладу K.Demyttenaere процитировал высказывание профессора McGoey (2010 г.): «Никогда ранее неадекватность РКИ не была столь очевидна многим. Но в то же время никогда ранее столь многие, начиная от регуляторных органов и заканчивая практикующими врачами, не полагались столь широко на результаты РКИ».
В подтверждение этих слов докладчик сослался на собственный анализ результатов исследований, свидетельствующий о «ежегодном снижении на 1% разницы соотношения уровня респондеров к антидепрессивной терапии по сравнению с плацебо».
В другом представленном примере наглядно демонстрировалась субъективность оценки и относительность достоверности заполнения психометрических шкал исследователями в зависимости от дизайна научной работы (периодичность визитов); табл. 1.
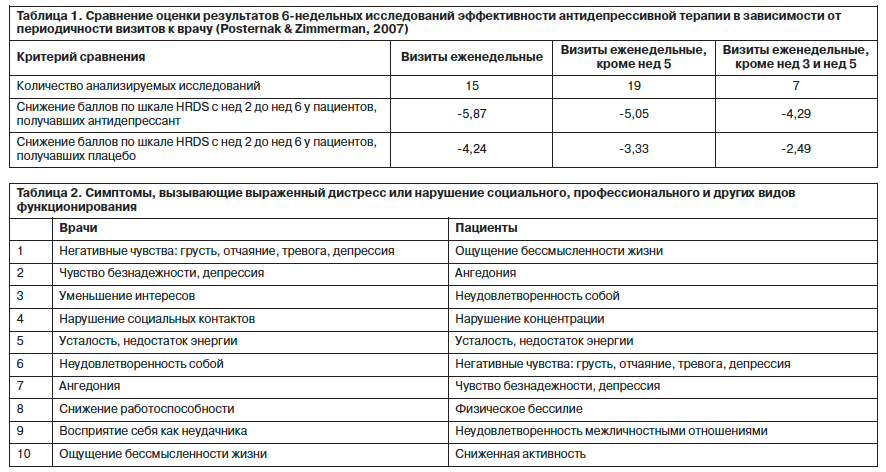
Кроме того, K.Demyttenaere обратил внимание на основные типы ошибок анализа результатов исследований и их публикаций. Например, лишь 8% исследований с негативными результатами находят отражение в печатных работах, до 61% исследований с негативными результатами не публикуются, остальные попадают в печать с большими задержками. При этом в 31% публикаций отрицательные результаты трактуются авторами как позитивные, либо расцениваются как ошибочные.
В качестве примера адекватного отражения полученной в ходе исследования информации докладчик привел данные изучения эффективности и переносимости антидепрессанта агомелатина.
В большинстве плацебо-контролируемых исследований (но не всех) эффективность препарата у взрослых и пожилых пациентов достоверно подтверждена. При кратковременной терапии агомелатином разница общего балла по шкале HAMD с плацебо на 6–8-й неделе увеличивается с увеличением тяжести исходного состояния.
Долгосрочное лечение агомелатином в профилактических целях позволяет, по данным метаанализа, добиться 56% редукции риска повторных экзацербаций депрессий. При этом большинство исследователей отмечают преимущество препарата при 24-недельной терапии пациентов с более тяжелой депрессией (25 баллов и более по HAMD) в сравнении с эсциталопрамом, сертралином, флуоксетином.
Также достоверно подтверждается эффективность агомелатина в отношении симптомов тревоги у пациентов с депрессией (по HAMD пункт 10 – психическая тревога, пункт 11 – соматическая тревога).
Существенное значение K.Demyttenaere придает оценке возможности антидепрессанта редуцировать отдельные симптомы, вызывающие нарушение социального, профессионального и других видов функционирования по мнению и врачей, и пациентов (табл. 2).
Из представленных в табл. 2 ответов следует, что врачи в отличие от пациентов чаще оценивают уменьшение проявлений негативного аффекта, а не увеличение проявлений позитивного аффекта. В данной ситуации действие агомелатина выгодно отличается от препаратов СИОЗС и селективных ингибиторов обратного захвата серотонина и норадреналина (СИОЗСН).
Таким образом, заключает автор, необходимо оценивать влияние антидепрессанта не только на депрессию в целом, но и на отдельные симптомы депрессии по DSM-V. В этом контексте современный антидепрессант агомелатин обладает значительной и достоверной краткосрочной и долгосрочной эффективностью, доказанной у пациентов с тяжелым БДР, а также при тревожных депрессиях.
Ключевые слова: DSM-V, аффективные расстройства, агомелатин.
Treatment of anxiety-depressive continuum disorders
V.E.Medvedev
People’s Friendship University of Russia, Moscow
Summary. Article presents the review of DSM-V diagnostic criteria for affective disorders adapted from ECNP symposium. Contemporary aspects of treatment of anxiety and affective disorders are discussed.
Key words: DSM-V, affective disorders, agomelatine.
Симпозиум, посвященный проблемам диагностики и терапии расстройств тревожно-депрессивного спектра, состоялся в рамках Конгресса ECNP-2013 (Барселона) 7 октября 2013 г. В приветственном слове профессор G.Racagni (Италия) анонсировал обсуждение изменений подходов к диагностике тревожных и депрессивных расстройств в DSM-V и биологических и фармакологических основ терапии депрессий в контексте новой классификации.
Развернутый доклад «DSM-V: что нового в аффективных и тревожных расстройствах» один из главных координаторов и разработчиков DSM-V профессор D.Kupfer (США) начал с описания ключевых принципов формирования классификации. В частности, было акцентировано внимание на том, что в отличие от предшествующей версии в новой учтены: возможность коморбидности нескольких видов психических расстройств, наличие возрастной динамики и патоморфоза, а также межкультуральные отличия клинической картины психопатологических нарушений. Особо докладчик подчеркнул мобильность новой версии классификации: наличие ее электронного варианта должно позволить в будущем оперативнее вносить изменения в отдельные главы.
Описывая структуру DSM-V, D.Kupfer помимо базовой, содержащей определения психических расстройств, и второй части (критерии и коды) указал на особую роль третьей части в качестве сборника описаний наиболее дискутабельных психопатологических состояний (например, интернет-зависимость, латентная шизофрения, динамика расстройств личности и т.п.), требующих дальнейшего всестороннего изучения.
Раздел «Аффективные расстройства» претерпел значимые изменения. В частности, предпринята попытка улучшить диагностику биполярного аффективного расстройства (БАР) за счет добавления нового критерия А: «Активность или энергичность» для мании/гипомании. Данное предложение основано на исследованиях J.Angst, H.Akiskal и других ученых, свидетельствующих, что изменения энергичности и активности так же важны, как и изменения настроения. Более того, «активность или энергичность», определяемые как «период аномально повышенного настроения, раздражительности» и «аномально и постоянно повышенная энергия и активность», по мнению выступающего, могут даже рассматриваться в качестве ключевых симптомов мании/гипомании.
Переходя к обсуждению причин исключения из классификации «реакции тяжелой утраты», докладчик указал на то, что тяжелая утрата представляет собой скорее выраженный психологический дистресс, который может вызвать или усилить большой депрессивный эпизод (БДЭ) у предрасположенных пациентов. При этом подчеркивалось, что вероятность реакции тяжелой утраты и природа ее симптомов не отличаются от таковых при воздействии других тяжелых психологических стрессоров, приводящих к развитию БДЭ. Наличие БДЭ, так же как и реакции утраты, связано с высокой встречаемостью ощущения душевного неблагополучия, идей малоценности, «плохого самочувствия», суицидальных мыслей и нарушения социального и профессионального функционирования. Наконец, согласно диагностическим указаниям DSM-IV реакции тяжелой утраты длятся до 2 мес, хотя чаще всего, по утверждению D.Kupfer, их длительность составляет 1–2 года.
В то же время разработчики классификации предусмотрительно сохранили в разделе сноску о том, что БДЭ может диагностироваться наряду с (в дополнении к) нормальной реакцией на значимую утрату. Имеется также сноска, объясняющая разницу между реакцией тяжелой утраты и БДЭ.
Касаясь изменений в спецификаторах тяжести (легкий, умеренный, тяжелый, с психотическими симптомами, в частичной ремиссии, в полной ремиссии, неспецифицировано) аффективных расстройств, автор подчеркнул, что в DSM-IV отсутствовала возможность указать на наличие психотической симптоматики при отсутствии выраженной тяжести расстройства, в то время как результаты многих исследований доказывают, что не все тяжелые аффективные эпизоды являются психотическими и не все психотические аффективные эпизоды являются тяжелыми.
Особый раздел в обновленной DSM составили спецификаторы смешанных аффективных расстройств (смешанные эпизоды). В классификации представления о смешанных состояниях расширены за счет уменьшения числа симптоматических характеристик «противоположного полюса», требующихся для диагностики. Исключены перекрывающиеся симптомы «противоположного полюса» (например, симптом БДЭ «психомоторное возбуждение» не считается признаком смешанности для маниакального эпизода; маниакальная повышенная отвлекаемость не считается признаком смешанности для БДЭ). В качестве критерия смешанности рассматриваются при маниакальных и гипоманиакальных состояниях: три и более депрессивных симптома (депрессивное настроение, снижение интереса, усталость, психомоторная заторможенность, чувство бессмысленности жизни, суицидальные мысли) в течение большей части дней; при БДЭ: три и более симптомов мании (повышенный фон настроения, самоуверенность, болтливость, скачка идей, повышенная энергия или активность, участие в мероприятиях, доставляющих удовольствие, сниженная потребность во сне) в течение большинства дней.
Интересным и требующим дальнейшего обсуждения представляется включение в раздел аффективных расстройств критерия «Тревожный дистресс» (легкий, умеренный, умеренно-тяжелый, с ажитацией – тяжелый), относимого как к маниакальному эпизоду, БДЭ, гипоманиакальным эпизодам при БАР I и II типа, к большому депрессивному расстройству (БДР) и к персистирующему депрессивному расстройству (дистимия). Как минимум два симптома «тревожного дистресса» (чувство взвинченности, беспокойство, трудности сосредоточения, концентрации внимания, предчувствие надвигающихся неприятностей, страх потери контроля на протяжении большинства дней) должны присутствовать в течение большинства дней во время аффективного эпизода. Коморбидность с тревогой ассоциируется с худшим прогнозом (например, повышенным суицидальным риском, резистентностью к терапии).
Учитывая данные о том, что панические атаки могут возникать не только в рамках любого тревожного расстройства, но и при любом аффективном расстройстве, в раздел введен самостоятельный спецификатор «с паническими атаками» (например, ПТСР с ПА).
Наконец, в рубрике, посвященной генерализованному тревожному расстройству (ГТР), удалено исключение случаев, когда ГТР манифестирует во время БДЭ; теперь ГТР и БДЭ «могут быть коморбидными друг другу». В остальном прежние критерии ГТР не претерпели изменений.
Все перечисленные нововведения должны, по мнению докладчика, упростить и улучшить диагностику аффективных расстройств и расширить возможности подбора терапии в случаях коморбидности с тревожными расстройствами.
Профессор S.Stahl (США) в начале своего выступления, посвященного современным биологическим аспектам терапии расстройств «тревожно-депрессивного контину-ума», остановился на обсуждении возможности и значения перекрывания симптомов БДР и тревожных расстройств. Докладчик отметил, что несмотря на то что ключевые симптомы депрессии (депрессивный аффект, утрата интересов, ангедония, идеи малоценности, суицидальные мысли) отличаются от таковых при тревожных расстройствах (тревога, беспокойство, раздражительность, мышечное напряжение, компульсии, фобическое избегание, ПА), существует большая вероятность «перекрывания» симптомов (нарушения сна, концентрации внимания, утомляемость, психомоторное возбуждение), считающихся диагностическими и для БДЭ, и для нескольких видов тревожных расстройств. Таким образом, выявление или невыявление всего лишь нескольких симптомов может «превратить» БДЭ в тревожное расстройство и наоборот.
В то же время, по мнению S.Stahl, с терапевтической точки зрения точный диагноз в пределах этого спектра расстройств не имеет большого значения. То есть психофармакотерапия первого ряда может не сильно отличаться для пациента с БДЭ и симптомами тревоги по сравнению с пациентом с БДЭ и коморбидным тревожным расстройством с полным «набором» симптомов тревоги. Терапевтическая стратегия для пациентов с любым из этих расстройств состоит в следующем: разделение расстройства на определенные симптомы – соотнесение этих симптомов с определенными проводящими путями головного мозга (ГМ), функционирование которых нарушено, – рациональный выбор препарата с учетом специфических нейротрансмиттеров, влияющих на функционирование этих путей.
Каждый из диагностических симптомов депрессии гипотетически связан с нарушением передачи информации в определенных проводящих путях (цепях нейронов) ГМ; различные симптомы топографически локализованы в определенных участках ГМ. В частности, при депрессии регистрируется низкая активность в покое в дорсолатеральной префронтальной коре и высокая – в вентро-медиальной префронтальной коре и амигдале.
Кроме того, симптомы депрессии могут характеризоваться по их аффективной экспрессии, т.е. вызывают ли они снижение позитивного аффекта (гипотимия, отсутствие счастья, интереса, удовольствия, снижение энергии, энтузиазма, снижение бдительности и уверенности в себе) или увеличение негативного аффекта (чувство вины, одиночества, страха, тревоги, враждебность, раздражительность).
Редукция позитивного аффекта предположительно связана с дисфункцией дофаминергической и, возможно, норадренергической систем. Усиление негативной аффективности более вероятно сопряжено с дисфункцией серотонинерической и норадренергической систем.
В свою очередь развитие симптомов страха (паника, фобии) связано с патологией проводящих путей, ведущих к амигдале, и с ее повышенной активацией, а проявления тревожной обеспокоенности (дурные предчувствия, ожидания, обсессии) – с патологией в кортико-стриато-таламокортикальном пути. К нейротрансмиттерам, регулирующим нейрональные цепи, идущие к амигдале, относятся серотонин, ГАМК, глутамат, кортикотропин-рилизинг-фактор, норэпинефрин. Также в нейротрансмиссии в данных нейрональных цепях принимают участие потенциалзависимые ионные каналы. К нейромедиаторам тревожной обеспокоенности докладчик также отнес глутамат, ГАМК, серотонин, норэпинефрин и дофамин.
Еще один возможный общий механизм развития тревожной и депрессивной симптоматики – супрессия мозгового фактора некроза (brain derivate nekrosis factor, BDNF). BDNF играет заметную роль в правильном росте и формировании нейронов и межнейронных связей. Если ген, кодирующий BDNF, выключен, снижение концентрации BDNF может уменьшать способность мозга продуцировать нейроны и формировать нейрональные связи. Это ведет к уменьшению числа синапсов и даже нейронов. Также, по мнению автора, ген, кодирующий выработку BDNF, может выключаться при хроническом стрессе, что вносит свой вклад в формирование атрофии вещества ГМ.
В этой связи интересны представленные докладчиком данные, свидетельствующие, что антидепрессант агомелатин повышает уровень BDNF в префронтальной коре ГМ. Кроме того, уникальная синергия агомелатина необходима для ингибирования стресс-индуцированного высвобождения глутамата. Нейрональная активность дофамина и норэпинефрина также меняется в результате мелатонинергической активации на фоне назначения агомелатина.
В завершение своего сообщения S.Stahl подчеркнул, что проводящие пути ГМ, связанные с развитием симптомов депрессии и тревоги, в значительной степени перекрываются. Нейротрансмиттеры регулируют эффективность передачи информации в этих проводящих путях, и таким образом продукция симптомов связана как с тревогой, так и с депрессией. Таким образом, нейрофармакологические мишени для тревожных и депрессивных симптомов также перекрываются; что объясняет наличие анксиолитического эффекта у антидепрессантов (пример: агомелатин).
Имеющее важное практическое значение сообщение представил профессор K.Demyttenaere (Бельгия), критически оценивший результаты современных рандомизированных клинических исследований (РКИ) эффективности антидепрессивной терапии.
В предисловии к своему докладу K.Demyttenaere процитировал высказывание профессора McGoey (2010 г.): «Никогда ранее неадекватность РКИ не была столь очевидна многим. Но в то же время никогда ранее столь многие, начиная от регуляторных органов и заканчивая практикующими врачами, не полагались столь широко на результаты РКИ».
В подтверждение этих слов докладчик сослался на собственный анализ результатов исследований, свидетельствующий о «ежегодном снижении на 1% разницы соотношения уровня респондеров к антидепрессивной терапии по сравнению с плацебо».
В другом представленном примере наглядно демонстрировалась субъективность оценки и относительность достоверности заполнения психометрических шкал исследователями в зависимости от дизайна научной работы (периодичность визитов); табл. 1.

Кроме того, K.Demyttenaere обратил внимание на основные типы ошибок анализа результатов исследований и их публикаций. Например, лишь 8% исследований с негативными результатами находят отражение в печатных работах, до 61% исследований с негативными результатами не публикуются, остальные попадают в печать с большими задержками. При этом в 31% публикаций отрицательные результаты трактуются авторами как позитивные, либо расцениваются как ошибочные.
В качестве примера адекватного отражения полученной в ходе исследования информации докладчик привел данные изучения эффективности и переносимости антидепрессанта агомелатина.
В большинстве плацебо-контролируемых исследований (но не всех) эффективность препарата у взрослых и пожилых пациентов достоверно подтверждена. При кратковременной терапии агомелатином разница общего балла по шкале HAMD с плацебо на 6–8-й неделе увеличивается с увеличением тяжести исходного состояния.
Долгосрочное лечение агомелатином в профилактических целях позволяет, по данным метаанализа, добиться 56% редукции риска повторных экзацербаций депрессий. При этом большинство исследователей отмечают преимущество препарата при 24-недельной терапии пациентов с более тяжелой депрессией (25 баллов и более по HAMD) в сравнении с эсциталопрамом, сертралином, флуоксетином.
Также достоверно подтверждается эффективность агомелатина в отношении симптомов тревоги у пациентов с депрессией (по HAMD пункт 10 – психическая тревога, пункт 11 – соматическая тревога).
Существенное значение K.Demyttenaere придает оценке возможности антидепрессанта редуцировать отдельные симптомы, вызывающие нарушение социального, профессионального и других видов функционирования по мнению и врачей, и пациентов (табл. 2).
Из представленных в табл. 2 ответов следует, что врачи в отличие от пациентов чаще оценивают уменьшение проявлений негативного аффекта, а не увеличение проявлений позитивного аффекта. В данной ситуации действие агомелатина выгодно отличается от препаратов СИОЗС и селективных ингибиторов обратного захвата серотонина и норадреналина (СИОЗСН).
Таким образом, заключает автор, необходимо оценивать влияние антидепрессанта не только на депрессию в целом, но и на отдельные симптомы депрессии по DSM-V. В этом контексте современный антидепрессант агомелатин обладает значительной и достоверной краткосрочной и долгосрочной эффективностью, доказанной у пациентов с тяжелым БДР, а также при тревожных депрессиях.


