Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№04 2014
Депрессии и патология печени: современные возможности терапии №04 2014
Номера страниц в выпуске:52-57
На сегодняшний день как для психиатров, так и для гастроэнтерологов и терапевтов становится все более очевидным, что проблема тревожно-депрессивных состояний имеет тесное отношение к соматическим заболеваниям, в том числе к патологии желудочно-кишечного тракта (ЖКТ).
Резюме. От 60 до 85% хронических заболеваний пищеварительной системы сопровождается эмоциональными расстройствами разной степени выраженности. Депрессивные расстройства характерны и для хронических диффузных заболеваний печени различного генеза и их осложнений. Основой лечения депрессии является адекватный по длительности прием антидепрессантов, который сопровождается большим количеством побочных эффектов, подчас снижающих приверженность терапии. К числу средств, влияющих на аффективную сферу, относится препарат, обладающий уникальным сочетанием свойств гепатопротектора и антидепрессанта, – адеметионин (Гептрал, «Эбботт»). Эффективность препарата доказана в многочисленных экспериментальных и клинических исследованиях. Важно вовремя выявить признаки депрессии у пациентов с заболеваниями печени для своевременного купирования возникающих аффективных расстройств назначением адеметионина.
Ключевые слова: депрессия, заболевания печени, антидепрессанты, адеметионин.
Depression and pathology of the liver: modern therapy
E.B.Grishchenko, M.I.Shchekina
Consultative-diagnostic center MEDSI, Moscow
Summary. From 60 to 85% of chronic diseases of alimentary system are accompanied by emotional disorders of different degree. Usage of which is accompanied by a large number of side effects, occasionally reducing the adherence to therapy. Antidepressant intake of adequate duration is the basic treatment of depression. The agent, having unique combination of hepatoprotector and antidepressant properties, – ademetionine (Heptral, «Abbott») is one of the drugs, influencing affective sphere. Efficiency of drugs is proved by numerous experimental and clinic studies. It is important to detect symptoms of depression in time in patients with liver disease for well-timed treatment of developing affective disorders by prescription of antidepressants, in particular – ademetionine.
Key words: googleсом, depression, liver disease, antidepressants, ademetionine.
На сегодняшний день как для психиатров, так и для гастроэнтерологов и терапевтов становится все более очевидным, что проблема тревожно-депрессивных состояний имеет тесное отношение к соматическим заболеваниям, в том числе к патологии желудочно-кишечного тракта (ЖКТ).
Ведь, согласно статистическим данным, при заболеваниях органов пищеварения вторичные психопатологические проявления отсутствуют лишь у 10,3% больных. Отдельные фрагментарные астенические нарушения отмечаются у 22,1% больных, а у 67,3% – более сложные психопатологические состояния. Результаты исследований подтверждают: от 40 до 60% больных, поступающих в гастроэнтерологические стационары, страдают депрессивным или тревожным расстройством. Особенно актуальным является вопрос маскированной (соматоформной) депрессии, депрессивное ядро которой замаскировано, скрыто соматическими расстройствами. Медико-социальное значение депрессии в общеклинической практике определяется еще и тем, что эта патология занимает 4-е место в мире среди других заболеваний по величине расходов, налагаемых на общество, которые на 97% обусловлены нетрудоспособностью больных и только на 3% – расходами на антидепрессанты.
Встречаемая в повседневной клинической практике врача-гастроэнтеролога депрессия может не только провоцировать гастроэнтерологическую патологию, но и быть реакцией на диагноз, нарушение привычного образа жизни, вызванные заболеванием и необходимостью получать лечение. Подобные реактивные состояния усиливают симптомы основного заболевания, отрицательно изменяют течение болезни и значительно осложняют его лечение. Это приводит к усугублению тяжести заболевания, снижает эффективность назначаемой терапии, повышает число дополнительных исследований. Депрессия является фактором, препятствующим установлению конструктивного контакта между пациентом и врачом, угнетает волю и инициативность больного, снижает приверженность лечению. Важнейшим аспектом депрессивных расстройств является суицидальный риск: 2/3 пациентов с диагностированной тяжелой депрессией склонны к суициду, из них 10–15% осуществляют его.
У больных с вирусными гепатитами может развиться астенодепрессивный синдром. В некоторых исследованиях отмечается повышенная частота депрессий после перенесенных острых вирусных гепатитов вплоть до случаев суицида на стадии выздоровления. У больных с хроническими вирусными гепатитами В и С риск развития депрессий повышен, что связано с побочными эффектами интерферонотерапии, которая может также спровоцировать и другие психоневрологические расстройства (повышенную возбудимость, нервозность, тревожные состояния). Возникающая в процессе применения противовирусных препаратов депрессия занимает значимое место среди причин неудачной терапии заболевания. Депрессивные расстройства различной степени выраженности вынуждают врача не только снижать дозировки, сокращать длительность курса, но и нередко досрочно прекращать лечение.
Основной патогенетический механизм депрессии, индуцированной интерфероном a (ИФН-a), заключается скорее всего в конкурентном метаболизме незаменимой аминокислоты триптофана индоламин-2,3-диоксигеназой и триптофан-диоксигеназой в хинолиновые кислоты. Повышение активности этих ферментов потенцируется экзогенным ИФН-a. При этом постепенно возникает дефицит триптофана и гидрокситриптофана – предшественника нейромедиатора серотонина, отвечающего за состояние настроения, с последующим истощением серотониновой системы в лимбических структурах головного мозга и развитием лекарственной депрессии, тревожности, нарушения памяти и внимания.
Следует отметить, что депрессия у 1/4 больных с хроническим вирусным гепатитом С может проявляться еще до начала интерферонотерапии. Это связано с неадекватным представлением о заболевании, с высокой распространенностью алкогольной и наркотической зависимости среди лиц, инфицированных вирусом гепатита С, зачастую протекающих на фоне депрессии, особенно в период абстиненции.
Проблема депрессивных расстройств в настоящее время достаточно остро стоит в развитых странах при отборе кандидатов для трансплантации печени, в связи с чем тщательное психиатрическое обследование у таких пациентов является неотъемлемой частью лечебно-диагностического процесса. Каждый 4-й пациент после трансплантации печени нуждаются в специальном лечении депрессивных расстройств.
У 2/3 лиц, страдающих хроническим алкоголизмом, имеются те или иные проявления психических заболеваний, и у 1/2 больных выявлены симптомы общей депрессии и биполярных аффективных расстройств. При этом 10% страдают тяжелой суицидоопасной депрессией, в связи с чем риск самоубийства при хроническом алкоголизме достигает 7%, превышая этот показатель при шизофрении и аффективных расстройствах. При развившейся алкогольной болезни печени психоневрологические проявления встречаются значительно чаще (примерно у 67% пациентов), чем у лиц с другими заболеваниями печени (около 1/3 пациентов), а наиболее типичными являются депрессивные и тревожные расстройства. Примерно у 25% больных с неалкогольными циррозами печени наблюдают определенные психические нарушения, чаще всего диагностируют депрессию и тревожные расстройства.
Таким образом, депрессивный синдром – это одно из достаточно частых проявлений патологии печени, которое может выступать в качестве как основного, так и второстепенного симптома заболевания.
Однако при терапии тревожного синдрома у пациентов с болезнями ЖКТ следует учитывать ряд обстоятельств: во-первых, многие из часто назначаемых анксиолитиков сами вызывают моторно-эвакуаторные нарушения верхних отделов желудка; во-вторых, следует избегать употребления седативных снотворных и транквилизаторов – они могут вызвать дискинезию. Наконец, транквилизаторы бензодиазепинового ряда приводят к развитию эффекта привыкания и физической зависимости.
Трициклические антидепрессанты (ТЦА), блокируя мускариновые рецепторы, вызывает седацию, сухость во рту, нарушения зрения, запоры, задержку мочеиспускания, дисфункцию памяти. Блокада гистаминовых рецепторов (Н1) может приводить к увеличению массы тела, блокада адренергических рецепторов (a1) – к ортостатической гипотензии, рефлекторной тахикардии. Подобные эффекты чаще наблюдаются у людей пожилого возраста и у пациентов, принимающих другие лекарственные средства с подобными эффектами. ТЦА замедляют сердечную проводимость и обладают антиаритмическим действием. Соответственно, их применения следует избегать у пациентов с нарушением сердечной проводимости и у пациентов со сниженной функцией желудочков. Эти препараты не должны применять пациенты с проявляющейся аденомой предстательной железы, нейрогенным мочевым пузырем, открытоугольной глаукомой, деменцией. Кроме того, ТЦА довольно часто вступают в нежелательные взаимодействия с соматотропными препаратами – тиреоидными и стероидными гормонами, сердечными гликозидами (дигоксином), антиаритмическими препаратами (верапамилом), b-адреноблокаторами – b-АБ (пропранололом), антикоагулянтами (варфарином).
Среди нежелательных эффектов терапии селективными ингибиторами обратного захвата серотонина (СИОЗС) чаще всего наблюдаются нарушения именно со стороны ЖКТ (потеря аппетита, тошнота, реже рвота, диарея, запоры). Другим достаточно серьезным побочным эффектом является нарушение сексуальной функции. СИОЗС – активные ингибиторы системы цитохромов Р-450, ответственных за метаболизм большинства лекарственных средств. Наиболее неблагоприятными считаются сочетания СИОЗС с сердечными гликозидами (дигоксином),
b-АБ (пропранололом), антикоагулянтами непрямого действия (варфарином), прокинетиками (цизапридом), антигистаминными средствами (терфенадином, астемизолом). Кроме того, следует обязательно учитывать гепатотоксические эффекты препаратов, резко ограничивающие их применение при поражении печени.
По степени гепатотоксического риска антидепрессанты делятся на:
• Препараты с низким риском гепатотоксического действия (пароксетин, циталопрам, миансерин, тианептин) могут назначаться больным с сопутствующей патологией в обычных дозах.
• Препараты со средним риском токсического воздействия на печень (амитриптилин, тразодон, флуоксетин, моклобемид) предпочтительно рекомендовать больным в уменьшенных суточных дозах.
• Препараты с высоким риском гепатотоксического действия (сертралин), которые противопоказаны пациентам с заболеваниями печени.
Адеметионин как нейрометаболический стимулятор с тимоаналептическим действием занимает особое положение среди препаратов с гепатопротективным действием.
Адеметионин (S-аденозил-L-метионин) – активный серосодержащий метаболит метионина, является важной метаболически плейотропной молекулой, которая принимает участие во многих клеточных реакциях в качестве предшественника синтеза глутатиона и основного донатора метильной группы, необходимой для метилирования нуклеиновых кислот, фосфолипидов, гистонов, биогенных аминов и белков. Печеночный метаболизм и физиологическая роль адеметионина Адеметионин синтезируется из пищевого метионина посредством реакции, которая катализируется ферментом метионинаденозилтрансферазой (MAT). Для данной реакции необходима метаболическая энергия аденозинтрифосфата. Фермент MAT существует в трех разных формах. Различия в регуляторных и кинетических свойствах трех изоформ MAT приводят к тому, что MAT II вносит незначительный вклад в синтез адеметионина в печени. Проходя путь трансметилирования, адеметионин превращается в гомоцистеин. Последний попадает в путь транссульфурирования и превращается в глутатион, характеризующийся важными функциями – противоокислительной и гепатопротекторной. Адеметионин также является предшественником в синтезе полиаминов, который проходит посредством реакции декарбоксилирования. Снижение уровня адеметионина может быть связано с нарушением функции данного пути (см. рисунок).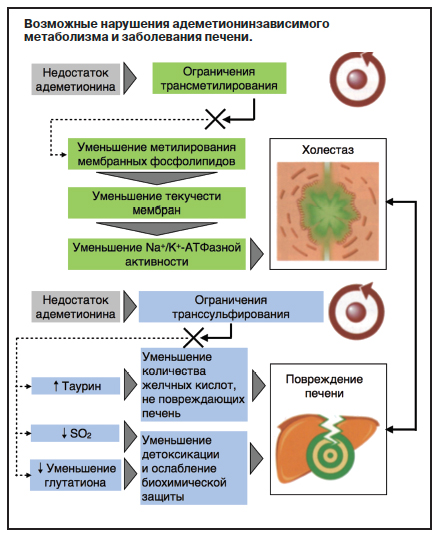
Окислительный стресс, развитию которого способствуют потребление алкоголя, вирусный гепатит и т.п., высокий уровень синтеза NO, воспалительных цитокинов (например, фактора некроза опухоли – TNF), снижают активность MAT I/III, а следовательно, и синтез адеметионина и глутатиона. Низкие уровни глутатиона в свою очередь ведут к снижению защиты от окислительного стресса, и это усугубляет поражение печени.
Адеметионин может модулировать баланс между про- и противовоспалительными цитокинами, поскольку он снижает продукцию TNF и индуцирует синтез противовоспалительных цитокинов. SAMe не только ингибирует апоптоз в нормальных гепатоцитах, но и индуцирует апоптоз в линиях раковых клеток. Таким образом, адеметионин может предотвращать внутрипеченочный канцерогенез.
Учитывая современное понимание метаболизма метионина и физиологической роли SAMe, было выдвинуто предположение, что лечение адеметионином способно снижать интенсивность поражения печени и уменьшать риск развития гепатоцеллюлярной карциномы при хроническом заболевании печени. Важно, что эти результаты не могут быть достигнуты путем повышения поступления метионина с пищей, поскольку даже 7-кратное увеличение потребления метионина неспособно значительно увеличить SAMe печени и в то же время может усилить потенциально вредное накопление метионина, которое наблюдается у больных циррозом.
В клинической практике адеметионин широко применяется в первую очередь как эффективный гепатопротектор, поскольку его эффективность в этом отношении доказана в многочисленных экспериментальных и клинических исследованиях.
Метаанализ клинических исследований свидетельствует о выраженной гепатопротекторной и клинической эффективности адеметионина при холестатических заболеваниях печени, в частности при первичном билиарном циррозе, алкогольной болезни печени, хронических вирусных гепатитах, медикаментозных поражениях печени. Он оказывает холеретическое и холекинетическое действие, обладает детоксикационными, регенерирующими, антиоксидантными, антифиброзирующими и нейропротекторными свойствами.
Одно из первых клинических исследований адеметионина при внутрипеченочном холестазе (ВПХ) было многоцентровым двойным слепым плацебо-контролируемым и включало 220 пациентов: 68% – с циррозом печени, 26% – с хроническим вирусным гепатитом, 6% – с первичным билиарным циррозом (M.Frezza и соавт., 1990). Лечение с применением адеметионина (1,6 г/сут) привело к значительному уменьшению симптомов (зуда и общей слабости) и улучшению уровня биохимических маркеров ВПХ. Значительно больше пациентов, которые получали лечение с применением адеметионина (84%), сообщали о существенном (более чем на 50%) улучшении общего самочувствия по сравнению с таковым участников, принимавших плацебо (29%).
Эти результаты подтверждаются данными, полученными в нерандомизированном наблюдательном исследовании без контроля плацебо (Fiorelli и соавт., 1999), в котором сравнивали два парентеральных режима дозирования адеметионина. Авторы метаанализа 4 менее крупных гетерогенных исследований, в которых принимали участие пациенты с ВПХ смешанной этиологии, не связанным с беременностью, пришли к выводу, что терапия с применением SAMe превосходит плацебо, значительно уменьшая зуд и уровень билирубина в сыворотке (p=0,02).
В исследованиях с применением биопсии печени у пациентов с алкогольным гепатитом было выявлено снижение уровня адеметионина и экспрессии гена MAT1A. Схожие результаты были получены у больных как с алкогольным, так и с неалкогольным циррозом печени. В многоцентровом исследовании адеметионина 123 пациента с АБП (у 1/4 из них также присутствовал хронический вирусный гепатит) были рандомизированы для получения адеметионина 1,2 г/сут или плацебо (J.Mato и соавт., 1999). Оценивались показатели общей смертности, трансплантации печени, осложнений заболеваний печени и клинической биохимии. Как показали результаты, совокупная конечная точка общей смертности и трансплантации в
2 группах статистически не отличалась (p=0,077). Однако при исключении из анализа пациентов с более поздней стадией заболевания разница была достоверной (29% в группе плацебо vs 12% в группе адеметионина; p=0,025). Результаты этого исследования свидетельствуют о потенциальном положительном эффекте адеметионина у пациентов с хроническим заболеванием печени легкой или умеренной степени.
АБП и неалкогольная жировая болезнь печени (НАЖБП) обладают достаточно сходными гистологическими чертами и некоторыми патогенетическими механизмами. Адеметионин способен оказывать благоприятное влияние на патогенез НАЖБП, поскольку он является предшественником глутатиона и донатором метильной группы для фосфатидилхолина, который необходим для структуры липопротеинов очень низкой плотности и экспорта триглицеридов в печени.
Доказательства роли адеметионина при НАЖБП были получены в доклинических исследованиях. У грызунов длительное следование рациону с дефицитом метионин холина приводило к снижению уровня SAMe и развитию стеатогепатита. У мышей MATO без гена MAT1A наблюдалось снижение мобилизации триглицеридов, секреции триглицеридов в липопротеины очень низкой плотности и синтеза фосфатидилхолина. При этом 7-дневная терапия с применением адеметионина восполняла данный дефицит (A.Cano и соавт., 2011).
Большой интерес представляют недавние исследования, в которых продемонстрировано, что адеметионин может быть эффективной дополнительной терапией для лечения хронического гепатита С. В клиническом исследовании в группе 24 пациентов с HCV генотипа 1 и отсутствием клинического ответа было установлено, что добавление адеметионина к терапии с применением пегилированного ИФН-a и рибавирина ассоциируется с улучшенной вирусной кинетикой и более высокими уровнями раннего и продолжительного вирусного клиренса (Q.Liu и соавт., 2011). При лечении адеметионином также наблюдался более высокий уровень экспрессии интерферон-стимулирующих генов в мононуклеарных клетках периферической крови. На основании полученных результатов авторы исследования пришли к выводу, что адеметионин является первым интерферон-сенсибилизирующим препаратом с эффективностью in vivo и может быть полезным добавлением к терапии, основанной на ИФН.
Таким образом, на сегодня получены убедительные доказательства того, что адеметионин играет важнейшую физиологическую роль в поддержании нормальной функции печени и здоровья в целом. Гепатоцеллюлярная концентрация адеметионина может влиять на различные патофизиологические процессы, включая окислительный стресс тканей, функции митохондрий, гепатоцеллюлярный апоптоз и злокачественные трансформации. Результаты разностороннего действия адеметионина на метаболизм явились основанием для его широкого применения в гепатологии для профилактики и лечения ВПХ, защиты печени от влияния гепатотоксических веществ, алкоголя, медикаментов и инфекционных агентов.
К сожалению, врачи общей практики не всегда достаточно осведомлены о том, что препарат обладает выраженной антидепрессивной активностью; более того, он рассматривается как атипичный антидепрессант-стимулятор.
Антидепрессивная активность адеметионина изучается более 20 лет. Еще в начале 1970-х годов были проведены первые клинические исследования, посвященные его эффективности при депрессиях. Однако общая концепция, которая достаточно подробно объясняла бы механизм антидепрессивного действия этого соединения, до сих пор не разработана. Очевидно, что адеметионин отличается от антидепрессантов всех известных на сегодня химических групп, ингибирующих захват и распад нейромедиаторов в синаптической щели. Соответственно, адеметионин принято относить к атипичным антидепрессантам, а его нейрофармакологическое действие связывать со стимулированием образования нейромедиаторов. В связи с этим адеметионин самостоятельно используется в психиатрической клинике при терапии депрессий, алкоголизма, наркоманий и аффективных расстройств, поскольку наряду с соматотропным действием препарат выявляет тимоаналептический эффект.
Результаты современных открытых и двойных слепых исследований подтвердили статистически достоверное превосходство терапии адеметионином сравнительно с плацебо и сопоставимую со стандартными ТЦА эффективность препарата при депрессиях, а также достоверно лучшую переносимость и безопасность. Статистическое обобщение (метаанализ) результатов 19 сравнительных клинических исследований с участием 498 больных с депрессиями разной степени тяжести позволило установить достоверное (на 38–60%) превышение антидепрессивной активности адеметионина (Гептрала) над активностью плацебо и схожую интенсивность его действия с антидепрессантными эффектами стандартных три- и гетероциклических антидепрессантов – имипрамина, дезипрамина, амитриптилина и других – при практически полном отсутствии свойственных им побочных эффектов. Антидепрессивная активность проявляется постепенно (начиная с конца 1-й недели лечения) и стабилизируется в течение 2-й недели терапии.
В стандартных клинических исследованиях адеметионин статистически значимо превосходил по эффективности плацебо и ТЦА при рекуррентных эндогенной и невротической депрессиях, резистентных к амитриптилину, отличаясь от них способностью прерывать рецидивы и отсутствием побочных эффектов. Практически все исследователи отмечают более быстрое развитие и стабилизацию антидепрессивного действия адеметионина (1 и 2-я недели соответственно) по сравнению со стандартными антидепрессантами, особенно при парентеральном введении. В частности, в открытом многоцентровом клиническом исследовании 195 больных с депрессией ремиссия наступила через 7–15 дней парентерального введения адеметионина по 400 мг/сут, а при его комбинировании с ТЦА эффекты наступали значительно быстрее и были более выраженными, чем при их комбинации с плацебо.
Выраженный положительный эффект терапии адеметионином проявляется при соматизированной депрессии. Результаты исследования показывают, что клинические признаки улучшения в процессе терапии адеметионином отмечаются со 2-й недели лечения, что выражается редукцией соматизированных расстройств и одновременно гипотимии. Субъективно действие препарата характеризуется нормализацией мышечного тонуса, повышением активности, улучшением переносимости нагрузок, восстановлением способности испытывать удовольствие.
Несмотря на то что молекула адеметионина известна уже более 50 лет (она была открыта еще в 1952 г.), только в последние годы благодаря большому числу научных исследований стали известны ее многочисленные плейо-тропные эффекты. Препарат может назначаться как в форме монотерапии, так и в качестве дополнительного средства для усиления действия традиционных антидепрессантов.
Адеметионин хорошо переносится и имеет небольшое количество побочных действий, поэтому может быть рекомендован пациентам с плохой реакцией на традиционные антидепрессанты. При его использовании не было выявлено токсических побочных эффектов, однако отмечена вероятность манифестации тревоги, а также нарушений маниакального спектра у больных с биполярным расстройством.
При приеме адеметионина быстро наступает антидепрессивный и противотревожный эффект (улучшение наблюдается через 3–7–14 дней в зависимости от тяжести состояния). При лечении депрессии у больных гастроэнтерологического профиля можно рекомендовать следующую схему назначения Гептрала: начальная терапия –
400 мг/сут внутривенно или внутримышечно в течение 15–20 дней, в дальнейшем поддерживающая терапия – внутрь 2–3 таблетки в сутки (800–1200 мг/сут).
Особое место при лечении депрессивных состояний, сопровождающих патологию печени, занимает адеметионин, оказывающий сочетанное гепатопротективное и антидепрессивное действие. В связи с уникальностью своих плейотропных эффектов и безопасностью адеметионин следует рассматривать как универсальный препарат выбора для широкого применения в гастроэнтерологии, гепатологии и психиатрии. Препарат может применяться самостоятельно в качестве антидепрессанта при депрессиях малой и средней выраженности, а также соматизированных депрессиях.
E-mail: katerinastepp@mail.ru
Щекина Марина Игоревна – канд. мед. наук, зав. отд-нием гастроэнтерологии КДЦ МЕДСИ. E-mail: marina_gastro@mail.ru
Ключевые слова: депрессия, заболевания печени, антидепрессанты, адеметионин.
Depression and pathology of the liver: modern therapy
E.B.Grishchenko, M.I.Shchekina
Consultative-diagnostic center MEDSI, Moscow
Summary. From 60 to 85% of chronic diseases of alimentary system are accompanied by emotional disorders of different degree. Usage of which is accompanied by a large number of side effects, occasionally reducing the adherence to therapy. Antidepressant intake of adequate duration is the basic treatment of depression. The agent, having unique combination of hepatoprotector and antidepressant properties, – ademetionine (Heptral, «Abbott») is one of the drugs, influencing affective sphere. Efficiency of drugs is proved by numerous experimental and clinic studies. It is important to detect symptoms of depression in time in patients with liver disease for well-timed treatment of developing affective disorders by prescription of antidepressants, in particular – ademetionine.
Key words: googleсом, depression, liver disease, antidepressants, ademetionine.
На сегодняшний день как для психиатров, так и для гастроэнтерологов и терапевтов становится все более очевидным, что проблема тревожно-депрессивных состояний имеет тесное отношение к соматическим заболеваниям, в том числе к патологии желудочно-кишечного тракта (ЖКТ).
Ведь, согласно статистическим данным, при заболеваниях органов пищеварения вторичные психопатологические проявления отсутствуют лишь у 10,3% больных. Отдельные фрагментарные астенические нарушения отмечаются у 22,1% больных, а у 67,3% – более сложные психопатологические состояния. Результаты исследований подтверждают: от 40 до 60% больных, поступающих в гастроэнтерологические стационары, страдают депрессивным или тревожным расстройством. Особенно актуальным является вопрос маскированной (соматоформной) депрессии, депрессивное ядро которой замаскировано, скрыто соматическими расстройствами. Медико-социальное значение депрессии в общеклинической практике определяется еще и тем, что эта патология занимает 4-е место в мире среди других заболеваний по величине расходов, налагаемых на общество, которые на 97% обусловлены нетрудоспособностью больных и только на 3% – расходами на антидепрессанты.
Встречаемая в повседневной клинической практике врача-гастроэнтеролога депрессия может не только провоцировать гастроэнтерологическую патологию, но и быть реакцией на диагноз, нарушение привычного образа жизни, вызванные заболеванием и необходимостью получать лечение. Подобные реактивные состояния усиливают симптомы основного заболевания, отрицательно изменяют течение болезни и значительно осложняют его лечение. Это приводит к усугублению тяжести заболевания, снижает эффективность назначаемой терапии, повышает число дополнительных исследований. Депрессия является фактором, препятствующим установлению конструктивного контакта между пациентом и врачом, угнетает волю и инициативность больного, снижает приверженность лечению. Важнейшим аспектом депрессивных расстройств является суицидальный риск: 2/3 пациентов с диагностированной тяжелой депрессией склонны к суициду, из них 10–15% осуществляют его.
Депрессии и заболевания печени
Помимо функциональных заболеваний ЖКТ, депрессивные расстройства характерны также для хронических диффузных заболеваний печени различного генеза и их осложнений. Так, при хронической печеночной энцефалопатии возникают эпизоды депрессии, перемежающиеся с эпизодами гипомании и возбуждения.У больных с вирусными гепатитами может развиться астенодепрессивный синдром. В некоторых исследованиях отмечается повышенная частота депрессий после перенесенных острых вирусных гепатитов вплоть до случаев суицида на стадии выздоровления. У больных с хроническими вирусными гепатитами В и С риск развития депрессий повышен, что связано с побочными эффектами интерферонотерапии, которая может также спровоцировать и другие психоневрологические расстройства (повышенную возбудимость, нервозность, тревожные состояния). Возникающая в процессе применения противовирусных препаратов депрессия занимает значимое место среди причин неудачной терапии заболевания. Депрессивные расстройства различной степени выраженности вынуждают врача не только снижать дозировки, сокращать длительность курса, но и нередко досрочно прекращать лечение.
Основной патогенетический механизм депрессии, индуцированной интерфероном a (ИФН-a), заключается скорее всего в конкурентном метаболизме незаменимой аминокислоты триптофана индоламин-2,3-диоксигеназой и триптофан-диоксигеназой в хинолиновые кислоты. Повышение активности этих ферментов потенцируется экзогенным ИФН-a. При этом постепенно возникает дефицит триптофана и гидрокситриптофана – предшественника нейромедиатора серотонина, отвечающего за состояние настроения, с последующим истощением серотониновой системы в лимбических структурах головного мозга и развитием лекарственной депрессии, тревожности, нарушения памяти и внимания.
Следует отметить, что депрессия у 1/4 больных с хроническим вирусным гепатитом С может проявляться еще до начала интерферонотерапии. Это связано с неадекватным представлением о заболевании, с высокой распространенностью алкогольной и наркотической зависимости среди лиц, инфицированных вирусом гепатита С, зачастую протекающих на фоне депрессии, особенно в период абстиненции.
Проблема депрессивных расстройств в настоящее время достаточно остро стоит в развитых странах при отборе кандидатов для трансплантации печени, в связи с чем тщательное психиатрическое обследование у таких пациентов является неотъемлемой частью лечебно-диагностического процесса. Каждый 4-й пациент после трансплантации печени нуждаются в специальном лечении депрессивных расстройств.
У 2/3 лиц, страдающих хроническим алкоголизмом, имеются те или иные проявления психических заболеваний, и у 1/2 больных выявлены симптомы общей депрессии и биполярных аффективных расстройств. При этом 10% страдают тяжелой суицидоопасной депрессией, в связи с чем риск самоубийства при хроническом алкоголизме достигает 7%, превышая этот показатель при шизофрении и аффективных расстройствах. При развившейся алкогольной болезни печени психоневрологические проявления встречаются значительно чаще (примерно у 67% пациентов), чем у лиц с другими заболеваниями печени (около 1/3 пациентов), а наиболее типичными являются депрессивные и тревожные расстройства. Примерно у 25% больных с неалкогольными циррозами печени наблюдают определенные психические нарушения, чаще всего диагностируют депрессию и тревожные расстройства.
Таким образом, депрессивный синдром – это одно из достаточно частых проявлений патологии печени, которое может выступать в качестве как основного, так и второстепенного симптома заболевания.
Фармакотерапия депрессии на фоне заболеваний печени
Основой лечения депрессии является назначение антидепрессантов. Основными показаниями к назначению этой группы лекарственных средств в гастроэнтерологии являются функциональные расстройства ЖКТ, хронические диффузные заболевания печени, упорный болевой синдром при хроническом панкреатите, ожирение, нарушения пищевого поведения.Однако при терапии тревожного синдрома у пациентов с болезнями ЖКТ следует учитывать ряд обстоятельств: во-первых, многие из часто назначаемых анксиолитиков сами вызывают моторно-эвакуаторные нарушения верхних отделов желудка; во-вторых, следует избегать употребления седативных снотворных и транквилизаторов – они могут вызвать дискинезию. Наконец, транквилизаторы бензодиазепинового ряда приводят к развитию эффекта привыкания и физической зависимости.
Трициклические антидепрессанты (ТЦА), блокируя мускариновые рецепторы, вызывает седацию, сухость во рту, нарушения зрения, запоры, задержку мочеиспускания, дисфункцию памяти. Блокада гистаминовых рецепторов (Н1) может приводить к увеличению массы тела, блокада адренергических рецепторов (a1) – к ортостатической гипотензии, рефлекторной тахикардии. Подобные эффекты чаще наблюдаются у людей пожилого возраста и у пациентов, принимающих другие лекарственные средства с подобными эффектами. ТЦА замедляют сердечную проводимость и обладают антиаритмическим действием. Соответственно, их применения следует избегать у пациентов с нарушением сердечной проводимости и у пациентов со сниженной функцией желудочков. Эти препараты не должны применять пациенты с проявляющейся аденомой предстательной железы, нейрогенным мочевым пузырем, открытоугольной глаукомой, деменцией. Кроме того, ТЦА довольно часто вступают в нежелательные взаимодействия с соматотропными препаратами – тиреоидными и стероидными гормонами, сердечными гликозидами (дигоксином), антиаритмическими препаратами (верапамилом), b-адреноблокаторами – b-АБ (пропранололом), антикоагулянтами (варфарином).
Среди нежелательных эффектов терапии селективными ингибиторами обратного захвата серотонина (СИОЗС) чаще всего наблюдаются нарушения именно со стороны ЖКТ (потеря аппетита, тошнота, реже рвота, диарея, запоры). Другим достаточно серьезным побочным эффектом является нарушение сексуальной функции. СИОЗС – активные ингибиторы системы цитохромов Р-450, ответственных за метаболизм большинства лекарственных средств. Наиболее неблагоприятными считаются сочетания СИОЗС с сердечными гликозидами (дигоксином),
b-АБ (пропранололом), антикоагулянтами непрямого действия (варфарином), прокинетиками (цизапридом), антигистаминными средствами (терфенадином, астемизолом). Кроме того, следует обязательно учитывать гепатотоксические эффекты препаратов, резко ограничивающие их применение при поражении печени.
По степени гепатотоксического риска антидепрессанты делятся на:
• Препараты с низким риском гепатотоксического действия (пароксетин, циталопрам, миансерин, тианептин) могут назначаться больным с сопутствующей патологией в обычных дозах.
• Препараты со средним риском токсического воздействия на печень (амитриптилин, тразодон, флуоксетин, моклобемид) предпочтительно рекомендовать больным в уменьшенных суточных дозах.
• Препараты с высоким риском гепатотоксического действия (сертралин), которые противопоказаны пациентам с заболеваниями печени.
Адеметионин как нейрометаболический стимулятор с тимоаналептическим действием занимает особое положение среди препаратов с гепатопротективным действием.
Адеметионин (S-аденозил-L-метионин) – активный серосодержащий метаболит метионина, является важной метаболически плейотропной молекулой, которая принимает участие во многих клеточных реакциях в качестве предшественника синтеза глутатиона и основного донатора метильной группы, необходимой для метилирования нуклеиновых кислот, фосфолипидов, гистонов, биогенных аминов и белков. Печеночный метаболизм и физиологическая роль адеметионина Адеметионин синтезируется из пищевого метионина посредством реакции, которая катализируется ферментом метионинаденозилтрансферазой (MAT). Для данной реакции необходима метаболическая энергия аденозинтрифосфата. Фермент MAT существует в трех разных формах. Различия в регуляторных и кинетических свойствах трех изоформ MAT приводят к тому, что MAT II вносит незначительный вклад в синтез адеметионина в печени. Проходя путь трансметилирования, адеметионин превращается в гомоцистеин. Последний попадает в путь транссульфурирования и превращается в глутатион, характеризующийся важными функциями – противоокислительной и гепатопротекторной. Адеметионин также является предшественником в синтезе полиаминов, который проходит посредством реакции декарбоксилирования. Снижение уровня адеметионина может быть связано с нарушением функции данного пути (см. рисунок).

Окислительный стресс, развитию которого способствуют потребление алкоголя, вирусный гепатит и т.п., высокий уровень синтеза NO, воспалительных цитокинов (например, фактора некроза опухоли – TNF), снижают активность MAT I/III, а следовательно, и синтез адеметионина и глутатиона. Низкие уровни глутатиона в свою очередь ведут к снижению защиты от окислительного стресса, и это усугубляет поражение печени.
Адеметионин может модулировать баланс между про- и противовоспалительными цитокинами, поскольку он снижает продукцию TNF и индуцирует синтез противовоспалительных цитокинов. SAMe не только ингибирует апоптоз в нормальных гепатоцитах, но и индуцирует апоптоз в линиях раковых клеток. Таким образом, адеметионин может предотвращать внутрипеченочный канцерогенез.
Учитывая современное понимание метаболизма метионина и физиологической роли SAMe, было выдвинуто предположение, что лечение адеметионином способно снижать интенсивность поражения печени и уменьшать риск развития гепатоцеллюлярной карциномы при хроническом заболевании печени. Важно, что эти результаты не могут быть достигнуты путем повышения поступления метионина с пищей, поскольку даже 7-кратное увеличение потребления метионина неспособно значительно увеличить SAMe печени и в то же время может усилить потенциально вредное накопление метионина, которое наблюдается у больных циррозом.
В клинической практике адеметионин широко применяется в первую очередь как эффективный гепатопротектор, поскольку его эффективность в этом отношении доказана в многочисленных экспериментальных и клинических исследованиях.
Метаанализ клинических исследований свидетельствует о выраженной гепатопротекторной и клинической эффективности адеметионина при холестатических заболеваниях печени, в частности при первичном билиарном циррозе, алкогольной болезни печени, хронических вирусных гепатитах, медикаментозных поражениях печени. Он оказывает холеретическое и холекинетическое действие, обладает детоксикационными, регенерирующими, антиоксидантными, антифиброзирующими и нейропротекторными свойствами.
Одно из первых клинических исследований адеметионина при внутрипеченочном холестазе (ВПХ) было многоцентровым двойным слепым плацебо-контролируемым и включало 220 пациентов: 68% – с циррозом печени, 26% – с хроническим вирусным гепатитом, 6% – с первичным билиарным циррозом (M.Frezza и соавт., 1990). Лечение с применением адеметионина (1,6 г/сут) привело к значительному уменьшению симптомов (зуда и общей слабости) и улучшению уровня биохимических маркеров ВПХ. Значительно больше пациентов, которые получали лечение с применением адеметионина (84%), сообщали о существенном (более чем на 50%) улучшении общего самочувствия по сравнению с таковым участников, принимавших плацебо (29%).
Эти результаты подтверждаются данными, полученными в нерандомизированном наблюдательном исследовании без контроля плацебо (Fiorelli и соавт., 1999), в котором сравнивали два парентеральных режима дозирования адеметионина. Авторы метаанализа 4 менее крупных гетерогенных исследований, в которых принимали участие пациенты с ВПХ смешанной этиологии, не связанным с беременностью, пришли к выводу, что терапия с применением SAMe превосходит плацебо, значительно уменьшая зуд и уровень билирубина в сыворотке (p=0,02).
В исследованиях с применением биопсии печени у пациентов с алкогольным гепатитом было выявлено снижение уровня адеметионина и экспрессии гена MAT1A. Схожие результаты были получены у больных как с алкогольным, так и с неалкогольным циррозом печени. В многоцентровом исследовании адеметионина 123 пациента с АБП (у 1/4 из них также присутствовал хронический вирусный гепатит) были рандомизированы для получения адеметионина 1,2 г/сут или плацебо (J.Mato и соавт., 1999). Оценивались показатели общей смертности, трансплантации печени, осложнений заболеваний печени и клинической биохимии. Как показали результаты, совокупная конечная точка общей смертности и трансплантации в
2 группах статистически не отличалась (p=0,077). Однако при исключении из анализа пациентов с более поздней стадией заболевания разница была достоверной (29% в группе плацебо vs 12% в группе адеметионина; p=0,025). Результаты этого исследования свидетельствуют о потенциальном положительном эффекте адеметионина у пациентов с хроническим заболеванием печени легкой или умеренной степени.
АБП и неалкогольная жировая болезнь печени (НАЖБП) обладают достаточно сходными гистологическими чертами и некоторыми патогенетическими механизмами. Адеметионин способен оказывать благоприятное влияние на патогенез НАЖБП, поскольку он является предшественником глутатиона и донатором метильной группы для фосфатидилхолина, который необходим для структуры липопротеинов очень низкой плотности и экспорта триглицеридов в печени.
Доказательства роли адеметионина при НАЖБП были получены в доклинических исследованиях. У грызунов длительное следование рациону с дефицитом метионин холина приводило к снижению уровня SAMe и развитию стеатогепатита. У мышей MATO без гена MAT1A наблюдалось снижение мобилизации триглицеридов, секреции триглицеридов в липопротеины очень низкой плотности и синтеза фосфатидилхолина. При этом 7-дневная терапия с применением адеметионина восполняла данный дефицит (A.Cano и соавт., 2011).
Большой интерес представляют недавние исследования, в которых продемонстрировано, что адеметионин может быть эффективной дополнительной терапией для лечения хронического гепатита С. В клиническом исследовании в группе 24 пациентов с HCV генотипа 1 и отсутствием клинического ответа было установлено, что добавление адеметионина к терапии с применением пегилированного ИФН-a и рибавирина ассоциируется с улучшенной вирусной кинетикой и более высокими уровнями раннего и продолжительного вирусного клиренса (Q.Liu и соавт., 2011). При лечении адеметионином также наблюдался более высокий уровень экспрессии интерферон-стимулирующих генов в мононуклеарных клетках периферической крови. На основании полученных результатов авторы исследования пришли к выводу, что адеметионин является первым интерферон-сенсибилизирующим препаратом с эффективностью in vivo и может быть полезным добавлением к терапии, основанной на ИФН.
Таким образом, на сегодня получены убедительные доказательства того, что адеметионин играет важнейшую физиологическую роль в поддержании нормальной функции печени и здоровья в целом. Гепатоцеллюлярная концентрация адеметионина может влиять на различные патофизиологические процессы, включая окислительный стресс тканей, функции митохондрий, гепатоцеллюлярный апоптоз и злокачественные трансформации. Результаты разностороннего действия адеметионина на метаболизм явились основанием для его широкого применения в гепатологии для профилактики и лечения ВПХ, защиты печени от влияния гепатотоксических веществ, алкоголя, медикаментов и инфекционных агентов.
К сожалению, врачи общей практики не всегда достаточно осведомлены о том, что препарат обладает выраженной антидепрессивной активностью; более того, он рассматривается как атипичный антидепрессант-стимулятор.
Антидепрессивная активность адеметионина изучается более 20 лет. Еще в начале 1970-х годов были проведены первые клинические исследования, посвященные его эффективности при депрессиях. Однако общая концепция, которая достаточно подробно объясняла бы механизм антидепрессивного действия этого соединения, до сих пор не разработана. Очевидно, что адеметионин отличается от антидепрессантов всех известных на сегодня химических групп, ингибирующих захват и распад нейромедиаторов в синаптической щели. Соответственно, адеметионин принято относить к атипичным антидепрессантам, а его нейрофармакологическое действие связывать со стимулированием образования нейромедиаторов. В связи с этим адеметионин самостоятельно используется в психиатрической клинике при терапии депрессий, алкоголизма, наркоманий и аффективных расстройств, поскольку наряду с соматотропным действием препарат выявляет тимоаналептический эффект.
Результаты современных открытых и двойных слепых исследований подтвердили статистически достоверное превосходство терапии адеметионином сравнительно с плацебо и сопоставимую со стандартными ТЦА эффективность препарата при депрессиях, а также достоверно лучшую переносимость и безопасность. Статистическое обобщение (метаанализ) результатов 19 сравнительных клинических исследований с участием 498 больных с депрессиями разной степени тяжести позволило установить достоверное (на 38–60%) превышение антидепрессивной активности адеметионина (Гептрала) над активностью плацебо и схожую интенсивность его действия с антидепрессантными эффектами стандартных три- и гетероциклических антидепрессантов – имипрамина, дезипрамина, амитриптилина и других – при практически полном отсутствии свойственных им побочных эффектов. Антидепрессивная активность проявляется постепенно (начиная с конца 1-й недели лечения) и стабилизируется в течение 2-й недели терапии.
В стандартных клинических исследованиях адеметионин статистически значимо превосходил по эффективности плацебо и ТЦА при рекуррентных эндогенной и невротической депрессиях, резистентных к амитриптилину, отличаясь от них способностью прерывать рецидивы и отсутствием побочных эффектов. Практически все исследователи отмечают более быстрое развитие и стабилизацию антидепрессивного действия адеметионина (1 и 2-я недели соответственно) по сравнению со стандартными антидепрессантами, особенно при парентеральном введении. В частности, в открытом многоцентровом клиническом исследовании 195 больных с депрессией ремиссия наступила через 7–15 дней парентерального введения адеметионина по 400 мг/сут, а при его комбинировании с ТЦА эффекты наступали значительно быстрее и были более выраженными, чем при их комбинации с плацебо.
Выраженный положительный эффект терапии адеметионином проявляется при соматизированной депрессии. Результаты исследования показывают, что клинические признаки улучшения в процессе терапии адеметионином отмечаются со 2-й недели лечения, что выражается редукцией соматизированных расстройств и одновременно гипотимии. Субъективно действие препарата характеризуется нормализацией мышечного тонуса, повышением активности, улучшением переносимости нагрузок, восстановлением способности испытывать удовольствие.
Несмотря на то что молекула адеметионина известна уже более 50 лет (она была открыта еще в 1952 г.), только в последние годы благодаря большому числу научных исследований стали известны ее многочисленные плейо-тропные эффекты. Препарат может назначаться как в форме монотерапии, так и в качестве дополнительного средства для усиления действия традиционных антидепрессантов.
Адеметионин хорошо переносится и имеет небольшое количество побочных действий, поэтому может быть рекомендован пациентам с плохой реакцией на традиционные антидепрессанты. При его использовании не было выявлено токсических побочных эффектов, однако отмечена вероятность манифестации тревоги, а также нарушений маниакального спектра у больных с биполярным расстройством.
При приеме адеметионина быстро наступает антидепрессивный и противотревожный эффект (улучшение наблюдается через 3–7–14 дней в зависимости от тяжести состояния). При лечении депрессии у больных гастроэнтерологического профиля можно рекомендовать следующую схему назначения Гептрала: начальная терапия –
400 мг/сут внутривенно или внутримышечно в течение 15–20 дней, в дальнейшем поддерживающая терапия – внутрь 2–3 таблетки в сутки (800–1200 мг/сут).
Заключение
Таким образом, широко распространенные в общемедицинской практике депрессивные состояния подчас являются неотъемлемой частью различной гастроэнтерологической патологии, отягощая течение заболевания и ухудшая прогноз. Их частое сочетание с заболеваниями печени существенно затрудняет лечение и снижает качество жизни больных.Особое место при лечении депрессивных состояний, сопровождающих патологию печени, занимает адеметионин, оказывающий сочетанное гепатопротективное и антидепрессивное действие. В связи с уникальностью своих плейотропных эффектов и безопасностью адеметионин следует рассматривать как универсальный препарат выбора для широкого применения в гастроэнтерологии, гепатологии и психиатрии. Препарат может применяться самостоятельно в качестве антидепрессанта при депрессиях малой и средней выраженности, а также соматизированных депрессиях.
Сведения об авторах
Грищенко Екатерина Борисовна – канд. мед. наук, врач-гастроэнтеролог, отд-ние гастроэнтерологии КДЦ МЕДСИ.E-mail: katerinastepp@mail.ru
Щекина Марина Игоревна – канд. мед. наук, зав. отд-нием гастроэнтерологии КДЦ МЕДСИ. E-mail: marina_gastro@mail.ru
Список исп. литературыСкрыть список1. Ткач С.М. Современные подходы к назначению антидепрессантов в гастроэнтерологической практике. Здоровье Украины. 2010; 7: 12–4.
2. Буеверов А.О., Ивашкин В.Т., Богомолов П.О. и др. Предварительные результаты применения адеметионина в комплексной терапии хронического гепатита. Здоровье Украины. 2010; 9: 3–4.
3. Барановский А.Ю., Райхельсон К.Л. и др. Применение Гептрала в терапии неалкогольного стеатогепатита. Здоровье Украины. 2010; 23 (253): 42–3.
4. Яковлев А.А., Котляров С.И. Возможности объективного улучшения результатов терапии хронических вирусных гепатитов препаратом Гептрал. Фарматека. 2008; 8: 36–9.
5. Снеговой А.В., Манзюк Л.В. Эффективность Гептрала® в лечении печеночной токсичности, обусловленной цитостатической химиотерапией. Фарматека. 2010; 6: 20–5.
6. Палий И.Г., Резниченко И.Г., Севак Н.М. Психосоматические расстройства в гастроэнтерологической практике: особенности клинического течения и медикаментозной терапии. Новости медицины и фармации. 2007; 6.
7. El-Serag HB, Kunik M, Richardson P, Rabeneck L. Psychiatric disorders among veterans with hepatitis C infection. Gastroenterol 2002; 123 (2): 476–82.
8. Hauser P, Khosla J, Aurora H et al. A prospective study of the incidence and open-label treatment of interferon-induced major depressive disorder in patients with hepatitis C. Mol Psychiat 2002; 7 (9): 942–47.
9. Manns MP, McHutchison JG, Gordon SC et al. Peginterferon a2b plus ribavirin compared with interferon a2b plus ribavirin for initial treatment of chronic hepatitis C: a randomised trial. Lancet 2001; 358 (9286): 958–65.
10. Otsubo T, Miyaoka H, Kamijima K et al. Depression during interferon therapy in chronic hepatitis C patients – a prospective study. Seishin Shinkeigaku Zasshi 1997; 99 (3): 101–27.
11. Capuron L, Neurauter G, Musselman DL et al. Interferon-alpha-induced changes in tryptophan metabolism: relationship to depression and paroxetine treatment. Biol Psychiat 2003; 54: 906–14.
12. Оганов Р.Г., Ольбинская Л.И., Смулевич А.Б. и др. Депрессии и расстройства депрессивного спектра в общемедицинской практике. Результаты программы КОМПАС. Кардиология. 2004; 1: 48–9.
13. Решетова Т.В., Согомонян Е.Э., Мордвинов А.В. Клинические перспективы различных эффектов препарата Гептрал.
14. Смулевич А.Б. Депрессия как общемедицинская проблема: вопросы клиники и терапии. Психиатр. и психофармакотер. 2006; 8 (3).
15. Смулевич А.Б., Дубницкая Э.Б., Иванов С.В. Опыт и перспективы применения Гептрала при терапии депрессий. Психиатр. и психофармакотер. 2002; 4 (3): 1–4.
16. Горбаков В.В., Галик В.П., Кириллов С.М. Опыт применения Гептрала в лечении диффузных заболеваний печени. Тер. архив. 1998; 10: 82–6.
17. Полуэктова Е.А. Наиболее распространенные психические нарушения у больных терапевтического профиля. Справ. поликлинич. врача. 2006; 6: 12–8.
18. Еганян Г.А. Небензодиазепиновые анксиолитики в комплексной терапии гастроэзофагеальной рефлюксной болезни и неязвенной диспепсии желудка. Лечащий врач. 2006; 7: 92–4.
19. Jiang W et al. Relationship of depression to increased risk of mortality and rehospitalization in patients with congestive heart failure. Arch Intern Med 2001; 161: 1849–56.
20. Лазебник Л.Б., Звенигородская Л.А. Метаболический синдром и органы пищеварения. М.: Анахарсис, 2009.
21. Зотов П.Б., Уманский М.С. Депрессии в общемедицинской практике (клиника, диагностика, лекарственная терапия). Метод. пособие для врачей. Тюмень, 2006.
22. Крылов В.И. Антидепрессанты в общемедицинской практике. Эффективность и безопасность терапии. ФАРМиндекс-Практик, 2003; 5: 22–32.
23. Дробижев М.Ю. Психофармакотерапия в общесоматической сети (соматотропные эффекты, совместимость с соматотропными препаратами). Психиатр. и психофармакотер. 2000; 2 (2).
24. Васюк Ю.А., Довженко Т.В. Депрессии и сердечно-сосудистые заболевания. M., 2005.
