Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№02 2012
Алгоритмы дифференцированной терапии депрессий с применением современных антидепрессантов №02 2012
Номера страниц в выпуске:56-60
Настоящая публикация представляет собой обзор литературы, посвященный современным стратегиям терапии депрессий с использованием антидепрессантов последних поколений. Внимание акцентируется на уровне доказательности данных относительно предпочтительного использования тех или иных тимоаналептиков в зависимости от значимых клинических параметров.
Резюме. Настоящая публикация представляет собой обзор литературы, посвященный современным стратегиям терапии депрессий с использованием антидепрессантов последних поколений. Внимание акцентируется на уровне доказательности данных относительно предпочтительного использования тех или иных тимоаналептиков в зависимости от значимых клинических параметров.
Ключевые слова: депрессия, алгоритмы лечения, современные антидепрессанты.
Algorithms of differential therapy of depression with modern antidepressants
D.V.Romanov
The First Moscow State Medical University I.M.Sechenov, Department of Psychiatry and Psychosomatics
Summary. The review article is devoted to up-to-date approaches to depression therapy with the use of modern antidepressants.
The attention is focused on a grade of treatment recommendations and a level of evidence based on significant clinical characteristics of depression meaningful for choice of antidepressants.
Key words: depression, algorithms of therapy, modern antidepressants.
Учитывая клиническую гетерогенность депрессивных расстройств по целому ряду параметров, включая степень тяжести, синдромальную структуру, нозологическую принадлежность и т.п., а также наблюдающееся в настоящее время значительное разнообразие терапевтических модальностей, направленных на коррекцию аффективных нарушений, сохраняет свою актуальность проблема дифференцированного подхода к лечению депрессий. Настоящая публикация ограничивается обсуждением принципов фармакотерапии депрессий с акцентом на тимоаналептики современных генераций при учете наиболее значимых факторов, определяющих выбор тех или иных средств, и доказательности подтверждающих такой выбор данных. По возможности в тексте приводятся конкретные показатели ранга терапевтических рекомендаций (A, B, C, D) и значения уровня доказательности по рейтинговой системе SMOH (2007 г.) (табл. 1, 2).
В существующих практических рекомендациях [11, 13, 23] при выборе терапевтического подхода прежде всего предлагается ориентироваться на выраженность депрессии. В качестве терапии 1-й линии при депрессии средней степени тяжести и тяжелой или при неглубоких депрессиях, носящих затяжной характер (более 2 лет), обоснованным является использование антидепрессантов (ранг A, уровень 1+), предпочтительных психотерапии, самостоятельное применение которой рекомендовано лимитировать случаями легкой и умеренной депрессии. При легкой же депрессии использование препаратов предлагается ограничивать рекуррентным вариантом расстройства с умеренными и тяжелыми эпизодами в анамнезе, а также при коморбидности с соматической и другой психической патологией (ранг D, уровень 4).
Среди тимоаналептиков, дифференцируемых по химической структуре и механизмам действия, принято выделять препараты I поколения: трициклические (ТЦА) и тетрациклические (мапротилин), а также необратимые ингибиторы моноаминоксидазы (ИМАО). К современным антидепрессантам II и III поколения [1] относят селективные ингибиторы обратного захвата серотонина (СИОЗС), включая флуоксетин, флувоксамин, пароксетин, сертралин, циталопрам, эсциталопрам; селективные ингибиторы обратного захвата серотонина и норадреналина (СИОЗСН) – венлафаксин, дулоксетин, милнаципран; другие антидепрессанты с разной структурой и механизмами действия, включая миртазапин, агомелатин, бупропион и т.п. Хотя в некоторых исследованиях предполагаются преимущества эффективности одних механизмов действия антидепрессантов над другими, однако однозначных и непротиворечивых доказательств, которые позволили бы обосновать значимость таких различий, в клинических исследованиях в настоящее время не получено. Согласно данным, приводимым в официальных рекомендациях по лечению депрессий [11, 13, 23], для большинства пациентов эффективность антидепрессантов в основном сопоставима между классами препаратов и в их пределах (ранг A, уровень 1+) доли респондеров в клинических исследованиях варьируют от 50 до 75%. При этом по ряду данных эффективность по сравнению с плацебо выше при тяжелой депрессии, чем при легкой и средней степени тяжести [19, 24, 27].
По мнению ряда экспертов [2, 9], наилучшие результаты при тяжелых (включая психотические) депрессиях наблюдаются при использовании препаратов I поколения – ТЦА и мапротилин (ранг D, уровень 4). Однако подчеркивается, что лечение таких состояний необходимо проводить в специализированных психиатрических отделениях.
В свою очередь, считается, что антидепрессанты II и III поколения с моноаминергическим механизмом действия (СИОЗС, СИОЗСН и др.), а также ОИМАО-А уступают ТЦА по уровню терапевтического эффекта при тяжелых депрессиях, но оказываются сопоставимыми при умеренных депрессивных состояниях, а в случаях легких депрессий даже превосходят антидепрессанты I поколения, в первую очередь за счет более высокой переносимости, что позволяет широко применять их в амбулаторной практике [9].
При сравнении эффективности препаратов, относимых к антидепрессантам современных генераций, были выявлены минимальные преимущества одних средств над другими. Так, в обзоре метаанализов, подготовленном Agency for Healthcare Research and Quality – AHRQ [19], при сопоставлении разных СИОЗС установлено, что, например, у больных, получающих терапию сертралином, по сравнению с флуоксетином отмечается дополнительная статистически незначимая редукция среднего балла по шкале Гамильтона (HAM-D-17), равная 0,75 (95% доверительный интервал [ДИ] -0,45–1,95). Однако относительный риск (ОР) положительного ответа на терапию оказался статистически значимо выше при приеме сертралина, чем на лечении флуоксетином (ОР 1,11; 95% ДИ 1,01–1,21). При этом количество больных, которых нужно пролечить (number needed to treat – NNT) для получения дополнительного респондера на 6–12-й неделе, составило 14 (95% ДИ 8–22). Аналогичным образом зафиксирована тенденция к несколько более высокой эффективности эсциталопрама по сравнению с циталопрамом. При терапии эсциталопрамом достигался эффект в виде дополнительной редукции 1,25 балла (95% ДИ 0,10–2,39) по шкале депрессии Монтгомери–Асберга (MADRS). ОР положительного ответа на терапию при приеме эсциталопрама был статистически значимо выше, чем при приеме циталопрама (ОР 1,14; 95% ДИ 1,04–1,26). Количество больных, которых нужно пролечить (NNT) для получения дополнительного респондера на 8-й неделе при приеме эсциталопрама, также составило 14 (95% ДИ 7–11,1). Каких-либо статистически значимых различий по динамике симптомов или доле респондеров между парами сравнения «флуоксетин–пароксетин» и «пароксетин–сертралин» зафиксировано не было.
Аналогичные результаты о сравнительной эффективности современных антидепрессантов (в качестве основного препарата для сравнения выбран сертралин) были получены в результате метаанализа 59 РКИ [15]. Авторами показано, что по доле респондеров сертралин сопоставим с ТЦА как единой группой, статистически значимо уступая только амитриптилину (ОР 1,23; 95% ДИ 0,99–1,52, p=0,07; 7 исследований, 1345 пациентов). При сравнении с мапротиллином отличий сертралина по параметрам эффективности также не зафиксировано. Сертралин превзошел флуоксетин (ОР 0,73; 95% ДИ 0,59–0,92, p=0,007; 8 исследований, 1352 пациента), тогда как не было отмечено различий эффективности с остальными СИОЗС и другими современными антидепрессантами, включая бупропион, миртазапин, моклобемид, нефазодон, ребоксетин, тианептин, тразодон и венлафаксин. Таким образом, согласно большинству исследований по эффективности антидепрессанты в основном сопоставимы, а выявляемые преимущества одних препаратов над другими невелики, притом что клиническая значимость таких различий остается неопределенной [14]. Соответственно, в настоящее время при выборе антидепрессантов предлагается ориентироваться прежде всего на соотношение «риск–польза» и учитывать переносимость и безопасность (нежелательные явления, суицидальный риск), предпочтения пациента, стоимость препарата, данные о предыдущем лечении, коморбидную соматическую и психическую патологию, период полувыведения и потенциальные лекарственные взаимодействия, обусловленные способностью связываться с белками плазмы или метаболизироваться системой цитохрома P-450.
Исходя из приведенных принципов, в ряде публикаций [13, 23] предлагается серия приводимых ниже и обладающих разным уровнем доказательности рекомендаций, представляющих собой алгоритм, облегчающий принятие решений в отношении дифференцированного назначения антидепрессантов.
В качестве препаратов 1-й линии при лечении депрессии рассматриваются СИОЗС из-за наиболее благоприятного соотношения «риск–польза», хорошей переносимости и безопасности при передозировке (ранг A, уровень 1++). Благодаря указанным свойствам СИОЗС являются препаратами выбора при депрессии у больных с сопутствующей сердечно-сосудистой патологией (ранг A, уровень 1++). В случаях высокого риска лекарственных взаимодействий с другими медикаментами другим СИОЗС следует предпочесть сертралин или эсциталопрам благодаря их более низкому потенциалу к нежелательным интеракциям с соматотропными средствами, за счет чего обеспечивается большая безопасность и нивелируются возможные кардиальные нежелательные явления (ранг D, уровень 4). Так, поскольку сертралин обладает лишь слабым блокирующим действием в отношении изоферментов печени (цитохромы P-450IID-6, P-450IA2 и P-450IIIA4), участвующих в биотрансформации соматотропных препаратов, риск нежелательного лекарственного взаимодействия значительно снижается [10]. Из-за высокой частоты кардиотоксических побочных эффектов, напротив, следует избегать применения ТЦА у больных с высоким риском сердечно-сосудистой патологии, аритмиями и сердечной недостаточностью (ранг A, уровень 1++).
Препараты I поколения, включая ТЦА и ИМАО, должны оставаться в резерве (2-я линия) для ситуаций, когда лечение средствами 1-й линии оказалось неэффективным (ранг A, уровень 1+). При назначении антидепрессанта необходимо адаптировать препарат к пациенту с депрессией и хронической соматической патологией, учитывая следующие факторы: конкретный диагноз соматического заболевания; потенциальные побочные эффекты антидепрессантов, способные влиять на такое заболевание (например, СИОЗС могут провоцировать или усиливать гипонатриемию, особенно у пожилых больных) (ранг D, уровень 3).
Переход с одного антидепрессанта на другой (как в пределах группы СИОЗС, так и на препараты другого класса, и наоборот) является адекватной стратегией (ранг A, уровень 1++). При этом, несмотря на то что закономерным кажется предпочтительность назначения препарата другого класса, в целом ряде РКИ и метаанализов [33, 34] показано, что частота положительных исходов не отличается при смене фармакотерапии в пределах класса (например, одного СИОЗС на другой) от замены на тимоаналептик с другим механизмом действия (например, СИОЗС на не-СИОЗС). Так, в исследовании STAR*D не удалось зафиксировать отличий ни по частоте респондеров, ни по частоте ремиттеров, когда циталопрам меняли на сертралин или другой антидепрессант (бупропион-SR или венлафаксин-XR) [35]. Если есть данные относительно того, что больной ранее успешно лечился каким-либо антидепрессантом и хорошо его переносил, такой препарат является предпочтительным. Напротив, если пациент прежде не ответил на адекватную терапию тем или иным препаратом или не перенес его в связи с побочными эффектами, такого средства следует избегать (ранг D, уровень 4).
Выбрав определенный антидепрессант, следует начинать лечение с низкой дозы и постепенно титровать ее до терапевтической, одновременно оценивая динамику психического статуса и фиксируя побочные эффекты. Частота мониторинга зависит от тяжести депрессии, степени суицидального риска, комплаентности больного и доступности социальной поддержки (ранг A, уровень 1+). При отмене антидепрессантов дозы препаратов необходимо снижать постепенно, а не отменять резко, чтобы минимизировать риск возможных проявлений отмены (ранг A, уровень 1++).
Терапия любым антидепрессантом должна продолжаться не менее 4–6 нед (ранг C, уровень 2+).
Использование высоких доз антидепрессантов может быть обоснованным у пациентов, давших частичный ответ на терапию, и если применялись только низкие и средние дозы. При повышении дозы необходим пристальный мониторинг побочных эффектов (ранг B, уровень 2++).
По данным метаанализов [12, 20], современные антидепрессанты обнаруживают некоторые различия по предпочтительности тех или иных побочных эффектов, что необходимо учитывать при индивидуальных назначениях, особенно если имеются сведения о нежелательных явлениях, развивавшихся в процессе тимоаналептической терапии ранее. Например, среди СИОЗС флуоксетин считается лидером по частоте гастроинтестинальных расстройств (тошнота, рвота, диарея), флувоксамин – по частоте тошноты, пароксетин – по потливости и седации, сертралин – по диареи. При этом частота тошноты и рвоты при приеме СИОЗСН (дулоксетина и венлафаксина) выше, чем у СИОЗС. При приеме миртазапина и пароксетина отмечается более выраженная прибавка массы тела, а у миртазапина и тразодона – более высокая степень седации.
Если в структуре депрессии имеются тревога, ажитация и/или бессонница, в начале лечения может возникнуть необходимость в кратковременном (2–4 нед) назначении сопутствующей тимоаналептикам терапии бензодиазепиновыми транквилизаторами (ранг A, уровень 1++). Особенно внимательно следует следить за суицидальными мыслями и поведением на начальном этапе лечения антидепрессантами (обычно первые 1–2 мес), особенно у детей, подростков и пациентов юношеского возраста между 18 и 24 годами (ранг C, уровень 2+).
Дифференцированное применение антидепрессантов
в зависимости от психопатологических особенностей депрессивного синдрома во многих случаях до сих пор опирается на тезис P.Kielholz (1965 г.) [26] об использовании тимоаналептиков с седативными и анксиолитическими свойствами при тревожных депрессиях, а со стимулирующим (активирующим) действием – при заторможенных (апато-анергических) формах [3]. Однако значение этого положения в настоящее время несколько менее актуально, нежели ранее. Данному принципу, например, затруднительно следовать при депрессиях смешанной психопатологической структуры (тревожно-апатических), когда доминирующий аффективный радикал выделить трудно или он претерпевает изменения во времени. Соответственно, в целом ряде случаев препаратами выбора становятся современные тимоаналептики со сбалансированным механизмом действия (СИОЗС – сертралин, пароксетин, СИОЗСН – венлафаксин и т.д.). В стремлении преодолеть существующие противоречия последние годы предлагаются альтернативные модели дифференцированной терапии депрессий, опирающиеся на иные психопатологические дименсии, отличные от предложенных P.Kielholz. Так, в ряде публикаций А.Б.Смулевича (1997, 2003, 2005, 2011 гг.) [4–8] показано, что выбор антидепрессантов может зависеть от соотношения двух сфер клинических проявлений депрессии – собственно гипотимии (позитивная аффективность: голотимный с патологическим циркадианным ритмом, кататимный и катестетический аффекты) и отчуждения (негативная аффективность: аутопсихическая деперсонализация, психическая анестезия, ангедония). В случаях депрессивных состояний (эндогенные и эндогеноморфные депрессии), протекающих с преобладанием позитивной аффективности (тоска с чувством душевной боли, сниженная самооценка, идеи малоценности и/или вины, подверженные циркадианным колебаниям), автор указывает на эффективность всех антидепрессантов как традиционных, так и новых поколений. При депрессиях же с преобладанием негативной аффективности и явлениями психического отчуждения (анестетическая депрессия и др.), т.е. более резистентных к фармакологическому воздействию психопатологических расстройств, предполагается проявление избирательной чувствительности к препаратам разной химической структуры и механизмов действия. При формировании негативной аффективности, выражающейся признаками девитализации аффекта (сознание утраты жизненного тонуса и спонтанной активности) и явлениями моральной ипохондрии (чувство изменения эмоциональной сопричастности к внешним объектам, «существования за преградой», сознание падения психической активности, обедненности воображения), наиболее полный терапевтический эффект достигается при использовании препаратов серотонинергической группы – СИОЗС. При депрессиях с заимствованными у коморбидных соматических заболеваний ритмами (нозогенные, соматогенные), психопатологические проявления которых ограничены рамками гипотимии и невротическим регистром расстройств (невротическая, истерическая, соматизированная, астеническая депрессия), клиническое действие антидепрессантов реализуется по другим закономерностям. Приоритетными при выборе препарата становятся минимальная выраженность поведенческой токсичности и спектр побочных действий препарата. Особое значение в этом случае приобретают индивидуальная чувствительность и исходное отношение больного к антидепрессанту и психофармакотерапии в целом. В качестве препаратов выбора выступают антидепрессанты различной структуры, сочетающие мягкий тимоаналептический эффект с хорошей переносимостью (препараты класса СИОЗС, пирлиндол, тианептин и др.).
При депрессиях же с преобладанием негативной аффективности и явлениями психического отчуждения (анестетическая депрессия и др.), т.е. более резистентных к фармакологическому воздействию психопатологических расстройств, предполагается проявление избирательной чувствительности к препаратам разной химической структуры и механизмов действия. При формировании негативной аффективности, выражающейся признаками девитализации аффекта (сознание утраты жизненного тонуса и спонтанной активности) и явлениями моральной ипохондрии (чувство изменения эмоциональной сопричастности к внешним объектам, «существования за преградой», сознание падения психической активности, обедненности воображения), наиболее полный терапевтический эффект достигается при использовании препаратов серотонинергической группы – СИОЗС. При депрессиях с заимствованными у коморбидных соматических заболеваний ритмами (нозогенные, соматогенные), психопатологические проявления которых ограничены рамками гипотимии и невротическим регистром расстройств (невротическая, истерическая, соматизированная, астеническая депрессия), клиническое действие антидепрессантов реализуется по другим закономерностям. Приоритетными при выборе препарата становятся минимальная выраженность поведенческой токсичности и спектр побочных действий препарата. Особое значение в этом случае приобретают индивидуальная чувствительность и исходное отношение больного к антидепрессанту и психофармакотерапии в целом. В качестве препаратов выбора выступают антидепрессанты различной структуры, сочетающие мягкий тимоаналептический эффект с хорошей переносимостью (препараты класса СИОЗС, пирлиндол, тианептин и др.).
Приходится констатировать, что в официальных рекомендациях, подготовленных рядом национальных психиатрических ассоциаций [11, 13, 23], выбор антидепрессантов в зависимости от психопатологической структуры депрессии практически не обсуждается. Утверждается, что подбор тимоаналептика в соответствии с типологической принадлежностью депрессии имеет лишь «историческое значение». По мнению авторов, практически нет оснований считать, что существуют различия в исходах при применении препаратов 1-й линии в отношении, например, меланхолической или атипичной депрессии. Напротив, при некоторых вариантах депрессии (с психотическими симптомами, сезонная, послеродовая и т.п.) такие различия обнаруживаются. Так, приводятся убедительные (уровень 1) доказательства того, что при большой депрессии с психотическими симптомами показано комбинированное назначение антидепрессантов с антипсихотиками [16], хотя, согласно Кохрейновскому систематическому обзору, такое сочетанное лечение эффективнее монотерапии антипсихотиком, но не антидепрессантом [38]. В отношении большой депрессии с сезонным паттерном существуют доказательства 1-го уровня, что для профилактики зимних обострений наиболее эффективен бупропион [30].
В ряде публикаций последнего десятилетия наряду с перечисленными факторами, определяющими выбор антидепрессантов, обсуждается еще ряд параметров (возраст, пол, генетические особенности), способных, по мнению исследователей, влиять на эффективность дифференцированной терапии депрессий.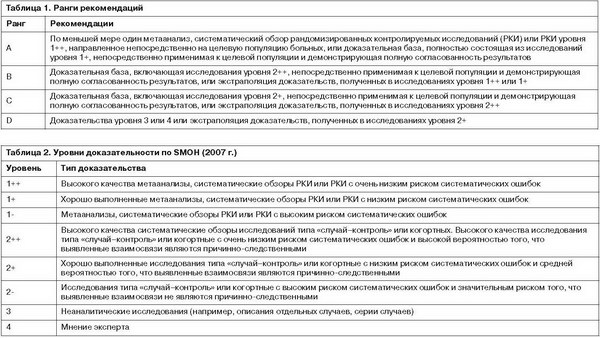 Однако результаты таких работ чаще всего противоречивы. Получены сведения, что пациенты молодого возраста лучше отвечают на терапию серотонинергическими средствами, нежели норадренергическими тимоаналептиками, тогда как больные пожилого возраста никакой предпочтительности не обнаруживают [31].
Однако результаты таких работ чаще всего противоречивы. Получены сведения, что пациенты молодого возраста лучше отвечают на терапию серотонинергическими средствами, нежели норадренергическими тимоаналептиками, тогда как больные пожилого возраста никакой предпочтительности не обнаруживают [31].
В заключение необходимо отметить, что несмотря на обширную доказательную базу, лежащую в основе подходов к дифференцированному назначению современных антидепрессантов, сохраняется необходимость в проведении и обобщении результатов крупных исследований, направленных на поиск предикторов, определяющих оптимальные результаты тимоаналептической терапии. Возможно, выявление ассоциации ряда до сих пор неизвестных биологических и биосоциальных параметров с психопатологическими особенностями депрессивных нарушений, а также дальнейшее расширение арсенала тимоаналептиков за счет препаратов современных генераций, обладающих оптимальным соотношением эффективности и безопасности, станут интегративной предпосылкой к дальнейшему развитию методов дифференцированной терапии депрессий, приближающейся к максимально индивидуализированному лечению.
Сведения об авторе
Д.В.Романов – канд. мед. наук, ассистент каф. психиатрии и психосоматики ФППОВ ГОУ ВПО Первый МГМУ
им. И.М.Сеченова. E-mail: newt777@mail.ru
Ключевые слова: депрессия, алгоритмы лечения, современные антидепрессанты.
Algorithms of differential therapy of depression with modern antidepressants
D.V.Romanov
The First Moscow State Medical University I.M.Sechenov, Department of Psychiatry and Psychosomatics
Summary. The review article is devoted to up-to-date approaches to depression therapy with the use of modern antidepressants.
The attention is focused on a grade of treatment recommendations and a level of evidence based on significant clinical characteristics of depression meaningful for choice of antidepressants.
Key words: depression, algorithms of therapy, modern antidepressants.
Учитывая клиническую гетерогенность депрессивных расстройств по целому ряду параметров, включая степень тяжести, синдромальную структуру, нозологическую принадлежность и т.п., а также наблюдающееся в настоящее время значительное разнообразие терапевтических модальностей, направленных на коррекцию аффективных нарушений, сохраняет свою актуальность проблема дифференцированного подхода к лечению депрессий. Настоящая публикация ограничивается обсуждением принципов фармакотерапии депрессий с акцентом на тимоаналептики современных генераций при учете наиболее значимых факторов, определяющих выбор тех или иных средств, и доказательности подтверждающих такой выбор данных. По возможности в тексте приводятся конкретные показатели ранга терапевтических рекомендаций (A, B, C, D) и значения уровня доказательности по рейтинговой системе SMOH (2007 г.) (табл. 1, 2).
В существующих практических рекомендациях [11, 13, 23] при выборе терапевтического подхода прежде всего предлагается ориентироваться на выраженность депрессии. В качестве терапии 1-й линии при депрессии средней степени тяжести и тяжелой или при неглубоких депрессиях, носящих затяжной характер (более 2 лет), обоснованным является использование антидепрессантов (ранг A, уровень 1+), предпочтительных психотерапии, самостоятельное применение которой рекомендовано лимитировать случаями легкой и умеренной депрессии. При легкой же депрессии использование препаратов предлагается ограничивать рекуррентным вариантом расстройства с умеренными и тяжелыми эпизодами в анамнезе, а также при коморбидности с соматической и другой психической патологией (ранг D, уровень 4).
Среди тимоаналептиков, дифференцируемых по химической структуре и механизмам действия, принято выделять препараты I поколения: трициклические (ТЦА) и тетрациклические (мапротилин), а также необратимые ингибиторы моноаминоксидазы (ИМАО). К современным антидепрессантам II и III поколения [1] относят селективные ингибиторы обратного захвата серотонина (СИОЗС), включая флуоксетин, флувоксамин, пароксетин, сертралин, циталопрам, эсциталопрам; селективные ингибиторы обратного захвата серотонина и норадреналина (СИОЗСН) – венлафаксин, дулоксетин, милнаципран; другие антидепрессанты с разной структурой и механизмами действия, включая миртазапин, агомелатин, бупропион и т.п. Хотя в некоторых исследованиях предполагаются преимущества эффективности одних механизмов действия антидепрессантов над другими, однако однозначных и непротиворечивых доказательств, которые позволили бы обосновать значимость таких различий, в клинических исследованиях в настоящее время не получено. Согласно данным, приводимым в официальных рекомендациях по лечению депрессий [11, 13, 23], для большинства пациентов эффективность антидепрессантов в основном сопоставима между классами препаратов и в их пределах (ранг A, уровень 1+) доли респондеров в клинических исследованиях варьируют от 50 до 75%. При этом по ряду данных эффективность по сравнению с плацебо выше при тяжелой депрессии, чем при легкой и средней степени тяжести [19, 24, 27].
По мнению ряда экспертов [2, 9], наилучшие результаты при тяжелых (включая психотические) депрессиях наблюдаются при использовании препаратов I поколения – ТЦА и мапротилин (ранг D, уровень 4). Однако подчеркивается, что лечение таких состояний необходимо проводить в специализированных психиатрических отделениях.
В свою очередь, считается, что антидепрессанты II и III поколения с моноаминергическим механизмом действия (СИОЗС, СИОЗСН и др.), а также ОИМАО-А уступают ТЦА по уровню терапевтического эффекта при тяжелых депрессиях, но оказываются сопоставимыми при умеренных депрессивных состояниях, а в случаях легких депрессий даже превосходят антидепрессанты I поколения, в первую очередь за счет более высокой переносимости, что позволяет широко применять их в амбулаторной практике [9].
При сравнении эффективности препаратов, относимых к антидепрессантам современных генераций, были выявлены минимальные преимущества одних средств над другими. Так, в обзоре метаанализов, подготовленном Agency for Healthcare Research and Quality – AHRQ [19], при сопоставлении разных СИОЗС установлено, что, например, у больных, получающих терапию сертралином, по сравнению с флуоксетином отмечается дополнительная статистически незначимая редукция среднего балла по шкале Гамильтона (HAM-D-17), равная 0,75 (95% доверительный интервал [ДИ] -0,45–1,95). Однако относительный риск (ОР) положительного ответа на терапию оказался статистически значимо выше при приеме сертралина, чем на лечении флуоксетином (ОР 1,11; 95% ДИ 1,01–1,21). При этом количество больных, которых нужно пролечить (number needed to treat – NNT) для получения дополнительного респондера на 6–12-й неделе, составило 14 (95% ДИ 8–22). Аналогичным образом зафиксирована тенденция к несколько более высокой эффективности эсциталопрама по сравнению с циталопрамом. При терапии эсциталопрамом достигался эффект в виде дополнительной редукции 1,25 балла (95% ДИ 0,10–2,39) по шкале депрессии Монтгомери–Асберга (MADRS). ОР положительного ответа на терапию при приеме эсциталопрама был статистически значимо выше, чем при приеме циталопрама (ОР 1,14; 95% ДИ 1,04–1,26). Количество больных, которых нужно пролечить (NNT) для получения дополнительного респондера на 8-й неделе при приеме эсциталопрама, также составило 14 (95% ДИ 7–11,1). Каких-либо статистически значимых различий по динамике симптомов или доле респондеров между парами сравнения «флуоксетин–пароксетин» и «пароксетин–сертралин» зафиксировано не было.
Аналогичные результаты о сравнительной эффективности современных антидепрессантов (в качестве основного препарата для сравнения выбран сертралин) были получены в результате метаанализа 59 РКИ [15]. Авторами показано, что по доле респондеров сертралин сопоставим с ТЦА как единой группой, статистически значимо уступая только амитриптилину (ОР 1,23; 95% ДИ 0,99–1,52, p=0,07; 7 исследований, 1345 пациентов). При сравнении с мапротиллином отличий сертралина по параметрам эффективности также не зафиксировано. Сертралин превзошел флуоксетин (ОР 0,73; 95% ДИ 0,59–0,92, p=0,007; 8 исследований, 1352 пациента), тогда как не было отмечено различий эффективности с остальными СИОЗС и другими современными антидепрессантами, включая бупропион, миртазапин, моклобемид, нефазодон, ребоксетин, тианептин, тразодон и венлафаксин. Таким образом, согласно большинству исследований по эффективности антидепрессанты в основном сопоставимы, а выявляемые преимущества одних препаратов над другими невелики, притом что клиническая значимость таких различий остается неопределенной [14]. Соответственно, в настоящее время при выборе антидепрессантов предлагается ориентироваться прежде всего на соотношение «риск–польза» и учитывать переносимость и безопасность (нежелательные явления, суицидальный риск), предпочтения пациента, стоимость препарата, данные о предыдущем лечении, коморбидную соматическую и психическую патологию, период полувыведения и потенциальные лекарственные взаимодействия, обусловленные способностью связываться с белками плазмы или метаболизироваться системой цитохрома P-450.
Исходя из приведенных принципов, в ряде публикаций [13, 23] предлагается серия приводимых ниже и обладающих разным уровнем доказательности рекомендаций, представляющих собой алгоритм, облегчающий принятие решений в отношении дифференцированного назначения антидепрессантов.
В качестве препаратов 1-й линии при лечении депрессии рассматриваются СИОЗС из-за наиболее благоприятного соотношения «риск–польза», хорошей переносимости и безопасности при передозировке (ранг A, уровень 1++). Благодаря указанным свойствам СИОЗС являются препаратами выбора при депрессии у больных с сопутствующей сердечно-сосудистой патологией (ранг A, уровень 1++). В случаях высокого риска лекарственных взаимодействий с другими медикаментами другим СИОЗС следует предпочесть сертралин или эсциталопрам благодаря их более низкому потенциалу к нежелательным интеракциям с соматотропными средствами, за счет чего обеспечивается большая безопасность и нивелируются возможные кардиальные нежелательные явления (ранг D, уровень 4). Так, поскольку сертралин обладает лишь слабым блокирующим действием в отношении изоферментов печени (цитохромы P-450IID-6, P-450IA2 и P-450IIIA4), участвующих в биотрансформации соматотропных препаратов, риск нежелательного лекарственного взаимодействия значительно снижается [10]. Из-за высокой частоты кардиотоксических побочных эффектов, напротив, следует избегать применения ТЦА у больных с высоким риском сердечно-сосудистой патологии, аритмиями и сердечной недостаточностью (ранг A, уровень 1++).
Препараты I поколения, включая ТЦА и ИМАО, должны оставаться в резерве (2-я линия) для ситуаций, когда лечение средствами 1-й линии оказалось неэффективным (ранг A, уровень 1+). При назначении антидепрессанта необходимо адаптировать препарат к пациенту с депрессией и хронической соматической патологией, учитывая следующие факторы: конкретный диагноз соматического заболевания; потенциальные побочные эффекты антидепрессантов, способные влиять на такое заболевание (например, СИОЗС могут провоцировать или усиливать гипонатриемию, особенно у пожилых больных) (ранг D, уровень 3).
Переход с одного антидепрессанта на другой (как в пределах группы СИОЗС, так и на препараты другого класса, и наоборот) является адекватной стратегией (ранг A, уровень 1++). При этом, несмотря на то что закономерным кажется предпочтительность назначения препарата другого класса, в целом ряде РКИ и метаанализов [33, 34] показано, что частота положительных исходов не отличается при смене фармакотерапии в пределах класса (например, одного СИОЗС на другой) от замены на тимоаналептик с другим механизмом действия (например, СИОЗС на не-СИОЗС). Так, в исследовании STAR*D не удалось зафиксировать отличий ни по частоте респондеров, ни по частоте ремиттеров, когда циталопрам меняли на сертралин или другой антидепрессант (бупропион-SR или венлафаксин-XR) [35]. Если есть данные относительно того, что больной ранее успешно лечился каким-либо антидепрессантом и хорошо его переносил, такой препарат является предпочтительным. Напротив, если пациент прежде не ответил на адекватную терапию тем или иным препаратом или не перенес его в связи с побочными эффектами, такого средства следует избегать (ранг D, уровень 4).
Выбрав определенный антидепрессант, следует начинать лечение с низкой дозы и постепенно титровать ее до терапевтической, одновременно оценивая динамику психического статуса и фиксируя побочные эффекты. Частота мониторинга зависит от тяжести депрессии, степени суицидального риска, комплаентности больного и доступности социальной поддержки (ранг A, уровень 1+). При отмене антидепрессантов дозы препаратов необходимо снижать постепенно, а не отменять резко, чтобы минимизировать риск возможных проявлений отмены (ранг A, уровень 1++).
Терапия любым антидепрессантом должна продолжаться не менее 4–6 нед (ранг C, уровень 2+).
Использование высоких доз антидепрессантов может быть обоснованным у пациентов, давших частичный ответ на терапию, и если применялись только низкие и средние дозы. При повышении дозы необходим пристальный мониторинг побочных эффектов (ранг B, уровень 2++).
По данным метаанализов [12, 20], современные антидепрессанты обнаруживают некоторые различия по предпочтительности тех или иных побочных эффектов, что необходимо учитывать при индивидуальных назначениях, особенно если имеются сведения о нежелательных явлениях, развивавшихся в процессе тимоаналептической терапии ранее. Например, среди СИОЗС флуоксетин считается лидером по частоте гастроинтестинальных расстройств (тошнота, рвота, диарея), флувоксамин – по частоте тошноты, пароксетин – по потливости и седации, сертралин – по диареи. При этом частота тошноты и рвоты при приеме СИОЗСН (дулоксетина и венлафаксина) выше, чем у СИОЗС. При приеме миртазапина и пароксетина отмечается более выраженная прибавка массы тела, а у миртазапина и тразодона – более высокая степень седации.
Если в структуре депрессии имеются тревога, ажитация и/или бессонница, в начале лечения может возникнуть необходимость в кратковременном (2–4 нед) назначении сопутствующей тимоаналептикам терапии бензодиазепиновыми транквилизаторами (ранг A, уровень 1++). Особенно внимательно следует следить за суицидальными мыслями и поведением на начальном этапе лечения антидепрессантами (обычно первые 1–2 мес), особенно у детей, подростков и пациентов юношеского возраста между 18 и 24 годами (ранг C, уровень 2+).
Дифференцированное применение антидепрессантов
в зависимости от психопатологических особенностей депрессивного синдрома во многих случаях до сих пор опирается на тезис P.Kielholz (1965 г.) [26] об использовании тимоаналептиков с седативными и анксиолитическими свойствами при тревожных депрессиях, а со стимулирующим (активирующим) действием – при заторможенных (апато-анергических) формах [3]. Однако значение этого положения в настоящее время несколько менее актуально, нежели ранее. Данному принципу, например, затруднительно следовать при депрессиях смешанной психопатологической структуры (тревожно-апатических), когда доминирующий аффективный радикал выделить трудно или он претерпевает изменения во времени. Соответственно, в целом ряде случаев препаратами выбора становятся современные тимоаналептики со сбалансированным механизмом действия (СИОЗС – сертралин, пароксетин, СИОЗСН – венлафаксин и т.д.). В стремлении преодолеть существующие противоречия последние годы предлагаются альтернативные модели дифференцированной терапии депрессий, опирающиеся на иные психопатологические дименсии, отличные от предложенных P.Kielholz. Так, в ряде публикаций А.Б.Смулевича (1997, 2003, 2005, 2011 гг.) [4–8] показано, что выбор антидепрессантов может зависеть от соотношения двух сфер клинических проявлений депрессии – собственно гипотимии (позитивная аффективность: голотимный с патологическим циркадианным ритмом, кататимный и катестетический аффекты) и отчуждения (негативная аффективность: аутопсихическая деперсонализация, психическая анестезия, ангедония). В случаях депрессивных состояний (эндогенные и эндогеноморфные депрессии), протекающих с преобладанием позитивной аффективности (тоска с чувством душевной боли, сниженная самооценка, идеи малоценности и/или вины, подверженные циркадианным колебаниям), автор указывает на эффективность всех антидепрессантов как традиционных, так и новых поколений.
 При депрессиях же с преобладанием негативной аффективности и явлениями психического отчуждения (анестетическая депрессия и др.), т.е. более резистентных к фармакологическому воздействию психопатологических расстройств, предполагается проявление избирательной чувствительности к препаратам разной химической структуры и механизмов действия. При формировании негативной аффективности, выражающейся признаками девитализации аффекта (сознание утраты жизненного тонуса и спонтанной активности) и явлениями моральной ипохондрии (чувство изменения эмоциональной сопричастности к внешним объектам, «существования за преградой», сознание падения психической активности, обедненности воображения), наиболее полный терапевтический эффект достигается при использовании препаратов серотонинергической группы – СИОЗС. При депрессиях с заимствованными у коморбидных соматических заболеваний ритмами (нозогенные, соматогенные), психопатологические проявления которых ограничены рамками гипотимии и невротическим регистром расстройств (невротическая, истерическая, соматизированная, астеническая депрессия), клиническое действие антидепрессантов реализуется по другим закономерностям. Приоритетными при выборе препарата становятся минимальная выраженность поведенческой токсичности и спектр побочных действий препарата. Особое значение в этом случае приобретают индивидуальная чувствительность и исходное отношение больного к антидепрессанту и психофармакотерапии в целом. В качестве препаратов выбора выступают антидепрессанты различной структуры, сочетающие мягкий тимоаналептический эффект с хорошей переносимостью (препараты класса СИОЗС, пирлиндол, тианептин и др.).
При депрессиях же с преобладанием негативной аффективности и явлениями психического отчуждения (анестетическая депрессия и др.), т.е. более резистентных к фармакологическому воздействию психопатологических расстройств, предполагается проявление избирательной чувствительности к препаратам разной химической структуры и механизмов действия. При формировании негативной аффективности, выражающейся признаками девитализации аффекта (сознание утраты жизненного тонуса и спонтанной активности) и явлениями моральной ипохондрии (чувство изменения эмоциональной сопричастности к внешним объектам, «существования за преградой», сознание падения психической активности, обедненности воображения), наиболее полный терапевтический эффект достигается при использовании препаратов серотонинергической группы – СИОЗС. При депрессиях с заимствованными у коморбидных соматических заболеваний ритмами (нозогенные, соматогенные), психопатологические проявления которых ограничены рамками гипотимии и невротическим регистром расстройств (невротическая, истерическая, соматизированная, астеническая депрессия), клиническое действие антидепрессантов реализуется по другим закономерностям. Приоритетными при выборе препарата становятся минимальная выраженность поведенческой токсичности и спектр побочных действий препарата. Особое значение в этом случае приобретают индивидуальная чувствительность и исходное отношение больного к антидепрессанту и психофармакотерапии в целом. В качестве препаратов выбора выступают антидепрессанты различной структуры, сочетающие мягкий тимоаналептический эффект с хорошей переносимостью (препараты класса СИОЗС, пирлиндол, тианептин и др.).
Приходится констатировать, что в официальных рекомендациях, подготовленных рядом национальных психиатрических ассоциаций [11, 13, 23], выбор антидепрессантов в зависимости от психопатологической структуры депрессии практически не обсуждается. Утверждается, что подбор тимоаналептика в соответствии с типологической принадлежностью депрессии имеет лишь «историческое значение». По мнению авторов, практически нет оснований считать, что существуют различия в исходах при применении препаратов 1-й линии в отношении, например, меланхолической или атипичной депрессии. Напротив, при некоторых вариантах депрессии (с психотическими симптомами, сезонная, послеродовая и т.п.) такие различия обнаруживаются. Так, приводятся убедительные (уровень 1) доказательства того, что при большой депрессии с психотическими симптомами показано комбинированное назначение антидепрессантов с антипсихотиками [16], хотя, согласно Кохрейновскому систематическому обзору, такое сочетанное лечение эффективнее монотерапии антипсихотиком, но не антидепрессантом [38]. В отношении большой депрессии с сезонным паттерном существуют доказательства 1-го уровня, что для профилактики зимних обострений наиболее эффективен бупропион [30].
В ряде публикаций последнего десятилетия наряду с перечисленными факторами, определяющими выбор антидепрессантов, обсуждается еще ряд параметров (возраст, пол, генетические особенности), способных, по мнению исследователей, влиять на эффективность дифференцированной терапии депрессий.
 Однако результаты таких работ чаще всего противоречивы. Получены сведения, что пациенты молодого возраста лучше отвечают на терапию серотонинергическими средствами, нежели норадренергическими тимоаналептиками, тогда как больные пожилого возраста никакой предпочтительности не обнаруживают [31].
Однако результаты таких работ чаще всего противоречивы. Получены сведения, что пациенты молодого возраста лучше отвечают на терапию серотонинергическими средствами, нежели норадренергическими тимоаналептиками, тогда как больные пожилого возраста никакой предпочтительности не обнаруживают [31].В заключение необходимо отметить, что несмотря на обширную доказательную базу, лежащую в основе подходов к дифференцированному назначению современных антидепрессантов, сохраняется необходимость в проведении и обобщении результатов крупных исследований, направленных на поиск предикторов, определяющих оптимальные результаты тимоаналептической терапии. Возможно, выявление ассоциации ряда до сих пор неизвестных биологических и биосоциальных параметров с психопатологическими особенностями депрессивных нарушений, а также дальнейшее расширение арсенала тимоаналептиков за счет препаратов современных генераций, обладающих оптимальным соотношением эффективности и безопасности, станут интегративной предпосылкой к дальнейшему развитию методов дифференцированной терапии депрессий, приближающейся к максимально индивидуализированному лечению.
Сведения об авторе
Д.В.Романов – канд. мед. наук, ассистент каф. психиатрии и психосоматики ФППОВ ГОУ ВПО Первый МГМУ
им. И.М.Сеченова. E-mail: newt777@mail.ru
Список исп. литературыСкрыть список1. Аведисова А.С. Современная классификация антидепрессантов: возможности повышения эффективности и безопасности. Психиатр. и психофармакотер. 2000; 2.
2. Краснов В.Н. Современные подходы к терапии депрессий. Рус. мед. журн. 2002; (12–13): 553.
3. Мосолов С.Н. Клиническое применение современных антидепрессантов. СПб., 1995.
4. Смулевич А.Б. Депрессия и коморбидные расстройства. М., 1997.
5. Смулевич А.Б. Депрессия в общей медицине. М., 2001.
6. Смулевич А.Б. Клинико-фармакологические эффекты антидепрессантов. Психиатр. и психофармакотер. (Прил.). 2003; 1: 3–6.
7. Смулевич А.Б. Депрессии при соматических и психических заболеваниях. М., 2003.
8. Смулевич А.Б. Психокардиология. М., 2005.
9. Смулевич А.Б. Психические расстройства в клинической практике. М., 2011.
10. Яковлева О.Б. Вопросы эффективности и безопасности антидепрессантов при лечении депрессий позднего возраста. Клин. психофармакология. 1998; 1 (4).
11. American Psychiatric Association – APA. Practice guideline for the treatment of patients with major depressive disorder. 3rd ed. Arlington (VA). Am Psychiat Assoc 2010.
12. Brambilla P, Cipriani A, Hotopf M, Barbui C. Side-effect profile of fluoxetine in comparison with other SSRIs, tricyclic and newer antidepressants: a meta-analysis of clinical trial data. Pharmacopsychiat 2005; 38 (2): 69–77.
13. Chua HC, Chan LL, Chee KS et al. Ministry of health clinical practice guidelines: depression. Singapore Med J 2012; 53 (2): 137–43.
14. Cipriani A, Brambilla P, Furukawa TA et al. Fluoxetine versus other types of pharmacotherapy for depression. Cochrane Database of Systematic Rev 2005; 4. CD004185. DOI: 10.1002/14651858.CD004185.pub2
15. Cipriani A, La Ferla T, Furukawa TA et al. Sertraline vs other antidepressive agents for depression. Cochrane Database Syst Rev 2010; 14 (4): CD006117.
16. Dannon PN, Lowengrub K, Gonopolski Y, Kotler M. Current and emerging somatic treatment strategies in psychotic major depression. Expert Rev 2006; 6: 73–80.
17. Eberhard-Gran M, Eskild A, Opjordsmoen S. Use of psychotropic medications in treating mood disorders during lactation: practical recommendations. CNS Drugs 2006; 20: 187–98.
18. Entsuah AR, Huang H, Thase ME. Response and remission rates in different subpopulations with major depressive disorder administered venlafaxine, selective serotonin reuptake inhibitors, or placebo. J Clin Psychiat 2001; 62: 869–77.
19. Fournier JC, DeRubeis RJ, Hollon SD et al. Antidepressant drug effects and depression severity: a patientlevel meta-analysis. JAMA 2010; 303: 47–53.
20. Gartlehner G, Hansen RA, Morgan LC et al. Second-generation antidepressants in the pharmacologic treatment of adult depression: an update of the 2007 comparative effectiveness review. Rockville (MD). Agency for Healthcare Research and Quality (US) 2011; 12-EHC012-EF.
21. Grigoriadis S, Konarski JZ, Kennedy SH et al. Sex differences in antidepressant response in a Canadian primary care sample. J Clin Psychopharmacol 2007; 27: 95–8.
22. Kato M, Fukuda T, Serretti A et al. ABCB1 (MDR1) gene polymorphisms are associated with the clinical response to paroxetine in patientswithmajor depressive disorder. Prog Neuropsychopharmacol Biol Psychiat 2008; 32: 398–404.
23. Kennedy SH, Lam RW, Parikh SV et al. Canadian network for mood and anxiety treatments (CANMAT) clinical guidelines for the management of major depressive disorder in adults. Introduction. J Affect Dis 2009; 117 (Suppl. 1): s1–2.
24. Khan A, Leventhal RM, Khan SR, Brown WA. Severity of depression and response to antidepressants and placebo: an analysis of the Food and Drug Administration database. J Clin Psychopharmacol 2002; 22: 40–5.
25. Khan A, Brodhead AE, Schwartz KA et al. Sex differences in antidepressant response in recent antidepressant clinical trials. J Clin Psychopharmacol 2005; 25: 318–24.
26. Kielholz P. Psychiatrische Pharmakotherapie in Klinik und Praxis. Bern, Stuttgart 1965.
27. Kirsch I, Deacon BJ, Huedo-Medina TB et al. Initial severity and antidepressant benefits: a meta-analysis of data submitted to the Food and Drug Administration. PLoS Med 2008; 5: e45.
28. Kornstein SG, Wohlreich MM, Mallinckrodt CH et al. Duloxetine efficacy for major depressive disorder in male vs female patients: data from 7 randomized, double-blind, placebo-controlled trials. J Clin Psychiat 2006; 67: 761–70.
29. McMahon FJ, Buervenich S, Charney D et al. Variation in the gene encoding the serotonin 2A-receptor is associated with outcome of antidepressant treatment. Am J Hum Genet 2006; 78: 804–14.
30. Modell JG, Rosenthal NE, Harriett AE et al. Seasonal affective disorder and its prevention by anticipatory treatment with bupropion XL. Biol Psychiat 2005; 58: 658–67.
31. Mulder RT, Watkins WG, Joyce PR, Luty SE. Age may affect response to antidepressants with serotonergic and noradrenergic actions. J Affect Dis 2003; 76: 143–9.
32. Papakostas GI, Kornstein SG, Clayton AH et al. Relative antidepressant efficacy of bupropion and the selective serotonin reuptake inhibitors in major depressive disorder: gender-age interactions. Int Clin Psychopharmacol 2007; 22: 226–9.
33. Papakostas GI, Fava M, Thase ME. Treatment of SSRI-resistant depression: a meta-analysis comparing within vs across-class switches. Biol Psychiat 2008; 63 (7): 699–704.
34. Ruhé HG, Huyser J, Swinkels JA, Schene AH. Switching antidepressants after a 1st selective serotonin reuptake inhibitor in major depressive disorder: a systematic review. J Clin Psychiat 2006; 67 (12): 1836–55.
35. Rush AJ, Trivedi MH, Wisniewski SR et al. Bupropion-SR, sertraline, or venlafaxine-XR after failure of SSRIs for depression. N Engl J Med 2006; 354 (12): 1231–42.
36. Serretti A, Kato M, De Ronchi D, Kinoshita T. Meta-analysis of serotonin transporter gene promoter polymorphism (5-HTTLPR) association with selective serotonin reuptake inhibitor efficacy in depressed patients. Mol Psychiat 2007; 12: 247–57.
37. Weissman AM, Levy BT, Hartz AJ et al. Pooled analysis of antidepressant levels in lactating mothers, breast milk, and nursing infants. Am J Psychiat 2004; 161: 1066–78.
38. Wijkstra J, Lijmer J, Balk FJ et al. Pharmacological treatment for unipolar psychotic depression: systematic review and meta-analysis. Br J Psychiat 2006; 188: 410–5.
39. Wisner KL, Perel JM, Peindl KS et al. Prevention of recurrent postpartum depression: a randomized clinical trial. J Clin Psychiat 2001; 62: 82–6.
40. Wisner KL, Perel JM, Peindl KS et al. Prevention of postpartum depression: a pilot randomized clinical trial. Am J Psychiat 2004; 161: 1290–2.
41. Young EA, Kornstein SG, Marcus SM et al. Sex differences in response to citalopram: a STAR*D report. J Psychiat 2008.


