Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
O.V. Kotova, V.I. Frolova, V.E. Medvedev
Abstract
The prevalence of depressive disorders among cardiac patients is extremely high and continues to increase steadily. Selective serotonin reuptake inhibitors (SSRIs) are not only effective antidepressants but also reduce postinfarction morbidity and mortality. The purpose of the study was to investigate the efficacy, tolerability, and safety of the SSRI antidepressant fluvoxamine for the treatment of depression in patients with cardiovascular disease. The findings concerning the therapeutic efficacy of fluvoxamine in treatment of depressive disorders of mild to moderate severity, its tolerability and safety allow the authors to conclude that it is reasonable to use the drug in treatment of depression in patients with concomitant cardiac pathology .
Keywords: depression, cardiovascular disease, treatment, antidepressants, fluvoxamine.
For citation: O.V. Kotova, V.I. Frolova, V.E. Medvedev. Efficacy and tolerability of fluvoxamine (Rokona) in the treatment of depression in patients with cardiovascular pathology. Psychiatry and psychopharmacotherapy. 2022; 2: 34–39.
Распространенность депрессивных расстройств среди пациентов кардиологической сети чрезвычайно велика (от 20% до 45%) и продолжает неуклонно увеличиваться [1-5].
С увеличением числа пациентов с сердечно-сосудистым заболеваниями, страдающих коморбидными депрессивными расстройствами, возрастает потребность в дифференцированном назначении антидепрессантов на основании данных об индивидуальных характеристиках (спектр клинической активности и нежелательных явлений (НЯ), безопасность, переносимость, межлекарственные взаимодействия и т.д.) препаратов. Длительное время оценка таких характеристик во многом основывалась на обобщении данных об эффективности и НЯ тимолептиков, полученных в ходе их изучения у соматически благополучных пациентов. Кроме того, исследования, непосредственно связанные с назначением антидепрессантов больным с актуальной патологией внутренних органов, по-прежнему, немногочисленны, а появление новых генерических препаратов не сопровождается целенаправленным исследованием их эффектов у больных с сердечно-сосудистой патологией. При этом современные данные свидетельствуют, что селективные ингибиторы обратного захвата серотонина (СИОЗС) не только являются эффективными антидепрессантами, но и снижают постинфарктную заболеваемость и смертность. Активация серотонинергической системы во внутренних органах способствует снижению агрегации тромбоцитов, препятствует тромбообразованию и оказывает протективное воздействие на эндотелий сосудов [6-7].
Например, H. Tagashira с соавт. (2010) в экспериментах с животными, исследуя роль стимуляции σ(1)-рецептора (σ(1)R) флувоксамином на гипертрофию миокарда и восстановление функции сердца, указывают, что введение флувоксамина значительно ослабляет гипертрофию миокарда, восстанавливает экспрессии σ(1)R в левом желудочке, ослабляет вызванное гипертрофией нарушение фракционного укорочения ЛЖ. Лечение флувоксамином также значимо восстанавливает ТАС-индуцированные нарушения AKT и эндотелиальный синтез окиси азота [8].
Собственно антидепрессивный механизм действия флувоксамина связан с избирательным ингибированием обратного захвата серотонина нейронами головного мозга и характеризуется минимальным влиянием на норадренергическую передачу. Флувоксамин обладает невыраженной способностью связываться с α-адренергическими, β-адренергическими, гистаминергическими, мускариновыми холинергическими, дофаминергическими или серотонинергическими рецепторами. Кроме того, флувоксамин имеет свойства агониста и высокое сродство к σ1-рецепторам, находящимся в эндоплазматическом ретикулуме и связанным с аберрантной глутаматной нейротрансмиссией [9-10].
В ряде работ показано, что в ночное время под воздействием флувоксамина повышается концентрация мелатонина за счет ингибирования флувоксамином нескольких ферментов системы цитохрома P450 (CYP1A2, CYP2C19), метаболизирующих мелатонин [9].
В то же время эффективность флувоксамина при лечении депрессий у пациентов с коморбидной сердечно-сосудистой патологией ранее изучена в единичных краткосрочных исследованиях. В частности, V.M. Tebbs с соавт. (1987) на обширном материале (1096 пожилых – средний возраст 67 лет, страдающих CCЗ и депрессией с симптомами тревоги пациентов) представляют данные о том, что препарат в дозе от 100 мг/сутки через шесть недель обеспечивает в среднем 61% улучшение показателей по шкале MADRS [11]. J.S. Wakelin (1986) приводит объединенные данные восьми двойных слепых плацебо-контролируемых исследований (76 пожилых пациентах – возраст 60-71 года, у которых депрессия сочеталась с сердечно-сосудистым заболеванием), согласно которым флувоксамин (50-150 мг/сут) при лечении большой депрессии не уступает в эффективности антидепрессантам других групп [12]. Наконец, E. Jaquenoud с соавт. (1997) в открытом исследовании (137 пациентов в возрасте от 75 до 97 лет с депрессией, осложненной кардиальной патологией, получавших кардиотропную терапию) назначают флувоксамин в дозах 50-300 мг/сут в течение шести недель. На момент окончания исследования количество больных, оценивающих выраженность депрессии по CGI как умеренную или тяжелую, снижается с 66% до 10% [13].
В ходе реализации программы кафедры психиатрии, психотерапии и психосоматической патологии ФНМО МИ РУДН (заведующий кафедрой – В.Э. Медведев), направленной на накопление большего объема данных об использовании тимолептиков-генериков у пациентов с соматическими заболеваниями, проведено натуралистическое психофармакологическое исследование.
Цель исследования – изучение эффективности, переносимости и безопасности СИОЗС антидепрессанта флувоксамина (Рокона) для лечения депрессий у пациентов с сердечно-сосудистыми заболеваниями.
Материалы и методы исследования
В исследование включались пациенты в возрасте от 20 до 60 лет с депрессивными эпизодами легкой или средней степени тяжести (F32.0, F32.1), биполярным аффективным расстройством (текущий эпизод легкой или умеренной депрессии – F31.3), рекуррентным депрессивным расстройством (депрессивный эпизод легкой или средней степени – F33.0, F33.1), циклотимией (F34.0), пролонгированными депрессивными реакциями в рамках расстройств адаптации (F43.2), страдающие сердечно-сосудистой патологией, прошедшие обследование в специализированных клинических базах кафедры (ФГБУ “Клиническая больница №1” УДП РФ, АО “Семейный доктор”, ООО “Международный институт психосоматического здоровья”).
Пациенты в выборке имели стабильные соматические показатели и находились на стабильных, установленных как минимум за 2 недели до включения пациента в исследование, дозах стандартизированной соматотропной терапии, соответствующей критериям вкючения/невключения.Критериями исключения являлись склонность к аллергическим реакциям, в т.ч. гиперчувствительность к флувоксамину в анамнезе; прием других психотропных препаратов; зависимость от психоактивных веществ; признаки психической патологии, не удовлетворяющей критериям включения; перенесенная или актуальная коронавирусная инфекция; тяжелая печеночная и/или почечная недостаточность, злокачественные новообразования, неврологические заболевания, закрытоугольная глаукома и иные тяжелые соматические заболевания в стадии декомпенсации, препятствующие участию в исследовании; беременность, лактация; участие в каких-либо исследованиях за четыре недели до включения в настоящее исследование. Также в связи с ингибированием флувоксамином цитохромов 1А2, 2С9 и 2С19 [8-13] в исследование не включались пациенты, принимающие такие антиаритмические средства, как амиодарон, пропранолол, мексилетин, дезагреганты тиклопидин и варфарин, гипотензивные препараты мибефрадил, триамтерен и верапамил. Наблюдение и терапия проводились в течение 3 месяцев в интервале суточных доз от 50 до 200 мг. Доза постепенно и индивидуально титровалась до обычно эффективной, со средней дозой 150 мг/сут. Препарат принимался во время еды. Динамика состояния пациентов регистрировалась в ходе 5 визитов: до начала исследования (Н0), через 1 (Н1), 2 (Н2), 4 (Н4), 8 (Н8) и 12 (завершающий визит Н12) недель. Использовались стандартные оценочные шкалы: шкала для оценки депрессии Гамильтона (HDRS) и Шкала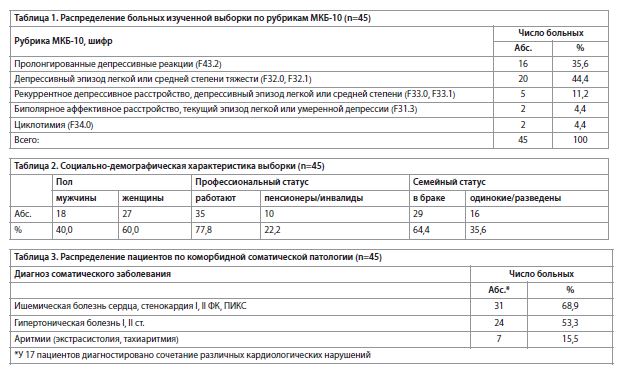 общего клинического впечатления (CGI). Критерием эффективности считались: снижение на 50% и более от исходных значений среднего балла по шкале HDRS, показатели “существенное улучшение”, “выраженное улучшение” и “умеренное улучшение” по шкале CGI-I, а также баллы CGI-S ≤ 2 («нет симптомов» или «пограничное расстройство»).
общего клинического впечатления (CGI). Критерием эффективности считались: снижение на 50% и более от исходных значений среднего балла по шкале HDRS, показатели “существенное улучшение”, “выраженное улучшение” и “умеренное улучшение” по шкале CGI-I, а также баллы CGI-S ≤ 2 («нет симптомов» или «пограничное расстройство»).
Для оценки переносимости и безопасности учитывались следующие показатели: 1) нежелательные явления, выявленные в результате спонтанных жалоб пациентов и целенаправленных вопросов при обследовании на каждом из предусмотренных визитов, 2) изменения в стартовых лабораторных и инструментальных показателях соматического статуса на фоне терапии флувоксамином (Рокона). Методы обследования соответствовали стандартам курации больных c CCЗ: вес, АД в положении сидя, ЧСС, 12-канальная ЭКГ в покое, ортостатическая проба, суточное мониторирование по Холтеру, лабораторные показатели (общий и биохимический анализ крови, коагулограмма).
C целью оценки риска лекарственных взаимодействий между флувоксамином и препаратами соматотропного действия регистрировались случаи усиления/манифестации нежелательных эффектов, потенциально связанные с изменениями метаболизма одного лекарственного средства под влиянием другого препарата, назначаемых в рамках комбинированной фармакотерапии. Для верификации побочных эффектов использовалась шкала побочных эффектов UKU. Для статистической обработки данных использовалась программа Statistica (компания StatSoft, США). Достоверность различий оценивалась с применением теста Колмогорова-Смирнова.
Результаты
Выборку составили 45 пациентов (26 женщин, 19 мужчин), из них 20 больных с депрессивными эпизодами легкой или средней степени тяжести, 16 – с пролонгированными депрессивными реакциями в рамках расстройств адаптации (нозогенные депрессии на совокупность ситуационных психотравмирующих факторов, связанных с соматическим заболеванием), 5 – с рекуррентным депрессивным расстройством, по 2 – с биполярным аффективным расстройством и циклотимией (Таблица 1). Средний возраст пациентов в выборке – 56,9 года.
Оценка патогенных факторов в изученной выборке свидетельствует о непосредственной связи болезненных состояний, составивших предмет исследования, с психотравмирующими ситуациями. Превалировало (35,6%) эмоционально неблагоприятное воздействие ухудшения соматического состояния, ассоциировавшееся у пациентов с развитием представления о неизлечимости болезни, страхом грядущей потери трудоспособности, возможности внезапной смерти. В другой части случаев психотравмирующая ситуация была связана с нестабильностью в сфере профессиональной трудовой деятельности (20%) (конфликты с начальством, смена места работы, понижение должностного статуса, необходимость решения нестандартных задач, расширение сферы круга обязанностей) или семейными неурядицами (4,4%). На фоне указанных психотравмирующих ситуаций у больных отмечалось не только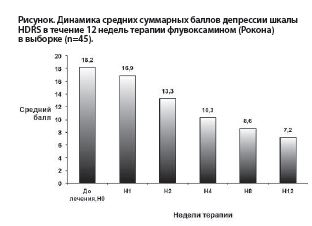 развитие депрессивного состояния, но и ухудшение соматического состояния (гипертонический криз, приступ стенокардии или аритмии), послужившее причиной обращения к врачу. В анамнезе у этих пациентов выявлялись психопатологические состояния, также формировавшиеся по механизму реактивной лабильности. Синдромальная характеристика депрессивных состояний была различна. Наиболее часто наблюдались пациенты с тревожно-ипохондрическими депрессиями – 76,7% (23 наблюдения), у 16,7% (5 наблюдений) в структуре депрессивного состояния преобладали апато-адинамические проявления и у 6,7% (2 наблюдения) – аффект тоски. Независимо от диагностической классификации депрессий у изученных больных значительное место в структуре аффективного синдрома занимали соматовегетативные проявления. Как правило, они выступали в виде гомономных (напоминающих симптомы сердечно-сосудистой патологии), полиморфных соматизированных и конверсионных симптомов. Социально-демографические характеристики изученных пациентов приведены в Таблице 2. ССЗ представлены в Таблице 3. Все больные получали подобранную гипотензивную, антиангинальную и противоаритмическую терапию: антиагреганты (ацетилсалициловая кислота 27 набл., клопидогрель 18 набл.), диуретики (гипотиазид, 21 набл.), ингибиторы АПФ (периндоприл, 8 набл., эналаприл, 11 набл.), антагонисты кальция (дилтиазем, амлодипин по 12 набл.), бета-адреноблокаторы (метопролол, 14 набл., бисопролол 9 набл.), пролонгированные нитраты (изосорбида динитрат, 13 набл.), антагонисты рецепторов ангиотензина II (лозартан 15 набл.), ингибиторы ГМГ-КоА-редуктазы (аторвастатин 17 набл., розувастатин 7 набл.), блокаторы калиевых каналов (амиодарон, 3 набл.).
развитие депрессивного состояния, но и ухудшение соматического состояния (гипертонический криз, приступ стенокардии или аритмии), послужившее причиной обращения к врачу. В анамнезе у этих пациентов выявлялись психопатологические состояния, также формировавшиеся по механизму реактивной лабильности. Синдромальная характеристика депрессивных состояний была различна. Наиболее часто наблюдались пациенты с тревожно-ипохондрическими депрессиями – 76,7% (23 наблюдения), у 16,7% (5 наблюдений) в структуре депрессивного состояния преобладали апато-адинамические проявления и у 6,7% (2 наблюдения) – аффект тоски. Независимо от диагностической классификации депрессий у изученных больных значительное место в структуре аффективного синдрома занимали соматовегетативные проявления. Как правило, они выступали в виде гомономных (напоминающих симптомы сердечно-сосудистой патологии), полиморфных соматизированных и конверсионных симптомов. Социально-демографические характеристики изученных пациентов приведены в Таблице 2. ССЗ представлены в Таблице 3. Все больные получали подобранную гипотензивную, антиангинальную и противоаритмическую терапию: антиагреганты (ацетилсалициловая кислота 27 набл., клопидогрель 18 набл.), диуретики (гипотиазид, 21 набл.), ингибиторы АПФ (периндоприл, 8 набл., эналаприл, 11 набл.), антагонисты кальция (дилтиазем, амлодипин по 12 набл.), бета-адреноблокаторы (метопролол, 14 набл., бисопролол 9 набл.), пролонгированные нитраты (изосорбида динитрат, 13 набл.), антагонисты рецепторов ангиотензина II (лозартан 15 набл.), ингибиторы ГМГ-КоА-редуктазы (аторвастатин 17 набл., розувастатин 7 набл.), блокаторы калиевых каналов (амиодарон, 3 набл.).
Результаты
Группа респондеров
К моменту завершения исследования клинически значимое улучшение (пациенты, квалифицированные как респондеры по принятым в исследовании критериям) фиксируется у 34 (75,6%) из 45 пациентов. Согласно шкале CGI-I “существенное улучшение” отмечается у 17 (37,8%), “выраженное улучшение” – у 22 (48,9%) пациентов.
Сходные результаты получены при анализе динамики тяжести психопатологических расстройств по шкале CGI-S. На момент завершающей оценки исходный средний балл CGI-S (4,3) снижается до уровня ≤ 2 у 32 (71,1%) больных. Полученные данные соответствуют приводимым в литературе результатам исследований эффективности флувоксамина [14-21].
Отчетливая редукция психопатологических состояний отмечается в среднем к концу второй недели лечения. Средняя эффективная доза флувоксамина (Рокона) составила 150 мг/сут.
Выраженное клиническое действие флувоксамина (Рокона), установленное по критерию эффективности (шкалы CGI-I и CGI-S), подтверждается достоверной редукцией исходных баллов депрессии шкалы HDRS. Значимое обратное развитие депрессивных симптомов регистрируется на 14 день лечения (р<0.05) и становится более выраженным на фоне дальнейшей терапии с непрерывным улучшением показателей вплоть до последнего дня исследования (p<0.001). Динамика средних баллов депрессии по шкале для оценки депрессии Гамильтона (HDRS) представлена на Рисунке. К окончанию курса терапии наибольшая редукция психопатологической симптоматики регистрируется у пациентов с тревожно-ипохондрической 73,1% (19 из 26 наблюдений) и апато-адинамической депрессией 62,5% (5 из 8 наблюдений). Клинически это проявляется уменьшением выраженности гипотимии, редукцией депрессивного содержательного комплекса. К концу первой недели лечения редуцируются трудности засыпания, кошмарные сновидения, заметно сокращается частота ночных пробуждений.
Улучшение настроения больные отмечают со 2 недели лечения с одновременным уменьшением вялости, подавленности, эмоциональной напряженности, чувства тревоги, раздражительности. Дезактуализируются ипохондрические идеи. Отмечая восстановление прежнего душевного равновесия, пациенты констатируют, что раньше слишком пессимистично оценивали ситуацию, "неосознанно" преувеличивали опасность текущего соматического состояния и его социальных последствий.
Значимая положительная динамика соматовегетативных и когнитивных нарушений регистрируется позже: на 4-8 неделе приема флувоксамина постепенно уменьшаются проявления вегетативной лабильности, истеро-конверсионных расстройств (ощущение “кома” в горле, “ватности” ног, “прилива жара” к голове, “онемение” рук и ног по типу “перчаток” и “носков”, приступы дрожи в теле, головокружения и “обмороки” без потери сознания, афония и др.); нормализуется память и концентрация внимания.
Группа нонреспондеров
К моменту окончания исследования, несмотря на положительную динамику самочувствия, клинически значимое улучшение по принятым в исследовании критериям не отмечено у 11 (24,4%) пациентов из числа завершивших полный курс терапии, что указывает на необходимость дальнейшего продолжения терапии с возможной титрацией среднесуточной дозы антидепрессанта в сторону повышения (до максимально допустимой 300 мг/сут).
Группу нонреспондеров составили семь пациентов с психогенными депрессиями и четыре – с соматогенно обусловленными депрессивными эпизодами. У большинства больных (8 наблюдений) в анамнезе выявляются две и более депрессий, по поводу которых пациентам проводилось лечение различными группами антидепрессантов (полициклические, селективные). Средняя длительность актуальной депрессии среди нонреспондеров достигает 7,5 месяца. При анализе психопатологических особенностей аффективных расстройств в данной группе не отмечается существенного влияния флувоксамина у больных с тоскливой депрессией, а также у 5 пациентов с апато-адинамическим и у 5 – с затяжным (более 1 года) ипохондрическим депрессивным состоянием.
Переносимость препарата
Установлен благоприятный профиль безопасности препарата. Нежелательные явления, связанные с флувоксамином (Рокона), зарегистрированы у 9 (20%) пациентов преимущественно в течение первых 2 недель терапии. В соответствии с целью исследования особое внимание уделялось влиянию флувоксамина (Рокона) на основные гемодинамические показатели. Ни в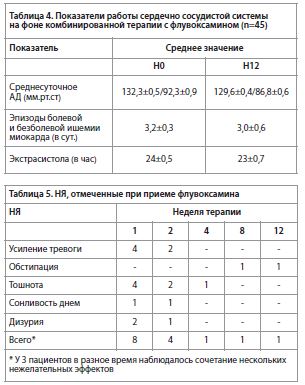 одном из наблюдений не зарегистрированы клинически значимые взаимодействия между флувоксамином и средствами, направленными на коррекцию сердечно-сосудистой патологии.
одном из наблюдений не зарегистрированы клинически значимые взаимодействия между флувоксамином и средствами, направленными на коррекцию сердечно-сосудистой патологии.
На момент окончания терапии у больных изученной выборки не зафиксировано появления жизнеопасных аритмий и/или внутрисердечных блокад. В ходе исследования не отмечено клинически значимого изменения артериального давления (включая ортостатическую гипотензию), а также значимых изменений частоты сердечных сокращений. Относительно результатов холтеровского мониторирования можно отметить отсутствие достоверных отличий по показателям суправентрикулярной и вентрикулярной эктопической активности, а также динамики сегмента ST. Также следует отметить отсутствие динамики интервала QT и QTc на фоне приема препарата, на что особенно обращают внимание при назначении некоторых (например, трициклических) антидепрессантов, способных удлинять интервал QT и вызывать угрожающие жизни желудочковые тахикардии типа “пируэт” (torsades de роintes) [22-23]. В течение 12-недельной терапии не обнаружено и отрицательного влияния флувоксамина на показатели крови. Напротив, при соматическом обследовании в ходе исследования установлено, что на фоне лечения антидепрессантом флувоксамином в сочетании с подобранной кардиотропной терапией отмечается тенденция к улучшению основных гемодинамических показателей: уменьшение частоты возникновения и продолжительности стенокардитических приступов, подъемов АД (Таблица 4). Связанными с препаратом нежелательными явлениями являлись в 4 случаях – усиление чувства тревоги с соматовегетативными проявлениями, в 3 – тошнота, по 1 случаю – сонливости в дневное время, затрудненное мочеиспускание, диарея, обстипация (Таблица 5).
Самостоятельная отмена флувоксамина (Рокона) у 12 пациентов по окончании исследования не сопровождалась развитием признаков синдрома отмены (утомляемость, сонливость, головная боль, тошнота, рвота, анорексия, сухость во рту, головокружение, понос, бессонница, тревога, раздражимость, дезориентация, парестезии, потливость).
Обсуждение
В результате проведенного исследования получены достоверные доказательства эффективности флувоксамина (Рокона) при 12-недельной терапии депрессивных расстройств легкой или средней степени тяжести у больных с сердечно-сосудистой патологией. Препарат обеспечивает редукцию психопатологических состояний у больных с соматическими заболеваниями. Терапевтический эффект препарата реализуется быстро. Клинически значимая редукция психопатологических нарушений, наряду с улучшением самочувствия пациентов, регистрируется у большинства больных с 14 дня терапии. При использовании в терапии депрессивных расстройств у соматически больных флувоксамина (Рокона) препарат обладает благоприятным профилем переносимости и безопасности. Полученные результаты свидетельствую о том, что флувоксамин (Рокона) не оказывает отрицательного влияния на течение соматической патологии (ишемическая болезнь сердца, артериальная гипертония, аритмии) и обеспечивает высокий уровень комплаентности пациентов. Такие данные полностью согласуются с имеющимися в литературе указаниями на то, что среди побочных эффектов препарата чаще всего упоминаются тошнота и умеренный седативный эффект [24-28].
В исследовании не отмечено признаков взаимодействия флувоксамина (Рокона) в средних терапевтических дозах (150 мг/день) с современными препаратами, применяющимися для лечения сердечно-сосудистых заболеваний, что также соотносится с имеющимися в литературе данными о безопасности комбинированной терапии с использованием тимоаналептика [29-32].
Полученные данные о терапевтической эффективности флувоксамина (Рокона) при лечении депрессивных расстройств легкой или средней степени тяжести, его переносимости и безопасности позволяют сделать вывод о целесообразности использования препарата при лечении депрессивных состояний у больных с сопутствующей кардиологической патологией.
Сведения об авторах:
Медведев Владимир Эрнстович – заведующий кафедрой психиатрии, психотерапии и психосоматической патологии ФНМО МИ РУДН, доцент, к.м.н., Medvedev_ve@pfur.ru, ORCID 0000-0001-8653-596X
Котова Ольга Владимировна - доцент кафедры психиатрии, психотерапии и психосоматической патологии ФНМО МИ РУДН, к.м.н., ORCID 0000-0002-3908-0381
Фролова Вероника Игоревна - доцент кафедры психиатрии, психотерапии и психосоматической патологии ФНМО МИ РУДН, к.м.н., ORCID 0000-0003-2261-3812
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№02 2022
Эффективность и переносимость флувоксамина (Рокона) при лечении депрессий у пациентов с сердечно-сосудистой патологией №02 2022
Абстракт
Распространенность депрессивных расстройств среди пациентов кардиологической сети чрезвычайно велика и продолжает неуклонно увеличиваться. Селективные ингибиторы обратного захвата серотонина (СИОЗС) не только являются эффективными антидепрессантами, но и снижают постинфарктную заболеваемость и смертность. Цель исследования – изучение эффективности, переносимости и безопасности СИОЗС антидепрессанта флувоксамина (Рокона) для лечения депрессий у пациентов с сердечно-сосудистыми заболеваниями. Полученные данные о терапевтической эффективности флувоксамина (Рокона) при лечении депрессивных расстройств легкой или средней степени тяжести, его переносимости и безопасности позволяют сделать вывод о целесообразности использования препарата при лечении депрессивных состояний у больных с сопутствующей кардиологической патологией.
Ключевые слова: депрессия, сердечно-сосудистые заболевания, лечение, антидепрессанты, флувоксамин, Рокона.
Для цитирования: О.В. Котова, В.И. Фролова, В.Э. Медведев. Эффективность и переносимость флувоксамина (Рокона) при лечении депрессий у пациентов с сердечно-сосудистой патологией. Психиатрия и психофармакотерапия. 2022; 2: 34–39.
Efficacy and tolerability of fluvoxamine (Rokona) in the treatment of depression in patients with cardiovascular pathology
Распространенность депрессивных расстройств среди пациентов кардиологической сети чрезвычайно велика и продолжает неуклонно увеличиваться. Селективные ингибиторы обратного захвата серотонина (СИОЗС) не только являются эффективными антидепрессантами, но и снижают постинфарктную заболеваемость и смертность. Цель исследования – изучение эффективности, переносимости и безопасности СИОЗС антидепрессанта флувоксамина (Рокона) для лечения депрессий у пациентов с сердечно-сосудистыми заболеваниями. Полученные данные о терапевтической эффективности флувоксамина (Рокона) при лечении депрессивных расстройств легкой или средней степени тяжести, его переносимости и безопасности позволяют сделать вывод о целесообразности использования препарата при лечении депрессивных состояний у больных с сопутствующей кардиологической патологией.
Ключевые слова: депрессия, сердечно-сосудистые заболевания, лечение, антидепрессанты, флувоксамин, Рокона.
Для цитирования: О.В. Котова, В.И. Фролова, В.Э. Медведев. Эффективность и переносимость флувоксамина (Рокона) при лечении депрессий у пациентов с сердечно-сосудистой патологией. Психиатрия и психофармакотерапия. 2022; 2: 34–39.
Efficacy and tolerability of fluvoxamine (Rokona) in the treatment of depression in patients with cardiovascular pathology
O.V. Kotova, V.I. Frolova, V.E. Medvedev
Abstract
The prevalence of depressive disorders among cardiac patients is extremely high and continues to increase steadily. Selective serotonin reuptake inhibitors (SSRIs) are not only effective antidepressants but also reduce postinfarction morbidity and mortality. The purpose of the study was to investigate the efficacy, tolerability, and safety of the SSRI antidepressant fluvoxamine for the treatment of depression in patients with cardiovascular disease. The findings concerning the therapeutic efficacy of fluvoxamine in treatment of depressive disorders of mild to moderate severity, its tolerability and safety allow the authors to conclude that it is reasonable to use the drug in treatment of depression in patients with concomitant cardiac pathology .
Keywords: depression, cardiovascular disease, treatment, antidepressants, fluvoxamine.
For citation: O.V. Kotova, V.I. Frolova, V.E. Medvedev. Efficacy and tolerability of fluvoxamine (Rokona) in the treatment of depression in patients with cardiovascular pathology. Psychiatry and psychopharmacotherapy. 2022; 2: 34–39.
Распространенность депрессивных расстройств среди пациентов кардиологической сети чрезвычайно велика (от 20% до 45%) и продолжает неуклонно увеличиваться [1-5].
С увеличением числа пациентов с сердечно-сосудистым заболеваниями, страдающих коморбидными депрессивными расстройствами, возрастает потребность в дифференцированном назначении антидепрессантов на основании данных об индивидуальных характеристиках (спектр клинической активности и нежелательных явлений (НЯ), безопасность, переносимость, межлекарственные взаимодействия и т.д.) препаратов. Длительное время оценка таких характеристик во многом основывалась на обобщении данных об эффективности и НЯ тимолептиков, полученных в ходе их изучения у соматически благополучных пациентов. Кроме того, исследования, непосредственно связанные с назначением антидепрессантов больным с актуальной патологией внутренних органов, по-прежнему, немногочисленны, а появление новых генерических препаратов не сопровождается целенаправленным исследованием их эффектов у больных с сердечно-сосудистой патологией. При этом современные данные свидетельствуют, что селективные ингибиторы обратного захвата серотонина (СИОЗС) не только являются эффективными антидепрессантами, но и снижают постинфарктную заболеваемость и смертность. Активация серотонинергической системы во внутренних органах способствует снижению агрегации тромбоцитов, препятствует тромбообразованию и оказывает протективное воздействие на эндотелий сосудов [6-7].
Например, H. Tagashira с соавт. (2010) в экспериментах с животными, исследуя роль стимуляции σ(1)-рецептора (σ(1)R) флувоксамином на гипертрофию миокарда и восстановление функции сердца, указывают, что введение флувоксамина значительно ослабляет гипертрофию миокарда, восстанавливает экспрессии σ(1)R в левом желудочке, ослабляет вызванное гипертрофией нарушение фракционного укорочения ЛЖ. Лечение флувоксамином также значимо восстанавливает ТАС-индуцированные нарушения AKT и эндотелиальный синтез окиси азота [8].
Собственно антидепрессивный механизм действия флувоксамина связан с избирательным ингибированием обратного захвата серотонина нейронами головного мозга и характеризуется минимальным влиянием на норадренергическую передачу. Флувоксамин обладает невыраженной способностью связываться с α-адренергическими, β-адренергическими, гистаминергическими, мускариновыми холинергическими, дофаминергическими или серотонинергическими рецепторами. Кроме того, флувоксамин имеет свойства агониста и высокое сродство к σ1-рецепторам, находящимся в эндоплазматическом ретикулуме и связанным с аберрантной глутаматной нейротрансмиссией [9-10].
В ряде работ показано, что в ночное время под воздействием флувоксамина повышается концентрация мелатонина за счет ингибирования флувоксамином нескольких ферментов системы цитохрома P450 (CYP1A2, CYP2C19), метаболизирующих мелатонин [9].
В то же время эффективность флувоксамина при лечении депрессий у пациентов с коморбидной сердечно-сосудистой патологией ранее изучена в единичных краткосрочных исследованиях. В частности, V.M. Tebbs с соавт. (1987) на обширном материале (1096 пожилых – средний возраст 67 лет, страдающих CCЗ и депрессией с симптомами тревоги пациентов) представляют данные о том, что препарат в дозе от 100 мг/сутки через шесть недель обеспечивает в среднем 61% улучшение показателей по шкале MADRS [11]. J.S. Wakelin (1986) приводит объединенные данные восьми двойных слепых плацебо-контролируемых исследований (76 пожилых пациентах – возраст 60-71 года, у которых депрессия сочеталась с сердечно-сосудистым заболеванием), согласно которым флувоксамин (50-150 мг/сут) при лечении большой депрессии не уступает в эффективности антидепрессантам других групп [12]. Наконец, E. Jaquenoud с соавт. (1997) в открытом исследовании (137 пациентов в возрасте от 75 до 97 лет с депрессией, осложненной кардиальной патологией, получавших кардиотропную терапию) назначают флувоксамин в дозах 50-300 мг/сут в течение шести недель. На момент окончания исследования количество больных, оценивающих выраженность депрессии по CGI как умеренную или тяжелую, снижается с 66% до 10% [13].
В ходе реализации программы кафедры психиатрии, психотерапии и психосоматической патологии ФНМО МИ РУДН (заведующий кафедрой – В.Э. Медведев), направленной на накопление большего объема данных об использовании тимолептиков-генериков у пациентов с соматическими заболеваниями, проведено натуралистическое психофармакологическое исследование.
Цель исследования – изучение эффективности, переносимости и безопасности СИОЗС антидепрессанта флувоксамина (Рокона) для лечения депрессий у пациентов с сердечно-сосудистыми заболеваниями.
Материалы и методы исследования
В исследование включались пациенты в возрасте от 20 до 60 лет с депрессивными эпизодами легкой или средней степени тяжести (F32.0, F32.1), биполярным аффективным расстройством (текущий эпизод легкой или умеренной депрессии – F31.3), рекуррентным депрессивным расстройством (депрессивный эпизод легкой или средней степени – F33.0, F33.1), циклотимией (F34.0), пролонгированными депрессивными реакциями в рамках расстройств адаптации (F43.2), страдающие сердечно-сосудистой патологией, прошедшие обследование в специализированных клинических базах кафедры (ФГБУ “Клиническая больница №1” УДП РФ, АО “Семейный доктор”, ООО “Международный институт психосоматического здоровья”).
Пациенты в выборке имели стабильные соматические показатели и находились на стабильных, установленных как минимум за 2 недели до включения пациента в исследование, дозах стандартизированной соматотропной терапии, соответствующей критериям вкючения/невключения.Критериями исключения являлись склонность к аллергическим реакциям, в т.ч. гиперчувствительность к флувоксамину в анамнезе; прием других психотропных препаратов; зависимость от психоактивных веществ; признаки психической патологии, не удовлетворяющей критериям включения; перенесенная или актуальная коронавирусная инфекция; тяжелая печеночная и/или почечная недостаточность, злокачественные новообразования, неврологические заболевания, закрытоугольная глаукома и иные тяжелые соматические заболевания в стадии декомпенсации, препятствующие участию в исследовании; беременность, лактация; участие в каких-либо исследованиях за четыре недели до включения в настоящее исследование. Также в связи с ингибированием флувоксамином цитохромов 1А2, 2С9 и 2С19 [8-13] в исследование не включались пациенты, принимающие такие антиаритмические средства, как амиодарон, пропранолол, мексилетин, дезагреганты тиклопидин и варфарин, гипотензивные препараты мибефрадил, триамтерен и верапамил. Наблюдение и терапия проводились в течение 3 месяцев в интервале суточных доз от 50 до 200 мг. Доза постепенно и индивидуально титровалась до обычно эффективной, со средней дозой 150 мг/сут. Препарат принимался во время еды. Динамика состояния пациентов регистрировалась в ходе 5 визитов: до начала исследования (Н0), через 1 (Н1), 2 (Н2), 4 (Н4), 8 (Н8) и 12 (завершающий визит Н12) недель. Использовались стандартные оценочные шкалы: шкала для оценки депрессии Гамильтона (HDRS) и Шкала
Для оценки переносимости и безопасности учитывались следующие показатели: 1) нежелательные явления, выявленные в результате спонтанных жалоб пациентов и целенаправленных вопросов при обследовании на каждом из предусмотренных визитов, 2) изменения в стартовых лабораторных и инструментальных показателях соматического статуса на фоне терапии флувоксамином (Рокона). Методы обследования соответствовали стандартам курации больных c CCЗ: вес, АД в положении сидя, ЧСС, 12-канальная ЭКГ в покое, ортостатическая проба, суточное мониторирование по Холтеру, лабораторные показатели (общий и биохимический анализ крови, коагулограмма).
C целью оценки риска лекарственных взаимодействий между флувоксамином и препаратами соматотропного действия регистрировались случаи усиления/манифестации нежелательных эффектов, потенциально связанные с изменениями метаболизма одного лекарственного средства под влиянием другого препарата, назначаемых в рамках комбинированной фармакотерапии. Для верификации побочных эффектов использовалась шкала побочных эффектов UKU. Для статистической обработки данных использовалась программа Statistica (компания StatSoft, США). Достоверность различий оценивалась с применением теста Колмогорова-Смирнова.
Результаты
Выборку составили 45 пациентов (26 женщин, 19 мужчин), из них 20 больных с депрессивными эпизодами легкой или средней степени тяжести, 16 – с пролонгированными депрессивными реакциями в рамках расстройств адаптации (нозогенные депрессии на совокупность ситуационных психотравмирующих факторов, связанных с соматическим заболеванием), 5 – с рекуррентным депрессивным расстройством, по 2 – с биполярным аффективным расстройством и циклотимией (Таблица 1). Средний возраст пациентов в выборке – 56,9 года.
Оценка патогенных факторов в изученной выборке свидетельствует о непосредственной связи болезненных состояний, составивших предмет исследования, с психотравмирующими ситуациями. Превалировало (35,6%) эмоционально неблагоприятное воздействие ухудшения соматического состояния, ассоциировавшееся у пациентов с развитием представления о неизлечимости болезни, страхом грядущей потери трудоспособности, возможности внезапной смерти. В другой части случаев психотравмирующая ситуация была связана с нестабильностью в сфере профессиональной трудовой деятельности (20%) (конфликты с начальством, смена места работы, понижение должностного статуса, необходимость решения нестандартных задач, расширение сферы круга обязанностей) или семейными неурядицами (4,4%). На фоне указанных психотравмирующих ситуаций у больных отмечалось не только
Результаты
Группа респондеров
К моменту завершения исследования клинически значимое улучшение (пациенты, квалифицированные как респондеры по принятым в исследовании критериям) фиксируется у 34 (75,6%) из 45 пациентов. Согласно шкале CGI-I “существенное улучшение” отмечается у 17 (37,8%), “выраженное улучшение” – у 22 (48,9%) пациентов.
Сходные результаты получены при анализе динамики тяжести психопатологических расстройств по шкале CGI-S. На момент завершающей оценки исходный средний балл CGI-S (4,3) снижается до уровня ≤ 2 у 32 (71,1%) больных. Полученные данные соответствуют приводимым в литературе результатам исследований эффективности флувоксамина [14-21].
Отчетливая редукция психопатологических состояний отмечается в среднем к концу второй недели лечения. Средняя эффективная доза флувоксамина (Рокона) составила 150 мг/сут.
Выраженное клиническое действие флувоксамина (Рокона), установленное по критерию эффективности (шкалы CGI-I и CGI-S), подтверждается достоверной редукцией исходных баллов депрессии шкалы HDRS. Значимое обратное развитие депрессивных симптомов регистрируется на 14 день лечения (р<0.05) и становится более выраженным на фоне дальнейшей терапии с непрерывным улучшением показателей вплоть до последнего дня исследования (p<0.001). Динамика средних баллов депрессии по шкале для оценки депрессии Гамильтона (HDRS) представлена на Рисунке. К окончанию курса терапии наибольшая редукция психопатологической симптоматики регистрируется у пациентов с тревожно-ипохондрической 73,1% (19 из 26 наблюдений) и апато-адинамической депрессией 62,5% (5 из 8 наблюдений). Клинически это проявляется уменьшением выраженности гипотимии, редукцией депрессивного содержательного комплекса. К концу первой недели лечения редуцируются трудности засыпания, кошмарные сновидения, заметно сокращается частота ночных пробуждений.
Улучшение настроения больные отмечают со 2 недели лечения с одновременным уменьшением вялости, подавленности, эмоциональной напряженности, чувства тревоги, раздражительности. Дезактуализируются ипохондрические идеи. Отмечая восстановление прежнего душевного равновесия, пациенты констатируют, что раньше слишком пессимистично оценивали ситуацию, "неосознанно" преувеличивали опасность текущего соматического состояния и его социальных последствий.
Значимая положительная динамика соматовегетативных и когнитивных нарушений регистрируется позже: на 4-8 неделе приема флувоксамина постепенно уменьшаются проявления вегетативной лабильности, истеро-конверсионных расстройств (ощущение “кома” в горле, “ватности” ног, “прилива жара” к голове, “онемение” рук и ног по типу “перчаток” и “носков”, приступы дрожи в теле, головокружения и “обмороки” без потери сознания, афония и др.); нормализуется память и концентрация внимания.
Группа нонреспондеров
К моменту окончания исследования, несмотря на положительную динамику самочувствия, клинически значимое улучшение по принятым в исследовании критериям не отмечено у 11 (24,4%) пациентов из числа завершивших полный курс терапии, что указывает на необходимость дальнейшего продолжения терапии с возможной титрацией среднесуточной дозы антидепрессанта в сторону повышения (до максимально допустимой 300 мг/сут).
Группу нонреспондеров составили семь пациентов с психогенными депрессиями и четыре – с соматогенно обусловленными депрессивными эпизодами. У большинства больных (8 наблюдений) в анамнезе выявляются две и более депрессий, по поводу которых пациентам проводилось лечение различными группами антидепрессантов (полициклические, селективные). Средняя длительность актуальной депрессии среди нонреспондеров достигает 7,5 месяца. При анализе психопатологических особенностей аффективных расстройств в данной группе не отмечается существенного влияния флувоксамина у больных с тоскливой депрессией, а также у 5 пациентов с апато-адинамическим и у 5 – с затяжным (более 1 года) ипохондрическим депрессивным состоянием.
Переносимость препарата
Установлен благоприятный профиль безопасности препарата. Нежелательные явления, связанные с флувоксамином (Рокона), зарегистрированы у 9 (20%) пациентов преимущественно в течение первых 2 недель терапии. В соответствии с целью исследования особое внимание уделялось влиянию флувоксамина (Рокона) на основные гемодинамические показатели. Ни в
На момент окончания терапии у больных изученной выборки не зафиксировано появления жизнеопасных аритмий и/или внутрисердечных блокад. В ходе исследования не отмечено клинически значимого изменения артериального давления (включая ортостатическую гипотензию), а также значимых изменений частоты сердечных сокращений. Относительно результатов холтеровского мониторирования можно отметить отсутствие достоверных отличий по показателям суправентрикулярной и вентрикулярной эктопической активности, а также динамики сегмента ST. Также следует отметить отсутствие динамики интервала QT и QTc на фоне приема препарата, на что особенно обращают внимание при назначении некоторых (например, трициклических) антидепрессантов, способных удлинять интервал QT и вызывать угрожающие жизни желудочковые тахикардии типа “пируэт” (torsades de роintes) [22-23]. В течение 12-недельной терапии не обнаружено и отрицательного влияния флувоксамина на показатели крови. Напротив, при соматическом обследовании в ходе исследования установлено, что на фоне лечения антидепрессантом флувоксамином в сочетании с подобранной кардиотропной терапией отмечается тенденция к улучшению основных гемодинамических показателей: уменьшение частоты возникновения и продолжительности стенокардитических приступов, подъемов АД (Таблица 4). Связанными с препаратом нежелательными явлениями являлись в 4 случаях – усиление чувства тревоги с соматовегетативными проявлениями, в 3 – тошнота, по 1 случаю – сонливости в дневное время, затрудненное мочеиспускание, диарея, обстипация (Таблица 5).
Самостоятельная отмена флувоксамина (Рокона) у 12 пациентов по окончании исследования не сопровождалась развитием признаков синдрома отмены (утомляемость, сонливость, головная боль, тошнота, рвота, анорексия, сухость во рту, головокружение, понос, бессонница, тревога, раздражимость, дезориентация, парестезии, потливость).
Обсуждение
В результате проведенного исследования получены достоверные доказательства эффективности флувоксамина (Рокона) при 12-недельной терапии депрессивных расстройств легкой или средней степени тяжести у больных с сердечно-сосудистой патологией. Препарат обеспечивает редукцию психопатологических состояний у больных с соматическими заболеваниями. Терапевтический эффект препарата реализуется быстро. Клинически значимая редукция психопатологических нарушений, наряду с улучшением самочувствия пациентов, регистрируется у большинства больных с 14 дня терапии. При использовании в терапии депрессивных расстройств у соматически больных флувоксамина (Рокона) препарат обладает благоприятным профилем переносимости и безопасности. Полученные результаты свидетельствую о том, что флувоксамин (Рокона) не оказывает отрицательного влияния на течение соматической патологии (ишемическая болезнь сердца, артериальная гипертония, аритмии) и обеспечивает высокий уровень комплаентности пациентов. Такие данные полностью согласуются с имеющимися в литературе указаниями на то, что среди побочных эффектов препарата чаще всего упоминаются тошнота и умеренный седативный эффект [24-28].
В исследовании не отмечено признаков взаимодействия флувоксамина (Рокона) в средних терапевтических дозах (150 мг/день) с современными препаратами, применяющимися для лечения сердечно-сосудистых заболеваний, что также соотносится с имеющимися в литературе данными о безопасности комбинированной терапии с использованием тимоаналептика [29-32].
Полученные данные о терапевтической эффективности флувоксамина (Рокона) при лечении депрессивных расстройств легкой или средней степени тяжести, его переносимости и безопасности позволяют сделать вывод о целесообразности использования препарата при лечении депрессивных состояний у больных с сопутствующей кардиологической патологией.
Сведения об авторах:
Медведев Владимир Эрнстович – заведующий кафедрой психиатрии, психотерапии и психосоматической патологии ФНМО МИ РУДН, доцент, к.м.н., Medvedev_ve@pfur.ru, ORCID 0000-0001-8653-596X
Котова Ольга Владимировна - доцент кафедры психиатрии, психотерапии и психосоматической патологии ФНМО МИ РУДН, к.м.н., ORCID 0000-0002-3908-0381
Фролова Вероника Игоревна - доцент кафедры психиатрии, психотерапии и психосоматической патологии ФНМО МИ РУДН, к.м.н., ORCID 0000-0003-2261-3812
25 марта 2022
Количество просмотров: 1721


