Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№02 2013
Психические нарушения, развивающиеся при противовирусной терапии хронического гепатита С №02 2013
Номера страниц в выпуске:4-8
В настоящее время нет единого мнения по поводу частоты возникновения психических расстройств при ПВТ ХГС, их психопатологической квалификации, значимости тех или иных факторов риска. Существуют разные точки зрения относительно возможности продолжения курса ПВТ при развитии психических нарушений. Отсутствуют протоколы ПВТ больных ХГС с отягощенным психиатрическим анамнезом.
Резюме. Обследованы 278 больных хроническим гепатитом С, получавших противовирусную терапию. У 169 больных при проведении противовирусной терапии развились депрессивные расстройства. Определены клинические и фармакотерапевтические особенности таких депрессий. Выявлены предикторы, влияющие на частоту возникновения и структуру депрессивного синдрома. Установлена неоднородность депрессий по клиническим и демографическим показателям. Выделены основные типы депрессивных расстройств, развивающихся при интерферонотерапии хронического гепатита С, разработаны алгоритмы, позволяющие оптимизировать лечебно-диагностический процесс, в том числе повысить эффективность терапии основного заболевания (хронического гепатита С).
Ключевые слова: хронический гепатит С, противовирусная терапия, интерферон, депрессия, кластерный анализ.
Mental disorders developing during antiviral therapy for chronic hepatitis C
N.N.Ivanets, M.A.Kinkulkina, Yu.G.Tikhonova, D.I.Morozov
I.M.Sechenov First Moscow State Medical University, Ministry of Health of the Russian Federation
Summary. 278 patients with chronic hepatitis C who had received antiviral therapy were examined. During this therapy, 169 patients developed depressive disorders. Their clinical and pharmacotherapeutic features were determined. The predictors affecting the incidence and pattern of depressive syndrome were found. There was heterogeneity of depressions in terms of clinical and demographic indicators. The main types of depressive disorders developing during interferon therapy for chronic hepatitis were identified; algorithms that allowed the optimization of a therapeutic and diagnostic process and the enhanced efficiency of therapy for the underlying disease (chronic hepatitis C) were elaborated.
Key words: chronic hepatitis C, antiviral therapy, interferon, depression, cluster analysis.
Хронический гепатит С (ХГС) является одним из наиболее распространенных в мире инфекционных заболеваний, вызывает тяжелые медицинские и социальные последствия (Т.М.Игнатова, 2000; S.Sockalingam, S.Abbey, 2009). Адекватная противовирусная терапия (ПВТ) ХГС включает препараты интерферона-a (ИФН-a), применение которого провоцирует возникновение психопатологической симптоматики (C.Crone и соавт., 2004; A.Shakoor и соавт., 2010; Z.Pavlović и соавт., 2011). Распространенность аффективных расстройств в период ПВТ больных ХГС варьирует в пределах от 23 до 67%, при этом наиболее часто отмечается развитие депрессивной симптоматики (А.О.Морозов, 2006; А.В.Волков, 2011; A.Valentine и соавт., 1998; C.Crone и соавт., 2004).
В настоящее время нет единого мнения по поводу частоты возникновения психических расстройств при ПВТ ХГС, их психопатологической квалификации, значимости тех или иных факторов риска. Существуют разные точки зрения относительно возможности продолжения курса ПВТ при развитии психических нарушений. Отсутствуют протоколы ПВТ больных ХГС с отягощенным психиатрическим анамнезом.
Цель исследования – комплексное клинико-психопатологическое изучение психических нарушений у больных ХГС, получающих ПВТ, определение факторов, влияющих на развитие и структуру психопатологических нарушений, сравнительная оценка психофармакотерапии различными антидепрессантами (АДП) и разработка дифференцированных рекомендаций по терапии данной категории больных.
Материалы и методы
Проведено проспективное исследование больных ХГС старше 18 лет, получавших ПВТ препаратами ИФН. Больные проходили стационарное или амбулаторное лечение в Клинике нефрологии, внутренних и профессиональных болезней им. Е.М.Тареева ГБОУ ВПО Первый МГМУ
им. И.М.Сеченова с 2003 по 2012 г. Из исследования были исключены больные с шизофренией и шизоаффективным расстройством; с тяжелой соматической патологией, приводящей к появлению дополнительной психопатологической симптоматики (в том числе цирроз печени и проявления печеночной энцефалопатии); больные, злоупотреблявшие психоактивными веществами (ПАВ), включая алкоголь, в течение 6 мес до начала ПВТ.
Для оценки состояния больных использовались клинико-психопатологический, клинико-катамнестический методы; применялись стандартизированные психометрические шкалы: шкала Монтгомери–Асберга для оценки депрессий (MADRS), шкала Бека для самооценки тяжести депрессии (BDI), шкалы оценки патологического влечения к алкоголю и наркотикам (ПВА и ПВН).
Для лечения депрессий у больных ХГС применялись АДП, различные по механизму действия и спектру психофармакологической активности: миртазапин, тианептин, миансерин, пароксетин, флувоксамин, эсциталопрам, пирлиндол, амитриптилин, кломипрамин. Терапия АДП оценивалась как эффективная, если отмечалось отчетливое клиническое улучшение состояния и редукция симптомов по шкале MADRS составляла более 50%. Оценивалась скорость уменьшения выраженности психопатологической симптоматики, отмечался факт достижения ремиссии (клинически и по психометрическим шкалам).
Анализ результатов исследования проводился с использованием методов статистической обработки, включая описательную статистику, непараметрические методы статистического анализа, в том числе медианный тест, критерий c2, методы Мак-Немара, Манна–Уитни, Вилкоксона, коэффициент ранговой корреляции Спирмена и двусторонний критерий Фишера. Для получения объективной информации о значимости исследованных показателей использовался кластерный и дисперсионный анализ. Достоверным считался уровень значимости p<0,05.
Результаты
Были обследованы 278 больных ХГС. Их клинико-демографические характеристики представлены в табл. 1.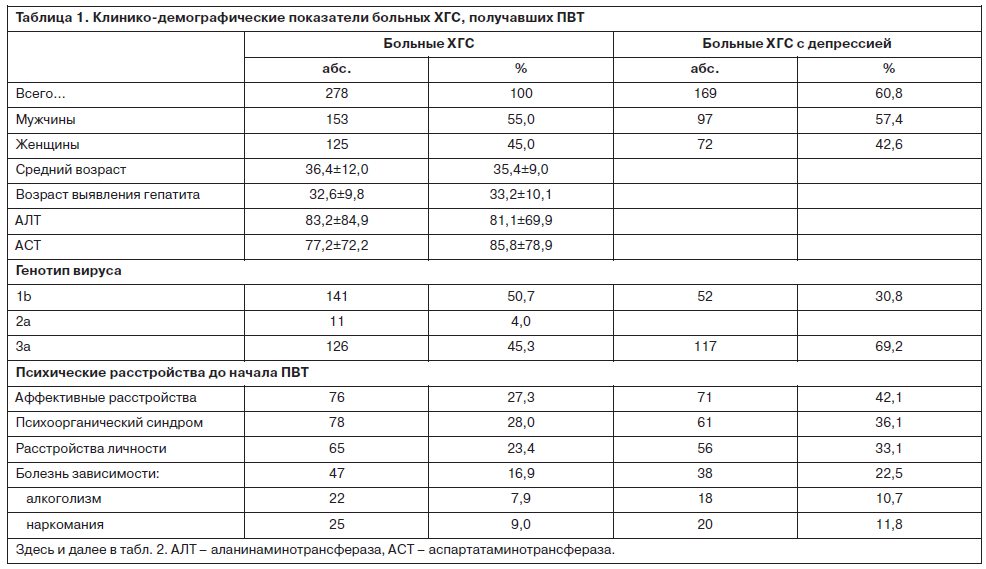
До начала ПВТ уровень депрессии у 90% больных был ниже порогового значения для ремиссии (по субъективной и врачебной оценке; шкалы BDI и MADRS соответственно);
у 10% больных превышение порога ремиссии составляло 1–2 балла, выявлялись отдельные депрессивные симптомы, клинически не достигавшие уровня очерченного депрессивного синдрома.
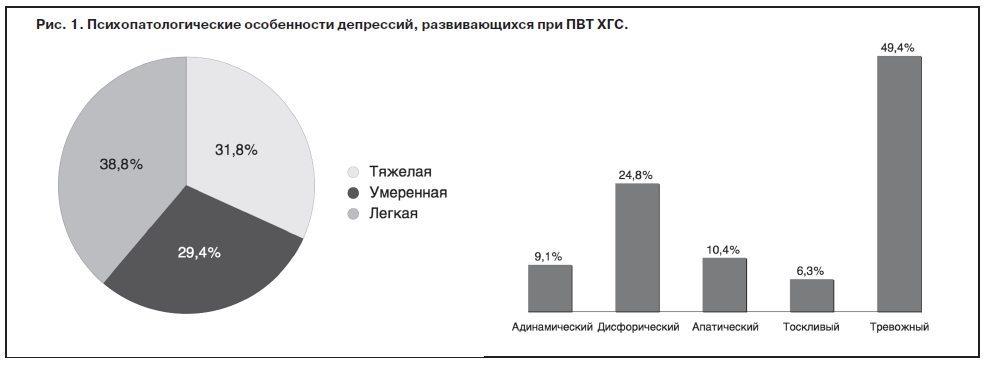
После начала ПВТ у 169 (60,8%) больных ХГС развивалась депрессивная симптоматика различной степени выраженности. Манифестация клинически очерченного депрессивного эпизода приходилась преимущественно на 3–12-ю неделю терапии противовирусными препаратами. При клинико-психопатологической оценке преобладали пациенты с тяжелой и умеренной депрессией – 27 (31,8%) и 25 (29,4%) соответственно. Средний суммарный балл выраженности депрессивной симптоматики по шкале MADRS составлял 28,3±5,1. Синдромальная оценка выявленных депрессий показала преобладание тревожных (49,4%) и дисфорических (24,8%) форм. Реже встречались апатическая (10,4%), адинамическая (9,1%) и тоскливая (6,3%) депрессии (рис. 1).
Выявлено, что наиболее значимым предиктором развития депрессии при ПВТ ХГС является наличие аффективной патологии в анамнезе (до начала проведения интерферонотерапии). У больных с аффективными расстройствами в анамнезе депрессия при ПВТ ХГС развивалась значительно чаще, чем в группе больных без депрессии в анамнезе (93,4% против 48,5%). Риск развития депрессии при проведении ПВТ ХГС также был выше у больных с сопутствующей психоорганической патологией, расстройствами личности и отягощенной психопатологически наследственностью. Важным прогностическим признаком развития депрессии являлся генотип вируса: у больных ХГС с генотипом 3а чаще развивалась депрессия при ПВТ, чем у больных с генотипами 1b и 2а.
Терапия депрессивных расстройств, развивающихся при проведении ПВТ ХГС, проводилась с учетом требований к применению фармакопрепаратов в соматопсихиатрической практике. Выбор АДП и дозы препарата проводился в соответствии с синдромальной структурой депрессии, соматическим состоянием больного, возрастом, индивидуальной переносимостью, учетом рекомендаций для лечения больных с заболеваниями печени. При необходимости (для купирования бессонницы, коррекции грубых психопатоподобных и дисфорических расстройств) дополнительно назначались препараты других фармакологических групп: антипсихотики (в малых дозах с целью коррекции поведения и усиления снотворного действия АДП), антиконвульсанты, анксиолитики.
Несмотря на тяжесть депрессивных расстройств у больных ХГС, получавших ПВТ, отмечена высокая эффективность антидепрессивной терапии. У всех больных, получавших АДП, клинически отмечено улучшение психического состояния. Доля больных с 50% редукцией депрессивной симптоматики после 12 нед терапии АДП составила 78,5%. Выявлены факторы, достоверно влияющие на эффективность антидепрессивной терапии, где наиболее интересным представляется взаимосвязь большей исходной тяжести депрессии с эффективностью психофармакотерапии (табл. 2).
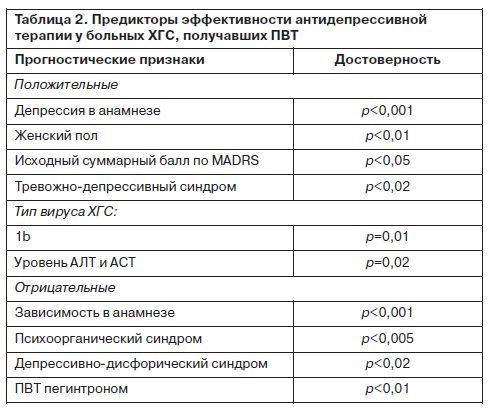
Купирование симптомов депрессии позволило продолжить проведение интерферонотерапии в полном объеме у большинства включенных в исследование больных. Не удалось продолжить ПВТ у 10 (5,9%) больных: у 5 больных депрессивная симптоматика являлась проявлением обострения патологического влечения к ПАВ, и причиной выхода из исследования становились отсутствие достаточного комплаенса и рецидив болезни зависимости; в 2 случаях больные отказались от продолжения ПВТ после развития тяжелой депрессии; 3 больных выбыли из программы ПВТ по причине развития тяжелых соматических осложнений интерферонотерапии.
Полученные с помощью одномерных методов статистического анализа данные о взаимосвязи различных признаков не позволяли в полном объеме оценить структуру всей совокупности клинических наблюдений. Необходимо было выделить из множества исходных данных наиболее значимые параметры, характеризующие элементы выборки, что позволило бы разработать диагностические и терапевтические алгоритмы. Значительное количество данных с высоким уровнем достоверности позволило провести дополнительный статистический анализ с использованием многомерных методов статистики.
Учитывая, что каждый клинический случай характеризовался большим количеством признаков, анализировалось наличие взаимосвязи не только между признаками, но и среди объектов наблюдения. Использование кластерного анализа дало возможность разбить всю совокупность полученных результатов на группы (кластеры) таким образом, чтобы элементы каждого кластера значимо коррелировали между собой, а представители разных групп характеризовались слабой корреляционной связью.
Для определения числа кластеров был проведен иерархический кластерный анализ с помощью различных методов объединения. При пошаговой кластеризации были выявлены 3 кластера как наиболее оптимальное число групп объектов наблюдения (клинических случаев), в которых внутригрупповое сходство между объектами больше, чем межгрупповое (рис. 2). При последующей агломерации терялась наглядность группирования. На представленной дендрограмме горизонтальная ось представляет наблюдения, вертикальная – расстояние объединения.
Учитывая полученные данные о конечном числе кластеров, был проведен кластерный анализ по методу k-средних Мак-Кина. Анализ средних значений переменных для каждого кластера позволил увидеть различия между кластерами по некоторым признакам (рис. 3). Включение в процедуру кластеризации дополнительных признаков показало, что значимость этих признаков как кластеризационных переменных является низкой.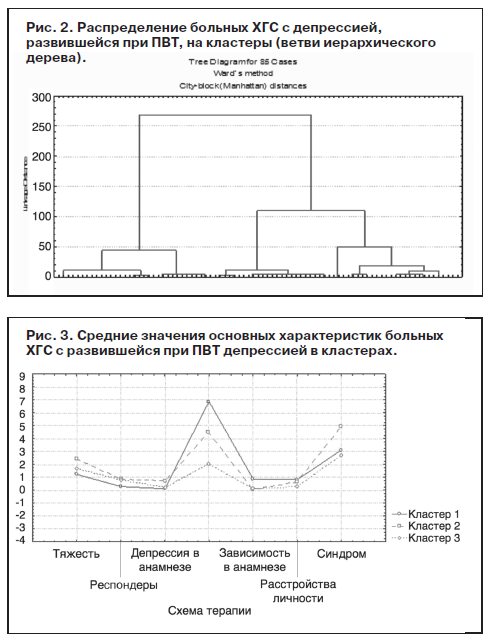
С помощью непараметрического дисперсионного анализа Краскела–Уоллиса были выявлены достоверные различия в распределении признаков в выделенных группах. Для бинарных признаков использовался логлинейный анализ – метод максимального правдоподобия c2 (табл. 3, 4).
По результатам разбиения основной совокупности наблюдений на кластеры были выявлены значимые отличия основных клинических характеристик депрессивного синдрома в группах. Проведенный далее анализ клинико-анамнестических данных и результатов психофармакотерапии позволил выделить 3 основных типа наблюдаемых при проведении ПВТ ХГС депрессивных расстройств и предложить дифференцированные схемы лечения.
В первом кластере при анализе частоты сопутствующей психической патологии было выявлено значительное преобладание пациентов с сопутствующей болезнью зависимости от ПАВ. Для этой группы были характерны преимущественно умеренные депрессии (средний балл MADRS до начала терапии АДП 26,7±4,04) с преобладанием дисфорической симптоматики. Оценка по шкалам ПВН и ПВА показала достоверное повышение при ПВТ суммарной выраженности патологического влечения к ПАВ (средний балл ПВН 1,61; ПВА 1,46) и достоверный рост значений по всем субшкалам. Наиболее высокий прирост отмечен по шкале аффективных нарушений как для больных опийной наркоманией, так и для больных алкоголизмом. Результаты анализа показали, что ИФН-индуцированная депрессия и синдром патологического влечения у больных ХГС с болезнью зависимости от ПАВ тесно связаны между собой (отмечена сильная и высокодостоверная корреляция симптоматики).
Депрессии, развивающиеся при ПВТ ХГС у больных с зависимостью, являются проявлением аффективного компонента обострения патологического влечения. Эффективность антидепрессивной терапии, несмотря на высокие дозы препаратов, была значительно ниже, чем в других кластерах. Таким больным требовались дополнительные назначения препаратов других психофармакологических групп (нейролептиков, нормотимиков) для купирования различных компонентов синдрома патологического влечения к ПАВ.
Во втором кластере превалировали больные с аффективной патологией в анамнезе (до начала ПВТ). Депрессии у таких больных рассматривались как депрессивные фазы, спровоцированные применением ИФН. Они отличались наибольшей выраженностью депрессивной симптоматики (средний балл MADRS до начала терапии АДП 32,3±4,15), с преобладанием тревожного компонента в структуре депрессивного синдрома, в то время как депрессии в анамнезе таких больных протекали преимущественно с меланхолическим аффектом. Эффективность антидепрессивной терапии в группе больных ХГС с рекуррентными депрессиями была высокая (более 75%). Уровень достижения ремиссии (суммарный балл по MADRS<12) к
12-й неделе антидепрессивной терапии в группе больных с фазным течением аффективной патологии был достоверно ниже: 51,9% по сравнению с 71,2% больных без аффективной патологии в анамнезе.
Большинство больных 3-й группы не имели сопутствующей психической патологии, т.е. у данной категории больных ПВТ являлась причиной впервые развившейся депрессии. Интервал распределения наиболее типичных показателей тяжести депрессий в 3-й группе был шире, чем в других; выраженность аффективных переживаний варьировала от легких до тяжелых (от 21 до 33 баллов по MADRS; средний балл MADRS до начала терапии АДП 26,4±3,9). С примерно равной частотой встречались тревожный и дисфорический синдромы, у меньшего числа пациентов – апатические и адинамические депрессии. Отмечена высокая эффективность антидепрессивной терапии: доля респондеров к 12-й неделе психофармакотерапии превысила 83%. В этой группе больных чаще встречались депрессии тяжелые или умеренной тяжести (более 50%), при этом редукции депрессивной симптоматики удалось добиться с применением невысоких доз АДП. Была выявлена достоверная прямая корреляция исходной тяжести депрессии и эффективности антидепрессивной терапии.
Обсуждение
Проведенное исследование выявило, что более чем у половины больных ХГС при проведении интерферонотерапии развивается депрессивная симптоматика. ИФН-индуцированные депрессии отличаются значительной выраженностью депрессивной симптоматики с преобладанием в структуре депрессивного синдрома тревоги и дисфории. И если тревожно-депрессивная симптоматика довольно часто наблюдается при соматогенных депрессиях, то значительное количество дисфорических форм говорит об особом характере именно ИФН-индуцированных депрессий. На характер депрессии оказывают влияние клинические характеристики ХГС: генотип вируса гепатита 3а является положительным предиктором развития и большей тяжести депрессий, развивающихся при ПВТ ХГС.
Учитывая высокую частоту развития и выраженность депрессий у больных ХГС, получающих ПВТ, особое значение приобретают своевременная диагностика и адекватное лечение этих расстройств, что позволяет эффективно проводить терапию основного заболевания, в том числе в полном объеме применять ПВТ. Пристальное внимание следует обращать на психическое состояние больных с такими факторами риска, как аффективная патология и злоупотребление ПАВ в анамнезе; наличие текущих психических расстройств (особенно патологии личности, в том числе органического генеза) и генотип вируса гепатита.
Выявлена неоднородность депрессий, развивающихся при ПВТ ХГС. В результате исследования схем группирования объектов наблюдения с помощью статистических методов (кластерный анализ) разработана классификационная модель. Выполненная с помощью иерархических методов процедура кластеризации позволила разбить совокупность всех объектов исследования (больных ХГС, получавших ПВТ, с депрессией) на 3 группы, достоверно отличающиеся друг от друга по набору признаков. Выявлены значимые отличия между кластерами и проведен анализ распределения клинических характеристик ХГС, психопатологической симптоматики и особенностей проводимой антидепрессивной терапии в отдельных кластерах (дисперсионный анализ).
На основе полученных данных выделено несколько типов депрессий, развивающихся при ПВТ ХГС, достоверно отличающихся друг от друга по набору признаков:
Выводы
Ключевые слова: хронический гепатит С, противовирусная терапия, интерферон, депрессия, кластерный анализ.
Mental disorders developing during antiviral therapy for chronic hepatitis C
N.N.Ivanets, M.A.Kinkulkina, Yu.G.Tikhonova, D.I.Morozov
I.M.Sechenov First Moscow State Medical University, Ministry of Health of the Russian Federation
Summary. 278 patients with chronic hepatitis C who had received antiviral therapy were examined. During this therapy, 169 patients developed depressive disorders. Their clinical and pharmacotherapeutic features were determined. The predictors affecting the incidence and pattern of depressive syndrome were found. There was heterogeneity of depressions in terms of clinical and demographic indicators. The main types of depressive disorders developing during interferon therapy for chronic hepatitis were identified; algorithms that allowed the optimization of a therapeutic and diagnostic process and the enhanced efficiency of therapy for the underlying disease (chronic hepatitis C) were elaborated.
Key words: chronic hepatitis C, antiviral therapy, interferon, depression, cluster analysis.
Хронический гепатит С (ХГС) является одним из наиболее распространенных в мире инфекционных заболеваний, вызывает тяжелые медицинские и социальные последствия (Т.М.Игнатова, 2000; S.Sockalingam, S.Abbey, 2009). Адекватная противовирусная терапия (ПВТ) ХГС включает препараты интерферона-a (ИФН-a), применение которого провоцирует возникновение психопатологической симптоматики (C.Crone и соавт., 2004; A.Shakoor и соавт., 2010; Z.Pavlović и соавт., 2011). Распространенность аффективных расстройств в период ПВТ больных ХГС варьирует в пределах от 23 до 67%, при этом наиболее часто отмечается развитие депрессивной симптоматики (А.О.Морозов, 2006; А.В.Волков, 2011; A.Valentine и соавт., 1998; C.Crone и соавт., 2004).
В настоящее время нет единого мнения по поводу частоты возникновения психических расстройств при ПВТ ХГС, их психопатологической квалификации, значимости тех или иных факторов риска. Существуют разные точки зрения относительно возможности продолжения курса ПВТ при развитии психических нарушений. Отсутствуют протоколы ПВТ больных ХГС с отягощенным психиатрическим анамнезом.
Цель исследования – комплексное клинико-психопатологическое изучение психических нарушений у больных ХГС, получающих ПВТ, определение факторов, влияющих на развитие и структуру психопатологических нарушений, сравнительная оценка психофармакотерапии различными антидепрессантами (АДП) и разработка дифференцированных рекомендаций по терапии данной категории больных.
Материалы и методы
Проведено проспективное исследование больных ХГС старше 18 лет, получавших ПВТ препаратами ИФН. Больные проходили стационарное или амбулаторное лечение в Клинике нефрологии, внутренних и профессиональных болезней им. Е.М.Тареева ГБОУ ВПО Первый МГМУ
им. И.М.Сеченова с 2003 по 2012 г. Из исследования были исключены больные с шизофренией и шизоаффективным расстройством; с тяжелой соматической патологией, приводящей к появлению дополнительной психопатологической симптоматики (в том числе цирроз печени и проявления печеночной энцефалопатии); больные, злоупотреблявшие психоактивными веществами (ПАВ), включая алкоголь, в течение 6 мес до начала ПВТ.
Для оценки состояния больных использовались клинико-психопатологический, клинико-катамнестический методы; применялись стандартизированные психометрические шкалы: шкала Монтгомери–Асберга для оценки депрессий (MADRS), шкала Бека для самооценки тяжести депрессии (BDI), шкалы оценки патологического влечения к алкоголю и наркотикам (ПВА и ПВН).
Для лечения депрессий у больных ХГС применялись АДП, различные по механизму действия и спектру психофармакологической активности: миртазапин, тианептин, миансерин, пароксетин, флувоксамин, эсциталопрам, пирлиндол, амитриптилин, кломипрамин. Терапия АДП оценивалась как эффективная, если отмечалось отчетливое клиническое улучшение состояния и редукция симптомов по шкале MADRS составляла более 50%. Оценивалась скорость уменьшения выраженности психопатологической симптоматики, отмечался факт достижения ремиссии (клинически и по психометрическим шкалам).
Анализ результатов исследования проводился с использованием методов статистической обработки, включая описательную статистику, непараметрические методы статистического анализа, в том числе медианный тест, критерий c2, методы Мак-Немара, Манна–Уитни, Вилкоксона, коэффициент ранговой корреляции Спирмена и двусторонний критерий Фишера. Для получения объективной информации о значимости исследованных показателей использовался кластерный и дисперсионный анализ. Достоверным считался уровень значимости p<0,05.
Результаты
Были обследованы 278 больных ХГС. Их клинико-демографические характеристики представлены в табл. 1.

До начала ПВТ уровень депрессии у 90% больных был ниже порогового значения для ремиссии (по субъективной и врачебной оценке; шкалы BDI и MADRS соответственно);
у 10% больных превышение порога ремиссии составляло 1–2 балла, выявлялись отдельные депрессивные симптомы, клинически не достигавшие уровня очерченного депрессивного синдрома.
После начала ПВТ у 169 (60,8%) больных ХГС развивалась депрессивная симптоматика различной степени выраженности. Манифестация клинически очерченного депрессивного эпизода приходилась преимущественно на 3–12-ю неделю терапии противовирусными препаратами. При клинико-психопатологической оценке преобладали пациенты с тяжелой и умеренной депрессией – 27 (31,8%) и 25 (29,4%) соответственно. Средний суммарный балл выраженности депрессивной симптоматики по шкале MADRS составлял 28,3±5,1. Синдромальная оценка выявленных депрессий показала преобладание тревожных (49,4%) и дисфорических (24,8%) форм. Реже встречались апатическая (10,4%), адинамическая (9,1%) и тоскливая (6,3%) депрессии (рис. 1).

Выявлено, что наиболее значимым предиктором развития депрессии при ПВТ ХГС является наличие аффективной патологии в анамнезе (до начала проведения интерферонотерапии). У больных с аффективными расстройствами в анамнезе депрессия при ПВТ ХГС развивалась значительно чаще, чем в группе больных без депрессии в анамнезе (93,4% против 48,5%). Риск развития депрессии при проведении ПВТ ХГС также был выше у больных с сопутствующей психоорганической патологией, расстройствами личности и отягощенной психопатологически наследственностью. Важным прогностическим признаком развития депрессии являлся генотип вируса: у больных ХГС с генотипом 3а чаще развивалась депрессия при ПВТ, чем у больных с генотипами 1b и 2а.
Терапия депрессивных расстройств, развивающихся при проведении ПВТ ХГС, проводилась с учетом требований к применению фармакопрепаратов в соматопсихиатрической практике. Выбор АДП и дозы препарата проводился в соответствии с синдромальной структурой депрессии, соматическим состоянием больного, возрастом, индивидуальной переносимостью, учетом рекомендаций для лечения больных с заболеваниями печени. При необходимости (для купирования бессонницы, коррекции грубых психопатоподобных и дисфорических расстройств) дополнительно назначались препараты других фармакологических групп: антипсихотики (в малых дозах с целью коррекции поведения и усиления снотворного действия АДП), антиконвульсанты, анксиолитики.
Несмотря на тяжесть депрессивных расстройств у больных ХГС, получавших ПВТ, отмечена высокая эффективность антидепрессивной терапии. У всех больных, получавших АДП, клинически отмечено улучшение психического состояния. Доля больных с 50% редукцией депрессивной симптоматики после 12 нед терапии АДП составила 78,5%. Выявлены факторы, достоверно влияющие на эффективность антидепрессивной терапии, где наиболее интересным представляется взаимосвязь большей исходной тяжести депрессии с эффективностью психофармакотерапии (табл. 2).

Купирование симптомов депрессии позволило продолжить проведение интерферонотерапии в полном объеме у большинства включенных в исследование больных. Не удалось продолжить ПВТ у 10 (5,9%) больных: у 5 больных депрессивная симптоматика являлась проявлением обострения патологического влечения к ПАВ, и причиной выхода из исследования становились отсутствие достаточного комплаенса и рецидив болезни зависимости; в 2 случаях больные отказались от продолжения ПВТ после развития тяжелой депрессии; 3 больных выбыли из программы ПВТ по причине развития тяжелых соматических осложнений интерферонотерапии.
Полученные с помощью одномерных методов статистического анализа данные о взаимосвязи различных признаков не позволяли в полном объеме оценить структуру всей совокупности клинических наблюдений. Необходимо было выделить из множества исходных данных наиболее значимые параметры, характеризующие элементы выборки, что позволило бы разработать диагностические и терапевтические алгоритмы. Значительное количество данных с высоким уровнем достоверности позволило провести дополнительный статистический анализ с использованием многомерных методов статистики.
Учитывая, что каждый клинический случай характеризовался большим количеством признаков, анализировалось наличие взаимосвязи не только между признаками, но и среди объектов наблюдения. Использование кластерного анализа дало возможность разбить всю совокупность полученных результатов на группы (кластеры) таким образом, чтобы элементы каждого кластера значимо коррелировали между собой, а представители разных групп характеризовались слабой корреляционной связью.
Для определения числа кластеров был проведен иерархический кластерный анализ с помощью различных методов объединения. При пошаговой кластеризации были выявлены 3 кластера как наиболее оптимальное число групп объектов наблюдения (клинических случаев), в которых внутригрупповое сходство между объектами больше, чем межгрупповое (рис. 2). При последующей агломерации терялась наглядность группирования. На представленной дендрограмме горизонтальная ось представляет наблюдения, вертикальная – расстояние объединения.
Учитывая полученные данные о конечном числе кластеров, был проведен кластерный анализ по методу k-средних Мак-Кина. Анализ средних значений переменных для каждого кластера позволил увидеть различия между кластерами по некоторым признакам (рис. 3). Включение в процедуру кластеризации дополнительных признаков показало, что значимость этих признаков как кластеризационных переменных является низкой.

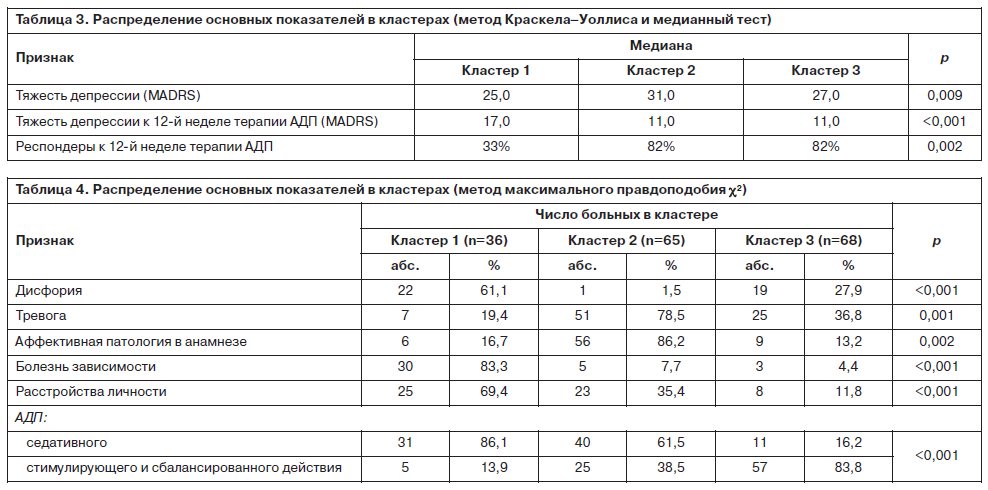
С помощью непараметрического дисперсионного анализа Краскела–Уоллиса были выявлены достоверные различия в распределении признаков в выделенных группах. Для бинарных признаков использовался логлинейный анализ – метод максимального правдоподобия c2 (табл. 3, 4).
По результатам разбиения основной совокупности наблюдений на кластеры были выявлены значимые отличия основных клинических характеристик депрессивного синдрома в группах. Проведенный далее анализ клинико-анамнестических данных и результатов психофармакотерапии позволил выделить 3 основных типа наблюдаемых при проведении ПВТ ХГС депрессивных расстройств и предложить дифференцированные схемы лечения.

В первом кластере при анализе частоты сопутствующей психической патологии было выявлено значительное преобладание пациентов с сопутствующей болезнью зависимости от ПАВ. Для этой группы были характерны преимущественно умеренные депрессии (средний балл MADRS до начала терапии АДП 26,7±4,04) с преобладанием дисфорической симптоматики. Оценка по шкалам ПВН и ПВА показала достоверное повышение при ПВТ суммарной выраженности патологического влечения к ПАВ (средний балл ПВН 1,61; ПВА 1,46) и достоверный рост значений по всем субшкалам. Наиболее высокий прирост отмечен по шкале аффективных нарушений как для больных опийной наркоманией, так и для больных алкоголизмом. Результаты анализа показали, что ИФН-индуцированная депрессия и синдром патологического влечения у больных ХГС с болезнью зависимости от ПАВ тесно связаны между собой (отмечена сильная и высокодостоверная корреляция симптоматики).
Депрессии, развивающиеся при ПВТ ХГС у больных с зависимостью, являются проявлением аффективного компонента обострения патологического влечения. Эффективность антидепрессивной терапии, несмотря на высокие дозы препаратов, была значительно ниже, чем в других кластерах. Таким больным требовались дополнительные назначения препаратов других психофармакологических групп (нейролептиков, нормотимиков) для купирования различных компонентов синдрома патологического влечения к ПАВ.
Во втором кластере превалировали больные с аффективной патологией в анамнезе (до начала ПВТ). Депрессии у таких больных рассматривались как депрессивные фазы, спровоцированные применением ИФН. Они отличались наибольшей выраженностью депрессивной симптоматики (средний балл MADRS до начала терапии АДП 32,3±4,15), с преобладанием тревожного компонента в структуре депрессивного синдрома, в то время как депрессии в анамнезе таких больных протекали преимущественно с меланхолическим аффектом. Эффективность антидепрессивной терапии в группе больных ХГС с рекуррентными депрессиями была высокая (более 75%). Уровень достижения ремиссии (суммарный балл по MADRS<12) к
12-й неделе антидепрессивной терапии в группе больных с фазным течением аффективной патологии был достоверно ниже: 51,9% по сравнению с 71,2% больных без аффективной патологии в анамнезе.
Большинство больных 3-й группы не имели сопутствующей психической патологии, т.е. у данной категории больных ПВТ являлась причиной впервые развившейся депрессии. Интервал распределения наиболее типичных показателей тяжести депрессий в 3-й группе был шире, чем в других; выраженность аффективных переживаний варьировала от легких до тяжелых (от 21 до 33 баллов по MADRS; средний балл MADRS до начала терапии АДП 26,4±3,9). С примерно равной частотой встречались тревожный и дисфорический синдромы, у меньшего числа пациентов – апатические и адинамические депрессии. Отмечена высокая эффективность антидепрессивной терапии: доля респондеров к 12-й неделе психофармакотерапии превысила 83%. В этой группе больных чаще встречались депрессии тяжелые или умеренной тяжести (более 50%), при этом редукции депрессивной симптоматики удалось добиться с применением невысоких доз АДП. Была выявлена достоверная прямая корреляция исходной тяжести депрессии и эффективности антидепрессивной терапии.
Обсуждение
Проведенное исследование выявило, что более чем у половины больных ХГС при проведении интерферонотерапии развивается депрессивная симптоматика. ИФН-индуцированные депрессии отличаются значительной выраженностью депрессивной симптоматики с преобладанием в структуре депрессивного синдрома тревоги и дисфории. И если тревожно-депрессивная симптоматика довольно часто наблюдается при соматогенных депрессиях, то значительное количество дисфорических форм говорит об особом характере именно ИФН-индуцированных депрессий. На характер депрессии оказывают влияние клинические характеристики ХГС: генотип вируса гепатита 3а является положительным предиктором развития и большей тяжести депрессий, развивающихся при ПВТ ХГС.
Учитывая высокую частоту развития и выраженность депрессий у больных ХГС, получающих ПВТ, особое значение приобретают своевременная диагностика и адекватное лечение этих расстройств, что позволяет эффективно проводить терапию основного заболевания, в том числе в полном объеме применять ПВТ. Пристальное внимание следует обращать на психическое состояние больных с такими факторами риска, как аффективная патология и злоупотребление ПАВ в анамнезе; наличие текущих психических расстройств (особенно патологии личности, в том числе органического генеза) и генотип вируса гепатита.
Выявлена неоднородность депрессий, развивающихся при ПВТ ХГС. В результате исследования схем группирования объектов наблюдения с помощью статистических методов (кластерный анализ) разработана классификационная модель. Выполненная с помощью иерархических методов процедура кластеризации позволила разбить совокупность всех объектов исследования (больных ХГС, получавших ПВТ, с депрессией) на 3 группы, достоверно отличающиеся друг от друга по набору признаков. Выявлены значимые отличия между кластерами и проведен анализ распределения клинических характеристик ХГС, психопатологической симптоматики и особенностей проводимой антидепрессивной терапии в отдельных кластерах (дисперсионный анализ).
На основе полученных данных выделено несколько типов депрессий, развивающихся при ПВТ ХГС, достоверно отличающихся друг от друга по набору признаков:
- Впервые развившиеся депрессии, индуцированные применением ИФН: для них характерны большая тяжесть депрессивных переживаний, частые жалобы на тревогу и раздражительность, высокая эффективность АДП в малых и средних дозах.
- Депрессивные фазы, индуцированные ИФН: умеренные и тяжелые депрессии с тревожным аффектом, что отличает их от депрессивных эпизодов в анамнезе, которые протекали с превалированием меланхолического аффекта. Эффективна терапия АДП седативного действия в средних и высоких дозах.
- Депрессии, развившиеся при ПВТ ХГС у больных с зависимостью от ПАВ: аффективные расстройства являются проявлением аффективного компонента патологического влечения, обострение которого провоцирует ПВТ. Психофармакотерапия таких расстройств эффективна при сочетании АДП с седативным компонентом действия с антипсихотиками и антиконвульсантами-нормотимиками.
Выводы
- ПВТ ХГС более чем у половины больных сопровождается развитием депрессий. Преобладают депрессии умеренной и тяжелой степени выраженности с тревожной и дисфорической симптоматикой. Манифестация клинически очерченного депрессивного эпизода происходит на 3–12-й неделе терапии противовирусными препаратами.
- Факторы, влияющие на частоту и психопатологическую структуру ИФН-индуцированных депрессий: сопутствующая психическая патология (аффективная патология в анамнезе, болезнь зависимости, психоорганический синдром, расстройства личности), генотип вируса гепатита С.
- Психофармакотерапия ИФН-индуцированных депрессий успешна более чем у 3/4 больных, причем положительным предиктором эффективности терапии является исходная тяжесть депрессии. На эффективность антидепрессивной терапии также влияют: гендерный фактор, сопутствующие психические расстройства, генотип вируса гепатита С, форма применяемого ИФН.
- Результаты анализа взаимосвязи структуры психопатологических проявлений и их динамики при ПВТ, эффективности антидепрессивной терапии, особенностей ХГС и его лечения позволили выделить следующие основные типы депрессивных расстройств: ИФН-индуцированные депрессии, ИФН-индуцированные депрессивные фазы в рамках рекуррентного аффективного расстройства и депрессивные расстройства у пациентов с болезнью зависимости в рамках обострения патологического влечения к ПАВ.
- Различные типы депрессий, развивающихся при ПВТ ХГС, отличаются психопатологической структурой, особенностями психофармакотерапии.
- Рекуррентное депрессивное расстройство и болезнь зависимости не являются противопоказанием для назначения ПВТ больным ХГС. Своевременная диагностика и адекватное дифференцированное лечение психических расстройств, развивающихся при ПВТ ХГС, позволяют эффективно проводить терапию основного заболевания, в полном объеме применять ПВТ.
Список исп. литературыСкрыть список1. Волков А.В. Психические нарушения у больных опийной наркоманией и алкоголизмом, развивающиеся на фоне проведения противовирусной терапии хронического гепатита С. Автореф. дис. … канд. мед. наук. М., 2011.
2. Гланц С. Медико-биологическая статистика. М.: Практика, 1999.
3. Игнатова Т.М. Хронический гепатит С: клинико-морфологическая характеристика, течение, лечение. Автореф. дис. … д-ра мед. наук. М., 2000.
4. Кендалл М., Стьюарт А. Многомерный статистический анализ и временные ряды. М.: Наука, 1976.
5. Морозов А.О. Депрессии у больных хроническим вирусным гепатитом С, получающих противовирусную терапию. Автореф. дис. … канд. мед. наук. М., 2006.
6. Crone C, Gabriel GM, Wise TN. Managing the neuropsychiatric side effects of interferon-based therapy for hepatitis C. Cleveland Clin J Med 2004; 71 (3): 27–32.
7. Loftis JM, Hauser P. Comanagement of depression and HCV treatment. Psychiat Ann 2003; 33: 385–91.
8. Mistler LA, Brunette MF, Marsh BJ et al. Hepatitis C treatment for people with severe mental illness. Psychosomat 2006; 47: 93–107.
9. Park SH. Completion of chronic hepatitis C virus treatment in interferon-induced major depressive disorder with psychotic features. Psychiat Inv 2011; 8 (4): 381–3.
10. Pavlović Z, Delić D, Marić NP et al. Depressive symptoms in patients with hepatitis C treated with pegylated interferon alpha therapy: a 24-week prospective study. Psychiat Danub 2011; 23 (4): 370–7.
11. Shakoor A, Shafqat F, Mehmud T et al. Frequency of depression and somatic symptoms in patients on interferon-a/ribavirin for chronic hepatitis C. J Ayub Med Coll Abbottabad 2010; 22 (4): 6–9.
12. Sockalingam S, Abbey SE. Managing depression during hepatitis C treatment. Can J Psychiat 2009; 54 (9): 614–25.
13. Valentine AD, Meyers CA, Kling MA et al. Mood and cognitive side effects of interferon-a therapy. Semin Oncol 1998; 25: 39–47.
1 мая 2013
Количество просмотров: 3867
