Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№03 2013
Взаимоотношения «ген-среда» при психических расстройствах: трансляция прогресса нейронаук в персонифицированную медицину №03 2013
Номера страниц в выпуске:53-61
Противоречия между доказательной и персонифицированной медициной являются предметом широких дискуссий [1]. Потенциалом к достижению компромисса между этими двумя направлениями обладают исследования в области нейронаук ввиду того, что они на доказательном уровне предоставляют более тонкий по сравнению с традиционными клиническими исследованиями подход, учитывающий состояние отдельного пациента, особенности его заболевания, генетической предиспозиции, факторов, сопутствующих развитию, состояние биологических систем организма, стрессовые факторы и условия окружающей среды.
Резюме. Данная статья является одной из серии публикаций, посвященных материалам 21-го конгресса Европейской ассоциации психиатров, прошедшего 6–9 апреля 2013 г. в г. Ницце (Франция). Приведен обзор наиболее важных сообщений, посвященных последним достижениям в области понимания взаимоотношений «ген–среда» при психических расстройствах и их значения с позиций трансляционной психиатрии и персонифицированной медицины.
Ключевые слова: взаимоотношения «ген–среда», депрессия, тревожные расстройства, шизофрения, конгресс EPA.
Gene-Environment interactions in psychiatric disorders: translation of neuroscientific developments into personalized medicine
T.S.Syunyakov
FSBI Zakusov Institute of Pharmacology RAMS, Moscow
Summary. This paper is the one of the series of papers dedicated to materials, presented at the 21st Congress of the European Psychiatric Association that took place in the Nice (France). Here we discuss major communications on the neuroscientific developments in the field of gene-environment interactions in psychiatric disorders and their application to the translational psychiatry and personalized medicine.
Key words: gene-environment interaction, depression, anxiety disorders, schizophrenia, EPA congress.
Противоречия между доказательной и персонифицированной медициной являются предметом широких дискуссий [1]. Потенциалом к достижению компромисса между этими двумя направлениями обладают исследования в области нейронаук ввиду того, что они на доказательном уровне предоставляют более тонкий по сравнению с традиционными клиническими исследованиями подход, учитывающий состояние отдельного пациента, особенности его заболевания, генетической предиспозиции, факторов, сопутствующих развитию, состояние биологических систем организма, стрессовые факторы и условия окружающей среды. Обсуждение этих вопросов стало одной из основных тем конгресса, а ключевое место при их освещении заняла проходившая 7 апреля теоретическая лекция профессора Джулио Лицинио (Julio Licinio) из Южноавстралийского исследовательского института здоровья и медицины (Аделаида, Австралия) «От взаимодействий между генетическими и средовыми факторами к терапии и профилактике», отразившая результаты многолетних работ и наметившая дальнейшие перспективы исследований.
В самом начале своего сообщения Джулио Лицинио указал, что экономическое бремя психических расстройств очень велико (800 млрд евро в год для стран Европы), а для фармакологических компаний рынок психотропных препаратов является крайне прибыльным (с оборотом около 80,5 млрд дол. только в США). Однако парадокс заключается в том, что прагматичные фармакологические компании закрывают подразделения, занимающиеся разработкой психотропных лекарственных препаратов. Комментируя данную проблему, докладчик отметил, что прежде всего это связано с трудностями, возникающими «при наведении мостов между фундаментальной наукой и клиническими дисциплинами», т.е. перед трансляционными нейронауками. Наиболее красноречивой иллюстрацией данного тезиса является тот факт, что на сегодняшний день наиболее широко используемые антидепрессанты опираются на механизмы, выявленные 60 лет назад Джулиусом Аксельродом, а открытия позднего периода практически не были внедрены в практическую сферу. Это связано с тем, что осуществление всего комплекса процесса трансляции (научная идея или открытие → апробирование на людях → проведение клинических исследований → внедрение их результатов в руководства и политику здравоохранения → отслеживание долгосрочных эффектов, позитивных и негативных → распространение новых данных по миру → окончательное понимание значимости открытия для глобального здравоохранения) является затратным по ресурсам и времени. В этой связи профессор Лицинио предлагает фокусировать усилия на устранении пробелов между научной гипотезой, доказательными данными и эмпирическими свидетельствами. Таких слабых мест, по мнению докладчика, имеется три. Во-первых, может возникнуть расхождение на уровне знаний, когда эмпирические наблюдения не имеют под собой ни доказательной базы, ни гипотезы, и в этом случае необходимо направить усилия на поиск лежащих в основе эмпирических наблюдений причин и механизмов. Во-вторых, может наблюдаться ситуация, когда пробел между имеющимися эмпирическими данными и научной гипотезой заключается в отсутствии доказательной базы, и данный пробел должен быть устранен путем повышения «транслируемости» научных данных. В-третьих, эмпирический опыт может не соответствовать ожиданиям, основанным на научном открытии, подтвержденном на доказательном уровне. Рациональным объяснением подобного рода разногласий может служить несоблюдение рекомендаций. Решением данной проблемы может быть только приведение действий и поведения больных и врачей в соответствие рекомендациям. Кроме того, по ходу доклада подчеркивается значимость правильного выбора объекта и методологии исследований для более эффективного переноса научных данных в практическую деятельность.
В качестве иллюстрации автор привлек результаты собственных исследований депрессий и ожирения – двух широко распространенных расстройств, имеющих сложные причины. Предпосылками для рассмотрения этих патологических состояний в одной связке явились также примерно одинаковая распространенность (порядка 25%) ожирения и аффективных/тревожных (родственных генетической основой, механизмами и терапией) расстройств и их частое сосуществование. Оба заболевания обусловлены генетическими механизмами и средовыми влияниями (стрессами). Они взаимно повышают риск возникновения друг друга, имеют пересекающийся круг осложнений и коморбидных состояний. При депрессивных расстройствах нарушается функционирование основных органов и систем, что наряду с суицидальным поведением является причиной высокой смертности при данном расстройстве. Так, большое депрессивное расстройство в 2 раза повышает риск ишемической болезни сердца и на 60% вероятность возникновения сахарного диабета 2-го типа, которые также являются осложнениями ожирения. Депрессивным нарушениям в долгосрочной перспективе часто сопутствуют кардиометаболические расстройства и увеличение веса,
а при сосуществовании депрессивных нарушений и сахарного диабета увеличение веса даже на 5 кг в 1,5 раза увеличивает риск возникновения ишемической болезни сердца. Следует также отметить, что предпосылками фактически начавшейся эпидемии ожирения считаются снижение физической активности и повышенное потребление пищи, которые часто встречаются при депрессивных состояниях. Важно, что некоторые нейропептидные и нейротрансмиттерные системы, в том числе кортиколиберин (CRHR1), нейропептид Y (NPY), серотонин и норадреналин, вовлечены в контроль и настроения, и веса тела. При этом препараты, применяемые при лечении ожирения (механизм их действия заключается во влиянии на содержание серотонина и норадреналина в центральной нервной системе – ЦНС), часто приводят к формированию пониженного настроения, а терапия депрессивных расстройств осуществляется антидепрессантами (главным образом влияющими на обратный захват серотонина и норадреналина), которые часто способствуют увеличению веса в долгосрочной перспективе, а также повышают риск сахарного диабета, независимо от исходного индекса массы тела. В свою очередь с увеличением веса также связан повышенный риск и других болезней, в частности онкологических (на 60%). На актуальность изучения данной проблемы также указывает то, что все указанные последствия в клинической практике недооцениваются и должным образом не лечатся. Таким образом, депрессия и ожирение значительно больше связаны друг с другом, чем представлялось раньше. При этом существуют биологические системы, значение которых для этих двух заболеваний не вполне ясно, – это нейропептиды стресса, медиаторы иммунитета, адипокины и нейрокины. И хотя постановка данной проблемы отнюдь не заслуга последних достижений, новые науки (фармакогеномика и геномика) позволяют взглянуть на нее с иной стороны.
В связи со всеми указанными фактами представляются правомерными следующие вопросы. Совпадение ли это или следствие общих биологических механизмов? Каков характер взаимоотношений между депрессией и ожирением и каково место стрессовой системы в этих взаимоотношениях? Любое ли из этих состояний может являться отправной точкой для других? Какие взаимодействия возникают у людей, склонных к ожирению, на фоне приема антидепрессантов? Отличается ли ожирение в контексте приема антидепрессантов от ожирения вследствие нарушений энергетического обмена?
Пытаясь ответить на часть поставленных вопросов, Джулио Лицинио продемонстрировал результаты эксперимента, направленного на выявление взаимодействий между стрессом, средовыми и фармакологическими факторами [2]. В рамках этого исследования крыс подвергали воздействию краткосрочного (на протяжении 1 нед) стрессового воздействия (ограничение активности). При этом части животных в этот период давали антидепрессанты, а части – вводили физиологический раствор. После завершения данного этапа животным в течение длительного времени давалась пища, обогащенная жирами. Оказалось, что животные, которым назначались антидепрессанты, не только компенсировали снизившийся на фоне стресса вес, но и прибавили в весе значительно больше, чем крысы из контрольной группы. Таким образом, даже краткосрочный прием антидепрессантов вызывает длительно существующую сенситизацию к повышению веса. При этом антидепрессанты в условиях стрессового воздействия оказывали на животных и благоприятное («антидепрессивное») действие. Оказалось, что у животных опытной группы повышена экспрессия ряда факторов роста: мозгового нейротрофного фактора (BDNF), фактора роста нервов (NGF) и, что важнее всего, инсулиноподобного фактора роста
(IGF-1), который и мог обусловить увеличение веса животных. Таким образом, данный эксперимент (парадигма «стресс–диета–антидепрессанты»), с одной стороны, продемонстрировал влияние даже краткосрочного приема антидепрессантов на вес (и это при том, что антидепрессанты занимают в мире 2-е место по продажам, а многие больные принимают их бесконтрольно). С другой стороны, показана важность стрессовой реакции – координированного ответа нейроэндокринной системы на неблагоприятные внешние или внутренние факторы – повышение веса в долгосрочном периоде.
В патогенезе ожирения играют роль взаимодействия генетической предрасположенности и средовых факторов (обнаружена взаимосвязь ожирения с доступностью пищи, снижением физической активности, инфекционными заболеваниями, возрастом матери, высокой плодовитостью и ассортативностью браков, содержанием в окружающей среде химических веществ, вызывающих эндокринные расстройства, малыми перепадами температуры окружающей среды, внутриутробными факторами, приемом препаратов). Таким образом, складывается континуум в ряду влияния на вес внешних и генетических факторов:
у части людей большую роль играют алиментарные факторы, у части – повышенное потребление пищи возникает в связи со стрессами и эмоциональными проблемами, а еще одна часть людей страдает избытком веса в связи с генетической предрасположенностью. При этом при ожирении в отличие от депрессии генетический фактор может играть колоссальную роль. Несмотря на то что контроль веса тела также вовлекает множество генетически детерминированных систем (моноамины, нейропептид Y, гормоны и прогормоны гипоталамуса и гипофиза, галанин, орехины, холецистокинин, бомбезин), настоящим прорывом в области знаний об ожирении является выявление роли лептина при данной патологии. Лептин является передаточным звеном между жировой тканью и головным мозгом, а исследования магнитно-резонансной томографии показали, что лептин регулирует активность островковой зоны головного мозга в ответ на предоставление пищи [3]1. Видимо, при ожирении играет роль также другой нейропептид – грелин, который вызывает активацию в тех же областях, что и лептин2. Однако похоже, что влияния содержания грелина и лептина на повышение аппетита находятся в реципрокных взаимоотношениях [4]. Также автор приводит данные собственных исследований, показавших, что терапия лептином при тяжелых семейных формах ожирения, при которых выявляются дефекты гена, кодирующего лептин приводит к драматическому снижению веса, появлению контроля за приемом пищи и увеличению продолжительности жизни [5].
Переходя к следующей части доклада, профессор Лицинио указал, что сложность анализа депрессивных расстройств с позиций взаимодействия генетических и средовых факторов заключается в разнообразии фенотипических проявлений, которые могут различаться по течению, его этапу, периодичности, синдромальной картине, тяжести, причинам и времени возникновения в течение жизни. И это поднимает вопрос о нозологическом единстве депрессивных нарушений. Является ли депрессивный фенотип проявлением эквифинальности разных патогенетических процессов, какие причины лежат в основе болезни и сколько их, могут ли они быть связаны со специфическим генетическим фактором или с влиянием на генетическую уязвимость других факторов, не являющимися причинными, насколько состояние обусловлено несколькими большими генетическими факторами, а на сколько – множеством генетических факторов с небольшим эффектом, какова роль внешней среды, особенностей развития и эпигенетических факторов?
Депрессивные расстройства являются следствием сложной констелляции генетических и средовых факторов (пренатальных стрессов, стрессов, связанных с потерями близких, горем, лишениями, естественными катастрофами, войной, а также с социальным окружением и поддержкой, питанием, заболеваниями и применяемыми препаратами). При этом давно известно, что депрессивные расстройства носят полигенный характер и не выделено какого-либо одного генетического фактора, который бы по значимости для патогенеза намного превосходил другие.
В этих условиях Джулио Лицинио предлагает для оптимальной оценки взаимоотношений между генетическими и средовыми факторами проводить систематическую оценку социальных и средовых влияний (особенно в перинатальном периоде) и тщательно изучать состояние биологических систем-кандидатов на хорошо охарактеризованных группах больных, а поиск новых механизмов, с его точки зрения, должен осуществляться без оглядки на предварительно сформулированные концепции, которые могут внести искажение при интерпретации новых данных. Докладчик указывает, что одним из наиболее жестко детерминированных фенотипов при рассмотрении депрессий является терапевтический ответ на антидепрессивную терапию, в связи с чем он наилучшим образом подходит для оценки взаимоотношений между генетикой и внешней средой. И уже с учетом разделения депрессивных фенотипов по наличию или отсутствию антидепрессивного ответа должны осуществляться оценка генотипа, рассмотрение вовлеченных систем-кандидатов (как специфических, так и выявляемых на всех этапах патогенетических путей с использованием биоинформационного подхода по поиску однонуклеотидных полиморфизмов), поиск новых мишеней (на основе данных по экспрессии генов, с последующим генным или полногеномным секвенированием, генотипированием экзома – совокупности несущих информацию участков генов), оценка применимости этих данных в практической сфере.
Учитывая, что в патогенезе как депрессивных расстройств, так и ожирения существенная роль принадлежит стрессовой системе3 как системе, опосредующей взаимосвязь между средовыми и генетическими факторами, и основываясь на позитивном опыте выявления связи между терапевтическим ответом и вариантами генов, кодирующих рецепторы к кортиколиберину при бронхиальной астме, Лицинио предположил, что такого рода взаимосвязи могут быть выявлены и при депрессивных расстройствах [6]. В исследование, направленное на тестирование данной гипотезы, вошли 80 пациентов с депрессивными расстройствами (американские мексиканцы). У больных были генотипированы гаплотипы CRHR1 и выявлены их частоты и варианты. Оказалось, что гаплотип-1 (GAG-гаплотип для вариантов rs1876828, rs242939 и rs242941) встречался у большинства (63%) больных, однако у некоторых он находился в гомозиготном, а у некоторых в гетерозиготном состоянии. Оказалось, что у больных с высокими степенями тревоги на фоне депрессии, у которых гаплотип-1 находился в гомозиготном состоянии, терапевтический ответ на флуоксетин и дезипрамин (а для этих препаратов получены данные об их влиянии на кортиколиберин) был достоверно более выраженным. Данный пример является показательным, и с использованием данного подхода (с поэтапным смещением акцента исследований от патогенеза через однонуклеотидный полиморфизм к гаплотипам и геному) группой Лицинио было выявлено 1500 однонуклеотидных полиморфизмов в генах, имеющих значение для терапевтического ответа на антидепрессанты.
Принимая во внимание, что стрессовый ответ в целом и кортиколиберин в частности отчетливо связаны с иммунным ответом, состояние иммунной системы, цитокинов и нейрокинов является другой потенциальной мишенью для изучения взаимодействия генетических и средовых факторов при депрессиях. Автор отметил значительные сходства между течением аутоиммунных заболеваний и депрессий в контексте вариантов течения – хронического, периодического с усилением и послаблением симптоматики, эпизодического. Кроме того, применение цитокинов в качестве терапевтических средств приводит к возникновению депрессивных расстройств. Все это указывает на возможность участия дисфункции медиаторов иммунитета при депрессии (при этом данная дисфункция может быть первичной, генетически-детерминированной, либо вторичной, вследствие инфекционных заболеваний или стрессовых воздействий).
Рассматривая цитокиновую теорию депрессии с позиций молекулярной биологии, экспериментальных моделей, клинических, генетических и фармакогенетических исследований, Лицинио сформулировал рабочую гипотезу о том, что нейрокины являются синтезируемыми в головном мозге цитокинами, однако их регуляция в головном мозге отличается от их регуляции на периферии; нейрокины участвуют в биологии настроения, когнитивных функций и поведения; регулирование нейрокинов в головном мозге необязательно требует присутствия инфекционных агентов или аутоиммунного процесса. В поддержку высказанной гипотезы профессор Лицинио привел данные, полученные на той же группе американских мексиканцев. В этом исследовании [7] была продемонстрирована взаимосвязь между большим депрессивным расстройством и полиморфизмом генов PSMB4 (b4-субъединица протеосомы, играющая роль в презентации антигена) и TBX21 (кодирует одноименный белок, играющий роль в пролиферации Т-лимфоцитов). При этом на долю их полиморфизмов rs2296840 и rs17244587, соответственно, приходится 47,8% риска, а их объединенный эффект (взаимодействие «ген–ген») на 26% выше, чем можно было бы ожидать от простого суммирования рисков. Анализ показал, что у лиц, имеющих 1, 2 и 3 аллели этих вариантов генов, риск депрессивных расстройств возрастает в 2,3, 3,2 и 9,8 раза, что свидетельствует о значительном эффекте дозы генов. Представляет интерес также то, что экспрессия гена цитокина CXCL10/IP-10 при депрессии повышена, а при реализации антидепрессивного эффекта снижается. Кроме того, выявлена ассоциация и других факторов, указывающих на роль Т-клеточного иммунитета (CD3E, PRKCH, PSMD9, STAT3) и функций гипоталамо-гипофизарно-надпочечниковой системы (UCN3) при реализации антидепрессивного ответа. Эти результаты согласуются с данными о преобладании при депрессии Т-хелперной активности 1-го (провоспалительного) типа над активностью 2-го (противовоспалительного) типа. Также была подтверждена роль интерлейкина-6 в механизмах депрессий. Эти данные были подтверждены в другом исследовании – при угнетении Т-ростка иммунитета животные демонстрировали повышенную устойчивость в тестах на формирование депрессивного поведения [8].
Следуя намеченной последовательности изучения, Джулио Лицинио приводит результаты секвенирования генов на всех этапах реализации эффектов антидепрессантов (начиная от печеночного метаболизма, способности проникать через гематоэнцефалический барьер, взаимодействовать с первичными рецепторами, влиять на внутриклеточные мишени с отслеживанием дальнейшего каскада изменений) флуоксетина и дезипрамина с целью выявления ассоциированных с депрессией однонуклеотидных полиморфизмов. При этом только в отношении мозгового нейротрофного фактора (BDNF) было выявлено 47 ранее идентифицированных и 83 новых однонуклеотидных полиморфизмов [9]. В отношении других звеньев в цепи реализации механизмов терапевтического ответа (транспортеры серотонина, норадреналина, дофамина, ген CREB1, ген рецепторов к CRH и BDNF) выявлено 419 однонуклеотидных полиморфизмов, ассоциирующихся с ответом на антидепрессанты [10]. Таким образом, существует множество свидетельств того, что терапевтический ответ на антидепрессивную терапию во многом детерминирован генетически.
Под конец данного фрагмента своего сообщения докладчик анонсировал, что с появлением новых технологических решений стали возможными исследования экзома, которые в настоящее время проводятся его научной группой. Кроме того, он очертил будущие направления исследований и сформулировал новый подход: поиск новых генов-кандидатов, бинарная оценка их значимости для определенной патологии с последующей их группировкой при помощи древовидного анализа в соответствии с местом, занимаемым в патогенезе, и выяснением суммарного вклада того или иного пути в предрасположенность к болезни.
Таким образом, в данном разделе доклада было продемонстрировано успешное использование нового подхода на примере выявления факторов, в том числе опосредующих взаимодействие генетических и средовых влияний, через систему стресса и связанных с ней функций иммунитета, ассоциирующихся с риском депрессивных расстройств и фармакологическим ответом на антидепрессанты.
Таким образом, если сделать вывод из всего сказанного профессором Лицинио, то необходимо отметить, что на сегодняшний день существуют значительные пробелы между результатами нейронаучных исследований и клинической практикой, однако появление новых технологических решений и предлагаемые автором методология и новые подходы к изучению данного вопроса могут позволить их решить. В этом направлении уже сделаны существенные шаги. На примере взаимоотношений двух тесно связанных друг с другом заболеваний – депрессии и ожирения – получены новые данные об их генетической природе, участии генов, имеющих «большое» и «малое» значение», открыты многочисленные новые однонуклеотидные полиморфизмы, имеющие функциональное значение. На примере парадигмы «стресс–диета–ожирение» продемонстрировано взаимодействие патологического процесса, внешних средовых факторов и фактора применения антидепрессантов, которые в сочетании запускают внутренние механизмы, приводящие к повышению веса, показана опасность бесконтрольного применения антидепрессантов. Выявлены дополнительные доказательства генетической детерминированности антидепрессивного ответа и роли состояния иммунной системы в генезе и терапии депрессивных нарушений. С учетом новых разработок вновь осуществляется активное изучение роли стрессовой системы и системы иммунитета как ее части в формировании комплексных расстройств, при которых велико значение и генетических, и средовых факторов.
Переходя от общих вопросов к более частным, логическим продолжением доклада Джулио Лицинио явилась исследовательская сессия «Краткосрочные и долгосрочные эффекты иммунного стресса в пренатальном и перинатальном периоде: от основ к клинике», проводившейся под председательством Ай Му Минт (Aye Mu Myint) из Университетской клиники г. Мюнхена (Германия) ввиду отсутствия профессора Маркуса Шварца (Marcus Schwarz). Как следует из названия сессии, здесь изучались нейроиммунологические гипотезы разных психических расстройств: депрессий и шизофрении, и в том числе послеродовых депрессий и психозов. В этой связи не лишним будет еще раз указать на тесные взаимоотношения между иммунной и нейроэндокринной системой в ответе на стресс, определяющие реактивность организма к внешним факторам, а также вспомнить, что некоторые авторы рассматривают иммунную систему вообще в качестве шестого «некогнитивного» органа чувств [11], а в соответствии с цитокиновой гипотезой Брайана Леонарда активация иммунитета играет важную роль в патогенезе депрессивных расстройств [12].
Среди представленных на сессии четырех докладов наибольший интерес представляли два экспериментальных исследования, в которых данные гипотезы рассматривались с позиций роли нарушений нормального развития головного мозга в генезе депрессивных нарушений и шизофрении и с точки зрения взаимодействия «гены–среда». Предпосылками к проведению этих работ послужили данные литературы о том, что инфекционные заболевания, возникающие у матери в ходе беременности, могут влиять на ход развития головного мозга у потомства ввиду облегченного проникновения медиаторов воспаления через несформированный гематоэнцефалический барьер, последующей активации микроглии, в том числе перекисного окисления; это приводит к истощению запасов ионов железа и цинка, составляющих активные центры многих ферментов, участвующих в окислительно-восстановительных процессах, что способствует к изменению траектории развития ЦНС, формируя дополнительную уязвимость (наряду с генетической) к психическим заболеваниям. Наряду с этим пренатальное воспаление запускает патологическую сенсибилизацию микроглии и астроцитов, что по времени совпадает с возникновением первых нарушений (мягких неврологических знаков и психомоторного дефицита). Сенсибилизированные клетки глии либо сами по себе, либо после дополнительной активации средовыми стрессорами в постнатальном периоде запускают воспалительные процессы в развивающемся головном мозге, вызывая нарастание патологических изменений, способствуя таким образом манифестации заболевания (рис. 1) [13].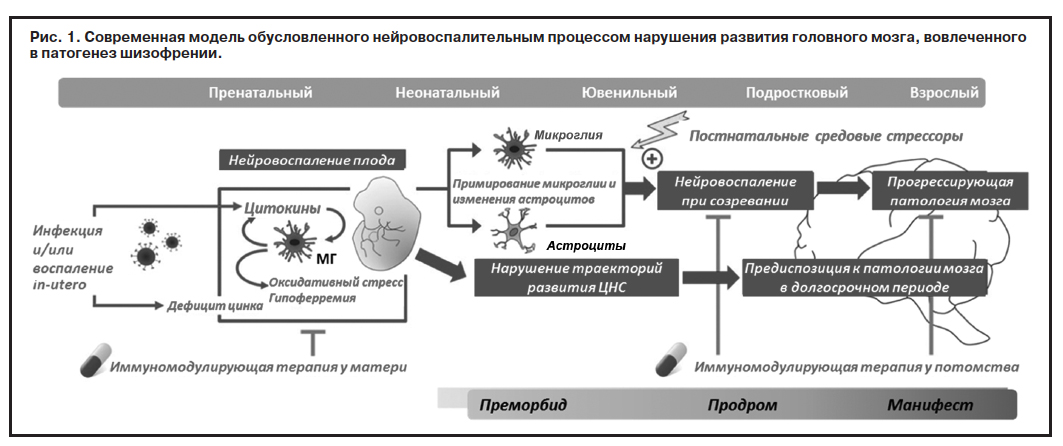
Для оценки влияния пренатального иммунного стресса на предрасположенность к психическим заболеваниям
(в первую очередь шизофрении) предложена экспериментальная модель с использованием иммунологической провокации [14]. Ее суть заключается в том, что самкам мышей, находящимся на разных сроках беременности, вводились антигены, провоцировавшие иммунный ответ при отсутствии инфекционного возбудителя. Затем у потомства при использовании валидных методик регистрировались поведенческие нарушения. При этом, на основании литературных данных, иммунная провокация вирусным антигеном, полирибоинозиловой-полирибоцитозиновой кислотой (PolyL:C – синтетический аналог двуцепочечной ДНК) в отличие от липополисахарида4 (бактериального антигена) и интерлейкина-6 (провоспалительного цитокина, хронически повышенные уровни которого вызывают нейродегенерацию) приводила к возникновению у потомства широкого круга поведенческих расстройств и изменений, характерных для шизофрении. В частности, у них отмечалось снижение преимпульсного и латентного торможения5, социального поведения, исследовательской активности, рабочей памяти, а также повышение чувствительности к агонистам дофаминовых и NMDA-рецепторов. Кроме того, валидность данного моделирования шизофрении с точки зрения патологии развития подтверждает также время возникновения поведенческих расстройств у мышей, соответствующее раннему зрелому возрасту (т.е. возрасту, характерному для манифестации шизофрении), и то, что они купировались применением антипсихотиков [15]. В экспериментальных исследованиях было показано, что при такого рода моделировании роль играет время проведения провокации: в частности, угнетение преимпульсного торможения у потомства наблюдалось при введении PolyL:C на 9-й день беременности, но не на 17-й день [16].
Следует отметить, что такое достаточно полноценное моделирование особенностей шизофрении на первый взгляд идет вразрез с расчетами об относительно малом вкладе вирусных инфекций в этиологию шизофрении. Однако в работе M.Clarke и соавт. (2009 г.) [17] приводятся сведения о том, что влияние пренатальных инфекций у лиц с наследственным отягощением психотическими расстройствами в 4 раза больше в сравнении с лицами, не имеющими отягощения, что отчетливо указывает на взаимодействие инфекционных заболеваний с генетической предрасположенностью. Данное положение было подтверждено в некоторых работах. В частности, у мышей с мутантной аллелью гена mhDISC1 (mutant human disrupted-in-schizophrenia-1) пренатальная иммунная стимуляция приводила к повышенной тревожности, «депрессивному» поведению, нарушениям «социального поведения», снижению стресс-реактивности, а также ассоциировалась с рядом структурных изменений головного мозга [18]. Синергичное усиление дофаминергических нарушений наблюдалось и при комбинировании модели с гетерозиготной делецией гена Nurr1 (генетический фактор) с моделью PolyL:C-провокации (средовой фактор) [19].
В своей работе Сандра Джованьоли (Sandra Giovanoli, Цюрих, Швейцария) предлагает нам использовать модель «двойного удара» средовых факторов: после проведения иммунной вирусной провокации PolyL:C на 9-й день беременности («первый удар») на 30–40-е дни жизни потомство (опытная группа) подвергали ряду субхронических стрессовых воздействий («второй удар»: удары электрическим током по лапам, ограничение активности, плавательный стресс, животным не давали пить, повторно меняли клетки). Через 1 мес после завершения «второго удара» у животных отслеживались отдаленные эффекты. Оказалось, что животные опытной группы, подвергавшиеся стрессу (POL и S+), демонстрировали повышенную тревожность (рис. 2, а), угнетение препульсового торможения (рис. 2, б), а также повышенную чувствительность к агонистам дофаминовых рецепторов и антагонистам глутаматергических NMDA-рецепторов (рис. 2, в и 2, г соответственно) в сравнении с потомством животных, у которых не проводилось иммунологической провокации, (контрольная группа: CON, S+ и S-) и с животными опытной группы, не подвергавшимися стрессовым воздействиям в пубертатном возрасте (POL и S-). При изучении нейрохимических изменений выявлялось увеличение содержания дофамина в прилежащем ядре (обусловленное иммунной провокацией) и гиппокампе (как результат взаимодействия двух средовых влияний).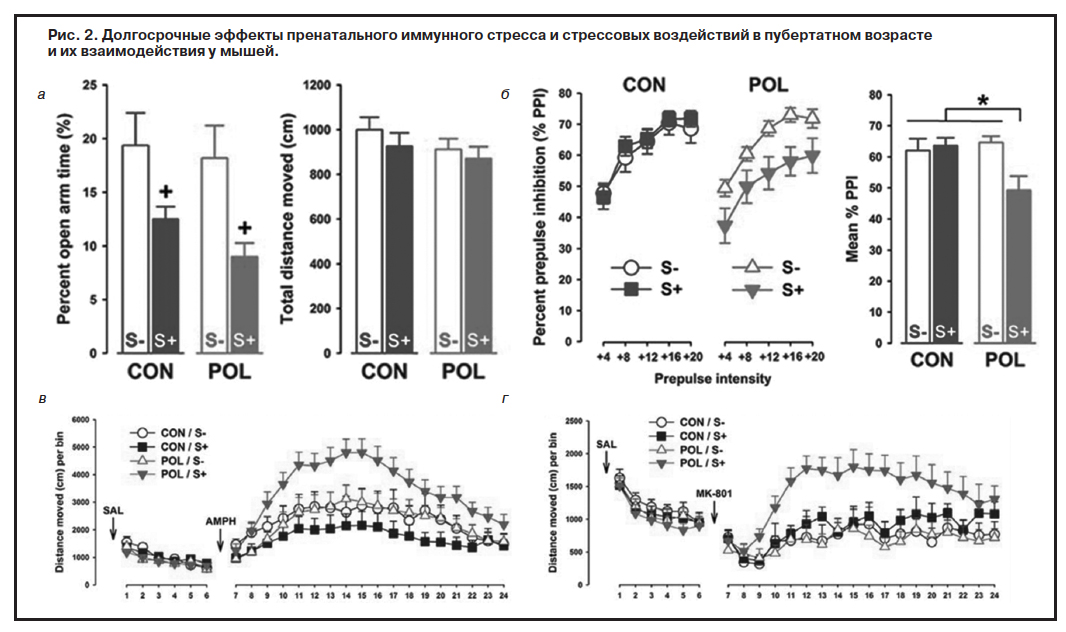
Ай Мю Минт представила результаты своего исследования, в котором она, используя модель пренатальной иммунной провокации на более поздних сроках гестации (17-й день) с липополисахаридным (бактериальным) антигеном, смоделировала нарушения нормального развития головного мозга при депрессивных расстройствах. На 13-й неделе жизни у мышей из экспериментальной группы выявлялось «депрессивное» поведение при проведении теста с принудительным плаванием, выражающееся в достоверном увеличении частоты и продолжительности периодов прекращения двигательной активности и зависаний в воде. Наряду с этим наблюдалось усиление процессов эпигенетических изменений в тканях головного мозга, что выражалось в снижении активности гистон-деацетилазы и повышении активности ДНК-метилтрансферазы, а также изменении экспрессии генов, определяющих соотношение нейротоксических (гены Cideb, Txnip, Drd2, Nostrin, Tacr1) и нейропротективных (Nrg1, Ngrf, Il1r1) процессов, в сторону увеличения первых и снижения вторых, что может свидетельствовать об участии данного механизма в формировании депрессивных расстройств.
Таким образом, в этих двух сообщениях был представлен обзор научных работ, демонстрирующих роль пренатального воспаления в формировании уязвимости к таким заболеваниям, как шизофрения и депрессивное расстройство, для которых в последние годы была показана, с одной стороны, тесная связь с состоянием иммунной системы, а с другой – с нарушением нормального процесса развития головного мозга. Эти данные легли в основу создания экспериментальной модели пренатальной иммунной провокации, обладающей превосходной конструктивной валидностью в отношении шизофрении и в некоторой степени депрессивного расстройства, которая позволяет объяснить не только особенности клинической картины и течения заболеваний, но и особенности их формирования в условиях сложного взаимодействия генетической предрасположенности и внешних воздействий (иммунологических и стрессовых). Более того, работы, выполняемые в этом направлении, открывают широкие перспективы как для дальнейшего изучения природы психических расстройств, так и для создания принципиально новых подходов к их терапии и профилактике.
Конечно же, не могли обойти стороной проблему взаимодействия генетических и средовых факторов и на сателлитном симпозиуме компании Pfizer «Генерализованное тревожное расстройство: почему люди беспокоятся?», проводимом под председательством профессора Кристера Аллгуландера (Christer Allgulander) из Каролинского института в Швеции. Доклад «Патологическая генетика тревоги» в блестящей манере представила молодая профессор Катарина Домшке (Katharina Domshke) из Университетской психосоматической и психотерапевтической клиники г. Вюрцберга (Германия).
Свой доклад Катарина Домшке начала с указания того, что, как и при многих других психических заболеваниях, в этиологии тревожных расстройств значение имеют и биологические, и средовые факторы. При этом среди биологических ключевое место занимают генетические. Об этом свидетельствуют результаты семейно-генетических исследований, выявивших 1,5–3-кратное увеличение риска тревожных расстройств у родственников 1-й степени родства больных [20], что приводит к накоплению в подверженных семьях случаев тревожных расстройств, указывая на их генетическую обусловленность. Однако эти результаты не снимают всех вопросов о наследственной основе, поскольку в семьях «наследуется» не только генетический материал, но и «атмосфера». Близнецовые исследования, позволяющие исключить данные влияния, свидетельствуют, что конкордантность в случае генерализованного тревожного расстройства (ГТР) составляет 20–40%, при паническом расстройстве она достигает 48%, а в отношении одновременного возникновения обоих заболеваний – 23% [21, 22]. Кроме того, у ГТР имеется общая генетическая основа с большим депрессивным расстройством. О чем же могут говорить эти цифры? С одной стороны, они подводят черту под доказательствами наследуемости тревожных расстройств, с другой – свидетельствуют, что в 50–80% случаев роль в возникновении тревожных расстройств играют внешние, негенетические факторы, а также указывают на значимость взаимоотношений «ген–среда».
Однако ни семейно-генетические, ни близнецовые исследования не решают вопросов о том, какие гены играют ключевую роль в предрасположении. К ним адресованы молекулярно-генетические исследования, анализ сцепленных генов и изучение генетических ассоциаций. В этих исследованиях были выявлены общие для спектра тревожных расстройств (паническое расстройство, ГТР и тревожная депрессия) гены риска, и прежде всего это гены серотонинового 5-HT1A-рецептора – транспортера серотонина и моноаминоксидазы типа А (МАО-А), вовлеченной в метаболизм серотонина и норадреналина, подтверждая таким образом на генном уровне нейрохимические гипотезы о вовлечении серотонинергической и норадренергической систем нейропередачи в генез тревожных расстройств. Однако за последнее десятилетие открыт ряд новых генов-кандидатов, вовлеченных в контроль тревоги: ген рецептора к нейропептиду S (NPS), нейропептид Y (NPY), ген небольшого пептида RGS2, участвующего в качестве сигнальной молекулы в каскадах основных нейротрансмиттерных систем6. Хочется отметить, что в докладе было приведено лишь незначительное число из рассматриваемых в настоящее время генов-кандидатов. В 2011 г. в журнале Translational Psychiatry была опубликована экспериментальная работа, показавшая, что с тревожными состояниями ассоциировано порядка нескольких сотен генов [23].
Переходя к анализу взаимоотношений генетических и средовых факторов, профессор Домшке ссылается на исследование, изучавшее влияние полиморфизма гена NPY (NPY 399C/T) на возникновение тревожных расстройств среди жертв урагана [24]. Носители гомозиготной аллели NPY 399C/С имели наибольшую подверженность по сравнению с носителями С/Т- и T/T-аллели, причем в сравнении с гомозиготами по T-варианту гена риск тревожных расстройств возрастал в 8 раз.
Этиологическую мозаику тревожных расстройств осложняют эпигенетические влияния: процессы метилирования ДНК и ацетилирования гистонов. Суть этих явлений заключается в следующем: ацетилирование гистонов вызывает активацию процессов транскрипции на определенном участке ДНК, который может содержать патологический ген, а при соединении метильной группы с промотором гена, наоборот, происходит «выключение» гена. Особенностью подобных эпигенетических процессов является их существенная нестабильность и динамичность. Таким образом, даже наличие генетического предрасположения может не проявляться в случае, например, если экспрессия патологических генов не осуществляется ввиду их инактивации. Однако процессы метилирования/деметилирования обратимы, что привело к возникновению гипотезы об индукции эпигенетических процессов стрессорами. И эта гипотеза получила подтверждение. Так, у больных с паническим расстройством отмечается недостаточное метилирование гена МАО-А, причем было показано, что негативно окрашенные события в течение года, предшествовавшего возникновению заболевания, вызывали усиление процессов деметилирования гена МАО-А, тогда как позитивные события вызывали его метилирование (инактивацию) (рис. 3) [25].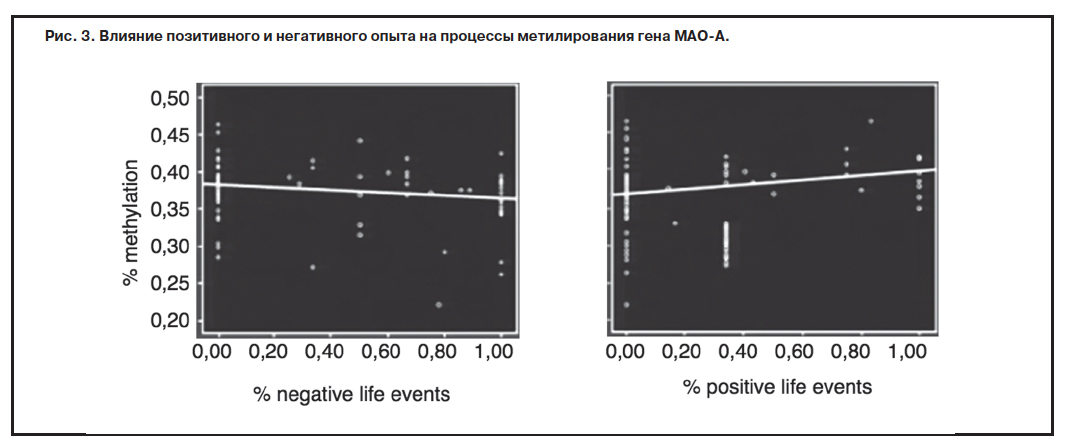
Другим аспектом патогенетики тревожных расстройств, затронутым в данном сообщении, явилось то, что гены оказывают свое влияние не только в рамках одной клетки, но и на уровне нейрональных систем. Раскрыть данную сторону проблемы позволяют нейровизуализационные исследования. Ключевыми структурами в системе тревоги–страха являются миндалевидные тела. У больных с ГТР выявляется их повышенная активация в ответ на предоставление негативно или нейтрально окрашенных стимулов, а применение анксиолитиков (бензодиазепинов, селективных ингибиторов обратного захвата серотонина и прегабалина) снижало активность этих структур [26–28]. Другой важной анатомической структурой, имеющей значение при тревожных расстройствах, является дорсолатеральная префронтальная кора (DLPFC), представляющая собой зону, отвечающую за когнитивный контроль – ингибирующие влияния на гиперактивные лимбические области. Ее активность при тревожных расстройствах (ГТР и паническом расстройстве) снижена, что указывает на нарушение кортикально-лимбических связей, лежащее в основе нарушений регулирования эмоций [29]. Важным представляется то, что в исследованиях у больных с тревожными расстройствами были показаны эффекты генетического предрасположения на активность этих структур. Так, у носителей короткой аллели полиморфизма гена транспортера серотонина (5HTTLPRs/l) и патологического C-полиморфизма гена NPY выявляется повышенная активность миндалевидных тел [30, 31]. Пониженная же активация DLPFC ассоциируется с G-полиморфизмом гена 5-HT1A-рецептора и с TT-полиморфизмом гена рецептора к нейропептиду S [32, 33].
Наконец, профессор Домшке продемонстрировала, что генетические факторы опосредуют и анксиолитическую эффективность противотревожных препаратов. Так, больные с ГТР, гомозиготные по А-варианту гена 5-HT2A-рецепторов, демонстрировали менее выраженный ответ на терапию венлафаксином [34]. Аналогичные результаты были продемонстрированы в отношении s/s аллели гена транспортера серотонина при изучении терапии эсциталопрамом больных с ГТР [35] и в исследованиях эффективности пароксетина при паническом расстройстве и тревожных депрессиях [36, 37].
Таким образом, докладчик очертила основные достижения в понимании взаимоотношений между генетическими и средовыми факторами в этиопатогенезе тревожных расстройств, которые необходимо учитывать при терапии анксиолитиками.
В заключение хочется вернуться к основному назначению трансляционной психиатрии – переносу научных данных в практическую плоскость. Какова же область применения этих представленных на 21-м конгрессе EPA данных? Во-первых, эта информация может быть полезна при проведении психообразования пациентов, она может позволить снизить ассоциирующуюся с заболеванием самостигматизацию, дать надежду и настроить больных на соблюдение терапевтических предписаний. Кроме того, обнаружение новых звеньев этиопатогенеза от генетических до средовых факторов может помочь в определении новых мишеней для терапевтического воздействия и являться точкой приложения усилий, направленных на поиск перспективных лекарственных средств. В-третьих, углубленное понимание нюансов заболевания может позволить более точно осуществлять выбор терапевтических подходов – лечить больного, а не болезнь, а в глобальном плане – навести мосты между экспериментальной и клинической психиатрией, устранить противоречия между персонифицированной и доказательной медициной, расширив их возможности.
Сведения об авторе
Сюняков Тимур Сергеевич – ст. науч. сотр. ФГБУ НИИ фармакологии им. В.В.Закусова РАМН, Москва. E-mail: Sjunja@bk.ru
Ключевые слова: взаимоотношения «ген–среда», депрессия, тревожные расстройства, шизофрения, конгресс EPA.
Gene-Environment interactions in psychiatric disorders: translation of neuroscientific developments into personalized medicine
T.S.Syunyakov
FSBI Zakusov Institute of Pharmacology RAMS, Moscow
Summary. This paper is the one of the series of papers dedicated to materials, presented at the 21st Congress of the European Psychiatric Association that took place in the Nice (France). Here we discuss major communications on the neuroscientific developments in the field of gene-environment interactions in psychiatric disorders and their application to the translational psychiatry and personalized medicine.
Key words: gene-environment interaction, depression, anxiety disorders, schizophrenia, EPA congress.
Противоречия между доказательной и персонифицированной медициной являются предметом широких дискуссий [1]. Потенциалом к достижению компромисса между этими двумя направлениями обладают исследования в области нейронаук ввиду того, что они на доказательном уровне предоставляют более тонкий по сравнению с традиционными клиническими исследованиями подход, учитывающий состояние отдельного пациента, особенности его заболевания, генетической предиспозиции, факторов, сопутствующих развитию, состояние биологических систем организма, стрессовые факторы и условия окружающей среды. Обсуждение этих вопросов стало одной из основных тем конгресса, а ключевое место при их освещении заняла проходившая 7 апреля теоретическая лекция профессора Джулио Лицинио (Julio Licinio) из Южноавстралийского исследовательского института здоровья и медицины (Аделаида, Австралия) «От взаимодействий между генетическими и средовыми факторами к терапии и профилактике», отразившая результаты многолетних работ и наметившая дальнейшие перспективы исследований.
В самом начале своего сообщения Джулио Лицинио указал, что экономическое бремя психических расстройств очень велико (800 млрд евро в год для стран Европы), а для фармакологических компаний рынок психотропных препаратов является крайне прибыльным (с оборотом около 80,5 млрд дол. только в США). Однако парадокс заключается в том, что прагматичные фармакологические компании закрывают подразделения, занимающиеся разработкой психотропных лекарственных препаратов. Комментируя данную проблему, докладчик отметил, что прежде всего это связано с трудностями, возникающими «при наведении мостов между фундаментальной наукой и клиническими дисциплинами», т.е. перед трансляционными нейронауками. Наиболее красноречивой иллюстрацией данного тезиса является тот факт, что на сегодняшний день наиболее широко используемые антидепрессанты опираются на механизмы, выявленные 60 лет назад Джулиусом Аксельродом, а открытия позднего периода практически не были внедрены в практическую сферу. Это связано с тем, что осуществление всего комплекса процесса трансляции (научная идея или открытие → апробирование на людях → проведение клинических исследований → внедрение их результатов в руководства и политику здравоохранения → отслеживание долгосрочных эффектов, позитивных и негативных → распространение новых данных по миру → окончательное понимание значимости открытия для глобального здравоохранения) является затратным по ресурсам и времени. В этой связи профессор Лицинио предлагает фокусировать усилия на устранении пробелов между научной гипотезой, доказательными данными и эмпирическими свидетельствами. Таких слабых мест, по мнению докладчика, имеется три. Во-первых, может возникнуть расхождение на уровне знаний, когда эмпирические наблюдения не имеют под собой ни доказательной базы, ни гипотезы, и в этом случае необходимо направить усилия на поиск лежащих в основе эмпирических наблюдений причин и механизмов. Во-вторых, может наблюдаться ситуация, когда пробел между имеющимися эмпирическими данными и научной гипотезой заключается в отсутствии доказательной базы, и данный пробел должен быть устранен путем повышения «транслируемости» научных данных. В-третьих, эмпирический опыт может не соответствовать ожиданиям, основанным на научном открытии, подтвержденном на доказательном уровне. Рациональным объяснением подобного рода разногласий может служить несоблюдение рекомендаций. Решением данной проблемы может быть только приведение действий и поведения больных и врачей в соответствие рекомендациям. Кроме того, по ходу доклада подчеркивается значимость правильного выбора объекта и методологии исследований для более эффективного переноса научных данных в практическую деятельность.
В качестве иллюстрации автор привлек результаты собственных исследований депрессий и ожирения – двух широко распространенных расстройств, имеющих сложные причины. Предпосылками для рассмотрения этих патологических состояний в одной связке явились также примерно одинаковая распространенность (порядка 25%) ожирения и аффективных/тревожных (родственных генетической основой, механизмами и терапией) расстройств и их частое сосуществование. Оба заболевания обусловлены генетическими механизмами и средовыми влияниями (стрессами). Они взаимно повышают риск возникновения друг друга, имеют пересекающийся круг осложнений и коморбидных состояний. При депрессивных расстройствах нарушается функционирование основных органов и систем, что наряду с суицидальным поведением является причиной высокой смертности при данном расстройстве. Так, большое депрессивное расстройство в 2 раза повышает риск ишемической болезни сердца и на 60% вероятность возникновения сахарного диабета 2-го типа, которые также являются осложнениями ожирения. Депрессивным нарушениям в долгосрочной перспективе часто сопутствуют кардиометаболические расстройства и увеличение веса,
а при сосуществовании депрессивных нарушений и сахарного диабета увеличение веса даже на 5 кг в 1,5 раза увеличивает риск возникновения ишемической болезни сердца. Следует также отметить, что предпосылками фактически начавшейся эпидемии ожирения считаются снижение физической активности и повышенное потребление пищи, которые часто встречаются при депрессивных состояниях. Важно, что некоторые нейропептидные и нейротрансмиттерные системы, в том числе кортиколиберин (CRHR1), нейропептид Y (NPY), серотонин и норадреналин, вовлечены в контроль и настроения, и веса тела. При этом препараты, применяемые при лечении ожирения (механизм их действия заключается во влиянии на содержание серотонина и норадреналина в центральной нервной системе – ЦНС), часто приводят к формированию пониженного настроения, а терапия депрессивных расстройств осуществляется антидепрессантами (главным образом влияющими на обратный захват серотонина и норадреналина), которые часто способствуют увеличению веса в долгосрочной перспективе, а также повышают риск сахарного диабета, независимо от исходного индекса массы тела. В свою очередь с увеличением веса также связан повышенный риск и других болезней, в частности онкологических (на 60%). На актуальность изучения данной проблемы также указывает то, что все указанные последствия в клинической практике недооцениваются и должным образом не лечатся. Таким образом, депрессия и ожирение значительно больше связаны друг с другом, чем представлялось раньше. При этом существуют биологические системы, значение которых для этих двух заболеваний не вполне ясно, – это нейропептиды стресса, медиаторы иммунитета, адипокины и нейрокины. И хотя постановка данной проблемы отнюдь не заслуга последних достижений, новые науки (фармакогеномика и геномика) позволяют взглянуть на нее с иной стороны.
В связи со всеми указанными фактами представляются правомерными следующие вопросы. Совпадение ли это или следствие общих биологических механизмов? Каков характер взаимоотношений между депрессией и ожирением и каково место стрессовой системы в этих взаимоотношениях? Любое ли из этих состояний может являться отправной точкой для других? Какие взаимодействия возникают у людей, склонных к ожирению, на фоне приема антидепрессантов? Отличается ли ожирение в контексте приема антидепрессантов от ожирения вследствие нарушений энергетического обмена?
Пытаясь ответить на часть поставленных вопросов, Джулио Лицинио продемонстрировал результаты эксперимента, направленного на выявление взаимодействий между стрессом, средовыми и фармакологическими факторами [2]. В рамках этого исследования крыс подвергали воздействию краткосрочного (на протяжении 1 нед) стрессового воздействия (ограничение активности). При этом части животных в этот период давали антидепрессанты, а части – вводили физиологический раствор. После завершения данного этапа животным в течение длительного времени давалась пища, обогащенная жирами. Оказалось, что животные, которым назначались антидепрессанты, не только компенсировали снизившийся на фоне стресса вес, но и прибавили в весе значительно больше, чем крысы из контрольной группы. Таким образом, даже краткосрочный прием антидепрессантов вызывает длительно существующую сенситизацию к повышению веса. При этом антидепрессанты в условиях стрессового воздействия оказывали на животных и благоприятное («антидепрессивное») действие. Оказалось, что у животных опытной группы повышена экспрессия ряда факторов роста: мозгового нейротрофного фактора (BDNF), фактора роста нервов (NGF) и, что важнее всего, инсулиноподобного фактора роста
(IGF-1), который и мог обусловить увеличение веса животных. Таким образом, данный эксперимент (парадигма «стресс–диета–антидепрессанты»), с одной стороны, продемонстрировал влияние даже краткосрочного приема антидепрессантов на вес (и это при том, что антидепрессанты занимают в мире 2-е место по продажам, а многие больные принимают их бесконтрольно). С другой стороны, показана важность стрессовой реакции – координированного ответа нейроэндокринной системы на неблагоприятные внешние или внутренние факторы – повышение веса в долгосрочном периоде.
В патогенезе ожирения играют роль взаимодействия генетической предрасположенности и средовых факторов (обнаружена взаимосвязь ожирения с доступностью пищи, снижением физической активности, инфекционными заболеваниями, возрастом матери, высокой плодовитостью и ассортативностью браков, содержанием в окружающей среде химических веществ, вызывающих эндокринные расстройства, малыми перепадами температуры окружающей среды, внутриутробными факторами, приемом препаратов). Таким образом, складывается континуум в ряду влияния на вес внешних и генетических факторов:
у части людей большую роль играют алиментарные факторы, у части – повышенное потребление пищи возникает в связи со стрессами и эмоциональными проблемами, а еще одна часть людей страдает избытком веса в связи с генетической предрасположенностью. При этом при ожирении в отличие от депрессии генетический фактор может играть колоссальную роль. Несмотря на то что контроль веса тела также вовлекает множество генетически детерминированных систем (моноамины, нейропептид Y, гормоны и прогормоны гипоталамуса и гипофиза, галанин, орехины, холецистокинин, бомбезин), настоящим прорывом в области знаний об ожирении является выявление роли лептина при данной патологии. Лептин является передаточным звеном между жировой тканью и головным мозгом, а исследования магнитно-резонансной томографии показали, что лептин регулирует активность островковой зоны головного мозга в ответ на предоставление пищи [3]1. Видимо, при ожирении играет роль также другой нейропептид – грелин, который вызывает активацию в тех же областях, что и лептин2. Однако похоже, что влияния содержания грелина и лептина на повышение аппетита находятся в реципрокных взаимоотношениях [4]. Также автор приводит данные собственных исследований, показавших, что терапия лептином при тяжелых семейных формах ожирения, при которых выявляются дефекты гена, кодирующего лептин приводит к драматическому снижению веса, появлению контроля за приемом пищи и увеличению продолжительности жизни [5].
Переходя к следующей части доклада, профессор Лицинио указал, что сложность анализа депрессивных расстройств с позиций взаимодействия генетических и средовых факторов заключается в разнообразии фенотипических проявлений, которые могут различаться по течению, его этапу, периодичности, синдромальной картине, тяжести, причинам и времени возникновения в течение жизни. И это поднимает вопрос о нозологическом единстве депрессивных нарушений. Является ли депрессивный фенотип проявлением эквифинальности разных патогенетических процессов, какие причины лежат в основе болезни и сколько их, могут ли они быть связаны со специфическим генетическим фактором или с влиянием на генетическую уязвимость других факторов, не являющимися причинными, насколько состояние обусловлено несколькими большими генетическими факторами, а на сколько – множеством генетических факторов с небольшим эффектом, какова роль внешней среды, особенностей развития и эпигенетических факторов?
Депрессивные расстройства являются следствием сложной констелляции генетических и средовых факторов (пренатальных стрессов, стрессов, связанных с потерями близких, горем, лишениями, естественными катастрофами, войной, а также с социальным окружением и поддержкой, питанием, заболеваниями и применяемыми препаратами). При этом давно известно, что депрессивные расстройства носят полигенный характер и не выделено какого-либо одного генетического фактора, который бы по значимости для патогенеза намного превосходил другие.
В этих условиях Джулио Лицинио предлагает для оптимальной оценки взаимоотношений между генетическими и средовыми факторами проводить систематическую оценку социальных и средовых влияний (особенно в перинатальном периоде) и тщательно изучать состояние биологических систем-кандидатов на хорошо охарактеризованных группах больных, а поиск новых механизмов, с его точки зрения, должен осуществляться без оглядки на предварительно сформулированные концепции, которые могут внести искажение при интерпретации новых данных. Докладчик указывает, что одним из наиболее жестко детерминированных фенотипов при рассмотрении депрессий является терапевтический ответ на антидепрессивную терапию, в связи с чем он наилучшим образом подходит для оценки взаимоотношений между генетикой и внешней средой. И уже с учетом разделения депрессивных фенотипов по наличию или отсутствию антидепрессивного ответа должны осуществляться оценка генотипа, рассмотрение вовлеченных систем-кандидатов (как специфических, так и выявляемых на всех этапах патогенетических путей с использованием биоинформационного подхода по поиску однонуклеотидных полиморфизмов), поиск новых мишеней (на основе данных по экспрессии генов, с последующим генным или полногеномным секвенированием, генотипированием экзома – совокупности несущих информацию участков генов), оценка применимости этих данных в практической сфере.
Учитывая, что в патогенезе как депрессивных расстройств, так и ожирения существенная роль принадлежит стрессовой системе3 как системе, опосредующей взаимосвязь между средовыми и генетическими факторами, и основываясь на позитивном опыте выявления связи между терапевтическим ответом и вариантами генов, кодирующих рецепторы к кортиколиберину при бронхиальной астме, Лицинио предположил, что такого рода взаимосвязи могут быть выявлены и при депрессивных расстройствах [6]. В исследование, направленное на тестирование данной гипотезы, вошли 80 пациентов с депрессивными расстройствами (американские мексиканцы). У больных были генотипированы гаплотипы CRHR1 и выявлены их частоты и варианты. Оказалось, что гаплотип-1 (GAG-гаплотип для вариантов rs1876828, rs242939 и rs242941) встречался у большинства (63%) больных, однако у некоторых он находился в гомозиготном, а у некоторых в гетерозиготном состоянии. Оказалось, что у больных с высокими степенями тревоги на фоне депрессии, у которых гаплотип-1 находился в гомозиготном состоянии, терапевтический ответ на флуоксетин и дезипрамин (а для этих препаратов получены данные об их влиянии на кортиколиберин) был достоверно более выраженным. Данный пример является показательным, и с использованием данного подхода (с поэтапным смещением акцента исследований от патогенеза через однонуклеотидный полиморфизм к гаплотипам и геному) группой Лицинио было выявлено 1500 однонуклеотидных полиморфизмов в генах, имеющих значение для терапевтического ответа на антидепрессанты.
Принимая во внимание, что стрессовый ответ в целом и кортиколиберин в частности отчетливо связаны с иммунным ответом, состояние иммунной системы, цитокинов и нейрокинов является другой потенциальной мишенью для изучения взаимодействия генетических и средовых факторов при депрессиях. Автор отметил значительные сходства между течением аутоиммунных заболеваний и депрессий в контексте вариантов течения – хронического, периодического с усилением и послаблением симптоматики, эпизодического. Кроме того, применение цитокинов в качестве терапевтических средств приводит к возникновению депрессивных расстройств. Все это указывает на возможность участия дисфункции медиаторов иммунитета при депрессии (при этом данная дисфункция может быть первичной, генетически-детерминированной, либо вторичной, вследствие инфекционных заболеваний или стрессовых воздействий).
Рассматривая цитокиновую теорию депрессии с позиций молекулярной биологии, экспериментальных моделей, клинических, генетических и фармакогенетических исследований, Лицинио сформулировал рабочую гипотезу о том, что нейрокины являются синтезируемыми в головном мозге цитокинами, однако их регуляция в головном мозге отличается от их регуляции на периферии; нейрокины участвуют в биологии настроения, когнитивных функций и поведения; регулирование нейрокинов в головном мозге необязательно требует присутствия инфекционных агентов или аутоиммунного процесса. В поддержку высказанной гипотезы профессор Лицинио привел данные, полученные на той же группе американских мексиканцев. В этом исследовании [7] была продемонстрирована взаимосвязь между большим депрессивным расстройством и полиморфизмом генов PSMB4 (b4-субъединица протеосомы, играющая роль в презентации антигена) и TBX21 (кодирует одноименный белок, играющий роль в пролиферации Т-лимфоцитов). При этом на долю их полиморфизмов rs2296840 и rs17244587, соответственно, приходится 47,8% риска, а их объединенный эффект (взаимодействие «ген–ген») на 26% выше, чем можно было бы ожидать от простого суммирования рисков. Анализ показал, что у лиц, имеющих 1, 2 и 3 аллели этих вариантов генов, риск депрессивных расстройств возрастает в 2,3, 3,2 и 9,8 раза, что свидетельствует о значительном эффекте дозы генов. Представляет интерес также то, что экспрессия гена цитокина CXCL10/IP-10 при депрессии повышена, а при реализации антидепрессивного эффекта снижается. Кроме того, выявлена ассоциация и других факторов, указывающих на роль Т-клеточного иммунитета (CD3E, PRKCH, PSMD9, STAT3) и функций гипоталамо-гипофизарно-надпочечниковой системы (UCN3) при реализации антидепрессивного ответа. Эти результаты согласуются с данными о преобладании при депрессии Т-хелперной активности 1-го (провоспалительного) типа над активностью 2-го (противовоспалительного) типа. Также была подтверждена роль интерлейкина-6 в механизмах депрессий. Эти данные были подтверждены в другом исследовании – при угнетении Т-ростка иммунитета животные демонстрировали повышенную устойчивость в тестах на формирование депрессивного поведения [8].
Следуя намеченной последовательности изучения, Джулио Лицинио приводит результаты секвенирования генов на всех этапах реализации эффектов антидепрессантов (начиная от печеночного метаболизма, способности проникать через гематоэнцефалический барьер, взаимодействовать с первичными рецепторами, влиять на внутриклеточные мишени с отслеживанием дальнейшего каскада изменений) флуоксетина и дезипрамина с целью выявления ассоциированных с депрессией однонуклеотидных полиморфизмов. При этом только в отношении мозгового нейротрофного фактора (BDNF) было выявлено 47 ранее идентифицированных и 83 новых однонуклеотидных полиморфизмов [9]. В отношении других звеньев в цепи реализации механизмов терапевтического ответа (транспортеры серотонина, норадреналина, дофамина, ген CREB1, ген рецепторов к CRH и BDNF) выявлено 419 однонуклеотидных полиморфизмов, ассоциирующихся с ответом на антидепрессанты [10]. Таким образом, существует множество свидетельств того, что терапевтический ответ на антидепрессивную терапию во многом детерминирован генетически.
Под конец данного фрагмента своего сообщения докладчик анонсировал, что с появлением новых технологических решений стали возможными исследования экзома, которые в настоящее время проводятся его научной группой. Кроме того, он очертил будущие направления исследований и сформулировал новый подход: поиск новых генов-кандидатов, бинарная оценка их значимости для определенной патологии с последующей их группировкой при помощи древовидного анализа в соответствии с местом, занимаемым в патогенезе, и выяснением суммарного вклада того или иного пути в предрасположенность к болезни.
Таким образом, в данном разделе доклада было продемонстрировано успешное использование нового подхода на примере выявления факторов, в том числе опосредующих взаимодействие генетических и средовых влияний, через систему стресса и связанных с ней функций иммунитета, ассоциирующихся с риском депрессивных расстройств и фармакологическим ответом на антидепрессанты.
Таким образом, если сделать вывод из всего сказанного профессором Лицинио, то необходимо отметить, что на сегодняшний день существуют значительные пробелы между результатами нейронаучных исследований и клинической практикой, однако появление новых технологических решений и предлагаемые автором методология и новые подходы к изучению данного вопроса могут позволить их решить. В этом направлении уже сделаны существенные шаги. На примере взаимоотношений двух тесно связанных друг с другом заболеваний – депрессии и ожирения – получены новые данные об их генетической природе, участии генов, имеющих «большое» и «малое» значение», открыты многочисленные новые однонуклеотидные полиморфизмы, имеющие функциональное значение. На примере парадигмы «стресс–диета–ожирение» продемонстрировано взаимодействие патологического процесса, внешних средовых факторов и фактора применения антидепрессантов, которые в сочетании запускают внутренние механизмы, приводящие к повышению веса, показана опасность бесконтрольного применения антидепрессантов. Выявлены дополнительные доказательства генетической детерминированности антидепрессивного ответа и роли состояния иммунной системы в генезе и терапии депрессивных нарушений. С учетом новых разработок вновь осуществляется активное изучение роли стрессовой системы и системы иммунитета как ее части в формировании комплексных расстройств, при которых велико значение и генетических, и средовых факторов.
Переходя от общих вопросов к более частным, логическим продолжением доклада Джулио Лицинио явилась исследовательская сессия «Краткосрочные и долгосрочные эффекты иммунного стресса в пренатальном и перинатальном периоде: от основ к клинике», проводившейся под председательством Ай Му Минт (Aye Mu Myint) из Университетской клиники г. Мюнхена (Германия) ввиду отсутствия профессора Маркуса Шварца (Marcus Schwarz). Как следует из названия сессии, здесь изучались нейроиммунологические гипотезы разных психических расстройств: депрессий и шизофрении, и в том числе послеродовых депрессий и психозов. В этой связи не лишним будет еще раз указать на тесные взаимоотношения между иммунной и нейроэндокринной системой в ответе на стресс, определяющие реактивность организма к внешним факторам, а также вспомнить, что некоторые авторы рассматривают иммунную систему вообще в качестве шестого «некогнитивного» органа чувств [11], а в соответствии с цитокиновой гипотезой Брайана Леонарда активация иммунитета играет важную роль в патогенезе депрессивных расстройств [12].
Среди представленных на сессии четырех докладов наибольший интерес представляли два экспериментальных исследования, в которых данные гипотезы рассматривались с позиций роли нарушений нормального развития головного мозга в генезе депрессивных нарушений и шизофрении и с точки зрения взаимодействия «гены–среда». Предпосылками к проведению этих работ послужили данные литературы о том, что инфекционные заболевания, возникающие у матери в ходе беременности, могут влиять на ход развития головного мозга у потомства ввиду облегченного проникновения медиаторов воспаления через несформированный гематоэнцефалический барьер, последующей активации микроглии, в том числе перекисного окисления; это приводит к истощению запасов ионов железа и цинка, составляющих активные центры многих ферментов, участвующих в окислительно-восстановительных процессах, что способствует к изменению траектории развития ЦНС, формируя дополнительную уязвимость (наряду с генетической) к психическим заболеваниям. Наряду с этим пренатальное воспаление запускает патологическую сенсибилизацию микроглии и астроцитов, что по времени совпадает с возникновением первых нарушений (мягких неврологических знаков и психомоторного дефицита). Сенсибилизированные клетки глии либо сами по себе, либо после дополнительной активации средовыми стрессорами в постнатальном периоде запускают воспалительные процессы в развивающемся головном мозге, вызывая нарастание патологических изменений, способствуя таким образом манифестации заболевания (рис. 1) [13].

Для оценки влияния пренатального иммунного стресса на предрасположенность к психическим заболеваниям
(в первую очередь шизофрении) предложена экспериментальная модель с использованием иммунологической провокации [14]. Ее суть заключается в том, что самкам мышей, находящимся на разных сроках беременности, вводились антигены, провоцировавшие иммунный ответ при отсутствии инфекционного возбудителя. Затем у потомства при использовании валидных методик регистрировались поведенческие нарушения. При этом, на основании литературных данных, иммунная провокация вирусным антигеном, полирибоинозиловой-полирибоцитозиновой кислотой (PolyL:C – синтетический аналог двуцепочечной ДНК) в отличие от липополисахарида4 (бактериального антигена) и интерлейкина-6 (провоспалительного цитокина, хронически повышенные уровни которого вызывают нейродегенерацию) приводила к возникновению у потомства широкого круга поведенческих расстройств и изменений, характерных для шизофрении. В частности, у них отмечалось снижение преимпульсного и латентного торможения5, социального поведения, исследовательской активности, рабочей памяти, а также повышение чувствительности к агонистам дофаминовых и NMDA-рецепторов. Кроме того, валидность данного моделирования шизофрении с точки зрения патологии развития подтверждает также время возникновения поведенческих расстройств у мышей, соответствующее раннему зрелому возрасту (т.е. возрасту, характерному для манифестации шизофрении), и то, что они купировались применением антипсихотиков [15]. В экспериментальных исследованиях было показано, что при такого рода моделировании роль играет время проведения провокации: в частности, угнетение преимпульсного торможения у потомства наблюдалось при введении PolyL:C на 9-й день беременности, но не на 17-й день [16].
Следует отметить, что такое достаточно полноценное моделирование особенностей шизофрении на первый взгляд идет вразрез с расчетами об относительно малом вкладе вирусных инфекций в этиологию шизофрении. Однако в работе M.Clarke и соавт. (2009 г.) [17] приводятся сведения о том, что влияние пренатальных инфекций у лиц с наследственным отягощением психотическими расстройствами в 4 раза больше в сравнении с лицами, не имеющими отягощения, что отчетливо указывает на взаимодействие инфекционных заболеваний с генетической предрасположенностью. Данное положение было подтверждено в некоторых работах. В частности, у мышей с мутантной аллелью гена mhDISC1 (mutant human disrupted-in-schizophrenia-1) пренатальная иммунная стимуляция приводила к повышенной тревожности, «депрессивному» поведению, нарушениям «социального поведения», снижению стресс-реактивности, а также ассоциировалась с рядом структурных изменений головного мозга [18]. Синергичное усиление дофаминергических нарушений наблюдалось и при комбинировании модели с гетерозиготной делецией гена Nurr1 (генетический фактор) с моделью PolyL:C-провокации (средовой фактор) [19].
В своей работе Сандра Джованьоли (Sandra Giovanoli, Цюрих, Швейцария) предлагает нам использовать модель «двойного удара» средовых факторов: после проведения иммунной вирусной провокации PolyL:C на 9-й день беременности («первый удар») на 30–40-е дни жизни потомство (опытная группа) подвергали ряду субхронических стрессовых воздействий («второй удар»: удары электрическим током по лапам, ограничение активности, плавательный стресс, животным не давали пить, повторно меняли клетки). Через 1 мес после завершения «второго удара» у животных отслеживались отдаленные эффекты. Оказалось, что животные опытной группы, подвергавшиеся стрессу (POL и S+), демонстрировали повышенную тревожность (рис. 2, а), угнетение препульсового торможения (рис. 2, б), а также повышенную чувствительность к агонистам дофаминовых рецепторов и антагонистам глутаматергических NMDA-рецепторов (рис. 2, в и 2, г соответственно) в сравнении с потомством животных, у которых не проводилось иммунологической провокации, (контрольная группа: CON, S+ и S-) и с животными опытной группы, не подвергавшимися стрессовым воздействиям в пубертатном возрасте (POL и S-). При изучении нейрохимических изменений выявлялось увеличение содержания дофамина в прилежащем ядре (обусловленное иммунной провокацией) и гиппокампе (как результат взаимодействия двух средовых влияний).

Ай Мю Минт представила результаты своего исследования, в котором она, используя модель пренатальной иммунной провокации на более поздних сроках гестации (17-й день) с липополисахаридным (бактериальным) антигеном, смоделировала нарушения нормального развития головного мозга при депрессивных расстройствах. На 13-й неделе жизни у мышей из экспериментальной группы выявлялось «депрессивное» поведение при проведении теста с принудительным плаванием, выражающееся в достоверном увеличении частоты и продолжительности периодов прекращения двигательной активности и зависаний в воде. Наряду с этим наблюдалось усиление процессов эпигенетических изменений в тканях головного мозга, что выражалось в снижении активности гистон-деацетилазы и повышении активности ДНК-метилтрансферазы, а также изменении экспрессии генов, определяющих соотношение нейротоксических (гены Cideb, Txnip, Drd2, Nostrin, Tacr1) и нейропротективных (Nrg1, Ngrf, Il1r1) процессов, в сторону увеличения первых и снижения вторых, что может свидетельствовать об участии данного механизма в формировании депрессивных расстройств.
Таким образом, в этих двух сообщениях был представлен обзор научных работ, демонстрирующих роль пренатального воспаления в формировании уязвимости к таким заболеваниям, как шизофрения и депрессивное расстройство, для которых в последние годы была показана, с одной стороны, тесная связь с состоянием иммунной системы, а с другой – с нарушением нормального процесса развития головного мозга. Эти данные легли в основу создания экспериментальной модели пренатальной иммунной провокации, обладающей превосходной конструктивной валидностью в отношении шизофрении и в некоторой степени депрессивного расстройства, которая позволяет объяснить не только особенности клинической картины и течения заболеваний, но и особенности их формирования в условиях сложного взаимодействия генетической предрасположенности и внешних воздействий (иммунологических и стрессовых). Более того, работы, выполняемые в этом направлении, открывают широкие перспективы как для дальнейшего изучения природы психических расстройств, так и для создания принципиально новых подходов к их терапии и профилактике.
Конечно же, не могли обойти стороной проблему взаимодействия генетических и средовых факторов и на сателлитном симпозиуме компании Pfizer «Генерализованное тревожное расстройство: почему люди беспокоятся?», проводимом под председательством профессора Кристера Аллгуландера (Christer Allgulander) из Каролинского института в Швеции. Доклад «Патологическая генетика тревоги» в блестящей манере представила молодая профессор Катарина Домшке (Katharina Domshke) из Университетской психосоматической и психотерапевтической клиники г. Вюрцберга (Германия).
Свой доклад Катарина Домшке начала с указания того, что, как и при многих других психических заболеваниях, в этиологии тревожных расстройств значение имеют и биологические, и средовые факторы. При этом среди биологических ключевое место занимают генетические. Об этом свидетельствуют результаты семейно-генетических исследований, выявивших 1,5–3-кратное увеличение риска тревожных расстройств у родственников 1-й степени родства больных [20], что приводит к накоплению в подверженных семьях случаев тревожных расстройств, указывая на их генетическую обусловленность. Однако эти результаты не снимают всех вопросов о наследственной основе, поскольку в семьях «наследуется» не только генетический материал, но и «атмосфера». Близнецовые исследования, позволяющие исключить данные влияния, свидетельствуют, что конкордантность в случае генерализованного тревожного расстройства (ГТР) составляет 20–40%, при паническом расстройстве она достигает 48%, а в отношении одновременного возникновения обоих заболеваний – 23% [21, 22]. Кроме того, у ГТР имеется общая генетическая основа с большим депрессивным расстройством. О чем же могут говорить эти цифры? С одной стороны, они подводят черту под доказательствами наследуемости тревожных расстройств, с другой – свидетельствуют, что в 50–80% случаев роль в возникновении тревожных расстройств играют внешние, негенетические факторы, а также указывают на значимость взаимоотношений «ген–среда».
Однако ни семейно-генетические, ни близнецовые исследования не решают вопросов о том, какие гены играют ключевую роль в предрасположении. К ним адресованы молекулярно-генетические исследования, анализ сцепленных генов и изучение генетических ассоциаций. В этих исследованиях были выявлены общие для спектра тревожных расстройств (паническое расстройство, ГТР и тревожная депрессия) гены риска, и прежде всего это гены серотонинового 5-HT1A-рецептора – транспортера серотонина и моноаминоксидазы типа А (МАО-А), вовлеченной в метаболизм серотонина и норадреналина, подтверждая таким образом на генном уровне нейрохимические гипотезы о вовлечении серотонинергической и норадренергической систем нейропередачи в генез тревожных расстройств. Однако за последнее десятилетие открыт ряд новых генов-кандидатов, вовлеченных в контроль тревоги: ген рецептора к нейропептиду S (NPS), нейропептид Y (NPY), ген небольшого пептида RGS2, участвующего в качестве сигнальной молекулы в каскадах основных нейротрансмиттерных систем6. Хочется отметить, что в докладе было приведено лишь незначительное число из рассматриваемых в настоящее время генов-кандидатов. В 2011 г. в журнале Translational Psychiatry была опубликована экспериментальная работа, показавшая, что с тревожными состояниями ассоциировано порядка нескольких сотен генов [23].
Переходя к анализу взаимоотношений генетических и средовых факторов, профессор Домшке ссылается на исследование, изучавшее влияние полиморфизма гена NPY (NPY 399C/T) на возникновение тревожных расстройств среди жертв урагана [24]. Носители гомозиготной аллели NPY 399C/С имели наибольшую подверженность по сравнению с носителями С/Т- и T/T-аллели, причем в сравнении с гомозиготами по T-варианту гена риск тревожных расстройств возрастал в 8 раз.
Этиологическую мозаику тревожных расстройств осложняют эпигенетические влияния: процессы метилирования ДНК и ацетилирования гистонов. Суть этих явлений заключается в следующем: ацетилирование гистонов вызывает активацию процессов транскрипции на определенном участке ДНК, который может содержать патологический ген, а при соединении метильной группы с промотором гена, наоборот, происходит «выключение» гена. Особенностью подобных эпигенетических процессов является их существенная нестабильность и динамичность. Таким образом, даже наличие генетического предрасположения может не проявляться в случае, например, если экспрессия патологических генов не осуществляется ввиду их инактивации. Однако процессы метилирования/деметилирования обратимы, что привело к возникновению гипотезы об индукции эпигенетических процессов стрессорами. И эта гипотеза получила подтверждение. Так, у больных с паническим расстройством отмечается недостаточное метилирование гена МАО-А, причем было показано, что негативно окрашенные события в течение года, предшествовавшего возникновению заболевания, вызывали усиление процессов деметилирования гена МАО-А, тогда как позитивные события вызывали его метилирование (инактивацию) (рис. 3) [25].

Другим аспектом патогенетики тревожных расстройств, затронутым в данном сообщении, явилось то, что гены оказывают свое влияние не только в рамках одной клетки, но и на уровне нейрональных систем. Раскрыть данную сторону проблемы позволяют нейровизуализационные исследования. Ключевыми структурами в системе тревоги–страха являются миндалевидные тела. У больных с ГТР выявляется их повышенная активация в ответ на предоставление негативно или нейтрально окрашенных стимулов, а применение анксиолитиков (бензодиазепинов, селективных ингибиторов обратного захвата серотонина и прегабалина) снижало активность этих структур [26–28]. Другой важной анатомической структурой, имеющей значение при тревожных расстройствах, является дорсолатеральная префронтальная кора (DLPFC), представляющая собой зону, отвечающую за когнитивный контроль – ингибирующие влияния на гиперактивные лимбические области. Ее активность при тревожных расстройствах (ГТР и паническом расстройстве) снижена, что указывает на нарушение кортикально-лимбических связей, лежащее в основе нарушений регулирования эмоций [29]. Важным представляется то, что в исследованиях у больных с тревожными расстройствами были показаны эффекты генетического предрасположения на активность этих структур. Так, у носителей короткой аллели полиморфизма гена транспортера серотонина (5HTTLPRs/l) и патологического C-полиморфизма гена NPY выявляется повышенная активность миндалевидных тел [30, 31]. Пониженная же активация DLPFC ассоциируется с G-полиморфизмом гена 5-HT1A-рецептора и с TT-полиморфизмом гена рецептора к нейропептиду S [32, 33].
Наконец, профессор Домшке продемонстрировала, что генетические факторы опосредуют и анксиолитическую эффективность противотревожных препаратов. Так, больные с ГТР, гомозиготные по А-варианту гена 5-HT2A-рецепторов, демонстрировали менее выраженный ответ на терапию венлафаксином [34]. Аналогичные результаты были продемонстрированы в отношении s/s аллели гена транспортера серотонина при изучении терапии эсциталопрамом больных с ГТР [35] и в исследованиях эффективности пароксетина при паническом расстройстве и тревожных депрессиях [36, 37].
Таким образом, докладчик очертила основные достижения в понимании взаимоотношений между генетическими и средовыми факторами в этиопатогенезе тревожных расстройств, которые необходимо учитывать при терапии анксиолитиками.
В заключение хочется вернуться к основному назначению трансляционной психиатрии – переносу научных данных в практическую плоскость. Какова же область применения этих представленных на 21-м конгрессе EPA данных? Во-первых, эта информация может быть полезна при проведении психообразования пациентов, она может позволить снизить ассоциирующуюся с заболеванием самостигматизацию, дать надежду и настроить больных на соблюдение терапевтических предписаний. Кроме того, обнаружение новых звеньев этиопатогенеза от генетических до средовых факторов может помочь в определении новых мишеней для терапевтического воздействия и являться точкой приложения усилий, направленных на поиск перспективных лекарственных средств. В-третьих, углубленное понимание нюансов заболевания может позволить более точно осуществлять выбор терапевтических подходов – лечить больного, а не болезнь, а в глобальном плане – навести мосты между экспериментальной и клинической психиатрией, устранить противоречия между персонифицированной и доказательной медициной, расширив их возможности.
Сведения об авторе
Сюняков Тимур Сергеевич – ст. науч. сотр. ФГБУ НИИ фармакологии им. В.В.Закусова РАМН, Москва. E-mail: Sjunja@bk.ru
Список исп. литературыСкрыть список1. de Leon J. Evidence-based medicine versus personalized medicine: are they enemies? J Clin Psychopharmacol 2012;. 32 (2): 153–64.
2. Mastronardi C, Paz-Filho GJ, Valdez E et al. Long-term body weight outcomes of antidepressant-environment interactions. Mol Psychiatry 2011; 16 (3): 265–72.
3. Baicy K, London ED, Monterosso J et al. Leptin replacement alters brain response to food cues in genetically leptin-deficient adults. Proc Natl Acad Sci USA 2007; 104 (46): 18276–9.
4. Naqvi N H, Rudrauf D, Damasio H, Bechara A. Damage to the insula disrupts addiction to cigarette smoking. Science 2007; 315 (5811): 531–4.
5. Licinio J, Caglayan S, Ozata M et al. Phenotypic effects of leptin replacement on morbid obesity, diabetes mellitus, hypogonadism, and behavior in leptin-deficient adults. Proc Natl Acad Sci USA 2004; 101 (13): 4531–6.
6. Licinio J, O’Kirwan F, Irizarry K et al. Association of a corticotropin-releasing hormone receptor 1 haplotype and antidepressant treatment response in Mexican-Americans. Mol Psychiatry 2004; 9 (12): 1075–82.
7. Wong ML, Dong C, Maestre-Mesa J, Licinio J. Polymorphisms in inflammation-related genes are associated with susceptibility to major depression and antidepressant response. Mol Psychiatry 2008; 13 (8): 800–12.
8. Kim S J, Lee H, Joung HY et al. T-bet deficient mice exhibit resistance to stress-induced development of depression-like behaviors. J Neuroimmunol 2011; 240–1: 45–51.
9. Licinio J, Dong C, Wong ML. Novel sequence variations in the brain-derived neurotrophic factor gene and association with major depression and antidepressant treatment response. Arch Gen Psychiatry 2009; 66 (5): 488–97.
10. Dong C, Wong M L, Licinio J. Sequence variations of ABCB1, SLC6A2, SLC6A3, SLC6A4, CREB1, CRHR1 and NTRK2: association with major depression and antidepressant response in Mexican-Americans. Mol Psychiatry 2009; 14 (12): 1105–18.
11. Blalock J E. The immune system as a sensory organ. J Immunol 1984; 132 (3): 1067–70.
12. Leonard BE. The immune system, depression and the action of antidepressants. Prog Neuropsychopharmacol Biol Psychiatry 2001; 25 (4): 767–80.
13. Meyer U. Developmental neuroinflammation and schizophrenia. Prog Neuropsychopharmacol Biol Psychiatry 2013; 42: 20–34.
14. Meyer U, Feldon J, Fatemi S. H. In-vivo rodent models for the experimental investigation of prenatal immune activation effects in neurodevelopmental brain disorders. Neurosci Biobehav Rev 2009; 33 (7): 1061–79.
15. Vuillermot S, Weber L, Feldon J, Meyer U. A longitudinal examination of the neurodevelopmental impact of prenatal immune activation in mice reveals primary defects in dopaminergic development relevant to schizophrenia. J Neurosci 2010; 30 (4): 1270–87.
16. Meyer U, Nyffeler M, Yee BK et al. Adult brain and behavioral pathological markers of prenatal immune challenge during early/middle and late fetal development in mice. Brain Behav Immun 2008; 22 (4): 469–86.
17. Clarke MC, Tanskanen A, Huttunen M et al.. Evidence for an interaction between familial liability and prenatal exposure to infection in the causation of schizophrenia. Am J Psychiatry 2009; 166 (9): 1025–30.
18. Abazyan B, Nomura J, Kannan G et al. Prenatal interaction of mutant DISC1 and immune activation produces adult psychopathology. Biol Psychiatry 2010; 68 (12): 1172–81.
19. Vuillermot S, Joodmardi E, Perlmann T et al. Prenatal immune activation interacts with genetic Nurr1 deficiency in the development of attentional impairments. J Neurosci 2012; 32 (2): 436–51.
20. Newman SC, Bland RC. A population-based family study of DSM-III generalized anxiety disorder. Psychol Med 2006; 36 (9): 1275–81.
21. Hettema JM, Neale MC, Kendler KS. A review and meta-analysis of the genetic epidemiology of anxiety disorders. Am J Psychiatry 2001; 158 (10) : 1568–78.
22. Scherrer JF, True WR, Xian H et al. Evidence for genetic influences common and specific to symptoms of generalized anxiety and panic. J Affect Disord 2000; 57 (1–3): 25–35.
23. Le-Niculescu H., Balaraman Y, Patel SD et al. B. Convergent functional genomics of anxiety disorders: translational identification of genes, biomarkers, pathways and mechanisms. Transl Psychiatry 2011; 1: e9.
24. Amstadter AB, Koenen KC, Ruggiero K J et al. NPY moderates the relation between hurricane exposure and generalized anxiety disorder in an epidemiologic sample of hurricane-exposed adults. Depress Anxiety 2010; 27 (3): 270–5.
25. Domschke K, Tidow N, Kuithan H et al. Monoamine oxidase A gene DNA hypomethylation – a risk factor for panic disorder? Int J Neuropsychopharmacol 2012; 15 (9): 1217–28.
26. Nitschke JB, Sarinopoulos I, Oathes DJ et al. H. Anticipatory activation in the amygdala and anterior cingulate in generalized anxiety disorder and prediction of treatment response. Am J Psychiatry 2009; 166 (3): 302–10.
27. Arce E, Miller DA, Feinstein JS et al. Lorazepam dose-dependently decreases risk-taking related activation in limbic areas. Psychopharmacology (Berl) 2006; 189: (1): 105–16.
28. Aupperle RL, Ravindran L, Tankersley D et al. Pregabalin influences insula and amygdala activation during anticipation of emotional images. Neuropsychopharmacology 2011; 36 (7): 1466–77.
29. Ball TM, Ramsawh HJ, Campbell-Sills L et al. Prefrontal dysfunction during emotion regulation in generalized anxiety and panic disorders. Psychol Med 2012.10.1017/S0033291712002383): 1–12.
30. Hariri AR, Mattay VS, Tessitore A et al. Serotonin transporter genetic variation and the response of the human amygdala. Science 2002; 297 (5580): 400–3.
31. Zhou Z, Zhu G, Hariri AR et al. Genetic variation in human NPY expression affects stress response and emotion. Nature 2008; 452 (7190): 997–1001.
32. Domschke K, Reif A, Weber H et al. Neuropeptide S receptor gene – converging evidence for a role in panic disorder. Mol Psychiatry 2011; 16 (9.): 938–48.
33. Domschke K, Braun M, Ohrmann P et al. Association of the functional -1019C/G 5-HT1A polymorphism with prefrontal cortex and amygdala activation measured with 3 T fMRI in panic disorder. Int J Neuropsychopharmacol 2006; 9 (3): 349–55.
34. Lohoff FW, Aquino TD, Narasimhan S et al. Serotonin receptor 2A (HT2A) gene polymorphism predicts treatment response to venlafaxine XR in generalized anxiety disorder. Pharmacogenomics J 2013; 13 (1): 21–6.
35. Lenze EJ, Goate AM, Nowotny P et al. Relation of serotonin transporter genetic variation to efficacy of escitalopram for generalized anxiety disorder in older adults. J Clin Psychopharmacol 2010; 30 (6): 672–7.
36. Perna G, Favaron E, Di Bella D et al. Antipanic efficacy of paroxetine and polymorphism within the promoter of the serotonin transporter gene. Neuropsychopharmacology 2005; 30 (12): 2230–5.
37. Baffa A, Hohoff C, Baune BT et al. Norepinephrine and serotonin transporter genes: impact on treatment response in depression. Neuropsychobiology 2010; 62 (2) 121–31.


