Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№03 2010
Эффективность и переносимость Лирики при фармакорезистентной эпилепсии у взрослых №03 2010
Номера страниц в выпуске:8-12
Эпилепсия является распространенным неврологическим заболеванием с числом заболевших порядка 50 млн во всем мире. Хотя больные эпилепсией могут со временем излечиваться, приблизительно у 20–30% всех пациентов заболевание будет пожизненным. Многие пациенты с эпилепсией имеют сопутствующие поведенческие, неврологические и интеллектуальные нарушения.
Эпилепсия является распространенным неврологическим заболеванием с числом заболевших порядка 50 млн во всем мире [4, 6, 14]. Хотя больные эпилепсией могут со временем излечиваться, приблизительно у 20–30% всех пациентов заболевание будет пожизненным. Многие пациенты с эпилепсией имеют сопутствующие поведенческие, неврологические и интеллектуальные нарушения.
Патофизиология большинства форм эпилепсии остается недостаточно изученной, однако общеизвестно, что эпилептические припадки происходят из чрезмерно синхронизированной и продолжительно разряжающейся группы нейронов. Характерной чертой всех эпилептических синдромов является персистирующее увеличение нейрональной возбудимости. Базисные противоэпилептические препараты (ПЭП) снижают нейрональную мембранную возбудимость, воздействуя на ионные каналы (натриевые, калиевые, кальциевые, хлорные) или на нейротрансмиттерные рецепторные комплексы (главным образом на усиление ГАМКергической нейротрансмиссии или ослабление глутаматной системы).
В настоящее время фармакотерапия ПЭП парциальных форм эпилепсии остается важной проблемой клинической эпилептологии. Большинство ПЭП, воздействуя на центральную нервную систему, имеет сходные побочные эффекты, такие как седация, сонливость, нистагм, тремор, атаксия и др. Специфические побочные эффекты являются результирующей фармакокинетики и фармакодинамики ПЭП, с одной стороны, и индивидуальных особенностей организма пациента – с другой, что требует порой кропотливого подбора индивидуальных терапевтических режимов для каждого пациента.
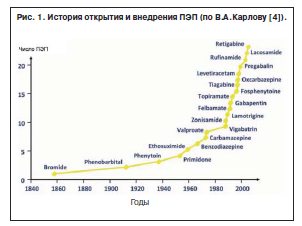
Однако до сих пор до 20–30% пациентов остаются фармакорезистентными при лечении традиционными ПЭП [8, 18]. Попытки понизить уровень фармакорезистентных форм эпилепсии и улучшить переносимость ПЭП привели к массовому направленному поиску новых ПЭП. В последние 10–15 лет были созданы и начали активно внедряться в клиническую практику несколько новых ПЭП: габапентин, ламотриджин, топирамат, леветирацетам, окскарбазепин, прегабалин и др. (рис. 1).
Одним из самых последних ПЭП является прегабалин (лицензированное торговое название – Лирика).
Механизм действия
Прегабалин является S-энантомером 3-(аминометил)-5-метилгексановой кислоты [(S)-3-(aminomethyl)-5-methylhexanoic acid] (рис. 2).
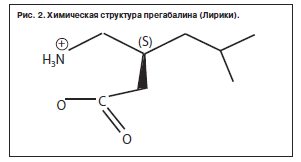
Прегабалин, как и габапентин, относится к тому же классу средств, имеющих высокую аффинность к α2-σ-субъединице нейронального потенциалозависимого кальциевого канала [9, 22, 23], результатом связывания прегабалина с данным лигандом является снижение индуцированного деполяризацией втока Ca2+ в нервные терминали с последующим снижением высвобождения возбуждающих нейротрансмиттеров (глутамата, субстанции Р, норадреналина) из синаптической щели [5, 17]. Прегабалин представляет собой дериват ГАМК и является по сути его аналогом, однако активно не влияет на ГАМК. Особенность препарата заключается в воздействии только на патологически измененные нейроны и отсутствие влияния на нормально функционирующие нейроны. Перечисленные механизмы действия прегабалина обусловливают его противоэпилептический, анальгетический и анксиолитический эффекты [10, 11, 13].
Прегабалин имеет благоприятный фармакокинетический профиль. Подробные данные по фармакокинетике прегабалина и ее клинической значимости представлены в табл. 1.
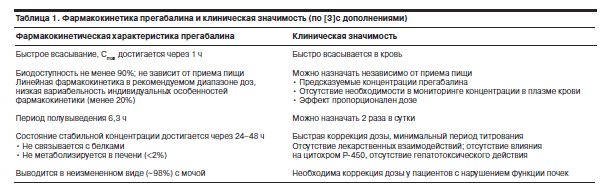
У прегабалина (Лирики) предсказуемая концентрация в плазме крови, отсутствуют лекарственные взаимодействия (см. табл. 1). В 2007 г. T.May и соавт. с помощью терапевтического лекарственного мониторинга исследовали влияние дозы прегабалина, возраста больных и сопутствующих препаратов на его плазменную концентрацию у 167 взрослых пациентов с парциальной эпилепсией с вторичной генерализацией или без таковой при наиболее часто встречаемых комбинациях ПЭП (n=97). В ходе исследования авторами показано, что концентрации прегабалина были ниже при комбинации с энзиминдуцирующими ПЭП (фенитоином, карбамазепином, окскарбазепином) и были возрастзависимы (выше у пожилых пациентов). Так, энзиминдуцирующие ПЭП (такие как карбамазепин) могут умеренно снижать плазменную концентрацию прегабалина (приблизительно на 20–30%). Повышение концентрации прегабалина в плазме крови у пожилых пациентов объяснялось авторами замедлением преимущественной почечной экскрецией препарата [21].
В клинических исследованиях показаны высокая эффективность Лирики (прегабалин) при эпилепсии (в качестве аддитивного препарата), при лечении нейропатической боли и терапии генерализованного тревожного расстройства. Эффективные пероральные дозы прегабалина находятся в диапазоне 150–600 мг/сут [1, 3, 17 и др].
Безопасность и переносимость
Прегабалин достаточно хорошо переносился. Объединенные данные всех контролируемых испытаний препарата оценивают суммарную частоту регистрации побочных явлений у 13% пациентов, принимающих прегабалин, в сравнении с 7% для плацебо [20]. Наиболее частыми побочными эффектами были головокружение (28,9% против 9% для плацебо) и сонливость (23,7% против 8,8% соответственно). Также побочные эффекты со стороны центральной нервной системы включали парестезию и атаксию. Другими побочными эффектами были периферический отек и увеличение массы тела пациента, однако частота их возникновения не превышала 1%. В настоящее время данные о пригодности и безопасности прегабалина во время беременности отсутствуют [17, 24]. Подробный обзор литературы о политерапии парциальной эпилепсии с применением прегабалина представлен в работе С.Г.Бурда и соавт. (2009 г.) [2].
Результаты собственных наблюдений
Прегабалин в качестве дополнительного ПЭП был применен у 11 пациентов с парциальной фармакорезистентной эпилепсией в возрасте 18–30 лет. Истинная фармакорезистентность характеризовалась использованием не менее 4 схем терапии в качестве моно- и политерапии при применении максимально переносимых суточных дозировках ПЭП, несмотря на которые парциальные с вторичной генерализацией приступы продолжали регистрироваться с частотой более 2–3 раз в месяц. Двое пациентов до введения в схему прегабалина получали один препарат, 8 – 2 ПЭП и один пациент – 3 ПЭП (ранее все пациенты получали барбитураты, карбамазепины, гидантоины, вальпроаты, топирамат, леветирацетам). Наиболее часто в качестве базисной терапии применялись вальпроаты, карбамазепины, топирамат, леветирацетам и их сочетания. Криптогенная эпилепсия выявлена в 9 случаях и в 2 – симптоматическая. В 10 наблюдениях длительность заболевания составила более 5 лет, в одном – 2 года. Максимальная длительность применения прегабалина в качестве дополнительного ПЭП – 16 мес. Суточные дозировки прегабалина составляли 150–450 мг, распределенные равномерно на 2 приема. Титрация дозы начиналась с 75 мг 2 раза в сутки начиная с вечернего приема. В дальнейшем доза увеличивалась еженедельно на 150 мг до максимальной. К концу периода наблюдения продолжали принимать прегабалин 8 пациентов с длительностью приема не менее 6 мес.
Препарат проявил высокую эффективность в качестве дополнительного ПЭП: ремиссия отмечена в 3 наблюдениях – все пациенты с криптогенной парциальной эпилепсией лобной и височной локализации. Из них у 2 пациентов наблюдались парциальные и вторично генерализованные припадки бодрствования, а в одном случае – исключительно вторично генерализованные припадки сна (наблюдение с коротким анамнезом по эпилепсии – 2 года). Снижение частоты припадков более 50% зарегистрировано у 7 пациентов, однако в 2 наблюдениях эффект был нестойким: в одном случае приступы вновь участились через 2 мес приема, в другом – через 4 мес и в дальнейшем прегабалин был отменен.
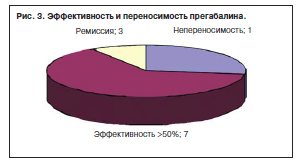
Исходная эффективность Лирики оценивалась через 1 мес после 1-го визита (рис. 3).
К концу периода наблюдения (16 мес) 3 пациентки не принимали прегабалин: 2 – в связи с нестойкостью клинического эффекта от комбинированной терапии и 1 – в результате побочных явлений после однократного приема препарата. Случай нестойкого эффекта Лирики с префронтальной эпилепсией, полиморфными припадками высокой частоты и выраженными изменениями личности в виде грубых дисфорических расстройств характеризовался достижением существенного эффекта при суточной дозе 300 мг прегабалина, однако когда вновь была зарегистрирована тенденция к учащению припадков, дозировка прегабалина была доведена до 450 мг/сут и от дальнейшего увеличения дозировки, несмотря на отсутствие побочных явлений, пациентка отказалась. Исходно пациентка получала вальпроаты в суточной дозе 2500 мг и фенобарбитал 200 мг. Эффект терапии был преходящим: на протяжении титрации дозы и последующих 2 мес наблюдения удалось снизить частоту припадков более чем на 50%, однако в дальнейшем частота приступов вновь стала нарастать и через 4 мес суммарного приема прегабалин был отменен. В другом наблюдении пациентка совместно с мамой решили отменить препарат «ввиду его недостаточной эффективности» при применении максимальной суточной дозировки всего 150 мг. Особенностью данного наблюдения являлось то, что пациентка «плохо переносила любой ПЭП» в среднетерапевтических дозах, больная и ее родственники отмечали и утверждали, что титрация доз в районе среднетерапевтических обычно приводит к парадоксальному учащению эпилептических приступов, и лечащему врачу обычно заявляли, что увеличение дозировки приводит к парадоксальному эффекту – учащению припадков, в результате чего максимально переносимые дозировки практически ни одного ПЭП апробированы не были.
Все случаи побочных явлений регистрировались после приема хотя бы одной дозы прегабалина. Фактически у одной из пациенток причиной отказа явилась выраженная сонливость после применения первой дозы препарата (75 мг на ночь), которая наблюдалась 15 ч. У пациентки наблюдалась префронтальная эпилепсия с частыми вторично генерализованными судорожными припадками сна и сопутствующим выраженным астеноневрастеническим синдромом. Еще в 2 наблюдениях пациенты отмечали преходящую, длящуюся до 3–5 сут легкую сонливость во время титрации дозы (до 150 мг/сут), что потребовало более медленной титрации прегабалина.
К положительным качествам препарата следует отнести его анксиолитическое действие, которое отмечали практически все пациенты. Чрезвычайно интересным мы считаем наблюдение по применению Лирики в качестве дополнительного препарата при мигрень-эпилепсии у молодого мужчины 19 лет, наблюдавшегося нами на протяжении 3 лет по поводу сложных парциальных припадков, начинающихся с типичных приступов «мигрени с аурой» в виде исчезновения четкости зрения с последующей пульсирующей головной болью височно-лобной локализации и потерей сознания на десятки секунд без вторичной генерализации. Вторично генерализованные припадки на протяжении всего заболевания зарегистрированы в единичных случаях. Также у больного до нескольких раз в неделю регистрировались головные боли напряжения. В разные периоды назначался вазобрал, топирамат. На момент назначения прегабалина пациент получал 200 мг/сут топирамата и 1800 мг/сут трилептала, на фоне приема которых приступы регистрировались с частотой более 4 раз в месяц. Назначение Лирики в суточной дозировке 300 мг привело к 4-месячной ремиссии приступов. К настоящему времени Лирика принимается на протяжении 6 мес: отмечен всего однократный парциальный приступ на фоне длительного переутомления. За это время приступы мигрени не регистрировались, головная боль напряжения отмечалась не больше 4 раз с малой интенсивностью. Сопутствующий астеноневрастенический синдром полностью регрессировал. Учитывая хорошую переносимость прегабалина, при последнем обращении пациента дозировка препарата была увеличена до 450 мг/сут. Также на время сдачи статьи в печать у одной пациентки с фармакорезистентной эпилепсией на политерапии с включением 300 мг Лирики на ночь благоприятно протекала беременность на сроке 34–35 нед. Ультразвуковое исследование плода, показатели фетоплацентарного комплекса и данные кардиотокографии свидетельствовали об адекватном развитии плода в соответствии со сроками гестации.
В результате проведенной работы установлена эффективность использования прегабалина в качестве дополнительной терапии у пациентов с симптоматической фокальной эпилепсией с частыми, резистентными к лечению полиморфными приступами, получающих в качестве базового лечения различные ПЭП в высоких дозах, что согласуется с результатами исследования И.И.Бондаренко (2008 г.), проведенного у 50 пациентов Санкт-Петербургского эпилептологического центра с симптоматической парциальной эпилепсией с частыми полиморфными припадками с базовой терапией карбамазепином (1500–2000 мг/сут) или вальпроатами (2000–3000 мг/сут). В исследовании прегабалин назначался в качестве аддитивного средства в суточных дозах 300 и 600 мг. Автором выявлено статистически значимое снижение частоты приступов уже с 1-го месяца лечения прегабалином как в комбинации с вальпроатами, так и в сочетании с карбамазепином при более высокой эффективности комбинации вальпроатов и прегабалина в дозе 600 мг/сут. Отмечена хорошая переносимость прегабалина, что согласуется с данными, полученными в настоящем исследовании. Побочные эффекты (транзиторные сонливость и головокружение, замедление скорости ассоциативных процессов и ослабление концентрации внимания), присутствовавшие у некоторых больных во время титрования дозы, в дальнейшем регрессировали [1].
Результаты рандомизированных плацебо-контролируемых исследований демонстрируют высокую эффективность прегабалина в качестве дополнительного препарата в терапии взрослых пациентов для контроля парциальных припадков с вторичной генерализацией или без таковой [7, 19, 25]. Прегабалин в этих исследованиях не воздействовал на плазменные концентрации сопутствующих назначенных лекарственных средств, его эффективность не может быть объяснена фармакокинетическими взаимодействиями с базовыми ПЭП.
В исследованиях короткой длительности прегабалин редуцировал частоту припадков в дозах от 150 до 600 мг/сут с отчетливой зависимостью реакции от дозы и с быстрым началом действия. Возникшая эффективность была постоянной в течение длительной терапии, с неотчетливым подтверждением о развившейся толерантности в течение последовательного 4-летнего периода. В продолжительном открытом исследовании около 8% пациентов, леченных прегабалином, были свободны от припадков в течение последних 6 мес наблюдения и 3,7% находились в ремиссии в течение предшествовавших 12 мес [24]. Таким образом, прегабалин может быть препаратом выбора в качестве аддитивного терапевтического средства для клиницистов, беспокоящихся о длительной курации пациентов с рефрактерной парциальной эпилепсией.
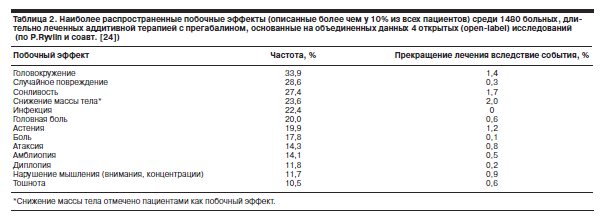
В исследованиях с фиксированной дозой препарата головокружение и седация были наиболее частыми дозолимитирующими побочными событиями. Встречаемые побочные эффекты у пациентов, принимающих прегабалин как аддитивное средство, представлены в табл. 2.
В наших наблюдениях выраженная сонливость в 1 случае, потребовавшая отмены прегабалина, расценена как особенность индивидуальной чувствительности к препарату, в 2 остальных случаях легкая сонливость была преходящей, дозозависимой на этапе титрации препарата.
Несмотря на то что большинство пациентов могут переносить дозы 600 мг/сут без титрования, переносимость лекарственного препарата отчетливо повышалась при постепенном титровании дозы и индивидуальном подборе дозы в соответствии с клиническим ответом [12]. При этом может быть использован режим 3-кратного дозирования с целью улучшения переносимости высоких дозировок прегабалина [24].
Показано, что прегабалин не может применяться у пациентов с первично генерализованными эпилепсиями, так как может даже аггравировать у них припадки. Особенно это касается синдрома прогрессирующей миоклонической эпилепсии [16]. В более ранней работе H.J.Huppertz и соавт. (2001 г.) также показана относительно высокая доля (у 4 из 19 пациентов) появления миоклонуса, ассоциированного с аддитивной терапией прегабалином у фармакорезистентных больных фокальной эпилепсией [15].
В качестве других показаний подтверждена эффективность прегабалина в терапии генерализованного тревожного расстройства и нейропатической боли, поэтому кандидатами для фармакотерапии прегабалином будут особенно пациенты с этими коморбидными состояниями. Наше наблюдение свидетельствует о потенциальной эффективности Лирики при мигрень-эпилепсии, а возможно, и при мигрени без сопутствующей эпилепсии, однако требуется проведение дальнейших исследований и накопление фактического материала.
Согласно полученным данным в настоящем исследовании эффективной стартовой дозой могут быть 150 мг/сут, разделенные на 2 приема, без необходимости исходного титрования. Для усиления эффективности могут быть использованы дозы 300 и 600 мг/сут, однако максимально достигнутая суточная доза препарата в нашем исследовании была ограничена 450 мг. По нашему мнению, гибкое повышение дозы препарата в соотношении с эффективностью и переносимостью выглядит наилучшей стратегией для обеспечения оптимального клинического ответа. Однако нам не удалось установить специфические факторы, которые могли бы быть полезными для прогнозирования эффективности прегабалина.
Таким образом, многочисленные клинические публикации и наш скромный опыт применения препарата свидетельствуют о том, что прегабалин оказался эффективным в терапии парциальных фармакорезистентных эпилепсий, практически с 1-й недели применения; более чем у 25% пациентов удалось достичь медикаментозной ремиссии на период более полугода, а у всех остальных – урежение приступов более чем на 50%; препарат оказался эффективным уже начиная с дозировки 150 мг/сут независимо от количества и фармакокинетических характеристик базовых ПЭП. Среди побочных эффектов у 25% пациентов отмечена преходящая сонливость, и лишь в одном наблюдении сонливость ввиду ее выраженности и стойкости потребовала отмены препарата. Особенностью настоящего исследования явилось то, что, несмотря на фармакорезистентные случаи, потребовалась умеренная максимальная терапевтическая суточная дозировка препарата, которая не превышала 450 мг.
Применяя препарат впервые, врач ориентируется на результаты опубликованных ранее исследований и при накоплении собственного опыта в случае недостаточного эффекта препарата или тяжелых побочных явлений в дальнейшей своей практике будет избегать применения такого лекарственного средства. Проведенный анализ собственных наблюдений эффективности и переносимости прегабалина (Лирики) при фармакорезистентной эпилепсии позволяет предполагать дальнейшее широкое внедрение препарата при парциальной эпилепсии, а такие свойства прегабалина, как циркуляция в плазме крови в свободном виде (несвязываемость с транспортными протеинами), неметаболизируемость, высокая эффективность, хорошая переносимость и 2-кратный прием, делают его высокоперспективным в терапии парциальной эпилепсии у взрослых.
Патофизиология большинства форм эпилепсии остается недостаточно изученной, однако общеизвестно, что эпилептические припадки происходят из чрезмерно синхронизированной и продолжительно разряжающейся группы нейронов. Характерной чертой всех эпилептических синдромов является персистирующее увеличение нейрональной возбудимости. Базисные противоэпилептические препараты (ПЭП) снижают нейрональную мембранную возбудимость, воздействуя на ионные каналы (натриевые, калиевые, кальциевые, хлорные) или на нейротрансмиттерные рецепторные комплексы (главным образом на усиление ГАМКергической нейротрансмиссии или ослабление глутаматной системы).
В настоящее время фармакотерапия ПЭП парциальных форм эпилепсии остается важной проблемой клинической эпилептологии. Большинство ПЭП, воздействуя на центральную нервную систему, имеет сходные побочные эффекты, такие как седация, сонливость, нистагм, тремор, атаксия и др. Специфические побочные эффекты являются результирующей фармакокинетики и фармакодинамики ПЭП, с одной стороны, и индивидуальных особенностей организма пациента – с другой, что требует порой кропотливого подбора индивидуальных терапевтических режимов для каждого пациента.

Однако до сих пор до 20–30% пациентов остаются фармакорезистентными при лечении традиционными ПЭП [8, 18]. Попытки понизить уровень фармакорезистентных форм эпилепсии и улучшить переносимость ПЭП привели к массовому направленному поиску новых ПЭП. В последние 10–15 лет были созданы и начали активно внедряться в клиническую практику несколько новых ПЭП: габапентин, ламотриджин, топирамат, леветирацетам, окскарбазепин, прегабалин и др. (рис. 1).
Одним из самых последних ПЭП является прегабалин (лицензированное торговое название – Лирика).
Механизм действия
Прегабалин является S-энантомером 3-(аминометил)-5-метилгексановой кислоты [(S)-3-(aminomethyl)-5-methylhexanoic acid] (рис. 2).

Прегабалин, как и габапентин, относится к тому же классу средств, имеющих высокую аффинность к α2-σ-субъединице нейронального потенциалозависимого кальциевого канала [9, 22, 23], результатом связывания прегабалина с данным лигандом является снижение индуцированного деполяризацией втока Ca2+ в нервные терминали с последующим снижением высвобождения возбуждающих нейротрансмиттеров (глутамата, субстанции Р, норадреналина) из синаптической щели [5, 17]. Прегабалин представляет собой дериват ГАМК и является по сути его аналогом, однако активно не влияет на ГАМК. Особенность препарата заключается в воздействии только на патологически измененные нейроны и отсутствие влияния на нормально функционирующие нейроны. Перечисленные механизмы действия прегабалина обусловливают его противоэпилептический, анальгетический и анксиолитический эффекты [10, 11, 13].
Прегабалин имеет благоприятный фармакокинетический профиль. Подробные данные по фармакокинетике прегабалина и ее клинической значимости представлены в табл. 1.

У прегабалина (Лирики) предсказуемая концентрация в плазме крови, отсутствуют лекарственные взаимодействия (см. табл. 1). В 2007 г. T.May и соавт. с помощью терапевтического лекарственного мониторинга исследовали влияние дозы прегабалина, возраста больных и сопутствующих препаратов на его плазменную концентрацию у 167 взрослых пациентов с парциальной эпилепсией с вторичной генерализацией или без таковой при наиболее часто встречаемых комбинациях ПЭП (n=97). В ходе исследования авторами показано, что концентрации прегабалина были ниже при комбинации с энзиминдуцирующими ПЭП (фенитоином, карбамазепином, окскарбазепином) и были возрастзависимы (выше у пожилых пациентов). Так, энзиминдуцирующие ПЭП (такие как карбамазепин) могут умеренно снижать плазменную концентрацию прегабалина (приблизительно на 20–30%). Повышение концентрации прегабалина в плазме крови у пожилых пациентов объяснялось авторами замедлением преимущественной почечной экскрецией препарата [21].
В клинических исследованиях показаны высокая эффективность Лирики (прегабалин) при эпилепсии (в качестве аддитивного препарата), при лечении нейропатической боли и терапии генерализованного тревожного расстройства. Эффективные пероральные дозы прегабалина находятся в диапазоне 150–600 мг/сут [1, 3, 17 и др].
Безопасность и переносимость
Прегабалин достаточно хорошо переносился. Объединенные данные всех контролируемых испытаний препарата оценивают суммарную частоту регистрации побочных явлений у 13% пациентов, принимающих прегабалин, в сравнении с 7% для плацебо [20]. Наиболее частыми побочными эффектами были головокружение (28,9% против 9% для плацебо) и сонливость (23,7% против 8,8% соответственно). Также побочные эффекты со стороны центральной нервной системы включали парестезию и атаксию. Другими побочными эффектами были периферический отек и увеличение массы тела пациента, однако частота их возникновения не превышала 1%. В настоящее время данные о пригодности и безопасности прегабалина во время беременности отсутствуют [17, 24]. Подробный обзор литературы о политерапии парциальной эпилепсии с применением прегабалина представлен в работе С.Г.Бурда и соавт. (2009 г.) [2].
Результаты собственных наблюдений
Прегабалин в качестве дополнительного ПЭП был применен у 11 пациентов с парциальной фармакорезистентной эпилепсией в возрасте 18–30 лет. Истинная фармакорезистентность характеризовалась использованием не менее 4 схем терапии в качестве моно- и политерапии при применении максимально переносимых суточных дозировках ПЭП, несмотря на которые парциальные с вторичной генерализацией приступы продолжали регистрироваться с частотой более 2–3 раз в месяц. Двое пациентов до введения в схему прегабалина получали один препарат, 8 – 2 ПЭП и один пациент – 3 ПЭП (ранее все пациенты получали барбитураты, карбамазепины, гидантоины, вальпроаты, топирамат, леветирацетам). Наиболее часто в качестве базисной терапии применялись вальпроаты, карбамазепины, топирамат, леветирацетам и их сочетания. Криптогенная эпилепсия выявлена в 9 случаях и в 2 – симптоматическая. В 10 наблюдениях длительность заболевания составила более 5 лет, в одном – 2 года. Максимальная длительность применения прегабалина в качестве дополнительного ПЭП – 16 мес. Суточные дозировки прегабалина составляли 150–450 мг, распределенные равномерно на 2 приема. Титрация дозы начиналась с 75 мг 2 раза в сутки начиная с вечернего приема. В дальнейшем доза увеличивалась еженедельно на 150 мг до максимальной. К концу периода наблюдения продолжали принимать прегабалин 8 пациентов с длительностью приема не менее 6 мес.
Препарат проявил высокую эффективность в качестве дополнительного ПЭП: ремиссия отмечена в 3 наблюдениях – все пациенты с криптогенной парциальной эпилепсией лобной и височной локализации. Из них у 2 пациентов наблюдались парциальные и вторично генерализованные припадки бодрствования, а в одном случае – исключительно вторично генерализованные припадки сна (наблюдение с коротким анамнезом по эпилепсии – 2 года). Снижение частоты припадков более 50% зарегистрировано у 7 пациентов, однако в 2 наблюдениях эффект был нестойким: в одном случае приступы вновь участились через 2 мес приема, в другом – через 4 мес и в дальнейшем прегабалин был отменен.

Исходная эффективность Лирики оценивалась через 1 мес после 1-го визита (рис. 3).
К концу периода наблюдения (16 мес) 3 пациентки не принимали прегабалин: 2 – в связи с нестойкостью клинического эффекта от комбинированной терапии и 1 – в результате побочных явлений после однократного приема препарата. Случай нестойкого эффекта Лирики с префронтальной эпилепсией, полиморфными припадками высокой частоты и выраженными изменениями личности в виде грубых дисфорических расстройств характеризовался достижением существенного эффекта при суточной дозе 300 мг прегабалина, однако когда вновь была зарегистрирована тенденция к учащению припадков, дозировка прегабалина была доведена до 450 мг/сут и от дальнейшего увеличения дозировки, несмотря на отсутствие побочных явлений, пациентка отказалась. Исходно пациентка получала вальпроаты в суточной дозе 2500 мг и фенобарбитал 200 мг. Эффект терапии был преходящим: на протяжении титрации дозы и последующих 2 мес наблюдения удалось снизить частоту припадков более чем на 50%, однако в дальнейшем частота приступов вновь стала нарастать и через 4 мес суммарного приема прегабалин был отменен. В другом наблюдении пациентка совместно с мамой решили отменить препарат «ввиду его недостаточной эффективности» при применении максимальной суточной дозировки всего 150 мг. Особенностью данного наблюдения являлось то, что пациентка «плохо переносила любой ПЭП» в среднетерапевтических дозах, больная и ее родственники отмечали и утверждали, что титрация доз в районе среднетерапевтических обычно приводит к парадоксальному учащению эпилептических приступов, и лечащему врачу обычно заявляли, что увеличение дозировки приводит к парадоксальному эффекту – учащению припадков, в результате чего максимально переносимые дозировки практически ни одного ПЭП апробированы не были.
Все случаи побочных явлений регистрировались после приема хотя бы одной дозы прегабалина. Фактически у одной из пациенток причиной отказа явилась выраженная сонливость после применения первой дозы препарата (75 мг на ночь), которая наблюдалась 15 ч. У пациентки наблюдалась префронтальная эпилепсия с частыми вторично генерализованными судорожными припадками сна и сопутствующим выраженным астеноневрастеническим синдромом. Еще в 2 наблюдениях пациенты отмечали преходящую, длящуюся до 3–5 сут легкую сонливость во время титрации дозы (до 150 мг/сут), что потребовало более медленной титрации прегабалина.
К положительным качествам препарата следует отнести его анксиолитическое действие, которое отмечали практически все пациенты. Чрезвычайно интересным мы считаем наблюдение по применению Лирики в качестве дополнительного препарата при мигрень-эпилепсии у молодого мужчины 19 лет, наблюдавшегося нами на протяжении 3 лет по поводу сложных парциальных припадков, начинающихся с типичных приступов «мигрени с аурой» в виде исчезновения четкости зрения с последующей пульсирующей головной болью височно-лобной локализации и потерей сознания на десятки секунд без вторичной генерализации. Вторично генерализованные припадки на протяжении всего заболевания зарегистрированы в единичных случаях. Также у больного до нескольких раз в неделю регистрировались головные боли напряжения. В разные периоды назначался вазобрал, топирамат. На момент назначения прегабалина пациент получал 200 мг/сут топирамата и 1800 мг/сут трилептала, на фоне приема которых приступы регистрировались с частотой более 4 раз в месяц. Назначение Лирики в суточной дозировке 300 мг привело к 4-месячной ремиссии приступов. К настоящему времени Лирика принимается на протяжении 6 мес: отмечен всего однократный парциальный приступ на фоне длительного переутомления. За это время приступы мигрени не регистрировались, головная боль напряжения отмечалась не больше 4 раз с малой интенсивностью. Сопутствующий астеноневрастенический синдром полностью регрессировал. Учитывая хорошую переносимость прегабалина, при последнем обращении пациента дозировка препарата была увеличена до 450 мг/сут. Также на время сдачи статьи в печать у одной пациентки с фармакорезистентной эпилепсией на политерапии с включением 300 мг Лирики на ночь благоприятно протекала беременность на сроке 34–35 нед. Ультразвуковое исследование плода, показатели фетоплацентарного комплекса и данные кардиотокографии свидетельствовали об адекватном развитии плода в соответствии со сроками гестации.
В результате проведенной работы установлена эффективность использования прегабалина в качестве дополнительной терапии у пациентов с симптоматической фокальной эпилепсией с частыми, резистентными к лечению полиморфными приступами, получающих в качестве базового лечения различные ПЭП в высоких дозах, что согласуется с результатами исследования И.И.Бондаренко (2008 г.), проведенного у 50 пациентов Санкт-Петербургского эпилептологического центра с симптоматической парциальной эпилепсией с частыми полиморфными припадками с базовой терапией карбамазепином (1500–2000 мг/сут) или вальпроатами (2000–3000 мг/сут). В исследовании прегабалин назначался в качестве аддитивного средства в суточных дозах 300 и 600 мг. Автором выявлено статистически значимое снижение частоты приступов уже с 1-го месяца лечения прегабалином как в комбинации с вальпроатами, так и в сочетании с карбамазепином при более высокой эффективности комбинации вальпроатов и прегабалина в дозе 600 мг/сут. Отмечена хорошая переносимость прегабалина, что согласуется с данными, полученными в настоящем исследовании. Побочные эффекты (транзиторные сонливость и головокружение, замедление скорости ассоциативных процессов и ослабление концентрации внимания), присутствовавшие у некоторых больных во время титрования дозы, в дальнейшем регрессировали [1].
Результаты рандомизированных плацебо-контролируемых исследований демонстрируют высокую эффективность прегабалина в качестве дополнительного препарата в терапии взрослых пациентов для контроля парциальных припадков с вторичной генерализацией или без таковой [7, 19, 25]. Прегабалин в этих исследованиях не воздействовал на плазменные концентрации сопутствующих назначенных лекарственных средств, его эффективность не может быть объяснена фармакокинетическими взаимодействиями с базовыми ПЭП.
В исследованиях короткой длительности прегабалин редуцировал частоту припадков в дозах от 150 до 600 мг/сут с отчетливой зависимостью реакции от дозы и с быстрым началом действия. Возникшая эффективность была постоянной в течение длительной терапии, с неотчетливым подтверждением о развившейся толерантности в течение последовательного 4-летнего периода. В продолжительном открытом исследовании около 8% пациентов, леченных прегабалином, были свободны от припадков в течение последних 6 мес наблюдения и 3,7% находились в ремиссии в течение предшествовавших 12 мес [24]. Таким образом, прегабалин может быть препаратом выбора в качестве аддитивного терапевтического средства для клиницистов, беспокоящихся о длительной курации пациентов с рефрактерной парциальной эпилепсией.
В исследованиях с фиксированной дозой препарата головокружение и седация были наиболее частыми дозолимитирующими побочными событиями. Встречаемые побочные эффекты у пациентов, принимающих прегабалин как аддитивное средство, представлены в табл. 2.

В наших наблюдениях выраженная сонливость в 1 случае, потребовавшая отмены прегабалина, расценена как особенность индивидуальной чувствительности к препарату, в 2 остальных случаях легкая сонливость была преходящей, дозозависимой на этапе титрации препарата.
Несмотря на то что большинство пациентов могут переносить дозы 600 мг/сут без титрования, переносимость лекарственного препарата отчетливо повышалась при постепенном титровании дозы и индивидуальном подборе дозы в соответствии с клиническим ответом [12]. При этом может быть использован режим 3-кратного дозирования с целью улучшения переносимости высоких дозировок прегабалина [24].
Показано, что прегабалин не может применяться у пациентов с первично генерализованными эпилепсиями, так как может даже аггравировать у них припадки. Особенно это касается синдрома прогрессирующей миоклонической эпилепсии [16]. В более ранней работе H.J.Huppertz и соавт. (2001 г.) также показана относительно высокая доля (у 4 из 19 пациентов) появления миоклонуса, ассоциированного с аддитивной терапией прегабалином у фармакорезистентных больных фокальной эпилепсией [15].
В качестве других показаний подтверждена эффективность прегабалина в терапии генерализованного тревожного расстройства и нейропатической боли, поэтому кандидатами для фармакотерапии прегабалином будут особенно пациенты с этими коморбидными состояниями. Наше наблюдение свидетельствует о потенциальной эффективности Лирики при мигрень-эпилепсии, а возможно, и при мигрени без сопутствующей эпилепсии, однако требуется проведение дальнейших исследований и накопление фактического материала.
Согласно полученным данным в настоящем исследовании эффективной стартовой дозой могут быть 150 мг/сут, разделенные на 2 приема, без необходимости исходного титрования. Для усиления эффективности могут быть использованы дозы 300 и 600 мг/сут, однако максимально достигнутая суточная доза препарата в нашем исследовании была ограничена 450 мг. По нашему мнению, гибкое повышение дозы препарата в соотношении с эффективностью и переносимостью выглядит наилучшей стратегией для обеспечения оптимального клинического ответа. Однако нам не удалось установить специфические факторы, которые могли бы быть полезными для прогнозирования эффективности прегабалина.
Таким образом, многочисленные клинические публикации и наш скромный опыт применения препарата свидетельствуют о том, что прегабалин оказался эффективным в терапии парциальных фармакорезистентных эпилепсий, практически с 1-й недели применения; более чем у 25% пациентов удалось достичь медикаментозной ремиссии на период более полугода, а у всех остальных – урежение приступов более чем на 50%; препарат оказался эффективным уже начиная с дозировки 150 мг/сут независимо от количества и фармакокинетических характеристик базовых ПЭП. Среди побочных эффектов у 25% пациентов отмечена преходящая сонливость, и лишь в одном наблюдении сонливость ввиду ее выраженности и стойкости потребовала отмены препарата. Особенностью настоящего исследования явилось то, что, несмотря на фармакорезистентные случаи, потребовалась умеренная максимальная терапевтическая суточная дозировка препарата, которая не превышала 450 мг.
Применяя препарат впервые, врач ориентируется на результаты опубликованных ранее исследований и при накоплении собственного опыта в случае недостаточного эффекта препарата или тяжелых побочных явлений в дальнейшей своей практике будет избегать применения такого лекарственного средства. Проведенный анализ собственных наблюдений эффективности и переносимости прегабалина (Лирики) при фармакорезистентной эпилепсии позволяет предполагать дальнейшее широкое внедрение препарата при парциальной эпилепсии, а такие свойства прегабалина, как циркуляция в плазме крови в свободном виде (несвязываемость с транспортными протеинами), неметаболизируемость, высокая эффективность, хорошая переносимость и 2-кратный прием, делают его высокоперспективным в терапии парциальной эпилепсии у взрослых.
Список исп. литературыСкрыть список1. Бондаренко И.И. Опыт использования антиконвульсанта прегабалина в качестве вспомогательного средства у больных парциальной формой эпилепсии с полиморфными приступами. Журн. неврол. психиатр. им. С.С.Корсакова. 2008; 108 (10): 73–4.
2. Бурд С.Г., Крикова Е.В., Бадалян О.Л. и др. Прегабалин в политерапии парциальной эпилепсии. Журн. неврол. психиатр. им. С.С.Корсакова. 2009; 109 (7): 96–8.
3. Данилов А.Б., Давыдов О.С. Нейропатическая боль. М.: Боргес, 2007.
4. Карлов В.А. Эпилепсия у детей и взрослых, женщин и мужчин. М.: Медицина, 2010.
5. Arroyo S, Anhut H, Kugler AR et al. Pregabalin 1008-011 International Study Group. Pregabalin add-on treatment: a randomized, double-blind, placebo-controlled, dose-response study in adults with partial seizures. Epilepsia 2004; 45 (1): 20–7.
6. Atlas: Epilepsy Care in the World. World Health Organization, 2005; р. 20–7.
7. Beydoun A, Nasreddine W, Atwch S. Efficacy ant tolerability of pregabalin in partial epilepsy. Expert Rev Neurother 2008; 8: 1013–24.
8. Brodie M. Do we need any more antiepileptic drags? Epilepsy Res 2001; 45: 3–6.
9. Cosford ND, Meinke PT, Stauderman KA, Hess SD. Recent advances in the modulation of voltage-gated ion channels for the treatment of epilepsy. Curr Drug Targets CNS Neurol Disord 2002; 1 (1): 81–104.
10. Dooley DJ, Mieske CA, Borosky SA. Inhibition of K+-evoked glutamate release from rat neocortical and hyppocampal slices by gabapentin. Neurosci Lett 2000; 280: 107–10.
11. Dooley DJ, Donovan CM, Pugsley TA. Stimulus-dependent modulation of [3H] norepinephrine release from rat neocortical slices by gabapentin and pregabalin. J Pharmacol Exp Ther 2000; 295: 1086–93.
12. Elger CEBrodie MJ, Anhut H et al. Pregabalin add-on treatment in patients with partial seizures: a novel evaluation of flexible-dose and fixed-dose treatment in a double-blind, placebo-controlled study. Epilepsia 2005; 46: 1926–36.
13. Fink K, Dooley DJ, Meder WP et al. Inhibition of neuronal Ca(2+) influx by gabapentin and pregabalin in the human neocortex. Neuropharmacol 2002; 42: 229–36.
14. Hauser WA. Incidence and prevalence. In: Engel J Jr, Pedley TA, eds. Epilepsy: A Comprehensive Textbook. Philadelphia: Lippincott-Raven Publishers. 1997; p. 47–57.
15. Huppertz HJ, Feuerstein TJ, Schulze Bonhage A. Myoclonus in epilepsy patients with anticonvulsive add-on therapy with pregabalin. Epilepsia 2001; 42 (6): 790–2.
16. Kalviainen R, Khyuppenen J, Koskenkorva P et al. Clinical picture of EPMI-Unverricht-Lundborg disease. Epilepsia 2008; 49: 549–56.
17. Kwan P. Pregabalin: a new drug for epilepsy, neuropathic pain and anxiety. The Hong Kong Medical Diary 2006; 11 (4): 15–6.
18. Kwan P, Brodie M. Early identification of refractory epilepsy. N Engl J Med 2000; 342: 314–9.
19. Losezadi D, Hemming K, Marson AG. Pregabalin add-on for drug-rasistant partial epilepsy. Cochrane Database Syst Rev 1: CD005612.
20. Lyrica (pregabalin) Prodact Monograph. Pfizer Global Pharmaceuticals. Australia: Pfizer; 2005.
21. May TW, Rambeck B, Neb R, Jürgens U. Serum concentrations of Pregabalin in patients with epilepsy: the influence of dose, age and comedication. Ther Drug Monitor 2007; 29 (6): 789–94.
22. Meldrum BS, Rogawsky MA. Molecular targets for antiepileptic drug development. Neurotherapeutics 2007; 4 (1): 18–61.
23. Rogawsky MA, Bazil CW. New molecular targets for antiepileptic drugs: alpha(2)delta, SV2A, and K(v)7/KCNQ/M potassium channels. Curr Neurol Neurosci Rep 2008; 8 (4): 345–52.
24. Ryvlin P, Perucca E, Rheims S. Pregabalin for the managrment of partial epilepsy. Neuropsych Dis Treat 2008; 4 (6): 1211–24.
25. Ryvlin P, Rheims S, Semah F et al. Meta-Analysis of add-on treatment in drug resistant partial epilepsy: a comprehensive study of 41 randomized controlled trials among 10 AEDs. Neurology 2006; 66 (suppl. 2): A36.

