Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№05 2004
Коаксил: клиническая эффективность и переносимость при депрессии (открытое мультицентровое исследование) №05 2004
Одним из представителей антидепрессантов нового поколения является препарат “Тианептин” (коаксил), созданный фирмой “Сервье” (Франция). В отличие от других антидепрессантов он облегчает обратный захват серотонина пресинаптической мембраной, не оказывая влияния на функцию норадренергической и дофаминергической систем. Установление отчетливых антидепрессивных свойств этого препарата стало одним из аргументов в пользу пересмотра существующей концепции о дефиците серотонинергической системы как основного механизма развития депрессивных состояний. Получены данные, показывающие, что нарушение серотонинергической передачи не играет ключевой роли в развитии депрессии, а отражает лишь одну из стадий депрессивного “каскада” [19], который включает и дисфункцию гипоталамо-гипофизарно-надпочечниковой системы [29].
Эффективность тианептина при депрессии была установлена в ряде сравнительных плацебо-контролируемых исследований. Она сопоставима с таковой при применении трициклических антидепрессантов в средних дозах. Так, двойные слепые сравнительные исследования показали, что тимоаналептическое действие тианептина, применяемого в дозе 25–50 мг/сут, при умеренной и тяжелой непсихотической депрессии сравнимо с действием амитриптилина в дозе 50–100 мг/сут [21, 23, 27], кломипрамина в дозе 100–200 мг/сут [30], имипрамина в дозе 25–200 мг/сут [15, 24], но тианептин лучше переносится. Некоторые авторы [17, 18] подчеркивают эффективность тианептина при тяжелой депрессии и рекуррентном депрессивном расстройстве, при этом отмечается противорецидивная эффективность тианептина при рекуррентной депрессии [18].
Сравнительные исследования эффективности тианептина и селективных ингибиторов обратного захвата серотонина показали, что действие препарата в дозе 25–37 мг/сут сопоставимо с эффектом флуоксетина в дозе 20 мг/сут [13, 28], пароксетина – 20 мг/сут [26, 32], сертралина – 50 мг/сут [31]. Эти данные нашли подтверждение и в результатах метаанализа лечения 1348 пациентов [25].
Оказалось, что тианептин проявляет выраженную эффективность и при тревожной депрессии [21], с успехом применяется при терапии тревожно-депрессивных состояний в позднем возрасте [16], а также в наркологической практике [27].
В России исследования клинической эффективности тианептина касались в большей степени легкой и умеренной депрессии у больных, наблюдавшихся в учреждениях общей медицинской практики [5, 8, 11, 12], при наркологической [6] и неврологической [3] патологии, а также у амбулаторных психически больных [4, 7, 8] и у больных пожилого возраста [1, 10]. Помимо того, в отдельных клинических наблюдениях показана эффективность тианептина при депрессии с соматизированным расстройством, пароксизмальной тревогой, сенестопатиями [2].
Целью настоящего исследования было изучение особенностей тимоаналептического действия и переносимости тианептина у больных с умеренной и тяжелой депрессией.
Материал и методы
Исследование было открытым, несравнительным и проводилось по единой методике в 7 центрах.
В исследование включали стационарных или амбулаторных пациентов в возрасте не моложе 18 лет, подписавших добровольное информированное согласие на участие в нем и имевших по Международной классификации болезней 10-го пересмотра (МКБ-10) следующие диагнозы: депрессивный эпизод умеренной тяжести (F32.1) или тяжелый без психотических симптомов (F32.2); биполярное аффективное расстройство (F31), эпизод умеренной или тяжелой депрессии без психотических симптомов (F31.3 и F31.4). В момент включения суммарный балл по 17 пунктам шкалы Гамильтона (HAM-D) [22] должен был составлять не менее 17, оценка по шкале глобального клинического впечатления (CGI) [21] – не менее 3 баллов.
Критериями исключения являлись: период беременности и лактации у женщин; высокий суицидальный риск; любые клинически значимые заболевания почек, печени, сердечно-сосудистой системы в стадии декомпенсации; нарушения метаболизма или онкологические заболевания, эпилепсия, органические заболевания ЦНС, клинически значимые отклонения от нормы лабораторных показателей, обнаруженные в период скрининга; аллергическая реакция на коаксил в анамнезе или его неэффективность при предыдущей терапии, лекарственная либо алкогольная зависимость в анамнезе; участие в клинических исследованиях в течение последних 3 мес, а также лечение ингибиторами моноаминоксидазы или флуоксетином (2 нед), депо-формами нейролептиков (4 нед), солями лития, препаратами вальпроевой кислоты и карбамазепином (4 нед).
Для больных, принимавших какие-либо психотропные препараты до начала исследования, проводили 7-дневные “лекарственные каникулы” (“wash out”). Допускалось назначение снотворных препаратов для коррекции расстройств сна и анксиолитиков (за исключением алпразолама) при симптомах тревоги, которые могли привести к преждевременному выбыванию из исследования. Проведение психотерапии не допускалось.
В ходе наблюдения выраженность депрессивной симптоматики регистрировали с помощью шкалы Гамильтона (HAM) [23] для депрессии (из 21 пункта, HAM-D21), госпитальной шкалы самооценки тревоги и депрессии (HADS-A и HADS-D) [33], шкалы CGI до назначения препарата (день 0), затем на 7, 14, 21, 28 и 42-й дни терапии (соответственно 1–6-я неделя). На 42-й день лечения пациент проводил самооценку качества жизни.
Регистрировали любые возникающие нежелательные явления с указанием степени их тяжести, времени возникновения и продолжительности. К таким явлениям относили любое неблагоприятное (с медицинской точки зрения) событие, произошедшее с получавшим исследуемый препарат больным вне зависимости от его причинной связи с приемом препарата. Все нежелательные явления в случае их возникновения регистрировались при каждом визите и прослеживались до тех пор, пока они не исчезали или не были адекватно объяснены, даже после завершения больным приема исследуемого препарата.
Во время первого, второго и заключительного визитов регистрировали жизненно важные показатели (артериальное давление, частота сердечных сокращений); при каждом визите определяли массу тела, при вводном визите (ВВ) и заключительном визите анализировали гематологические и биохимические показатели крови.
Тианептин назначали по 12,5 мг 3 раза в день, т.е. по 37,5 мг/сут; пациенты старше 65 лет получали его в суточной дозе 25 мг.
Статистический анализ результатов проводило ЗАО “КлинФармТест” с использованием t-критерия Стьюдента при сравнении количественных случайных величин, распределенных по нормальному закону; непараметрических ранговых критериев при сравнении случайных количественных величин, функция распределения которых существенно отличалась от нормальной; критерия c2 при сравнении случайных качественных или случайных количественных величин, имеющих очень небольшое число значений. Для всех используемых статистических критериев уровень значимости устанавливали равным 5%. Использовали только двусторонние статистические параметры.
Первоначально в исследование были включены 142 пациента, но полностью завершили исследование 124 больных. Основными причинами преждевременного выбывания из исследования были: отзыв согласия – 38,9% (7 больных), ухудшение состояния – 27,8% (5 больных), ошибочное включение – 16,7% (3 больных), неявка, несоблюдение режима – 16,7% (3 больных). В основной группе пациентов были 81 женщина и 43 мужчины. Средний возраст составлял 40,5±1,3 года. Соотношение больных с разными диагнозами по МКБ-10 было следующим: рекуррентное депрессивное расстройство – 71 (57,2%), единичный депрессивный эпизод – 35 (28,2%), биполярное аффективное расстройство – 18 (14,5%). В их числе депрессия умеренной тяжести диагностировалась у 89,5% пациентов, тяжелая депрессия – у 10,5%. Резистентность к предшествующей терапии имелась у 14 (99,9%) больных. Длительность последнего эпизода депрессии до лечения в среднем составила 7,1±1,7 мес.
Исходный средний по группе суммарный балл по HAM-D составлял 24,4±4,0. Средний по группе показатель тяжести депрессивного расстройства по шкале HADS-D составлял 11,1±4,49 балла, по шкале HADS-A – 10,7±3,37 балла. По CGI тяжесть депрессии в большинстве случаев (73,4%) оценивалась как умеренная. Медикаментозное лечение текущего депрессивного эпизода до начала исследования проводилось 63 (44,37%) больным.
Эффективность. Общая эффективность терапии к концу исследования по HAM-D составила 70,4%.
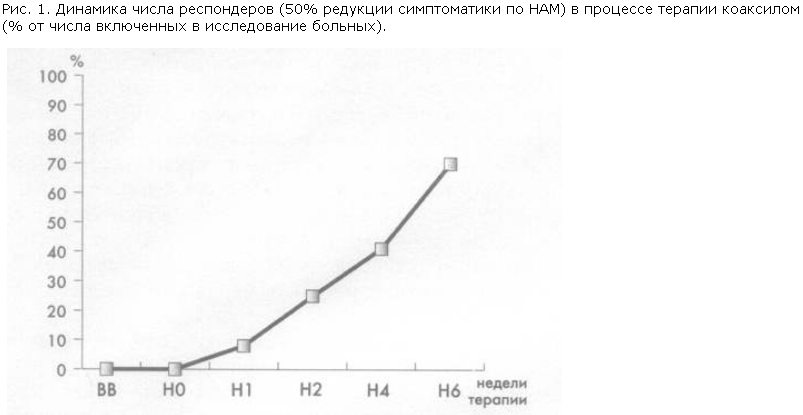
Эффект имел место уже в первые недели лечения и далее нарастал равномерно и поступательно. На 2-й неделе лечения процент больных с положительным ответом на терапию составлял 25,35, а к 4-й неделе превысил 50% барьер (57,04) (рис. 1).
Значительное увеличение числа респондеров к 4-й неделе лечения характерно для большинства антидепрессантов, а поступательное увеличение этого показателя к 6-й неделе терапии позволяет распространить на тианептин общепринятые для других антидепрессантов рекомендации по продолжительности такой терапии не менее 6 нед.
Эти данные подтверждаются и анализом динамики показателей тяжести депрессии по CGI. Положительный эффект (выраженное и существенное улучшение) регистрировался уже в 10-ю неделю терапии и к концу исследования наблюдался у 80,65% пациентов.
Эффект достигался достаточно быстро. У закончивших исследование пациентов суммарный показатель по HAV-D после 1-й недели терапии тианептином с очень высокой степенью достоверности (p<10–27) уменьшился по сравнению с исходным, и в последующем на протяжении всего исследования статистическая значимость его изменений возрастала. Отчетливое тимоаналептическое действие препарата подтверждает также анализ числа пациентов с практически полной редукцией депрессивной симптоматики, у которых суммарный балл по HAM-D составлял не более 10. Как видно из рис. 2, количество больных с полной редукцией депрессивной симптоматики уже в 1-ю неделю терапии составляло 4,23% от числа включенных в исследование пациентов.
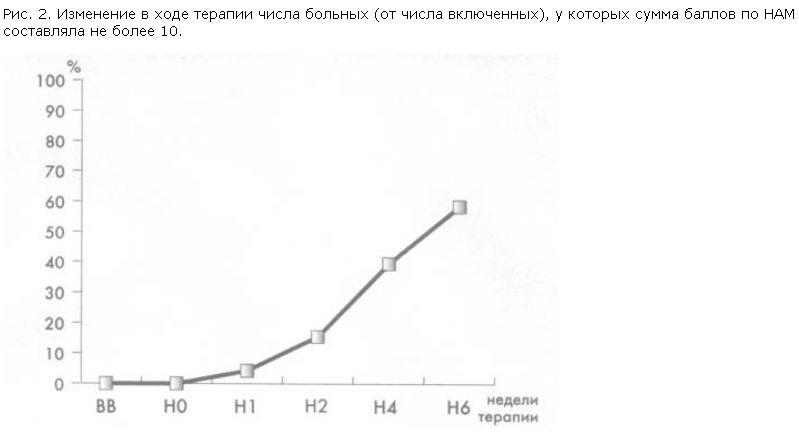
В последующем процент таких пациентов постоянно увеличивался и к концу исследования составлял уже 58,45. Другими словами, через 6 нед терапии почти у 60% больных было зарегистрировано достижение ремиссии. Эти данные, с одной стороны, характеризуют быстроту и полноту тимоаналептического действия препарата, а с другой – говорят о необходимости исключения плацебо-эффекта. С этой целью отдельно была проанализирована динамика показателей течения болезни у тех пациентов, у которых уже в 1-ю неделю терапии наблюдалась полная редукция депрессивной симптоматики. У этих больных эффект сохранялся до 6-й недели лечения, в то время как для плацебо-эффекта, как известно, более характерно его снижение с течение времени [9]. Вместе с тем, принимая во внимание открытый и несравнительный характер исследования, полностью исключить роль плацебо-эффекта в достижении столь высоких показателей эффективности тианептина не представляется возможным. Известно, что эффект плацебо при депрессиях варьирует от 30 до 50% и может быть идентичен таковому наиболее действенных антидепрессантов [14, 20].
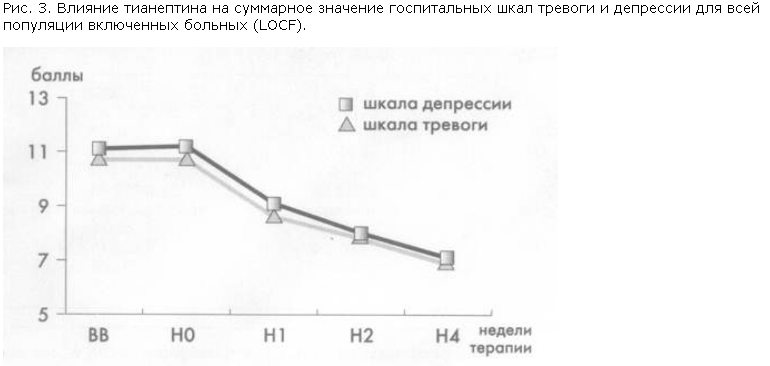
Статистически достоверная редукция показателей тревоги и депрессии по HADS отмечалась уже через 1 нед применения тианептина, и при каждом последующем визите больных значения шкал были достоверно меньшими, чем при предыдущем.
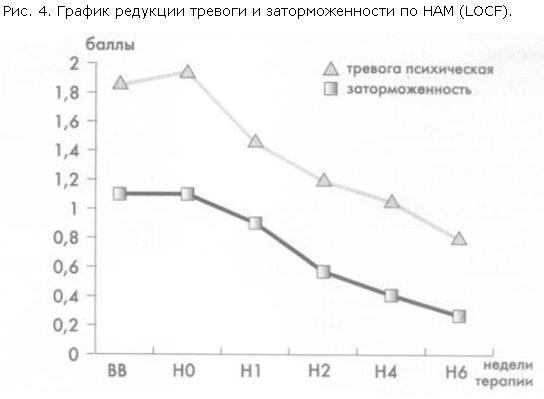
Динамика изменения тяжести состояния по этим шкалам была последовательной и в целом не отличалась от таковой при оценке по шкале HAM-D (рис. 4). Основные показатели, определяющие спектр психотропного действия антидепрессанта (психическая тревога и заторможенность), редуцировались достаточно равномерно, хотя статистически значимая редукция заторможенности определялась несколько позднее симптомов психической тревоги и сниженного настроения, что свидетельствует о сбалансированном характере тимоаналептического действия тианептина с некоторым преобладанием анксиолитических свойств (см. рис. 4).
Интересен тот факт, что быстро редуцировалась не только тревога (выраженный анксиолитический эффект тианептина хорошо известен из ряда предыдущих работ), но и заторможенность. При анализе соотношения редукции этих симптомов было выявлено преобладание редукции тревоги в 1-ю неделю терапии и заторможенности в последующие недели (рис. 5).
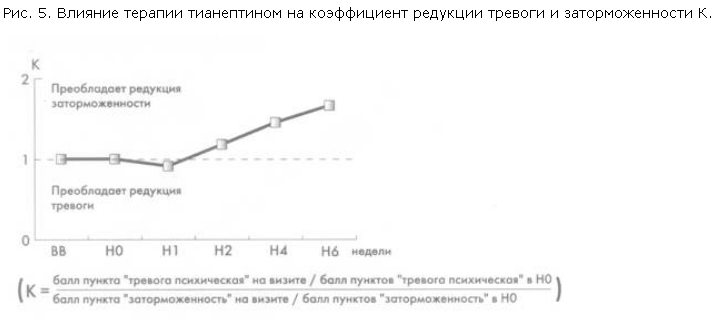
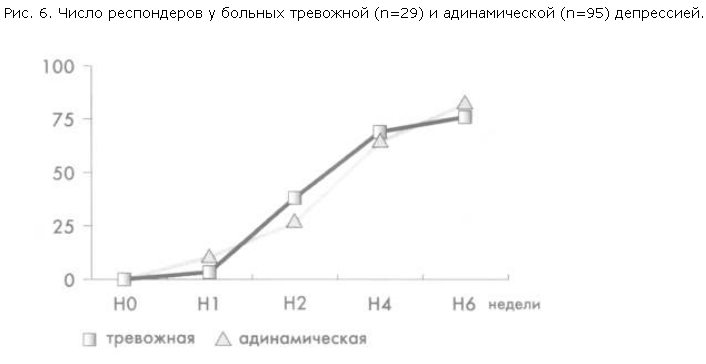
Сбалансированный характер тимоаналептического действия тианептина подтверждается также анализом эффективности терапии в подгруппах больных с адинамической и с тревожной депрессией. Как видно из рис. 6, статистически достоверных различий в числе респондеров между этими подгруппами на всем протяжении терапии не зафиксировано.
Анализ результатов исследования показывает, что тианептин достаточно эффективно устраняет расстройства сна, связанные с депрессией.
Антидепрессивное действие исследуемого препарата проявлялось не только анксиолитическим и некоторым активирующим компонентом, но и гармоничной редукцией всего депрессивного синдрома, включая так называемый соматический симптомокомплекс. Уже после 1-й недели терапии уменьшалась выраженность таких показателей шкалы HAM-D, как ранние пробуждения, типичная суточная ритмика, снижение аппетита, масса тела и либидо. Отчетливым было также влияние тианептина на имевшую место в структуре депрессии ипохондрическую, деперсонализационную и обсессивно-компульсивную симптоматику.
С целью выявления прогностических факторов эффективности тианептина был проведен сравнительный анализ клинико-демографических характеристик и различных показателей динамики течения депрессии в группе респондеров и нонреспондеров.
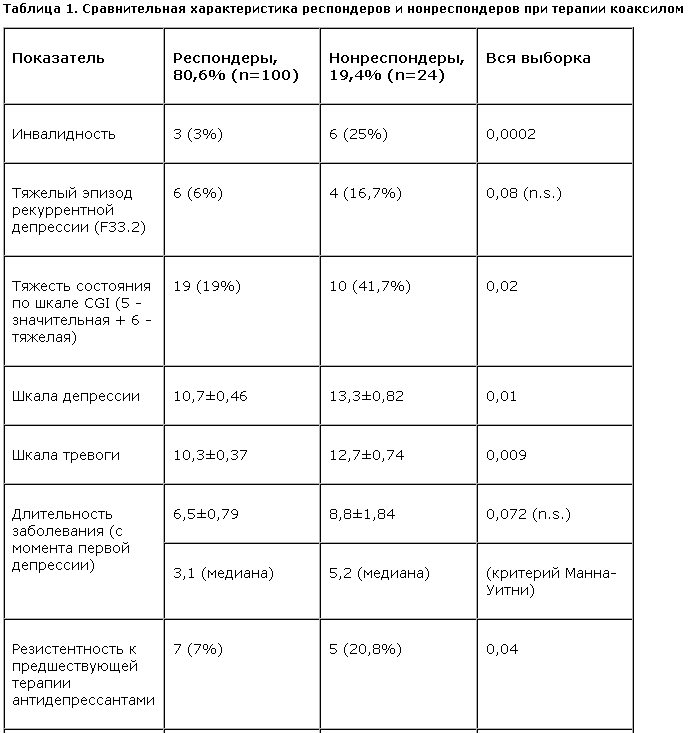
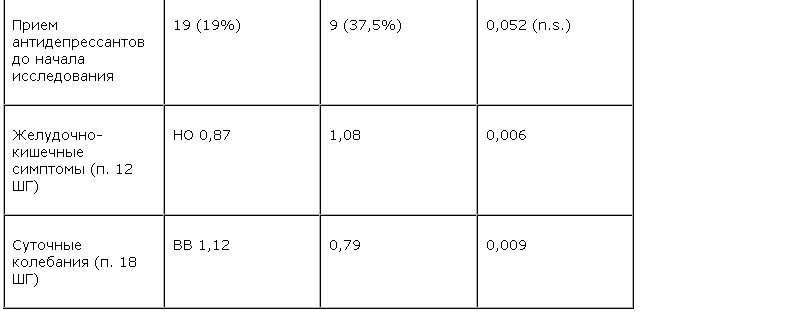
Обращает на себя внимание преобладание (с высокой степенью статистической значимости) в группе нонреспондеров по сравнению с группой респондеров больных с большей тяжестью состояния (по шкале CGI), большей выраженностью симптоматики депрессии и тревоги (по HADS-A и HADS-D), большей тяжестью желудочно-кишечных симптомов (по HAM), резистентностью к предшествующей терапии антидепрессантами, типичной суточной ритмикой и имеющих инвалидность. Прослеживалась также тенденция, не достигавшая статистической значимости, к преобладанию в группе нонреспондеров больных с тяжелым эпизодом рекуррентной депрессии, большими длительностью заболевания и продолжительностью приема антидепрессантов до начала терапии тианептином. Уже из различий основных клинико-демографических характеристик (табл. 1) очевидно, что группа нонреспондеров по сравнению с группой респондеров в значительно большей степени тяготела к полюсу тяжелой меланхолической (соматической) депрессии.
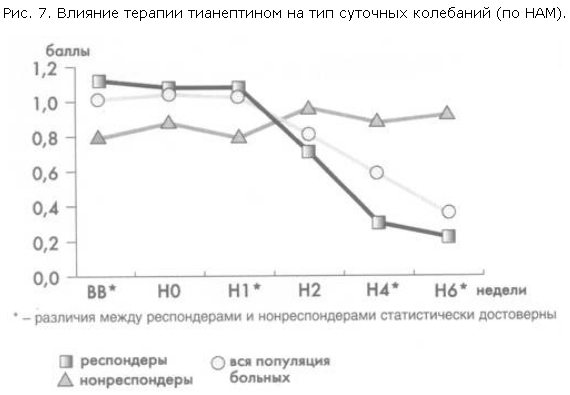
Имевшая место у респондеров критическая редукция выраженности суточных колебаний уже в 1-ю неделю лечения также более характерна для астенических или реактивных состояний, нежели для тяжелой эндогенной депрессии (рис. 7). У нонреспондеров тип суточной ритмики и ее выраженность если и подвергались динамике в процессе терапии, то в весьма незначительной степени.
Интересно, что в 1-ю неделю терапии и у респондеров, и у нонреспондеров наблюдалась отчетливая положительная динамика таких ключевых симптомов депрессии, как депрессивное настроение и суицидальные тенденции. В дальнейшем, начиная со 2-й недели и до конца исследования, показатели оценки этих симптомов различались у респондеров и нонреспондеров статистически достоверно.
Аналогичная динамика отмечалась и в отношении других симптомов депрессии, таких как работоспособность и активность, ранняя и средняя бессонница, заторможенность, ипохондрические расстройства. Если в группе респондеров наблюдалась поступательная редукция симптоматики, то у нонреспондеров происходили утрата первоначального положительного эффекта и усиление выраженности перечисленных симптомов. Такая динамика в группе нонреспондеров, вероятно, объясняется плацебо-эффектом в 1-ю неделю терапии и его утратой в последующем.
Переносимость. Исследование подтвердило хорошую переносимость тианептина. Препарат не влиял на такие соматические характеристики, как масса тела, артериальное давление, частота сердечных сокращений, и только в одном случае было обнаружено повышение уровня печеночных трансаминаз.
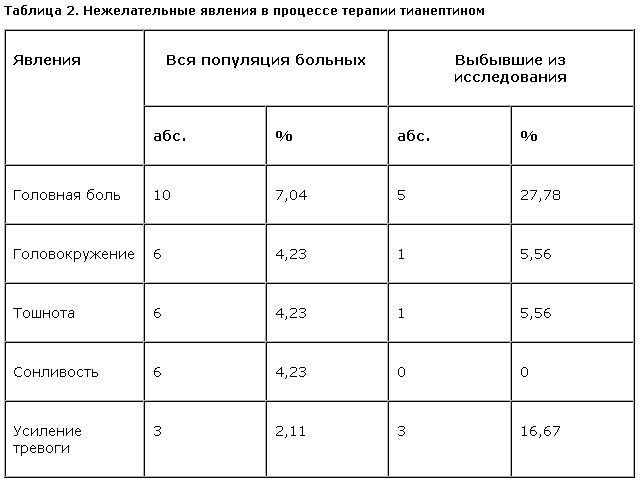
В целом в процессе терапии тианептином у 40 (28,16%) из 142 больных было зарегистрировано 72 нежелательных явления, из них у 40 пациентов зарегистрировано одно, у 17 (11,97%) – не менее двух, у 8 (5,63%) – не менее трех, а у 3 (2,11%) больных – четыре различных расстройства. Наиболее частым (у 7,04% больных) была головная боль, реже (4,23% случаев) отмечались головокружение, тошнота и сонливость. У 3 (2,11%) больных имело место усиление тревоги, однако связь этого явления с приемом тианептина маловероятна (табл. 2).
Анализ исходов нежелательных явления показал, что в подавляющем большинстве случаев они были преходящими. Как правило, они развивались в 1-ю неделю терапии при применении дозы 37,5 мг/сут и в дальнейшем при продолжении терапии редуцировались. Подавляющее большинство пациентов оценивали переносимость тианептина как “хорошую” или “отличную”, и у 72% больных побочных явлений не было.
В процессе терапии тианептином существенно улучшалось качество жизни пациентов. Через 6 нед лечения 67% больных оценили качество жизни как “хорошее” и “отличное”, еще 25% пациентов отметили его “умеренное улучшение”.
Заключение
Монотерапия тианептином больных с выраженной депрессией показала, что этот препарат вызывает отчетливый тимоаналептический, анксиолитический и активизирующий эффект, т.е. является антидепрессантом сбалансированного действия. В целом его эффективность через 6 нед терапии составляла 70,4%, при этом у 58% больных удалось добиться ремиссии. Эти данные соответствуют результатам предшествующих зарубежных двойных слепых плацебо-контролируемых исследований. Более низкая эффективность терапии тяжелых и резистентных депрессий в сравнении с относительно легкими – закономерность для любых антидепрессантов, и в данном случае тианептин не является исключением. Вопрос уточнения его эффективности у этого контингента больных является сложной методической задачей и требует проведения рандомизированных сравнительных исследований.
Особенно важным результатом настоящего исследования представляется возможность эффективного применения тианептина при лечении различных синдромальных форм депрессии умеренной тяжести. Хорошая переносимость препарата, преходящий характер нежелательных явлений, их незначительная выраженность являются важными преимуществами при лечении широкого контингента больных депрессиями.
Список исп. литературыСкрыть список1. Андрусенко М.П., Шешенин В.С., Яковлева О.Б. Использование тианептина (коаксила) при лечении поздних депрессий. Журн. неврол. и психиатр. 1999; 6: 25–30.
2. Бобров А.С. Эндогенная депрессия. Иркутск, 2001; 336–48.
3. Вейн А.М., Воробьева О.В. Неврологические маски депрессии (эффективность тианептина). Журн. неврол. и психиатр. 2000; 100: 21–4.
4. Гурович И.Я., Шмуклер А.Б. Амбулаторное лечение коаксилом. Социал. и клин. психиатр. 1996; 6 (3): 89–96.
5. Дробижев М.Ю., Лебедева О.И., Добровольский А.В. Опыт применения тианептина при лечении тревожных депрессий у больных ишемической болезнью сердца. Тревога и обсессии. М., 1998; 269–78.
6. Иванец Н.Н., Анохина И.П., Чирко В.В. и др. О результатах и перспективах применения коаксила в наркологической практике. Социал. и клин. психиатр. 1998; 8 (1): 68–73.
7. Иванец Н.Н., Тювина Н.А., Балабанова В.В. и др. Эффективнсоть тианептина (коксила) при депрессивных расстройствах невротического и субпсихотического уровня. Психиатр. и психофармакотер. 2001; 5: 166–8.
8. Иванов С.В. Результаты применения коаксила при терапии 414 пациентов с депрессивным эпизодом в условиях клинической практики. Психиатр. и психофармакотер. 2001; 1.
9. Мосолов С.Н., Костюкова Е.Г., Аведисова А.С. и др. Некоторые методологические проблемы клинического изучения антидепрессантов (на примере российского мультицентрового двойного слепого плацебо-контролируемого исследования ребоксина). В кн.: Новые достижения в терапии психических заболеваний. Под ред. С.Н.Мосолова. М., 2002; 245–66.
10. Нуллер Ю.Л., Жарницакая Д.З., Ишукова Л.В. Лечение коаксилом депресси у больных пожилого возраста. Психиатр. и психофармакотер. 2001; 6: 216–8.
11. Смулевич А.Б., Раппопорт С.М., Иванов С.В. и др. Тианептин (коаксил) в гастроэнтерологии (синдром раздраженной кишки). Международная специализированная выставка “Аптека 99”, 6-я. Тезисы докладов. М., 1999; 47.
12. Смулевич А.Б. Депрессии в общесоматической практике. М., 2000; 108–10.
13. Alby JM, Ferreri M, Cabanne J et al. Efficacy of tiantptine for the treatment of major depression and disthymia with somatic complaints, comparative study versus fluoxetine. Ann Psychiat 1993; 8 (2): 136–44.
14. Brown WA. Predictors of placebo-response in depression. Psychopharmacol Bull 1988; 24: 14–7.
15. Cassano GB, Heinze G, Loo H et al. A double-blind comparison of tianeptine, imipramine and placebo in the treatment of major depressive episodes. Eur Psychiat 1996; 1 (5): 254–9.
16. Chapuy P, Grinsztein A, Weitzman JJ et al. Depression in the elderly: 1 – year open study of tianeptine in 140 elderly patients with depression. Press Med 1991; 37: 1844 52.
17. Costa e Silva JA, Raschel SI, Caetanno D et al. Placebo-controlled study of tianeptine in major depressive episodes. Meuropsychobiology 1997; 35: 24–9.
18. Dalery J, Dagens-Lafont V, De Bodinat C. Efficacy of tianeptine versus placebo in the long-term treatment (16,5) of unipolar major recurrent
depression. Encephalon 1997; 23: 56–64.
19. Dinan TO, Thakore J, Lavelle E, Scott L. Hypotalamic-pituitary adrenal axis dysregulation in depression: neurotransmitter induced? CINP Glasgo 1998.
20. Greenbert RP, Fisher S. Examining antidepressant effectiveness: findings, ambiguities, and some vexing puzzles. The limits of biological treatments for psychological distress: comparisons with psychotherapy and placebo. New York 1989; 1–37.
21. Guelfi JD, Pichot P, Dreyfus JF. Efficacy of tianeptine in anxiousdepressed patients: results of controlled multicenter trial versus amitriptyline. Neuropsychobiology 1989; 22: 41–8.
22. Hamilton M. A rating scale for depression. J Neurol Neurosurg Psychiat 1960; 23: 56–62.
23. Invernizzi G, Aguglia E, Berlino A et al. The efficacy and safety of tianeptine in the treatment of depressive disorder: results of a controlled double-blind multicentre study vs. Amitriptyline.
Neuropsychobiology 1984; 30: 85–93.
24. Kamoun A, Delalleaeu B, Ozun M. Can a serotonin uptake agonist be an authentic antidepressant? Results of a multicenter therapeutic study. encephalon 1994; 20: 521–5.
25. Rasper S, Olie JP. A meta-analysis of randomized controlled trial of tianeptin versus SSRI in the short trem treatment of depression. Eur psychiat 2002; 17 (Suppl. 3): 293–340.
26. Lepine JP, Altramura C, Ansseau M et al. Tianeptine and paroxetine in major depressive disorder, with a special focus on the anxious component on depressive disorder, with a special focus on the anxious component on depression: an international, 6-week double-blind study. Hum Psychopharmacol 1001; 16: 219–27.
27. Loo H. Malka R, Defrance R et al. Tianeptine and amitriptyline: controlled double-blind trial in depressed alcoholic patients. Neuropsychobiology 1988; 19: 79–85.
28. Loo H, Saiz-Ruiz J, Coata e Silva JA et al. Doubleblind study comparing tianeptine and fluoxetine in patient with depressive disorders (ICD-10) with or without somatic syndrome. J Affect Disord 1999; 56: 109–18.
29. Nemeroff CB, Owens MJ, Heim C et al. Early life stress and vulnerability to depression: Preclinical and clinical studies. CINP Glasgow 1998.
30. Paes de Sousa M, Figueria L, Ferreira L et al. Efficacy of tianeptine in the ling-term treatment major depressionl. Double-blind trial: tianeptine vs clomipramine. Servier Especialidades Farmaceiutices. 2000.
31. Szadoczky E, Furedio J. Efficacy and acceptability of tianeptine and sertraline in acute treatment phase of depression. Neuropsychopharmacologia Hungrica 2000; 11 (4): 171–7.
32. Waintraub L, Septien L, Azoulay P. Efficacy and safety of tiuantptine in major depression: evidens from a 3-month clinical trial versus paroxetine. Etu Neuropsychopharmacol 2000; 10 (Suppl. 2): 51.
33. Zigmond AS, Snaith RP. The Hospital Anxiety and depression scale. Acta Psychiat Scand 1983; 67: 361–70.


