Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№05 2004
Селективные ингибиторы обратного захвата серотонина и норадреналина: возможно ли сочетание эффективности и безопасности? №05 2004
Принято считать, что психотропная активность у большинства антидепрессантов независимо от их механизма действия и химической структуры связана с их способностью ликвидировать лежащий в основе патогенеза депрессивных состояний “дефицит” норадреналина и/или серотонина в некоторых (стволовых, лимбических) структурах головного мозга. При этом все антидепрессанты могут быть дифференцированы по их влиянию на обмен моноаминов. Так, выделяют преимущественно “серотонинергические” и “норадренергические” антидепрессанты, а также тимолептики “двойного действия”, способные восполнять “дефицит” как серотонина, так и норадреналина. К последним антидепрессантам относятся все ИМАО, которые блокируют ферменты, участвующие в метаболизме обоих указанных моноаминов.
Принято считать, что психотропная активность у большинства антидепрессантов независимо от их механизма действия и химической структуры (см. таблицу) связана с их способностью ликвидировать лежащий в основе патогенеза депрессивных состояний “дефицит” норадреналина и/или серотонина в некоторых (стволовых, лимбических) структурах головного мозга.
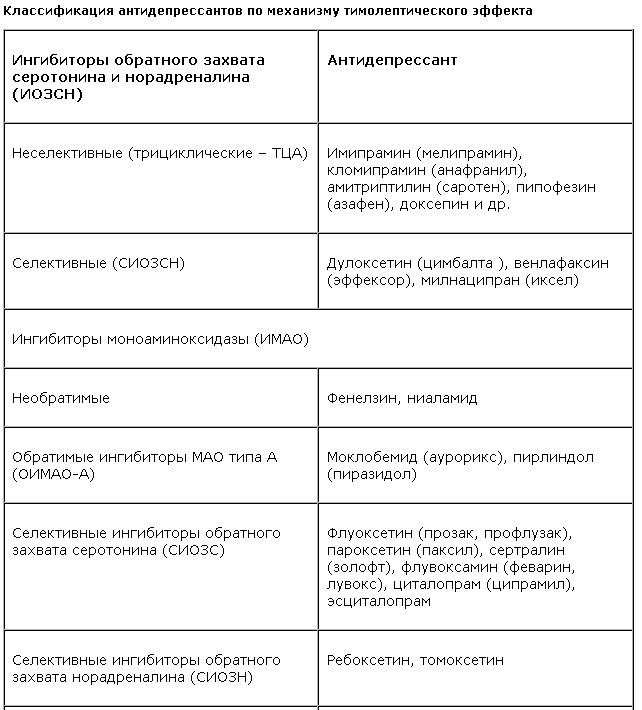
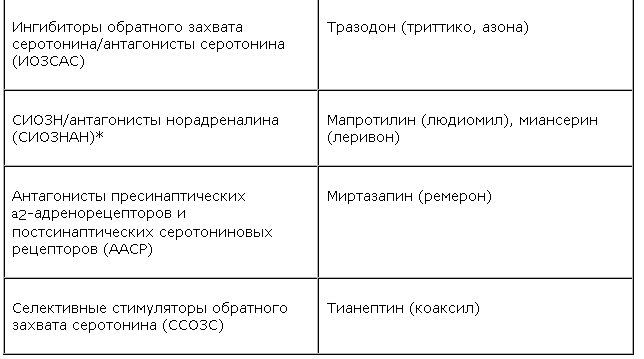
При этом все антидепрессанты могут быть дифференцированы по их влиянию на обмен моноаминов. Так, выделяют преимущественно “серотонинергические” и “норадренергические” антидепрессанты, а также тимолептики “двойного действия”, способные восполнять “дефицит” как серотонина, так и норадреналина. К последним антидепрессантам относятся все ИМАО, которые блокируют ферменты, участвующие в метаболизме обоих указанных моноаминов. “Двойным действием” обладает миртазапин – антагонист пресинаптических a2-адренорецепторов и постсинаптических серотониновых рецепторов (АПАПСР) [1]. Роль этих рецепторов связана с механизмом обратной связи, позволяющим прекратить избыточное выделение моноаминов. При этом блокада a2-ауто- и гетерорецепторов приводит к тому, что высвобождение норадреналина и серотонина ускоряется.
– ТЦА [1], а также такие новые и в значительной мере более селективные (в плане воздействия на различные рецепторы) препараты, как дулоксетин (цимбалта), венлафаксин (эффексор), милнаципран (иксел).
Некоторые тимолептики способны воздействовать прежде всего на обмен норадреналина. Так, антагонисты пресинаптических a2-адренорецепторов (АПАР) мапротилин, миансерин, как и миртазапин, блокируют a2- ауто- и гетерорецепторы, что потенциально может приводить к высвобождению норадреналина и серотонина. Вместе с тем в отличие от миртазапина блокируют еще и a1-адренорецепторы. Последние играют важную роль в передаче возбуждения с норадренергического на серотониновый нейрон. Соответственно, тимолептики рассматриваемой группы АПАР реализуют влияние преимущественно на обмен норадреналина [1].
Другая группа “норадренергических” антидепрессантов – СИОЗН – ребоксетин и томоксетин, терапевтический эффект которых связан с затруднением возврата норадреналина из межсинаптической щели в пресинаптический нейрон.
Наконец, существует несколько групп антидепрессантов, обладающих избирательным воздействием на обмен серотонина. К одной их таких групп относится ИОЗСАС – тразодон [2, 3]. Этот антидепрессант действует как на пресинаптическом, так и постсинаптическом уровне. Препарат обладает умеренно выраженным (в сравнении с СИОЗС) свойством ингибировать обратный захват серотонина (пресинаптический нейрон) и достаточно выраженной способностью блокировать серотониновые 2А-рецепторы (постсинаптический нейрон). Роль последних сводится, по всей видимости, к тому, что при их активации снижается эффективность другого типа постсинаптических серотониновых рецепторов – 1А, играющих важную роль при проведении возбуждения. Соответственно, блокада серотониновых рецепторов типа 2А и небольшое угнетение обратного захвата серотонина приводят не только к росту концентрации рассматриваемого нейротрансмиттера в межсинаптической щели, но и к повышению эффективности работы синаптической передачи.
Другой группой серотонинергических антидепрессантов являются СИОЗС. В настоящее время считается, что фармакологическая активность СИОЗС может быть дифференцирована на три последовательных этапа [1]. На первом из них происходит ингибирование обратного захвата серотонина как в ЦНС, так и в периферической нервной системе. При этом возможна манифестация побочных эффектов СИОЗС. На втором этапе нарушается блокирующая функция серотониновых 1А-рецепторов, расположенных в соматодендритной части нейронов области шва среднего мозга. При этом отмечаются первые признаки терапевтического действия СИОЗС. Наконец, на третьем этапе серотониновые нейроны растормаживаются (дезингибируются) и серотонин начинает быстро высвобождаться из аксонов, ведущих к разным структурам головного мозга.
В отличие от всех перечисленных выше серотонинергических антидепрессантов ССОЗС не блокируют, а напротив, стимулируют обратный захват серотонина. Как свидетельствуют данные экспериментальных исследований, ССОЗС (тианептин) в значительной степени увеличивает амплитуду синаптической пластичности, приводит к нормализации мозгового обмена. Длительное введение тианептина активирует нейрональную жизнеспособность (так называемый нейропластический эффект) [4–6].
Существующее на сегодняшний день большое число групп антидепрессантов не должно вводить в заблуждение. Только две из них – традиционные ТЦА и СИОЗС – в настоящее время определяют психофармакотерапию депрессий См. также предшествующий обзор, посвященный фармакоэпидемиологии. Так, в многочисленных исследованиях указывается, что ТЦА и
СИОЗС являются чаще всего использующимися антидепрессантами в большинстве стран мира [7, 8]. Не является исключением и Россия. В Перечень жизненно необходимых и важнейших лекарственных средств, утвержденный распоряжением Правительства Российской Федерации от 20 марта 2003 г. (№357-р), включены 4 из 5 использующихся на сегодняшний день СИОЗС (циталопрам, пароксетин, сертралин, флуоксетин) и 3 ТЦА (амитриптилин, имипрамин, кломипрамин). Все остальные антидепрессанты представлены единичными медикаментозными средствами.
Второй подход, при котором на первый план выдвигается безопасность, получает свое воплощение при использовании СИОЗС. Последние в отличие от ТЦА не обладают выраженными поведенческой токсичностью [10, 11], антихолинергическими побочными эффектами [12], неблагоприятными гепато- и кардиотропным действием и, по всей видимости, тератогенностью (особенно при их применении лишь во II и III триместрах беременности). Соответственно, возникает возможность широко использовать СИОЗС не только в стационаре, но и в амбулаторной практике как для лечения депрессий, так и для проведения длительной поддерживающей терапии у широкого круга больных, включая пациентов, страдающих соматическими заболеваниями. В результате во многих странах мира СИОЗС даже опережают ТЦА по частоте использования. Так, в Италии за период с 1997 по 2003 г. доля СИОЗС среди всех используемых антидепрессантов возросла с 30 до 36% [13, 14], при этом ТЦА назначают в 1,5 раза реже (21%).
По всей видимости, особенно велика популярность СИОЗС в США. Так, по данным некоторых фармакоэпидемиологических исследований, доля больных, получающих СИОЗС, от всех пациентов этой страны, принимающих антидепрессанты, составляет 47% [15]. В то же время аналогичный показатель для ТЦА достигает лишь 19%. По данным другого фармакоэпидемиологического исследования, соотношение долей больных, получающих СИОЗС и ТЦА, при лечении некоторых депрессивных состояний (первый эпизод депрессии) составляет 82 к 18% [16].
Вместе c тем СИОЗС, обладая значительными преимуществами перед ТЦА в плане безопасности и переносимости, могут уступать им в эффективности. Так, в недавнем исследовании G. Parker [17] сообщается, что эффективность СИОЗС ниже, чем у ТЦА, при лечении меланхолических депрессий. Сходные данные представлены и отечественными авторами. Так, в фундаментальной монографии, посвященной депрессиям при соматических и психических заболеваниях [9], сообщается об опыте, накопленном в клинике по изучению пограничных состояний и психосоматических расстройств НЦПЗ РАМН. Этот опыт однозначно свидетельствует о том, что купирование остро возникших депрессивных эпизодов (подавленность с чувством безнадежности и суицидальными мыслями или тенденциями), сопровождающихся тревогой, достигающей степени ажитации, либо двигательным торможением с явлениями депрессивного ступора предпочтительно проводить не с помощью СИОЗС, а такими препаратами, как имипрамин, кломипрамин, амитриптилин, при необходимости вводимых парентерально.
Представленные данные позволяют предположить, что как в психиатрии, так и в общемедицинской сети значительным преимуществом будет пользоваться антидепрессант, сопоставимый с ТЦА по эффективности, а с СИОЗС по безопасности и переносимости. И действительно, в настоящее время активно ведется поиск тимолептиков, удовлетворяющих указанным требованиям. При этом предлагается несколько вариантов стратегии такого поиска. Первая из них связана с разработкой СИОЗС второго поколения. При этом одним из наиболее перспективных направлений исследований является повышение фармакологической активности препарата за счет изменения молекулярной геометрии антидепрессанта, так чтобы он как можно точнее “укладывался” в рецептор – был ему комплементарен [18]. Так, при сравнении S- и R-энантиомеров оказалось, что эсциталопрам (S-энантиомеру активного вещества) является в 30 раз более сильным ингибитором обратного захвата серотонина, чем его оптический антипод [19]. Вместе с тем из-за различий в распределении изомеров в организме реальная доля эсциталопрама, получаемая пациентом из циталопрама (смеси S- и R-энантиомеров), составляет всего лишь 35% [20]. Соответственно, при переходе от циталопрама к эсциталопраму возникает возможность повысить эффективность СИОЗС. Следует, однако, отметить, что по своему характеру два из пяти препаратов этой группы (пароксетин и сертралин) уже содержат один энантиомер и, соответственно, могут рассматриваться как СИОЗС второго поколения [21]. И хотя оба указанных препарата находятся среди самых востребованных антидепрессантов из группы СИОЗС, это не привело к существенному изменению ситуации, связанной с клиническим использованием тимолептиков.
Вторая стратегия поиска связана с попытками одновременного использования серотонинергических и норадренергических препаратов – СИОЗС и СИОЗН, воспроизводя, таким образом, механизм действия ТЦА. Соответственно этому предпринимаются попытки оценить эффективность комбинированной терапии резистентных депрессий флуоксетином и ребоксетином [22, 23]. Аналогичным образом изучается возможность применения ципрамила и ребоксетина у пациентов, страдающих депрессией с коморбидным паническим расстройством [24]. Следует, однако, отметить, что реализация этой стратегии существенно затруднена в связи с необходимостью назначать два препарата вместе одного, что ведет не только к усложнению терапии, но и в значительной степени к снижению фармакоэкономических показателей.
Наконец, последняя стратегия основана на использовании современных антидепрессантов двойного действия –
СИОЗСН, которые, обладая сопоставимым с ТЦА механизмом действия, в отличие от последних не воздействуют на холинергические, адренергические и гистаминовые рецепторы.
Накопленный в мире опыт использования СИОЗСН позволяет предполагать, что по своей эффективности эти антидепрессанты сопоставимы с ТЦА, но превосходят традиционные СИОЗС [25]. В частности, показано, что венлафаксин по тимолептическому эффекту может быть соотнесен с амитриптилином [26] или нортриптилином [27]. Сообщается о результатах сравнительных плацебо-контролированных работ, сравнивающих дулоксетин с флуоксетином у больных с тревожными депрессиями [28]. Данные этих работ свидетельствуют, что эффективность СИОЗСН превосходит тимолептическую активность СИОЗС. Так, редукция психопатологических расстройств на фоне приема первого из этих препаратов наблюдается в 65% случаях, когда как такой показатель для второго не достигает и 50%. Кроме того, в ряде работ было показано, что использование СИОЗСН значимо чаще приводит к устойчивой ремиссии, чем при приеме некоторых СИОЗС. Так, стойкая ремиссия регистрировалась при терапии дулоксетином в 56% наблюдений. Тот же показатель для флуоксетина достигает лишь 30% [29]. В аспекте рассматриваемой проблемы важно, что эффективность СИОЗСН (дулоксетин) показана и при терапии депрессий, резистентных к СИОЗС [30].
Что же касается переносимости и безопасности, то данные ряда исследований свидетельствуют о том, что СИОЗСН по этим показателям превосходят ТЦА и вполне сопоставимы с СИОЗС. Так, в исследовании французских авторов, опросивших более 200 психиатров, показано, что венлафаксин относится (наряду с циталопрамом и пароксетином) к наиболее переносимым антидепрессантам [31, 32].
Завершая характеристику рассматриваемой стратегии поиска новых антидепрессантов, необходимо указать, что представленные клинические преимущества СИОЗСН проявляются и при фармакоэкономическом анализе. Так, в недавно проведенном во Франции исследовании [33] показано, что в силу сочетания высокой эффективности с переносимостью и безопасностью лечение одним из препаратов группы СИОЗСН – милнаципраном – более выгодно с экономических позиций, чем терапия ТЦА или СИОЗС.
Подводя итог данным по трем основным стратегиям поиска, следует указать, что представленные в настоящем обзоре сведения носят предварительный характер, безусловно нуждаются в уточнении и могут приобрести реальный смысл в аспекте эффективной помощи больным только после проведения широких клинических, фармакоэпидемиологических и фармакоэкономических исследований. Тем не менее уже сейчас можно констатировать, что на современном этапе развития психофармакологии наметился пересмотр стратегии широкого использования селективных антидепрессантов в пользу тимолептиков, обладающих более широким спектром механизмов действия.


При этом все антидепрессанты могут быть дифференцированы по их влиянию на обмен моноаминов. Так, выделяют преимущественно “серотонинергические” и “норадренергические” антидепрессанты, а также тимолептики “двойного действия”, способные восполнять “дефицит” как серотонина, так и норадреналина. К последним антидепрессантам относятся все ИМАО, которые блокируют ферменты, участвующие в метаболизме обоих указанных моноаминов. “Двойным действием” обладает миртазапин – антагонист пресинаптических a2-адренорецепторов и постсинаптических серотониновых рецепторов (АПАПСР) [1]. Роль этих рецепторов связана с механизмом обратной связи, позволяющим прекратить избыточное выделение моноаминов. При этом блокада a2-ауто- и гетерорецепторов приводит к тому, что высвобождение норадреналина и серотонина ускоряется.
– ТЦА [1], а также такие новые и в значительной мере более селективные (в плане воздействия на различные рецепторы) препараты, как дулоксетин (цимбалта), венлафаксин (эффексор), милнаципран (иксел).
Некоторые тимолептики способны воздействовать прежде всего на обмен норадреналина. Так, антагонисты пресинаптических a2-адренорецепторов (АПАР) мапротилин, миансерин, как и миртазапин, блокируют a2- ауто- и гетерорецепторы, что потенциально может приводить к высвобождению норадреналина и серотонина. Вместе с тем в отличие от миртазапина блокируют еще и a1-адренорецепторы. Последние играют важную роль в передаче возбуждения с норадренергического на серотониновый нейрон. Соответственно, тимолептики рассматриваемой группы АПАР реализуют влияние преимущественно на обмен норадреналина [1].
Другая группа “норадренергических” антидепрессантов – СИОЗН – ребоксетин и томоксетин, терапевтический эффект которых связан с затруднением возврата норадреналина из межсинаптической щели в пресинаптический нейрон.
Наконец, существует несколько групп антидепрессантов, обладающих избирательным воздействием на обмен серотонина. К одной их таких групп относится ИОЗСАС – тразодон [2, 3]. Этот антидепрессант действует как на пресинаптическом, так и постсинаптическом уровне. Препарат обладает умеренно выраженным (в сравнении с СИОЗС) свойством ингибировать обратный захват серотонина (пресинаптический нейрон) и достаточно выраженной способностью блокировать серотониновые 2А-рецепторы (постсинаптический нейрон). Роль последних сводится, по всей видимости, к тому, что при их активации снижается эффективность другого типа постсинаптических серотониновых рецепторов – 1А, играющих важную роль при проведении возбуждения. Соответственно, блокада серотониновых рецепторов типа 2А и небольшое угнетение обратного захвата серотонина приводят не только к росту концентрации рассматриваемого нейротрансмиттера в межсинаптической щели, но и к повышению эффективности работы синаптической передачи.
Другой группой серотонинергических антидепрессантов являются СИОЗС. В настоящее время считается, что фармакологическая активность СИОЗС может быть дифференцирована на три последовательных этапа [1]. На первом из них происходит ингибирование обратного захвата серотонина как в ЦНС, так и в периферической нервной системе. При этом возможна манифестация побочных эффектов СИОЗС. На втором этапе нарушается блокирующая функция серотониновых 1А-рецепторов, расположенных в соматодендритной части нейронов области шва среднего мозга. При этом отмечаются первые признаки терапевтического действия СИОЗС. Наконец, на третьем этапе серотониновые нейроны растормаживаются (дезингибируются) и серотонин начинает быстро высвобождаться из аксонов, ведущих к разным структурам головного мозга.
В отличие от всех перечисленных выше серотонинергических антидепрессантов ССОЗС не блокируют, а напротив, стимулируют обратный захват серотонина. Как свидетельствуют данные экспериментальных исследований, ССОЗС (тианептин) в значительной степени увеличивает амплитуду синаптической пластичности, приводит к нормализации мозгового обмена. Длительное введение тианептина активирует нейрональную жизнеспособность (так называемый нейропластический эффект) [4–6].
Существующее на сегодняшний день большое число групп антидепрессантов не должно вводить в заблуждение. Только две из них – традиционные ТЦА и СИОЗС – в настоящее время определяют психофармакотерапию депрессий См. также предшествующий обзор, посвященный фармакоэпидемиологии. Так, в многочисленных исследованиях указывается, что ТЦА и
СИОЗС являются чаще всего использующимися антидепрессантами в большинстве стран мира [7, 8]. Не является исключением и Россия. В Перечень жизненно необходимых и важнейших лекарственных средств, утвержденный распоряжением Правительства Российской Федерации от 20 марта 2003 г. (№357-р), включены 4 из 5 использующихся на сегодняшний день СИОЗС (циталопрам, пароксетин, сертралин, флуоксетин) и 3 ТЦА (амитриптилин, имипрамин, кломипрамин). Все остальные антидепрессанты представлены единичными медикаментозными средствами.
Второй подход, при котором на первый план выдвигается безопасность, получает свое воплощение при использовании СИОЗС. Последние в отличие от ТЦА не обладают выраженными поведенческой токсичностью [10, 11], антихолинергическими побочными эффектами [12], неблагоприятными гепато- и кардиотропным действием и, по всей видимости, тератогенностью (особенно при их применении лишь во II и III триместрах беременности). Соответственно, возникает возможность широко использовать СИОЗС не только в стационаре, но и в амбулаторной практике как для лечения депрессий, так и для проведения длительной поддерживающей терапии у широкого круга больных, включая пациентов, страдающих соматическими заболеваниями. В результате во многих странах мира СИОЗС даже опережают ТЦА по частоте использования. Так, в Италии за период с 1997 по 2003 г. доля СИОЗС среди всех используемых антидепрессантов возросла с 30 до 36% [13, 14], при этом ТЦА назначают в 1,5 раза реже (21%).
По всей видимости, особенно велика популярность СИОЗС в США. Так, по данным некоторых фармакоэпидемиологических исследований, доля больных, получающих СИОЗС, от всех пациентов этой страны, принимающих антидепрессанты, составляет 47% [15]. В то же время аналогичный показатель для ТЦА достигает лишь 19%. По данным другого фармакоэпидемиологического исследования, соотношение долей больных, получающих СИОЗС и ТЦА, при лечении некоторых депрессивных состояний (первый эпизод депрессии) составляет 82 к 18% [16].
Вместе c тем СИОЗС, обладая значительными преимуществами перед ТЦА в плане безопасности и переносимости, могут уступать им в эффективности. Так, в недавнем исследовании G. Parker [17] сообщается, что эффективность СИОЗС ниже, чем у ТЦА, при лечении меланхолических депрессий. Сходные данные представлены и отечественными авторами. Так, в фундаментальной монографии, посвященной депрессиям при соматических и психических заболеваниях [9], сообщается об опыте, накопленном в клинике по изучению пограничных состояний и психосоматических расстройств НЦПЗ РАМН. Этот опыт однозначно свидетельствует о том, что купирование остро возникших депрессивных эпизодов (подавленность с чувством безнадежности и суицидальными мыслями или тенденциями), сопровождающихся тревогой, достигающей степени ажитации, либо двигательным торможением с явлениями депрессивного ступора предпочтительно проводить не с помощью СИОЗС, а такими препаратами, как имипрамин, кломипрамин, амитриптилин, при необходимости вводимых парентерально.
Представленные данные позволяют предположить, что как в психиатрии, так и в общемедицинской сети значительным преимуществом будет пользоваться антидепрессант, сопоставимый с ТЦА по эффективности, а с СИОЗС по безопасности и переносимости. И действительно, в настоящее время активно ведется поиск тимолептиков, удовлетворяющих указанным требованиям. При этом предлагается несколько вариантов стратегии такого поиска. Первая из них связана с разработкой СИОЗС второго поколения. При этом одним из наиболее перспективных направлений исследований является повышение фармакологической активности препарата за счет изменения молекулярной геометрии антидепрессанта, так чтобы он как можно точнее “укладывался” в рецептор – был ему комплементарен [18]. Так, при сравнении S- и R-энантиомеров оказалось, что эсциталопрам (S-энантиомеру активного вещества) является в 30 раз более сильным ингибитором обратного захвата серотонина, чем его оптический антипод [19]. Вместе с тем из-за различий в распределении изомеров в организме реальная доля эсциталопрама, получаемая пациентом из циталопрама (смеси S- и R-энантиомеров), составляет всего лишь 35% [20]. Соответственно, при переходе от циталопрама к эсциталопраму возникает возможность повысить эффективность СИОЗС. Следует, однако, отметить, что по своему характеру два из пяти препаратов этой группы (пароксетин и сертралин) уже содержат один энантиомер и, соответственно, могут рассматриваться как СИОЗС второго поколения [21]. И хотя оба указанных препарата находятся среди самых востребованных антидепрессантов из группы СИОЗС, это не привело к существенному изменению ситуации, связанной с клиническим использованием тимолептиков.
Вторая стратегия поиска связана с попытками одновременного использования серотонинергических и норадренергических препаратов – СИОЗС и СИОЗН, воспроизводя, таким образом, механизм действия ТЦА. Соответственно этому предпринимаются попытки оценить эффективность комбинированной терапии резистентных депрессий флуоксетином и ребоксетином [22, 23]. Аналогичным образом изучается возможность применения ципрамила и ребоксетина у пациентов, страдающих депрессией с коморбидным паническим расстройством [24]. Следует, однако, отметить, что реализация этой стратегии существенно затруднена в связи с необходимостью назначать два препарата вместе одного, что ведет не только к усложнению терапии, но и в значительной степени к снижению фармакоэкономических показателей.
Наконец, последняя стратегия основана на использовании современных антидепрессантов двойного действия –
СИОЗСН, которые, обладая сопоставимым с ТЦА механизмом действия, в отличие от последних не воздействуют на холинергические, адренергические и гистаминовые рецепторы.
Накопленный в мире опыт использования СИОЗСН позволяет предполагать, что по своей эффективности эти антидепрессанты сопоставимы с ТЦА, но превосходят традиционные СИОЗС [25]. В частности, показано, что венлафаксин по тимолептическому эффекту может быть соотнесен с амитриптилином [26] или нортриптилином [27]. Сообщается о результатах сравнительных плацебо-контролированных работ, сравнивающих дулоксетин с флуоксетином у больных с тревожными депрессиями [28]. Данные этих работ свидетельствуют, что эффективность СИОЗСН превосходит тимолептическую активность СИОЗС. Так, редукция психопатологических расстройств на фоне приема первого из этих препаратов наблюдается в 65% случаях, когда как такой показатель для второго не достигает и 50%. Кроме того, в ряде работ было показано, что использование СИОЗСН значимо чаще приводит к устойчивой ремиссии, чем при приеме некоторых СИОЗС. Так, стойкая ремиссия регистрировалась при терапии дулоксетином в 56% наблюдений. Тот же показатель для флуоксетина достигает лишь 30% [29]. В аспекте рассматриваемой проблемы важно, что эффективность СИОЗСН (дулоксетин) показана и при терапии депрессий, резистентных к СИОЗС [30].
Что же касается переносимости и безопасности, то данные ряда исследований свидетельствуют о том, что СИОЗСН по этим показателям превосходят ТЦА и вполне сопоставимы с СИОЗС. Так, в исследовании французских авторов, опросивших более 200 психиатров, показано, что венлафаксин относится (наряду с циталопрамом и пароксетином) к наиболее переносимым антидепрессантам [31, 32].
Завершая характеристику рассматриваемой стратегии поиска новых антидепрессантов, необходимо указать, что представленные клинические преимущества СИОЗСН проявляются и при фармакоэкономическом анализе. Так, в недавно проведенном во Франции исследовании [33] показано, что в силу сочетания высокой эффективности с переносимостью и безопасностью лечение одним из препаратов группы СИОЗСН – милнаципраном – более выгодно с экономических позиций, чем терапия ТЦА или СИОЗС.
Подводя итог данным по трем основным стратегиям поиска, следует указать, что представленные в настоящем обзоре сведения носят предварительный характер, безусловно нуждаются в уточнении и могут приобрести реальный смысл в аспекте эффективной помощи больным только после проведения широких клинических, фармакоэпидемиологических и фармакоэкономических исследований. Тем не менее уже сейчас можно констатировать, что на современном этапе развития психофармакологии наметился пересмотр стратегии широкого использования селективных антидепрессантов в пользу тимолептиков, обладающих более широким спектром механизмов действия.
Список исп. литературыСкрыть список1. Stahl SM. Essential psychopharmacology of depression and bipolar disorder. Cambridge, Cambridge university press, 2000, 175P.
2. Kasper S. Biological consequences and clinical relevancies of serotonin antagonism and reuptake inhibition. Int J Neuropsychopharmacol 2004; 7 (Suppl. 1): 117.
3. Stahl SM. Serotonin antagonism and reuptake inhibition; pharmacology and physiology of CNS serotonin housekeeping Int J Neuropsychopharmacology. 2004; 7(Suppl.1): 117.
4. Fuchs E, Czeh B, Michaelis T et al. Altreations of neuroplasticity in depression: the hippocampus and beyond. Int J Neuropsychopharmacol 2004; 7 (Suppl.1): 101.
5. McEwen B.C. Molecular mechanism of neuroplasticity and pharmacological implications Int J Neuropsychopharmacol 2004; 7 (Suppl.1): 101.
6. Olie JP, Costa e Silva, Macher JP. Neuroplastisity. A new approach to the pathophysiology of depression. Science Press, London. 2004.
7. Grohmann R, Ruther E, Engel RR, Hippius H. Assessment of adverse drug reactions in psychiatric inpatients with the AMSP drug safety program: methods and first results for tricyclic antidepressants and SSRI. Pharmacopsychiatry. 1999 Jan; 32(1): 21–8.
8. Hida H, Faber M, Alberto-Gondouin MC, Jalaguier E. [Analysis of prescriptions for psychotropic drugs in a psychiatric hospital] Therapie 1997 Nov-Dec; 52(6): 573–8.
9. Смулевич А.Б. Депрессия при соматических и психических заболеваниях. ООО "Медицинское информационное агенство". М., 2003.
10. Van Laar MW, Volkerts ER, Verbaten MN, Trooster S et al. Differential effects of amitriptyline, nefazodone and paroxetine on performance and brain indices of visual selective attention and working memory. Psychopharmacology (Berl) 2002 Aug; 162(4): 351–63.
11. Sattler HD, Richter P, Fritzsche M et al. Neurophysiologic tests during antidepressive treatment – an exploratory study. Pharmacopsychiatry 2000 Nov; 33(6): 229–33.
12. Pezzella G, Moslinger-Gehmayr R, Contu A. Treatment of depression in patients with breast cancer: a comparison between paroxetine and amitriptyline. Breast Cancer Res Treat 2001 Nov; 70(1): 1–10.
13. Balestrieri M, Carta MG, Leonetti S et al. Recognition of depression and appropriateness of antidepressant treatment in Italian primary care. Soc Psychiatry Psychiatr Epidemiol (2004) 39: 171–6.
14. Barbui C, Campomori A, D'Avanzo B et al. Antidepressant drug use in Italy since the introduction of SSRIs: national trends, regional differences and impact on suicide rates Soc Psychiatry Psychiatr Epidemiol 1999; 34: 152–6.
15. Ackerman DL, Unutzer J, Greenland S, Gitlin M. Inpatient treatment of depression and associated hospital charges. Pharmacoepidemiol Drug Saf 2002 Apr-May; 11(3): 219–27.
16. Sclar DA, Skaer TL, Robison LM, Galin RS Economic appraisal of citalopram in the management of single-episode depression. J Clin Psychopharmacol 1999 Oct;19(5 Suppl 1):47S-54S]
17. Parker G. Differential effectiveness of newer and older antidepressants appears mediated by an age effect on the phenotypic expression of depression. Acta Psychiatr Scand 2002 Sep; 106(3): 168–70.
18. Fabre V, Hamon M. [Mechanisms of action of antidepressants: new data from Escitalopram] Encephale 2003 May-Jun; 29 (3 Pt 1): 259–65.
19. Sanchez C, Bergqvist PB, Brennum LT et al. Escitalopram, the S-(+)-enantiomer of citalopram, is a selective serotonin reuptake inhibitor with potent effects in animal models predictive of antidepressant and anxiolytic activities. Psychopharmacology (Berl) 2003 Jun; 167(4): 353–62.
20. Rochat B, Amey M, Gillet M et al. Identification of three cytochrome P450 isozymes involved in N-demethylation of citalopram enantiomers in human liver microsomes. Pharmacogenetics 1997; 7: 1–10.
21. Owens MJ, Knight DL, Nemeroff CB Second-Generation SSRIs: Human Monoamine Transporter Binding Profile of Escitalopram and R-Fluoxetine. Biol Psychiatry 2001; 50: 345–50.
22. Fava M, McGrath PJ, Sheu WP. Switching to reboxetine: an efficacy and safety study in patients with major depressive disorder unresponsive to fluoxetine.J Clin Psychopharmacol 2003 Aug; 23(4): 365–9.
23. Rubio G, San L, Lopez-Munoz F et al. Combination therapy with reboxetine for major depression patients who are partial or nonresponders to serotonin selective reuptake inhibitors Actas Esp Psiquiatr. 2003 Nov-Dec; 31(6): 315–24.
24. Seedat S, van Rheede van Oudtshoorn E, Muller JE et al. Reboxetine and citalopram in panic disorder: a single-blind, cross-over, flexible-dose pilot study. Int Clin Psychopharmacol 2003 Sep; 18(5): 279–84.
25. Smith D, Dempster C, Glanville J et al. Efficacy and tolerability of venlafaxine compared with selective serotonin reuptake inhibitors and other antidepressants: a meta-analysis. ACP J Club 2002 Nov–Dec; 137(3): 101.
26. Sauer H, Huppertz-Helmhold S, Dierkes W. Efficacy and safety of venlafaxine ER vs. amitriptyline ER in patients with major depression of moderate severity. Pharmacopsychiatry 2003 Sep; 36(5): 169–75.
27. Gasto C, Navarro V, Marcos T, et al. Single-blind comparison of venlafaxine and nortriptyline in elderly major depression. J Clin Psychopharmacol 2003 Feb; 23 (1): 21–6.
28. Dunner DL, Goldstein DJ, Mallinckrodt C, et al. Duloxetine in treatment of anxiety symptoms associated with depression. Depress Anxiety 2003; 18(2): 53–61.
29. Bymaster FP, Dreshfield Ahmed LJ, Threlkeld PG et al. Comparative affinity of duloxetine and venlafaxine for serotonin and norepinephrine transporters in vitro and in vivo, hyman serotonin receptor subtypes, and other neuronal receptors. Neuropsychopharmacology 2001; 25: 871–80.
30. Saiz-Ruiz J, Ibanez A, Diaz-Marsa M et al. Efficacy of venlafaxine in major depression resistant to selective serotonin reuptake inhibitors. Prog Neuropsychopharmacol Biol Psychiatry 2002, Oct; 26(6): 1129–34.
31. Depont F., Rambelomanana S., Puil S. et al. Antidepressants: psychiatrists’ opinions and clinical practice. Acta Psychiatr Scand 2003: 108: 24–31.
32. Vieta E, Martinez-Aran A, Goikolea JM et al. A randomized trial comparing paroxetine and venlafaxine in the treatment of bipolar depressed patients taking mood stabilizers. J Clin Psychiatry 2002 Jun; 63(6): 508–12.
33. Dardennes R, Berdeaux G, Lafuma A, Fagnani F. Comparison of the cost-effectiveness of milnacipran (a SNRI) with TCAs and SSRIs: a modeling approach. Eur Psychiatry 1999 Jun;14(3): 152–62.


