Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№03 2003
Объективная и субъективная оценки нежелательных явлений при изучении сравнительной переносимости антидепрессантов №03 2003
Изучение переносимости тимоаналептической терапии является одним из актуальных вопросов современной психофармакотерапии депрессивных расстройств. Наибольшее распространение получил метод оценки переносимости антидепрессантов путем регистрации их побочных эффектов. Частота возникновения побочных эффектов при терапии антидепрессантами может варьировать в широких пределах. Так, по данным Л.И.Спивак и соавт. [1], побочные эффекты наблюдаются у 15–30% пациентов, принимающих трициклические антидепрессанты (ТЦА) и у 11–27% – при использовании ингибиторов моноаминоксидазы (ИМАО). По данным многочисленных исследований, тимоаналептики нового поколения, прежде всего селективные ингибиторы обратного захвата серотонина (СИОЗС), хотя и не отличаются по своей эффективности от ТЦА и ИМАО, но обладают лучшей переносимостью по сравнению с предшественниками [2–6]. Вместе с тем частота отдельных побочных эффектов при терапии СИОЗС достигает 75% [7]. Такая вариабельность показателей обусловлена различиями в дизайнах клинических исследований, их продолжительности, а также в методах оценки побочных эффектов [7].
Инструменты для регистрации побочных реакций психофармакотерапии (шкалы, опросники) сходны с оценочными шкалами выраженности симптомов в том смысле, что также сосредоточены на выявлении клинических нарушений, хотя и вызываемых лекарственными средствами [8–10]. Целесообразность использования специализированных шкал по сравнению со спонтанными сообщениями обусловлена тем, что пациент не всегда считает нужным сообщать о побочных эффектах в ходе терапии, забывает об этом, не хочет "беспокоить" врача, а также может не расценивать появление новых или утяжеление имеющихся симптомов как возможные последствия психофармакотерапии [7].
Специальных шкал для регистрации побочного действия антидепрессантов не существует. С этой целью чаще других используется структурированная шкала побочных эффектов UKU [11]. Она включает перечень из 48 наиболее часто возникающих вследствие психофармакотерапии симптомов, распределенных по группам: психические, неврологические, вегетативные и др. В состав шкалы UKU также входит субшкала, оценивающая общее впечатление о влиянии побочных эффектов на повседневную жизнь пациента (по мнению врача и самого пациента).
Помимо отсутствия унификации методов регистрации побочных эффектов антидепрессантов, существует также проблема их интерпретации в ходе психофармакотерапии вследствие неспецифичности многих побочных эффектов и симптомов основного заболевания [12]. По этой причине при проведении клинических исследований фармакологических препаратов рекомендуется использовать термин "нежелательное явление", который в отличие от побочного эффекта рассматривается вне причинно-следственной связи с фармакологическим действием препарата и определяется как любое неблагоприятное явление (с медицинской точки зрения) в жизни пациента или субъекта исследования, возникшее во время фармакотерапии.
Целью настоящего исследования явилось изучение сравнительной переносимости антидепрессантов, различных по своей химической структуре и механизму действия. Для сравнительного изучения переносимости тимоаналептиков были отобраны пациенты, соответствующие следующим критериям включения: 1) наличие депрессивного расстройства в виде легкого или умеренного депрессивного эпизода, рекуррентного депрессивного расстройства с текущим эпизодом легкой или умеренной степени (не менее 15 баллов по шкале Гамильтона); 2) возраст от 18 до 65 лет. Критериями исключения являлись: 1) возраст моложе 18 и старше 65 лет; 2) органическое поражение ЦНС; 3) шизофрения; 4) биполярное расстройство; 5) алкоголизм; 6) острые или в стадии обострения хронические соматические и неврологические заболевания; 7) противопоказания к применению антидепрессантов.
В строгом соответствии с критериями включения/исключения в настоящее исследование вошли 90 человек. В изучаемом контингенте больных преобладали женщины (85,6%). Средний возраст пациентов составил 41,3±10,8 года. Большинство пациентов имели высшее образование (70%). Профессионально заняты были 81,1% пациентов, 13,3% составляли пенсионеры и 5,6% – инвалиды. В браке состояли 56,7% больных. Первичный депрессивный эпизод выявлен у 67,8%, рекуррентное депрессивное расстройство – у 32,2% больных. Тяжесть депрессивного эпизода во всей группе больных была расценена как легкая в 61,1% и как умеренная в 38,9% случаев. Синдромальная оценка депрессии позволила выделить тревожный (у 33,3% больных), астенический (25,6%), тоскливый (24,4%), истерический (16,7%) и ипохондрический (3,3%) варианты.
Для решения поставленных задач было проведено клиническое изучение 3 антидепрессантов, различных по своей химической структуре и механизму действия: амитриптилина – ТЦА, флуоксетина – СИОЗС и тианептина (коаксила), основной механизм действия которого основан на усилении обратного захвата серотонина (ССОЗС). Схема проведения исследования включала недельный период "wash-out" и 4-недельный период тимоаналептической монотерапии. Состояние больных оценивали каждые 7 дней.
Было сформировано 3 группы пациентов по 30 человек в каждой. Первая группа больных получала амитриптилин (по 25 мг 4 раза в день), вторая – флуоксетин (по 20 мг утром), третья – тианептин (по 12,5 мг 3 раза в день). Больные в трех группах сопоставимо распределились по большинству из изучаемых факторов.
Общую эффективность тимоаналептической терапии оценивали по редукции общего балла шкалы депрессии Гамильтона. За 4 нед курсовой терапии антидепрессантами полная редукция депрессивной симптоматики (на 50% и более) отмечена у 81,1%, частичная редукция (на 25–49%) – у 13,3%, а отсутствие редукции (менее 25%) – у 5,6% больных. К концу 4-й недели изучаемые тимоаналептики практически не отличались друг от друга по эффективности.
Оценку нежелательных явлений проводили с помощью структурированной шкалы побочных эффектов UKU и шкалы общего впечатления о влиянии побочных эффектов на повседневную жизнь пациента (самооценка).
Нежелательные явления, регистрируемые по шкале UKU, выявлены у 30 (100%) пациентов, принимавших амитриптилин, у 25 (83,3%) – флуоксетин и у 24 (80%) – тианептин. Наиболее частыми нежелательными явлениями у всех антидепрессантов были сонливость (у 100% больных, принимавших амитриптилин, 46,7% – флуоксетин и 30% – тианептин) и сухость во рту (100% – амитриптилин, 40% – флуоксетин и 16,7% – тианептин).
В отношении количества нежелательных явлений, возникающих во время применения изучаемых антидепрессантов, установлено, что больше всего их отмечено в группе флуоксетина (22 симптома); на втором месте – группа тианептина (18 симптомов) и меньше всего – в группе амитриптилина (16 симптомов).
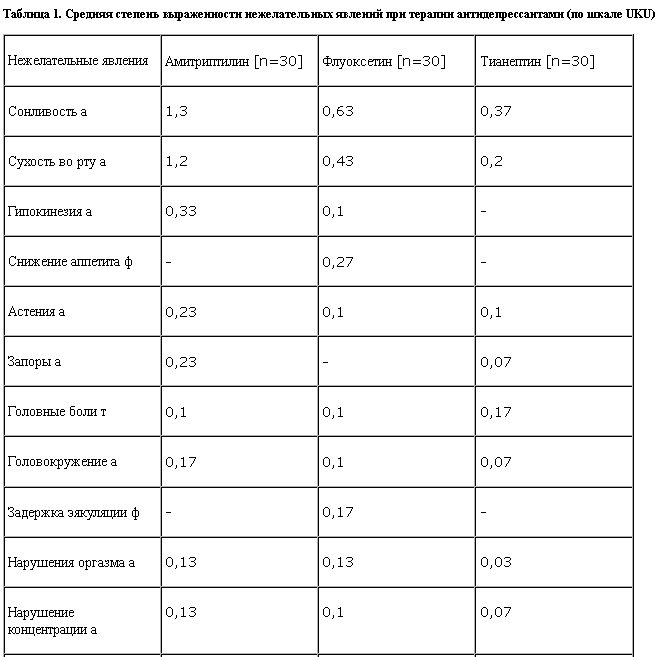
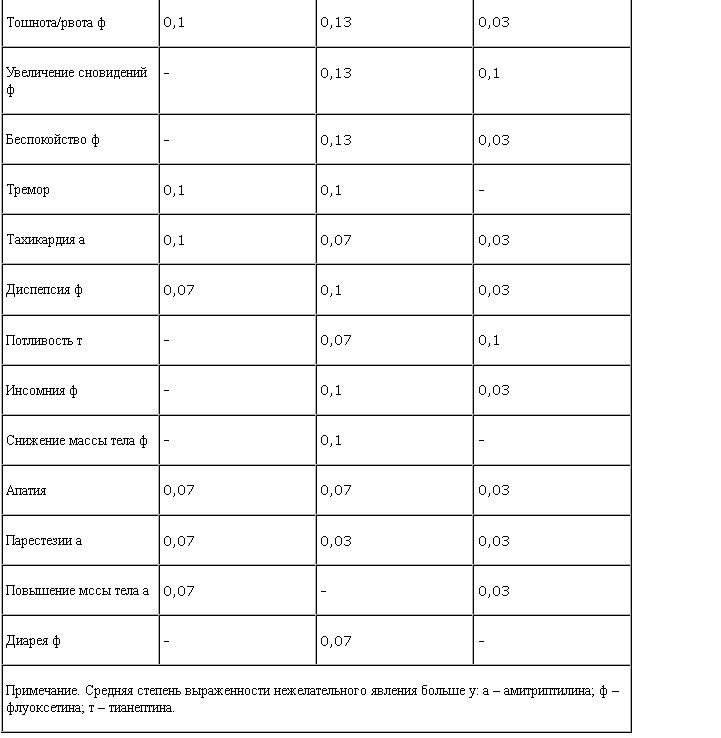
Максимальное значение средней степени выраженности нежелательных явлений было наибольшим – в группе амитриптилина (1,3), меньше – в группе флуоксетина (0,63) и наименьшим в группе тианептина (0,37).
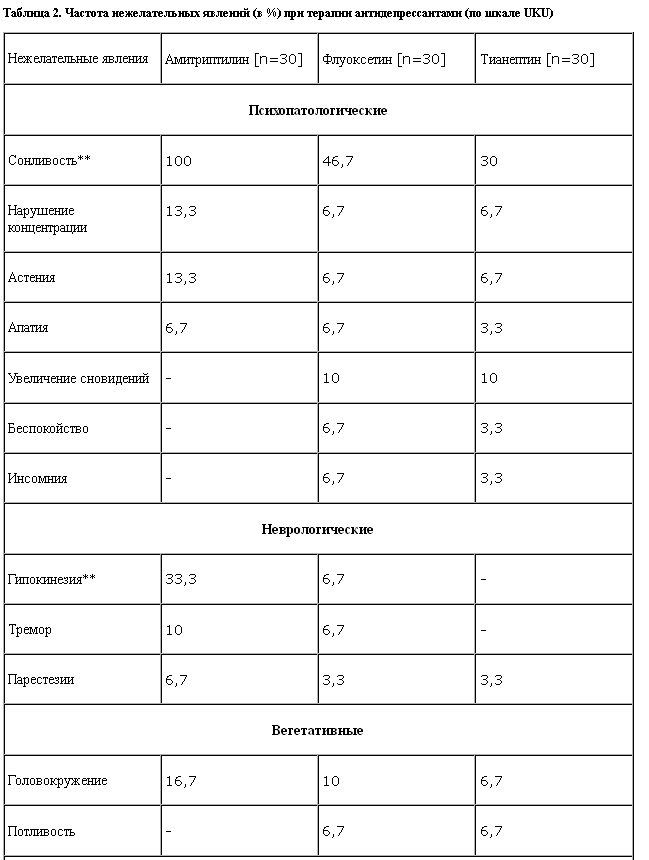
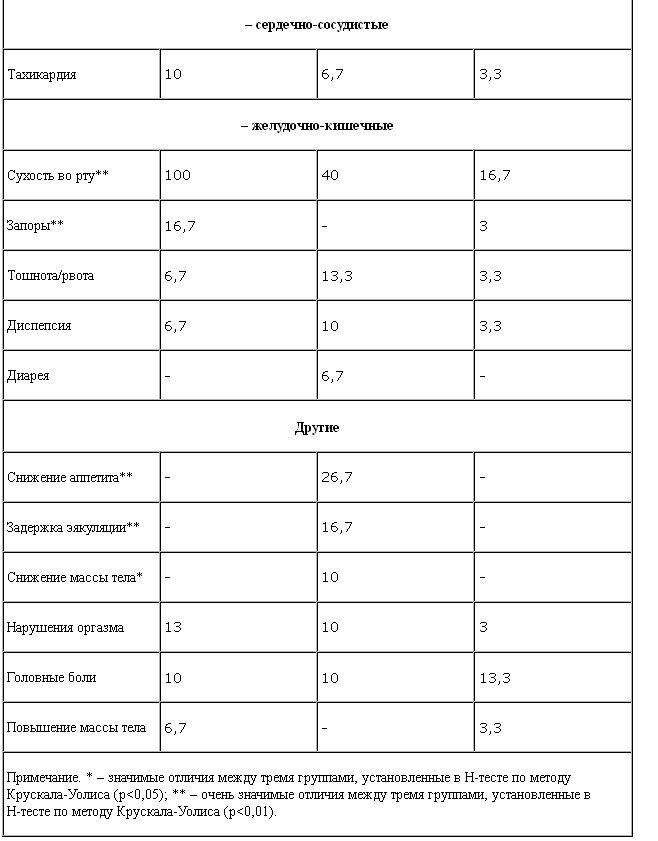

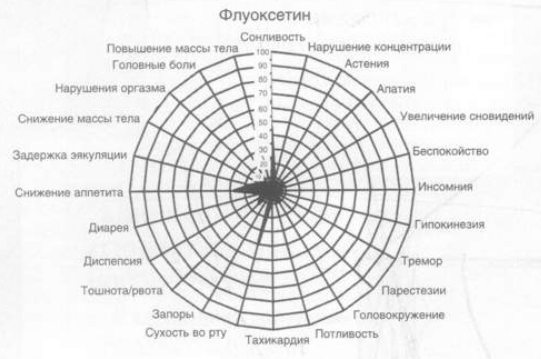
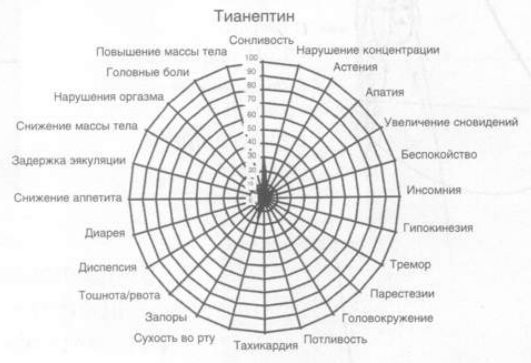
Динамическая оценка переносимости антидепрессантов на протяжении 4 нед терапии показала, что выявленные различия в частоте их нежелательных явлений исчезают к концу 3–4-й недели терапии по большинству показателей. Исключение составляют только 2 показателя: снижение аппетита и массы тела, отмечаемые при приеме флуоксетина, частота которых нарастает в процессе терапии (рис. 2).
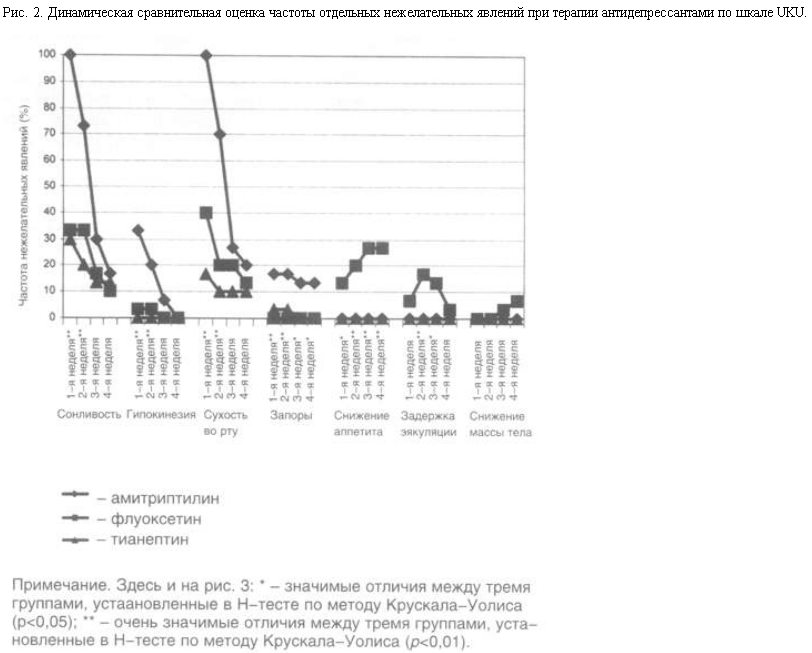
Полученные данные свидетельствуют о постепенной адаптации пациентов в процессе психофармакотерапии, приводящей к повышению толерантности, к нежелательным явлениям антидепрессантов.
Аналогичная тенденция к уменьшению значимости различий между частотами нежелательных явлений антидепрессантов на протяжении 4-недельной терапии отмечена и по данным их самооценки (рис. 3).
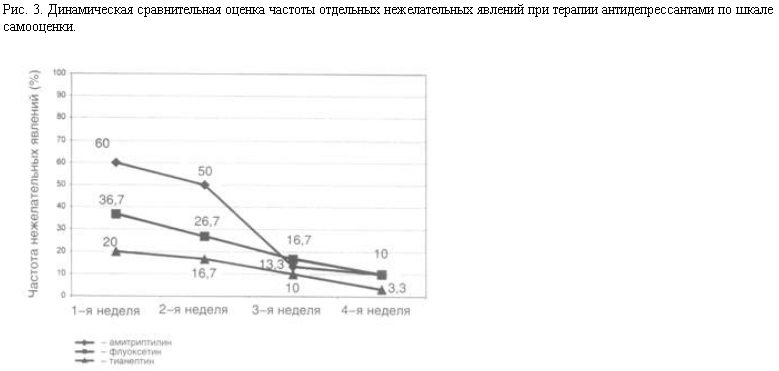
Полученные данные об объективной и субъективной оценке свидетельствуют о наличии общей тенденции к уменьшению числа больных с нежелательными явлениями в ряду амитриптилин > флуоксетин > тианептин. При этом объективная оценка выявила на 30–53,3% больше больных с нежелательными явлениями, чем их субъективная оценка (рис. 4).
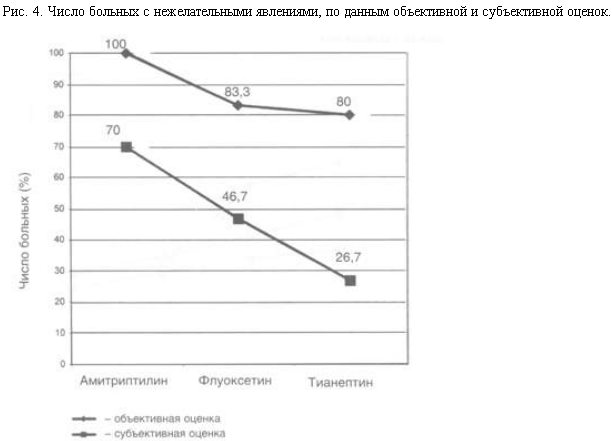
Анализ различий между показателями субъективной и объективной оценок выявил, что для части нежелательных явлений (инсомния, апатия, увеличение сновидений, снижение аппетита, сухость во рту, потливость, запоры, головные боли, нарушения оргазма), была характерна их субъективная агнозия. Большинство этих симптомов имманентны депрессивному состоянию пациентов, что объясняет факт их агнозии у изучаемых больных.
Другие нежелательные явления, представленные преимущественно соматоневрологическими симптомами, присоединившимися к клинической картине основного психического расстройства и отягощающими психическое состояние больных ухудшением их соматического состояния, субъективно отмечены пациентами. При этом большая часть таких нежелательных явлений (беспокойство, головокружение, парестезии, тремор, тахикардия, диспепсия, снижение или повышение массы тела, задержка эякуляции) относительно легко переносилась больными, и лишь небольшое число симптомов (сонливость, астения, гипокинезия, тошнота, рвота и диарея) оказывалось субъективно непереносимыми вследствие их значительного влияния на повседневную активность пациентов, что приводило к отказам от терапии тимоаналептиками.
Таким образом, в результате проведенного исследования было установлено, что антидепрессанты различной химической структуры и механизма действия (амитриптилин, флуоксетин, тианептин) отличаются по частоте, выраженности и профилю вызываемых ими нежелательных явлений. Сравнительный анализ их переносимости выявил уменьшение числа больных с нежелательными явлениями в ряду амитриптилин > флуоксетин > тианептин. При динамической оценке переносимости терапии антидепрессантами обнаружены статистически достоверные различия в спектре нежелательных явлений амитриптилина, флуоксетина и тианептина, отмечаемые в первые 2 нед терапии, которые нивелируются к концу 3–4-й недели курсовой терапии вследствие адаптации больных к нежелательным явлениям. Также показано, что объективная регистрация нежелательных явлений и их субъективная оценка являются относительно самостоятельными показателями переносимости терапии антидепрессантами у больных с депрессивными расстройствами. При субъективной оценке нежелательных явлений определяется на 30–53,3% больных меньше, чем при их объективной регистрации за счет агнозии пациентами части симптомов.
Настоящее исследование затрагивает лишь некоторые аспекты оценки переносимости тимоаналептической фармакотерапии, нуждающиеся в дальнейшем изучении.
Список исп. литературыСкрыть список1. Спивак Л.И., Райский В.А., Виленский Б.С. Осложнения психофармакотерапии. Л.: Медицина, 1988; 168 с.
2. Аведисова А.С. Лимит эффективности антидепрессантов. XIII Съезд психиатров России (материалы съезда). М., 2000; 171 с.
3. Anderson IM. Meta-analytical studies on new antidepressants. Br Med Bull 2001; 57: 161–78.
4. Montgomery SA et al. Selective Serotonin Reuptake Inhibitors: Meta-Analysis of Discontinuation Rates, International Clinical Pharmacology 1994, 9: 47–53.
5. Preskorn SH. The Adverse Effect Profiles of the Selective Serotonin Reuptake Inhibitors: Relationship to In Vitro Pharmacology, Journal of Practical Psychiatry and Behavioral Health, May 2000, 153–7.
6. Richelson E. 2001 Pharmacology of Antidepressants. Mayo Clin Proc 2001; 76: 511–27.
7. Ferguson JM. SSRI Antidepressant Medications: Adverse Effects and Tolerability, Primary Care Companion J Clin Psychiatry 2001; 3: 22–7.
8. Castle WM. Problems in assessing drug safety: A plea for improved methodology and a possible route. Drug Info J 1986; 20: 323–6.
9. Laughren TP, Levine J, Levine J, Thompson WL. Premarketing safety evaluation of psychotropic drugs. In: Prien RF, Robinson DS, eds. Clinical Evaluation of Psychotropic Agents: Principles and Guidelines. New York: Raven Press, 1994; 185–216.
10. Levine J, Schooler N. Strategies for analysing side effects data from SAFTEE. Psychopharmacol Bull 1986; 22: 343–81.
11. Lingjarde O, Ahlfors UG, Bech P. The UKU side effect rating scale. A new comprehensive rating. Acta Psychiatr Scand (Suppl) 1987; 334: 1–100.
12. Naranjo CA et al. A method for estimating the probability of adverse drug reactions. Clin Pharmacol Ther 1981; 30 (2): 239–45.


