Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№04 2003
Использование антидепрессанта циталопрам при лечении больных с алкогольной зависимостью №04 2003
Лечение алкогольной зависимости остается одной из самых актуальных проблем наркологии. Его важным принципом является дифференцированное применение психофармакотерапии с учетом всего спектра психопатологических расстройств [1, 2]. Патологическое влечение к алкоголю (ПВА) – стержневое расстройство синдрома зависимости. Изучение механизмов патологического влечения к алкоголю показало ведущую роль катехоламиновой системы как биологической основы алкогольной зависимости [3]. Нормализация катехоламиновой нейромедиации приводит к дезактуализации ПВА, сглаживанию аффективных нарушений, стабилизации поведения больных. В настоящее время появились данные о возможности регуляции метаболизма катехоламинов посредством воздействия на серотониновую нейромедиацию [1, 4]. Важно при этом подчеркнуть, что если совсем недавно антидепрессанты использовались только при лечении депрессивных расстройств, развившихся в клинике алкогольной зависимости, то сегодня серотонинергические антидепрессанты применяются как средства, купирующие ПВА (anticraving), в том числе и у больных без признаков депрессивных расстройств. Это обстоятельство свидетельствует об актуальности и важности разработки нового направления патогенетической терапии алкогольной зависимости – использования антидепрессантов как средств, подавляющих ПВА.
Циталопрам относится к группе селективных ингибиторов обратного захвата серотонина (СИОЗС). Он является представителем группы антидепрессантов со сбалансированным механизмом действия, т.е. его седативный и стимулирующий эффекты практически уравновешивают друг друга. Циталопрам хорошо зарекомендовал себя в психиатрической практике при лечении тревожных состояний, панических расстройств, атипичных депрессий, сопровождающихся дисфорическими явлениями [5]. Следует отдельно отметить, что у циталопрама не обнаружено холинолитических и кардиотоксических побочных эффектов, что расширяет спектр его применения. Препарат отличается малым потенциалом взаимодействия с другими лекарственными средствами.
В связи с вышесказанным целью данного исследования явилось изучение эффективности циталопрама при терапии ПВА, аффективных расстройств, связанных с алкогольной зависимостью.
Материал и методы исследования
В открытое контролируемое исследование было включено 30 мужчин с алкогольной зависимостью средней стадии, проходивших стационарный курс лечения в отделении клинической психофармакологии ННЦ наркологии Минздрава РФ. Возраст пациентов варьировал от 22 до 62 лет, средний возраст составил 45±7,8 года. Длительность алкогольной зависимости – от 5 до 25 лет.
Клинические проявления заболевания характеризовались сформированным ПВА, алкогольным абстинентным синдромом, постоянной или псевдозапойной формой пьянства, симптомом утраты количественного контроля, повышенной толерантностью к алкоголю. Алкогольный абстинентный синдром включал в себя сочетание соматовегетативных и психопатологических расстройств.
У 20 пациентов в структуре психопатологических расстройств абстинентного синдрома, ПВА превалировали: подавленное настроение, пассивность, медлительность, вялость, раздражительность, дисфория, внутренняя напряженность, нарушения сна в сочетании с тревогой. Помимо этого, отмечены фиксация на жизненных невзгодах и понесенных обидах, пессимистическая оценка прошлого, настоящего и будущего, нежелание чем-либо заниматься, ощущение внутреннего дискомфорта, чувство угнетенности.
У 10 больных не выявлено депрессивных проявлений (или они были незначительно выражены) ни в структуре абстинентного синдрома, ни при актуализации ПВА. В картине обострения ПВА преобладали поведенческие и идеаторные компоненты.
У всех больных в структуре абстинентного синдрома отмечены гипергидроз, жажда, тремор, диспепсические нарушения, колебания артериального давления, тахикардия, слабость, разбитость. Степень его выраженности расценивали как легкую у 20 больных, средней тяжести – у 10 больных.
Изменения личности проявлялись, в основном, заострением преморбидных особенностей, среди которых преобладали черты неустойчивости, синтонности, астеничности; реже встречались черты шизоидности, истеровозбудимости, эпилептоидности. Практически во всех случаях отмечены неблагоприятные социальные последствия заболевания: нарушение семейных отношений, неприятности на работе, снижение профессиональной квалификации. У большинства (25 пациентов) темп прогредиентности заболевания был квалифицирован как средний; у 90% (27 больных) отмечена периодическая форма злоупотребления, у 10% (3 больных) – постоянная на фоне высокой толерантности.
Первично госпитализированные больные составляли 70% (21 пациент); повторно госпитализированные – 30% (9 больных).
Из исследования исключали больных с острыми психотическими расстройствами, высоким суицидальным риском, хроническими соматическими заболеваниями в стадии обострения; получавших лечение в течение 30 дней, предшествующих включению в исследование, антидепрессантами, антиконвульсантами, нейролептиками, транквилизаторами; принимавших участие в исследованиях в течение 3 предшествующих месяцев.
Основными методами исследования являлись клинико-психопатологический, статистический. При оценке спектра терапевтической эффективности препарата использовали специально разработанные в отделении клинической психофармакологии шкалы оценки психопатологических и соматовегетативных проявлений в алкогольном абстинентном синдроме, постабстинентном состоянии, шкалу Гамильтона для оценки депрессии, шкалу общего клинического впечатления.
Клиническое исследование препаратов проводили с использованием специально разработанного "Протокола", максимально отвечающего международным требованиям GCP.
Статистическую обработку полученных результатов проводили с использованием компьютерной программы Microsoft Excel 2000. В связи с поставленными задачами проводили внутригрупповое сравнение. Проверяли достоверность изменения ПВА, выраженность аффективных и поведенческих расстройств под влиянием циталопрама. Критерием достоверности считали достижение уровня pЈ0,05 и меньше. Количественные показатели сравнивали при помощи t-критерия Стьюдента.
Исследование проводили в три этапа.
Первый этап – купирование аффективных расстройств в структуре алкогольного абстинентного синдрома. Применение циталопрама начинали с первого дня отказа от алкоголя. Терапевтическая доза – 20–40 мг в день. Лечение было комплексным: дезинтоксикационные мероприятия, общеукрепляющее и симптоматическое лечение. При выраженных расстройствах сна дополнительно, в течение 2–3 дней, пациенты получили феназепам – 1–2 мг на ночь. Длительность первого этапа составляла до 10 дней.
Второй этап – лечение аффективных расстройств в постабстинентном состоянии и на этапе формирования ремиссии. Циталопрам являлся единственным психотропным средством в комплексной терапии. Терапевтическая доза – 20–40 мг в день. Длительность второго этапа составляла до 2 мес.
Со всеми больными на первом и втором этапах проводили рациональную психотерапию алкогольной зависимости.
Третий этап – катамнестическое наблюдение за больными с целью оценки эффективности профилактики ранних рецидивов без медикаментозной терапии. Длительность третьего этапа исследования – до 3 мес.
Обследование больных осуществляли в день поступления (0-й день), в дальнейшем – на 3, 7, 14, 21, 30, 45, 60, 90-й дни терапии.
Результаты исследования
При анализе результатов применения циталопрама у 30 больных с алкогольной зависимостью выявлено, что препарат обладает достаточно выраженным воздействием на ПВА. У больных с преобладанием аффективных проявлений в структуре абстинентного синдрома циталопрам начинал действовать уже с первых дней приема. Об этом свидетельствовала следующая динамика. На 3-й день лечения у больных значительно уменьшалась тревога, стабилизировался фон настроения; одновременно снижалась интенсивность ПВА (табл. 1). Дисфорическая симптоматика и раздражительность редуцировались несколько медленнее – к 5–6-му дню терапии.
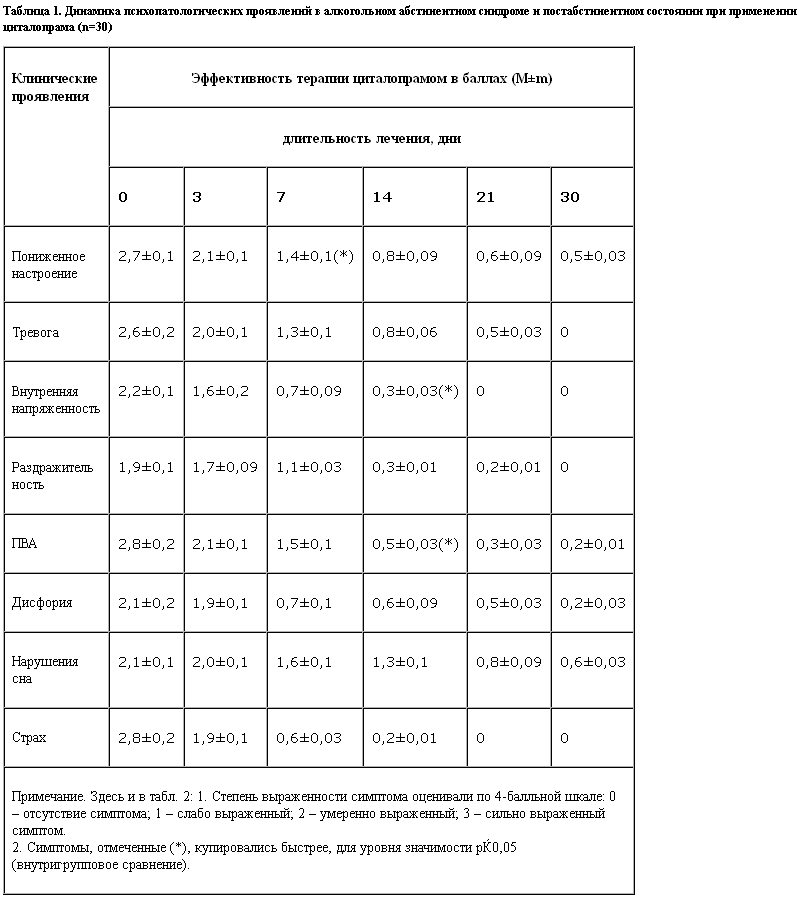
Несколько иными оказались результаты применения циталопрама у пациентов с преобладанием поведенческих и идеаторных расстройств в структуре ПВА. Видимое терапевтическое действие на ПВА препарат проявлял к 4–7-му дню терапии. Быстрее купировалась интенсивность его идеаторного компонента. Влияние циталопрама на поведенческую сферу происходило медленнее: на 10–14-й день уменьшались такие нарушения, как несобранность, непоседливость, стремление уклониться от лечения, недовольство режимом отделения, желание ускорить выписку из больницы. С 5–6-го дня лечения у пациентов исчезали сновидения с алкогольной тематикой.
Седативный и снотворный эффекты препарата можно оценить как слабо выраженные. Сон у больных при лечении циталопрамом обычно восстанавливался лишь к 7–8-му дню терапии. В то же время при сочетании инсомнических и тревожных расстройств по мере снижения интенсивности тревоги сон нормализовался к 4–5-му дню терапии. При значительных пресомнических и интрасомнических расстройствах (7 клинических случаев) назначали небольшие дозы бензодиазепинов.
Влияние циталопрама на соматовегетативную симптоматику в рамках абстинентного синдрома можно оценить как положительное, но слабо выраженное (табл. 2). Более высокая терапевтическая активность наблюдалась при купировании таких симптомов, как колебания артериального давления, тошнота, жажда. У больных на 2–3-й дни лечения заметно улучшалось физическое состояние, исчезали слабость, вялость, истощаемость и пассивность.
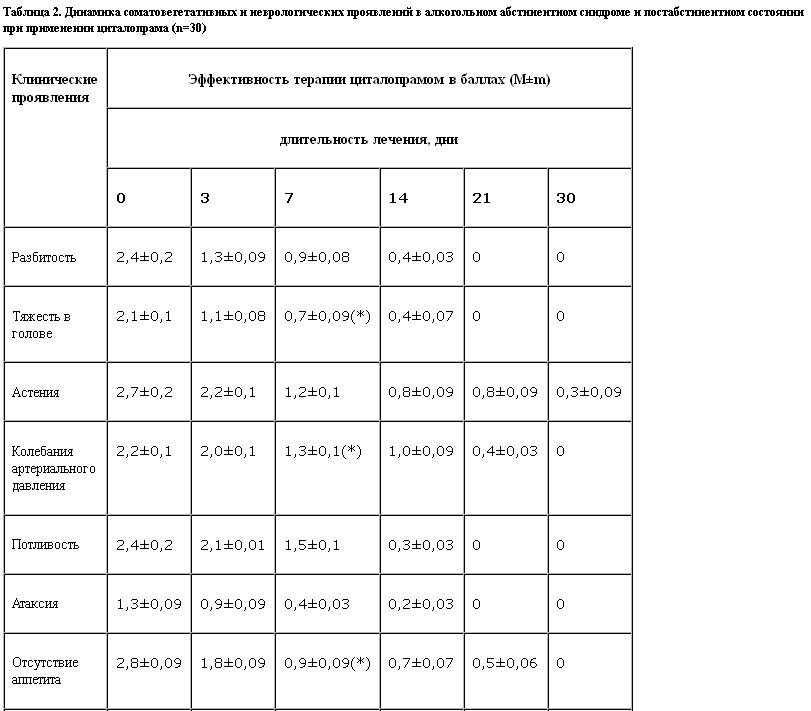
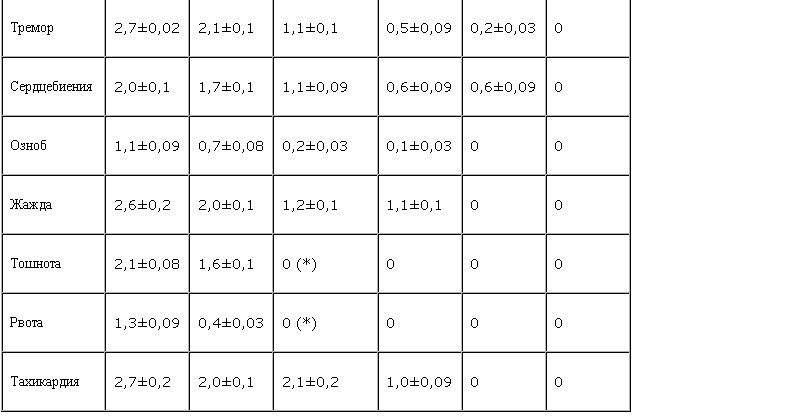
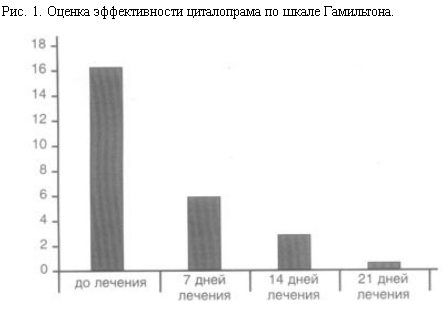
Результаты исследования показали, что на данной выборке больных циталопрам обладает достаточно выраженным антидепрессивным действием. К 7-му дню терапии у больных отмечено снижение общего числа по шкале Гамильтона на 65% по сравнению с исходным, а к 21-му дню депрессивные расстройства полностью исчезали (рис. 1).
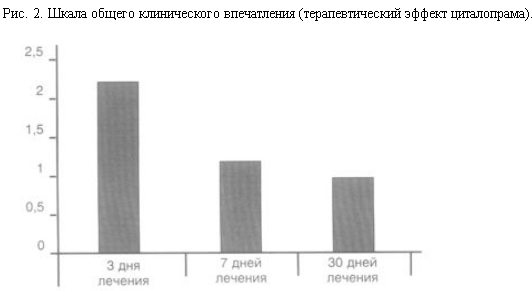
Использование шкалы общего клинического впечатления позволило подтвердить значительный терапевтический эффект циталопрама, который квалифицировался как значительное улучшение в рамках его купирующего действия на ПВА и антидепрессивного действия (рис. 2).
Высокая терапевтическая эффективность циталопрама в отношении ПВА, отсутствие угнетающего эффекта на когнитивные и психомоторные функции способствовали более быстрому включению пациентов в психотерапевтический процесс, повышали мотивацию больных на лечение и отказ от алкоголя.
Осложнений при назначении циталопрама не наблюдали; прекращение его приема не сопровождалось развитием синдрома отмены. По данным самоотчетов больных, в 2 случаях в конце второго этапа исследования наблюдали побочный эффект – задержка эякуляции. При прекращении приема препарата пациенты не предъявляли жалоб на сексуальные нарушения. На фоне приема циталопрама не было отмечено усиления ПВА, нарастания тревоги, дисфорической симптоматики.
По данным катамнестического наблюдения в течение 3 мес (12 нед) рецидивов не наблюдали.
Обсуждение
Проведенное клиническое исследование позволило сделать следующие выводы. Циталопрам оказался эффективным препаратом при лечении больных с алкогольной зависимостью. Выявлена его эффективность не только при терапии депрессивных проявлений в структуре алкогольного абстинентного синдрома и ПВА, но и при купировании ПВА с преобладанием поведенческого и идеаторного компонентов. Таким образом, циталопрам непосредственно влияет на ПВА, в том числе и у больных без депрессивных расстройств.
При алкогольном абстинентном синдроме выявлена его достаточная терапевтическая эффективность по отношению к таким психопатологическим проявлениям, как сниженное настроение и тревожность. Влияние на дисфорическую симптоматику можно оценить как умеренно выраженное. Вегетостабилизирующее действие выражено слабо и проявляется на 3–4-й день его применения.
Седативный и снотворный эффекты препарата также слабо выражены. Лучше снотворный эффект препарата проявлялся при сочетании инсомнических и тревожных расстройств, когда по мере снижения интенсивности тревоги восстанавливался и сон.
Отдельно следует отметить, что циталопрам достаточно хорошо и быстро купировал адинамический компонент депрессивных расстройств и проявления астенодепрессивного симптомокомплекса. При этом на всем протяжении приема препарата не отмечено ни чрезмерной стимуляции, ни актуализации ПВА, ни нарастания тревоги, ни оживления дисфорической симптоматики.
К положительным свойствам препарата следует также отнести отсутствие угнетения когнитивных и психомоторных функций, осложнений при приеме. Хорошая переносимость циталопрама высоко значима при длительном его применении и проведении поддерживающей терапии.
Полученные результаты имеют большое значение для лечения больных с алкогольной зависимостью и позволяют рекомендовать включение циталопрама как достаточно эффективного и безопасного антидепрессанта в комплексные терапевтические программы.
