Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№06 2008
Терапия депрессивных нарушений при хирургической менопаузе №06 2008
Номера страниц в выпуске:35-38
В последние годы отмечается рост гинекологических заболеваний, таких как доброкачественные опухоли матки и ее придатков, эндометриоз, требующих радикального оперативного вмешательства, и происходит омоложение контингента оперированных женщин. Согласно данным литературы, постовариэктомический синдром, при хирургической менопаузе наблюдается у 60–80% женщин. У 70–75% женщин обратное его развитие происходит в течение 1-го года после операции, у 25% пациенток наблюдается тяжелое течение, продолжающееся 2–5 лет и более. Аффективные нарушения разной степени выраженности развиваются у 40–68% женщин с хирургической менопаузой. Своей сложностью проблема аффективных расстройств, возникающих при хирургической менопаузе, обязана большому количеству факторов, ее обусловливающих.
Признаваемое всеми исследователями преобладание лиц женского пола среди пациентов, страдающих депрессиями (в соотношении около 2,5:1), требует особого внимания к изучению причин, способствующих формированию и особенностям течения аффективных расстройств и поискам новых адекватных подходов к лечению с учетом комплекса факторов, способствующих их развитию.
В последние годы отмечается рост гинекологических заболеваний, таких как доброкачественные опухоли матки и ее придатков, эндометриоз, требующих радикального оперативного вмешательства, и происходит омоложение контингента оперированных женщин.
Согласно данным литературы, постовариэктомический синдром, при хирургической менопаузе наблюдается у 60–80% женщин. У 70–75% женщин обратное его развитие происходит в течение 1-го года после операции, у 25% пациенток наблюдается тяжелое течение, продолжающееся 2–5 лет и более. Аффективные нарушения разной степени выраженности развиваются у 40–68% женщин с хирургической менопаузой. Своей сложностью проблема аффективных расстройств, возникающих при хирургической менопаузе, обязана большому количеству факторов, ее обусловливающих. Фундаментальные исследования последних лет показали, что разные типы эстрогеновых (альфа и бета), прогестероновых (А и Б) и тестостероновых рецепторов расположены не только в репродуктивных органах-мишенях (матке и молочных железах). Они обнаружены также в центральной нервной системе, клетках костной ткани, эндотелии сосудов, миокардиоцитах, фибробластах, соединительной ткани, урогенитальном тракте, в слизистых оболочках рта, гортани, конъюнктивы, толстом кишечнике. Следовательно, резко возникающий дефицит половых стероидов (прежде всего эстрогенов) способствует системным изменениям в органах и тканях вследствие нарушения гормонального гомеостаза. К последствиям дефицита половых гормонов после билатеральной овариэктомии с гистерэктомией можно отнести ряд симптомов. Наиболее значимыми являются: нейровегетативные симптомы, аффективные расстройства, урогенитальные расстройства, потеря кальция и коллагена из костной ткани (остеопороз), повышение частоты сердечно-сосудистых заболеваний.
Однако при достаточном интересе к этой проблеме специалистов разных специальностей опыт применения современных антидепрессантов, при указанных состояниях невелик, а данные о комбинированной терапии в сочетании с препаратами натуральных эстрогенов практически отсутствует. До настоящего времени не разработаны комплексные подходы с использованием заместительной гормональной терапии (ЗГТ) и психофармакотерапии, отсутствуют общепринятые рекомендации по комплексной терапии депрессивных расстройств, развивающихся при хирургической менопаузе.
Целью исследования явилось изучение эффективности препарата Коаксил (тианептин) при лечении депрессивных нарушений, развивающихся при хирургической менопаузе.
Материалы и методы
Исследование проведено на базе ФГУ Научный центр акушерства, гинекологии и перинатологии им. акад. В.И.Кулакова Федерального агентства по высокотехнологичной медицинской помощи. С помощью скринингового опросника выявлены женщины с признаками аффективных нарушений в возрасте до 50 лет, наблюдающиеся врачами-гинекологами по поводу расстройств, связанных с хирургической менопаузой.
Анализировалась эффективность терапии в двух основных терапевтических группах больных, выделенных на основании критерия последовательности назначения антидепрессантов и ЗГТ.
Последовательность назначения антидепрессантов и ЗГТ определялась с учетом особенностей клинической картины: при преобладании аффективных расстройств первично назначали курс психофармакотерапии, за которым следовал курс ЗГТ (АГ-вариант; n=26), при доминировании соматовегетативных нарушений и наличии показаний для неотложного проведения гормонотерапии в связи с нарастающими признаками гормонодефицита курс ЗГТ предшествовал курсу терапии антидепрессантом (ГА-вариант, n=20).
Для оценки тяжести симптомов депрессии и тревоги, а также динамики состояния пациентов при проведении фармакотерапии использовались шкалы тревоги и депрессии Гамильтона (версия шкалы Гамильтона, состоящая из 17 пунктов – HDRS17).
Для ЗГТ применялись препараты натуральных эстрогенов – 17b-эстрадиола валерат (Эстрофем; 1 мг/сут перорально), эстрадиола гемигидрат (Дивигель; 0,5–1,0 г геля для наружного применения), трансдермальная система эстрадиола (Климара; 0,05 мг/сут). Продолжительность терапии составляла не менее 3 мес. ЗГТ назначалась врачом-гинекологом. Решение вопроса о целесообразности ЗГТ в каждом конкретном случае принималось с учетом не только появившихся симптомов, но и возможности возникновения системных нарушений и имеющихся противопоказаний. Следует отметить, что уровень содержания фолликулостимулирующего гормона (ФСГ) и эстрадиола в крови был сопоставимым в обеих группах и соответствовал уровню гормонов в постменопаузальном периоде – ФСГ 74,8±4,3 МЕ/л (N: 28,0–190 МЕ/л), эстрадиол – 77,1±7,8 пмоль/л (N:12,0–296 пмоль/л). На фоне проведения ЗГТ уровень гормонов достоверно менялся. Такая динамика позволила оценивать влияние психофармакотерапии в обеих описываемых группах без дополнительного учета влияния ЗГТ.
В исследовании применяли препарат Коаксил, представленный в виде таблеток, содержащих 12,5 мг тианептина. Препарат назначали в начальной дозе 25 мг/сут (по 12,5 мг 2 раза в день), в процессе терапии дозу увеличивали до 37,5 мг/сут (по 12,5 мг 3 раза в день).
Основной метод исследования – клинико-терапевтический. При выборе препарата для проведения исследования руководствовались особенностями фармакологических эффектов, в частности наличием наряду с антидепрессивным анксиолитического и рединамизирующего эффекта при отсутствии седативных свойств и отрицательного влияния на когнитивные процессы, а также адаптогенных эффектов за счет способности понижать реактивность гипоталамо-гипофизарно-надпочечниковой системы в ответ на стресс. Задачей исследования также являлась оценка возможности сочетания действие антидепрессанта с ЗГТ. Для этого был необходим препарат с незначительным числом нежелательных побочных соматотропных эффектов.
Результаты исследования
Отобрано 50 пациенток с клиническими признаками депрессивного расстройства легкой, умеренной степени тяжести. Средний возраст составил 43,8±3,5 года. В конечную группу анализа вошли 46 пациенток, 2 пациентки после проведения ЗГТ отказались от лечения антидепрессантами, 2 прекратили участие в исследовании из-за побочных эффектов.
В исследование были включены случаи, соответствовавшие следующим диагностическим рубрикам по классификации МКБ-10:
У пациенток 2-й группы выраженность собственно аффективных нарушений была менее значительной, на первое место в клинической картине этих состояний выходили соматовегетативные проявления (приливы, сердцебиения, озноб, жар, потливость, головные боли) как наиболее дезадаптирующие, в то же время отчасти маскирующие всю остальную психопатологическую симптоматику. У пациенток этой группы в процессе гормональной терапии эстрогенами частично редуцировались соматовегетативные проявления, выравнивался общий фон настроения, улучшался сон, повышалась работоспособность.
По HDRS уровень депрессии в среднем составил 17±4 балла, а уровень психической и соматической тревоги – 9 и 10 баллов соответственно.
При сравнении показателей шкалы депрессии HDRS, соматических и психических компонентов тревоги HARS у больных обеих групп установлено следующее. В 1-й группе (АГ) показатель HDRS был достоверно выше. Значение психического компонента тревоги преобладало над уровнем соматической тревоги у больных 1-й группы, а соматической тревоги над психической – во 2-й группе (ГА).
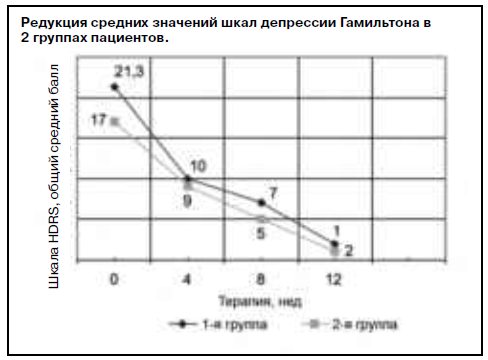
Подтверждением эффективности проведенной терапии служит прогрессирующая редукция средних значений шкал депрессии Гамильтона (см. рисунок). Динамика показателей HDRS свидетельствует о статистически достоверном снижении выраженности депрессивной симптоматики в процессе лечения. На основе показателей редукции суммарного рейтинга баллов шкалы Гамильтона к окончанию курса терапии в общей группе больных, получавших тианептин, были выделены группа респондеров – 38 человек и нонреспондеров – 8 человек. В 1-й группе были 24 респондера и 2 нонреспондера, во 2-й – 14 респондеров и 6 нонреспондеров.
В группу респондеров были включены пациенты, у которых редукция суммарного рейтинга баллов по шкале Гамильтона составила 50% и более.
Психопатологическая симптоматика в большинстве случаев в группе респондеров носила тревожно-тоскливый характер с моторной и идеаторной заторможенностью, витальным ощущением тоски, периодической безотчетной тревогой, суточными колебаниями аффекта с улучшением к вечеру, снижением аппетита, нарушениями сна и ранними пробуждениями, сверхценными идеями бесперспективности, виновности, ненужности, брошенности. Идеаторный компонент был выражен менее отчетливо. Наблюдались ипохондрические симптомы с фиксацией на состоянии своего здоровья, выраженными соматовегетативными расстройствами по типу приливов, несмотря на массивность и представленность собственно психопатологической симптоматики.
В группу нонреспондеров вошли 8 пациенток, у которых редукция рейтинга баллов по шкале Гамильтона составила менее 50% от исходного уровня. Клинико-анамнестические характеристики этой группы отличались от таковых группы респондеров. Имелись четкие указания на перенесенные ранее аффективные нарушения, при этом 3 пациентки получали терапию амитриптилином и леривоном.
В клинической картине у пациенток этой группы наряду с умеренно сниженным настроением доминировали проявления тревоги, часто ситуационной, связанной с беспокойством за себя и близких, ангедонические жалобы, чувство апатии, утрата “жизненного тонуса”, астения.
В исследовании отмечалась хорошая переносимость препаратов, незначительное количество побочных эффектов. Пациенты предъявляли ряд жалоб (тианептин: тошнота, чувство слабости, сухость во рту, головные боли, парестезии).
Обсуждение
В последние годы отмечается рост гинекологических заболеваний, таких как доброкачественные опухоли матки и ее придатков, эндометриоз, требующих радикального оперативного вмешательства, и происходит омоложение контингента оперированных женщин.
Согласно данным литературы, постовариэктомический синдром, при хирургической менопаузе наблюдается у 60–80% женщин. У 70–75% женщин обратное его развитие происходит в течение 1-го года после операции, у 25% пациенток наблюдается тяжелое течение, продолжающееся 2–5 лет и более. Аффективные нарушения разной степени выраженности развиваются у 40–68% женщин с хирургической менопаузой. Своей сложностью проблема аффективных расстройств, возникающих при хирургической менопаузе, обязана большому количеству факторов, ее обусловливающих.
Проблема расстройств депрессивного спектра, развивающихся при хирургической менопаузе, становится все более актуальной в связи с увеличением числа пациенток, перенесших овариэктомию с тотальной или субтотальной резекцией матки. Патогенетически обоснованной для лечения пациенток при хирургической менопаузе в репродуктивном возрасте является ЗГТ. Назначение ЗГТ сразу после операции способствует плавной адаптации организма женщины к условиям остро возникающего дефицита половых стероидов и предупреждению развития других проявлений гормональной недостаточности. Для оценки эффективности ЗГТ при лечении депрессивных нарушений при хирургической менопаузе требуется ее проведение сроком не менее 3 мес. Однако даже адекватная ЗГТ, начатая в ранние периоды после операции, при достаточной для достижения эффектов длительности лечения не решает полностью задачи лечения депрессивных нарушений при этих состояниях. При сохранении/появлении стойких жалоб на подавленное настроение, снижении интересов, ангедонии, снижении активности, идеях малоценности и сохраняющихся соматических симптомах необходимо присоединение антидепрессантов. При использовании современных антидепрессантов выделяют более переносимый профиль побочных эффектов и более широкую границу безопасности при передозировке. Для лечения аффективных расстройств депрессивного спектра при хирургической менопаузе оптимальной является комбинированная терапия. Последовательность назначения ЗГТ и антидепрессантов определяется соотношением соматовегетативных и собственно психических компонентов депрессивного синдрома: первичное назначение ЗГТ с последующим присоединением антидепрессантов оправдано при доминировании соматовегетативных компонентов депрессии; первоначальное проведение курса монотерапии антидепрессантами с последующим присоединением ЗГТ показано при вариантах депрессии, близких к эндогенной структуре. Поскольку для большинства пациенток визит к специалисту-психиатру в связи с депрессивным расстройством, возникшим после перенесенного оперативного вмешательства, является первым обращением, возможно использование минимально достаточных терапевтических доз. Имеющиеся данные литературы о синергическом действии препаратов натуральных эстрогенов и антидепрессантов, влияющих на обмен серотонина, позволяют придерживаться подобной тактики.
Анализ данных, полученных в результате проведенного исследования, позволяет выделить ряд клинических особенностей действия тианептина при лечении депрессивных нарушений в структуре расстройств при хирургической менопаузе. Терапия тианептином не требует отмены проводимой ЗГТ препаратами натуральных эстрогенов. Под влиянием тианептина у больных с депрессивными расстройствами, развивающимися при хирургической менопаузе, происходит гармоничная, равномерная редукция основных депрессивных проявлений, таких как витальные симптомы, моторная и идеаторная заторможенность. Скорость наступления клинического эффекта при применении тианептина достаточно велика. Первые признаки клинического улучшения появляются уже через 10–14 дней приема препарата, а иногда и раньше, в чем он приближается к трициклическим антидепрессантам.
Тианептин продемонстрировал хорошую переносимость у большинства больных. Результаты проведенного исследования позволяют считать обоснованным при рассматриваемых состояниях применение современных антидепрессантов. Выбор конкретного препарата может быть сделан с учетом индивидуальных клинических характеристик состояния пациента. Коаксил может быть рекомендован как препарат выбора при комбинированной терапии указанных расстройств.
В последние годы отмечается рост гинекологических заболеваний, таких как доброкачественные опухоли матки и ее придатков, эндометриоз, требующих радикального оперативного вмешательства, и происходит омоложение контингента оперированных женщин.
Согласно данным литературы, постовариэктомический синдром, при хирургической менопаузе наблюдается у 60–80% женщин. У 70–75% женщин обратное его развитие происходит в течение 1-го года после операции, у 25% пациенток наблюдается тяжелое течение, продолжающееся 2–5 лет и более. Аффективные нарушения разной степени выраженности развиваются у 40–68% женщин с хирургической менопаузой. Своей сложностью проблема аффективных расстройств, возникающих при хирургической менопаузе, обязана большому количеству факторов, ее обусловливающих. Фундаментальные исследования последних лет показали, что разные типы эстрогеновых (альфа и бета), прогестероновых (А и Б) и тестостероновых рецепторов расположены не только в репродуктивных органах-мишенях (матке и молочных железах). Они обнаружены также в центральной нервной системе, клетках костной ткани, эндотелии сосудов, миокардиоцитах, фибробластах, соединительной ткани, урогенитальном тракте, в слизистых оболочках рта, гортани, конъюнктивы, толстом кишечнике. Следовательно, резко возникающий дефицит половых стероидов (прежде всего эстрогенов) способствует системным изменениям в органах и тканях вследствие нарушения гормонального гомеостаза. К последствиям дефицита половых гормонов после билатеральной овариэктомии с гистерэктомией можно отнести ряд симптомов. Наиболее значимыми являются: нейровегетативные симптомы, аффективные расстройства, урогенитальные расстройства, потеря кальция и коллагена из костной ткани (остеопороз), повышение частоты сердечно-сосудистых заболеваний.
Однако при достаточном интересе к этой проблеме специалистов разных специальностей опыт применения современных антидепрессантов, при указанных состояниях невелик, а данные о комбинированной терапии в сочетании с препаратами натуральных эстрогенов практически отсутствует. До настоящего времени не разработаны комплексные подходы с использованием заместительной гормональной терапии (ЗГТ) и психофармакотерапии, отсутствуют общепринятые рекомендации по комплексной терапии депрессивных расстройств, развивающихся при хирургической менопаузе.
Целью исследования явилось изучение эффективности препарата Коаксил (тианептин) при лечении депрессивных нарушений, развивающихся при хирургической менопаузе.
Материалы и методы
Исследование проведено на базе ФГУ Научный центр акушерства, гинекологии и перинатологии им. акад. В.И.Кулакова Федерального агентства по высокотехнологичной медицинской помощи. С помощью скринингового опросника выявлены женщины с признаками аффективных нарушений в возрасте до 50 лет, наблюдающиеся врачами-гинекологами по поводу расстройств, связанных с хирургической менопаузой.
Анализировалась эффективность терапии в двух основных терапевтических группах больных, выделенных на основании критерия последовательности назначения антидепрессантов и ЗГТ.
Последовательность назначения антидепрессантов и ЗГТ определялась с учетом особенностей клинической картины: при преобладании аффективных расстройств первично назначали курс психофармакотерапии, за которым следовал курс ЗГТ (АГ-вариант; n=26), при доминировании соматовегетативных нарушений и наличии показаний для неотложного проведения гормонотерапии в связи с нарастающими признаками гормонодефицита курс ЗГТ предшествовал курсу терапии антидепрессантом (ГА-вариант, n=20).
Для оценки тяжести симптомов депрессии и тревоги, а также динамики состояния пациентов при проведении фармакотерапии использовались шкалы тревоги и депрессии Гамильтона (версия шкалы Гамильтона, состоящая из 17 пунктов – HDRS17).
Для ЗГТ применялись препараты натуральных эстрогенов – 17b-эстрадиола валерат (Эстрофем; 1 мг/сут перорально), эстрадиола гемигидрат (Дивигель; 0,5–1,0 г геля для наружного применения), трансдермальная система эстрадиола (Климара; 0,05 мг/сут). Продолжительность терапии составляла не менее 3 мес. ЗГТ назначалась врачом-гинекологом. Решение вопроса о целесообразности ЗГТ в каждом конкретном случае принималось с учетом не только появившихся симптомов, но и возможности возникновения системных нарушений и имеющихся противопоказаний. Следует отметить, что уровень содержания фолликулостимулирующего гормона (ФСГ) и эстрадиола в крови был сопоставимым в обеих группах и соответствовал уровню гормонов в постменопаузальном периоде – ФСГ 74,8±4,3 МЕ/л (N: 28,0–190 МЕ/л), эстрадиол – 77,1±7,8 пмоль/л (N:12,0–296 пмоль/л). На фоне проведения ЗГТ уровень гормонов достоверно менялся. Такая динамика позволила оценивать влияние психофармакотерапии в обеих описываемых группах без дополнительного учета влияния ЗГТ.
В исследовании применяли препарат Коаксил, представленный в виде таблеток, содержащих 12,5 мг тианептина. Препарат назначали в начальной дозе 25 мг/сут (по 12,5 мг 2 раза в день), в процессе терапии дозу увеличивали до 37,5 мг/сут (по 12,5 мг 3 раза в день).
Основной метод исследования – клинико-терапевтический. При выборе препарата для проведения исследования руководствовались особенностями фармакологических эффектов, в частности наличием наряду с антидепрессивным анксиолитического и рединамизирующего эффекта при отсутствии седативных свойств и отрицательного влияния на когнитивные процессы, а также адаптогенных эффектов за счет способности понижать реактивность гипоталамо-гипофизарно-надпочечниковой системы в ответ на стресс. Задачей исследования также являлась оценка возможности сочетания действие антидепрессанта с ЗГТ. Для этого был необходим препарат с незначительным числом нежелательных побочных соматотропных эффектов.
Результаты исследования
Отобрано 50 пациенток с клиническими признаками депрессивного расстройства легкой, умеренной степени тяжести. Средний возраст составил 43,8±3,5 года. В конечную группу анализа вошли 46 пациенток, 2 пациентки после проведения ЗГТ отказались от лечения антидепрессантами, 2 прекратили участие в исследовании из-за побочных эффектов.
В исследование были включены случаи, соответствовавшие следующим диагностическим рубрикам по классификации МКБ-10:
• легкий депрессивный эпизод F32.0 (n=8);При оценке состояния пациенток по HDRS в 1-й группе (вариант терапии АГ) уровень депрессии составил 21±6 баллов, а психическая и соматическая тревога имели одинаковое значение – 13±8 баллов. На фоне терапии тианептином отмечалось непрерывное и достоверное (р<0,01) снижение суммарного балла как по шкале депрессии, так и по шкале тревоги с 1-го месяца терапии до окончания курса терапии (D90). Снижение выраженности соматической составляющей тревоги по шкале HARS несколько отставало от психической, на 8-й неделе терапии (D56) показатели психической и соматической тревоги выравнивались и имели клинически незначимые различия. На 12-й неделе терапии (D90) уровень тревоги значительно снижался.
• умеренный депрессивный эпизод F32,1 (n=19);
• рекуррентное депрессивное расстройство, текущий эпизод легкой степени выраженности F33,0 (n=5);
• рекуррентное депрессивное расстройство, текущий эпизод умеренной степени выраженности F33,1(n=9);
• дистимия F34 (n=5).
У пациенток 2-й группы выраженность собственно аффективных нарушений была менее значительной, на первое место в клинической картине этих состояний выходили соматовегетативные проявления (приливы, сердцебиения, озноб, жар, потливость, головные боли) как наиболее дезадаптирующие, в то же время отчасти маскирующие всю остальную психопатологическую симптоматику. У пациенток этой группы в процессе гормональной терапии эстрогенами частично редуцировались соматовегетативные проявления, выравнивался общий фон настроения, улучшался сон, повышалась работоспособность.
По HDRS уровень депрессии в среднем составил 17±4 балла, а уровень психической и соматической тревоги – 9 и 10 баллов соответственно.
При сравнении показателей шкалы депрессии HDRS, соматических и психических компонентов тревоги HARS у больных обеих групп установлено следующее. В 1-й группе (АГ) показатель HDRS был достоверно выше. Значение психического компонента тревоги преобладало над уровнем соматической тревоги у больных 1-й группы, а соматической тревоги над психической – во 2-й группе (ГА).

Подтверждением эффективности проведенной терапии служит прогрессирующая редукция средних значений шкал депрессии Гамильтона (см. рисунок). Динамика показателей HDRS свидетельствует о статистически достоверном снижении выраженности депрессивной симптоматики в процессе лечения. На основе показателей редукции суммарного рейтинга баллов шкалы Гамильтона к окончанию курса терапии в общей группе больных, получавших тианептин, были выделены группа респондеров – 38 человек и нонреспондеров – 8 человек. В 1-й группе были 24 респондера и 2 нонреспондера, во 2-й – 14 респондеров и 6 нонреспондеров.
В группу респондеров были включены пациенты, у которых редукция суммарного рейтинга баллов по шкале Гамильтона составила 50% и более.
Психопатологическая симптоматика в большинстве случаев в группе респондеров носила тревожно-тоскливый характер с моторной и идеаторной заторможенностью, витальным ощущением тоски, периодической безотчетной тревогой, суточными колебаниями аффекта с улучшением к вечеру, снижением аппетита, нарушениями сна и ранними пробуждениями, сверхценными идеями бесперспективности, виновности, ненужности, брошенности. Идеаторный компонент был выражен менее отчетливо. Наблюдались ипохондрические симптомы с фиксацией на состоянии своего здоровья, выраженными соматовегетативными расстройствами по типу приливов, несмотря на массивность и представленность собственно психопатологической симптоматики.
В группу нонреспондеров вошли 8 пациенток, у которых редукция рейтинга баллов по шкале Гамильтона составила менее 50% от исходного уровня. Клинико-анамнестические характеристики этой группы отличались от таковых группы респондеров. Имелись четкие указания на перенесенные ранее аффективные нарушения, при этом 3 пациентки получали терапию амитриптилином и леривоном.
В клинической картине у пациенток этой группы наряду с умеренно сниженным настроением доминировали проявления тревоги, часто ситуационной, связанной с беспокойством за себя и близких, ангедонические жалобы, чувство апатии, утрата “жизненного тонуса”, астения.
В исследовании отмечалась хорошая переносимость препаратов, незначительное количество побочных эффектов. Пациенты предъявляли ряд жалоб (тианептин: тошнота, чувство слабости, сухость во рту, головные боли, парестезии).
Обсуждение
В последние годы отмечается рост гинекологических заболеваний, таких как доброкачественные опухоли матки и ее придатков, эндометриоз, требующих радикального оперативного вмешательства, и происходит омоложение контингента оперированных женщин.
Согласно данным литературы, постовариэктомический синдром, при хирургической менопаузе наблюдается у 60–80% женщин. У 70–75% женщин обратное его развитие происходит в течение 1-го года после операции, у 25% пациенток наблюдается тяжелое течение, продолжающееся 2–5 лет и более. Аффективные нарушения разной степени выраженности развиваются у 40–68% женщин с хирургической менопаузой. Своей сложностью проблема аффективных расстройств, возникающих при хирургической менопаузе, обязана большому количеству факторов, ее обусловливающих.
Проблема расстройств депрессивного спектра, развивающихся при хирургической менопаузе, становится все более актуальной в связи с увеличением числа пациенток, перенесших овариэктомию с тотальной или субтотальной резекцией матки. Патогенетически обоснованной для лечения пациенток при хирургической менопаузе в репродуктивном возрасте является ЗГТ. Назначение ЗГТ сразу после операции способствует плавной адаптации организма женщины к условиям остро возникающего дефицита половых стероидов и предупреждению развития других проявлений гормональной недостаточности. Для оценки эффективности ЗГТ при лечении депрессивных нарушений при хирургической менопаузе требуется ее проведение сроком не менее 3 мес. Однако даже адекватная ЗГТ, начатая в ранние периоды после операции, при достаточной для достижения эффектов длительности лечения не решает полностью задачи лечения депрессивных нарушений при этих состояниях. При сохранении/появлении стойких жалоб на подавленное настроение, снижении интересов, ангедонии, снижении активности, идеях малоценности и сохраняющихся соматических симптомах необходимо присоединение антидепрессантов. При использовании современных антидепрессантов выделяют более переносимый профиль побочных эффектов и более широкую границу безопасности при передозировке. Для лечения аффективных расстройств депрессивного спектра при хирургической менопаузе оптимальной является комбинированная терапия. Последовательность назначения ЗГТ и антидепрессантов определяется соотношением соматовегетативных и собственно психических компонентов депрессивного синдрома: первичное назначение ЗГТ с последующим присоединением антидепрессантов оправдано при доминировании соматовегетативных компонентов депрессии; первоначальное проведение курса монотерапии антидепрессантами с последующим присоединением ЗГТ показано при вариантах депрессии, близких к эндогенной структуре. Поскольку для большинства пациенток визит к специалисту-психиатру в связи с депрессивным расстройством, возникшим после перенесенного оперативного вмешательства, является первым обращением, возможно использование минимально достаточных терапевтических доз. Имеющиеся данные литературы о синергическом действии препаратов натуральных эстрогенов и антидепрессантов, влияющих на обмен серотонина, позволяют придерживаться подобной тактики.
Анализ данных, полученных в результате проведенного исследования, позволяет выделить ряд клинических особенностей действия тианептина при лечении депрессивных нарушений в структуре расстройств при хирургической менопаузе. Терапия тианептином не требует отмены проводимой ЗГТ препаратами натуральных эстрогенов. Под влиянием тианептина у больных с депрессивными расстройствами, развивающимися при хирургической менопаузе, происходит гармоничная, равномерная редукция основных депрессивных проявлений, таких как витальные симптомы, моторная и идеаторная заторможенность. Скорость наступления клинического эффекта при применении тианептина достаточно велика. Первые признаки клинического улучшения появляются уже через 10–14 дней приема препарата, а иногда и раньше, в чем он приближается к трициклическим антидепрессантам.
Тианептин продемонстрировал хорошую переносимость у большинства больных. Результаты проведенного исследования позволяют считать обоснованным при рассматриваемых состояниях применение современных антидепрессантов. Выбор конкретного препарата может быть сделан с учетом индивидуальных клинических характеристик состояния пациента. Коаксил может быть рекомендован как препарат выбора при комбинированной терапии указанных расстройств.
Список исп. литературыСкрыть список1. Мосолов С.Н. Клиническое применение современных антидепрессантов. СПб., 1995.
2. Сметник В.П. Медицина климактерия. Ярославль: ООО “Издательство Литера”, 2006.
3. Смулевич А.Б. Депрессия при соматических и психических заболеваниях. М.: ООО “Медицинское информационное агентство”, 2003.
4. Archer JS. Depression, estrogen and neurotransmitters in the menopausal woman. The millennium review. Ed J Studd. 2000: 127–39.
5. Ballinger CB. Psychiatric aspects of the menopause. Br J Psychiatry 1990; 156: 773–87.
6. Benazzi F. Female depression before and after menopause. Psychother Psychosom 2000; 69 (5): 280–3.


