Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№05 2009
К проблеме антидепрессантов «первого выбора» при терапии депрессивного расстройства №05 2009
Номера страниц в выпуске:6-8
Вопрос обоснованного выбора терапевтических воздействий – один из самых важных в современной клинической психиатрии. Дифференцированный подход к выбору антидепрессанта являлся актуальной проблемой с появления первых препаратов с тимоаналептической активностью (трициклических антидепрессантов и ингибиторов моноаминоксидазы) и остается таковой в настоящее время. Важность этого вопроса определяется в первую очередь ограниченной эффективностью любых антидепрессантов у больных депрессией. Имеются данные о том, что только у одного из трех пациентов удается достичь полной ремиссии, 30–45% больных имеют частичное улучшение при использовании оценки 50% редукции имеющейся депрессивной симптоматики (Depression Guideline Panel. Depression in Primary Care, 1993). Исследования последних лет также показали, что у многих больных депрессией, даже при полученном в процессе лечения снижении рейтинга баллов по шкале депрессии Гамильтона на 50%, не удается добиться полноценного восстановления психической деятельности. В этих случаях остаточные состояния нередко включают проявления из числа основных синдромообразующих компонентов депрессии (D.Healey, H.Healey, 1998; R.Hirschfeld и соавт., 2000; E.Paykel и соавт., 1995; A.Nierenberg, 2002). В качестве вероятного объяснения обнаруженного психопатологического феномена, который касается утраты депрессией своего основного качества – признака дискретности, – рассматриваются две группы причин. Первая из них отражает сложность патогенеза этого заболевания и участие в нем наряду с собственно биологической составляющей большого числа личностно-обусловленных и психосоциальных факторов. Вторая группа причин связана с формированием так называемой фармакогенной недостаточности (N.Petrilowitch, 1969) при проведении лекарственной антидепрессивной терапии. Настоящая публикация направлена на рассмотрение возможностей, которыми обладают антидепрессанты селективного действия (одно- и двухмодальные) для преодоления причин, вошедших во вторую из приведенных групп причин. За последнее десятилетие число этих средств на отечественном рынке антидепрессантов существенно увеличилось, что подтверждают данные табл. 1.

Именно поэтому необходимым является разработка обоснованного подхода для выбора антидепрессанта в конкретной клинической ситуации.
Традиционно для отечественной психиатрии выбор тимоаналептической терапии основывается на нозологическом и синдромальном диагнозе депрессии и выраженности ее симптоматики (С.Н.Мосолов, 1995). Однако в настоящее время приоритет часто отдается другому подходу, который предусматривает определение антидепрессантов «первого выбора» для лечения депрессии. Основные критерии, которые предъявляются к антидепрессанту как препарату «первого выбора», представлены в табл. 2.
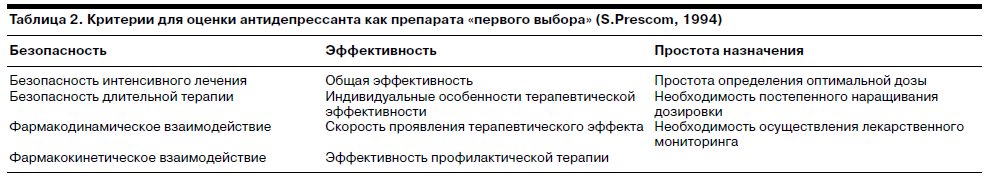
В табл. 2 приведены основные критерии, выделенные в работе S.Prescom (1994 г.), на основании которых проводится оценка антидепрессанта как препарата «первого выбора» в терапии депрессий. Учитывая эти критерии, рассмотрим, насколько им соответствуют препараты, наиболее часто использующиеся в практике.
Селективные ингибиторы обратного захвата серотонина (СИОЗС) в большинстве современных рекомендаций и алгоритмов терапии депрессии рассматриваются в качестве препаратов первого выбора (Lieberman, Golden, Stroup, & McEvoy, 2000; Peretti и соавт., 2000; А.Б.Смулевич, 2003). Основанием для такой оценки этой группы препаратов послужили следующие данные:
Однако для выбора препарата эффективность его применения не менее важна, чем переносимость. Согласно результатам исследований эффективность СИОЗС сравнима с эффективностью ТЦА только при терапии депрессий легкой и средней тяжести (Г.Э.Мазо, 1996; А.П.Музыченко, А.Н.Богдан, 1999; Н.А.Корнетов и соавт., 2001; M.Anderson, 2000). Данные метаанализа также свидетельствуют о том, что у пациентов с тяжелой депрессивной симптоматикой лучшие результаты получены при использовании традиционных антидепрессантов (влияющих как на серотониновую, так и адреналиновую трансмиссию), чем при использовании препаратов с селективной активностью (I.Anderson, B.Tomenson, 1994). Поэтому при рассмотрении антидепрессантов первого выбора интерес представляют препараты двойного действия, которые являются селективными ингибиторами обратного захвата норадреналина и серотонина (СИОЗСН). Тем самым по профилю фармакологической активности, который включает главным образом воздействие на структуры синапсов из двух приведенных нейромедиаторных систем, эти средства напоминают ТЦА. Однако широта спектра антидепрессивных воздействий, как (а может быть даже в большей мере) и показатели безопасности терапии этими препаратами, дают основания считать такое сопоставление этих групп антидепрессантов весьма условным. Для применения в отечественной врачебной практике зарегистрированы три антидепрессанта из группы СИОЗСН: венлафаксин, милнаципран и дулоксетин.
Согласно данным, приведенным в Национальном руководстве по психиатрии (М.В.Иванов, Н.Г.Незнанов, 2009) и аналогичных зарубежных изданиях (B.Sadock, V.Sadock, G.Kaplan, 2005), препараты из группы СИОЗСН различаются по характеру вовлеченности серотонинергической и норадреналинергической систем в механизм их действия. Венлафаксин в низких дозах (75–100 мг/сут) выступает как СИОЗС. При увеличении его дозы до 150 мг/сут и выше присоединяется воздействие на обратный захват норадреналина. Наконец, применение высоких доз препарата сопровождается также дополнительным влиянием на обратный захват допамина. Поэтому венлафаксин можно расценить как антидепрессант тройного действия. Однако по влиянию на серотониновую трансмиссию венлафаксин уступает сертралину. Выраженное воздействие на обмен норадреналина определяет менее благоприятный профиль переносимости венлафаксина по сравнению с СИОЗС (C.Nemeroff и соавт., 2003).
Милнаципран имеет более мощное влияние на норадреналиновую трансмиссию, чем на серотониновую. В минимальных дозах (50 мг/сут) милнаципран работает как селективный ингибитор обратного захвата норадреналина, но при повышении дозы присоединяется серотонинергический эффект. Как и остальные СИОЗСН, милнаципран не имеет сродства к м-холинорецепторам, a-адренорецепторам или гистаминовым Н1-рецепторам. По профилю побочных эффектов милнаципран близок к СИОЗС, но чаще регистрируются такие побочные эффекты, как головокружение, повышенное потоотделение и уринальные дисфункции.
Препарат дулоксетин (Симбалта), представитель антидепрессантов этой группы, заслуживает особого внимания. Это объясняется многократными подтверждениями того, что он обладает наиболее сбалансированным механизмом действия, которое проявляется в сопоставимо равном подавлении обратного захвата серотонина и допамина уже при использовании минимальной дозы (40 мг/сут) – в России есть дозировка 30 и 60 мг. К дополнительным преимуществам дулоксетина относится его способность воздействовать на соматические симптомы депрессии, включая состояния неполной ремиссии, в которых проявления соматического компонента являются стержневым феноменом. Вероятно, как тем, так и другим объясняется широкий круг проведенных к настоящему времени клинических исследований дулоксетина.
В работах, в которых эффективность дулоксетина для купирования депрессивных расстройств сравнивалась с плацебо, выявлено его превосходство по показателям антидепрессивной активности при меньшей частоте выявления нежелательных событий по сравнению с плацебо (D.Goldstein и соавт., 2002; M.Detke и соавт., 2002). Кроме того, отмечено, что использование дулоксетина в дозах от 40 до 120 мг/сут приводило к статистически значимой редукции депрессивной симптоматики уже по истечении 1-й недели терапии. Также установлена большая эффективность дулоксетина на этапе купирующей терапии депрессий по сравнению с антидепрессивными эффектами препаратов других групп.
Наряду с изучением эффективности дулоксетина при купировании депрессий к настоящему времени проведены исследования, касающиеся целесообразности его использования для профилактической терапии аффективных расстройств. J.Raskin и соавт. (2002 г.) представили результаты открытого многоцентрового исследования, в рамках которого изучали эффективность и безопасность дулоксетина в условиях длительной терапии (до 52 нед). В этой работе показано статистически достоверное улучшение главного дополнительного показателя эффективности через 6, 28 и 52 нед терапии (n=1279). По завершении 52 нед лечения балл по CGI-S от исходного 4,6 снизился до 1,6, а балл HAMD-17 уменьшился до 5,0 (исходно 22,5). Доля респондеров составила 89,1%, показатель частоты ремиссий – 81,8%.
Отдельного внимания заслуживают результаты, полученные при изучении анальгетического компонента антидепрессивного эффекта дулоксетина и его более широкого воздействия на соматическую сферу депрессии. В работе L.DeLoach и соавт. (1998 г.) для оценки динамики болевого синдрома использовали визуальную аналоговую шкалу – ВАШ (Visual analog scale). Дизайн исследования предполагал исключение приема анальгетиков из терапии для депрессивных больных для повышения достоверности измерений. На фоне лечения отмечено статистически достоверное улучшение всех показателей по ВАШ, кроме головной боли. Согласно данным, полученным к окончанию исследования, дулоксетин достоверно превосходил плацебо по степени редукции боли в спине (p<0,001) и общего показателя боли (p=0,019).
В отношении безопасности применения дулоксетина установлены следующие данные. При сравнении с плацебо терапия дулоксетином достоверно чаще сопровождается такими явлениями, как тошнота, сухость во рту, инсомния и астения (P.Norton и соавт., 2002; D.Goldstein и соавт., 2002). Вместе с тем развитие этих побочных эффектов, как правило, наблюдается в первые дни терапии (примерно у 40% больных) с последующей редукцией большинства из них до уровня плацебо к концу 1-й недели лечения. Такие изменения в их выраженности, по-видимому, связаны с адаптацией рецепторов к действию препарата.
Нежелательные явления со стороны половой функции оценивали с помощью Аризонской шкалы сексуального опыта (arizona sexual experience scale). Достоверных различий между дулоксетином и плацебо по показателям этой шкалы не обнаружено (D.Goldstein и соавт., 2002). В ходе длительного открытого исследования отмена терапии из-за побочных эффектов со стороны половой функции потребовалась у 0,4% (n=6) пациентов (J.Raskin и соавт., 2002). В другом исследовании S.K.Brannan и соавт. (2003 г.), в котором также использовали шкалу ASEX, не получено убедительных данных о наличии у дулоксетина. На фоне приема дулоксетина у женщин, не страдающих изначально сексуальной дисфункцией, каких-либо изменений по сравнению с плацебо не выявлено. В свою очередь у мужчин, изначально не страдающих сексуальной дисфункцией, отмечено ухудшение (по сравнению с плацебо) только по двум показателям – по легкости достижения и удовлетворенности оргазмом.
Как отмечено выше, ТЦА и СИОЗС как средства, влияющие на обмен серотонина, часто вызывают нарушения функций сердечно-сосудистой системы. Поэтому в исследованиях дулоксетина при терапии депрессии оценивали влияние этого препарата на исходные показатели артериального давления (АД) и частоты сердечных сокращений (ЧСС). Установлено, что дулоксетин не провоцировал манифестации артериальной гипертензии (M.Detke и соавт., 2002). При оценке безопасности применения этого препарата на отдаленных (более 1 года) этапах статистически значимых изменений в показателях АД и ЧСС не получено (А.Sharma и соавт., 2000; D.Goldstein и соавт., 2002).
Заключение
Наличие широкого арсенала антидепрессантов разных фармакологических групп, используемых в современной клинической практике, создает для практикующего врача ситуацию, в которой требуется принять решение, каким критериям следует отдать предпочтение при выборе конкретного препарата. Выбор антидепрессантов из группы СИОЗС как средств, имеющих достаточно высокий уровень безопасности, облегчает достижение комплаенса пациентом, но, к сожалению, не может обеспечить в ряде случаев достижение столь же надежных результатов лечения в отношении его эффективности. Напротив, при использовании наиболее мощных тимоаналептиков, таких как ТЦА, наряду с высокой эффективностью терапии при разной выраженности депрессий, включая ее психотические формы, вероятность развития побочных эффектов значимо выше. Поэтому, согласно приведенным выше данным, препараты из группы СИОЗСН, в частности дулоксетин (Симбалта), обладающий сбалансированным действием на обе нейромедиаторные системы (сертониновую и норадреналиновую), с учетом выраженности антидепрессивного эффекта, быстроты его наступления, а также безопасности воздействия, могут в настоящее время рассматриваться как антидепрессанты «первого выбора» в терапии депрессии различной степени тяжести, в том числе при шизофрении.
Вместе с тем, говоря о проблеме выбора, необходимо еще раз отметить известную условность термина «препарат первого выбора», поскольку врачебный опыт позволяет ориентироваться не только в пределах уровней вмешательства, но и оперировать категорией медицинских показаний.

Именно поэтому необходимым является разработка обоснованного подхода для выбора антидепрессанта в конкретной клинической ситуации.
Традиционно для отечественной психиатрии выбор тимоаналептической терапии основывается на нозологическом и синдромальном диагнозе депрессии и выраженности ее симптоматики (С.Н.Мосолов, 1995). Однако в настоящее время приоритет часто отдается другому подходу, который предусматривает определение антидепрессантов «первого выбора» для лечения депрессии. Основные критерии, которые предъявляются к антидепрессанту как препарату «первого выбора», представлены в табл. 2.

В табл. 2 приведены основные критерии, выделенные в работе S.Prescom (1994 г.), на основании которых проводится оценка антидепрессанта как препарата «первого выбора» в терапии депрессий. Учитывая эти критерии, рассмотрим, насколько им соответствуют препараты, наиболее часто использующиеся в практике.
Селективные ингибиторы обратного захвата серотонина (СИОЗС) в большинстве современных рекомендаций и алгоритмов терапии депрессии рассматриваются в качестве препаратов первого выбора (Lieberman, Golden, Stroup, & McEvoy, 2000; Peretti и соавт., 2000; А.Б.Смулевич, 2003). Основанием для такой оценки этой группы препаратов послужили следующие данные:
• антидепрессанты практически всех классов, использующиеся в современной клинической практике, имеют примерно одинаковую максимальную эффективность, составляющую 70–80% у больных депрессией (А.С.Аведисова, 2000; P.Cowen, 1998). Некоторые исследователи связывают этот факт с существованием естественного лимита эффективности тимоаналептических средств;
• СИОЗС имеют убедительное преимущество перед ТЦА в отношении переносимости препаратов и безопасности их применения (Г.Э.Мазо, 1996, 2001; M.Keller и соавт., 1998; R.Hirschfeld, 1998; J.Edwards, I.Anderson, 1999; G.Sullivan, 1999; R.Entsuah и соавт., 2001).Именно последнее из этих положений стало решающим для рассмотрения СИОЗС в качестве препаратов “первого выбора” для терапии депрессии. Важность вопросов переносимости и безопасности применения антидепрессантов не вызывает сомнений. Действительно, этот фактор существенно влияет на качество жизни и социальное функционирование пациентов, позволяет избежать сопутствующих соматических проблем, которые могут определять и комплаенс. Переносимость препаратов – важная составляющая и результативности лечения, так как невозможность назначения адекватных доз антидепрессантов ведет к формированию отрицательной резистентности (В.Д.Вид, 1993).
Однако для выбора препарата эффективность его применения не менее важна, чем переносимость. Согласно результатам исследований эффективность СИОЗС сравнима с эффективностью ТЦА только при терапии депрессий легкой и средней тяжести (Г.Э.Мазо, 1996; А.П.Музыченко, А.Н.Богдан, 1999; Н.А.Корнетов и соавт., 2001; M.Anderson, 2000). Данные метаанализа также свидетельствуют о том, что у пациентов с тяжелой депрессивной симптоматикой лучшие результаты получены при использовании традиционных антидепрессантов (влияющих как на серотониновую, так и адреналиновую трансмиссию), чем при использовании препаратов с селективной активностью (I.Anderson, B.Tomenson, 1994). Поэтому при рассмотрении антидепрессантов первого выбора интерес представляют препараты двойного действия, которые являются селективными ингибиторами обратного захвата норадреналина и серотонина (СИОЗСН). Тем самым по профилю фармакологической активности, который включает главным образом воздействие на структуры синапсов из двух приведенных нейромедиаторных систем, эти средства напоминают ТЦА. Однако широта спектра антидепрессивных воздействий, как (а может быть даже в большей мере) и показатели безопасности терапии этими препаратами, дают основания считать такое сопоставление этих групп антидепрессантов весьма условным. Для применения в отечественной врачебной практике зарегистрированы три антидепрессанта из группы СИОЗСН: венлафаксин, милнаципран и дулоксетин.
Согласно данным, приведенным в Национальном руководстве по психиатрии (М.В.Иванов, Н.Г.Незнанов, 2009) и аналогичных зарубежных изданиях (B.Sadock, V.Sadock, G.Kaplan, 2005), препараты из группы СИОЗСН различаются по характеру вовлеченности серотонинергической и норадреналинергической систем в механизм их действия. Венлафаксин в низких дозах (75–100 мг/сут) выступает как СИОЗС. При увеличении его дозы до 150 мг/сут и выше присоединяется воздействие на обратный захват норадреналина. Наконец, применение высоких доз препарата сопровождается также дополнительным влиянием на обратный захват допамина. Поэтому венлафаксин можно расценить как антидепрессант тройного действия. Однако по влиянию на серотониновую трансмиссию венлафаксин уступает сертралину. Выраженное воздействие на обмен норадреналина определяет менее благоприятный профиль переносимости венлафаксина по сравнению с СИОЗС (C.Nemeroff и соавт., 2003).
Милнаципран имеет более мощное влияние на норадреналиновую трансмиссию, чем на серотониновую. В минимальных дозах (50 мг/сут) милнаципран работает как селективный ингибитор обратного захвата норадреналина, но при повышении дозы присоединяется серотонинергический эффект. Как и остальные СИОЗСН, милнаципран не имеет сродства к м-холинорецепторам, a-адренорецепторам или гистаминовым Н1-рецепторам. По профилю побочных эффектов милнаципран близок к СИОЗС, но чаще регистрируются такие побочные эффекты, как головокружение, повышенное потоотделение и уринальные дисфункции.
Препарат дулоксетин (Симбалта), представитель антидепрессантов этой группы, заслуживает особого внимания. Это объясняется многократными подтверждениями того, что он обладает наиболее сбалансированным механизмом действия, которое проявляется в сопоставимо равном подавлении обратного захвата серотонина и допамина уже при использовании минимальной дозы (40 мг/сут) – в России есть дозировка 30 и 60 мг. К дополнительным преимуществам дулоксетина относится его способность воздействовать на соматические симптомы депрессии, включая состояния неполной ремиссии, в которых проявления соматического компонента являются стержневым феноменом. Вероятно, как тем, так и другим объясняется широкий круг проведенных к настоящему времени клинических исследований дулоксетина.
В работах, в которых эффективность дулоксетина для купирования депрессивных расстройств сравнивалась с плацебо, выявлено его превосходство по показателям антидепрессивной активности при меньшей частоте выявления нежелательных событий по сравнению с плацебо (D.Goldstein и соавт., 2002; M.Detke и соавт., 2002). Кроме того, отмечено, что использование дулоксетина в дозах от 40 до 120 мг/сут приводило к статистически значимой редукции депрессивной симптоматики уже по истечении 1-й недели терапии. Также установлена большая эффективность дулоксетина на этапе купирующей терапии депрессий по сравнению с антидепрессивными эффектами препаратов других групп.
Наряду с изучением эффективности дулоксетина при купировании депрессий к настоящему времени проведены исследования, касающиеся целесообразности его использования для профилактической терапии аффективных расстройств. J.Raskin и соавт. (2002 г.) представили результаты открытого многоцентрового исследования, в рамках которого изучали эффективность и безопасность дулоксетина в условиях длительной терапии (до 52 нед). В этой работе показано статистически достоверное улучшение главного дополнительного показателя эффективности через 6, 28 и 52 нед терапии (n=1279). По завершении 52 нед лечения балл по CGI-S от исходного 4,6 снизился до 1,6, а балл HAMD-17 уменьшился до 5,0 (исходно 22,5). Доля респондеров составила 89,1%, показатель частоты ремиссий – 81,8%.
Отдельного внимания заслуживают результаты, полученные при изучении анальгетического компонента антидепрессивного эффекта дулоксетина и его более широкого воздействия на соматическую сферу депрессии. В работе L.DeLoach и соавт. (1998 г.) для оценки динамики болевого синдрома использовали визуальную аналоговую шкалу – ВАШ (Visual analog scale). Дизайн исследования предполагал исключение приема анальгетиков из терапии для депрессивных больных для повышения достоверности измерений. На фоне лечения отмечено статистически достоверное улучшение всех показателей по ВАШ, кроме головной боли. Согласно данным, полученным к окончанию исследования, дулоксетин достоверно превосходил плацебо по степени редукции боли в спине (p<0,001) и общего показателя боли (p=0,019).
В отношении безопасности применения дулоксетина установлены следующие данные. При сравнении с плацебо терапия дулоксетином достоверно чаще сопровождается такими явлениями, как тошнота, сухость во рту, инсомния и астения (P.Norton и соавт., 2002; D.Goldstein и соавт., 2002). Вместе с тем развитие этих побочных эффектов, как правило, наблюдается в первые дни терапии (примерно у 40% больных) с последующей редукцией большинства из них до уровня плацебо к концу 1-й недели лечения. Такие изменения в их выраженности, по-видимому, связаны с адаптацией рецепторов к действию препарата.
Нежелательные явления со стороны половой функции оценивали с помощью Аризонской шкалы сексуального опыта (arizona sexual experience scale). Достоверных различий между дулоксетином и плацебо по показателям этой шкалы не обнаружено (D.Goldstein и соавт., 2002). В ходе длительного открытого исследования отмена терапии из-за побочных эффектов со стороны половой функции потребовалась у 0,4% (n=6) пациентов (J.Raskin и соавт., 2002). В другом исследовании S.K.Brannan и соавт. (2003 г.), в котором также использовали шкалу ASEX, не получено убедительных данных о наличии у дулоксетина. На фоне приема дулоксетина у женщин, не страдающих изначально сексуальной дисфункцией, каких-либо изменений по сравнению с плацебо не выявлено. В свою очередь у мужчин, изначально не страдающих сексуальной дисфункцией, отмечено ухудшение (по сравнению с плацебо) только по двум показателям – по легкости достижения и удовлетворенности оргазмом.
Как отмечено выше, ТЦА и СИОЗС как средства, влияющие на обмен серотонина, часто вызывают нарушения функций сердечно-сосудистой системы. Поэтому в исследованиях дулоксетина при терапии депрессии оценивали влияние этого препарата на исходные показатели артериального давления (АД) и частоты сердечных сокращений (ЧСС). Установлено, что дулоксетин не провоцировал манифестации артериальной гипертензии (M.Detke и соавт., 2002). При оценке безопасности применения этого препарата на отдаленных (более 1 года) этапах статистически значимых изменений в показателях АД и ЧСС не получено (А.Sharma и соавт., 2000; D.Goldstein и соавт., 2002).
Заключение
Наличие широкого арсенала антидепрессантов разных фармакологических групп, используемых в современной клинической практике, создает для практикующего врача ситуацию, в которой требуется принять решение, каким критериям следует отдать предпочтение при выборе конкретного препарата. Выбор антидепрессантов из группы СИОЗС как средств, имеющих достаточно высокий уровень безопасности, облегчает достижение комплаенса пациентом, но, к сожалению, не может обеспечить в ряде случаев достижение столь же надежных результатов лечения в отношении его эффективности. Напротив, при использовании наиболее мощных тимоаналептиков, таких как ТЦА, наряду с высокой эффективностью терапии при разной выраженности депрессий, включая ее психотические формы, вероятность развития побочных эффектов значимо выше. Поэтому, согласно приведенным выше данным, препараты из группы СИОЗСН, в частности дулоксетин (Симбалта), обладающий сбалансированным действием на обе нейромедиаторные системы (сертониновую и норадреналиновую), с учетом выраженности антидепрессивного эффекта, быстроты его наступления, а также безопасности воздействия, могут в настоящее время рассматриваться как антидепрессанты «первого выбора» в терапии депрессии различной степени тяжести, в том числе при шизофрении.
Вместе с тем, говоря о проблеме выбора, необходимо еще раз отметить известную условность термина «препарат первого выбора», поскольку врачебный опыт позволяет ориентироваться не только в пределах уровней вмешательства, но и оперировать категорией медицинских показаний.
Список исп. литературыСкрыть список1. Аведисова А.С. Лимит эффективности антидепрессантов. XIII съезд психиатров России: Материалы съезда. М., 2000; с. 171.
2. Вид В.Д. Психоаналитическая психотерапия при шизофрении. СПб., 1993.
3. Иванов М.В., Незнанов Н.Г. Психофармакологическая терапия. Психиатрия: национальное руководство. Под ред. Т.Б.Дмитриевой, В.Н.Краснова, Н.Г.Незнанова и др. М.: ГЭОТАР-Медиа, 2009; с. 759–820.
4. Мазо Г.Э. Лечение депрессивных состояний серотонинергическими антидепрессантами (психофармакологические и психотерапевтические аспекты). Автореф. диc. … канд. мед. наук. СПб., 1996.
5. Мосолов С.Н. Клиническое применение современных антидепрессантов. СПб.: Медицинское информационное агентство, 1995.
6. Музыченко А.П., Богдан А.Н. Комбинированное применение антидепрессантов с избирательным обратным захватом серотонина в амбулаторной практике. Рос. псих. журн. М., 1999; 1: 27–31.
7. Корнетов Н.А., Счастный Е.Д., Корнетов А.Н. Эффективность терапии депрессивных расстройств циталопрамом. Псих. и психофармакотер. 2001; 3 (4): 132–5.
8. Смулевич А.Б. Депрессия при соматических и психических заболеваниях. М.: ООО "Медицинское информационное агентство", 2003.
9. Anderson M. Selective serotonin reuptake inhibitors versus tricyclic antidepressants: a meta – analysis efficacy and tolerability. J Affect Disord 2000; 58: 19–36.
10. Anderson I, Tomenson B. A meta analysis if the efficacy of serotonin reuptake inhibitors compared to tricyclic antidepressants in depression. Neuropsychopharmacology 1994; 10 (suppl.): 106.
11. Depression Guideline Panel. Depression in Primary Care. Detect Diagnosis 1993; p. 47.
12. Cowen PJ. Pharmacological management of treatment-resistant depression. Adv Psychiatr Treat 1998; 4: 320–7.
13. Edwards JG, Anderson I. Systematic review and guide to selection of selective serotonin reuptake inhibitors. Drugs 1999; 57: 507–33.
14. Entsuah R, Huang H, Thase M. Response and Remission Rates in Different Subpopulations With Major Depressive Disorder Administered Venlafaxine, Selective Serotonin Reuptake Inhibitors, or Placebo. J Clin Psychiatry 2001; 62: 869–77.
15. Healey D, Healey H. The clinical pharmacologic profile of reboxetine: does it involve the putative neurobiological substrates of well being? J Affect Disord 1998; 51: 313–22.
16. Hirschfeld RM, Russell JM et al. Predictors of Response to Acute Treatment of Chronic and Double Depression with Sertraline or Imipramine. J Clin Psychiatry 1998; 59: 669–75.
17. Hirschfeld RM, Montgomery SA, Keller MB et al. Social functioning in depression: a review. J Clin Psychiatry 2000; 61: 268–75.
18. Keller MB, Gelenberg AJ et al. A Double-Blind, Randomized Trial of Sertraline and Imipramine. J Clin Psychiatry 1998; 59: 598–607.
19. Nierenberg A. A review of treatment-resistant depression. Program and abstracts of the XII World Congress of Psychiatry; August 24–29, 2002; Yokohama, Japan. Symposium SS-1; 183–5.
20. Parker G. Classifying depression: should paradigms lost be regained? Am J Psychiatry 2000; 157: 1195–203.
21. Paykel ES, Ramana R, Cooper Z et al. Residual symptoms after partial remission: an important outcome in depression. Psychol Med 1995; 25: 1171–80.
22. Prescom S. Antidepressant drug selection – criteria and options. J Clin Psychiatry 1994; 55 (suppl. 9A): 6–22.
23. Sadock BJ, Sadock VA, Kaplan GI. Sadock`s comprehensive textbook of psychiatry (2 Volume Set), 8th ed. Lippincott Williams & Wilkins Publishers: Philadelphia et al. 2005; 1: 1–2054; 2: 2055–4064.
24. Sullivan GM, Coplan JD, Kent JM et al. The noradrenergic system in pathological anxiety: a focus on panic with relevance to generalized anxiety and phobias. Biological Psychiatry 1999; 46: 1205–18.
16 октября 2009
Количество просмотров: 2201


