Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№06 2009
Применение мексидола у больных с органическими заболеваниями головного мозга №06 2009
Номера страниц в выпуске:29-33
В последние годы появляется все больше лекарственных средств, обладающих широким спектром фармакологической активности, сочетающим анксиолитические, ноотропные, стимулирующие и другие свойства. В значительной мере это связано с целенаправленным поиском и разработкой таких препаратов, а также с выявлением новых компонентов в действии уже существующих при их детальном изучении. Препараты с такими свойствами являются проблемными с позиций традиционных классификаций психотропных и нейротропных средств [2, 6, 8], в связи с чем в ряде работ предлагается называть их «транквилоноотропами» или «ноотранквилизаторами».
Введение
В последние годы появляется все больше лекарственных средств, обладающих широким спектром фармакологической активности, сочетающим анксиолитические, ноотропные, стимулирующие и другие свойства. В значительной мере это связано с целенаправленным поиском и разработкой таких препаратов, а также с выявлением новых компонентов в действии уже существующих при их детальном изучении. Препараты с такими свойствами являются проблемными с позиций традиционных классификаций психотропных и нейротропных средств [2, 6, 8], в связи с чем в ряде работ предлагается называть их «транквилоноотропами» или «ноотранквилизаторами». Теоретически представляется вполне обоснованным практическое применение указанных средств при сложной и полиморфной клинической картине различных патологических состояний, при которых традиционно применяют комбинированную терапию. К такой патологии относятся органические поражения головного мозга, в частности те их варианты, при которых когнитивные нарушения сочетаются с неврозоподобной, в том числе псевдоневрастенической симптоматикой [14, 24–26]. Психиатры такие расстройства чаще рассматривают в рамках психоорганического синдрома, неврологи – как различные варианты энцефалопатий. Следует отметить, что относительно негрубые проявления психоорганических расстройств и легкие и умеренные нарушения когнитивной сферы в настоящее время приобретают все большую значимость с медицинской и социальной точек зрения. С терапевтических позиций все большую актуальность заслуживает разработка новых эффективных направлений лечения негрубых интеллектуально-мнестических нарушений, обозначаемых как «мягкое» когнитивное снижение [10–12, 22, 37, 38, 51, 53], «умеренное когнитивное расстройство» [37, 20–22], под которыми понимается ухудшение когнитивных функций, обусловленное патологическими или возрастными изменениями мозга и существенно не влияющее на бытовую, профессиональную и социальную деятельность [10, 11, 20, 21, 37, 39, 46, 47, 53]. Они весьма распространены в населении (от 25 до 55% у лиц старше 60 лет), причем их частота повышается с увеличением возраста [16, 18, 42, 44, 49, 50]. Примерно в 30% случаев умеренные когнитивные нарушения обусловлены сосудистым поражением головного мозга [12, 22, 37, 43]. Эти ранние проявления когнитивных расстройств без проведенной адекватной терапии в 15% случаев трансформируются в деменции и, соответственно, являются более перспективными с точки зрения возможности эффективных терапевтических вмешательств [12, 20, 38, 40, 47, 48, 50, 51]. При лечении этих расстройств используются препараты различных групп: вазоактивные средства, ноотропы, антигипоксанты и антиоксиданты, препараты, обладающие нейротрансмиттерным, нейротрофическим и нейромодуляторным эффектом [2, 6, 10–12, 15, 17, 21, 22, 29]. Как правило, в структуре комплексной терапии применяется сочетание препаратов, обладающих ноотропными свойствами, и других средств с психотропным действием, адресованным к проявлениям неврозоподобной симптоматики.
Одним из препаратов, обладающих широким спектром терапевтического действия, применяемым в неврологической, психиатрической, терапевтической и хирургической практике, является мексидол (2-этил-6-метил-3-оксипиридина сукцинат) [3–5, 7–9, 19, 23]. Препарат был синтезирован в Институте химической физики им. Н.Н.Семенова РАН и фармакологически детально изучен в НИИ фармакологии им. В.В.Закусова РАМН. Благодаря своему механизму действия и широкому спектру фармакологических эффектов (антиоксидантный, церебропротективный, антигипоксический, анксиолитический, антистрессорный, ноотропный, вегетотропный, противосудорожный; улучшение и стабилизация мозгового метаболизма и кровоснабжения головного мозга; улучшение микроциркуляции и реологических свойств крови, подавление агрегации тромбоцитов; активация иммунной системы) мексидол оказывает влияние на основные звенья патогенеза различных заболеваний, связанных с процессами свободнорадикального окисления и кислородозависимыми патологическими состояниями [3–5, 7, 8, 30, 31]. Свои фармакологические эффекты мексидол реализует по крайней мере на трех уровнях – нейрональном, сосудистом и метаболическом.
Указанные фармакологические свойства препарата явились предпосылкой к целенаправленному исследованию особенностей действия и изучению эффективности мексидола, применяемого в качестве терапевтического средства у больных с органическими поражениями головного мозга различного генеза, в клинической картине которых неглубокие когнитивные нарушения сочетались с неврозоподобными расстройствами.
Материал и методы
Изучение действия препарата проведено у больных двух групп: 1) с органическим поражением головного мозга травматического генеза [диагностические рубрики по МКБ-10 «Посткоммоционный синдром» F07.2 и «Органическое астеническое расстройство в связи с травмой головного мозга» F06.60] – 15 человек в возрасте от 18 до 45 лет (3 мужчин, 12 женщин, средний возраст 37±5,8 года); 2) с органическим поражением головного мозга сосудистого генеза (диагностическая рубрика «Органическое эмоционально-лабильное (астеническое) расстройство в связи с сосудистыми заболеваниями головного мозга» F06.61) – 16 человек в возрасте от 45 до 77 лет (2 мужчин, 14 женщин, средний возраст 58±3,7 года). У больных 1-й группы заболевание явилось следствием перенесенных (от 2 до 10 лет назад) черепно-мозговых травм (повторных сотрясений или ушибов головного мозга легкой и средней тяжести). У больных 2-й группы патология головного мозга обусловлена хроническим сосудистым заболеванием – гипертонической болезнью или церебральным атеросклерозом. Для исследования отбирали больных без обострений и декомпенсации сопутствующей соматической патологии, признаков хронического алкоголизма, лекарственной и наркотической зависимости. Наличие у пациентов психоорганического синдрома подтверждено параклиническими исследованиями (ЭЭГ, РЭГ, М-эхо, у 13 больных также компьютерной томографией головного мозга) и нейропсихологическим обследованием. У 19 больных имелись соматические заболевания в состоянии компенсации: у 12 – гипертоническая болезнь, у 10 – церебральный атеросклероз, у 7 – ишемическая болезнь сердца, у 4 – хронический бронхит, у 1 – бронхиальная астма, у 1 – ревматоидный артрит, у 3 – язвенная болезнь, у 7 – хронический холецистит, у 4 – миома матки, у 10 – остеохондроз позвоночника. Больные, принимавшие соматотропную терапию (6 человек – антигипертензивные средства, нитраты), продолжали ее прием без изменения дозы лекарственных средств на протяжении всего периода применения мексидола.
Дизайн работы был следующим: у отобранных для исследования больных, получавших препараты, обладающие психотропной активностью, проводили их отмену на срок не менее 7 дней. Далее на протяжении 5–7 дней больные получали плацебо для исключения плацебо-чувствительных пациентов. Мексидол применяли в таблетированной лекарственной форме в дозе 500 мг/сут, распределенной на 2 приема. Продолжительность терапии составляла 28–42 дня.
Использовали методики врачебной оценки и самооценки состояния: унифицированную систему оценки клинико-фармакологического действия психотропных препаратов [1], позволяющую оценить количественную (баллированную) выраженность психопатологической и соматовегетативной симптоматики в процессе терапии, а также дать характеристику конкретных фармакологических эффектов на основании ранее разработанной группировки соответствующих симптомов [32], шкалу тревоги Гамильтона [45]; тест дифференцированной самооценки состояния [13]; шкалу оценки ситуационной и личностной тревоги Спилбергера–Ханина [36]. Для оценки ноотропного эффекта также использованы шкала оценки познания [52] и компьютеризированная методика психофизиологического обследования, позволяющая проводить квантифицированную оценку параметров внимания, простой и сложной сенсомоторной реакций, оперативной зрительной памяти и интегрального параметра успешности операторской деятельности [27, 28].
Обработку результатов исследования производили с использованием критерия Манна–Уитни, критерия Уилкоксона и точного критерия Фишера – двусторонний вариант (стандартная статистическая программа STATISTICA).
Представляя и анализируя полученные результаты, необходимо отметить, что у исследованных больных с пост-травматическим (1-я группа) и сосудистым поражением головного мозга (2-я группа) имелись определенные различия в клинической картине психоорганических расстройств, что позволяло провести оценку действия мексидола на более объемной «мишени» терапевтического воздействия. У больных с посттравматическим поражением ЦНС выраженность расстройств была относительно неглубока и ограничивалась преимущественно церебрастенией с легкими дисмнестическими нарушениями (трудностями запоминания и воспроизведения информации), метеопатией, цефалгиями, плохой переносимостью духоты, жары, езды в транспорте. Суммарный балл по короткой шкале познания у этих больных составил 9,93±2,11, способность концентрации внимания и счета – 2,80±0,42, кратковременная память на текущие события – 2,13±0,34, долговременная память – 1,86±0,69, деятельность и самообслуживание – 2,01±0,40 балла. У 8 из них церебрастенические расстройства сочетались с выраженными соматовегетативными нарушениями и тревогой, у 1 в структуре психорганического синдрома имелись ипохондрические проявления. Нарушения ночного сна у 6 больных этой группы были в основном представлены затрудненным засыпанием, у 8 – поверхностным сном с частыми пробуждениями.
Клиническая картина нарушений у больных с органическим заболеванием головного мозга сосудистого генеза отличалась большей выраженностью церебрастении и интеллектуально-мнестических расстройств, нередко сочетавшихся с проявлениями очаговой корковой патологии (афазия, акалькулия и т.д.). Они характеризовались более грубыми нарушениями кратковременной и долговременной памяти, при этом в первую очередь страдали усвоение и фиксация текущей информации. Суммарный балл по короткой шкале познания у них составлял 11,19±2,25, способность концентрации внимания и счета – 3,18±0,61, кратковременная память на текущие события – 2,56±0,54, долговременная память – 2,25±0,56, деятельность и самообслуживание – 2,18±0,53 балла. Несмотря на отсутствие статистически достоверных различий (по критериям Фишера, Манна–Уитни) указанных показателей у изученных групп больных по выраженности когнитивных расстройств, отмечавшиеся отличия при клинической оценке проявлялись довольно отчетливо. У больных 2-й группы также имелись нарушения мышления в виде некоторой его вязкости, обстоятельности, плохой переключаемости, у 9 из них сочетавшиеся с общим снижением уровня личности. У них отмечено обеднение словарного запаса, ухудшение способности к обобщению, абстрагированию, выявлялись сложности в подборе слов, построении речи, в математических подсчетах. Повышенная утомляемость, снижение жизненного тонуса выявлены у всех больных этой группы, они проявлялись в быстро наступающем чувстве слабости после незначительных нагрузок, которая порой не проходила даже после отдыха. Это состояние у 8 из 16 больных этой группы сопровождалось дневной сонливостью, у 5 – апатичностью, неверием в свои силы, у 14 – повышенной раздражительностью, у 13 – тревожностью и тревожными опасениями, у 12 – недержанием аффекта, у 13 – легко возникающими эмоциональными реакциями в виде повышенной обидчивости, гипертрофированной ранимости, сенситивности, плаксивости по незначительному поводу. Ночной сон у 9 пациентов характеризовался трудностями засыпания, у 10 – нарушениями глубины ночного сна и частыми пробуждениями, у 5 – расстройствами пробуждения. Значительно чаще по сравнению с 1-й группой у этих больных отмечены соматовегетативные расстройства: головная боль (11 больных), подъем артериального давления (8 больных), головокружения (8 больных), повышенная потливость (8 больных).
У исследованных больных терапевтическое действие мексидола при курсовом применении в суточной дозе 500 мг проявлялось прежде всего в быстро реализующемся ослаблении тревоги, повышенной раздражительности, аффективной лабильности, астенических нарушений и расстройств ночного сна, во влиянии на проявления апатии, дневной сонливости, а к 28-му дню и на нарушения внимания и памяти (табл. 1). При терапии выявлено целостное, гармоничное действие препарата на неврозоподобные и психоорганические расстройства. Обращала на себя внимание естественность для больных наступающих изменений, улучшение состояния они часто не связывали с действием препарата, указывали на его хорошую переносимость.
Описанная динамика психопатологической симптоматики и особенности действия препарата принципиально не различались у больных молодого возраста с посткоммоционным синдромом и пожилого – с сосудистой патологией головного мозга.
При этом не выявлено статистически достоверных различий между выраженностью отдельных эффектов у больных с посттравматическим и сосудистым поражением ЦНС. Указанная композиция различных компонентов психотропной активности мексидола вполне соответствует результатам экспериментальных [3–5, 7, 8] и ранее проведенных клинических исследований [34, 35], а также первичному позиционированию препарата как анксиолитика с ноотропным компонентом действия [9, 30, 31].
Следует особо отметить отсутствие у мексидола в терапевтических дозах проявлений седации и сопоставимость его транквило-активирующего эффекта с действием атипичных анксиолитиков. Динамика показателей шкалы Гамильтона и психологических тестов при терапии мексидолом у больных с органическим поражением ЦНС травматического и сосудистого генеза (рис. 1) показывает уменьшение показателей тревоги по шкале Гамильтона и ситуационной тревожности по методике Спилбергера–Ханина, подтверждающие отчетливое анксиолитическое действие препарата.
Улучшение показателей самочувствия, активности и настроения, отмечающееся с 1-й недели терапии и более отчетливо проявляющееся к ее завершению (см. рис. 1), вероятно, детерминировано активирующим компонентом действия мексидола и косвенно характеризует его хорошую переносимость. Анализируя терапевтические изменения показателей субъективной оценки состояния, можно также отметить отсутствие достоверных различий в их динамике у исследованных больных разных групп при тенденции к их большей выраженности у больных более молодого возраста с посттравматическими расстройствами.
Особого внимания заслуживает оценка ноотропного действия мексидола, так как в проведенных ранее исследованиях эффективность его применения у аналогичного контингента больных связывалась с наличием у препарата анксиолитического действия [33].
По данным показателей короткой шкалы оценки познания, к 3-й неделе терапии у пациентов обеих групп отмечено достоверное улучшение концентрации внимания и счета, а у больных с органическим поражением ЦНС травматического генеза также достоверно улучшались показатели кратковременной памяти (рис. 2).
Достоверное улучшение показателей долговременной памяти в обеих группах было выявлено с 4-й недели лечения. Эти результаты соответствуют данным о ретардации специфического ноотропного эффекта, который проявляется начиная со 2-й недели терапии. Обращают на себя внимание различия во времени возникновения, достоверного улучшения показателей кратковременной памяти на текущие события у больных анализируемых групп. Для пациентов 1-й группы это улучшение отмечено с 14-го дня, а для 2-й группы – с 28-го дня. Эти данные могут быть объяснены большей выраженностью ноотропного действия мексидола у пациентов молодого возраста с органическим поражением ЦНС травматического генеза, а также большей тяжестью и, соответственно, определенной резистентностью, торпидностью мнестических расстройств у пожилых больных с органическим поражением ЦНС сосудистого генеза.
Одним из важных аспектов действия психотропных препаратов является их влияние на показатели психофизиологического состояния, отражающие отдельные параметры когнитивных функций и имеющие существенное значение для достижения эффективности терапии.
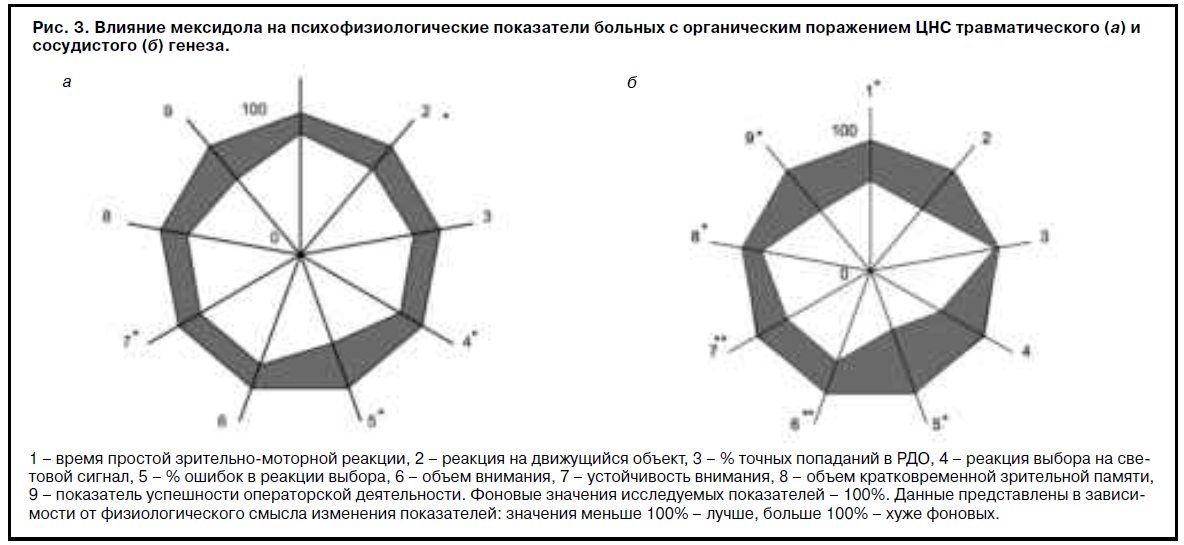
При оценке динамики психофизиологического состояния у исследуемых больных при применении мексидола (рис. 3) выявлено достоверное улучшение показателей процента ошибок в реакции выбора, внимания (объем и устойчивость), памяти, простой зрительно-моторной реакции и интегрального показателя успешности операторской деятельности. Значительно улучшались также параметры реакции на движущийся объект и реакции выбора при минимальной динамике показателя процента точных попаданий в РДО. Значимых различий по влиянию мексидола на психофизиологическое состояние больных с органическим поражением ЦНС травматического и сосудистого генеза не выявлено.
Анализ терапевтической эффективности мексидола у исследуемых групп пациентов показал, что при его применении эффективность терапии у больных с органическим поражением ЦНС травматического генеза была несколько выше, чем у больных с органическим поражением ЦНС сосудистого генеза (66,7 и 61,5% соответственно).
Отмеченные нежелательные явления при терапии мексидолом были единичными, кратковременными и слабовыраженными: миорелаксация у 7 (23%) человек, головная боль у 7 (23%), нарушение координации у 1 (3%), подъем артериального давления у 4 (13%), дневная сонливость у 3 (10%), нарушение ночного сна у 1 (3%) пациента.
Заключение
Таким образом, результаты исследования свидетельствуют о том, что по спектру психотропной активности мексидол можно отнести к особой группе препаратов, сочетающих анксиолитическое, активирующее и ноотропное действие. Выявленное положительное влияние мексидола на неврозоподобные расстройства, нарушения внимания, памяти и познавательной деятельности при хорошей переносимости препарата позволяет полагать возможность и перспективность его применения при умеренных когнитивных нарушениях различного генеза, в том числе при наличии в клинической картине церебрастенических и тревожных нарушений, а также при терапии психоорганических расстройств в геронтопсихиатрической практике.
В последние годы появляется все больше лекарственных средств, обладающих широким спектром фармакологической активности, сочетающим анксиолитические, ноотропные, стимулирующие и другие свойства. В значительной мере это связано с целенаправленным поиском и разработкой таких препаратов, а также с выявлением новых компонентов в действии уже существующих при их детальном изучении. Препараты с такими свойствами являются проблемными с позиций традиционных классификаций психотропных и нейротропных средств [2, 6, 8], в связи с чем в ряде работ предлагается называть их «транквилоноотропами» или «ноотранквилизаторами». Теоретически представляется вполне обоснованным практическое применение указанных средств при сложной и полиморфной клинической картине различных патологических состояний, при которых традиционно применяют комбинированную терапию. К такой патологии относятся органические поражения головного мозга, в частности те их варианты, при которых когнитивные нарушения сочетаются с неврозоподобной, в том числе псевдоневрастенической симптоматикой [14, 24–26]. Психиатры такие расстройства чаще рассматривают в рамках психоорганического синдрома, неврологи – как различные варианты энцефалопатий. Следует отметить, что относительно негрубые проявления психоорганических расстройств и легкие и умеренные нарушения когнитивной сферы в настоящее время приобретают все большую значимость с медицинской и социальной точек зрения. С терапевтических позиций все большую актуальность заслуживает разработка новых эффективных направлений лечения негрубых интеллектуально-мнестических нарушений, обозначаемых как «мягкое» когнитивное снижение [10–12, 22, 37, 38, 51, 53], «умеренное когнитивное расстройство» [37, 20–22], под которыми понимается ухудшение когнитивных функций, обусловленное патологическими или возрастными изменениями мозга и существенно не влияющее на бытовую, профессиональную и социальную деятельность [10, 11, 20, 21, 37, 39, 46, 47, 53]. Они весьма распространены в населении (от 25 до 55% у лиц старше 60 лет), причем их частота повышается с увеличением возраста [16, 18, 42, 44, 49, 50]. Примерно в 30% случаев умеренные когнитивные нарушения обусловлены сосудистым поражением головного мозга [12, 22, 37, 43]. Эти ранние проявления когнитивных расстройств без проведенной адекватной терапии в 15% случаев трансформируются в деменции и, соответственно, являются более перспективными с точки зрения возможности эффективных терапевтических вмешательств [12, 20, 38, 40, 47, 48, 50, 51]. При лечении этих расстройств используются препараты различных групп: вазоактивные средства, ноотропы, антигипоксанты и антиоксиданты, препараты, обладающие нейротрансмиттерным, нейротрофическим и нейромодуляторным эффектом [2, 6, 10–12, 15, 17, 21, 22, 29]. Как правило, в структуре комплексной терапии применяется сочетание препаратов, обладающих ноотропными свойствами, и других средств с психотропным действием, адресованным к проявлениям неврозоподобной симптоматики.
Одним из препаратов, обладающих широким спектром терапевтического действия, применяемым в неврологической, психиатрической, терапевтической и хирургической практике, является мексидол (2-этил-6-метил-3-оксипиридина сукцинат) [3–5, 7–9, 19, 23]. Препарат был синтезирован в Институте химической физики им. Н.Н.Семенова РАН и фармакологически детально изучен в НИИ фармакологии им. В.В.Закусова РАМН. Благодаря своему механизму действия и широкому спектру фармакологических эффектов (антиоксидантный, церебропротективный, антигипоксический, анксиолитический, антистрессорный, ноотропный, вегетотропный, противосудорожный; улучшение и стабилизация мозгового метаболизма и кровоснабжения головного мозга; улучшение микроциркуляции и реологических свойств крови, подавление агрегации тромбоцитов; активация иммунной системы) мексидол оказывает влияние на основные звенья патогенеза различных заболеваний, связанных с процессами свободнорадикального окисления и кислородозависимыми патологическими состояниями [3–5, 7, 8, 30, 31]. Свои фармакологические эффекты мексидол реализует по крайней мере на трех уровнях – нейрональном, сосудистом и метаболическом.
Указанные фармакологические свойства препарата явились предпосылкой к целенаправленному исследованию особенностей действия и изучению эффективности мексидола, применяемого в качестве терапевтического средства у больных с органическими поражениями головного мозга различного генеза, в клинической картине которых неглубокие когнитивные нарушения сочетались с неврозоподобными расстройствами.
Материал и методы
Изучение действия препарата проведено у больных двух групп: 1) с органическим поражением головного мозга травматического генеза [диагностические рубрики по МКБ-10 «Посткоммоционный синдром» F07.2 и «Органическое астеническое расстройство в связи с травмой головного мозга» F06.60] – 15 человек в возрасте от 18 до 45 лет (3 мужчин, 12 женщин, средний возраст 37±5,8 года); 2) с органическим поражением головного мозга сосудистого генеза (диагностическая рубрика «Органическое эмоционально-лабильное (астеническое) расстройство в связи с сосудистыми заболеваниями головного мозга» F06.61) – 16 человек в возрасте от 45 до 77 лет (2 мужчин, 14 женщин, средний возраст 58±3,7 года). У больных 1-й группы заболевание явилось следствием перенесенных (от 2 до 10 лет назад) черепно-мозговых травм (повторных сотрясений или ушибов головного мозга легкой и средней тяжести). У больных 2-й группы патология головного мозга обусловлена хроническим сосудистым заболеванием – гипертонической болезнью или церебральным атеросклерозом. Для исследования отбирали больных без обострений и декомпенсации сопутствующей соматической патологии, признаков хронического алкоголизма, лекарственной и наркотической зависимости. Наличие у пациентов психоорганического синдрома подтверждено параклиническими исследованиями (ЭЭГ, РЭГ, М-эхо, у 13 больных также компьютерной томографией головного мозга) и нейропсихологическим обследованием. У 19 больных имелись соматические заболевания в состоянии компенсации: у 12 – гипертоническая болезнь, у 10 – церебральный атеросклероз, у 7 – ишемическая болезнь сердца, у 4 – хронический бронхит, у 1 – бронхиальная астма, у 1 – ревматоидный артрит, у 3 – язвенная болезнь, у 7 – хронический холецистит, у 4 – миома матки, у 10 – остеохондроз позвоночника. Больные, принимавшие соматотропную терапию (6 человек – антигипертензивные средства, нитраты), продолжали ее прием без изменения дозы лекарственных средств на протяжении всего периода применения мексидола.
Дизайн работы был следующим: у отобранных для исследования больных, получавших препараты, обладающие психотропной активностью, проводили их отмену на срок не менее 7 дней. Далее на протяжении 5–7 дней больные получали плацебо для исключения плацебо-чувствительных пациентов. Мексидол применяли в таблетированной лекарственной форме в дозе 500 мг/сут, распределенной на 2 приема. Продолжительность терапии составляла 28–42 дня.
Использовали методики врачебной оценки и самооценки состояния: унифицированную систему оценки клинико-фармакологического действия психотропных препаратов [1], позволяющую оценить количественную (баллированную) выраженность психопатологической и соматовегетативной симптоматики в процессе терапии, а также дать характеристику конкретных фармакологических эффектов на основании ранее разработанной группировки соответствующих симптомов [32], шкалу тревоги Гамильтона [45]; тест дифференцированной самооценки состояния [13]; шкалу оценки ситуационной и личностной тревоги Спилбергера–Ханина [36]. Для оценки ноотропного эффекта также использованы шкала оценки познания [52] и компьютеризированная методика психофизиологического обследования, позволяющая проводить квантифицированную оценку параметров внимания, простой и сложной сенсомоторной реакций, оперативной зрительной памяти и интегрального параметра успешности операторской деятельности [27, 28].
Обработку результатов исследования производили с использованием критерия Манна–Уитни, критерия Уилкоксона и точного критерия Фишера – двусторонний вариант (стандартная статистическая программа STATISTICA).
Представляя и анализируя полученные результаты, необходимо отметить, что у исследованных больных с пост-травматическим (1-я группа) и сосудистым поражением головного мозга (2-я группа) имелись определенные различия в клинической картине психоорганических расстройств, что позволяло провести оценку действия мексидола на более объемной «мишени» терапевтического воздействия. У больных с посттравматическим поражением ЦНС выраженность расстройств была относительно неглубока и ограничивалась преимущественно церебрастенией с легкими дисмнестическими нарушениями (трудностями запоминания и воспроизведения информации), метеопатией, цефалгиями, плохой переносимостью духоты, жары, езды в транспорте. Суммарный балл по короткой шкале познания у этих больных составил 9,93±2,11, способность концентрации внимания и счета – 2,80±0,42, кратковременная память на текущие события – 2,13±0,34, долговременная память – 1,86±0,69, деятельность и самообслуживание – 2,01±0,40 балла. У 8 из них церебрастенические расстройства сочетались с выраженными соматовегетативными нарушениями и тревогой, у 1 в структуре психорганического синдрома имелись ипохондрические проявления. Нарушения ночного сна у 6 больных этой группы были в основном представлены затрудненным засыпанием, у 8 – поверхностным сном с частыми пробуждениями.
Клиническая картина нарушений у больных с органическим заболеванием головного мозга сосудистого генеза отличалась большей выраженностью церебрастении и интеллектуально-мнестических расстройств, нередко сочетавшихся с проявлениями очаговой корковой патологии (афазия, акалькулия и т.д.). Они характеризовались более грубыми нарушениями кратковременной и долговременной памяти, при этом в первую очередь страдали усвоение и фиксация текущей информации. Суммарный балл по короткой шкале познания у них составлял 11,19±2,25, способность концентрации внимания и счета – 3,18±0,61, кратковременная память на текущие события – 2,56±0,54, долговременная память – 2,25±0,56, деятельность и самообслуживание – 2,18±0,53 балла. Несмотря на отсутствие статистически достоверных различий (по критериям Фишера, Манна–Уитни) указанных показателей у изученных групп больных по выраженности когнитивных расстройств, отмечавшиеся отличия при клинической оценке проявлялись довольно отчетливо. У больных 2-й группы также имелись нарушения мышления в виде некоторой его вязкости, обстоятельности, плохой переключаемости, у 9 из них сочетавшиеся с общим снижением уровня личности. У них отмечено обеднение словарного запаса, ухудшение способности к обобщению, абстрагированию, выявлялись сложности в подборе слов, построении речи, в математических подсчетах. Повышенная утомляемость, снижение жизненного тонуса выявлены у всех больных этой группы, они проявлялись в быстро наступающем чувстве слабости после незначительных нагрузок, которая порой не проходила даже после отдыха. Это состояние у 8 из 16 больных этой группы сопровождалось дневной сонливостью, у 5 – апатичностью, неверием в свои силы, у 14 – повышенной раздражительностью, у 13 – тревожностью и тревожными опасениями, у 12 – недержанием аффекта, у 13 – легко возникающими эмоциональными реакциями в виде повышенной обидчивости, гипертрофированной ранимости, сенситивности, плаксивости по незначительному поводу. Ночной сон у 9 пациентов характеризовался трудностями засыпания, у 10 – нарушениями глубины ночного сна и частыми пробуждениями, у 5 – расстройствами пробуждения. Значительно чаще по сравнению с 1-й группой у этих больных отмечены соматовегетативные расстройства: головная боль (11 больных), подъем артериального давления (8 больных), головокружения (8 больных), повышенная потливость (8 больных).
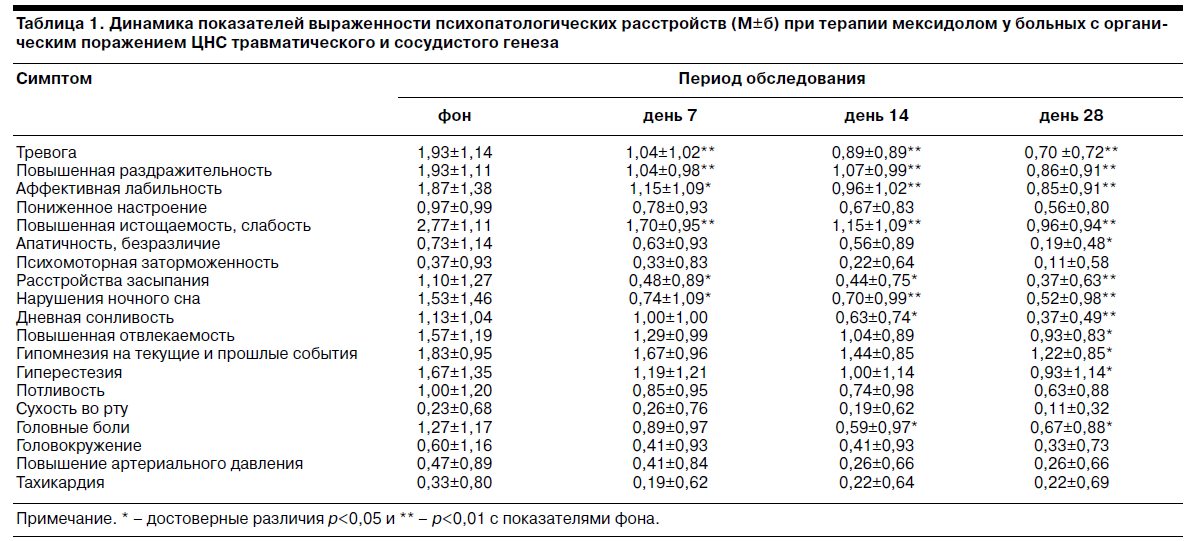
У исследованных больных терапевтическое действие мексидола при курсовом применении в суточной дозе 500 мг проявлялось прежде всего в быстро реализующемся ослаблении тревоги, повышенной раздражительности, аффективной лабильности, астенических нарушений и расстройств ночного сна, во влиянии на проявления апатии, дневной сонливости, а к 28-му дню и на нарушения внимания и памяти (табл. 1). При терапии выявлено целостное, гармоничное действие препарата на неврозоподобные и психоорганические расстройства. Обращала на себя внимание естественность для больных наступающих изменений, улучшение состояния они часто не связывали с действием препарата, указывали на его хорошую переносимость.

Описанная динамика психопатологической симптоматики и особенности действия препарата принципиально не различались у больных молодого возраста с посткоммоционным синдромом и пожилого – с сосудистой патологией головного мозга.

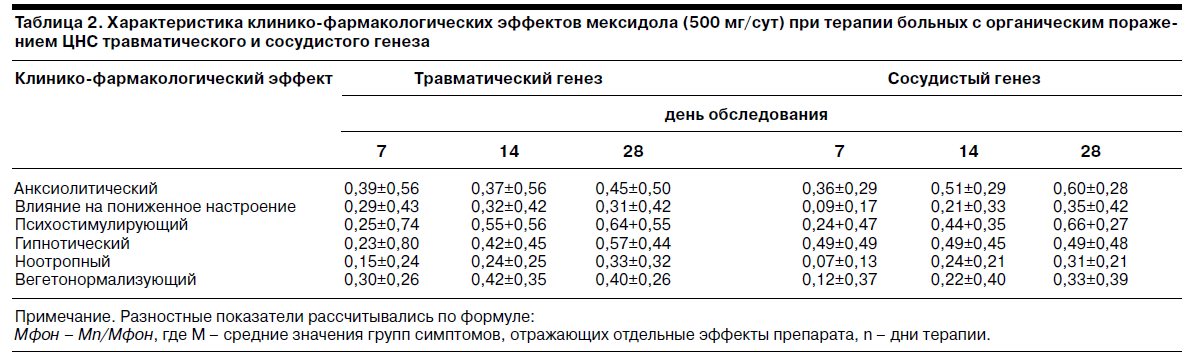
При этом не выявлено статистически достоверных различий между выраженностью отдельных эффектов у больных с посттравматическим и сосудистым поражением ЦНС. Указанная композиция различных компонентов психотропной активности мексидола вполне соответствует результатам экспериментальных [3–5, 7, 8] и ранее проведенных клинических исследований [34, 35], а также первичному позиционированию препарата как анксиолитика с ноотропным компонентом действия [9, 30, 31].

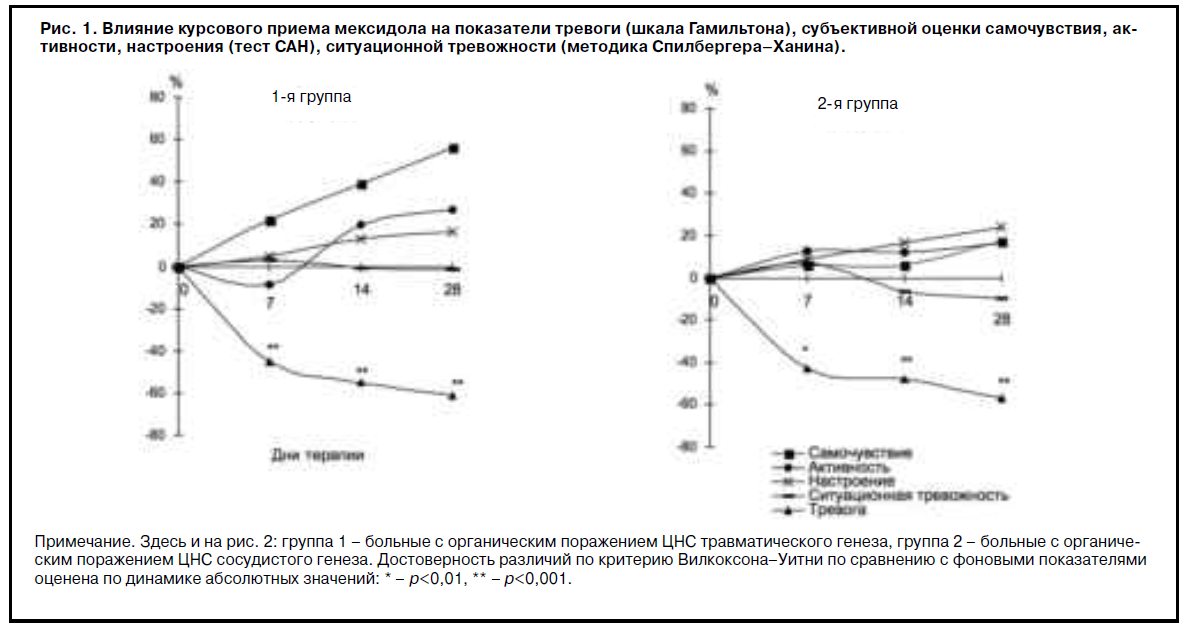
Следует особо отметить отсутствие у мексидола в терапевтических дозах проявлений седации и сопоставимость его транквило-активирующего эффекта с действием атипичных анксиолитиков. Динамика показателей шкалы Гамильтона и психологических тестов при терапии мексидолом у больных с органическим поражением ЦНС травматического и сосудистого генеза (рис. 1) показывает уменьшение показателей тревоги по шкале Гамильтона и ситуационной тревожности по методике Спилбергера–Ханина, подтверждающие отчетливое анксиолитическое действие препарата.
Улучшение показателей самочувствия, активности и настроения, отмечающееся с 1-й недели терапии и более отчетливо проявляющееся к ее завершению (см. рис. 1), вероятно, детерминировано активирующим компонентом действия мексидола и косвенно характеризует его хорошую переносимость. Анализируя терапевтические изменения показателей субъективной оценки состояния, можно также отметить отсутствие достоверных различий в их динамике у исследованных больных разных групп при тенденции к их большей выраженности у больных более молодого возраста с посттравматическими расстройствами.
Особого внимания заслуживает оценка ноотропного действия мексидола, так как в проведенных ранее исследованиях эффективность его применения у аналогичного контингента больных связывалась с наличием у препарата анксиолитического действия [33].

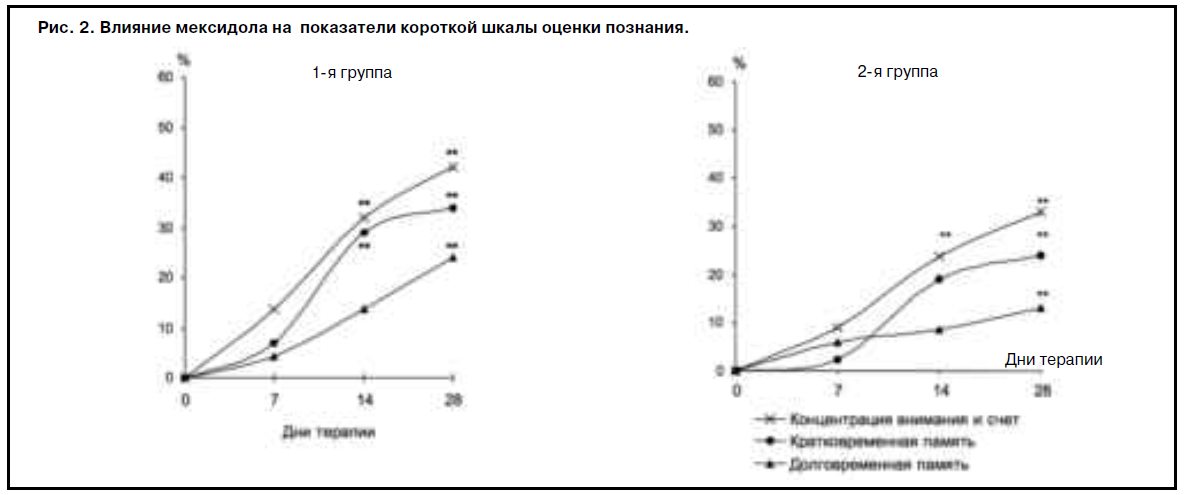
По данным показателей короткой шкалы оценки познания, к 3-й неделе терапии у пациентов обеих групп отмечено достоверное улучшение концентрации внимания и счета, а у больных с органическим поражением ЦНС травматического генеза также достоверно улучшались показатели кратковременной памяти (рис. 2).
Достоверное улучшение показателей долговременной памяти в обеих группах было выявлено с 4-й недели лечения. Эти результаты соответствуют данным о ретардации специфического ноотропного эффекта, который проявляется начиная со 2-й недели терапии. Обращают на себя внимание различия во времени возникновения, достоверного улучшения показателей кратковременной памяти на текущие события у больных анализируемых групп. Для пациентов 1-й группы это улучшение отмечено с 14-го дня, а для 2-й группы – с 28-го дня. Эти данные могут быть объяснены большей выраженностью ноотропного действия мексидола у пациентов молодого возраста с органическим поражением ЦНС травматического генеза, а также большей тяжестью и, соответственно, определенной резистентностью, торпидностью мнестических расстройств у пожилых больных с органическим поражением ЦНС сосудистого генеза.
Одним из важных аспектов действия психотропных препаратов является их влияние на показатели психофизиологического состояния, отражающие отдельные параметры когнитивных функций и имеющие существенное значение для достижения эффективности терапии.

При оценке динамики психофизиологического состояния у исследуемых больных при применении мексидола (рис. 3) выявлено достоверное улучшение показателей процента ошибок в реакции выбора, внимания (объем и устойчивость), памяти, простой зрительно-моторной реакции и интегрального показателя успешности операторской деятельности. Значительно улучшались также параметры реакции на движущийся объект и реакции выбора при минимальной динамике показателя процента точных попаданий в РДО. Значимых различий по влиянию мексидола на психофизиологическое состояние больных с органическим поражением ЦНС травматического и сосудистого генеза не выявлено.
Анализ терапевтической эффективности мексидола у исследуемых групп пациентов показал, что при его применении эффективность терапии у больных с органическим поражением ЦНС травматического генеза была несколько выше, чем у больных с органическим поражением ЦНС сосудистого генеза (66,7 и 61,5% соответственно).
Отмеченные нежелательные явления при терапии мексидолом были единичными, кратковременными и слабовыраженными: миорелаксация у 7 (23%) человек, головная боль у 7 (23%), нарушение координации у 1 (3%), подъем артериального давления у 4 (13%), дневная сонливость у 3 (10%), нарушение ночного сна у 1 (3%) пациента.
Заключение
Таким образом, результаты исследования свидетельствуют о том, что по спектру психотропной активности мексидол можно отнести к особой группе препаратов, сочетающих анксиолитическое, активирующее и ноотропное действие. Выявленное положительное влияние мексидола на неврозоподобные расстройства, нарушения внимания, памяти и познавательной деятельности при хорошей переносимости препарата позволяет полагать возможность и перспективность его применения при умеренных когнитивных нарушениях различного генеза, в том числе при наличии в клинической картине церебрастенических и тревожных нарушений, а также при терапии психоорганических расстройств в геронтопсихиатрической практике.
Список исп. литературыСкрыть список1. Александровский Ю.А., Руденко Г.М., Незнамов Г.Г. и др. Унифицированная система оценки клинико-фармакологического действия психотропных препаратов у больных с пограничными нервно-психическими расстройствами. М., 1984.
2. Вальдман А.В., Воронина Т.А. (ред.) Фармакология ноотропов (экспериментальное и клиническое изучение). Сборник трудов. М., 1989.
3. Вальдман А.В., Воронина Т.А., Смирнов Л.Д. Влияние производных 3-оксипиридина на центральную нервную систему. Бюл. эксперимент. биол. и мед. 1985; с. 35–9.
4. Воронина Т.А. Отечественный препарат нового поколения МЕКСИДОЛ® основные эффекты, механизм действия, применение. Методические рекомендации. М., 2005.
5. Воронина Т.А., Гарибова Т.Л., Хромова И.В. Диссоциация антиамнестического и противогипоксического эффектов у ноотропных препаратов. Фармакол. и токсикол. 1987; 3: 21–3.
6. Воронина Т.А., Середенин С.Б. Ноотропные препараты, достижения и новые проблемы. Эксперимент. и клин. фармакол. 1998; 61 (4): 3–9.
7. Воронина Т.А., Смирнов Л.Д., Дюмаев К.М. и др. Влияние мембраномодулятора из класса 3-оксипиридина на фармакологическую активность нейротропных препаратов. Бюл. эксперимент. биол. мед. 1985; ХС1Х (1): 60–2.
8. Воронина Т.А., Смирнов Л.Д., Дюмаев К.М. Производные 3-оксипиридина – перспективный класс психотропных соединений. Биоантиоксиданты: Тез. Всесоюзной конференции. т. 1. Черноголовка, 1986; с. 102–3.
9. Воронина Т.А., Смирнов Л.Д., Телешова Е.С. и др. Антистрессорные эффекты антиоксиданта мексидола и его аналогов в экстремальных ситуациях. Таврич. журн. психиат. 2002; 6 (2; 19): 73–4.
10. Гаврилова С.И. Мягкое когнитивное снижение – доклиническая стадия болезни Альцгеймера? Фармакотерапия болезни Альцгеймера. Ред. С.И.Гаврилова. М.: Пульс, 2003.
11. Гаврилова С.И. Синдром мягкого когнитивного снижения. Врач. 2005; 4: 21–4.
12. Дамулин И.В. Легкие когнитивные нарушения. Методическое пособие для врачей. М.: РКИ Северо пресс, 2004.
13. Доскин В.А., Лаврентьева Н.А., Мирошников Н.П и др. Тест дифференцированной самооценки функционального состояния. Вопр. психол. 1973; 6: 141–5.
14. Егоров С.В. Ноотропные препараты при лечении неврозоподобных расстройств сосудистого генеза у больных пожилого возраста. Дис. ... канд. мед. наук. М., 1996.
15. Завалишин И.А., Яхно Н.Н., Гаврилова С.И. (ред.) Нейродегенеративные болезни и старение. М., 2001.
16. Захаров В.В. Всероссийская программа исследований эпидемиологии и терапии когнитивных расстройств в пожилом возрасте («Прометей»). Неврол. журн. 2006; 11: 27–32.
17. Захаров В.В., Локшина А.Б. Применение препарата проноран (пирибедил) при легких когнитивных расстройствах у пожилых больных с дисциркуляторной энцефалопатией. Неврол. журн. 2004; 2: 30–5.
18. Калынь Я.Б. Психическое здоровье населения пожилого и старческого возраста (клинико-эпидемиологическое исследование). Автореф. дис.... докт. мед. наук. М., 2001.
19. Косенко В.Г., Карагезян Е.А., Лунева Л.В., Смоленко Л.Ф. Применение мексидола в психиатрической практике. Журн. неврол. и психиат. им. Корсакова. 2006; 6: 38–43.
20. Левин О.С. Диагностика и лечение умеренно выраженных когнитивных нарушений в пожилом возрасте. Журн. неврол. и психиат. 2006; 8: 42–9.
21. Левин О.С., Голубева Л.В. Гетерогенность умеренного когнитивного расстройства: диагностические и терапевтические аспекты. Cons. Med. 2006; 8 (2): 106–12.
22. Локшина А.Б., Захаров В.В. Легкие и умеренные когнитивные нарушения при дисциркуляторной энцефалопатии. Неврол. журн. (Прил. 1). 2006; 11: 57–63.
23. Мальгина Н.В. Применение мексидола в комплексном лечении острого панкреатита. Хирургия. Журн. им. Н.И.Пирогова. 2006; 10: 41–50.
24. Медведев А.В. Сосудистая деменция. Геронтопсихиатрия. Совр. психиат. им. П.В.Ганнушкина. 1998; 4: 20–4.
25. Михайлова Н.М. Невротические расстройства у пожилых пациентов общей практики. Геронтопсихиатрия. Совр. психиат. им. П.В.Ганнушкина. 1998; 4: 12–20.
26. Михайлова Н.М., Кладова А.Ю. Проблема психоорганического синдрома в амбулаторной психогериатрии. Материалы II Российской конференции.: «Болезнь Альцгеймера и старение: от нейробиологии к терапии». М., 1999; с. 74–82.
27. Морозов И.С., Жирнов Е.Н., Барчуков В.Г. и др. Методика изучения влияния лекарственных средств на психофизиологическое состояние и качество деятельности операторов различного профиля с использованием микро-ЭВМ. Эксперимент. и клин. фармакол. 1992; 55 (5): 68–70.
28. Морозов И.С., Жирнов Е.Н., Епишкин Г.К. и др. Комплексная компьютерная методика для оценки психофизиологического состояния и операторской работоспособности. Функциональное состояние человека и методы его исследования. М.: Наука, 1992; с. 3–8.
29. Незнамов Г.Г., Телешова Е.С., Сюняков С.А. и др. Лечение психических нарушений в практике невролога. Клиническое исследование нового пептидного препарата Ноопепт у больных с психоорганическими расстройствами. Cons. Med. Неврология. Психические расстройства. 2007; 9 (2): 10–5.
30. Незнамов Г.Г., Бочкарев В.К., Лыгалов С.И. Клинико-фармакологический анализ транквилизирующего действия мексидола. Медико-биологические аспекты применения антиоксидантов эмоксипина и мексидола (экспериментальное и клиническое изучение). Бюллетень Всесоюзного научн. центра по безопасности биологич. активных в-в. М., 1992; с. 47–54.
31. Незнамов Г.Г., Лыгалов С.И. Сравнительная клинико-фармакологическая характеристика гидазепама и мексидола – новых препаратов с транквилизирующими свойствами. Организационные и клинические вопросы пограничной психиатрии (сборник научных трудов). М., 1990; с. 119–28.
32. Незнамов Г.Г., Сбытов Ю.Г. Клинико-математический анализ быстрого и медленного действия психотропных препаратов у больных с невротическими и неврозоподобными расстройствами. Пограничные нервно-психические расстройства. Ставрополь, 1989; с. 46–58.
33. Незнамов Г.Г., Сюняков С.А., Давыдова И.А., Телешова Е.С. «Быстрые» и «медленные» компоненты психотропного действия препаратов с ноотропными свойствами. Журн. Неврол. и психиатр. 2000; 100 (6): 33–7.
34. Незнамов Г.Г., Телешова Е.С., Сюняков С.А., Давыдова И.А.. Применение мексидола при тревожных и психоорганических расстройствах. Журн. Нейрохир. и неврол. Казахстана. 2005; 3 (4): 20–5.
35. Сариев А.К., Давыдова И.А., Незнамов Г.Г. и др. Взаимосвязь глюкуроноконъюгации мексидола и особенностей его терапевтического действия у больных с органическим поражением ЦНС. Эксперимент. и клин. фармакол. 2001; 64 (3): 17–21.
36. Ханин Ю.Л. Краткое руководство к применению шкалы реактивной и личностной тревожности Г.Д.Спилбергера. Л., 1976; с. 5–21.
37. Яхно Н.Н., Локшина А.Б., Захаров В.В. Легкие и умеренные когнитивные расстройства при дисциркуляторной энцефалопатии. Клин. геронтол. 2005; 11: 38–9.
38. Arnaiz E, Almkvist O. Neuropsychological features of mild cognitive impairment and preclinical Alzheimer,s disease. Acta Neurol Scand 2003; 107 (Suppl. 179): 34–41.
39. Bennett DA. Mild cognitive impairment. Clin Geriatr Med 2004; 20: 15–25.
40. Comijs HC, Dik MG, Deeg DJH et al. The course of cognitive decline in older patients. Dement Geriatr Cogn Dis 2004; 17: 136–42.
41. Daly E, Zaitchik D, Copeland M et al. Clinical predictors of conversion to Alzheimer’s disease. In: Research and Practice in Alzheimer’s Disease. Vol. 5. Ed. By B.Vellas et al. Paris: Serdi Publisher, 2001; p. 44–9.
42. DiCarlo A, Baldereschi M, Amaducci L et al. Cognitive impairment without dementia in older people: prevalence, vascular risk factors, impact on disability. The Italian Longitudinal Study on Aging. J Am Ger Soc 2000; 48: 775–82.
43. Geroldi C, Ferrucci L, Bandinelli S et al. Mild cognitive deterioration with subcortical features: Prevalence, clinical characteristics, and association with cardiovascular risk factors in community-dwelling older persons (The InCHIANTI Study). J Am Ger Soc 2003; 51: 1064–71.
44. Graham JE, Rockwood K, Beattie EL et al Prevalence and severity of cognitive impairment with and without dementia in an elderly population. Lancet 1997; 349: 1793–6.
45. Hamilton M. Theassesment of anxiety states by rating. Br S Med Psychol 1959; 32: 50–5.
46. Jelic V, Kivipelto M, Winblad B. Clinical trials in mild cognitive impairment: lessons for the future. J Neurol Neurosurg Psychiat 2006; 77 (7): 892.
47. Knopman DS. Current treatment of mild cognitive impairment and Alzheimer’s disease. Curr Neurol Nerosci Rep 2006; 6 (5): 365–71.
48. Kurshner HS. Mild cognitive impairment: to treat or not to treat? Curr Neurol Neurosci Rep 2005; 5 (6): 455–7.
49. Larrabee GJ, Crook TH. Estimated prevalence of age-associated memory impairment derived from standardized tests of memory function. Int Psychogeriatr 1994; 6: 95–104.
50. Palmer K, Backman L, Winblad B, Fratiglioni L. Detection of Alzheimer,s disease and dementia in the preclinical phase: population based cohort study. Brit Med J 2003; 326: 245–9.
51. Petersen RS. Mild cognitive impairment: transition from aging to Alzheimer,s disease. Alzheimer,s Disease: Advances in Etiology, Pathogenesis and Therapeutics. Ed. by K.Igbal et al. Chichester etc.: Wiley. 2001; p. 140–51.
52. Reisberg B, Ferris SH, DeLeon MJ et al. The global deterioration scale for assessment of primary degenerative dementia. Am J Psychiat 1982; 139: 1136–9.
53. Ritchie K, Artero S, Touchon J. Classfication criteria for mild cognitive impairment. A population-based validation study. Neurology 2001; 56: 37–42.


