Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№02 2018
Пути повышения эффективности терапии тревожных расстройств в клинике нервных болезней №02 2018
Номера страниц в выпуске:10-15
Селективные ингибиторы обратного захвата серотонина (СИОЗС) большинством исследователей и врачей-практиков признаны препаратами первого выбора для лечения хронических тревожных расстройств. Приблизительно у 1/3 пациентов в первые недели лечения СИОЗС наблюдается усиление соматических симптомов тревоги, что потенциально ухудшает комплаентность. Дополнительное введение коротких курсов бензодиазепинов в инициальный период лечения СИОЗС тревожных расстройств дает ряд преимуществ: возможность быстрого достижения противотревожного эффекта, повышение комплаентности – и практически не влияет на тяжесть и спектр побочных эффектов проводимой терапии.
Ключевые слова: тревожные расстройства, лечение, бензодиазепины, Лорафен.
Для цитирования: Воробьева О.В. Пути повышения эффективности терапии тревожных расстройств в клинике нервных болезней. Психиатрия и психофармакотерапия. 2018; 20 (2): 10–15.
Ключевые слова: тревожные расстройства, лечение, бензодиазепины, Лорафен.
Для цитирования: Воробьева О.В. Пути повышения эффективности терапии тревожных расстройств в клинике нервных болезней. Психиатрия и психофармакотерапия. 2018; 20 (2): 10–15.
Селективные ингибиторы обратного захвата серотонина (СИОЗС) большинством исследователей и врачей-практиков признаны препаратами первого выбора для лечения хронических тревожных расстройств. Приблизительно у 1/3 пациентов в первые недели лечения СИОЗС наблюдается усиление соматических симптомов тревоги, что потенциально ухудшает комплаентность. Дополнительное введение коротких курсов бензодиазепинов в инициальный период лечения СИОЗС тревожных расстройств дает ряд преимуществ: возможность быстрого достижения противотревожного эффекта, повышение комплаентности – и практически не влияет на тяжесть и спектр побочных эффектов проводимой терапии.
Ключевые слова: тревожные расстройства, лечение, бензодиазепины, Лорафен.
Для цитирования: Воробьева О.В. Пути повышения эффективности терапии тревожных расстройств в клинике нервных болезней. Психиатрия и психофармакотерапия. 2018; 20 (2): 10–15.
I.M.Sechenov First Moscow State Medical University of the Ministry of Health of the Russian Federation. 119991, Russian Federation, Moscow, ul. Trubetskaia, d. 8, str. 2ovvorobeva@mail.ru
Selective serotonin reuptake inhibitors (SSRI) are considered first line therapy of chronic anxiety disorders by the majority of both researchers and practicing physicians. But during the first weeks of treatment nearly one third of patients experience worsening of somatic symptoms of anxiety, which can potentially effect compliance. Short course of benzodiazepines added at the initial period of treatment of anxiety disorders with SSRI can be beneficial as it can help to achieve antianxiety effect faster, enhance compliance and has little to no effect on severity and range of side effects of the treatment.
Key words: anxiety disorders, treatment, benzodiazepines, Lorafen.
For citation: Vorobyeva O.V. Efficacy enhancement in treatment of anxiety disorders in neurology. Psychiatry and Psychopharmacotherapy. 2018; 20 (2): 10–15.
Клинически значимая тревога встречается у 5–7% в общей популяции и у 25% или более пациентов, наблюдающихся врачами общей практики. Заболеваемость в течение жизни тревожными расстройствами (ТР) может составлять свыше 30%. Грань между «нормальным» ответом на угрозу и патологическим ТР часто весьма размыта, и, возможно, существует континуум от личностного дистресса до психического расстройства. Именно с этим связаны трудности диагностики патологической тревоги, которая диагностируется в 2 раза реже, чем депрессия. Определенную помощь в диагностике патологической тревоги могут оказать надежные диагностические критерии ТР, изложенные в Международной классификации болезней 10-го пересмотра. Согласно современным классификациям психических расстройств ТР распределены в 8 дискретных категорий: паническое расстройство (ПР), генерализованное ТР (ГТР), агорафобия с ПР, обсессивно-компульсивное расстройство, социальная фобия, специфические фобии, посттравматическое стрессорное расстройство, острое стрессорное расстройство. Среди хронических форм тревоги ПР и ГТР наиболее часто диагностируются врачами общей практики. Любое из перечисленных ТР может протекать в субклинической форме.
 Врач-невролог в своей повседневной практике встречается с ТР, находящимися в разных причинно-следственных отношениях с основным (неврологическим) заболеванием. Можно выделить как минимум 4 такие категории:
Врач-невролог в своей повседневной практике встречается с ТР, находящимися в разных причинно-следственных отношениях с основным (неврологическим) заболеванием. Можно выделить как минимум 4 такие категории:
• Острая тревога как реакция на стрессорное жизненное событие.
• Первичная патологическая тревога, проявляющаяся «неврологическими» знаками и симптомами (тревога проявляется симптомами, имитирующими неврологическое заболевание).
• ТР, коморбидное с текущим неврологическим заболеванием, или смешанное тревожно-депрессивное расстройство, коморбидное с текущим неврологическим заболеванием.
• Лекарственно индуцированная тревога, возникшая в результате терапии основного заболевания.
ГТР обычно возникает, как правило, до 40 лет (наиболее типичное начало между подростковым возрастом и третьим десятилетием жизни), течет хронически годами с выраженной флуктуацией симптомов. Женщины заболевают ГТР в два и более раз чаще, чем мужчины. Основным проявлением заболевания является чрезмерная тревога или беспокойство по поводу обыденных событий, которые пациент не может контролировать. Тревога ассоциирована с тремя или более из представленных ниже симптомов (табл. 1).
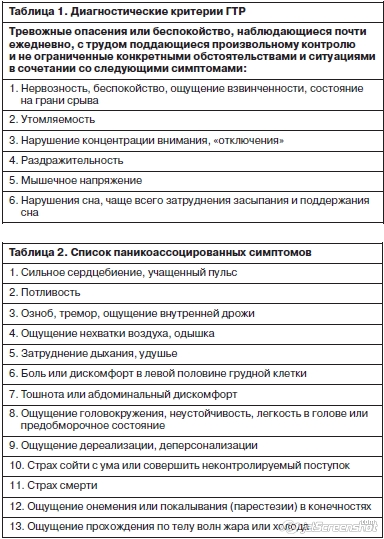 Кроме того, неограниченно могут быть представлены неспецифические симптомы тревоги: вегетативные (головокружение, тахикардия, эпигастральный дискомфорт, сухость во рту, потливость и др.); мрачные предчувствия (беспокойство о будущем, предчувствие «конца», трудности концентрации); моторное напряжение (двигательное беспокойство, суетливость, невозможность расслабиться, головные боли напряжения, озноб). Именно неспецифические соматические (вегетативные) симптомы часто становятся ведущими жалобами больных с ГТР, что объясняет принятые ранее термины «вегетативная дистония», «нейроциркуляторная дистония». Ранее ГТР большинством экспертов рассматривалось как мягкое расстройство, которое достигает клинической значимости только в случае коморбидности с депрессией. Но увеличение фактов, свидетельствующих о нарушении социальной и профессиональной адаптации больных с ГТР, заставляет более серьезно относиться к этому заболеванию.
Кроме того, неограниченно могут быть представлены неспецифические симптомы тревоги: вегетативные (головокружение, тахикардия, эпигастральный дискомфорт, сухость во рту, потливость и др.); мрачные предчувствия (беспокойство о будущем, предчувствие «конца», трудности концентрации); моторное напряжение (двигательное беспокойство, суетливость, невозможность расслабиться, головные боли напряжения, озноб). Именно неспецифические соматические (вегетативные) симптомы часто становятся ведущими жалобами больных с ГТР, что объясняет принятые ранее термины «вегетативная дистония», «нейроциркуляторная дистония». Ранее ГТР большинством экспертов рассматривалось как мягкое расстройство, которое достигает клинической значимости только в случае коморбидности с депрессией. Но увеличение фактов, свидетельствующих о нарушении социальной и профессиональной адаптации больных с ГТР, заставляет более серьезно относиться к этому заболеванию.
ПР – крайне распространенное, склонное к хронизации заболевание, манифестирующее в молодом, социально активном возрасте. Распространенность ПР, по данным эпидемиологических исследований, составляет 1,9–3,6% [1]. ПР в 2–3 раза чаще наблюдается у женщин. Основным проявлением ПР являются повторяющиеся пароксизмы тревоги (ПА). ПА представляет собой необъяснимый мучительный для больного приступ страха или тревоги в сочетании с различными вегетативными (соматическими) симптомами. В отечественной литературе долгое время использовался термин «вегетативный криз», отражающий представления о первичности дисфункции вегетативной нервной системы.
Диагностика ПА основывается на определенных клинических критериях. ПА характеризуется пароксизмальным страхом (часто сопровождающимся чувством неминуемой гибели) или тревогой и/или ощущением внутреннего напряжения в сочетании с 4 или более из списка паникоассоциированных симптомов (табл. 2).
Интенсивность основного критерия ПА – пароксизмальной тревоги – может варьировать в широких пределах от выраженного аффекта паники до ощущения внутреннего напряжения. В последнем случае, когда на первый план выступает вегетативная составляющая, говорят о «нестраховой» ПА или о «панике без паники». Атаки, обедненные эмоциональными проявлениями, чаще встречаются в терапевтической и неврологической практике. Паникоассоциированные симптомы развиваются внезапно и достигают своего пика в течение 10 мин. Послеприступный период характеризуется общей слабостью, разбитостью.
ПР имеет особый стереотип становления и развития симптоматики. Первые атаки оставляют неизгладимый след в памяти больного, что ведет к появлению синдрома тревоги «ожидания» приступа, который, в свою очередь, закрепляет повторяемость атак. Повторение атак в сходных ситуациях (в транспорте, пребывании в толпе и т.д.) способствует формированию ограничительного поведения, т.е. избегания потенциально опасных для развития ПА мест и ситуаций. Трактовка пациентом ПА как проявления какого-либо соматического заболевания приводит к частым посещениям врача, консультациям у специалистов разного профиля, неоправданным диагностическим исследованиям и создает у пациента впечатление о сложности и уникальности его заболевания. Неверные представления пациента о сути заболевания ведут к появлению ипохондрических симптомов, способствующих утяжелению течения болезни.
Коморбидность ПР психопатологическим синдромам имеет тенденцию нарастать по мере длительности заболевания. Лидирующее положение по коморбидности с ПР занимают агорафобия, депрессия, генерализованная тревога. Многими исследователями доказано, что при сочетании ПР и ГТР оба заболевания проявляются в более тяжелой форме, взаимно отягощают прогноз и снижают вероятность ремиссии.
Клиническая манифестация тревожных симптомов часто не удовлетворяет критериям очерченного ТР и представляет собой рекуррентную группу симптомов с меньшей длительностью и выраженностью, чем это требуется для синдромальной классификации. Эти субсиндромально выраженные тревожные нарушения наиболее трудны для диагностики и в связи с этим часто остаются нелечеными.
Коморбидное ТР независимо от степени выраженности оказывает существенное негативное влияние на течение основного (неврологического) заболевания. Например, тревога может привести к учащению эпилептических припадков или срыву лекарственной ремиссии, удлинить период реабилитации у пациентов, перенесших инсульт. Мягкие ТР соответствуют синдромальным по продолжительности, но включают меньшее количество (от 2 до 4) тревожных симптомов или более 4 симптомов, незначительная выраженность (тяжесть) которых не удовлетворяет полностью диагностическим критериям. Изучение качества жизни у пациентов, страдающих субсиндромальной или мягкой тревогой, показало, что по параметрам профессиональной и социальной активности снижение качества жизни у них сопоставимо с пациентами, имеющими развернутое ТР, и значительно хуже, чем у лиц, имеющих хроническое заболевание, не осложненное психопатологическими синдромами [2].
Хорошо известно, что отмена алкоголя вызывает тревогу и ажитацию. Многие патологические тревожные симптомы дебютируют в период абстиненции. Симптомы отмены седативных и снотворных препаратов близки по патогенезу и клиническим проявлениям к симптомам отмены алкоголя, но часто недооцениваются клиницистами как потенциальная причина тревоги. Оба эти состояния характеризуются следующими тревожными симптомами: нервозность, тахикардия, дрожь, потливость и тошнота.
 ТР диагностируются лишь у 50% пациентов с очевидными симптомами [4]. Меньше чем 50% пациентов получают какое-либо лечение и меньше 30% – адекватную терапию. Мягкие и субпороговые ТР часто вообще не рассматриваются как мишень для лечения. Вероятность лечения повышается по мере утяжеления симптоматики (табл. 3).
ТР диагностируются лишь у 50% пациентов с очевидными симптомами [4]. Меньше чем 50% пациентов получают какое-либо лечение и меньше 30% – адекватную терапию. Мягкие и субпороговые ТР часто вообще не рассматриваются как мишень для лечения. Вероятность лечения повышается по мере утяжеления симптоматики (табл. 3).
В то же время неадекватное лечение депрессии может спровоцировать появление тревоги как симптома частично леченной депрессии. ТР, являющееся остаточным проявлением леченой депрессии, большинством экспертов рассматривается как индикатор повышенного риска рекуррентной депрессии.
Несмотря на облигатность вегетативной дисфункции и часто маскированный характер эмоциональных расстройств, базовым методом лечения тревоги является психофармакологическое лечение. Терапевтическую стратегию необходимо выстраивать в зависимости от типа доминирующего расстройства и степени его выраженности. Выбор препарата зависит от степени выраженности уровня тревоги и длительности заболевания.
Лекарственные препараты, успешно используемые для лечения тревоги, воздействуют на различные нейротрансмиттеры, в частности на серотонин, норадреналин, g-аминомасляную кислоту (ГАМК). Спектр противотревожных препаратов чрезвычайно широк: транквилизаторы (бензодиазепиновые и небензодиазепиновые), седативные растительные сборы и, наконец, антидепрессанты (табл. 4). Так называемые вегетотропные и сосудисто-метаболические препараты, ранее широко используемые для коррекции вегетативных нарушений, в настоящее время практически не используются в силу низкой эффективности (не превышает плацебо-эффекта). Антидепрессанты успешно используются для лечения пароксизмальной тревоги (ПА) с 1960-годов.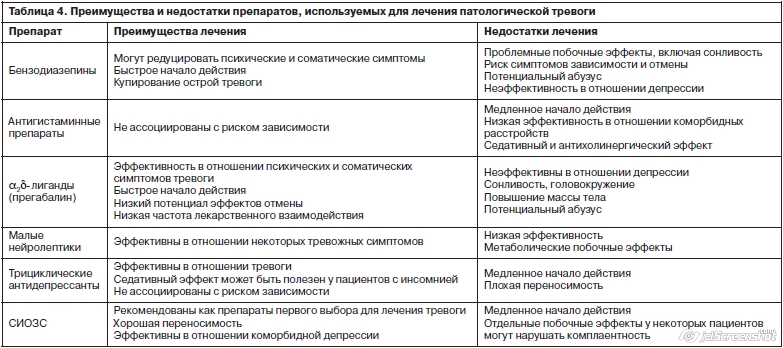
Но уже в 1990-е годы стало понятно, что независимо от типа хронической тревоги антидепрессанты эффективно купируют тревогу и демонстрируют лучший катамнестический результат, чем транквилизаторы. С появлением новых групп антидепрессантов – СИОЗС – началось интенсивное внедрение этих средств в лечение тревоги. В настоящее время СИОЗС большинством исследователей и врачей-практиков признаны препаратами первой очереди выбора для лечения хронических ТР. Это положение базируется на несомненной антитревожной эффективности и хорошей переносимости препаратов этой группы.
Однако отставленность развития анксиолитического эффекта не позволяет использовать антидепрессанты для купирования острой тревоги.
Основным преимуществом бензодиазепиновых транквилизаторов являются быстрое развитие и значительная выраженность противотревожного эффекта. Данное преимущество высоко востребовано для лечения острой тревоги (реакция горя, утраты). Наиболее полезными считаются препараты, обладающие высоким сродством к бензодиазепиновым рецепторам (высокопотенциальные бензодиазепины). Таким образом, препаратами первого выбора для лечения острой тревоги остаются диазепам и лоразепам. Существенной проблемой в использовании бензодиазепинов является развитие привыкания и зависимости. Поскольку эти побочные эффекты существенным образом зависят от дозы, длительности приема, последнее время наметилась отчетливая тенденция в использовании низких дозировок и коротких курсов терапии, которые обычно не превышают 4 нед. Короткие сроки лечения в большинстве случаев способны купировать «острую» тревогу.
Для лечения хронической тревоги препаратами первой линии являются СИОЗС. Основной недостаток антидепрессантов – это отставленность во времени их анксиолитической эффективности. Первое улучшение обычно наступает спустя как минимум 10 дней от начала лечения, а полный терапевтический ответ может проявиться спустя 3–4 нед. Приблизительно у 1/3 пациентов в первые недели лечения наблюдается усиление соматических симптомов тревоги. Хотя большинство антидепрессантов при длительных курсах демонстрируют выраженный анксиолитический эффект, при краткосрочном приеме любой представитель этого класса, напротив, может усилить тревогу. Пациенты с ТР часто оказываются гиперсенситивны к малейшему нарастанию уровня тревоги, а также к соматическим ощущениям, вызванным побочными эффектами антидепрессантов. Именно с этими свойствами антидепрессантов связано возможное усугубление тревоги в инициальный период лечения. Задержка во времени улучшения крайне неприятна для пациентов, ищущих непосредственного облегчения своему страданию. Неоправданные ожидания могут повлечь отказ пациента от применения лекарства.
В этот ответственный период лечения пациент особенно нуждается в психологической поддержке врача, а иногда и в применении дополнительных противотревожных лекарственных препаратов. Такими корректорами могут быть анксиолитики бензодиазепинового ряда. Главная задача врача – не допустить отказа от применения антидепрессантов на начальном этапе лечения. Низкие инициальные дозы антидепрессантов и медленное наращивание до полной терапевтической дозы, а также дополнительное использование анксиолитиков бензодиазепинового ряда позволяют минимизировать побочные эффекты и улучшить комплаентность.
Комбинированная терапия с включением бензодиазепиновых анксиолитиков может существенно повысить общую эффективность лечения хронических ТР. Это положение иллюстрирует проведенное нами открытое сравнительное исследование по оценке эффективности пароксетина в монотерапии и при сочетании пароксетина с лоразепамом у пациентов, страдающих ПР [6]. Исследуемую группу составили 32 пациента (7 мужчин; 25 женщин). Ведущей жалобой были приступы, клиническая структура которых позволяла квалифицировать их как ПА. Длительность заболевания варьировала от 1,5 до 8 лет (в среднем 3,45±0,87), длительность обострения, послужившего поводом для назначения настоящего лечения, составила в среднем 3,57±1,2 мес. Пациенты были случайным образом разделены в 2 группы:
• 14 человек принимали монотерапию пароксетином в течение 12 нед в дозе 20 мг/сут;
• 18 человек в течение первых 4 нед принимали сочетанную терапию (пароксетин 20 мг/сут + лоразепам 2,5 мг/сут), а затем продолжали прием только пароксетина до 12 нед.
Лоразепам (Лорафен) – яркий представитель высокопотенциальных бензодиазепинов, обладающий мощным противотревожным эффектом. Применение лоразепама в инициальном периоде лечения не только нивелирует негативные эффекты антидепрессантов, но и имеет самостоятельное патогенетическое значение. Одним из патогенетических звеньев развития острой и хронической тревоги является нарушение функционирования ГАМКергической медиации, что подтверждается дефицитарностью ГАМК-нейронального ответа на введение бензодиазепиновых препаратов у пациентов, страдающих ПР [7] и высокой эффективностью этих препаратов в купировании паники.
Анализ сравнительной понедельной динамики антипанической эффективности изучаемых схем лечения выявил значимые различия, касающиеся первых недель лечения. Если в 1-й группе (пароксетин) значимое снижение суммарной частоты ПА по сравнению с фоновым показателем (9,6±0,22) происходило на 3-й неделе лечения (4,1±0,37; р<0,05), то во 2-й группе (пароксетин + лоразепам) уже на 1-й неделе лечения отмечался значимый эффект лечения и количество атак сократилось более чем вдвое (10,4±0,24 против 4,7±0,21; р<0,05). На 14-й день лечения ПА полностью редуцировали у 8 (44%) пациентов, получавших сочетанную терапию пароксетин + лоразепам, ни у одного пациента в группе монотерапии пароксетином мы не наблюдали полной редукции ПА (р<0,05).
Следовательно, добавление лоразепама обеспечивает быстрый регресс ПА, главного симптома заболевания. Переносимость лечения при сочетанном использовании антидепрессанта с бензодиазепином оказалась выше, чем при монотерапии. Все пациенты в группе терапии пароксетин + лоразепам полностью прошли 12-недельный курс лечения. Среди пациентов, получавших только пароксетин, 4 (22%) человека отказались от приема препарата в инициальный период лечения (первые 2 нед), в дальнейшем они исключались из анализа. Основной причиной отказа служили неэффективность терапии и появление на фоне терапии «новых симптомов» болезни. В целом побочные явления наблюдались у 4 (22%) пациентов, получавших сочетанную терапию, и у 4 (29%) пациентов, получавших монотерапию. Ни у одного пациента мы не наблюдали ни ухудшения клинической картины после отмены лоразепама, ни обострения тревожных симптомов. Отсутствие синдрома отмены, вероятно, связано с эффектами пароксетина, который продолжали получать пациенты. Таким образом, добавление лоразепама к терапии антидепрессантами в инициальном периоде лечения ПР способствует более быстрому регрессу ПА, тревоги ожидания, лучшим показателям комплаентности.
Использование коротких курсов бензодиазепинов («бензодиазепиновый мост») в инициальном периоде лечения полностью отвечает требованиям Всемирной организации здравоохранения по срокам применения этих препаратов, а именно длительность лечения должна составлять 2–4 нед и не должна превышать 1–2 мес. Постепенная отмена бензодиазепинового препарата под «прикрытием» антидепрессанта из группы СИОЗС обеспечивает снижение риска развития синдрома отмены. Следовательно, «бензодиазепиновый мост» дает ряд преимуществ: возможность быстрого достижения противотревожного эффекта, повышение комплаентности – и практически не влияет на тяжесть и спектр побочных эффектов проводимой терапии. Кратковременное добавление лоразепама в инициальном периоде лечения может с успехом использоваться у большинства пациентов, страдающих хроническими ТР.
Сведения об авторе
Воробьева Ольга Владимировна – д-р мед. наук, проф. каф. нервных болезней ИПО ФГАОУ ВО «Первый МГМУ им. И.М.Сеченова». E-mail: ovvorobeva@mail.ru
Ключевые слова: тревожные расстройства, лечение, бензодиазепины, Лорафен.
Для цитирования: Воробьева О.В. Пути повышения эффективности терапии тревожных расстройств в клинике нервных болезней. Психиатрия и психофармакотерапия. 2018; 20 (2): 10–15.
Efficacy enhancement in treatment of anxiety disorders in neurology
O.V.VorobyevaI.M.Sechenov First Moscow State Medical University of the Ministry of Health of the Russian Federation. 119991, Russian Federation, Moscow, ul. Trubetskaia, d. 8, str. 2ovvorobeva@mail.ru
Selective serotonin reuptake inhibitors (SSRI) are considered first line therapy of chronic anxiety disorders by the majority of both researchers and practicing physicians. But during the first weeks of treatment nearly one third of patients experience worsening of somatic symptoms of anxiety, which can potentially effect compliance. Short course of benzodiazepines added at the initial period of treatment of anxiety disorders with SSRI can be beneficial as it can help to achieve antianxiety effect faster, enhance compliance and has little to no effect on severity and range of side effects of the treatment.
Key words: anxiety disorders, treatment, benzodiazepines, Lorafen.
For citation: Vorobyeva O.V. Efficacy enhancement in treatment of anxiety disorders in neurology. Psychiatry and Psychopharmacotherapy. 2018; 20 (2): 10–15.
Клинически значимая тревога встречается у 5–7% в общей популяции и у 25% или более пациентов, наблюдающихся врачами общей практики. Заболеваемость в течение жизни тревожными расстройствами (ТР) может составлять свыше 30%. Грань между «нормальным» ответом на угрозу и патологическим ТР часто весьма размыта, и, возможно, существует континуум от личностного дистресса до психического расстройства. Именно с этим связаны трудности диагностики патологической тревоги, которая диагностируется в 2 раза реже, чем депрессия. Определенную помощь в диагностике патологической тревоги могут оказать надежные диагностические критерии ТР, изложенные в Международной классификации болезней 10-го пересмотра. Согласно современным классификациям психических расстройств ТР распределены в 8 дискретных категорий: паническое расстройство (ПР), генерализованное ТР (ГТР), агорафобия с ПР, обсессивно-компульсивное расстройство, социальная фобия, специфические фобии, посттравматическое стрессорное расстройство, острое стрессорное расстройство. Среди хронических форм тревоги ПР и ГТР наиболее часто диагностируются врачами общей практики. Любое из перечисленных ТР может протекать в субклинической форме.
 Врач-невролог в своей повседневной практике встречается с ТР, находящимися в разных причинно-следственных отношениях с основным (неврологическим) заболеванием. Можно выделить как минимум 4 такие категории:
Врач-невролог в своей повседневной практике встречается с ТР, находящимися в разных причинно-следственных отношениях с основным (неврологическим) заболеванием. Можно выделить как минимум 4 такие категории:• Острая тревога как реакция на стрессорное жизненное событие.
• Первичная патологическая тревога, проявляющаяся «неврологическими» знаками и симптомами (тревога проявляется симптомами, имитирующими неврологическое заболевание).
• ТР, коморбидное с текущим неврологическим заболеванием, или смешанное тревожно-депрессивное расстройство, коморбидное с текущим неврологическим заболеванием.
• Лекарственно индуцированная тревога, возникшая в результате терапии основного заболевания.
Острая тревога
Острая тревога – наиболее узнаваемое состояние как для клинициста, так и для пациента. Пациенты видят причину нарушения своего состояния в пережитом негативном событии. Последствием болезненных симптомов является социальная дезадаптация. Чаще всего дезадаптация характеризуется тревожным настроением, ощущением неспособности справиться с ситуацией и даже снижением способности функционировать в повседневной жизни. Тревожность проявляется диффузным, крайне неприятным, часто неопределенным ощущением опасения чего-то, угрозы, чувством напряжения, повышенной раздражительностью, плаксивостью. В то же время тревога у этой категории пациентов может проявляться конкретными страхами, в первую очередь опасениями по поводу собственного здоровья.Первичная хроническая тревога
Пациенты, страдающие первичной хронической тревогой, наблюдаются врачами-неврологами чаще всего с диагнозами: вегетативная дистония, нейроциркуляторная дистония, вегетативные кризы, симпатоадреналовые кризы. Для категории пациентов, обращающихся к неврологу, характерно жаловаться на «соматические» симптомы тревоги, которые являются в большинстве своем следствием активации симпатического отдела вегетативной нервной системы. Психические симптомы могут не осознаваться больным или расцениваться как нормальная реакция на «непонятное» болезненное состояние. Только активный расспрос пациентов позволяет выявить наряду с вегетативной дисфункцией психические тревожные симптомы. Наиболее часто в поле зрения невролога попадают пациенты, страдающие ГТР и паническими атаками (ПА).ГТР обычно возникает, как правило, до 40 лет (наиболее типичное начало между подростковым возрастом и третьим десятилетием жизни), течет хронически годами с выраженной флуктуацией симптомов. Женщины заболевают ГТР в два и более раз чаще, чем мужчины. Основным проявлением заболевания является чрезмерная тревога или беспокойство по поводу обыденных событий, которые пациент не может контролировать. Тревога ассоциирована с тремя или более из представленных ниже симптомов (табл. 1).
 Кроме того, неограниченно могут быть представлены неспецифические симптомы тревоги: вегетативные (головокружение, тахикардия, эпигастральный дискомфорт, сухость во рту, потливость и др.); мрачные предчувствия (беспокойство о будущем, предчувствие «конца», трудности концентрации); моторное напряжение (двигательное беспокойство, суетливость, невозможность расслабиться, головные боли напряжения, озноб). Именно неспецифические соматические (вегетативные) симптомы часто становятся ведущими жалобами больных с ГТР, что объясняет принятые ранее термины «вегетативная дистония», «нейроциркуляторная дистония». Ранее ГТР большинством экспертов рассматривалось как мягкое расстройство, которое достигает клинической значимости только в случае коморбидности с депрессией. Но увеличение фактов, свидетельствующих о нарушении социальной и профессиональной адаптации больных с ГТР, заставляет более серьезно относиться к этому заболеванию.
Кроме того, неограниченно могут быть представлены неспецифические симптомы тревоги: вегетативные (головокружение, тахикардия, эпигастральный дискомфорт, сухость во рту, потливость и др.); мрачные предчувствия (беспокойство о будущем, предчувствие «конца», трудности концентрации); моторное напряжение (двигательное беспокойство, суетливость, невозможность расслабиться, головные боли напряжения, озноб). Именно неспецифические соматические (вегетативные) симптомы часто становятся ведущими жалобами больных с ГТР, что объясняет принятые ранее термины «вегетативная дистония», «нейроциркуляторная дистония». Ранее ГТР большинством экспертов рассматривалось как мягкое расстройство, которое достигает клинической значимости только в случае коморбидности с депрессией. Но увеличение фактов, свидетельствующих о нарушении социальной и профессиональной адаптации больных с ГТР, заставляет более серьезно относиться к этому заболеванию.ПР – крайне распространенное, склонное к хронизации заболевание, манифестирующее в молодом, социально активном возрасте. Распространенность ПР, по данным эпидемиологических исследований, составляет 1,9–3,6% [1]. ПР в 2–3 раза чаще наблюдается у женщин. Основным проявлением ПР являются повторяющиеся пароксизмы тревоги (ПА). ПА представляет собой необъяснимый мучительный для больного приступ страха или тревоги в сочетании с различными вегетативными (соматическими) симптомами. В отечественной литературе долгое время использовался термин «вегетативный криз», отражающий представления о первичности дисфункции вегетативной нервной системы.
Диагностика ПА основывается на определенных клинических критериях. ПА характеризуется пароксизмальным страхом (часто сопровождающимся чувством неминуемой гибели) или тревогой и/или ощущением внутреннего напряжения в сочетании с 4 или более из списка паникоассоциированных симптомов (табл. 2).
Интенсивность основного критерия ПА – пароксизмальной тревоги – может варьировать в широких пределах от выраженного аффекта паники до ощущения внутреннего напряжения. В последнем случае, когда на первый план выступает вегетативная составляющая, говорят о «нестраховой» ПА или о «панике без паники». Атаки, обедненные эмоциональными проявлениями, чаще встречаются в терапевтической и неврологической практике. Паникоассоциированные симптомы развиваются внезапно и достигают своего пика в течение 10 мин. Послеприступный период характеризуется общей слабостью, разбитостью.
ПР имеет особый стереотип становления и развития симптоматики. Первые атаки оставляют неизгладимый след в памяти больного, что ведет к появлению синдрома тревоги «ожидания» приступа, который, в свою очередь, закрепляет повторяемость атак. Повторение атак в сходных ситуациях (в транспорте, пребывании в толпе и т.д.) способствует формированию ограничительного поведения, т.е. избегания потенциально опасных для развития ПА мест и ситуаций. Трактовка пациентом ПА как проявления какого-либо соматического заболевания приводит к частым посещениям врача, консультациям у специалистов разного профиля, неоправданным диагностическим исследованиям и создает у пациента впечатление о сложности и уникальности его заболевания. Неверные представления пациента о сути заболевания ведут к появлению ипохондрических симптомов, способствующих утяжелению течения болезни.
Коморбидность ПР психопатологическим синдромам имеет тенденцию нарастать по мере длительности заболевания. Лидирующее положение по коморбидности с ПР занимают агорафобия, депрессия, генерализованная тревога. Многими исследователями доказано, что при сочетании ПР и ГТР оба заболевания проявляются в более тяжелой форме, взаимно отягощают прогноз и снижают вероятность ремиссии.
ТР, коморбидное с текущим неврологическим заболеванием
ТР у пациентов с коморбидным неврологическим или соматическим заболеванием может проявляться разными симптомами, которые описаны при первичной патологической тревоге. Тревога особенно часто ассоциирована со следующими хроническими неврологическими заболеваниями: эпилепсия, инсульт, дисциркуляторная энцефалопатия, рассеянный склероз, хронические болевые синдромы, мигрень, болезнь Паркинсона и другие дегенеративные заболевания. Необходимость дифференцировать многие соматические симптомы тревоги от симптомов соматического или неврологического заболевания в некоторых случаях становится значительной проблемой. Тревожные симптомы могут быть ошибочно расценены как признаки неврологического заболевания, что часто влечет за собой необоснованную терапию.Клиническая манифестация тревожных симптомов часто не удовлетворяет критериям очерченного ТР и представляет собой рекуррентную группу симптомов с меньшей длительностью и выраженностью, чем это требуется для синдромальной классификации. Эти субсиндромально выраженные тревожные нарушения наиболее трудны для диагностики и в связи с этим часто остаются нелечеными.
Коморбидное ТР независимо от степени выраженности оказывает существенное негативное влияние на течение основного (неврологического) заболевания. Например, тревога может привести к учащению эпилептических припадков или срыву лекарственной ремиссии, удлинить период реабилитации у пациентов, перенесших инсульт. Мягкие ТР соответствуют синдромальным по продолжительности, но включают меньшее количество (от 2 до 4) тревожных симптомов или более 4 симптомов, незначительная выраженность (тяжесть) которых не удовлетворяет полностью диагностическим критериям. Изучение качества жизни у пациентов, страдающих субсиндромальной или мягкой тревогой, показало, что по параметрам профессиональной и социальной активности снижение качества жизни у них сопоставимо с пациентами, имеющими развернутое ТР, и значительно хуже, чем у лиц, имеющих хроническое заболевание, не осложненное психопатологическими синдромами [2].
Лекарственно индуцированная тревога
Многие лекарственные препараты и другие химические субстанции могут стать причиной тревожных симптомов. Чрезмерное употребление кофеина или резкое прекращение его употребления вызывает значимые тревожные симптомы [3]. Различные рецепторные медикаменты вызывают манифестацию тревоги, что трактуется как побочный эффект препарата. Способностью вызывать тревогу обладают: адренергические агонисты, бронходилататоры, кортикостероиды, препараты, влияющие на функцию щитовидной железы, антигипертензивные препараты, кардиоваскулярные препараты, особенно дериваты дигиталиса. Психотропные препараты, такие как нейролептики и реже селективные ингибиторы обратного захвата серотонина (СИОЗС), могут быть причиной акатизии, которая ассоциирована с тревогой. Все антидепрессанты при длительном использовании демонстрируют противотревожный эффект. Однако в инициальном периоде лечения все антидепрессанты без исключения могут индуцировать тревогу, что во многих случаях является причиной отказа пациента от терапии. Комбинация антидепрессанта с противотревожным препаратом на инициальный период лечения делает терапию в целом более успешной.Хорошо известно, что отмена алкоголя вызывает тревогу и ажитацию. Многие патологические тревожные симптомы дебютируют в период абстиненции. Симптомы отмены седативных и снотворных препаратов близки по патогенезу и клиническим проявлениям к симптомам отмены алкоголя, но часто недооцениваются клиницистами как потенциальная причина тревоги. Оба эти состояния характеризуются следующими тревожными симптомами: нервозность, тахикардия, дрожь, потливость и тошнота.
Принципы терапии ТР
 ТР диагностируются лишь у 50% пациентов с очевидными симптомами [4]. Меньше чем 50% пациентов получают какое-либо лечение и меньше 30% – адекватную терапию. Мягкие и субпороговые ТР часто вообще не рассматриваются как мишень для лечения. Вероятность лечения повышается по мере утяжеления симптоматики (табл. 3).
ТР диагностируются лишь у 50% пациентов с очевидными симптомами [4]. Меньше чем 50% пациентов получают какое-либо лечение и меньше 30% – адекватную терапию. Мягкие и субпороговые ТР часто вообще не рассматриваются как мишень для лечения. Вероятность лечения повышается по мере утяжеления симптоматики (табл. 3). В то же время неадекватное лечение депрессии может спровоцировать появление тревоги как симптома частично леченной депрессии. ТР, являющееся остаточным проявлением леченой депрессии, большинством экспертов рассматривается как индикатор повышенного риска рекуррентной депрессии.
Несмотря на облигатность вегетативной дисфункции и часто маскированный характер эмоциональных расстройств, базовым методом лечения тревоги является психофармакологическое лечение. Терапевтическую стратегию необходимо выстраивать в зависимости от типа доминирующего расстройства и степени его выраженности. Выбор препарата зависит от степени выраженности уровня тревоги и длительности заболевания.
Лекарственные препараты, успешно используемые для лечения тревоги, воздействуют на различные нейротрансмиттеры, в частности на серотонин, норадреналин, g-аминомасляную кислоту (ГАМК). Спектр противотревожных препаратов чрезвычайно широк: транквилизаторы (бензодиазепиновые и небензодиазепиновые), седативные растительные сборы и, наконец, антидепрессанты (табл. 4). Так называемые вегетотропные и сосудисто-метаболические препараты, ранее широко используемые для коррекции вегетативных нарушений, в настоящее время практически не используются в силу низкой эффективности (не превышает плацебо-эффекта). Антидепрессанты успешно используются для лечения пароксизмальной тревоги (ПА) с 1960-годов.

Но уже в 1990-е годы стало понятно, что независимо от типа хронической тревоги антидепрессанты эффективно купируют тревогу и демонстрируют лучший катамнестический результат, чем транквилизаторы. С появлением новых групп антидепрессантов – СИОЗС – началось интенсивное внедрение этих средств в лечение тревоги. В настоящее время СИОЗС большинством исследователей и врачей-практиков признаны препаратами первой очереди выбора для лечения хронических ТР. Это положение базируется на несомненной антитревожной эффективности и хорошей переносимости препаратов этой группы.
Однако отставленность развития анксиолитического эффекта не позволяет использовать антидепрессанты для купирования острой тревоги.
Основным преимуществом бензодиазепиновых транквилизаторов являются быстрое развитие и значительная выраженность противотревожного эффекта. Данное преимущество высоко востребовано для лечения острой тревоги (реакция горя, утраты). Наиболее полезными считаются препараты, обладающие высоким сродством к бензодиазепиновым рецепторам (высокопотенциальные бензодиазепины). Таким образом, препаратами первого выбора для лечения острой тревоги остаются диазепам и лоразепам. Существенной проблемой в использовании бензодиазепинов является развитие привыкания и зависимости. Поскольку эти побочные эффекты существенным образом зависят от дозы, длительности приема, последнее время наметилась отчетливая тенденция в использовании низких дозировок и коротких курсов терапии, которые обычно не превышают 4 нед. Короткие сроки лечения в большинстве случаев способны купировать «острую» тревогу.
Для лечения хронической тревоги препаратами первой линии являются СИОЗС. Основной недостаток антидепрессантов – это отставленность во времени их анксиолитической эффективности. Первое улучшение обычно наступает спустя как минимум 10 дней от начала лечения, а полный терапевтический ответ может проявиться спустя 3–4 нед. Приблизительно у 1/3 пациентов в первые недели лечения наблюдается усиление соматических симптомов тревоги. Хотя большинство антидепрессантов при длительных курсах демонстрируют выраженный анксиолитический эффект, при краткосрочном приеме любой представитель этого класса, напротив, может усилить тревогу. Пациенты с ТР часто оказываются гиперсенситивны к малейшему нарастанию уровня тревоги, а также к соматическим ощущениям, вызванным побочными эффектами антидепрессантов. Именно с этими свойствами антидепрессантов связано возможное усугубление тревоги в инициальный период лечения. Задержка во времени улучшения крайне неприятна для пациентов, ищущих непосредственного облегчения своему страданию. Неоправданные ожидания могут повлечь отказ пациента от применения лекарства.
В этот ответственный период лечения пациент особенно нуждается в психологической поддержке врача, а иногда и в применении дополнительных противотревожных лекарственных препаратов. Такими корректорами могут быть анксиолитики бензодиазепинового ряда. Главная задача врача – не допустить отказа от применения антидепрессантов на начальном этапе лечения. Низкие инициальные дозы антидепрессантов и медленное наращивание до полной терапевтической дозы, а также дополнительное использование анксиолитиков бензодиазепинового ряда позволяют минимизировать побочные эффекты и улучшить комплаентность.
Комбинированная терапия с включением бензодиазепиновых анксиолитиков может существенно повысить общую эффективность лечения хронических ТР. Это положение иллюстрирует проведенное нами открытое сравнительное исследование по оценке эффективности пароксетина в монотерапии и при сочетании пароксетина с лоразепамом у пациентов, страдающих ПР [6]. Исследуемую группу составили 32 пациента (7 мужчин; 25 женщин). Ведущей жалобой были приступы, клиническая структура которых позволяла квалифицировать их как ПА. Длительность заболевания варьировала от 1,5 до 8 лет (в среднем 3,45±0,87), длительность обострения, послужившего поводом для назначения настоящего лечения, составила в среднем 3,57±1,2 мес. Пациенты были случайным образом разделены в 2 группы:
• 14 человек принимали монотерапию пароксетином в течение 12 нед в дозе 20 мг/сут;
• 18 человек в течение первых 4 нед принимали сочетанную терапию (пароксетин 20 мг/сут + лоразепам 2,5 мг/сут), а затем продолжали прием только пароксетина до 12 нед.
Лоразепам (Лорафен) – яркий представитель высокопотенциальных бензодиазепинов, обладающий мощным противотревожным эффектом. Применение лоразепама в инициальном периоде лечения не только нивелирует негативные эффекты антидепрессантов, но и имеет самостоятельное патогенетическое значение. Одним из патогенетических звеньев развития острой и хронической тревоги является нарушение функционирования ГАМКергической медиации, что подтверждается дефицитарностью ГАМК-нейронального ответа на введение бензодиазепиновых препаратов у пациентов, страдающих ПР [7] и высокой эффективностью этих препаратов в купировании паники.
Анализ сравнительной понедельной динамики антипанической эффективности изучаемых схем лечения выявил значимые различия, касающиеся первых недель лечения. Если в 1-й группе (пароксетин) значимое снижение суммарной частоты ПА по сравнению с фоновым показателем (9,6±0,22) происходило на 3-й неделе лечения (4,1±0,37; р<0,05), то во 2-й группе (пароксетин + лоразепам) уже на 1-й неделе лечения отмечался значимый эффект лечения и количество атак сократилось более чем вдвое (10,4±0,24 против 4,7±0,21; р<0,05). На 14-й день лечения ПА полностью редуцировали у 8 (44%) пациентов, получавших сочетанную терапию пароксетин + лоразепам, ни у одного пациента в группе монотерапии пароксетином мы не наблюдали полной редукции ПА (р<0,05).
Следовательно, добавление лоразепама обеспечивает быстрый регресс ПА, главного симптома заболевания. Переносимость лечения при сочетанном использовании антидепрессанта с бензодиазепином оказалась выше, чем при монотерапии. Все пациенты в группе терапии пароксетин + лоразепам полностью прошли 12-недельный курс лечения. Среди пациентов, получавших только пароксетин, 4 (22%) человека отказались от приема препарата в инициальный период лечения (первые 2 нед), в дальнейшем они исключались из анализа. Основной причиной отказа служили неэффективность терапии и появление на фоне терапии «новых симптомов» болезни. В целом побочные явления наблюдались у 4 (22%) пациентов, получавших сочетанную терапию, и у 4 (29%) пациентов, получавших монотерапию. Ни у одного пациента мы не наблюдали ни ухудшения клинической картины после отмены лоразепама, ни обострения тревожных симптомов. Отсутствие синдрома отмены, вероятно, связано с эффектами пароксетина, который продолжали получать пациенты. Таким образом, добавление лоразепама к терапии антидепрессантами в инициальном периоде лечения ПР способствует более быстрому регрессу ПА, тревоги ожидания, лучшим показателям комплаентности.
Использование коротких курсов бензодиазепинов («бензодиазепиновый мост») в инициальном периоде лечения полностью отвечает требованиям Всемирной организации здравоохранения по срокам применения этих препаратов, а именно длительность лечения должна составлять 2–4 нед и не должна превышать 1–2 мес. Постепенная отмена бензодиазепинового препарата под «прикрытием» антидепрессанта из группы СИОЗС обеспечивает снижение риска развития синдрома отмены. Следовательно, «бензодиазепиновый мост» дает ряд преимуществ: возможность быстрого достижения противотревожного эффекта, повышение комплаентности – и практически не влияет на тяжесть и спектр побочных эффектов проводимой терапии. Кратковременное добавление лоразепама в инициальном периоде лечения может с успехом использоваться у большинства пациентов, страдающих хроническими ТР.
Сведения об авторе
Воробьева Ольга Владимировна – д-р мед. наук, проф. каф. нервных болезней ИПО ФГАОУ ВО «Первый МГМУ им. И.М.Сеченова». E-mail: ovvorobeva@mail.ru
Список исп. литературыСкрыть список1. Perking A, Witt hen HU. Epidemiologie von Angststorungen. In: Kaster S, Muller HJ, eds. Angst- und Panikerkrankung. Jena: Gustav Fischer Verlag, 1995; p. 137–56.
2. Katon W, Hollifield M, Chapman T et al. Infrequent panic attacks: psychiatric comorbidity, personal characterisitics and functional disability. J Psych Research 1995; 29: 121–31.
3. Bruce M, Scott N, Shine P, Lader M. Anxiogenic effects of caffeine in patients with anxiety disorders. Arch Gen Psychiatry 1992; 49: 867–9.
4. Sartorius N, Ustun TB, Lecrubier Y, Wittchen HU. Depression comorbid with anxiety: results from the WHO study on psychological disorders in primary health care. Br J Psychiatry 1996; 168: 38–43.
5. Bebbington PE et al. Neurotic disorders and the receipt of psychiatric treatment. Psychol Med 2000; 30: 1369–76.
6. Воробьева О.В. Преимущества дополнительного кратковременного введения бензодиазепиновых анксиолитиков в инициальный период лечения панического расстройства (открытое сравнительное исследование эффективности монотерапии панического расстройства пароксетином и сочетанной терапии пароксетином и лоразепамом в инициальном периоде лечения). Журн. неврологии и психиатрии им. С.С.Корсакова. 2006; 106 (11): 39–41. / Vorob'eva O.V. Preimushchestva dopolnitel'nogo kratkovremennogo vvedeniia benzodiazepinovykh anksiolitikov v initsial'nyi period lecheniia panicheskogo rasstroistva (otkrytoe sravnitel'noe issledovanie effektivnosti monoterapii panicheskogo rasstroistva paroksetinom i sochetannoi terapii paroksetinom i lorazepamom v initsial'nom periode lecheniia). Zhurn. nevrologii i psikhiatrii im. S.S.Korsakova. 2006; 106 (11): 39–41. [in Russian]
7. Goddard AW, Mason GF, Appel M et al. Impaired GABA neuronal response to acute benzodiazepine administration in panic disorder. Am J Psychiatry 2004; 161 (12): 2186–93.
10 апреля 2018
Количество просмотров: 2489

