Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№06 2018
Сравнительная эффективность современных антидепрессантов: данные сетевых метаанализов №06 2018
Номера страниц в выпуске:9-13
В статье сравниваются результаты двух метаанализов эффективности современных антидепрессантов. В обеих метааналитических работах получены сходные результаты высокой степени доказательности. В обоих метаанализах одним из наиболее эффективных и хорошо переносимых препаратов оказался агомелатин.
Ключевые слова: мета-анализ, антидепрессанты, агомелатин.
Для цитирования: Фролова В.И. Сравнительная эффективность современных антидепрессантов: данные сетевых метаанализов. Психиатрия и психофармакотерапия. 2018; 20 (6): 9–13.
Ключевые слова: мета-анализ, антидепрессанты, агомелатин.
Для цитирования: Фролова В.И. Сравнительная эффективность современных антидепрессантов: данные сетевых метаанализов. Психиатрия и психофармакотерапия. 2018; 20 (6): 9–13.
В статье сравниваются результаты двух метаанализов эффективности современных антидепрессантов. В обеих метааналитических работах получены сходные результаты высокой степени доказательности. В обоих метаанализах одним из наиболее эффективных и хорошо переносимых препаратов оказался агомелатин.
Ключевые слова: мета-анализ, антидепрессанты, агомелатин.
Для цитирования: Фролова В.И. Сравнительная эффективность современных антидепрессантов: данные сетевых метаанализов. Психиатрия и психофармакотерапия. 2018; 20 (6): 9–13.
People’s Friendship University of Russia. 117198, Russian Federation, Moscow, ul. Miklukho-Maklaya, d. 6 hifrol@mail.ru
In this article results of two meta-analyses of contemporary antidepressants’ efficacy are compared. Both meta-analyses represent results of high degree of evidence. According to both meta-analyses agomelatin is one of the most effective and well-tolerated modern antidepressant.
Key words: meta-analyses, antidepressants, agomelatin.
For citation: Frolova V.I. The comparative efficacy of contemporary antidepressants: data of network meta-analyse. Psychiatry and Psychopharmacotherapy. 2018; 20 (6): 9–13.
 Сетевой метаанализ данных о сравнительной эффективности антидепрессантов делает возможным суммирование и интерпретацию доказательной базы, а также понимание относительных преимуществ того или иного препарата. Актуальность этого определяется тем, что идентификация новых молекулярных мишеней затруднена в основном из-за недостаточности знаний о механизмах развития депрессии и действия антидепрессантов. В рутинной практике врачам нужна доказательность для того, чтобы сделать наилучший выбор для каждого пациента.
Сетевой метаанализ данных о сравнительной эффективности антидепрессантов делает возможным суммирование и интерпретацию доказательной базы, а также понимание относительных преимуществ того или иного препарата. Актуальность этого определяется тем, что идентификация новых молекулярных мишеней затруднена в основном из-за недостаточности знаний о механизмах развития депрессии и действия антидепрессантов. В рутинной практике врачам нужна доказательность для того, чтобы сделать наилучший выбор для каждого пациента.
В последние годы проводятся сетевые метаанализы, включающие данные о все большем числе современных антидепрессантов.
Один из последних и самых крупных метаанализов опубликован А.Cipriani и соавт. в 2018 г. [1] и посвящен оценке эффективности терапии 21 антидепрессантом, используемым для купирования большого депрессивного эпизода. Целью этого систематического обзора и сетевого метаанализа являлось сравнение различных антидепрессантов, применяемых для лечения острой униполярной депрессии у взрослых.
Авторы изучали Центральный регистр контролируемых исследований Кохрана, а также базы CINAHL, Embase, LILACS database, MEDLINE, MEDLINE In-Process, PsycINFO, AMED, UK National Research Register PSYNDEX. Выявлялись опубликованные, неопубликованные и продолжающиеся рандомизированные контролируемые исследования (РКИ) из международных регистров исследований, сайтов по одобрению лекарственных препаратов и основных научных журналов по психиатрии. На сайте ClinicalTrials.gov осуществлялся поиск с использованием термина «большой депрессивный эпизод» в сочетании с названиями всех включенных антидепрессантов. А.Cipriani и соавт. запрашивали у фармацевтических компаний – производителей препаратов неопубликованную информацию о пре- и постмаркетинговых исследованиях антидепрессантов II поколения, а также контактировали с авторами исследований, чтобы дополнить данные из статей или найти неопубликованные результаты исследований.
Были проанализированы только двойные слепые РКИ, так как такой дизайн исследования повышает методологическую точность путем минимизации систематических ошибок, связанных с ходом исследования и качеством обследования пациентов. Исключались квазирандомизированные, незаконченные исследования, а также те, в которых участвовали более 20% пациентов с биполярным аффективным расстройством, психотической
 депрессией, резистентной депрессией, больные с серьезными сопутствующими заболеваниями.
депрессией, резистентной депрессией, больные с серьезными сопутствующими заболеваниями.
Оценивались работы, сравнивавшие антидепрессанты между собой либо с плацебо в качестве пероральной монотерапии для лечения взрослых обоих полов старше 18 лет с первичным диагнозом «большой депрессивный эпизод» (major depressive disorder) согласно стандартным операционализованным диагностическим критериям (критерии Feighner, исследовательские диагностические критерии Research Diagnostic Criteria, DSM-III, DSM-III-R, DSM-IV, DSM-V, Международная классификация болезней 10-го пересмотра).
Изучались все антидепрессанты II поколения, одобренные регуляторными органами в США, Европе и Японии: агомелатин, бупропион, циталопрам, дезвенлафаксин, дулоксетин, эсциталопрам, флуоксетин, флувоксамин, левомилнаципран, милнаципран, миртазапин, пароксетин, ребоксетин, сертралин, венлафаксин, вилазодон и вортиоксетин, а также тразодон, нефазодон и два трициклических антидепрессанта, включенных в Лист необходимых препаратов Всемирной организации здравоохранения, – амитриптилин и кломипрамин. Все препараты использовались в диапазоне рекомендованных терапевтических дозировок.
Основной конечной точкой считались эффективность (доля ответивших на терапию, определяемая общим числом пациентов, у которых было выявлено более чем 50% снижение балла по стандартизованным шкалам для оценки депрессии) и переносимость (прекращение лечения, измерявшееся числом пациентов, досрочно прекративших участие в исследовании по любым причинам).
Вторичными конечными точками считались общий балл по шкалам в конце исследования, доля ремиттеров и пропорция пациентов, преждевременно выбывших из исследования из-за побочных эффектов. Когда депрессивные симптомы измерялись более чем одной стандартизованной шкалой, использовалась определенная заранее иерархия, основанная на психометрических свойствах шкалы и частоте ее применения во включенных исследованиях. При отсутствии информации доля ответивших на лечение высчитывалась в соответствии с валидизированным условным (imputation) методом. Результаты регистрировались насколько возможно близко к 8 нед. Если информация о результатах к 8-й неделе терапии была недоступна, использовались данные, ранжированные от 4 до 12 нед.
При поиске было выявлено 28 552 цитирования. Включены данные 421 исследования из баз данных, 86 неопубликованных из регистров исследований и веб-сайтов фармацевтических компаний и 15 полученных при личном общении с авторами.
В соответствии с ограничениями GRADE качество многих исследований было оценено как низкое или очень низкое для амитриптилина, бупропиона и венлафаксина, в то время как оно оценивалось как среднее для агомелатина, эсциталопрама и миртазапина. Во многих исследованиях отсутствовала информация о рандомизации и способе распределения препарата, что ограничивало интерпретацию результатов.
 В итоге всего в анализ было включено 522 двойных слепых параллельных РКИ (116 477 пациентов), проведенных в период между 1979 и 2016 гг. В целом 9% исследований были признаны имеющими высокий риск систематических ошибок, 73% – средний риск ошибок, 18% – низкий риск ошибок.
В итоге всего в анализ было включено 522 двойных слепых параллельных РКИ (116 477 пациентов), проведенных в период между 1979 и 2016 гг. В целом 9% исследований были признаны имеющими высокий риск систематических ошибок, 73% – средний риск ошибок, 18% – низкий риск ошибок.
Средний размер выборки в исследовании составлял 224 человека (SD 186). Всего 86 052 пациента были случайным образом распределены для получения активного препарата и 29 425 – плацебо. Средний возраст пациентов составлял 44 года (SD 9) и для мужчин, и для женщин. Средняя длительность лечения – 8 нед (IQR 6–8). В 47% работ больные были случайным образом разделены на 3 или более групп, 58% исследований были плацебо-контролируемыми, 83% – мультицентровыми, 77% включали только амбулаторных больных; 48% – пациентов из Северной Америки, 7% – из Азии и 27% – из Европы.
Большинство участников отвечали критериям среднего и тяжелого депрессивного эпизода: средний балл по шкале Гамильтона на baseline составлял 25,7 (SD 3,97) в 89% исследований. Доля ответа на терапию была оценена в 17,7% исследований.
Средства экстренной терапии (бензодиазепины или другие седативные гипнотики) разрешены в 36% исследований.
На рисунке представлены итоги сетевого метаанализа основных результатов исследований. С точки зрения эффективности все антидепрессанты были более эффективны, чем плацебо. Что касается переносимости, только пациенты, принимавшие агомелатин и флуоксетин, реже, чем в группе плацебо, досрочно прекращали участие в исследовании.
Что касается досрочного прекращения участия в исследовании из-за нежелательных явлений (НЯ), у всех активных препаратов доля выбывших оказалась больше, чем у плацебо.
Авторы отдельно проводили сравнения между препаратами, чтобы определить разницу между ними. В таблице представлены эти данные для первичных (основных) конечных точек. Агомелатин, амитриптилин, эциталопрам, миртазапин, пароксетин, венлафаксин и вортиоксетин оказались более эффективны, чем остальные препараты, в то время как флуоксетин, флувоксамин, ребоксетин и тразодон – наименее эффективными. Что касается переносимости, агомелатин, циталопрам, эсциталопрам, флуоксетин, сертралин и вортиоксетин переносились лучше, чем другие препараты, в то время как амитриптилин, кломипрамин, дулоксетин, флувоксамин, ребоксетин, тразодон и венлафаксин оказались ассоциированными с наивысшим риском досрочного прерывания участия в исследовании.
Интересно, что в сравнительных исследованиях, в которых участвовал новый или экспериментальный препарат, он оказывался более эффективен, чем когда этот же препарат уже использовался некоторое время либо являлся контрольным. При учете такого «эффекта новизны» уменьшалась разница между антидепрессантами.

Точность оценки относительных эффектов лечения для эффективности и переносимости различались; они были умеренными для большинства сравнений с участием агомелатина, эсциталопрама, циталопрама и миртазапина и низкими или очень низкими для большинства сравнительных исследований с участием вортиоксетина, нефазодона, кломипрамина, бупропиона, амитриптилина.
Таким образом, А.Cipriani и соавт. обнаружили, что некоторые антидепрессанты, такие как эсциталопрам, миртазапин, пароксетин, агомелатин, демонстрируют более значимый ответ на терапию и более низкий уровень досрочного прекращения участия в исследовании, чем остальные антидепрессанты. И, наоборот, ребоксетин, тразодон и флувоксамин показали меньшую эффективность и худшую переносимость по сравнению с другими антидепрессантами, что делает их менее предпочтительными препаратами.
Установленная разница между препаратами была меньше в плацебо-контролируемых исследованиях, чем в прямых сравнениях. Этому есть несколько объяснений, так как много факторов связано с более высоким ответом на плацебо, например рандомизационные соотношения, ожидание получения активного препарата, частота визитов в исследовании. Согласно полученным данным ответ на терапию одним и тем же антидепрессантом в среднем меньше, а уровень досрочного прекращения относительно больше в плацебо-контролируемых исследованиях, чем в прямых сравнениях. Более того, для одного и того же препарата и одной и той же возможности получения плацебо более высокая доля досрочно прекративших участие в исследовании по любым причинам связана с возможным более низким ответом на терапию. Помимо этого, пациенты, случайным образом распределенные в группу активного препарата в двойных слепых плацебо-контролируемых исследованиях, способны заканчивать участие в исследовании раньше, чем в прямых сравнительных анализах, потому что они могут ожидать, что попали в группу плацебо. Другим возможным объяснением могут быть ошибки в проведении, анализе и репортировании результатов прямых сравнительных исследований в коммерческих целях. В результате истинная эффективность активного препарата может быть недооценена.
Оценки эффекта терапии в исследовании А.Cipriani и соавт. согласуются с предыдущими обзорами на эту же тему, но они значительно более точные, так как большой объем данных обеспечивает статистическую значимость.
Например, А.Khoo и соавт. (2015 г.) [2] провели сетевой метаанализ эффективности монотерапии 10 широко используемыми для купирования большого депрессивного расстройства (БДР) антидепрессантами: агомелатин, дулоксетин, эсциталопрам, флувоксамин, флуоксетин, миртазапин, пароксетин, сертралин, тразодон, венлафаксин. Осуществлялся систематический поиск в PubMed, Embase, the Cocrane Library прямых сравнительных РКИ длительностью как минимум 6 нед. В исследованиях участвовали пациенты старше 18 лет с БДР умеренной или тяжелой степени тяжести по критериям DSM (DSM-III, DSM-III-R, DSM-IV, DSM-IV-TR). В качестве критериев эффективности среди прочих оценивалась доля больных, ответивших на терапию и достигших ремиссии (по шкалам HDRS или MADRS). Ответ на терапию определялся как снижение общего балла по шкале HDRS или MADRS на 50% и более от исходного. Достижение ремиссии оценивалось как 7 баллов и ниже по шкале HDRS (версия, состоящая из 17 пунктов), или 8 баллов и ниже (более длинные версии шкалы HDRS), или 12 и менее баллов по шкале MADRS. Переносимость изучалась по показателю доли досрочно прекративших участие в исследовании из-за НЯ.
В конечном итоге для анализа были выбраны 76 исследований, проведенных с 1989 по 2014 г. Общее число пациентов – 16 389. Средний возраст больных составил от 36 до 75 лет; 67% женщины. В большинство исследований включали пациентов с умеренным и тяжелым БДР.
В 63 исследованиях были представлены данные о доле ответивших на терапию. Агомелатин, эсциталопрам, миртазапин и венлафаксин оказались значительно более эффективными, чем флуоксетин, в достижении 50% редукции общего балла по шкалам HDRS и MADRS по сравнению с исходным. В сравнении с флуоксетином у миртазапина и агомелатина был самый большой эффект лечения на долю ответивших на терапию (отношение шансов – ОШ 1,56; 95% доверительный интервал – ДИ 1,24–1,97 и ОШ 1,46; 95% ДИ 1,18–1,81); далее в порядке убывания эффекта оказались венлафаксин, эсциталопрам, пароксетин, сертралин.
В 50 исследованиях доля достигших ремиссии указывалась как конечная точка. Доли достигших ремиссии для агомелатина и венлафаксина значительно превышали таковые для флуоксетина и сертралина. У агомелатина в сравнении с флуоксетином оказался максимальный эффект лечения на долю достигших ремиссии; затем в порядке убывания величины эффекта лечения были венлафаксин, миртазапин, эсциталопрам. Результаты двух последних препаратов оказались незначимыми.
Что касается переносимости, агомелатин обладал статистически значимо меньшим риском досрочного прекращения участия в исследовании из-за НЯ в сравнении со всеми остальными препаратами, кроме сертралина. В последнем случае отличие не было статистически значимым (ОШ 1,58; 95% ДИ 0,96–2,59). На фоне терапии эсциталопрамом и сертралином риск досрочного прекращения участия в исследовании был значительно ниже, чем у пароксетина и венлафаксина. Несмотря на то, что терапия эсциталопрамом и сертралином также переносились лучше, чем флуоксетином, разница не достигала статистически значимых величин. В сравнении с флуоксетином лечение дулоксетином сопровождалось максимальным риском досрочного прекращения из-за НЯ (ОШ 2,23; 95% ДИ 1,52–3,28); на втором месте оказался венлафаксин (ОШ 1,41; 95% ДИ 1,10–1,81). Дулоксетин обладал худшей переносимостью, чем остальные препараты, особенно эсциталопрам, миртазапин, пароксетин, сертралин и венлафаксин (статистически значимая разница).
С целью оценки влияния характеристик больных на результаты терапии отдельно были проанализированы пожилые пациенты, а также с тяжелым БДР (определяемым как 25 и более баллов по шкале HDRS или 30 и более баллов по шкале MADRS на исходном визите). Не было выявлено значимой разницы в предполагаемой эффективности терапии по сравнению с основным анализом. Схожим образом анализ чувствительности характеристик исследования (например, риск систематической ошибки) также не привел к значимым изменениям результата.
Очевидно, что в обеих метааналитических работах получены сходные результаты высокой степени доказательности. В то же время следует обратить внимание на некоторые ограничения работ, обусловливающие дальнейшие исследования. Например, А.Cipriani и соавт. не оценивали потенциально важные клинические и демографические показатели, которые могут повлиять на ответ на терапию с учетом индивидуального уровня каждого пациента (возраст, пол, тяжесть симптомов, длительность болезни); не включали больных с психозом и резистентными депрессиями, что может ограничивать применение препаратов у данных категорий лиц; не изучали комбинацию с нефармакологическими методами лечения.
Также необходимо отметить – некоторые НЯ антидепрессантов возникают через продолжительный период лечения, это означает, что положительные результаты необходимо учитывать с большой осторожностью, а исследования, включенные в оба метаанализа, были краткосрочными.
Кроме того, оба исследования включали данные о различиях впервые назначаемых антидепрессантов и не содержали указания о препаратах второго выбора в случае неэффективности предшествовавшей терапии. Для этого необходимо проведение хорошо спланированных дополнительных исследований.
Таким образом, несмотря на перечисленные ограничения, данные приведенных сетевых метаанализов представляют собой наиболее полную доказательную базу для выбора первого препарата для лечения большого депрессивного эпизода у взрослых.
В обоих метаанализах агомелатин оказался одним из наиболее эффективных и хорошо переносимых препаратов. Такие данные согласуются с многочисленными результатами применения препарата в реальной клинической практике [3–6].
Сведения об авторе
Фролова Вероника Игоревна – канд. мед. наук, доц. каф. психиатрии, психотерапии и психосоматической патологии ФНМО ФГАОУ ВО РУДН. E-mail: hifrol@mail.ru
Ключевые слова: мета-анализ, антидепрессанты, агомелатин.
Для цитирования: Фролова В.И. Сравнительная эффективность современных антидепрессантов: данные сетевых метаанализов. Психиатрия и психофармакотерапия. 2018; 20 (6): 9–13.
The comparative efficacy of contemporary antidepressants: data of network meta-analyses
V.I.FrolovaPeople’s Friendship University of Russia. 117198, Russian Federation, Moscow, ul. Miklukho-Maklaya, d. 6 hifrol@mail.ru
In this article results of two meta-analyses of contemporary antidepressants’ efficacy are compared. Both meta-analyses represent results of high degree of evidence. According to both meta-analyses agomelatin is one of the most effective and well-tolerated modern antidepressant.
Key words: meta-analyses, antidepressants, agomelatin.
For citation: Frolova V.I. The comparative efficacy of contemporary antidepressants: data of network meta-analyse. Psychiatry and Psychopharmacotherapy. 2018; 20 (6): 9–13.
 Сетевой метаанализ данных о сравнительной эффективности антидепрессантов делает возможным суммирование и интерпретацию доказательной базы, а также понимание относительных преимуществ того или иного препарата. Актуальность этого определяется тем, что идентификация новых молекулярных мишеней затруднена в основном из-за недостаточности знаний о механизмах развития депрессии и действия антидепрессантов. В рутинной практике врачам нужна доказательность для того, чтобы сделать наилучший выбор для каждого пациента.
Сетевой метаанализ данных о сравнительной эффективности антидепрессантов делает возможным суммирование и интерпретацию доказательной базы, а также понимание относительных преимуществ того или иного препарата. Актуальность этого определяется тем, что идентификация новых молекулярных мишеней затруднена в основном из-за недостаточности знаний о механизмах развития депрессии и действия антидепрессантов. В рутинной практике врачам нужна доказательность для того, чтобы сделать наилучший выбор для каждого пациента.В последние годы проводятся сетевые метаанализы, включающие данные о все большем числе современных антидепрессантов.
Один из последних и самых крупных метаанализов опубликован А.Cipriani и соавт. в 2018 г. [1] и посвящен оценке эффективности терапии 21 антидепрессантом, используемым для купирования большого депрессивного эпизода. Целью этого систематического обзора и сетевого метаанализа являлось сравнение различных антидепрессантов, применяемых для лечения острой униполярной депрессии у взрослых.
Авторы изучали Центральный регистр контролируемых исследований Кохрана, а также базы CINAHL, Embase, LILACS database, MEDLINE, MEDLINE In-Process, PsycINFO, AMED, UK National Research Register PSYNDEX. Выявлялись опубликованные, неопубликованные и продолжающиеся рандомизированные контролируемые исследования (РКИ) из международных регистров исследований, сайтов по одобрению лекарственных препаратов и основных научных журналов по психиатрии. На сайте ClinicalTrials.gov осуществлялся поиск с использованием термина «большой депрессивный эпизод» в сочетании с названиями всех включенных антидепрессантов. А.Cipriani и соавт. запрашивали у фармацевтических компаний – производителей препаратов неопубликованную информацию о пре- и постмаркетинговых исследованиях антидепрессантов II поколения, а также контактировали с авторами исследований, чтобы дополнить данные из статей или найти неопубликованные результаты исследований.
Были проанализированы только двойные слепые РКИ, так как такой дизайн исследования повышает методологическую точность путем минимизации систематических ошибок, связанных с ходом исследования и качеством обследования пациентов. Исключались квазирандомизированные, незаконченные исследования, а также те, в которых участвовали более 20% пациентов с биполярным аффективным расстройством, психотической
 депрессией, резистентной депрессией, больные с серьезными сопутствующими заболеваниями.
депрессией, резистентной депрессией, больные с серьезными сопутствующими заболеваниями.Оценивались работы, сравнивавшие антидепрессанты между собой либо с плацебо в качестве пероральной монотерапии для лечения взрослых обоих полов старше 18 лет с первичным диагнозом «большой депрессивный эпизод» (major depressive disorder) согласно стандартным операционализованным диагностическим критериям (критерии Feighner, исследовательские диагностические критерии Research Diagnostic Criteria, DSM-III, DSM-III-R, DSM-IV, DSM-V, Международная классификация болезней 10-го пересмотра).
Изучались все антидепрессанты II поколения, одобренные регуляторными органами в США, Европе и Японии: агомелатин, бупропион, циталопрам, дезвенлафаксин, дулоксетин, эсциталопрам, флуоксетин, флувоксамин, левомилнаципран, милнаципран, миртазапин, пароксетин, ребоксетин, сертралин, венлафаксин, вилазодон и вортиоксетин, а также тразодон, нефазодон и два трициклических антидепрессанта, включенных в Лист необходимых препаратов Всемирной организации здравоохранения, – амитриптилин и кломипрамин. Все препараты использовались в диапазоне рекомендованных терапевтических дозировок.
Основной конечной точкой считались эффективность (доля ответивших на терапию, определяемая общим числом пациентов, у которых было выявлено более чем 50% снижение балла по стандартизованным шкалам для оценки депрессии) и переносимость (прекращение лечения, измерявшееся числом пациентов, досрочно прекративших участие в исследовании по любым причинам).
Вторичными конечными точками считались общий балл по шкалам в конце исследования, доля ремиттеров и пропорция пациентов, преждевременно выбывших из исследования из-за побочных эффектов. Когда депрессивные симптомы измерялись более чем одной стандартизованной шкалой, использовалась определенная заранее иерархия, основанная на психометрических свойствах шкалы и частоте ее применения во включенных исследованиях. При отсутствии информации доля ответивших на лечение высчитывалась в соответствии с валидизированным условным (imputation) методом. Результаты регистрировались насколько возможно близко к 8 нед. Если информация о результатах к 8-й неделе терапии была недоступна, использовались данные, ранжированные от 4 до 12 нед.
При поиске было выявлено 28 552 цитирования. Включены данные 421 исследования из баз данных, 86 неопубликованных из регистров исследований и веб-сайтов фармацевтических компаний и 15 полученных при личном общении с авторами.
В соответствии с ограничениями GRADE качество многих исследований было оценено как низкое или очень низкое для амитриптилина, бупропиона и венлафаксина, в то время как оно оценивалось как среднее для агомелатина, эсциталопрама и миртазапина. Во многих исследованиях отсутствовала информация о рандомизации и способе распределения препарата, что ограничивало интерпретацию результатов.
 В итоге всего в анализ было включено 522 двойных слепых параллельных РКИ (116 477 пациентов), проведенных в период между 1979 и 2016 гг. В целом 9% исследований были признаны имеющими высокий риск систематических ошибок, 73% – средний риск ошибок, 18% – низкий риск ошибок.
В итоге всего в анализ было включено 522 двойных слепых параллельных РКИ (116 477 пациентов), проведенных в период между 1979 и 2016 гг. В целом 9% исследований были признаны имеющими высокий риск систематических ошибок, 73% – средний риск ошибок, 18% – низкий риск ошибок.Средний размер выборки в исследовании составлял 224 человека (SD 186). Всего 86 052 пациента были случайным образом распределены для получения активного препарата и 29 425 – плацебо. Средний возраст пациентов составлял 44 года (SD 9) и для мужчин, и для женщин. Средняя длительность лечения – 8 нед (IQR 6–8). В 47% работ больные были случайным образом разделены на 3 или более групп, 58% исследований были плацебо-контролируемыми, 83% – мультицентровыми, 77% включали только амбулаторных больных; 48% – пациентов из Северной Америки, 7% – из Азии и 27% – из Европы.
Большинство участников отвечали критериям среднего и тяжелого депрессивного эпизода: средний балл по шкале Гамильтона на baseline составлял 25,7 (SD 3,97) в 89% исследований. Доля ответа на терапию была оценена в 17,7% исследований.
Средства экстренной терапии (бензодиазепины или другие седативные гипнотики) разрешены в 36% исследований.
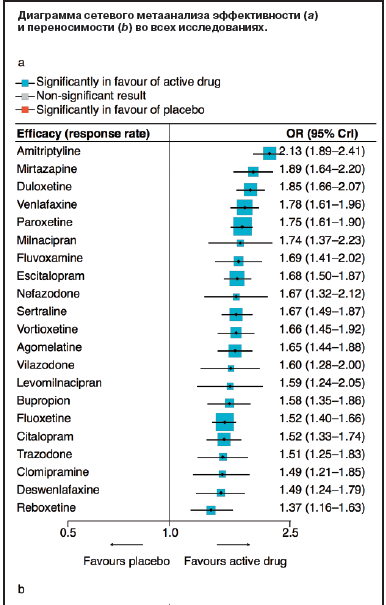
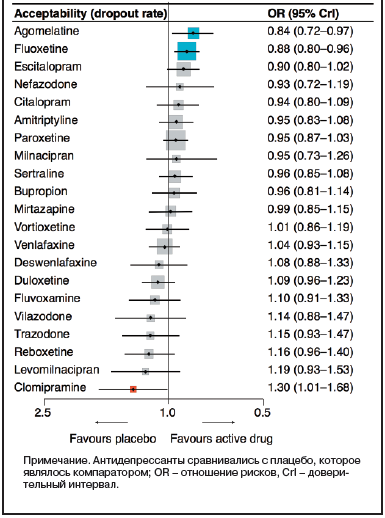
На рисунке представлены итоги сетевого метаанализа основных результатов исследований. С точки зрения эффективности все антидепрессанты были более эффективны, чем плацебо. Что касается переносимости, только пациенты, принимавшие агомелатин и флуоксетин, реже, чем в группе плацебо, досрочно прекращали участие в исследовании.
Что касается досрочного прекращения участия в исследовании из-за нежелательных явлений (НЯ), у всех активных препаратов доля выбывших оказалась больше, чем у плацебо.
Авторы отдельно проводили сравнения между препаратами, чтобы определить разницу между ними. В таблице представлены эти данные для первичных (основных) конечных точек. Агомелатин, амитриптилин, эциталопрам, миртазапин, пароксетин, венлафаксин и вортиоксетин оказались более эффективны, чем остальные препараты, в то время как флуоксетин, флувоксамин, ребоксетин и тразодон – наименее эффективными. Что касается переносимости, агомелатин, циталопрам, эсциталопрам, флуоксетин, сертралин и вортиоксетин переносились лучше, чем другие препараты, в то время как амитриптилин, кломипрамин, дулоксетин, флувоксамин, ребоксетин, тразодон и венлафаксин оказались ассоциированными с наивысшим риском досрочного прерывания участия в исследовании.
Интересно, что в сравнительных исследованиях, в которых участвовал новый или экспериментальный препарат, он оказывался более эффективен, чем когда этот же препарат уже использовался некоторое время либо являлся контрольным. При учете такого «эффекта новизны» уменьшалась разница между антидепрессантами.

Точность оценки относительных эффектов лечения для эффективности и переносимости различались; они были умеренными для большинства сравнений с участием агомелатина, эсциталопрама, циталопрама и миртазапина и низкими или очень низкими для большинства сравнительных исследований с участием вортиоксетина, нефазодона, кломипрамина, бупропиона, амитриптилина.
Таким образом, А.Cipriani и соавт. обнаружили, что некоторые антидепрессанты, такие как эсциталопрам, миртазапин, пароксетин, агомелатин, демонстрируют более значимый ответ на терапию и более низкий уровень досрочного прекращения участия в исследовании, чем остальные антидепрессанты. И, наоборот, ребоксетин, тразодон и флувоксамин показали меньшую эффективность и худшую переносимость по сравнению с другими антидепрессантами, что делает их менее предпочтительными препаратами.
Установленная разница между препаратами была меньше в плацебо-контролируемых исследованиях, чем в прямых сравнениях. Этому есть несколько объяснений, так как много факторов связано с более высоким ответом на плацебо, например рандомизационные соотношения, ожидание получения активного препарата, частота визитов в исследовании. Согласно полученным данным ответ на терапию одним и тем же антидепрессантом в среднем меньше, а уровень досрочного прекращения относительно больше в плацебо-контролируемых исследованиях, чем в прямых сравнениях. Более того, для одного и того же препарата и одной и той же возможности получения плацебо более высокая доля досрочно прекративших участие в исследовании по любым причинам связана с возможным более низким ответом на терапию. Помимо этого, пациенты, случайным образом распределенные в группу активного препарата в двойных слепых плацебо-контролируемых исследованиях, способны заканчивать участие в исследовании раньше, чем в прямых сравнительных анализах, потому что они могут ожидать, что попали в группу плацебо. Другим возможным объяснением могут быть ошибки в проведении, анализе и репортировании результатов прямых сравнительных исследований в коммерческих целях. В результате истинная эффективность активного препарата может быть недооценена.
Оценки эффекта терапии в исследовании А.Cipriani и соавт. согласуются с предыдущими обзорами на эту же тему, но они значительно более точные, так как большой объем данных обеспечивает статистическую значимость.
Например, А.Khoo и соавт. (2015 г.) [2] провели сетевой метаанализ эффективности монотерапии 10 широко используемыми для купирования большого депрессивного расстройства (БДР) антидепрессантами: агомелатин, дулоксетин, эсциталопрам, флувоксамин, флуоксетин, миртазапин, пароксетин, сертралин, тразодон, венлафаксин. Осуществлялся систематический поиск в PubMed, Embase, the Cocrane Library прямых сравнительных РКИ длительностью как минимум 6 нед. В исследованиях участвовали пациенты старше 18 лет с БДР умеренной или тяжелой степени тяжести по критериям DSM (DSM-III, DSM-III-R, DSM-IV, DSM-IV-TR). В качестве критериев эффективности среди прочих оценивалась доля больных, ответивших на терапию и достигших ремиссии (по шкалам HDRS или MADRS). Ответ на терапию определялся как снижение общего балла по шкале HDRS или MADRS на 50% и более от исходного. Достижение ремиссии оценивалось как 7 баллов и ниже по шкале HDRS (версия, состоящая из 17 пунктов), или 8 баллов и ниже (более длинные версии шкалы HDRS), или 12 и менее баллов по шкале MADRS. Переносимость изучалась по показателю доли досрочно прекративших участие в исследовании из-за НЯ.
В конечном итоге для анализа были выбраны 76 исследований, проведенных с 1989 по 2014 г. Общее число пациентов – 16 389. Средний возраст больных составил от 36 до 75 лет; 67% женщины. В большинство исследований включали пациентов с умеренным и тяжелым БДР.
В 63 исследованиях были представлены данные о доле ответивших на терапию. Агомелатин, эсциталопрам, миртазапин и венлафаксин оказались значительно более эффективными, чем флуоксетин, в достижении 50% редукции общего балла по шкалам HDRS и MADRS по сравнению с исходным. В сравнении с флуоксетином у миртазапина и агомелатина был самый большой эффект лечения на долю ответивших на терапию (отношение шансов – ОШ 1,56; 95% доверительный интервал – ДИ 1,24–1,97 и ОШ 1,46; 95% ДИ 1,18–1,81); далее в порядке убывания эффекта оказались венлафаксин, эсциталопрам, пароксетин, сертралин.
В 50 исследованиях доля достигших ремиссии указывалась как конечная точка. Доли достигших ремиссии для агомелатина и венлафаксина значительно превышали таковые для флуоксетина и сертралина. У агомелатина в сравнении с флуоксетином оказался максимальный эффект лечения на долю достигших ремиссии; затем в порядке убывания величины эффекта лечения были венлафаксин, миртазапин, эсциталопрам. Результаты двух последних препаратов оказались незначимыми.
Что касается переносимости, агомелатин обладал статистически значимо меньшим риском досрочного прекращения участия в исследовании из-за НЯ в сравнении со всеми остальными препаратами, кроме сертралина. В последнем случае отличие не было статистически значимым (ОШ 1,58; 95% ДИ 0,96–2,59). На фоне терапии эсциталопрамом и сертралином риск досрочного прекращения участия в исследовании был значительно ниже, чем у пароксетина и венлафаксина. Несмотря на то, что терапия эсциталопрамом и сертралином также переносились лучше, чем флуоксетином, разница не достигала статистически значимых величин. В сравнении с флуоксетином лечение дулоксетином сопровождалось максимальным риском досрочного прекращения из-за НЯ (ОШ 2,23; 95% ДИ 1,52–3,28); на втором месте оказался венлафаксин (ОШ 1,41; 95% ДИ 1,10–1,81). Дулоксетин обладал худшей переносимостью, чем остальные препараты, особенно эсциталопрам, миртазапин, пароксетин, сертралин и венлафаксин (статистически значимая разница).
С целью оценки влияния характеристик больных на результаты терапии отдельно были проанализированы пожилые пациенты, а также с тяжелым БДР (определяемым как 25 и более баллов по шкале HDRS или 30 и более баллов по шкале MADRS на исходном визите). Не было выявлено значимой разницы в предполагаемой эффективности терапии по сравнению с основным анализом. Схожим образом анализ чувствительности характеристик исследования (например, риск систематической ошибки) также не привел к значимым изменениям результата.
Очевидно, что в обеих метааналитических работах получены сходные результаты высокой степени доказательности. В то же время следует обратить внимание на некоторые ограничения работ, обусловливающие дальнейшие исследования. Например, А.Cipriani и соавт. не оценивали потенциально важные клинические и демографические показатели, которые могут повлиять на ответ на терапию с учетом индивидуального уровня каждого пациента (возраст, пол, тяжесть симптомов, длительность болезни); не включали больных с психозом и резистентными депрессиями, что может ограничивать применение препаратов у данных категорий лиц; не изучали комбинацию с нефармакологическими методами лечения.
Также необходимо отметить – некоторые НЯ антидепрессантов возникают через продолжительный период лечения, это означает, что положительные результаты необходимо учитывать с большой осторожностью, а исследования, включенные в оба метаанализа, были краткосрочными.
Кроме того, оба исследования включали данные о различиях впервые назначаемых антидепрессантов и не содержали указания о препаратах второго выбора в случае неэффективности предшествовавшей терапии. Для этого необходимо проведение хорошо спланированных дополнительных исследований.
Таким образом, несмотря на перечисленные ограничения, данные приведенных сетевых метаанализов представляют собой наиболее полную доказательную базу для выбора первого препарата для лечения большого депрессивного эпизода у взрослых.
В обоих метаанализах агомелатин оказался одним из наиболее эффективных и хорошо переносимых препаратов. Такие данные согласуются с многочисленными результатами применения препарата в реальной клинической практике [3–6].
Сведения об авторе
Фролова Вероника Игоревна – канд. мед. наук, доц. каф. психиатрии, психотерапии и психосоматической патологии ФНМО ФГАОУ ВО РУДН. E-mail: hifrol@mail.ru
Список исп. литературыСкрыть список1. Cipriani A, Furukawa TA, Salanti G et al. Comparative efficacy and acceptability of 21 antidepressant drugs for the acute treatment of adults with major depressive disorder: a systematic review and network meta-analysis. Lancet 2018; 391 (10128): 1357–66. DOI: 10/1016/S0140-6736(17)32802-7
2. Khoo AL, Zhou HJ, Teng M et al. Network Meta-Analysis and Cost-Effectiveness Generation Antidepressants. CNS Drugs 2015; 29 (8): 695–712. DOI: 10.1007/s40263-015-0267-6. DOI: 10.1007/s40263-015-0267-6
3. Medvedev V.E., Retyunskii K.Yu., Ovchinnikov A.A. et al. Differences in Assessment of the Severity of Depression by Doctors and Patients during Combined Therapy with Agomelatine (the EMOTION multicenter trial). Neurosci Behavioral Physiol 2018; 48 (3): 367–76. https://doi.org/10.1007/s11055-018-0572-x
4. Медведев В.Э., Ретюнский К.Ю., Овчинников А.А. и др. Различия в оценке тяжести депрессии врачами и пациентами в процессе комбинированной терапии агомелатином (мультицентровое исследование «ЭМОЦИЯ»). Журн. неврологии и психиатрии им. С.С.Корсакова. 2016; 11: 26–34. DOI: 10.17116/jnevro201611611126-34 / Medvedev V.E., Retyunskij K.Yu., Ovchinnikov A.A. i dr. Razlichiya v ocenke tyazhesti depressii vrachami i pacientami v processe kombinirovannoj terapii agomelatinom (multicentrovoe issledovanie “EMOCIYa”). Zhurn. nevrologii i psihiatrii im. S.S.Korsakova. 2016; 11: 26–34. DOI: 10.17116/jnevro201611611126-34 [in Russian]
5. Медведев В.Э. Монотерапия дисфорической депрессии Вальдоксаном. Психиатрия и психофармакотерапия. 2016; 18 (1): 20–3. / Medvedev V.E. Dysphoric Depression Monotherapy with Valdoxan. Psychiatry and Psychopharmacotherapy. 2016; 18 (1): 20–3. [in Russian]
6. Медведев В.Э., Тер-Исраелян А.Ю., Фролова В.И. и др. Опыт применения вальдоксана при депрессиях, протекающих с когнитивными нарушениями. Журн. неврологии и психиатрии им. С.С.Корсакова. 2018; 2: 77–80. DOI: 10.17116/jnevro 20181182177-80 / Medvedev V.E., Ter-Israelyan A.Yu., Frolova V.I. i dr. Opyt primeneniya valdoksana pri depressiyah, protekayushih s kognitivnymi narusheniyami. Zhurn. nevrologii i psihiatrii im. S.S.Korsakova. 2018; 2: 77–80. DOI: 10.17116/jnevro 20181182177-80 [in Russian]


