Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
1 Bekhtereva Institute of the Human Brain of the Russian Academy of Sciences, SaintPetersburg, Russia;
2 St. Petersburg State University, St. Petersburg, Russia;
3 Lesgaft National State University of Physical Culture, Sports and Health, St.Petersburg, Russia;
4 Almazov National Medical Research Center of the Ministry of Health of the Russian Federation, St. Petersburg, Russia
Abstract
Introduction. Neurocognitive deficit in schizophrenia is a topical issue in theoretical and clinical psychiatry. Currently, there are very few studies on the relationship between the characteristics of cognitive functioning of patients with the first episode of schizophrenia and immunological parameters.
Objective: to study the neurocognitive profile and cytokine levels in patients with the first episode of schizophrenia in remission.
Material and methods. At the stage of stable drug remission (more than 6 months), 51 patients with a diagnosis of F20.0 "Paranoid schizophrenia" (age 28.3±5.8 years) were examined. Inclusion criteria: verified diagnosis F20.0 "Paranoid schizophrenia" (according to the diagnostic criteria of ICD-10), disease duration of no more than 5 years and the number of hospitalizations of no more than 3. The comparison group consisted of 60 patients with a disease duration of more than 5 years and more than three registered episodes, including 25 women and 35 men (age 34.95±7.38 years). The control group (n=30) consisted of healthy subjects matched for age, gender and education level, without psychiatric and severe somatic diseases. The study used the clinical and psychopathological method and the Brief Assessment of Cognitive Functions in Schizophrenia (BACS) Scale. Venous blood was taken once in accordance with the general rules for collecting material for immunological studies. Laboratory methods (ELISA, Milliplex human Th17 magnetic bead panel — 25 analytes) included determination of cytokines, C-reactive protein.
Results. The obtained data indicate an increased level of some cytokines during remission at the early stage of schizophrenia (IL-6, IL-1β and TNF-α). The dynamics of the IL-10 level reflects a decrease in its protective function during disease progression. In women, a less pronounced immune response is determined compared to male patients, which correlates with a smaller neurocognitive deficit. Pronounced neurocognitive impairments were revealed in patients with the first episode of schizophrenia in remission, especially in men. The greatest decrease was found in working memory, verbal learning and information processing speed. The number of schizophrenia relapses affects the level of cognitive functioning and the level of cytokines. The results of the study demonstrate the relationship between immune dysfunction and neurocognitive deficit in schizophrenia both at early and late stages of the disease. Correlations of a number of cytokines with certain indicators of cognitive functioning were revealed. Demographic factors make a significant contribution to the variability of the initial data. In the group of patients with the first episode of schizophrenia in remission, correlations of a number of proinflammatory cytokines with the deterioration of executive functions and verbal memory were revealed. Anti-inflammatory IL-10 does not demonstrate significant relationships with cognitive domains at the early stages of the disease in remission. The nature of the relationship between cytokines and cognitive functions changes as the disease progresses.
Conclusion. The results of the study confirm that cognitive deficit in schizophrenia is not static, but is formed in the dynamics of the disease, where chronic inflammation can act as one of the key mechanisms of its progression. The obtained data, supported by modern research, emphasize the importance of inflammatory processes in the pathogenesis of cognitive impairment in schizophrenia.
Keywords: schizophrenia; neurocognitive deficit; inflammation; cytokines
For citation: Alpin V.S., Petrova N.N., Dorofeykov V.V., Slepoy V.V. Neurocognitive profile and cytokines in patients inremission at the early stage of schizophrenia. Psychiatry and psychopharmacotherapy. 2025; 6: 36–42. DOI: 10.62202/2075-1761-2025-27-6-36-42
Введение
Снижение когнитивных функций происходит на ранних стадиях шизофрении и сохраняется на протяжении всей болезни [1, 2]. Нейрокогнитивный дефицит — один из наиболее значимых факторов, влияющих на функционирование пациентов с шизофренией, такие как независимая жизнь, социальное и профессиональное функционирование [3]. Нейрокогнитивный дефицит включает снижение памяти, способности концентрировать внимание и исполнительных функций (проблемы с планированием, организацией и решением задач) [4].
Биологические механизмы, лежащие в основе снижения когнитивных функций при шизофрении, в значительной степени остаются неизвестными [5]. Ряд исследований показывает, что нарушенная регуляция нейробиохимических процессов и иммуновоспалительные реакции могут лежать в основе когнитивных дефицитов, наблюдаемых у пациентов с шизофренией [6-9].
Цитокины, как иммунные медиаторы, участвуют в механизмах синаптической пластичности, тесно связанных с когнитивными функциями [10]. Мишенями цитокинов в мозге являются нейротрансмиттеры и нейроцепи. Активация воспалительной реакции приводит к высвобождению воспалительных цитокинов и мобилизации иммунных клеток, которые проникают в мозг и изменяют поведение. Цитокины и их сигнальные пути, включая митоген-активируемую протеинкиназу p38, оказывают существенное влияние на метаболизм нейротрансмиттеров, таких как серотонин, дофамин и глутамат, через воздействие на их синтез, высвобождение и обратный захват. Цитокины активируют кинурениновый путь, который не только истощает триптофан, первичный аминокислотный предшественник серотонина, но и генерирует нейроактивные метаболиты, которые могут существенно влиять на регуляцию дофамина и глутамата. Через нейротрансмиттерные системы цитокины воздействуют на нейросети головного мозга, включая базальные ганглии и переднюю поясную извилину [11]. Имеются данные, что повышенные периферические воспалительные биомаркеры связаны с уменьшением толщины коры [12] и объема мозга [13] в областях, ответственных за некоторые когнитивные функции (например, внимание, визуальное обучение, беглость речи).
Локальная и системная активация врожденных иммунных реакций в мозге [14] может приводить к снижению когнитивных функций у здоровых и больных людей [15, 16]. Известно, что нарушения нейроразвития у подростков приводят к аномальной синаптической пластичности, связанной с когнитивным дефицитом [17]. Лонгитюдное исследование на протяжении двадцати лет показало, что системное воспаление во взрослом возрасте связано со снижением когнитивных функций у здоровых взрослых [18].
Такие цитокины, как TNF-α, IL-6 и IL-1, могут существенно влиять на когнитивные функции, главным образом на память [19-21]. Имеются данные, что повышенные уровни IL-1β и IL-6 связаны со снижением внимания, нарушениями рабочей памяти и исполнительной функции [22]. Повышенная экспрессия IL-1β может вызвать локализованное и постоянное воспаление в гиппокампе, препятствуя формированию памяти [23].
Модулируя развитие нейронов [24, 25] и пластичность синапсов [26], цитокины могут участвовать в формировании когнитивных и поведенческих нарушений, структурных аномалий мозга, наблюдаемым при психозах [27].
Нарушение взаимодействия между микроглиальными клетками и цитокинами может вызывать нейродегенеративные процессы при нейропсихиатрических заболеваниях, в том числе шизофрении [28].
Ribeiro-Santos с соавт. (2020) установили значимые отрицательные корреляции между некоторыми биомаркерами воспаления и когнитивными функциями у пациентов с шизофренией [29].
Систематический обзор Misiak c cоавт. (2018) выявил, что наиболее последовательные результаты указывают на худшие когнитивные функции у пациентов с шизофренией с более высоким уровнем С-реактивного белка. Менее последовательные данные свидетельствуют о лучшем когнитивном функционировании у пациентов с шизофренией с более высоким уровнем TNF-α. Доказательства участия других цитокинов в когнитивных нарушениях у пациентов с шизофренией менее убедительны из-за противоречивых результатов или небольшого количества исследований [30].
В исследовании Lesh с соавт. (2018) повышенные уровни TNF-α ассоциированы с уменьшением объема префронтальной коры (β = -0.32, p = 0.01), что может объяснять нарушения исполнительных функций и когнитивного контроля у пациентов. Повышенные уровни IL-1β коррелировали с нарушением исполнительных функций по результатам теста Струпа (r = -0.38, p = 0.02). Данные указывают на возможную связь между воспалительными процессами, опосредованными IL-1β, и когнитивным дефицитом при шизофрении [31].
Имеются данные о наличии корреляции между повышенными уровнями IL-6 и нарушенной обработкой информации у больных шизофренией [7]. В то же время Hori с соавт. (2017) не выявили связи между IL-6 и фактором некроза опухоли альфа (TNF) с когнитивными функциями у больных хронической шизофренией [32].
Установлено, что связь между когнитивной функцией и уровнем IL-18 при хронической шизофрении зависит от полиморфизма IL-18 -607 A/C. Уровни и генотип IL-18 были измерены у 693 госпитализированных пациентов и 422 контрольных лиц. Уровни сывороточного IL-18 были выше у пациентов, чем у здоровых лиц контрольной группы. Полиморфизм IL-18 -607 A/C коррелировал со зрительно-пространственным/конструктивным индексом только у больных шизофренией, а уровень IL-18 коррелировал с памятью только у пациентов с генотипом C/C, но не у пациентов с генотипами C/A или A/A. Таким образом, полиморфизм IL18 -607A/C и уровни сывороточного IL-18 были связаны с когнитивными нарушениями у пациентов с шизофренией [19].
Результаты метаанализа Patlola с соавт. (2023) продемонстрировали обратную зависимость между показателями в пяти когнитивных областях (скорость внимания, исполнительные функции, рабочая память, вербальное и визуальное обучение и память) и уровнями IL-6, IL-1β, TNF-α и С-реактивного белка в плазме крови у пациентов с шизофренией. Результаты метаанализа показывают, что когнитивные нарушения обусловлены повышенным уровнем этих провоспалительных биомаркеров [10].
В настоящее время имеется крайне мало исследований взаимосвязи провоспалительных и противовоспалительных цитокинов с когнитивной функцией у пациентов с первым эпизодом шизофрении.
Целью данного исследования было изучение нейрокогнитивного профиля и уровня цитокинов у пациентов с первым эпизодом шизофрении в ремиссии.
Материал и методы исследования
На этапе устойчивой лекарственной ремиссии (более 6 месяцев) был обследован 51 пациент с диагнозом F20.0 «Параноидная шизофрения» (возраст 28,3+5,8 года). Длительность заболевания составила 2,7±1,3 года. Средний возраст начала заболевания — 25,8+5,5 года. Доля женщин составила 53%, мужчин — 47%. Среднее число рецидивов достигло 1,77+0,69 случая. У 40% пациентов наблюдался один перенесенный эпизод, у 50% — два и у 10% — три перенесенных эпизода. Таким образом, пациенты основной группы соответствовали понятию первого эпизода шизофрении, находились на раннем этапе заболевания.
Критерии включения: верифицированный диагноз F20.0 «Шизофрения параноидная» (согласно диагностическим критериям МКБ-10), длительность заболевания не более
5 лет и количество госпитализаций не более 3.
Критерии исключения: органическое поражение головного мозга или тяжелые неврологические заболевания; обострение психоза, включая психомоторное возбуждение; обострение или острая стадия хронического соматического заболевания; злоупотребление психоактивными веществами.
Группу сравнения составили 60 пациентов с длительностью заболевания более 5 лет и наличием более трех зарегистрированных эпизодов, в том числе 25 женщин и
35 мужчин (возраст 34,95+7,38 года).
Контрольную группу (n=30) составили здоровые испытуемые, сопоставимые по возрасту, полу и уровню образования, без психиатрических и тяжелых соматических заболеваний.
В исследовании использовались клинико-психопатологическая метод и Шкала краткой оценки когнитивных функций у пациентов с шизофренией (BACS). Взятие венозной крови проводили однократно в соответствии с общими правилами сбора материала для иммунологических исследований. Лабораторные методы (ELISA, Milliplex human Th17 magnetic bead panel — 25 аналитов) включали определение CCL20/MIP3, IL-10, IL-12P70, IL-13, IL-15, IL-17A, IL-17E/IL-25, IL-17F, IL-1-бэта, IL-2, IL-21, IL-22, IL-23, IL-27, IL-31, IL-33, IL-4, IL-5, Il-6, IL-9, TNF-альфа, TNF-бэта, C-реактивный белок.
Для оценки значимости различий между исследуемыми группами применялся критерий Манна-Уитни, проводился корреляционный и регрессионный анализ.
Результаты
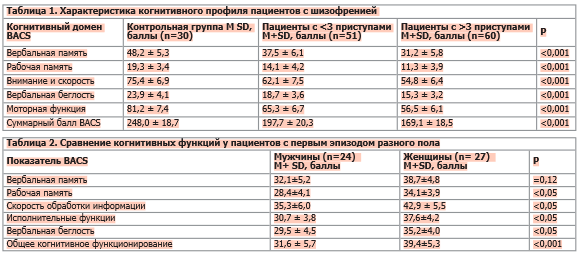
По данным BACS были выявлены значимые различия между группами исследования по всем когнитивным доменам (p < 0,001). Пациенты с шизофренией (как с первым эпизодом, так и с хроническим течением) показали более низкие результаты по сравнению с контрольной группой. При этом пациенты с хронической шизофренией демонстрировали более выраженный когнитивный дефицит, чем пациенты с 3 и менее эпизодами (табл. 1).
По большинству когнитивных показателей (рабочая память, скорость обработки информации, исполнительные функции, вербальная беглость и общее когнитивное функционирование) женщины отличались по сравнению с мужчинами в лучшую сторону (табл. 2). По показателю вербальной памяти различия не достигли статистической значимости.
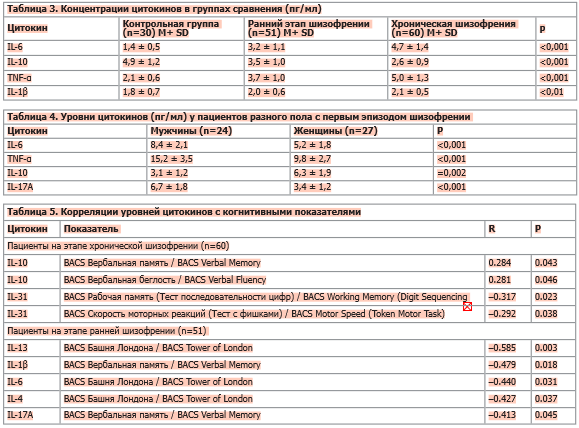
Повышенные уровни IL-6 и TNF-α, а также сниженные уровни IL-10 наблюдались как при первом эпизоде шизофрении, так и при хроническом течении заболевания по сравнению с контролем. Наибольшие изменения показателей выявлены у пациентов с 3 и более эпизодами шизофрении (табл. 3). Различий в уровнях других исследованных цитокинов у пациентов с первым эпизодом шизофрении и хронической шизофренией обнаружено не было.
У пациентов мужского пола показатели воспаления выражены больше по сравнению с женщинами, а у женщин выше по сравнению с мужчинами противовоспалительный цитокин IL-10 (табл. 4).
Полученные данные свидетельствуют, что более высокие показатели противовоспалительного маркера IL-10 у женщин соответствуют более высоким показателям когнитивного функционирования по BACS, в то время как более высокие показатели провоспалительных маркеров у мужчин IL-6 и TNF-α соответствуют более низким показателям BACS.
На этапе хронической шизофрении число рецидивов отрицательно коррелирует с показателями когнитивного функционирования. У пациентов с 3 и менее рецидивами число приступов значимо не связано с когнитивными показателями. Таким образом, именно множественные рецидивы связаны с более выраженным снижением когнитивных функций, особенно в области моторных навыков (r = -0.35, p < 0.01), планирования (тест «Башня Лондона») (r = -0.34, p < 0.01) и вербальной памяти (r = -0.33, p < 0.01).
В группе первого эпизода наблюдается системный отрицательный эффект провоспалительной активации в отношении когнитивных функций пациентов: более высокие уровни IL-13, IL-6 и IL-4 связаны с ухудшением исполнительных функций, IL-1β и IL-17A ассоциированы со снижением вербальной памяти. Противовоспалительный IL-10 не демонстрирует значимых связей с когнитивными доменами на ранних стадиях заболевания. У хронических пациентов отмечены умеренные положительные связи IL-10 с вербальной памятью и вербальной беглостью, что указывает на возможную протективную роль противовоспалительной регуляции в поддержании когнитивных функций при длительном течении шизофрении. Одновременно IL-31 отрицательно связан со скоростью обработки информации и моторикой (табл. 5).
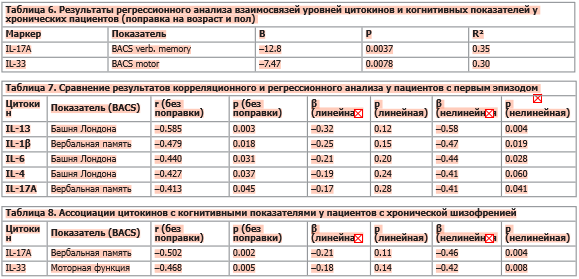
Регрессионные модели с поправкой на возраст и пол воспроизводят и уточняют взаимосвязи уровней цитокинов и когнитивных параметров: при хронической шизофрении уровни IL-17A и IL-33 оказались связаны с показателями вербальной памяти и моторики (табл. 6). В группе первого эпизода корреляции между уровнями цитокинов и когнитивными функциями исчезали после введения поправки на возраст и пол. Это может отражать как более узкий возрастной диапазон и меньшую выраженность когнитивного дефицита на ранних стадиях, так и значимую роль демографических характеристик в формировании наблюдаемых ассоциаций. Вклад иммуновоспалительных маркеров не достигает статистически устойчивого уровня. В отличие от этого, у хронических пациентов ассоциации сохраняются после поправки, что указывает на их независимый и более стабильный характер.
Уровни ключевых цитокинов (например, IL-6, IL-1β, IL-13) положительно связаны с возрастом (ρ в диапазоне 0.35-0.45, p < 0.01). Одновременно возраст отрицательно коррелирует с когнитивными шкалами (BACS London, BACS Verbal Memory: ρ около —0.40…-0.45, p < 0.01). Таким образом, пациенты более старшего возраста имели как более высокий уровень воспалительных маркеров, так и худшие когнитивные показатели. Это создавало видимость прямых связей между цитокинами и когницией: при включении возраста в качестве ковариаты объясняющая способность исходных ассоциаций исчезала, поскольку она приходилась именно на возраст. Пол также оказывал влияние: у мужчин медианы IL-6 и TNFα были выше, чем у женщин (p ≈ 0.04-0.05). Однако решающим фактором оказался именно возраст: поправка на него устраняла все исходные корреляции в группе первого эпизода, тогда как влияние пола имело лишь дополнительный характер. При проведении регрессионного анализа с учетом этих ковариат было показано, что ассоциации между уровнями цитокинов и когнитивными показателями на ранних стадиях шизофрении теряют статистическую значимость при использовании стандартной линейной поправки. Этот результат подтверждает существенное влияние возрастно-половой структуры выборки на когнитивное функционирование больных. Вместе с тем применение более гибкого подхода — моделирования нелинейного эффекта возраста с помощью сплайнов — позволило установить взаимосвязи между уровнями IL-13 и IL-6 с показателями исполнительных функций (тест «Башня Лондона»), а IL-1β и IL-17A — с показателями вербальной памяти (табл. 7).
Аналогичный паттерн наблюдается и у пациентов с хроническим течением заболевания: линейная поправка устраняет значимость исходных связей IL-17A с вербальной памятью и IL-33 с моторной функцией, однако при использовании нелинейного моделирования возраста ассоциации восстанавливаются и остаются статистически значимыми. Это указывает на то, что базовые корреляции не сводятся исключительно к возрастным или половым искажениям, а отражают устойчивые связи между воспалительными маркерами и когнитивными нарушениями на разных стадиях заболевания (табл. 8).
Обсуждение
Результаты исследования подтвердили наши более ранние данные и данные литературы о заметном снижении нейрокогнитивных функций у пациентов с первым эпизодом шизофрении по сравнению с контрольной группой здоровых лиц [1, 2, 22]. Когнитивный профиль пациентов с первым эпизодом отличается в лучшую сторону по сравнению с хронической шизофренией. Следует отметить, что нейрокогнитивный дефицит сохранялся у пациентов с первым эпизодом в период устойчивой лекарственной ремиссии. У женщин нейрокогнитивный дефицит выражен в меньшей степени по сравнению с пациентами мужского пола.
Сложная взаимосвязь между системным воспалением и мозгом может играть определенную роль в развитии шизофрении [33]. Результаты нейровизуализационных исследований связали полиморфизмы генов провоспалительных цитокинов с некоторыми структурными и функциональными изменениями, встречающимися при шизофрении [34]. При шизофрении наблюдаются измененные уровни цитокинов и цитокиновых рецепторов [35]. В метаанализе Miller с соавт. было показано значительное повышение уровня фактора некроза опухолей (TNF-α), IL-1β, IL-6 и IL-12 у пациентов с первым психотическим эпизодом [36]. Полученные нами результаты свидетельствуют, что уровень цитокинов IL-1β, IL-6, TNF-α повышен у пациентов на раннем этапе шизофрении и в ремиссии по сравнению с контрольной группой, но ниже по сравнению с хронической шизофренией.
IL-10 — противовоспалительный цитокин, способный блокировать действие провоспалительных цитокинов и играющий роль негативного модулятора как иммунопролиферативных, так и воспалительных реакций в головном мозге. В работе Wang с соавт. (2021) был подтвержден нейропротекторный эффект IL-10 при шизофрении [37]. В литературе имеются данные, что у пациентов с первым эпизодом шизофрении не наблюдается значительных изменений в уровнях противовоспалительных цитокинов IL-4 и IL-10 [38]. В нашем исследовании наблюдались заметные различия уровня IL-10 в группах сравнения и по сравнению с контролем, причем у пациентов с хронической шизофренией уровень был ниже, чем у пациентов с первым эпизодом. Результаты соответствуют данным Lesh с соавт. о том, что уровень IL-10 у пациентов с шизофренией снижен на 19,6% по сравнению с контрольной группой (p = 0,04). Снижение уровня IL-10 демонстрировало обратную корреляцию с длительностью нелеченого психоза (r = -0.29, p = 0.03), что, по мнению автора, может свидетельствовать о том, что снижение противовоспалительной активности IL-10 способствует прогрессированию заболевания и ухудшению клинических исходов [31]. У женщин уровень противовоспалительного цитокина IL-10 выше, чем у мужчин, что коррелирует с большей сохранностью у них нейрокогнитивных функций.
В доступной литературе имеется несколько работ, посвященных анализу взаимосвязи когнитивных функций и цитокинов на раннем этапе шизофрении. В поперечном исследовании случай-контроль Baek с соавт. (2022) изучали эффекты взаимодействия между когнитивной функцией и воспалительными цитокинами и мозговым нейротрофическим фактором (BDNF) при первом эпизоде шизофрении. Пациенты с шизофренией продемонстрировали повышенные уровни IL-1β и IL-6, сниженные уровни BDNF и сниженные показатели когнитивного функционирования (все p < 0,001). Скорость обработки информации отрицательно коррелировала с IL-6 (r = -0,315, P < 0,05) и положительно с BDNF (r = 0,290, P < 0,05); внимание, рабочая память, исполнительные функции отрицательно коррелировали с IL-1β и IL-6 (все p < 0,05) и положительно с BDNF (все p <0,05). Множественный регрессионный анализ показал, что IL-6 влияет на когнитивные параметры (β = -0,218 до -0,327, все p < 0,05); IL-1β — на внимание и исполнительные способности (β = -0,199 до -0,261, все p < 0,05); на исполнительные способности влияет BDNF (β = 0,209, p < 0,05). Авторы сделали вывод, что взаимосвязь между иммунной дисфункцией и нейротрофическим дефицитом может лежать в основе механизмов когнитивных нарушений у пациентов с первым эпизодом шизофрении [39]. Целью метаанализа Cui с соавт. (2024) явилось изучение взаимосвязи между медиаторами воспаления, такими как провоспалительные цитокины и С-реактивный белок, а также BDNF и когнитивными нарушениями при шизофрении. Было включено в общей сложности 25 исследований, 84 пациента с первым эпизодом шизофрении и 80 здоровых добровольцев. У пациентов с первым эпизодом шизофрении наблюдалось выраженное снижение когнитивных функций, особенно по показателям скорости обработки информации, внимания, рабочей памяти и исполнительных функций. Уровни IL-1β и IL-6 в группе шизофрении были выше, чем в контрольной группе (все p < 0,001), в то время как уровень BDNF был снижен. Изменения этих биомаркеров оказались тесно связаны с когнитивной дисфункцией. Показатель скорости обработки информации отрицательно коррелировал с IL-6 (r = -0,315, P < 0,05); внимание отрицательно коррелировало с IL-1β и IL-6 (r = -0,226, -0,412, все P < 0,05); рабочая память отрицательно коррелировала с IL-1β и IL-6 (r = -0,324, -0,236, все P < 0,05), исполнительная способность отрицательно коррелировала с IL-1β и IL-6 (r = -0,284, -0,386, все P < 0,05). Таким образом, IL-1β и IL-6 были расценены как факторы риска когнитивных нарушений, нарушающие передачу сигналов между нейронами. Была отмечена значительная роль воспалительных цитокинов и нейротрофических факторов в развитии когнитивных нарушений у пациентов с первым эпизодом шизофрении [22].
В исследовании Chen с соавт. (2023) оценивали уровни IL-2, IL-6, TNF-α и С-реактивного белка и когнитивные функции у 26, 35 и 29 подростков с первым эпизодом шизофрении, биполярным расстройством и большим депрессивным расстройством соответственно. Для оценки когнитивных функций использовались Висконсинский тест сортировки карточек (WCST) и тест на рабочую память. Было установлено, что у пациентов с биполярным расстройством наблюдались самые высокие уровни С-реактивного белка (p = 0,023), IL-6 (p = 0,022) и TNF-α (p = 0,011) и самые низкие уровни IL-2 (p = 0,034). Подростки с шизофренией продемонстрировали самые низкие показатели когнитивных функций. В этой группе только уровень С-реактивного белка был отрицательно связан с показателями WCST. Таким образом, нарушение регуляции про- и противовоспалительных цитокинов, а также снижение когнитивных функций наблюдались как при первом эпизоде подростковой шизофрении, так и при биполярном расстройстве и большом депрессивном расстройстве [40].
Заключение
Полученные данные свидетельствуют о повышенном уровне цитокинов в период ремиссии на раннем этапе шизофрении, что отражает сохраняющуюся активность процесса. Показательными служат повышение уровней IL-6, IL-1β и TNF-α и снижение IL-10. Динамика уровня IL-10 отражает уменьшение его протективной функции в процессе прогрессирования заболевания. У женщин определяется менее выраженный иммунный ответ в сравнении с пациентами мужского пола, что соотносится с меньшим нейрокогнитивным дефицитом.
Проведенное исследование продемонстрировало выраженные нейрокогнитивные нарушения у пациентов с первым эпизодом шизофрении в ремиссии, особенно у мужчин. Наибольшее снижение установлено по показателям рабочей памяти, вербального обучения и скорости обработки информации.
Показано, что число рецидивов шизофрении влияет на уровень когнитивного функционирования и уровень цитокинов, причем критическим является третий приступ.
Результаты исследования демонстрируют взаимосвязь между иммунной дисфункцией и нейрокогнитивным дефицитом при шизофрении как на ранних, так и на отдаленных этапах заболевания. В нашем исследовании выявлены корреляции ряда цитокинов с определенными показателями когнитивного функционирования. Демографические факторы вносят значимый вклад в вариабельность исходных данных, однако при корректном учете нелинейного влияния возраста сохраняется ряд ассоциаций. В группе пациентов с первым эпизодом шизофрении в ремиссии выявлены корреляции ряда провоспалительных цитокинов с ухудшением исполнительных функций и вербальной памяти. Противовоспалительный IL-10 не демонстрирует значимых связей с когнитивными доменами на ранних стадиях заболевания в ремиссии. Характер взаимосвязи цитокинов и когнитивных функций меняется по мере прогрессирования заболевания.
Результаты исследования подтверждают, что когнитивный дефицит при шизофрении не является статичным, а формируется в динамике заболевания, где хроническое воспаление может выступать в качестве одного из ключевых механизмов его прогрессирования.
Полученные данные, подкрепленные современными исследованиями, подчеркивают важность воспалительных процессов в патогенезе когнитивных нарушений при шизофрении и открывают перспективы для разработки новых терапевтических стратегий, направленных на модуляцию иммунного ответа с целью улучшения когнитивных функций у пациентов с шизофренией.
Ограничения исследования
Полученные данные подчеркивают необходимость более крупных выборок и применения гибких статистических моделей в будущих исследованиях для точной идентификации иммунно-когнитивных связей при шизофрении.
Дата поступления: 20.09.2025
Received: 20.09.2025
Принята к печати: 02.12.2025
Accepted: 02.12.2025
Автор заявляет об отсутствии конфликта интересов.
Author declares no conflicts of interest.
Информация об авторах:
Альпин В.С. — https://orcid.org/0000-0002-3404-0786
Петрова Н.Н. — https://orcid.org/0000-0003-4096-6208
Дорофейков В.В. — https://orcid.org/0000-0002-7272-1654
Слепой В.В. - https://orcid.org/0009-0009-3945-7837
Автор, ответственный за переписку: Петрова Н.Н. — e-mail: petrova_nn@mail.ru
Information about the authors:
Alpin V.S. — https://orcid.org/0000-0002-3404-0786
Petrova N.N. — https://orcid.org/0000-0003-4096-6208
Dorofeykov V.V. — https://orcid.org/0000-0002-7272-1654
Slepoy V.V. - https://orcid.org/0009-0009-3945-7837
Corresponding author: Petrova N.N. — e-mail: petrova_nn@mail.ru
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№06 2025
Нейрокогнитивный профиль и цитокины у пациентов в ремиссии на раннем этапе шизофрении №06 2025
Номера страниц в выпуске:36-42
Резюме
Введение. Нейрокогнитивный дефицит при шизофрении представляет собой актуальную проблему теоретической и клинической психиатрии.
В настоящее время имеется крайне мало исследований взаимосвязи характеристик когнитивного функционирования пациентов с первым эпизодом шизофрении и иммунологических показателей.
Цель исследования: изучение нейрокогнитивного профиля и уровня цитокинов у пациентов с первым эпизодом шизофрении в ремиссии.
Материал и методы. На этапе устойчивой лекарственной ремиссии (более 6 месяцев) был обследован 51 пациент с диагнозом F20.0 «Параноидная шизофрения» (возраст 28,3±5,8 года). Критерии включения: верифицированный диагноз F20.0 «Шизофрения параноидная» (согласно диагностическим критериям МКБ-10), длительность заболевания не более 5 лет и количество госпитализаций не более 3. Группу сравнения составили 60 пациентов с длительностью заболевания более 5 лет и наличием более трех зарегистрированных эпизодов, в том числе 25 женщин и 35 мужчин (возраст 34,95±7,38 года). Контрольную группу (n=30) составили здоровые испытуемые, сопоставимые по возрасту, полу и уровню образования, без психиатрических и тяжелых соматических заболеваний. В исследовании использовались клинико-психопатологическая метод и Шкала краткой оценки когнитивных функций у пациентов с шизофренией (BACS). Взятие венозной крови проводили однократно в соответствии с общими правилами сбора материала для иммунологических исследований. Лабораторные методы (ELISA, Milliplex human Th17 magnetic bead panel — 25 аналитов) включали определение цитокинов, C-реактивного белка.
Результаты. Полученные данные свидетельствуют о повышенном уровне ряда цитокинов в период ремиссии на раннем этапе шизофрении (IL-6, IL-1β и TNF-α). Динамика уровня IL-10 отражает уменьшение его протективной функции в процессе прогрессирования заболевания. У женщин определяется менее выраженный иммунный ответ в сравнении с пациентами мужского пола, что соотносится с меньшим нейрокогнитивным дефицитом. Выявлены выраженные нейрокогнитивные нарушения у пациентов с первым эпизодом шизофрении в ремиссии, особенно у мужчин. Наибольшее снижение установлено по показателям рабочей памяти, вербального обучения и скорости обработки информации. Число рецидивов шизофрении влияет на уровень когнитивного функционирования и уровень цитокинов. Результаты исследования демонстрируют взаимосвязь между иммунной дисфункцией и нейрокогнитивным дефицитом при шизофрении как на ранних, так и на отдаленных этапах заболевания. Выявлены корреляции ряда цитокинов с определенными показателями когнитивного функционирования. Демографические факторы вносят значимый вклад в вариабельность исходных данных. В группе пациентов с первым эпизодом шизофрении в ремиссии выявлены корреляции ряда провоспалительных цитокинов с ухудшением исполнительных функций и вербальной памяти. Противовоспалительный IL-10 не демонстрирует значимых связей с когнитивными доменами на ранних стадиях заболевания в ремиссии. Характер взаимосвязи цитокинов и когнитивных функций меняется по мере прогрессирования заболевания.
Заключение. Результаты исследования подтверждают, что когнитивный дефицит при шизофрении не является статичным, а формируется в динамике заболевания, где хроническое воспаление может выступать в качестве одного из ключевых механизмов его прогрессирования. Полученные данные, подкрепленные современными исследованиями, подчеркивают важность воспалительных процессов в патогенезе когнитивных нарушений при шизофрении.
Ключевые слова: шизофрения; нейрокогнитивный дефицит; воспаление; цитокины.
Для цитирования: Альпин В.С., Петрова Н.Н., Дорофейков В.В., Слепой В.В.. Нейрокогнитивный профиль и цитокины у пациентов в ремиссии
на раннем этапе шизофрении. Психиатрия и психофармакотерапия. 2025; 6: 36–42. DOI: 10.62202/2075-1761-2025-27-6-36-42
Введение. Нейрокогнитивный дефицит при шизофрении представляет собой актуальную проблему теоретической и клинической психиатрии.
В настоящее время имеется крайне мало исследований взаимосвязи характеристик когнитивного функционирования пациентов с первым эпизодом шизофрении и иммунологических показателей.
Цель исследования: изучение нейрокогнитивного профиля и уровня цитокинов у пациентов с первым эпизодом шизофрении в ремиссии.
Материал и методы. На этапе устойчивой лекарственной ремиссии (более 6 месяцев) был обследован 51 пациент с диагнозом F20.0 «Параноидная шизофрения» (возраст 28,3±5,8 года). Критерии включения: верифицированный диагноз F20.0 «Шизофрения параноидная» (согласно диагностическим критериям МКБ-10), длительность заболевания не более 5 лет и количество госпитализаций не более 3. Группу сравнения составили 60 пациентов с длительностью заболевания более 5 лет и наличием более трех зарегистрированных эпизодов, в том числе 25 женщин и 35 мужчин (возраст 34,95±7,38 года). Контрольную группу (n=30) составили здоровые испытуемые, сопоставимые по возрасту, полу и уровню образования, без психиатрических и тяжелых соматических заболеваний. В исследовании использовались клинико-психопатологическая метод и Шкала краткой оценки когнитивных функций у пациентов с шизофренией (BACS). Взятие венозной крови проводили однократно в соответствии с общими правилами сбора материала для иммунологических исследований. Лабораторные методы (ELISA, Milliplex human Th17 magnetic bead panel — 25 аналитов) включали определение цитокинов, C-реактивного белка.
Результаты. Полученные данные свидетельствуют о повышенном уровне ряда цитокинов в период ремиссии на раннем этапе шизофрении (IL-6, IL-1β и TNF-α). Динамика уровня IL-10 отражает уменьшение его протективной функции в процессе прогрессирования заболевания. У женщин определяется менее выраженный иммунный ответ в сравнении с пациентами мужского пола, что соотносится с меньшим нейрокогнитивным дефицитом. Выявлены выраженные нейрокогнитивные нарушения у пациентов с первым эпизодом шизофрении в ремиссии, особенно у мужчин. Наибольшее снижение установлено по показателям рабочей памяти, вербального обучения и скорости обработки информации. Число рецидивов шизофрении влияет на уровень когнитивного функционирования и уровень цитокинов. Результаты исследования демонстрируют взаимосвязь между иммунной дисфункцией и нейрокогнитивным дефицитом при шизофрении как на ранних, так и на отдаленных этапах заболевания. Выявлены корреляции ряда цитокинов с определенными показателями когнитивного функционирования. Демографические факторы вносят значимый вклад в вариабельность исходных данных. В группе пациентов с первым эпизодом шизофрении в ремиссии выявлены корреляции ряда провоспалительных цитокинов с ухудшением исполнительных функций и вербальной памяти. Противовоспалительный IL-10 не демонстрирует значимых связей с когнитивными доменами на ранних стадиях заболевания в ремиссии. Характер взаимосвязи цитокинов и когнитивных функций меняется по мере прогрессирования заболевания.
Заключение. Результаты исследования подтверждают, что когнитивный дефицит при шизофрении не является статичным, а формируется в динамике заболевания, где хроническое воспаление может выступать в качестве одного из ключевых механизмов его прогрессирования. Полученные данные, подкрепленные современными исследованиями, подчеркивают важность воспалительных процессов в патогенезе когнитивных нарушений при шизофрении.
Ключевые слова: шизофрения; нейрокогнитивный дефицит; воспаление; цитокины.
Для цитирования: Альпин В.С., Петрова Н.Н., Дорофейков В.В., Слепой В.В.. Нейрокогнитивный профиль и цитокины у пациентов в ремиссии
на раннем этапе шизофрении. Психиатрия и психофармакотерапия. 2025; 6: 36–42. DOI: 10.62202/2075-1761-2025-27-6-36-42
Neurocognitive profile and cytokines in patients inremission at the early stage of schizophrenia
Alpin V.S.1,4, Petrova N.N.1,2, Dorofeykov V.V.3, Slepoy V.V.41 Bekhtereva Institute of the Human Brain of the Russian Academy of Sciences, SaintPetersburg, Russia;
2 St. Petersburg State University, St. Petersburg, Russia;
3 Lesgaft National State University of Physical Culture, Sports and Health, St.Petersburg, Russia;
4 Almazov National Medical Research Center of the Ministry of Health of the Russian Federation, St. Petersburg, Russia
Abstract
Introduction. Neurocognitive deficit in schizophrenia is a topical issue in theoretical and clinical psychiatry. Currently, there are very few studies on the relationship between the characteristics of cognitive functioning of patients with the first episode of schizophrenia and immunological parameters.
Objective: to study the neurocognitive profile and cytokine levels in patients with the first episode of schizophrenia in remission.
Material and methods. At the stage of stable drug remission (more than 6 months), 51 patients with a diagnosis of F20.0 "Paranoid schizophrenia" (age 28.3±5.8 years) were examined. Inclusion criteria: verified diagnosis F20.0 "Paranoid schizophrenia" (according to the diagnostic criteria of ICD-10), disease duration of no more than 5 years and the number of hospitalizations of no more than 3. The comparison group consisted of 60 patients with a disease duration of more than 5 years and more than three registered episodes, including 25 women and 35 men (age 34.95±7.38 years). The control group (n=30) consisted of healthy subjects matched for age, gender and education level, without psychiatric and severe somatic diseases. The study used the clinical and psychopathological method and the Brief Assessment of Cognitive Functions in Schizophrenia (BACS) Scale. Venous blood was taken once in accordance with the general rules for collecting material for immunological studies. Laboratory methods (ELISA, Milliplex human Th17 magnetic bead panel — 25 analytes) included determination of cytokines, C-reactive protein.
Results. The obtained data indicate an increased level of some cytokines during remission at the early stage of schizophrenia (IL-6, IL-1β and TNF-α). The dynamics of the IL-10 level reflects a decrease in its protective function during disease progression. In women, a less pronounced immune response is determined compared to male patients, which correlates with a smaller neurocognitive deficit. Pronounced neurocognitive impairments were revealed in patients with the first episode of schizophrenia in remission, especially in men. The greatest decrease was found in working memory, verbal learning and information processing speed. The number of schizophrenia relapses affects the level of cognitive functioning and the level of cytokines. The results of the study demonstrate the relationship between immune dysfunction and neurocognitive deficit in schizophrenia both at early and late stages of the disease. Correlations of a number of cytokines with certain indicators of cognitive functioning were revealed. Demographic factors make a significant contribution to the variability of the initial data. In the group of patients with the first episode of schizophrenia in remission, correlations of a number of proinflammatory cytokines with the deterioration of executive functions and verbal memory were revealed. Anti-inflammatory IL-10 does not demonstrate significant relationships with cognitive domains at the early stages of the disease in remission. The nature of the relationship between cytokines and cognitive functions changes as the disease progresses.
Conclusion. The results of the study confirm that cognitive deficit in schizophrenia is not static, but is formed in the dynamics of the disease, where chronic inflammation can act as one of the key mechanisms of its progression. The obtained data, supported by modern research, emphasize the importance of inflammatory processes in the pathogenesis of cognitive impairment in schizophrenia.
Keywords: schizophrenia; neurocognitive deficit; inflammation; cytokines
For citation: Alpin V.S., Petrova N.N., Dorofeykov V.V., Slepoy V.V. Neurocognitive profile and cytokines in patients inremission at the early stage of schizophrenia. Psychiatry and psychopharmacotherapy. 2025; 6: 36–42. DOI: 10.62202/2075-1761-2025-27-6-36-42
Введение
Снижение когнитивных функций происходит на ранних стадиях шизофрении и сохраняется на протяжении всей болезни [1, 2]. Нейрокогнитивный дефицит — один из наиболее значимых факторов, влияющих на функционирование пациентов с шизофренией, такие как независимая жизнь, социальное и профессиональное функционирование [3]. Нейрокогнитивный дефицит включает снижение памяти, способности концентрировать внимание и исполнительных функций (проблемы с планированием, организацией и решением задач) [4].
Биологические механизмы, лежащие в основе снижения когнитивных функций при шизофрении, в значительной степени остаются неизвестными [5]. Ряд исследований показывает, что нарушенная регуляция нейробиохимических процессов и иммуновоспалительные реакции могут лежать в основе когнитивных дефицитов, наблюдаемых у пациентов с шизофренией [6-9].
Цитокины, как иммунные медиаторы, участвуют в механизмах синаптической пластичности, тесно связанных с когнитивными функциями [10]. Мишенями цитокинов в мозге являются нейротрансмиттеры и нейроцепи. Активация воспалительной реакции приводит к высвобождению воспалительных цитокинов и мобилизации иммунных клеток, которые проникают в мозг и изменяют поведение. Цитокины и их сигнальные пути, включая митоген-активируемую протеинкиназу p38, оказывают существенное влияние на метаболизм нейротрансмиттеров, таких как серотонин, дофамин и глутамат, через воздействие на их синтез, высвобождение и обратный захват. Цитокины активируют кинурениновый путь, который не только истощает триптофан, первичный аминокислотный предшественник серотонина, но и генерирует нейроактивные метаболиты, которые могут существенно влиять на регуляцию дофамина и глутамата. Через нейротрансмиттерные системы цитокины воздействуют на нейросети головного мозга, включая базальные ганглии и переднюю поясную извилину [11]. Имеются данные, что повышенные периферические воспалительные биомаркеры связаны с уменьшением толщины коры [12] и объема мозга [13] в областях, ответственных за некоторые когнитивные функции (например, внимание, визуальное обучение, беглость речи).
Локальная и системная активация врожденных иммунных реакций в мозге [14] может приводить к снижению когнитивных функций у здоровых и больных людей [15, 16]. Известно, что нарушения нейроразвития у подростков приводят к аномальной синаптической пластичности, связанной с когнитивным дефицитом [17]. Лонгитюдное исследование на протяжении двадцати лет показало, что системное воспаление во взрослом возрасте связано со снижением когнитивных функций у здоровых взрослых [18].
Такие цитокины, как TNF-α, IL-6 и IL-1, могут существенно влиять на когнитивные функции, главным образом на память [19-21]. Имеются данные, что повышенные уровни IL-1β и IL-6 связаны со снижением внимания, нарушениями рабочей памяти и исполнительной функции [22]. Повышенная экспрессия IL-1β может вызвать локализованное и постоянное воспаление в гиппокампе, препятствуя формированию памяти [23].
Модулируя развитие нейронов [24, 25] и пластичность синапсов [26], цитокины могут участвовать в формировании когнитивных и поведенческих нарушений, структурных аномалий мозга, наблюдаемым при психозах [27].
Нарушение взаимодействия между микроглиальными клетками и цитокинами может вызывать нейродегенеративные процессы при нейропсихиатрических заболеваниях, в том числе шизофрении [28].
Ribeiro-Santos с соавт. (2020) установили значимые отрицательные корреляции между некоторыми биомаркерами воспаления и когнитивными функциями у пациентов с шизофренией [29].
Систематический обзор Misiak c cоавт. (2018) выявил, что наиболее последовательные результаты указывают на худшие когнитивные функции у пациентов с шизофренией с более высоким уровнем С-реактивного белка. Менее последовательные данные свидетельствуют о лучшем когнитивном функционировании у пациентов с шизофренией с более высоким уровнем TNF-α. Доказательства участия других цитокинов в когнитивных нарушениях у пациентов с шизофренией менее убедительны из-за противоречивых результатов или небольшого количества исследований [30].
В исследовании Lesh с соавт. (2018) повышенные уровни TNF-α ассоциированы с уменьшением объема префронтальной коры (β = -0.32, p = 0.01), что может объяснять нарушения исполнительных функций и когнитивного контроля у пациентов. Повышенные уровни IL-1β коррелировали с нарушением исполнительных функций по результатам теста Струпа (r = -0.38, p = 0.02). Данные указывают на возможную связь между воспалительными процессами, опосредованными IL-1β, и когнитивным дефицитом при шизофрении [31].
Имеются данные о наличии корреляции между повышенными уровнями IL-6 и нарушенной обработкой информации у больных шизофренией [7]. В то же время Hori с соавт. (2017) не выявили связи между IL-6 и фактором некроза опухоли альфа (TNF) с когнитивными функциями у больных хронической шизофренией [32].
Установлено, что связь между когнитивной функцией и уровнем IL-18 при хронической шизофрении зависит от полиморфизма IL-18 -607 A/C. Уровни и генотип IL-18 были измерены у 693 госпитализированных пациентов и 422 контрольных лиц. Уровни сывороточного IL-18 были выше у пациентов, чем у здоровых лиц контрольной группы. Полиморфизм IL-18 -607 A/C коррелировал со зрительно-пространственным/конструктивным индексом только у больных шизофренией, а уровень IL-18 коррелировал с памятью только у пациентов с генотипом C/C, но не у пациентов с генотипами C/A или A/A. Таким образом, полиморфизм IL18 -607A/C и уровни сывороточного IL-18 были связаны с когнитивными нарушениями у пациентов с шизофренией [19].
Результаты метаанализа Patlola с соавт. (2023) продемонстрировали обратную зависимость между показателями в пяти когнитивных областях (скорость внимания, исполнительные функции, рабочая память, вербальное и визуальное обучение и память) и уровнями IL-6, IL-1β, TNF-α и С-реактивного белка в плазме крови у пациентов с шизофренией. Результаты метаанализа показывают, что когнитивные нарушения обусловлены повышенным уровнем этих провоспалительных биомаркеров [10].
В настоящее время имеется крайне мало исследований взаимосвязи провоспалительных и противовоспалительных цитокинов с когнитивной функцией у пациентов с первым эпизодом шизофрении.
Целью данного исследования было изучение нейрокогнитивного профиля и уровня цитокинов у пациентов с первым эпизодом шизофрении в ремиссии.
Материал и методы исследования
На этапе устойчивой лекарственной ремиссии (более 6 месяцев) был обследован 51 пациент с диагнозом F20.0 «Параноидная шизофрения» (возраст 28,3+5,8 года). Длительность заболевания составила 2,7±1,3 года. Средний возраст начала заболевания — 25,8+5,5 года. Доля женщин составила 53%, мужчин — 47%. Среднее число рецидивов достигло 1,77+0,69 случая. У 40% пациентов наблюдался один перенесенный эпизод, у 50% — два и у 10% — три перенесенных эпизода. Таким образом, пациенты основной группы соответствовали понятию первого эпизода шизофрении, находились на раннем этапе заболевания.
Критерии включения: верифицированный диагноз F20.0 «Шизофрения параноидная» (согласно диагностическим критериям МКБ-10), длительность заболевания не более
5 лет и количество госпитализаций не более 3.
Критерии исключения: органическое поражение головного мозга или тяжелые неврологические заболевания; обострение психоза, включая психомоторное возбуждение; обострение или острая стадия хронического соматического заболевания; злоупотребление психоактивными веществами.
Группу сравнения составили 60 пациентов с длительностью заболевания более 5 лет и наличием более трех зарегистрированных эпизодов, в том числе 25 женщин и
35 мужчин (возраст 34,95+7,38 года).
Контрольную группу (n=30) составили здоровые испытуемые, сопоставимые по возрасту, полу и уровню образования, без психиатрических и тяжелых соматических заболеваний.
В исследовании использовались клинико-психопатологическая метод и Шкала краткой оценки когнитивных функций у пациентов с шизофренией (BACS). Взятие венозной крови проводили однократно в соответствии с общими правилами сбора материала для иммунологических исследований. Лабораторные методы (ELISA, Milliplex human Th17 magnetic bead panel — 25 аналитов) включали определение CCL20/MIP3, IL-10, IL-12P70, IL-13, IL-15, IL-17A, IL-17E/IL-25, IL-17F, IL-1-бэта, IL-2, IL-21, IL-22, IL-23, IL-27, IL-31, IL-33, IL-4, IL-5, Il-6, IL-9, TNF-альфа, TNF-бэта, C-реактивный белок.
Для оценки значимости различий между исследуемыми группами применялся критерий Манна-Уитни, проводился корреляционный и регрессионный анализ.
Результаты


По данным BACS были выявлены значимые различия между группами исследования по всем когнитивным доменам (p < 0,001). Пациенты с шизофренией (как с первым эпизодом, так и с хроническим течением) показали более низкие результаты по сравнению с контрольной группой. При этом пациенты с хронической шизофренией демонстрировали более выраженный когнитивный дефицит, чем пациенты с 3 и менее эпизодами (табл. 1).
По большинству когнитивных показателей (рабочая память, скорость обработки информации, исполнительные функции, вербальная беглость и общее когнитивное функционирование) женщины отличались по сравнению с мужчинами в лучшую сторону (табл. 2). По показателю вербальной памяти различия не достигли статистической значимости.
Повышенные уровни IL-6 и TNF-α, а также сниженные уровни IL-10 наблюдались как при первом эпизоде шизофрении, так и при хроническом течении заболевания по сравнению с контролем. Наибольшие изменения показателей выявлены у пациентов с 3 и более эпизодами шизофрении (табл. 3). Различий в уровнях других исследованных цитокинов у пациентов с первым эпизодом шизофрении и хронической шизофренией обнаружено не было.
У пациентов мужского пола показатели воспаления выражены больше по сравнению с женщинами, а у женщин выше по сравнению с мужчинами противовоспалительный цитокин IL-10 (табл. 4).
Полученные данные свидетельствуют, что более высокие показатели противовоспалительного маркера IL-10 у женщин соответствуют более высоким показателям когнитивного функционирования по BACS, в то время как более высокие показатели провоспалительных маркеров у мужчин IL-6 и TNF-α соответствуют более низким показателям BACS.
На этапе хронической шизофрении число рецидивов отрицательно коррелирует с показателями когнитивного функционирования. У пациентов с 3 и менее рецидивами число приступов значимо не связано с когнитивными показателями. Таким образом, именно множественные рецидивы связаны с более выраженным снижением когнитивных функций, особенно в области моторных навыков (r = -0.35, p < 0.01), планирования (тест «Башня Лондона») (r = -0.34, p < 0.01) и вербальной памяти (r = -0.33, p < 0.01).
В группе первого эпизода наблюдается системный отрицательный эффект провоспалительной активации в отношении когнитивных функций пациентов: более высокие уровни IL-13, IL-6 и IL-4 связаны с ухудшением исполнительных функций, IL-1β и IL-17A ассоциированы со снижением вербальной памяти. Противовоспалительный IL-10 не демонстрирует значимых связей с когнитивными доменами на ранних стадиях заболевания. У хронических пациентов отмечены умеренные положительные связи IL-10 с вербальной памятью и вербальной беглостью, что указывает на возможную протективную роль противовоспалительной регуляции в поддержании когнитивных функций при длительном течении шизофрении. Одновременно IL-31 отрицательно связан со скоростью обработки информации и моторикой (табл. 5).

Регрессионные модели с поправкой на возраст и пол воспроизводят и уточняют взаимосвязи уровней цитокинов и когнитивных параметров: при хронической шизофрении уровни IL-17A и IL-33 оказались связаны с показателями вербальной памяти и моторики (табл. 6). В группе первого эпизода корреляции между уровнями цитокинов и когнитивными функциями исчезали после введения поправки на возраст и пол. Это может отражать как более узкий возрастной диапазон и меньшую выраженность когнитивного дефицита на ранних стадиях, так и значимую роль демографических характеристик в формировании наблюдаемых ассоциаций. Вклад иммуновоспалительных маркеров не достигает статистически устойчивого уровня. В отличие от этого, у хронических пациентов ассоциации сохраняются после поправки, что указывает на их независимый и более стабильный характер.
Уровни ключевых цитокинов (например, IL-6, IL-1β, IL-13) положительно связаны с возрастом (ρ в диапазоне 0.35-0.45, p < 0.01). Одновременно возраст отрицательно коррелирует с когнитивными шкалами (BACS London, BACS Verbal Memory: ρ около —0.40…-0.45, p < 0.01). Таким образом, пациенты более старшего возраста имели как более высокий уровень воспалительных маркеров, так и худшие когнитивные показатели. Это создавало видимость прямых связей между цитокинами и когницией: при включении возраста в качестве ковариаты объясняющая способность исходных ассоциаций исчезала, поскольку она приходилась именно на возраст. Пол также оказывал влияние: у мужчин медианы IL-6 и TNFα были выше, чем у женщин (p ≈ 0.04-0.05). Однако решающим фактором оказался именно возраст: поправка на него устраняла все исходные корреляции в группе первого эпизода, тогда как влияние пола имело лишь дополнительный характер. При проведении регрессионного анализа с учетом этих ковариат было показано, что ассоциации между уровнями цитокинов и когнитивными показателями на ранних стадиях шизофрении теряют статистическую значимость при использовании стандартной линейной поправки. Этот результат подтверждает существенное влияние возрастно-половой структуры выборки на когнитивное функционирование больных. Вместе с тем применение более гибкого подхода — моделирования нелинейного эффекта возраста с помощью сплайнов — позволило установить взаимосвязи между уровнями IL-13 и IL-6 с показателями исполнительных функций (тест «Башня Лондона»), а IL-1β и IL-17A — с показателями вербальной памяти (табл. 7).
Аналогичный паттерн наблюдается и у пациентов с хроническим течением заболевания: линейная поправка устраняет значимость исходных связей IL-17A с вербальной памятью и IL-33 с моторной функцией, однако при использовании нелинейного моделирования возраста ассоциации восстанавливаются и остаются статистически значимыми. Это указывает на то, что базовые корреляции не сводятся исключительно к возрастным или половым искажениям, а отражают устойчивые связи между воспалительными маркерами и когнитивными нарушениями на разных стадиях заболевания (табл. 8).
Обсуждение
Результаты исследования подтвердили наши более ранние данные и данные литературы о заметном снижении нейрокогнитивных функций у пациентов с первым эпизодом шизофрении по сравнению с контрольной группой здоровых лиц [1, 2, 22]. Когнитивный профиль пациентов с первым эпизодом отличается в лучшую сторону по сравнению с хронической шизофренией. Следует отметить, что нейрокогнитивный дефицит сохранялся у пациентов с первым эпизодом в период устойчивой лекарственной ремиссии. У женщин нейрокогнитивный дефицит выражен в меньшей степени по сравнению с пациентами мужского пола.
Сложная взаимосвязь между системным воспалением и мозгом может играть определенную роль в развитии шизофрении [33]. Результаты нейровизуализационных исследований связали полиморфизмы генов провоспалительных цитокинов с некоторыми структурными и функциональными изменениями, встречающимися при шизофрении [34]. При шизофрении наблюдаются измененные уровни цитокинов и цитокиновых рецепторов [35]. В метаанализе Miller с соавт. было показано значительное повышение уровня фактора некроза опухолей (TNF-α), IL-1β, IL-6 и IL-12 у пациентов с первым психотическим эпизодом [36]. Полученные нами результаты свидетельствуют, что уровень цитокинов IL-1β, IL-6, TNF-α повышен у пациентов на раннем этапе шизофрении и в ремиссии по сравнению с контрольной группой, но ниже по сравнению с хронической шизофренией.
IL-10 — противовоспалительный цитокин, способный блокировать действие провоспалительных цитокинов и играющий роль негативного модулятора как иммунопролиферативных, так и воспалительных реакций в головном мозге. В работе Wang с соавт. (2021) был подтвержден нейропротекторный эффект IL-10 при шизофрении [37]. В литературе имеются данные, что у пациентов с первым эпизодом шизофрении не наблюдается значительных изменений в уровнях противовоспалительных цитокинов IL-4 и IL-10 [38]. В нашем исследовании наблюдались заметные различия уровня IL-10 в группах сравнения и по сравнению с контролем, причем у пациентов с хронической шизофренией уровень был ниже, чем у пациентов с первым эпизодом. Результаты соответствуют данным Lesh с соавт. о том, что уровень IL-10 у пациентов с шизофренией снижен на 19,6% по сравнению с контрольной группой (p = 0,04). Снижение уровня IL-10 демонстрировало обратную корреляцию с длительностью нелеченого психоза (r = -0.29, p = 0.03), что, по мнению автора, может свидетельствовать о том, что снижение противовоспалительной активности IL-10 способствует прогрессированию заболевания и ухудшению клинических исходов [31]. У женщин уровень противовоспалительного цитокина IL-10 выше, чем у мужчин, что коррелирует с большей сохранностью у них нейрокогнитивных функций.
В доступной литературе имеется несколько работ, посвященных анализу взаимосвязи когнитивных функций и цитокинов на раннем этапе шизофрении. В поперечном исследовании случай-контроль Baek с соавт. (2022) изучали эффекты взаимодействия между когнитивной функцией и воспалительными цитокинами и мозговым нейротрофическим фактором (BDNF) при первом эпизоде шизофрении. Пациенты с шизофренией продемонстрировали повышенные уровни IL-1β и IL-6, сниженные уровни BDNF и сниженные показатели когнитивного функционирования (все p < 0,001). Скорость обработки информации отрицательно коррелировала с IL-6 (r = -0,315, P < 0,05) и положительно с BDNF (r = 0,290, P < 0,05); внимание, рабочая память, исполнительные функции отрицательно коррелировали с IL-1β и IL-6 (все p < 0,05) и положительно с BDNF (все p <0,05). Множественный регрессионный анализ показал, что IL-6 влияет на когнитивные параметры (β = -0,218 до -0,327, все p < 0,05); IL-1β — на внимание и исполнительные способности (β = -0,199 до -0,261, все p < 0,05); на исполнительные способности влияет BDNF (β = 0,209, p < 0,05). Авторы сделали вывод, что взаимосвязь между иммунной дисфункцией и нейротрофическим дефицитом может лежать в основе механизмов когнитивных нарушений у пациентов с первым эпизодом шизофрении [39]. Целью метаанализа Cui с соавт. (2024) явилось изучение взаимосвязи между медиаторами воспаления, такими как провоспалительные цитокины и С-реактивный белок, а также BDNF и когнитивными нарушениями при шизофрении. Было включено в общей сложности 25 исследований, 84 пациента с первым эпизодом шизофрении и 80 здоровых добровольцев. У пациентов с первым эпизодом шизофрении наблюдалось выраженное снижение когнитивных функций, особенно по показателям скорости обработки информации, внимания, рабочей памяти и исполнительных функций. Уровни IL-1β и IL-6 в группе шизофрении были выше, чем в контрольной группе (все p < 0,001), в то время как уровень BDNF был снижен. Изменения этих биомаркеров оказались тесно связаны с когнитивной дисфункцией. Показатель скорости обработки информации отрицательно коррелировал с IL-6 (r = -0,315, P < 0,05); внимание отрицательно коррелировало с IL-1β и IL-6 (r = -0,226, -0,412, все P < 0,05); рабочая память отрицательно коррелировала с IL-1β и IL-6 (r = -0,324, -0,236, все P < 0,05), исполнительная способность отрицательно коррелировала с IL-1β и IL-6 (r = -0,284, -0,386, все P < 0,05). Таким образом, IL-1β и IL-6 были расценены как факторы риска когнитивных нарушений, нарушающие передачу сигналов между нейронами. Была отмечена значительная роль воспалительных цитокинов и нейротрофических факторов в развитии когнитивных нарушений у пациентов с первым эпизодом шизофрении [22].
В исследовании Chen с соавт. (2023) оценивали уровни IL-2, IL-6, TNF-α и С-реактивного белка и когнитивные функции у 26, 35 и 29 подростков с первым эпизодом шизофрении, биполярным расстройством и большим депрессивным расстройством соответственно. Для оценки когнитивных функций использовались Висконсинский тест сортировки карточек (WCST) и тест на рабочую память. Было установлено, что у пациентов с биполярным расстройством наблюдались самые высокие уровни С-реактивного белка (p = 0,023), IL-6 (p = 0,022) и TNF-α (p = 0,011) и самые низкие уровни IL-2 (p = 0,034). Подростки с шизофренией продемонстрировали самые низкие показатели когнитивных функций. В этой группе только уровень С-реактивного белка был отрицательно связан с показателями WCST. Таким образом, нарушение регуляции про- и противовоспалительных цитокинов, а также снижение когнитивных функций наблюдались как при первом эпизоде подростковой шизофрении, так и при биполярном расстройстве и большом депрессивном расстройстве [40].
Заключение
Полученные данные свидетельствуют о повышенном уровне цитокинов в период ремиссии на раннем этапе шизофрении, что отражает сохраняющуюся активность процесса. Показательными служат повышение уровней IL-6, IL-1β и TNF-α и снижение IL-10. Динамика уровня IL-10 отражает уменьшение его протективной функции в процессе прогрессирования заболевания. У женщин определяется менее выраженный иммунный ответ в сравнении с пациентами мужского пола, что соотносится с меньшим нейрокогнитивным дефицитом.
Проведенное исследование продемонстрировало выраженные нейрокогнитивные нарушения у пациентов с первым эпизодом шизофрении в ремиссии, особенно у мужчин. Наибольшее снижение установлено по показателям рабочей памяти, вербального обучения и скорости обработки информации.
Показано, что число рецидивов шизофрении влияет на уровень когнитивного функционирования и уровень цитокинов, причем критическим является третий приступ.
Результаты исследования демонстрируют взаимосвязь между иммунной дисфункцией и нейрокогнитивным дефицитом при шизофрении как на ранних, так и на отдаленных этапах заболевания. В нашем исследовании выявлены корреляции ряда цитокинов с определенными показателями когнитивного функционирования. Демографические факторы вносят значимый вклад в вариабельность исходных данных, однако при корректном учете нелинейного влияния возраста сохраняется ряд ассоциаций. В группе пациентов с первым эпизодом шизофрении в ремиссии выявлены корреляции ряда провоспалительных цитокинов с ухудшением исполнительных функций и вербальной памяти. Противовоспалительный IL-10 не демонстрирует значимых связей с когнитивными доменами на ранних стадиях заболевания в ремиссии. Характер взаимосвязи цитокинов и когнитивных функций меняется по мере прогрессирования заболевания.
Результаты исследования подтверждают, что когнитивный дефицит при шизофрении не является статичным, а формируется в динамике заболевания, где хроническое воспаление может выступать в качестве одного из ключевых механизмов его прогрессирования.
Полученные данные, подкрепленные современными исследованиями, подчеркивают важность воспалительных процессов в патогенезе когнитивных нарушений при шизофрении и открывают перспективы для разработки новых терапевтических стратегий, направленных на модуляцию иммунного ответа с целью улучшения когнитивных функций у пациентов с шизофренией.
Ограничения исследования
Полученные данные подчеркивают необходимость более крупных выборок и применения гибких статистических моделей в будущих исследованиях для точной идентификации иммунно-когнитивных связей при шизофрении.
Дата поступления: 20.09.2025
Received: 20.09.2025
Принята к печати: 02.12.2025
Accepted: 02.12.2025
Автор заявляет об отсутствии конфликта интересов.
Author declares no conflicts of interest.
Информация об авторах:
Альпин В.С. — https://orcid.org/0000-0002-3404-0786
Петрова Н.Н. — https://orcid.org/0000-0003-4096-6208
Дорофейков В.В. — https://orcid.org/0000-0002-7272-1654
Слепой В.В. - https://orcid.org/0009-0009-3945-7837
Автор, ответственный за переписку: Петрова Н.Н. — e-mail: petrova_nn@mail.ru
Information about the authors:
Alpin V.S. — https://orcid.org/0000-0002-3404-0786
Petrova N.N. — https://orcid.org/0000-0003-4096-6208
Dorofeykov V.V. — https://orcid.org/0000-0002-7272-1654
Slepoy V.V. - https://orcid.org/0009-0009-3945-7837
Corresponding author: Petrova N.N. — e-mail: petrova_nn@mail.ru
Список исп. литературыСкрыть список1. Петрова Н.Н., Воинкова Е.Е. Особенности когнитивного функционирования у пациентов с первым психотическим эпизодом, получавших терапию антипсихотиками I и II поколения// Психиатрия и психофармакотерапия им. П.Б. Ганнушкина. №04.- 2015.-С.13-18.
2. Петрова Н.Н., Дорофейкова М.В., Воинкова Е.Е. Когнитивные нарушения у больных шизофренией на разных этапах течения заболевания// Журнал неврологии и психиатрии им. С.С. Корсакова. – 2016.- Т. 116.- №4.- С. 10-15.
3. Cowman M, Holleran L, Lonergan E, O'Connor K, Birchwood M, Donohoe G. Cognitive Predictors of Social and Occupational Functioning in Early Psychosis: A Systematic Review and Meta-analysis of Cross-Sectional and Longitudinal Data. Schizophr Bull.2021;47(5):1243-1253. doi: 10.1093/schbul/sbab033.
4. Петрова Н.Н., Дорофейкова М.В. Нейропсихиатрия. Когнитивные нарушения. Руководство для врачей. M.: ГЭОТАР-Медиа, 2023. 192с.
5. O'Connor TG, Ciesla AA. Maternal Immune Activation Hypotheses for Human Neurodevelopment: Some Outstanding Questions. Biol Psychiatry Cogn Neurosci Neuroimaging. 2022 May;7(5):471-479. doi: 10.1016/j.bpsc.2021.10.006. Epub 2021 Oct 21. PMID: 34688920; PMCID: PMC9021321.
6. Ушаков В.Л., Малашенкова И.К., Костюк Г.П., и др. Связь между воспалением, когнитивными нарушениями и данными нейровизуализации при шизофрении. Журнал неврологии и психиатрии им. С.С. Корсакова. 2020;120(11):70 78.
Ushakov VL, Malashenkova IK, Kostyuk GP, et al. The relationship between inflammation, cognitive disorders and neuroimaging data in schizophrenia. S.S. Korsakov Journal of Neurology and Psychiatry. 2020;120(11):70 78. (In Russ.) https://doi.org/10.17116/jnevro202012011170
7. Bora E. Peripheral inflammatory and neurotrophic biomarkers of cognitive impairment in schizophrenia: a meta-analysis. Psychol Med. 2019;49:1971–1979. doi: 10.1017/S0033291719001685.
8. Xiu MH, Li Z, Chen DC, Chen S, Curbo ME, Wu HE, Tong YS, Tan SP, Zhang XY. Interrelationships Between BDNF, Superoxide Dismutase, and Cognitive Impairment in Drug-Naive First-Episode Patients With Schizophrenia. Schizophr Bull. 2020 Dec 1;46(6):1498-1510. doi: 10.1093/schbul/sbaa062.
9. Mehterov N, Minchev D, Gevezova M, Sarafian V, Maes M. Interactions Among Brain-Derived Neurotrophic Factor and Neuroimmune Pathways Are Key Components of the Major Psychiatric Disorders. Mol Neurobiol. 2022;59:4926–4952. doi: 10.1007/s12035-022-02889-1.
10. Patlola SR, Donohoe G, McKernan DP. The relationship between inflammatory biomarkers and cognitive dysfunction in patients with schizophrenia: A systematic review and meta-analysis. Prog Neuropsychopharmacol Biol Psychiatry. 2023 Mar 8;121:110668. doi: 10.1016/j.pnpbp.2022.110668.
11. Miller AH, Haroon E, Raison CL, Felger JC. Cytokine targets in the brain: impact on neurotransmitters and neurocircuits. Depress Anxiety. 2013 Apr;30(4):297-306. doi: 10.1002/da.22084.
12. North HF, Bruggemann J, Cropley V, Swaminathan V, Sundram S, Lenroot R, Pereira AM, Zalesky A, Bousman C, Pantelis C, Weickert TW, Shannon Weickert C. Increased peripheral inflammation in schizophrenia is associated with worse cognitive performance and related cortical thickness reductions. Eur Arch Psychiatry Clin Neurosci. 2021 Jun;271(4):595-607. doi: 10.1007/s00406-021-01237-z.
13. Fillman SG, Weickert TW, Lenroot RK, Catts SV, Bruggemann JM, Catts VS, Weickert CS. Elevated peripheral cytokines characterize a subgroup of people with schizophrenia displaying poor verbal fluency and reduced Broca's area volume. Mol Psychiatry. 2016 Aug;21(8):1090-8. doi: 10.1038/mp.2015.90. Tripathi A, Kar SK, Shukla R. Cognitive Deficits in Schizophrenia: Understanding the Biological Correlates and Remediation Strategies. Clin Psychopharmacol Neurosci. 2018 Feb 28;16(1):7-17. doi: 10.9758/cpn.2018.16.1.7.
14. Rodrigues-Neves, A.C., Ambrósio, A.F. & Gomes, C.A. Microglia sequelae: brain signature of innate immunity in schizophrenia. Transl Psychiatry 12, 493 (2022). https://doi.org/10.1038/s41398-022-02197-1
15. Bilbo SD, Schwarz JM. The immune system and developmental programming of brain and behavior. Front Neuroendocrinol. 2012 Aug;33(3):267-86. doi: 10.1016/j.yfrne.2012.08.006. Epub 2012 Sep 9. PMID: 22982535; PMCID: PMC3484177.
16. Khandaker GM, Cousins L, Deakin J, Lennox BR, Yolken R, Jones PB. Inflammation and immunity in schizophrenia: implications for pathophysiology and treatment. Lancet Psychiatry. 2015 Mar;2(3):258-270. doi: 10.1016/S2215-0366(14)00122-9. Epub 2015 Feb 25. PMID: 26359903; PMCID: PMC4595998.
17. Tripathi A, Kar SK, Shukla R. Cognitive Deficits in Schizophrenia: Understanding the Biological Correlates and Remediation Strategies. Clin Psychopharmacol Neurosci. 2018 Feb 28;16(1):7-17. doi: 10.9758/cpn. 2018.16.1.7.
18. Walker LAS, Lindsay-Brown AP, Berard JA. Cognitive Fatigability Interventions in Neurological Conditions: A Systematic Review. Neurol Ther. 2019 Dec;8(2):251-271. doi: 10.1007/s40120-019-00158-3.
19. Guan X, Leng W, Hu Q, Xiu M, Zhang X. Association between cognitive function and IL-18 levels in schizophrenia: Dependent on IL18 - 607 A/C polymorphism. Psychoneuroendocrinology. 2023 Dec;158:106386. doi: 10.1016/j.psyneuen.2023.106386.
20. Levin MG, Klarin D, Georgakis MK, Lynch J, Liao KP, Voight BF, O'Donnell CJ, Chang KM, Assimes TL, Tsao PS, Damrauer SM; VA Million Veteran Program. A Missense Variant in the IL-6 Receptor and Protection From Peripheral Artery Disease. Circ Res. 2021 Oct 29;129(10):968-970. doi: 10.1161/CIRCRESAHA.121.319589.
21. Sellami M, Bragazzi NL, Aboghaba B, Elrayess MA. The Impact of Acute and Chronic Exercise on Immunoglobulins and Cytokines in Elderly: Insights From a Critical Review of the Literature. Front Immunol. 2021 Apr 14;12:631873. doi: 10.3389/fimmu.2021.631873.
22. Cui LJ, Cai LL, Na WQ, Jia RL, Zhu JL, Pan X. Interaction between serum inflammatory cytokines and brain-derived neurotrophic factor in cognitive function among first-episode schizophrenia patients. World J Psychiatry. 2024 Dec 19;14(12):1804-1814. doi: 10.5498/wjp.v14.i12.1804.
23. Wu MD, Hein AM, Moravan MJ, Shaftel SS, Olschowka JA, O'Banion MK. Adult murine hippocampal neurogenesis is inhibited by sustained IL-1β and not rescued by voluntary running. Brain Behav Immun. 2012;26:292–300. doi: 10.1016/j.bbi.2011.09.012.
24. Huang EJ, Reichardt LF. Neurotrophins: roles in neuronal development and function. Annu Rev Neurosci. 2001;24:677–736. doi: 10.1146/annurev. neuro.24.1.677.
25. Deverman BE, Patterson PH. Cytokines and CNS development. Neuron. 2009;64:61–78. doi: 10.1016/j.neuron.2009.09.002.
26. Boulanger LM. Immune proteins in brain development and synaptic plasticity. Neuron. 2009;64:93–109. doi: 10.1016/j.neuron.2009.09.001.
27. Li X, Yuan J, Qin W, Yang L, Yang S, Li Y, Hu W. Cerebral Microbleeds Are Associated with Impairments in Executive Function and Processing Speed. J Alzheimers Dis. 2021;81(1):255-262. doi: 10.3233/JAD-201202.
28. Brisch R, Wojtylak S, Saniotis A, Steiner J, Gos T, Kumaratilake J, Henneberg M, Wolf R. The role of microglia in neuropsychiatric disorders and suicide. Eur Arch Psychiatry Clin Neurosci. 2022 Sep;272(6):929-945. doi: 10.1007/s00406-021-01334-z. Epub 2021 Sep 30. PMID: 34595576; PMCID: PMC9388452.
29. Ribeiro-Santos R, de Campos-Carli SM, Ferretjans R, Teixeira-Carvalho A, Martins-Filho OA, Teixeira AL, Salgado JV. The association of cognitive performance and IL-6 levels in schizophrenia is influenced by age and antipsychotic treatment. Nord J Psychiatry. 2020 Apr;74(3):187-193. doi: 10.1080/08039488.2019.1688389. Epub 2019 Nov 18. PMID: 31738648.
30. Misiak B, Stańczykiewicz B, Kotowicz K, Rybakowski JK, Samochowiec J, Frydecka D. Cytokines and C-reactive protein alterations with respect to cognitive impairment in schizophrenia and bipolar disorder: A systematic review. Schizophr Res. 2018 Feb;192:16-29. doi: 10.1016/j.schres. 2017.04.015. Epub 2017 Apr 14. PMID: 28416092.
31. Lesh TA, Careaga M, Rose DR, McAllister AK, Van de Water J, Carter CS, Ashwood P. Cytokine alterations in first-episode schizophrenia and bipolar disorder: relationships to brain structure and symptoms. J Neuroinflammation. 2018 May 26;15(1):165. doi: 10.1186/s12974-018-1197-2. PMID: 29803226; PMCID: PMC5970482.
32. Hori H, Yoshimura R, Katsuki A, Atake K, Igata R, Konishi Y, Nakamura J. Relationships between serum brain-derived neurotrophic factor, plasma catecholamine metabolites, cytokines, cognitive function and clinical symptoms in Japanese patients with chronic schizophrenia treated with atypical antipsychotic monotherapy. World J Biol Psychiatry. 2017 Aug;18(5):401-408. doi: 10.1080/15622975.2016.1212172. Epub 2016 Aug 15. PMID: 27409727.
33. Massrali A, Adhya D, Srivastava DP, Baron-Cohen S, Kotter MR. Virus-Induced Maternal Immune Activation as an Environmental Factor in the Etiology of Autism and Schizophrenia. Front Neurosci. 2022 Apr 12;16:834058. doi: 10.3389/fnins.2022.834058. Erratum in: Front Neurosci. 2022 Jun 08;16:943903. doi: 10.3389/fnins.2022.943903.
34. Fineberg AM, Ellman LM. Inflammatory cytokines and neurological and neurocognitive alterations in the course of schizophrenia. Biol Psychiatry. 2013 May 15;73(10):951-66. doi: 10.1016/j.biopsych.2013.01.001.
35. Upthegrove R, Khandaker GM. Cytokines, Oxidative Stress and Cellular Markers of Inflammation in Schizophrenia. Curr Top Behav Neurosci. 2020;44:49-66. doi: 10.1007/7854_2018_88.
36. Miller BJ, Buckley P, Seabolt W, Mellor A, Kirkpatrick B. Meta-analysis of cytokine alterations in schizophrenia: clinical status and antipsychotic effects. Biol Psychiatry. 2011 Oct 1;70(7):663-71. doi: 10.1016/j.biopsych. 2011.04.013.
37. Wang J, Xu H, Wang D, Wei G, Zhou H, Wang L, Zhou Y, Zhang X. The interactive effect of genetic polymorphisms of IL-10 and COMT on cognitive function in schizophrenia. J Psychiatr Res. 2021 Apr;136:501-507. doi: 10.1016/j.jpsychires.2020.10.021. Epub 2020 Oct 22. PMID: 33127070.
38. Yan F, Meng X, Cheng X, Pei W, Chen Y, Chen L, Zheng M, Shi L, Zhu C, Zhang X. Potential role between inflammatory cytokines and Tie-2 receptor levels and clinical symptoms in patients with first-episode schizophrenia. BMC Psychiatry. 2023;23:538. doi: 10.1186/s12888-023-04913-7.
39. Baek SH, Kim H, Kim JW, Ryu S, Lee JY, Kim JM, Shin IS, Kim SW. Association between Peripheral Inflammatory Cytokines and Cognitive Function in Patients with First-Episode Schizophrenia. J Pers Med. 2022 Jul 14;12(7):1137. doi: 10.3390/jpm12071137.
40. Chen MH, Hsu JW, Huang KL, Tsai SJ, Tu PC, Bai YM. Inflammatory cytokines in and cognitive function of adolescents with first-episode schizophrenia, bipolar disorder, or major depressive disorder. CNS Spectr. 2023 Feb;28(1):70-77. doi: 10.1017/S1092852921000857. Epub 2021 Oct 19. PMID: 34664544.


