Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
1 RUDN University, Moscow, Russia
2 Scientific and practical center of child psychoneurology of department of public health, Moscow, Russia.
Corresponding author: Yury P. Sivolap, yura-sivolap@yandex.ru
Abstract
Antipsychotics are the only class of drugs that reduce the symptoms of schizophrenia and are widely used in the treatment of bipolar disorder, as well as anxiety disorders and a number of other neuropsychiatric conditions. With a certain convention, antipsychotics are divided into drugs of the first and second generations. A separate category of antipsychotics is represented by drugs of the third generation, the difference between which and drugs of the first two generations is the dual effect on dopamine neurotransmission. Second-generation antipsychotics vary significantly in their pharmacological profile, which determines the differences in indications for clinical use, as well as the predominant side effects. Antipsychotic therapy requires careful monitoring of possible side effects with control of neurological state, cardiac activity, body weight, blood cells, biochemical parameters of carbohydrate and lipid metabolism, as well as prolactin level.
Keywords: antipsychotics; chlorpromazine; risperidone; olanzapine; quetiapine; schizophrenia; bipolar disorder; extrapyramidal symptoms; metabolic disorders; prolactin; QT interval.
For citation: Sivolap Yu.P., Portnova A.A. Clinical use and comparative tolerability of antipsychotics. Psychiatry and psychopharmacotherapy. 2025; 6: 56–64. DOI: 10.62202/2075-1761-2025-27-6-56-64
Антипсихотики, наряду с антидепрессантами, стабилизаторами настроения1 и средствами лечения тревоги и бессонницы, составляют один из четырех классов лекарственных средств, применяемых в психиатрии.
Основное предназначение антипсихотиков – лечение шизофрении, а также психозов другого происхождения; исключения, при которых антипсихотики могут быть неэффективны или противопоказаны, представляют острая кататония, анти-NMDA-рецепторный энцефалит и, в определенной степени, алкогольные психозы.
Второе по значимости показание к назначению антипсихотиков – терапия биполярного расстройства, при котором антипсихотики либо служат альтернативой стабилизаторам настроения, либо используются в сочетании с ними.
Антипсихотики эффективны в лечении острой мании и при этом превосходят по скорости наступления антиманиакальных эффектов стабилизаторы настроения; отдельные препараты этого класса используются в лечении биполярной депрессии; многие антипсихотики по меньшей мере не уступают стабилизаторам настроения в поддерживающей терапии биполярного расстройства.
Антипсихотики назначаются при остром возбуждении и, наконец, выступают в качестве лекарственных средств третьей линии – после антидепрессантов и бензодиазепинов – в терапии тревожных расстройств.
Наряду со всем перечисленным выше антипсихотики применяются с целью аугментации эффектов антидепрессантов.
Сложным вопросом нейропсихиатрии является назначение антипсихотиков пациентам с болезнью Альцгеймера и деменцией другого происхождения.
Антипсихотики (видимо, разные препараты в разной степени) способны усугублять когнитивный дефицит, вызванный болезнью Альцгеймера; более того, антипсихотическая терапия повышает риск преждевременных смертей у пациентов с деменцией [1].
Вместе с тем у пациентов с болезнью Альцгеймера, осложненной психотическими симптомами, антипсихотики нередко служат незаменимой терапевтической опцией, и в этих случаях необходим выбор наиболее безопасного препарата в минимальных дозах и по возможности непродолжительным курсом.
С долей условности антипсихотики разделяются на препараты первого поколения (типичные, традиционные, конвенциональные антипсихотики) и антипсихотики второго поколения (атипичные антипсихотики) с существенными различиями между отдельными препаратами в пределах каждой из групп.
Общим свойством антипсихотиков первого и второго поколения служит антагонистическое влияние на дофаминовые D-рецепторы различных подтипов от D1 до D4 с наиболее частым воздействием на рецепторы D2-типа, что лежит в основе их основных фармакологических и клинических эффектов.
Многими (хотя и не всеми) экспертами в отдельную категорию антипсихотиков третьего поколения выделяются арипипразол, карипразин, брекспипразол и луматеперон, в отличие от препаратов первого и второго поколений оказывающие двойственное – антагонистическое и парциальное агонистическое – влияние на дофаминовые D2-рецепторы.
Дополнительные фармакологические свойства, клинические эффекты и побочные действия антипсихотиков определяются их связыванием с серотониновыми, гистаминовыми, ацетилхолиновыми и адреналиновыми рецепторами.
Первым антипсихотиком второго поколения, синтезированным в 1958 г., является клозапин, который до сих пор превосходит любой другой антипсихотик как второго, так и тем более первого поколения в эффективности лечения шизофрении, включая ее резистентные формы, и в снижении суицидального риска у пациентов с расстройствами шизофренического спектра [2].
Выраженные антипсихотические свойства клозапина и другие клинические эффекты, равно как и серьезные побочные действия, принято объяснять способностью препарата связываться с множеством различных рецепторов, что позволяет относить его к категории так называемых «грязных лекарств» (dirty drugs).
Любые антипсихотики, разработанные позже клозапина, обычно уступают ему в лечении резистентных форм шизофрении и в антисуицидальной активности, но при этом значительно превосходят этот препарат по переносимости и безопасности.
Наряду с тем, что клозапин, по-видимому, является самым мощным средством лечения шизофрении, его применение связано с максимальным риском осложнений, в том числе с возможным смертельным исходом, включая агранулоцитоз. Достаточно упомянуть, что клозапин, одобренный FDA (Food and Drug Administration) для применения в США по двум показаниям – шизофрения, резистентная к антипсихотикам, и рекуррентное суицидальное поведение у пациентов с шизофренией и шизоаффективным расстройством, отмечен этим же контролирующим агентством пятью «черными рамками предупреждений» (black box warning) FDA, что указывает на высокую опасность данного антипсихотика, и позволяет считать его, несмотря на безусловные терапевтические достоинства, препаратом последней инстанции (drug of last resort), назначаемым лишь в случае отсутствия эффекта при использовании не менее чем двух других антипсихотиков, причем по крайней мере один из них должен относиться к препаратам второго поколения.
Типичные побочные эффекты антипсихотиков включают заторможенность и дневную сонливость, экстрапирамидные расстройства, метаболические нарушения (избыточный вес и ожирение, дислипидемии, резистентность к инсулину и метаболический синдром), гиперпролактинемию и удлинение интервала QT при электрокардиографическом исследовании.
Антипсихотики первого поколения чаще вызывают экстрапирамидные расстройства, чем препараты второго поколения, тогда как применение антипсихотиков второго поколения в большей степени ассоциировано с метаболическими нарушениями [3], хотя разнородность фармакологического профиля и клинических эффектов лекарств обеих групп создает основу для определенных исключений из этого правила.
Условность объединения разных препаратов в единую категорию антипсихотиков второго (как, впрочем, и первого) поколения проявляется заметными различиями в профиле побочных эффектов, включая экстрапирамидные нарушения.
Анализ 9837 случаев терапии пероральными антипсихотиками в Японии показал, что прием луразидона был связан со значительно большей частотой сообщений о дистонии, чем прием рисперидона, арипипразола, кветиапина и оланзапина; частота случаев дистонии, связанных с приемом арипипразола, была ниже, чем при приеме палиперидона и рисперидона, но выше, чем при приеме кветиапина и оланзапина [4].
Предполагается, что более высокая частота поздней дискинезии, вызванной антипсихотиками первого поколения, может объясняться их назначением в то время, когда они широко использовались в лечении психозов в отсутствие современных альтернатив, в более высоких дозах, чем это принято сейчас. Например, несколько десятилетий назад ежедневная доза галоперидола нередко превышала 20 мг, и лишь позже исследования показали, что суточная доза, позволяющая добиться связывания с 80% дофаминовых D2-рецеторов как условия терапевтического эффекта, находится в пределах 2-5 мг, и более высокие дозы лишь увеличивают частоту и степень побочных действий [5].
Гиперпролактинемия может быть связана с терапией отдельными антипсихотиками как первого, так и второго поколений, тогда как препараты третьего поколения способны, напротив, подавлять синтез пролактина.
В настоящей статье рассмотрены четыре лекарственных средства, появление которых представляет определенные вехи в эволюции фармакологического класса антипсихотиков, – хлорпромазин как самый первый антипсихотик и три часто назначаемых антипсихотика второго поколения: рисперидон, оланзапин и кветиапин.
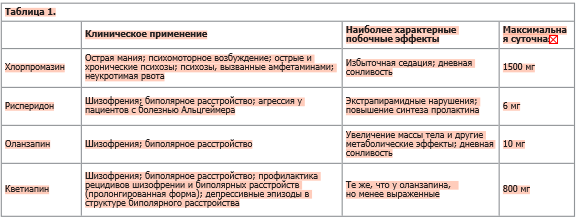
Фармакологические особенности, основные показания, преобладающие побочные эффекты и рекомендуемые дозы каждого из препаратов приведены в таблице 1.
Хлорпромазин
В 1952 г. J. Delay и соавторы опубликовали данные об уменьшении симптомов психоза у пациентов с шизофренией в Больничном центре Святой Анны в Париже (Centre hospitalier Sainte-Anne) под влиянием хлорпромазина, прежде находившего применение в анестезиологии в качестве седативного средства [6].
Многочисленные дальнейшие исследования подтвердили превосходство хлорпромазина над плацебо в лечении психозов, через два года после публикации французских авторов препарат был одобрен FDA для применения в США и стал широко применяться по всему миру, в первую очередь в лечении шизофрении.
С появлением хлорпромазина шизофрения оказалась болезнью, поддающейся лечению, и первичные наблюдения его терапевтического эффекта производили, без преувеличения, ошеломляющее впечатление на врачей [7], что позволило говорить о психофармакологической революции в психиатрии [8].
Благодаря быстрому смягчению симптомов острого психоза и способности устранять психомоторное возбуждение, связанного с шизофренией и другими психическими расстройствами, антипсихотики привели к значительному улучшению атмосферы психиатрических больниц, практически не существовавшей прежде возможности амбулаторной терапии психозов и к деинституционализации психиатрической помощи.
В отличие от предыдущих методов лечения, хлорпромазин делал пациентов с неконтролируемым поведением более управляемыми и при этом не приводил их в бессознательное состояние2 [7].
Применение хлорпромазина позволило заново оценить клинический полиморфизм шизофрении, что, в свою очередь, послужило поводом для разработки других антипсихотиков [9].
Препарат внесен в типовой перечень основных лекарственных средств ВОЗ (WHO Model List of Essential Medicines).
Хлорпромазин относится к производным фенотиазина с алифатической боковой цепью; позже в этой категории появились и другие препараты, в том числе левомепромазин и алимемазин.
Дальнейшее изменение структуры молекулы привело к появлению производных фенотиазина с пиперидиновой и пиперазиновой боковой цепью.
Некоторые из пиперидиновых производных фенотиазина – например, тиоридазин и перициазин – относятся к так называемым малым нейролептикам и в основном применяются в пограничной психиатрии.
Особенностью пиперазиновых производных фенотиазина – таких, как трифлуоперазин и перфеназин – являются избирательные антипсихотические эффекты с воздействием на бред и галлюцинации, что создает им дополнительные возможности в лечении шизофрении по сравнению с алифатическими производными фенотиазина.
Фармакологические эффекты хлорпромазина, включая его побочные действия, связаны с антагонистическим и агонистическим влиянием на дофаминовые D1, D2, D3 и D4, серотониновые 5-HT2, 5-HT6 и 5-HT7, гистаминовые H1, адренергические α1 and α2, а также мускариновые ацетилхолиновые M1 и M2.
Основное предназначение хлорпромазина – купирование острого психоза, особенно у пациентов с выраженной тревогой, возбуждением и нарушениями сна.
В отличие от пиперазиновых производных фенотиазина, а также галоперидола и ряда антипсихотиков второго поколения, хлорпромазин проявляет общее антипсихотическое действие, но не обладает избирательными антипсихотическими эффектами в отношении параноидных симптомов и рассматривается в качестве низкопотентного (low potency) антипсихотика – иными словами, лекарственного средства с умеренными антипсихотическими свойствами.
В кохрейновском систематическом обзоре, посвященном оценке клинической эффективности хлорпромазина, рассмотрены все рандомизированные плацебо-контролируемые исследования применения хлорпромазина в лечении шизофрении (а также неаффективных психозов), включенных в реестр кохрейновской группы по изучению шизофрении (Cochrane Schizophrenia Group’s Trials Register), с комментарием авторов об очень низком уровне доказательности включенных в обзор исследований: хлорпромазин превосходит плацебо по количеству участников с рецидивом психического расстройства в течение 6-24 месяцев после лечения; лишь немногие пациенты, принимавшие хлорпромазин, прекращали лечение раньше пациентов, получавших плацебо; самые частые побочные эффекты включали чрезмерную седацию, артериальную гипотензию в сочетании с головокружением, увеличение массы тела, острые двигательные расстройства и паркинсонизм, тогда как частота акатизии в связи с приемом хлорпромазина не превышала таковую у пациентов, получавших плацебо.
Авторы приходят к заключению, что полученные данные не опровергают представления о хлорпромазине как эталонном препарате для лечения шизофрении на протяжении пятидесяти с лишним лет3 и при этом считают применение хлорпромазина с этой целью неидеальной [10].
Эти же авторы в публикации, сделанной десятилетием позже, постулируют следующее: седативное действие низкопотентных фенотиазинов, в том числе хлорпромазина, имеет терапевтическое значение для одних пациентов и представляют побочный эффект для других; хлорпромазин может использоваться для аугментации атипичных антипсихотиков либо в качестве альтернативы атипичным антипсихотикам в случаях неудовлетворительного терапевтического ответа; пациентам с резистентными психозами, особенно при наличии импульсивности, агрессии и склонности к насилию, может назначаться комбинация атипичного антипсихотика и хлорпромазина при тщательном мониторинге побочных эффектов [11].
По-видимому, хлорпромазин обладает наибольшим среди антипсихотиков седативным действием, что, видимо, в первую очередь объясняется его антихолинергическими эффектами, и выраженные седативные эффекты позволяют использовать его при остром возбуждении.
Как и другие антипсихотики первого поколения, хлорпромазин проявляет очевидные антиманиакальные свойства и является единственным антипсихотиком первого поколения, одобренным для лечения острой мании, но доказательства его эффективности в лечении биполярной депрессии и поддерживающей терапии биполярного расстройства отсутствуют [5].
Хлорпромазин находит применение в лечении психозов, вызванных амфетаминами, и рассматривается в качестве антидота по отношению к галлюциногенам, применяемым в психоделической терапии, – диэтиламиду лизергиновой кислоты, псилоцибину и мескалину [12].
За пределами официальных показаний (off-label) хлорпромазин назначается при тяжелой мигрени [13].
Другие типичные побочные эффекты хлорпромазина – увеличение веса и постуральная гипотензия; при этом хлорпромазин в меньшей степени вызывает экстрапирамидные нарушения, чем более мощные антипсихотики первого поколения [5].
Считается, что частота поздней дискинезии, вызванной хлорпромазином в дозе не выше 600 мг, сопоставима с таковой при лечении рисперидоном и оланзапином в эквивалентных дозах [14].
Хлорпромазин до сих пор широко применяется в США, причем не только в психиатрии, но и в общей медицинской практике.
Заслуживают внимания данные исследования текущего года, проведенного в Северной Каролине, о применении антипсихотиков для пациентов, находящихся на гемодиализе, риск внезапной сердечной смерти у которых в 20 раз превышает общепопуляционный показатель. Это особенно важно принимать во внимание, учитывая способность отдельных антипсихотиков (особенно первого поколения) приводить к удлинению интервала QT на электрокардиограмме, отражающему нарушение сердечной проводимости как одной из причин внезапной сердечной смерти.
Анализ медицинских карт 846 400 пациентов, находившихся на поддерживающем гемодиализе в 2007-2019 гг., показал, что галоперидол (n = 10 813) и хлорпромазин (n = 5800) были наиболее часто назначаемыми пероральными типичными антипсихотиками, и внезапная сердечная смерть развилась у 9,9% и 5,9% пациентов, получавших галоперидол и хлорпромазин соответственно; анализ дополнительных кардиологических исходов дал аналогичные результаты, и на основании полученных данных авторы констатируют более высокую кардиологическую безопасность хлорпромазина по сравнению с галоперидолом [15].
Успешное применение хлорпромазина как первого антипсихотика послужило основанием для использования так называемого хлорпромазинового эквивалента как инструмента оценки сравнительной эффективности различных антипсихотиков.
V. Danivas и G. Venkatasubramanian (2013) в статье с красноречивым подзаголовком «Comparing apples and oranges!» («Сравнение яблок с апельсинами!»), отмечая использования хлорпромазинового эквивалента в профессиональном обучении многих поколений психиатров, указывают на то, что данный инструмент был более чем уместен в отношении антипсихотиков первого поколения, главной мишенью которых были дофаминовые D2-рецепторы, но в значительно меньшей мере пригоден для оценки эффективности атипичных антипсихотиков с их гораздо более широким фармакологическим спектром, включающим влияние на серотониновые, гистаминовые, ацетилхолиновые и норадреналиновые рецепторы4 [16].
Вместе с тем при очевидном несовершенстве хлорпромазиновый эквивалент по-прежнему используется в психофармакологии; в частности, процитированные авторы приводят таблицу, в который принятый внутрь хлорпромазин равноценен рассматриваемым в настоящей статье рисперидону, оланзапину и кветиапину в дозах 2 мг, 5 мг и 75 мг соответственно [16].
Обобщая приведенные данные, можно заключить, что хлорпромазин может назначаться в качестве альтернативы антипсихотикам второго поколения при острой мании, психомоторном возбуждении различного происхождения, психозах, вызванных амфетаминами или галлюциногенами, а также при параноидных психозах и расстройствах шизофренического спектра (остром приступе шизофрении, шизофреноподобном психозе или шизоаффективном расстройстве) в тех случаях, когда применение антипсихотиков второго поколения невозможно либо нежелательно.
Следует принимать во внимание, что предусмотренное официальными инструкциями показание к назначению хлорпромазина при аутизме не соответствует российским клиническим рекомендациям «Расстройство аутистического спектра» и аналогичным зарубежным клиническим рекомендациям.
Рисперидон
По истории разработки и клинического применения рисперидон является вторым после клозапина антипсихотиком второго поколения.
Препарат оказывает антагонистическое влияние в большей степени на дофаминовые D2, чем на D1-рецепторы, а также является антагонистом 5-HT2 и, возможно, 5-HT1-рецепторов.
Эффективность рисперидона при шизофрении в суточной дозе 6 мг по меньшей мере не уступает 20 мг галоперидола, с которым он обнаруживает сходство в фармакологическом профиле, но при этом отличается лучшей переносимостью [5].
Определенное сходство между фармакологическими профилями галоперидола и рисперидона, позволяющее некоторым экспертам (мнение которых разделяют авторы настоящей статьи) рассматривать второй в качестве улучшенной версии первого, можно считать закономерным, если принять во внимание, что молекула галоперидола в 1958 г. была синтезирована бельгийским химиком Полом Янссеном (Paul Janssen), а рисперидон является позднейшей разработкой основанной им фармацевтической компании Janssen.
Рисперидон относится к антипсихотикам, наиболее часто назначаемым при шизофрении, и по некоторым оценкам, в том числе специалистов психиатрической клиники McLean Hospital, является идеальным лекарственным средством первой линии в терапии данной болезни, несмотря на определенные побочные эффекты [5].
Уже самые ранние исследования эффективности рисперидона в лечении шизофрении продемонстрировали способность препарата уменьшать позитивные и негативные симптомы болезни, что подтверждается снижением показателей по шкале PANSS (Positive and Negative Syndrome Scale). Отмечено также уменьшение количества дней, проведенных в психиатрической больнице, и улучшение показателей социального функционирования по модифицированной шкале Штрауса-Карпентера (modified Strauss-Carpenter Scale) [17].
Помимо шизофрении, рисперидон применяется в лечении шизоаффективного расстройства, а также одобрен для терапии острой мании и смешанных состояний у пациентов с биполярным расстройством.
В российских и зарубежных клинических рекомендациях наряду с арипипразолом рисперидон одобрен для коррекции коморбидных нарушений поведения у детей с расстройством аутистического спектра [18].
Благодаря фармакологическому профилю, а именно сочетанию дофаминергических и серотонинергических эффектов, рисперидон находит применение не только в психиатрии, но и в неврологии; в частности, имеются данные об уменьшении нейровоспаления5, смягчении симптомов болезни Гентингтона, а также улучшении цикла сна и бодрствования [19]; разумеется, подобное использование препарата находится за пределами официальных показаний к его назначению.
Инструкция к рисперидону позволяет использовать его в краткосрочной (не дольше 6 недель) терапии непрекращающейся агрессии у пациентов с болезнью Альцгеймера.
Наиболее характерный побочный эффект рисперидона – экстрапирамидные нарушения, но при этом риск поздней дискинезии и злокачественного нейролептического синдрома при лечении рисперидоном рассматривается как меньший, чем при использовании других антипсихотиков второго поколения, и составляет 0,5-1% у молодых пациентов и приблизительно 2,6% у пациентов пожилого возраста [5].
Следует принимать во внимание, что рисперидон, подобно его фармакологически активному метаболиту палиперидону, применяемому в составе пролонгированных антипсихотических средств, а также галоперидолу и замещенным бензамидам, способен в значительной степени стимулировать синтез пролактина, и контроль уровня пролактина в крови служит обязательной мерой предупреждения осложнений терапии при назначении рисперидона.
Другие возможные побочные эффекты рисперидона включают увеличение массы тела (хотя и менее выраженное, чем у клозапина, оланзапина и кветиапина), чрезмерную седацию и ортостатическую гипотензию6.
Максимальная суточная доза рисперидона составляет 6 мг, при этом важно принимать во внимание, что в дозе 2 мг препарат может быть неэффективен, а превышение дозы в 6 мг приводит к снижению терапевтического эффекта и увеличению риска побочных действий.
Рисперидон в дозе 3-6 мг связывает 60-80% дофаминовых рецепторов [5]; как уже указывалось выше, превышение этой дозы не приводит к увеличению терапевтического эффекта, а лишь повышает вероятность побочных эффектов и осложнений терапии.
Фармакологические свойства и результаты многочисленных исследований позволяют обоснованно рассматривать рисперидон в качестве средства первой линии в терапии шизофрении, позволяющего контролировать ее позитивные и негативные симптомы, а также применять препарат в лечении биполярного расстройства, шизоаффективного расстройства, коморбидных нарушений поведения у пациентов с расстройством аутистического спектра.
Терапия рисперидоном требует тщательного мониторинга возможных побочных эффектов, включая контроль содержания пролактина в крови; не следует превышать максимальную суточную дозу в 6 мг.
Оланзапин
Подобно клозапину, с которым оланзапин проявляет структурное и фармакологическое сходство, оланзапин вызывает дофаминергические и серотонинергические эффекты, проявляет сродство к дофаминовым D1-D4 (преимущественно D2) и серотониновым 5-HT-2A рецепторам. Кроме того, оланзапин обладает антигистаминными и антихолинергическими свойствами и блокирует α1-адренорецепторы.
В определенном смысле оланзапин занимает промежуточное место между клозапином, связывающимся со множеством рецепторов, и рисперидоном, обладающим значительно более избирательным фармакологическим действием [5].
Оланзапин принадлежит к категории наиболее часто назначаемых антипсихотиков второго поколения, несмотря на высокую стоимость7 [5], что, безусловно, определяется его высокой эффективностью и приемлемой переносимостью.
Оланзапин по меньшей мере не уступает галоперидолу в краткосрочной терапии шизофрении и превосходит галоперидол по влиянию на негативные симптомы, коморбидную депрессию, суицидальность и когнитивные функции [5].
По сравнению с антипсихотиками первого поколения оланзапин реже вызывает экстрапирамидные симптомы, лишь в минимальной степени повышает уровень пролактина и характеризуется значительно лучшей переносимостью [20].
По данным исследования CATIE (n = 444), лечение шизофрении оланзапином в наименьшей степени в сравнении с антипсихотиками-компараторами ассоциировано с преждевременным прекращением приема препарата: отмечено, что в течение 18-месячного исследования приверженности терапии прием оланзапина прекратили 64% пациентов, тогда как частота прекращения приема других антипсихотиков составляла 74-82% [21].
Отмеченная выше способность связываться с большим количеством рецепторов, сближающая оланзапин с клозапином, создает ему дополнительные преимущества в эффективности лечения отдельных состояний в сравнении с другими антипсихотиками второго поколения – например, в лечении резистентных форм шизофрении и в снижении суицидального риска, связанного с расстройствами шизофренического спектра.
Именно по этой причине, несмотря на определенный риск метаболических побочных эффектов, включая увеличение массы тела, многие клиницисты продолжают назначать оланзапин для лечения шизофрении в расчете на дополнительную терапевтическую эффективность по сравнению с другими антипсихотиками первой линии [22].
Как уже говорилось выше, золотым стандартом лечения резистентной шизофрении служит клозапин, превосходящий все остальные антипсихотики в этом отношении. Вместе с тем систематический обзор и сетевой метаанализ 150 рандомизированных контролируемых исследований с участием 11 375 пациентов показал, что оланзапин лишь немногим уступает клозапину в монотерапии резистентной шизофрении и значительно превосходит другие антипсихотики в данной клинической ситуации [23].
Систематический обзор и метаанализ, проведенный в соответствии с рекомендацией PRISMA с включением двенадцати исследований, продемонстрировал лучшую общую переносимость оланзапина у пациентов с резистентной шизофренией при более низкой частоте отмены препарата из-за побочных эффектов, но некоторые исследования показали значительно большую прибавку в весе при приеме высоких доз оланзапина (≥20 мг/сут) по сравнению с клозапином (15,9 против 3,5 фунтов); авторы приходят к заключению о том, что хотя клозапин остается наиболее эффективным методом лечения резистентной шизофрении, особенно при положительных симптомах, оланзапин в высоких дозах представляет собой жизнеспособную альтернативу с иным профилем эффективности и риска [24].
Способность оланзапина уменьшать суицидальность при шизофрении составляет примерно на 75% от таковой у клозапина [2], что, по нашему мнению, является достаточно высоким показателем.
По-видимому, высокая эффективность оланзапина объясняется отмеченной выше широтой рецепторного связывания, сближающего этот антипсихотик с клозапином.
Оланзапин обнаруживает высокую эффективность в терапии биполярного расстройства и является первым из антипсихотиков второго поколения, получившим одобрение для лечения острой мании, в эффективности купирования которой он по меньшей мере не уступает литию и вальпроату при заметно более быстром терапевтическом ответе8 [5].
Наряду с кветиапином (а также луразидоном и карипразином) оланзапин относится к антипсихотикам, рекомендованным FDA для лечения биполярной депрессии9. В терапии депрессии, связанной с биполярным расстройством первого типа, а также резистентной депрессии в соответствии с одобрением FDA оланзапин применяется в сочетании с флуоксетином, с уточнением, что данная комбинация не разрешена в возрасте до 10 лет [25].
Оланзапин относится к предпочтительным антипсихотикам в терапии психотической депрессии.
Наряду с клозапином и рассматриваемым ниже кветиапином оланзапин применяется для аугментации эффектов антидепрессантов, в том числе дулоксетина [26].
Одну из трудных проблем клинической психиатрии составляет нервная анорексия, для лечения которой, в отличие от нервной булимии, до сих пор не получено ни одного лекарственного средства с эффективностью, доказанной рандомизированными контролируемыми исследованиями. Вместе с тем предпринимаются небезуспешные попытки лечения пациентов с анорексией с помощью антипсихотиков второго поколения, и в первую очередь с этой целью применяется оланзапин с обнадеживающими результатами для взрослых пациентов и менее определенными данными в терапии подростков [27].
Несмотря на очевидные достоинства оланзапина, а именно высокий терапевтический потенциал и широкий спектр клинических эффектов, следует принимать во внимание, что препарат в большей степени, чем другие антипсихотики второго поколения, вызывает метаболические нарушения, в том числе увеличение массы тела.
С другой стороны, бесспорным преимуществом оланзапина для клинической практики является редкость экстрапирамидных побочных эффектов и лишь единичные (в отличие от других антипсихотиков) случаи наблюдения злокачественного нейролептического синдрома.
Резюмируя приведенные данные, можно заключить, что оланзапин является одним из наиболее эффективных и в то же время достаточно безопасных препаратов для лечения шизофрении и биполярного расстройства.
В связи с возможными метаболическими нарушениями терапия оланзапином требует регулярного контроля массы тела, лабораторных показателей углеводного и липидного обмена, а также, в связи с другими потенциальными побочными эффектами, контроля других показателей при биохимическом исследовании крови, форменных элементов крови и пролактина. Наряду с этим необходимо принимать во внимание способность оланзапина удлинять интервал QT.
Кветиапин
Кветиапин обладает структурным и определенным фармакологическим сходством с клозапином и оланзапином.
Подобно клозапину, кветиапин проявляет более выраженный аффинитет к дофаминовым D4, чем к D1 и D2-рецепторам. Кроме того, степень связывания кветиапина (а также клозапина) с D2-рецепторами слабее, чем у дофамина, и поэтому кветиапин очень редко вызывает экстрапирамидные нарушения, в отличие от галоперидола, рисперидона и ряда других антипсихотиков, связывающихся с D2-рецепторами прочнее, чем дофамин [28].
Редкость возникновения экстрапирамидных нарушений и гиперпролактинемии объясняется также преимущественным влиянием кветиапина на мезолимбические, а не на нигростриарные и тубулоинфундибулярные нейроны [29].
Наряду с дофаминергическими эффектами кветиапин обладает серотонинергическими свойствами благодаря высокому аффинитету к серотониновым 5-HT2-рецепторам.
Период полужизни кветиапина в плазме крови составляет 6-8 часов, что определяет необходимость лекарственных форм для перорального приема с медленным высвобождением действующего вещества.
Компания «Канонфарма продакшн» (ЗАО «Канонфарма продакшн») выпускает четыре пролонгированных препарата кветиапина для приема внутрь: Кветиапин Канон Пролонг в таблетках по 150 мг, 200 мг, 300 мг и 400 мг.
Как и другие антипсихотики, кветиапин широко используется в фармакологической терапии шизофрении и биполярного расстройства.
В эффективности лечения шизофрении кветиапин в среднем на 15% превосходит хлорпромазин, зипрасидон и асенапин и сопоставим с галоперидолом и арипипразолом [30].
Кветиапин назначается при острой мании и смешанных состояниях и применяется в поддерживающем лечении биполярного расстройства – как в качестве средства монотерапии, так и в сочетании со стабилизаторами настроения. Как уже указывалось выше, кветиапин, наряду с оланзапином, луразидоном, карипразином и луматепероном, одобрен FDA для лечения биполярной депрессии, причем в дозе 300-600 мг достаточно успешно устраняет тревожный компонент депрессивного эпизода биполярного расстройства [31].
Сложную проблему психофармакологической терапии представляет биполярное расстройство с частой сменой аффективных фаз, или с быстрой цикличностью (rapid cycling bipolar disorder).
Средством выбора терапии биполярного расстройства с быстрой цикличностью считается вальпроат; наблюдение 14 пациентов позволяет констатировать достаточно успешное применение с этой целью кветиапина в широком диапазоне доз (в зависимости от типа аффективного эпизода и этапа терапии) с преимущественным влиянием на маниакальные и смешанные состояния без существенного улучшения у пациентов с депрессивными симптомами [32].
Кветиапин часто используется в качестве дополнения к антидепрессантам в терапии большого депрессивного расстройства и наряду с литием рассматривается в качестве препарата первой линии для аугментации антидепрессантов при резистентной депрессии [33, 34].
Открытое рандомизированное контролируемое исследование с включением 112 пациентов (97 [46%] мужчин и 115 [54%] женщин) в возрасте от 18 лет с текущим эпизодом большого депрессивного расстройства по критериям DSM-5 и не менее чем 14 баллами по шкале Гамильтона для оценки депрессии без адекватного терапевтического ответа на два и более антидепрессанта, получавших после случайного распределения кветиапин (n = 107) либо литий (n = 105), показало превосходство кветиапина над литием как по клинической эффективности, так и, возможно, по соотношению стоимости лечения и достигаемого результата [34].
Обзор девяти рандомизированных контролируемых исследований показал превосходство кветиапина, в том числе лекарственных форм с медленным высвобождением (extended release), над плацебо в терапии генерализованного тревожного расстройства, включая его резистентные формы, в сочетании с относительно хорошей переносимостью, в том числе по данным шкалы Гамильтона для оценки тревоги и шкалы общего клинического впечатления.
Авторы высказывают предположение, что при надлежащем мониторинге и коррекции побочных эффектов потенциальная польза от применения кветиапина у пациентов с резистентным к лечению генерализованным тревожным расстройством может перевесить риски, связанные с его назначением [35].
По мнению первого автора настоящей статьи, с точки зрения эффективности и безопасности кветиапин при осторожном дозировании является одним из предпочтительных антипсихотиков для устранения психотических симптомов у пациентов с болезнью Альцгеймера, и хорошая переносимость низких доз препарата (в частности, отсутствие заметного влияния на когнитивные функции) при назначении с этой целью подтверждается некоторыми исследованиями [36]. Вместе с тем назначение кветиапина, в соответствии с официальной инструкцией, пациентам с деменцией признано небезопасным.
Кветиапин может служить эффективным средством лечения шизофрении и биполярного расстройства как при острых состояниях, так и в структуре поддерживающей терапии обоих заболеваний с очевидными преимуществами применения пролонгированных форм препарата.
Наиболее распространенные побочные эффекты кветиапина включают дневную сонливость, увеличение массы тела и другие метаболические нарушения, а также изменения ряда лабораторных показателей крови, но в целом кветиапин характеризуется хорошей переносимостью по сравнению со многими антипсихотиками второго и особенно первого поколения.
Кветиапин является самым часто назначаемым антипсихотиком второго поколения в США [5] и самым часто назначаемым антипсихотиком в фармакологической терапии тревожных расстройств во всем мире.
В 2025 году констатирован глобальный рост количества назначений кветиапина, в том числе без рецепта врача [33], что, очевидно, отражает благоприятное соотношение его клинической эффективности и хорошей переносимости, и, что еще более важно, готовность многих пациентов к лечению данным антипсихотиком.
По нашему мнению, кветиапин в определенной мере можно рассматривать в качестве смягченной версии оланзапина с менее выраженной способностью вызывать дневную сонливость, метаболические нарушения и другие побочные эффекты.
В соответствии с инструкцией показаниями для назначения кветиапина служат шизофрения, маниакальный эпизод и депрессивный эпизод средней и выраженной тяжести у пациентов с биполярным расстройством, но не предупреждение новых депрессивных или маниакальных эпизодов.
Для противорецидивной и поддерживающей терапии как шизофрении, так и биполярного расстройства рекомендован прием кветиапина с постепенным (пролонгированным) высвобождением в таблетках по 150 мг, 200 мг, 300 мг и 400 мг.
Терапия кветиапином требует мониторинга возможных побочных эффектов с контролем массы тела, показателей углеводного и липидного обмена, форменных элементов крови, а также пролактина.
Следует также принимать во внимание возможность удлинения интервала QT на электрокардиограмме; в этой связи представляется небезопасным одновременный прием кветиапина с эсциталопрамом, гидроксизином и другими лекарственными средствами, влияющими на сердечную проводимость.
В связи с возможным синдромом отмены и повышением суицидального риска доза кветиапина при прекращении лечения снижается постепенно.
Заключение
Антипсихотики второго поколения имеют преимущества перед препаратами первого поколения в переносимости и должны назначаться в первую очередь. В некоторых случаях могут также применяться антипсихотики первого поколения, включая хлорпромазин.
Все антипсихотики демонстрируют приблизительно равную эффективность в лечении шизофрении; исключением служит хлорпромазин как антипсихотик с низкой мощностью (low potency).
Антипсихотики успешно применяются в острой и поддерживающей терапии биполярного расстройства, причем некоторые из них, включая рассмотренные здесь оланзапин и кветиапин, обладают преимуществами над другими препаратами в терапии биполярной депрессии.
Как в соответствии с официальными показаниями, так и за пределами утвержденной инструкции антипсихотики могут использоваться в других клинических ситуациях – при остром возбуждении и состояниях агрессии, в терапии тревожных расстройств и психозов, связанных с болезнью Альцгеймера.
Переносимость отдельных антипсихотиков во многом определяется как их фармакологическим профилем, так и индивидуальными особенностями реакции пациентов.
Одним из преимуществ рисперидона, при очевидно высокой эффективности в лечении шизофрении, служит сравнительная редкость метаболических нарушений, тогда как оланзапин и кветиапин относительно нечасто вызывают экстрапирамидные побочные эффекты и повышение уровня пролактина.
Антипсихотическая терапия требует тщательного контроля массы тела, неврологических функций, лабораторных показателей и сердечной деятельности. Побочные эффекты, вызванные тем или иным антипсихотиком, могут служить основанием для его замены на препарат с иным фармакологическим профилем.
Превышение максимальной суточной дозы антипсихотиков обычно не позволяет рассчитывать на повышение эффективности лечения, но существенно увеличивает риск побочных действий и осложнений терапии.
Одним из отечественных производителей современных антипсихотиков является фармацевтическая компания «Канонфарма продакшн».
Ключевые преимущества портфеля «Канонфарма продакшн», содержащего все четыре рассмотренных в статье антипсихотика:
• широкий ассортимент препаратов разных поколений, включая лекарственные средства первой линии,
• развитые линейки форм выпуска каждого препарата с оптимальным балансом экономической и клинической эффективности,
• доказанная биоэквивалентность препаратов и соответствие производства препаратов требованиям GMP.
Дата поступления: 07.10.2025
Received: 07.10.2025
Принята к печати: 02.12.2025
Accepted: 02.12.2025
Конфликт интересов: статья подготовлена при поддержке компании
«Канонфарма продакшн» (ЗАО «Канонфарма продакшн»).
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№06 2025
Клиническое применение и сравнительная переносимость антипсихотиков №06 2025
Номера страниц в выпуске:56-65
Резюме
Антипсихотики представляют собой единственный класс лекарственных средств, уменьшающих симптомы шизофрении, широко используются в лечении биполярного расстройства, а также тревожных расстройств и ряда других нейропсихиатрических состояний. С определенной условностью антипсихотики разделяются на препараты первого и второго поколений. Отдельную категорию антипсихотиков представляют препараты третьего поколения, отличием которых от лекарств первых двух поколений служит двойственное влияние на нейротрансмиссию дофамина.
Антипсихотики второго поколения существенно различаются между собой фармакологическим профилем, что определяет отличия в показаниях к клиническому применению, а также преобладающими побочными эффектами. Терапия антипсихотиками требует тщательного мониторинга возможных побочных эффектов с контролем неврологического состояния, сердечной деятельности, массы тела, форменных элементов крови, биохимических показателей углеводного и липидного обмена, а также уровня пролактина.
Ключевые слова: антипсихотики; хлорпромазин; рисперидон; оланзапин; кветиапин; шизофрения; биполярное расстройство; экстрапирамидные симптомы; метаболические нарушения; пролактин; интервал QT.
Для цитирования: Сиволап Ю.П., Портнова А.А. Клиническое применение и сравнительная переносимость антипсихотиков. Психиатрия и психофармакотерапия. 2025; 6: 56–64. DOI: 10.62202/2075-1761-2025-27-6-56-64
Антипсихотики представляют собой единственный класс лекарственных средств, уменьшающих симптомы шизофрении, широко используются в лечении биполярного расстройства, а также тревожных расстройств и ряда других нейропсихиатрических состояний. С определенной условностью антипсихотики разделяются на препараты первого и второго поколений. Отдельную категорию антипсихотиков представляют препараты третьего поколения, отличием которых от лекарств первых двух поколений служит двойственное влияние на нейротрансмиссию дофамина.
Антипсихотики второго поколения существенно различаются между собой фармакологическим профилем, что определяет отличия в показаниях к клиническому применению, а также преобладающими побочными эффектами. Терапия антипсихотиками требует тщательного мониторинга возможных побочных эффектов с контролем неврологического состояния, сердечной деятельности, массы тела, форменных элементов крови, биохимических показателей углеводного и липидного обмена, а также уровня пролактина.
Ключевые слова: антипсихотики; хлорпромазин; рисперидон; оланзапин; кветиапин; шизофрения; биполярное расстройство; экстрапирамидные симптомы; метаболические нарушения; пролактин; интервал QT.
Для цитирования: Сиволап Ю.П., Портнова А.А. Клиническое применение и сравнительная переносимость антипсихотиков. Психиатрия и психофармакотерапия. 2025; 6: 56–64. DOI: 10.62202/2075-1761-2025-27-6-56-64
Clinical use and comparative tolerability of antipsychotics
Sivolap Yu.P.1, Portnova A.A.21 RUDN University, Moscow, Russia
2 Scientific and practical center of child psychoneurology of department of public health, Moscow, Russia.
Corresponding author: Yury P. Sivolap, yura-sivolap@yandex.ru
Abstract
Antipsychotics are the only class of drugs that reduce the symptoms of schizophrenia and are widely used in the treatment of bipolar disorder, as well as anxiety disorders and a number of other neuropsychiatric conditions. With a certain convention, antipsychotics are divided into drugs of the first and second generations. A separate category of antipsychotics is represented by drugs of the third generation, the difference between which and drugs of the first two generations is the dual effect on dopamine neurotransmission. Second-generation antipsychotics vary significantly in their pharmacological profile, which determines the differences in indications for clinical use, as well as the predominant side effects. Antipsychotic therapy requires careful monitoring of possible side effects with control of neurological state, cardiac activity, body weight, blood cells, biochemical parameters of carbohydrate and lipid metabolism, as well as prolactin level.
Keywords: antipsychotics; chlorpromazine; risperidone; olanzapine; quetiapine; schizophrenia; bipolar disorder; extrapyramidal symptoms; metabolic disorders; prolactin; QT interval.
For citation: Sivolap Yu.P., Portnova A.A. Clinical use and comparative tolerability of antipsychotics. Psychiatry and psychopharmacotherapy. 2025; 6: 56–64. DOI: 10.62202/2075-1761-2025-27-6-56-64
Антипсихотики, наряду с антидепрессантами, стабилизаторами настроения1 и средствами лечения тревоги и бессонницы, составляют один из четырех классов лекарственных средств, применяемых в психиатрии.
Основное предназначение антипсихотиков – лечение шизофрении, а также психозов другого происхождения; исключения, при которых антипсихотики могут быть неэффективны или противопоказаны, представляют острая кататония, анти-NMDA-рецепторный энцефалит и, в определенной степени, алкогольные психозы.
Второе по значимости показание к назначению антипсихотиков – терапия биполярного расстройства, при котором антипсихотики либо служат альтернативой стабилизаторам настроения, либо используются в сочетании с ними.
Антипсихотики эффективны в лечении острой мании и при этом превосходят по скорости наступления антиманиакальных эффектов стабилизаторы настроения; отдельные препараты этого класса используются в лечении биполярной депрессии; многие антипсихотики по меньшей мере не уступают стабилизаторам настроения в поддерживающей терапии биполярного расстройства.
Антипсихотики назначаются при остром возбуждении и, наконец, выступают в качестве лекарственных средств третьей линии – после антидепрессантов и бензодиазепинов – в терапии тревожных расстройств.
Наряду со всем перечисленным выше антипсихотики применяются с целью аугментации эффектов антидепрессантов.
Сложным вопросом нейропсихиатрии является назначение антипсихотиков пациентам с болезнью Альцгеймера и деменцией другого происхождения.
Антипсихотики (видимо, разные препараты в разной степени) способны усугублять когнитивный дефицит, вызванный болезнью Альцгеймера; более того, антипсихотическая терапия повышает риск преждевременных смертей у пациентов с деменцией [1].
Вместе с тем у пациентов с болезнью Альцгеймера, осложненной психотическими симптомами, антипсихотики нередко служат незаменимой терапевтической опцией, и в этих случаях необходим выбор наиболее безопасного препарата в минимальных дозах и по возможности непродолжительным курсом.
С долей условности антипсихотики разделяются на препараты первого поколения (типичные, традиционные, конвенциональные антипсихотики) и антипсихотики второго поколения (атипичные антипсихотики) с существенными различиями между отдельными препаратами в пределах каждой из групп.
Общим свойством антипсихотиков первого и второго поколения служит антагонистическое влияние на дофаминовые D-рецепторы различных подтипов от D1 до D4 с наиболее частым воздействием на рецепторы D2-типа, что лежит в основе их основных фармакологических и клинических эффектов.
Многими (хотя и не всеми) экспертами в отдельную категорию антипсихотиков третьего поколения выделяются арипипразол, карипразин, брекспипразол и луматеперон, в отличие от препаратов первого и второго поколений оказывающие двойственное – антагонистическое и парциальное агонистическое – влияние на дофаминовые D2-рецепторы.
Дополнительные фармакологические свойства, клинические эффекты и побочные действия антипсихотиков определяются их связыванием с серотониновыми, гистаминовыми, ацетилхолиновыми и адреналиновыми рецепторами.
Первым антипсихотиком второго поколения, синтезированным в 1958 г., является клозапин, который до сих пор превосходит любой другой антипсихотик как второго, так и тем более первого поколения в эффективности лечения шизофрении, включая ее резистентные формы, и в снижении суицидального риска у пациентов с расстройствами шизофренического спектра [2].
Выраженные антипсихотические свойства клозапина и другие клинические эффекты, равно как и серьезные побочные действия, принято объяснять способностью препарата связываться с множеством различных рецепторов, что позволяет относить его к категории так называемых «грязных лекарств» (dirty drugs).
Любые антипсихотики, разработанные позже клозапина, обычно уступают ему в лечении резистентных форм шизофрении и в антисуицидальной активности, но при этом значительно превосходят этот препарат по переносимости и безопасности.
Наряду с тем, что клозапин, по-видимому, является самым мощным средством лечения шизофрении, его применение связано с максимальным риском осложнений, в том числе с возможным смертельным исходом, включая агранулоцитоз. Достаточно упомянуть, что клозапин, одобренный FDA (Food and Drug Administration) для применения в США по двум показаниям – шизофрения, резистентная к антипсихотикам, и рекуррентное суицидальное поведение у пациентов с шизофренией и шизоаффективным расстройством, отмечен этим же контролирующим агентством пятью «черными рамками предупреждений» (black box warning) FDA, что указывает на высокую опасность данного антипсихотика, и позволяет считать его, несмотря на безусловные терапевтические достоинства, препаратом последней инстанции (drug of last resort), назначаемым лишь в случае отсутствия эффекта при использовании не менее чем двух других антипсихотиков, причем по крайней мере один из них должен относиться к препаратам второго поколения.
Типичные побочные эффекты антипсихотиков включают заторможенность и дневную сонливость, экстрапирамидные расстройства, метаболические нарушения (избыточный вес и ожирение, дислипидемии, резистентность к инсулину и метаболический синдром), гиперпролактинемию и удлинение интервала QT при электрокардиографическом исследовании.
Антипсихотики первого поколения чаще вызывают экстрапирамидные расстройства, чем препараты второго поколения, тогда как применение антипсихотиков второго поколения в большей степени ассоциировано с метаболическими нарушениями [3], хотя разнородность фармакологического профиля и клинических эффектов лекарств обеих групп создает основу для определенных исключений из этого правила.

Условность объединения разных препаратов в единую категорию антипсихотиков второго (как, впрочем, и первого) поколения проявляется заметными различиями в профиле побочных эффектов, включая экстрапирамидные нарушения.
Анализ 9837 случаев терапии пероральными антипсихотиками в Японии показал, что прием луразидона был связан со значительно большей частотой сообщений о дистонии, чем прием рисперидона, арипипразола, кветиапина и оланзапина; частота случаев дистонии, связанных с приемом арипипразола, была ниже, чем при приеме палиперидона и рисперидона, но выше, чем при приеме кветиапина и оланзапина [4].
Предполагается, что более высокая частота поздней дискинезии, вызванной антипсихотиками первого поколения, может объясняться их назначением в то время, когда они широко использовались в лечении психозов в отсутствие современных альтернатив, в более высоких дозах, чем это принято сейчас. Например, несколько десятилетий назад ежедневная доза галоперидола нередко превышала 20 мг, и лишь позже исследования показали, что суточная доза, позволяющая добиться связывания с 80% дофаминовых D2-рецеторов как условия терапевтического эффекта, находится в пределах 2-5 мг, и более высокие дозы лишь увеличивают частоту и степень побочных действий [5].
Гиперпролактинемия может быть связана с терапией отдельными антипсихотиками как первого, так и второго поколений, тогда как препараты третьего поколения способны, напротив, подавлять синтез пролактина.
В настоящей статье рассмотрены четыре лекарственных средства, появление которых представляет определенные вехи в эволюции фармакологического класса антипсихотиков, – хлорпромазин как самый первый антипсихотик и три часто назначаемых антипсихотика второго поколения: рисперидон, оланзапин и кветиапин.
Фармакологические особенности, основные показания, преобладающие побочные эффекты и рекомендуемые дозы каждого из препаратов приведены в таблице 1.
Хлорпромазин
В 1952 г. J. Delay и соавторы опубликовали данные об уменьшении симптомов психоза у пациентов с шизофренией в Больничном центре Святой Анны в Париже (Centre hospitalier Sainte-Anne) под влиянием хлорпромазина, прежде находившего применение в анестезиологии в качестве седативного средства [6].
Многочисленные дальнейшие исследования подтвердили превосходство хлорпромазина над плацебо в лечении психозов, через два года после публикации французских авторов препарат был одобрен FDA для применения в США и стал широко применяться по всему миру, в первую очередь в лечении шизофрении.
С появлением хлорпромазина шизофрения оказалась болезнью, поддающейся лечению, и первичные наблюдения его терапевтического эффекта производили, без преувеличения, ошеломляющее впечатление на врачей [7], что позволило говорить о психофармакологической революции в психиатрии [8].
Благодаря быстрому смягчению симптомов острого психоза и способности устранять психомоторное возбуждение, связанного с шизофренией и другими психическими расстройствами, антипсихотики привели к значительному улучшению атмосферы психиатрических больниц, практически не существовавшей прежде возможности амбулаторной терапии психозов и к деинституционализации психиатрической помощи.
В отличие от предыдущих методов лечения, хлорпромазин делал пациентов с неконтролируемым поведением более управляемыми и при этом не приводил их в бессознательное состояние2 [7].
Применение хлорпромазина позволило заново оценить клинический полиморфизм шизофрении, что, в свою очередь, послужило поводом для разработки других антипсихотиков [9].
Препарат внесен в типовой перечень основных лекарственных средств ВОЗ (WHO Model List of Essential Medicines).
Хлорпромазин относится к производным фенотиазина с алифатической боковой цепью; позже в этой категории появились и другие препараты, в том числе левомепромазин и алимемазин.
Дальнейшее изменение структуры молекулы привело к появлению производных фенотиазина с пиперидиновой и пиперазиновой боковой цепью.
Некоторые из пиперидиновых производных фенотиазина – например, тиоридазин и перициазин – относятся к так называемым малым нейролептикам и в основном применяются в пограничной психиатрии.
Особенностью пиперазиновых производных фенотиазина – таких, как трифлуоперазин и перфеназин – являются избирательные антипсихотические эффекты с воздействием на бред и галлюцинации, что создает им дополнительные возможности в лечении шизофрении по сравнению с алифатическими производными фенотиазина.
Фармакологические эффекты хлорпромазина, включая его побочные действия, связаны с антагонистическим и агонистическим влиянием на дофаминовые D1, D2, D3 и D4, серотониновые 5-HT2, 5-HT6 и 5-HT7, гистаминовые H1, адренергические α1 and α2, а также мускариновые ацетилхолиновые M1 и M2.
Основное предназначение хлорпромазина – купирование острого психоза, особенно у пациентов с выраженной тревогой, возбуждением и нарушениями сна.
В отличие от пиперазиновых производных фенотиазина, а также галоперидола и ряда антипсихотиков второго поколения, хлорпромазин проявляет общее антипсихотическое действие, но не обладает избирательными антипсихотическими эффектами в отношении параноидных симптомов и рассматривается в качестве низкопотентного (low potency) антипсихотика – иными словами, лекарственного средства с умеренными антипсихотическими свойствами.
В кохрейновском систематическом обзоре, посвященном оценке клинической эффективности хлорпромазина, рассмотрены все рандомизированные плацебо-контролируемые исследования применения хлорпромазина в лечении шизофрении (а также неаффективных психозов), включенных в реестр кохрейновской группы по изучению шизофрении (Cochrane Schizophrenia Group’s Trials Register), с комментарием авторов об очень низком уровне доказательности включенных в обзор исследований: хлорпромазин превосходит плацебо по количеству участников с рецидивом психического расстройства в течение 6-24 месяцев после лечения; лишь немногие пациенты, принимавшие хлорпромазин, прекращали лечение раньше пациентов, получавших плацебо; самые частые побочные эффекты включали чрезмерную седацию, артериальную гипотензию в сочетании с головокружением, увеличение массы тела, острые двигательные расстройства и паркинсонизм, тогда как частота акатизии в связи с приемом хлорпромазина не превышала таковую у пациентов, получавших плацебо.
Авторы приходят к заключению, что полученные данные не опровергают представления о хлорпромазине как эталонном препарате для лечения шизофрении на протяжении пятидесяти с лишним лет3 и при этом считают применение хлорпромазина с этой целью неидеальной [10].
Эти же авторы в публикации, сделанной десятилетием позже, постулируют следующее: седативное действие низкопотентных фенотиазинов, в том числе хлорпромазина, имеет терапевтическое значение для одних пациентов и представляют побочный эффект для других; хлорпромазин может использоваться для аугментации атипичных антипсихотиков либо в качестве альтернативы атипичным антипсихотикам в случаях неудовлетворительного терапевтического ответа; пациентам с резистентными психозами, особенно при наличии импульсивности, агрессии и склонности к насилию, может назначаться комбинация атипичного антипсихотика и хлорпромазина при тщательном мониторинге побочных эффектов [11].
По-видимому, хлорпромазин обладает наибольшим среди антипсихотиков седативным действием, что, видимо, в первую очередь объясняется его антихолинергическими эффектами, и выраженные седативные эффекты позволяют использовать его при остром возбуждении.
Как и другие антипсихотики первого поколения, хлорпромазин проявляет очевидные антиманиакальные свойства и является единственным антипсихотиком первого поколения, одобренным для лечения острой мании, но доказательства его эффективности в лечении биполярной депрессии и поддерживающей терапии биполярного расстройства отсутствуют [5].
Хлорпромазин находит применение в лечении психозов, вызванных амфетаминами, и рассматривается в качестве антидота по отношению к галлюциногенам, применяемым в психоделической терапии, – диэтиламиду лизергиновой кислоты, псилоцибину и мескалину [12].
За пределами официальных показаний (off-label) хлорпромазин назначается при тяжелой мигрени [13].
Другие типичные побочные эффекты хлорпромазина – увеличение веса и постуральная гипотензия; при этом хлорпромазин в меньшей степени вызывает экстрапирамидные нарушения, чем более мощные антипсихотики первого поколения [5].
Считается, что частота поздней дискинезии, вызванной хлорпромазином в дозе не выше 600 мг, сопоставима с таковой при лечении рисперидоном и оланзапином в эквивалентных дозах [14].
Хлорпромазин до сих пор широко применяется в США, причем не только в психиатрии, но и в общей медицинской практике.
Заслуживают внимания данные исследования текущего года, проведенного в Северной Каролине, о применении антипсихотиков для пациентов, находящихся на гемодиализе, риск внезапной сердечной смерти у которых в 20 раз превышает общепопуляционный показатель. Это особенно важно принимать во внимание, учитывая способность отдельных антипсихотиков (особенно первого поколения) приводить к удлинению интервала QT на электрокардиограмме, отражающему нарушение сердечной проводимости как одной из причин внезапной сердечной смерти.
Анализ медицинских карт 846 400 пациентов, находившихся на поддерживающем гемодиализе в 2007-2019 гг., показал, что галоперидол (n = 10 813) и хлорпромазин (n = 5800) были наиболее часто назначаемыми пероральными типичными антипсихотиками, и внезапная сердечная смерть развилась у 9,9% и 5,9% пациентов, получавших галоперидол и хлорпромазин соответственно; анализ дополнительных кардиологических исходов дал аналогичные результаты, и на основании полученных данных авторы констатируют более высокую кардиологическую безопасность хлорпромазина по сравнению с галоперидолом [15].
Успешное применение хлорпромазина как первого антипсихотика послужило основанием для использования так называемого хлорпромазинового эквивалента как инструмента оценки сравнительной эффективности различных антипсихотиков.
V. Danivas и G. Venkatasubramanian (2013) в статье с красноречивым подзаголовком «Comparing apples and oranges!» («Сравнение яблок с апельсинами!»), отмечая использования хлорпромазинового эквивалента в профессиональном обучении многих поколений психиатров, указывают на то, что данный инструмент был более чем уместен в отношении антипсихотиков первого поколения, главной мишенью которых были дофаминовые D2-рецепторы, но в значительно меньшей мере пригоден для оценки эффективности атипичных антипсихотиков с их гораздо более широким фармакологическим спектром, включающим влияние на серотониновые, гистаминовые, ацетилхолиновые и норадреналиновые рецепторы4 [16].
Вместе с тем при очевидном несовершенстве хлорпромазиновый эквивалент по-прежнему используется в психофармакологии; в частности, процитированные авторы приводят таблицу, в который принятый внутрь хлорпромазин равноценен рассматриваемым в настоящей статье рисперидону, оланзапину и кветиапину в дозах 2 мг, 5 мг и 75 мг соответственно [16].
Обобщая приведенные данные, можно заключить, что хлорпромазин может назначаться в качестве альтернативы антипсихотикам второго поколения при острой мании, психомоторном возбуждении различного происхождения, психозах, вызванных амфетаминами или галлюциногенами, а также при параноидных психозах и расстройствах шизофренического спектра (остром приступе шизофрении, шизофреноподобном психозе или шизоаффективном расстройстве) в тех случаях, когда применение антипсихотиков второго поколения невозможно либо нежелательно.
Следует принимать во внимание, что предусмотренное официальными инструкциями показание к назначению хлорпромазина при аутизме не соответствует российским клиническим рекомендациям «Расстройство аутистического спектра» и аналогичным зарубежным клиническим рекомендациям.
Рисперидон
По истории разработки и клинического применения рисперидон является вторым после клозапина антипсихотиком второго поколения.
Препарат оказывает антагонистическое влияние в большей степени на дофаминовые D2, чем на D1-рецепторы, а также является антагонистом 5-HT2 и, возможно, 5-HT1-рецепторов.
Эффективность рисперидона при шизофрении в суточной дозе 6 мг по меньшей мере не уступает 20 мг галоперидола, с которым он обнаруживает сходство в фармакологическом профиле, но при этом отличается лучшей переносимостью [5].
Определенное сходство между фармакологическими профилями галоперидола и рисперидона, позволяющее некоторым экспертам (мнение которых разделяют авторы настоящей статьи) рассматривать второй в качестве улучшенной версии первого, можно считать закономерным, если принять во внимание, что молекула галоперидола в 1958 г. была синтезирована бельгийским химиком Полом Янссеном (Paul Janssen), а рисперидон является позднейшей разработкой основанной им фармацевтической компании Janssen.
Рисперидон относится к антипсихотикам, наиболее часто назначаемым при шизофрении, и по некоторым оценкам, в том числе специалистов психиатрической клиники McLean Hospital, является идеальным лекарственным средством первой линии в терапии данной болезни, несмотря на определенные побочные эффекты [5].
Уже самые ранние исследования эффективности рисперидона в лечении шизофрении продемонстрировали способность препарата уменьшать позитивные и негативные симптомы болезни, что подтверждается снижением показателей по шкале PANSS (Positive and Negative Syndrome Scale). Отмечено также уменьшение количества дней, проведенных в психиатрической больнице, и улучшение показателей социального функционирования по модифицированной шкале Штрауса-Карпентера (modified Strauss-Carpenter Scale) [17].
Помимо шизофрении, рисперидон применяется в лечении шизоаффективного расстройства, а также одобрен для терапии острой мании и смешанных состояний у пациентов с биполярным расстройством.
В российских и зарубежных клинических рекомендациях наряду с арипипразолом рисперидон одобрен для коррекции коморбидных нарушений поведения у детей с расстройством аутистического спектра [18].
Благодаря фармакологическому профилю, а именно сочетанию дофаминергических и серотонинергических эффектов, рисперидон находит применение не только в психиатрии, но и в неврологии; в частности, имеются данные об уменьшении нейровоспаления5, смягчении симптомов болезни Гентингтона, а также улучшении цикла сна и бодрствования [19]; разумеется, подобное использование препарата находится за пределами официальных показаний к его назначению.
Инструкция к рисперидону позволяет использовать его в краткосрочной (не дольше 6 недель) терапии непрекращающейся агрессии у пациентов с болезнью Альцгеймера.
Наиболее характерный побочный эффект рисперидона – экстрапирамидные нарушения, но при этом риск поздней дискинезии и злокачественного нейролептического синдрома при лечении рисперидоном рассматривается как меньший, чем при использовании других антипсихотиков второго поколения, и составляет 0,5-1% у молодых пациентов и приблизительно 2,6% у пациентов пожилого возраста [5].
Следует принимать во внимание, что рисперидон, подобно его фармакологически активному метаболиту палиперидону, применяемому в составе пролонгированных антипсихотических средств, а также галоперидолу и замещенным бензамидам, способен в значительной степени стимулировать синтез пролактина, и контроль уровня пролактина в крови служит обязательной мерой предупреждения осложнений терапии при назначении рисперидона.
Другие возможные побочные эффекты рисперидона включают увеличение массы тела (хотя и менее выраженное, чем у клозапина, оланзапина и кветиапина), чрезмерную седацию и ортостатическую гипотензию6.
Максимальная суточная доза рисперидона составляет 6 мг, при этом важно принимать во внимание, что в дозе 2 мг препарат может быть неэффективен, а превышение дозы в 6 мг приводит к снижению терапевтического эффекта и увеличению риска побочных действий.
Рисперидон в дозе 3-6 мг связывает 60-80% дофаминовых рецепторов [5]; как уже указывалось выше, превышение этой дозы не приводит к увеличению терапевтического эффекта, а лишь повышает вероятность побочных эффектов и осложнений терапии.
Фармакологические свойства и результаты многочисленных исследований позволяют обоснованно рассматривать рисперидон в качестве средства первой линии в терапии шизофрении, позволяющего контролировать ее позитивные и негативные симптомы, а также применять препарат в лечении биполярного расстройства, шизоаффективного расстройства, коморбидных нарушений поведения у пациентов с расстройством аутистического спектра.
Терапия рисперидоном требует тщательного мониторинга возможных побочных эффектов, включая контроль содержания пролактина в крови; не следует превышать максимальную суточную дозу в 6 мг.
Оланзапин
Подобно клозапину, с которым оланзапин проявляет структурное и фармакологическое сходство, оланзапин вызывает дофаминергические и серотонинергические эффекты, проявляет сродство к дофаминовым D1-D4 (преимущественно D2) и серотониновым 5-HT-2A рецепторам. Кроме того, оланзапин обладает антигистаминными и антихолинергическими свойствами и блокирует α1-адренорецепторы.
В определенном смысле оланзапин занимает промежуточное место между клозапином, связывающимся со множеством рецепторов, и рисперидоном, обладающим значительно более избирательным фармакологическим действием [5].
Оланзапин принадлежит к категории наиболее часто назначаемых антипсихотиков второго поколения, несмотря на высокую стоимость7 [5], что, безусловно, определяется его высокой эффективностью и приемлемой переносимостью.
Оланзапин по меньшей мере не уступает галоперидолу в краткосрочной терапии шизофрении и превосходит галоперидол по влиянию на негативные симптомы, коморбидную депрессию, суицидальность и когнитивные функции [5].
По сравнению с антипсихотиками первого поколения оланзапин реже вызывает экстрапирамидные симптомы, лишь в минимальной степени повышает уровень пролактина и характеризуется значительно лучшей переносимостью [20].
По данным исследования CATIE (n = 444), лечение шизофрении оланзапином в наименьшей степени в сравнении с антипсихотиками-компараторами ассоциировано с преждевременным прекращением приема препарата: отмечено, что в течение 18-месячного исследования приверженности терапии прием оланзапина прекратили 64% пациентов, тогда как частота прекращения приема других антипсихотиков составляла 74-82% [21].
Отмеченная выше способность связываться с большим количеством рецепторов, сближающая оланзапин с клозапином, создает ему дополнительные преимущества в эффективности лечения отдельных состояний в сравнении с другими антипсихотиками второго поколения – например, в лечении резистентных форм шизофрении и в снижении суицидального риска, связанного с расстройствами шизофренического спектра.
Именно по этой причине, несмотря на определенный риск метаболических побочных эффектов, включая увеличение массы тела, многие клиницисты продолжают назначать оланзапин для лечения шизофрении в расчете на дополнительную терапевтическую эффективность по сравнению с другими антипсихотиками первой линии [22].
Как уже говорилось выше, золотым стандартом лечения резистентной шизофрении служит клозапин, превосходящий все остальные антипсихотики в этом отношении. Вместе с тем систематический обзор и сетевой метаанализ 150 рандомизированных контролируемых исследований с участием 11 375 пациентов показал, что оланзапин лишь немногим уступает клозапину в монотерапии резистентной шизофрении и значительно превосходит другие антипсихотики в данной клинической ситуации [23].
Систематический обзор и метаанализ, проведенный в соответствии с рекомендацией PRISMA с включением двенадцати исследований, продемонстрировал лучшую общую переносимость оланзапина у пациентов с резистентной шизофренией при более низкой частоте отмены препарата из-за побочных эффектов, но некоторые исследования показали значительно большую прибавку в весе при приеме высоких доз оланзапина (≥20 мг/сут) по сравнению с клозапином (15,9 против 3,5 фунтов); авторы приходят к заключению о том, что хотя клозапин остается наиболее эффективным методом лечения резистентной шизофрении, особенно при положительных симптомах, оланзапин в высоких дозах представляет собой жизнеспособную альтернативу с иным профилем эффективности и риска [24].
Способность оланзапина уменьшать суицидальность при шизофрении составляет примерно на 75% от таковой у клозапина [2], что, по нашему мнению, является достаточно высоким показателем.
По-видимому, высокая эффективность оланзапина объясняется отмеченной выше широтой рецепторного связывания, сближающего этот антипсихотик с клозапином.
Оланзапин обнаруживает высокую эффективность в терапии биполярного расстройства и является первым из антипсихотиков второго поколения, получившим одобрение для лечения острой мании, в эффективности купирования которой он по меньшей мере не уступает литию и вальпроату при заметно более быстром терапевтическом ответе8 [5].
Наряду с кветиапином (а также луразидоном и карипразином) оланзапин относится к антипсихотикам, рекомендованным FDA для лечения биполярной депрессии9. В терапии депрессии, связанной с биполярным расстройством первого типа, а также резистентной депрессии в соответствии с одобрением FDA оланзапин применяется в сочетании с флуоксетином, с уточнением, что данная комбинация не разрешена в возрасте до 10 лет [25].
Оланзапин относится к предпочтительным антипсихотикам в терапии психотической депрессии.
Наряду с клозапином и рассматриваемым ниже кветиапином оланзапин применяется для аугментации эффектов антидепрессантов, в том числе дулоксетина [26].
Одну из трудных проблем клинической психиатрии составляет нервная анорексия, для лечения которой, в отличие от нервной булимии, до сих пор не получено ни одного лекарственного средства с эффективностью, доказанной рандомизированными контролируемыми исследованиями. Вместе с тем предпринимаются небезуспешные попытки лечения пациентов с анорексией с помощью антипсихотиков второго поколения, и в первую очередь с этой целью применяется оланзапин с обнадеживающими результатами для взрослых пациентов и менее определенными данными в терапии подростков [27].
Несмотря на очевидные достоинства оланзапина, а именно высокий терапевтический потенциал и широкий спектр клинических эффектов, следует принимать во внимание, что препарат в большей степени, чем другие антипсихотики второго поколения, вызывает метаболические нарушения, в том числе увеличение массы тела.
С другой стороны, бесспорным преимуществом оланзапина для клинической практики является редкость экстрапирамидных побочных эффектов и лишь единичные (в отличие от других антипсихотиков) случаи наблюдения злокачественного нейролептического синдрома.
Резюмируя приведенные данные, можно заключить, что оланзапин является одним из наиболее эффективных и в то же время достаточно безопасных препаратов для лечения шизофрении и биполярного расстройства.
В связи с возможными метаболическими нарушениями терапия оланзапином требует регулярного контроля массы тела, лабораторных показателей углеводного и липидного обмена, а также, в связи с другими потенциальными побочными эффектами, контроля других показателей при биохимическом исследовании крови, форменных элементов крови и пролактина. Наряду с этим необходимо принимать во внимание способность оланзапина удлинять интервал QT.
Кветиапин
Кветиапин обладает структурным и определенным фармакологическим сходством с клозапином и оланзапином.
Подобно клозапину, кветиапин проявляет более выраженный аффинитет к дофаминовым D4, чем к D1 и D2-рецепторам. Кроме того, степень связывания кветиапина (а также клозапина) с D2-рецепторами слабее, чем у дофамина, и поэтому кветиапин очень редко вызывает экстрапирамидные нарушения, в отличие от галоперидола, рисперидона и ряда других антипсихотиков, связывающихся с D2-рецепторами прочнее, чем дофамин [28].
Редкость возникновения экстрапирамидных нарушений и гиперпролактинемии объясняется также преимущественным влиянием кветиапина на мезолимбические, а не на нигростриарные и тубулоинфундибулярные нейроны [29].
Наряду с дофаминергическими эффектами кветиапин обладает серотонинергическими свойствами благодаря высокому аффинитету к серотониновым 5-HT2-рецепторам.
Период полужизни кветиапина в плазме крови составляет 6-8 часов, что определяет необходимость лекарственных форм для перорального приема с медленным высвобождением действующего вещества.
Компания «Канонфарма продакшн» (ЗАО «Канонфарма продакшн») выпускает четыре пролонгированных препарата кветиапина для приема внутрь: Кветиапин Канон Пролонг в таблетках по 150 мг, 200 мг, 300 мг и 400 мг.
Как и другие антипсихотики, кветиапин широко используется в фармакологической терапии шизофрении и биполярного расстройства.
В эффективности лечения шизофрении кветиапин в среднем на 15% превосходит хлорпромазин, зипрасидон и асенапин и сопоставим с галоперидолом и арипипразолом [30].
Кветиапин назначается при острой мании и смешанных состояниях и применяется в поддерживающем лечении биполярного расстройства – как в качестве средства монотерапии, так и в сочетании со стабилизаторами настроения. Как уже указывалось выше, кветиапин, наряду с оланзапином, луразидоном, карипразином и луматепероном, одобрен FDA для лечения биполярной депрессии, причем в дозе 300-600 мг достаточно успешно устраняет тревожный компонент депрессивного эпизода биполярного расстройства [31].
Сложную проблему психофармакологической терапии представляет биполярное расстройство с частой сменой аффективных фаз, или с быстрой цикличностью (rapid cycling bipolar disorder).
Средством выбора терапии биполярного расстройства с быстрой цикличностью считается вальпроат; наблюдение 14 пациентов позволяет констатировать достаточно успешное применение с этой целью кветиапина в широком диапазоне доз (в зависимости от типа аффективного эпизода и этапа терапии) с преимущественным влиянием на маниакальные и смешанные состояния без существенного улучшения у пациентов с депрессивными симптомами [32].
Кветиапин часто используется в качестве дополнения к антидепрессантам в терапии большого депрессивного расстройства и наряду с литием рассматривается в качестве препарата первой линии для аугментации антидепрессантов при резистентной депрессии [33, 34].
Открытое рандомизированное контролируемое исследование с включением 112 пациентов (97 [46%] мужчин и 115 [54%] женщин) в возрасте от 18 лет с текущим эпизодом большого депрессивного расстройства по критериям DSM-5 и не менее чем 14 баллами по шкале Гамильтона для оценки депрессии без адекватного терапевтического ответа на два и более антидепрессанта, получавших после случайного распределения кветиапин (n = 107) либо литий (n = 105), показало превосходство кветиапина над литием как по клинической эффективности, так и, возможно, по соотношению стоимости лечения и достигаемого результата [34].
Обзор девяти рандомизированных контролируемых исследований показал превосходство кветиапина, в том числе лекарственных форм с медленным высвобождением (extended release), над плацебо в терапии генерализованного тревожного расстройства, включая его резистентные формы, в сочетании с относительно хорошей переносимостью, в том числе по данным шкалы Гамильтона для оценки тревоги и шкалы общего клинического впечатления.
Авторы высказывают предположение, что при надлежащем мониторинге и коррекции побочных эффектов потенциальная польза от применения кветиапина у пациентов с резистентным к лечению генерализованным тревожным расстройством может перевесить риски, связанные с его назначением [35].
По мнению первого автора настоящей статьи, с точки зрения эффективности и безопасности кветиапин при осторожном дозировании является одним из предпочтительных антипсихотиков для устранения психотических симптомов у пациентов с болезнью Альцгеймера, и хорошая переносимость низких доз препарата (в частности, отсутствие заметного влияния на когнитивные функции) при назначении с этой целью подтверждается некоторыми исследованиями [36]. Вместе с тем назначение кветиапина, в соответствии с официальной инструкцией, пациентам с деменцией признано небезопасным.
Кветиапин может служить эффективным средством лечения шизофрении и биполярного расстройства как при острых состояниях, так и в структуре поддерживающей терапии обоих заболеваний с очевидными преимуществами применения пролонгированных форм препарата.
Наиболее распространенные побочные эффекты кветиапина включают дневную сонливость, увеличение массы тела и другие метаболические нарушения, а также изменения ряда лабораторных показателей крови, но в целом кветиапин характеризуется хорошей переносимостью по сравнению со многими антипсихотиками второго и особенно первого поколения.
Кветиапин является самым часто назначаемым антипсихотиком второго поколения в США [5] и самым часто назначаемым антипсихотиком в фармакологической терапии тревожных расстройств во всем мире.
В 2025 году констатирован глобальный рост количества назначений кветиапина, в том числе без рецепта врача [33], что, очевидно, отражает благоприятное соотношение его клинической эффективности и хорошей переносимости, и, что еще более важно, готовность многих пациентов к лечению данным антипсихотиком.
По нашему мнению, кветиапин в определенной мере можно рассматривать в качестве смягченной версии оланзапина с менее выраженной способностью вызывать дневную сонливость, метаболические нарушения и другие побочные эффекты.
В соответствии с инструкцией показаниями для назначения кветиапина служат шизофрения, маниакальный эпизод и депрессивный эпизод средней и выраженной тяжести у пациентов с биполярным расстройством, но не предупреждение новых депрессивных или маниакальных эпизодов.
Для противорецидивной и поддерживающей терапии как шизофрении, так и биполярного расстройства рекомендован прием кветиапина с постепенным (пролонгированным) высвобождением в таблетках по 150 мг, 200 мг, 300 мг и 400 мг.
Терапия кветиапином требует мониторинга возможных побочных эффектов с контролем массы тела, показателей углеводного и липидного обмена, форменных элементов крови, а также пролактина.
Следует также принимать во внимание возможность удлинения интервала QT на электрокардиограмме; в этой связи представляется небезопасным одновременный прием кветиапина с эсциталопрамом, гидроксизином и другими лекарственными средствами, влияющими на сердечную проводимость.
В связи с возможным синдромом отмены и повышением суицидального риска доза кветиапина при прекращении лечения снижается постепенно.
Заключение
Антипсихотики второго поколения имеют преимущества перед препаратами первого поколения в переносимости и должны назначаться в первую очередь. В некоторых случаях могут также применяться антипсихотики первого поколения, включая хлорпромазин.
Все антипсихотики демонстрируют приблизительно равную эффективность в лечении шизофрении; исключением служит хлорпромазин как антипсихотик с низкой мощностью (low potency).
Антипсихотики успешно применяются в острой и поддерживающей терапии биполярного расстройства, причем некоторые из них, включая рассмотренные здесь оланзапин и кветиапин, обладают преимуществами над другими препаратами в терапии биполярной депрессии.
Как в соответствии с официальными показаниями, так и за пределами утвержденной инструкции антипсихотики могут использоваться в других клинических ситуациях – при остром возбуждении и состояниях агрессии, в терапии тревожных расстройств и психозов, связанных с болезнью Альцгеймера.
Переносимость отдельных антипсихотиков во многом определяется как их фармакологическим профилем, так и индивидуальными особенностями реакции пациентов.
Одним из преимуществ рисперидона, при очевидно высокой эффективности в лечении шизофрении, служит сравнительная редкость метаболических нарушений, тогда как оланзапин и кветиапин относительно нечасто вызывают экстрапирамидные побочные эффекты и повышение уровня пролактина.
Антипсихотическая терапия требует тщательного контроля массы тела, неврологических функций, лабораторных показателей и сердечной деятельности. Побочные эффекты, вызванные тем или иным антипсихотиком, могут служить основанием для его замены на препарат с иным фармакологическим профилем.
Превышение максимальной суточной дозы антипсихотиков обычно не позволяет рассчитывать на повышение эффективности лечения, но существенно увеличивает риск побочных действий и осложнений терапии.
Одним из отечественных производителей современных антипсихотиков является фармацевтическая компания «Канонфарма продакшн».
Ключевые преимущества портфеля «Канонфарма продакшн», содержащего все четыре рассмотренных в статье антипсихотика:
• широкий ассортимент препаратов разных поколений, включая лекарственные средства первой линии,
• развитые линейки форм выпуска каждого препарата с оптимальным балансом экономической и клинической эффективности,
• доказанная биоэквивалентность препаратов и соответствие производства препаратов требованиям GMP.
Дата поступления: 07.10.2025
Received: 07.10.2025
Принята к печати: 02.12.2025
Accepted: 02.12.2025
Конфликт интересов: статья подготовлена при поддержке компании
«Канонфарма продакшн» (ЗАО «Канонфарма продакшн»).
Список исп. литературыСкрыть список1. Yunusa I., Rashid N., Abler V., Rajagopalan K. Comparative Efficacy, Safety, Tolerability, and Effectiveness of Antipsychotics in The Treatment of Dementia-Related Psychosis (DRP): A Systematic Literature Review. J-Prev-Alzheimers-Dis, 2021; 8 (4): 520-533; doi: 10.14283/jpad.2021.48.
2. Freudenreich O. Psychotic Disorders: A Practical Guide. – Second Edition. – Cham: Humana Press, 2020. – 479 p.
3. Cao B.-F., Chen H.-W., Xu Z.-Y., Zhong Q., Liao K.-Y., Liu K., Wang S.-L., Wei Y.-F., Wang S.-A., Shao Z.-H., Li Q.-R., Zhang C.-Y., Jin H.-Y., Wu X.-B. Effects of second-generation antipsychotics and long-term atherogenic indices trajectories on metabolic syndrome in patients with schizophrenia. Schizophr-Res, 2025: 282: 150-157; doi: 10.1016/j.schres.2025.05.016.
4. Ebina T., Iwamoto K., Ando M., Ikeda M. Second-generation antipsychotic-induced dystonia: Analysis using the Japanese Adverse Drug Event Report (JADER) database. Psychiatry-Clin-Neurosci, 2025; 79 (3): 117-124; doi: 10.1111/pcn.13785.
5. DeBattista C., Schatzberg A.F. Schatzberg’s Manual of Clinical Psychopharmacology. – Tenth Edition. – Washington, DC: American Psychiatric Association Publishing, 2024. – 868 p.
6. Delay J., Deniker P., Harl J.M. [Therapeutic use in psychiatry of phenothiazine of central elective action (4560 RP)] (in French). Ann-Med-Psychol (Paris), 1952; 110 (21): 112-117; PMID: 12986408.
7. Rosenbloom M. Chlorpromazine and the psychopharmacologic revolution. JAMA, 2002; 287 (14): 1860-1861.
8. López-Muñoz F., Alamo C., Cuenca E., Shen W.W., Clervoy P., Rubio G. History of the discovery and clinical introduction of chlorpromazine. Ann-Clin-Psychiatry, 2005; 17 (3): 113-135; doi: 10.1080/10401230591002002.
9. Ban T.A. Fifty years chlorpromazine: a historical perspective. Neuropsychiatr-Dis-Treat, 2007; 3 (4): 495-500.
10. Adams C.E., Awad G.A., Rathbone J., Thornley B., Soares-Weiser K. Chlorpromazine versus placebo for schizophrenia. Cochrane-Database-Syst-Rev, 2014; 2014 (1): CD000284; doi: 10.1002/14651858.CD000284.pub3.
11. Adams C. E., Awad G., Rathbone J., Thornley B., Ahmed U., Jones H., De Haan S.. CHLORPROMAZINE (continued). Prescriber's Guide: Stahl’s Essential Psychopharmacology, 2024; 394: 158.
12. Halman A., Kong G., Sarris J., Perkins D. Drug-drug interactions involving classic psychedelics: A systematic review. J-Psychopharmacol, 2024; 38 (1): 3-18; doi: 10.1177/02698811231211219.
13. Loga P., Lewis D. Chlorpromazine in migraine. Emergency-Medicine-Journal, 2007; 24 (4): 297-300; doi: 10.1136/emj.2007.047860.
14. Leucht S., Wahlbeck K., Hamann J., Kissling W. New generation antipsychotics versus low-potency conventional antipsychotics: a systematic review and meta-analysis. Lancet, 2003; 361 (9369): 1581-9; doi: 10.1016/S0140-6736(03)13306-5.
15. Nash R.P., Sherin Ismail S., Gaynes B.N., Flythe J.E. Comparative cardiac safety of haloperidol vs. chlorpromazine among people receiving hemodialysis. J-Psychiatr-Res, 2025; 188:235-242; doi: 10.1016/j.jpsychires.2025.05.065.
16. Danivas V., Venkatasubramanian G. Current perspectives on chlorpromazine equivalents: Comparing apples and oranges! Indian-J-Psychiatry, 2013; 55 (2): 207–208; doi: 10.4103/0019-5545.111475.
17. Lindström E., Eriksson B., Hellgren A., von Knorring L., Eberhard G. Efficacy and safety of risperidone in the long-term treatment of patients with schizophrenia. Clinical therapeutics, 1995; 17 (3): 402-412; doi: 10.1016/0149-2918(95)80105-7.
18. Fieiras C., Chen M.H., Liquitay C.M.E., Meza N., Rojas V., Franco J.V.A., Madrid E. Risperidone and aripiprazole for autism spectrum disorder in children: an overview of systematic reviews. BMJ-Evid-Based-Med, 2023; 28 (1): 7-14; doi: 10.1136/bmjebm-2021-111804.
19. Bhat A.A., Gupta G., Afzal O., Kazmi I., Al-Abbasi F.A., Altamimi A.S.A., Almalki W.H., Alzarea S.I., Singh S.K., Dua K. Neuropharmacological effect of risperidone: From chemistry to medicine. Chem-Biol-Interact, 2023: 369: 110296; doi: 10.1016/j.cbi.2022.110296.
20. Callaghan J.T., Bergstrom R.F., Ptak L.R., Beasley C.M. Olanzapine. Pharmacokinetic and pharmacodynamic profile. Clin-Pharmacokinet, 1999; 37 (3): 177-93; doi: 10.2165/00003088-199937030-00001.
21. Stroup T.S., Lieberman J.A., McEvoy J.P., Swartz M.S., Davis S.M., Rosenheck R.A., Perkins D.O., Keefe R.S.E., Davis C.E., Severe J., Hsiao J.K.; CATIE Investigators. Effectiveness of olanzapine, quetiapine, risperidone, and ziprasidone in patients with chronic schizophrenia following discontinuation of a previous atypical antipsychotic. Am-J-Psychiatry, 2006; 163 (4): 611-622; doi: 10.1176/ajp.2006.163.4.611.
22. Citrome L. McEvoy J.P., Todtenkopf M.S., McDonnell D., Weiden P.J. A commentary on the efficacy of olanzapine for the treatment of schizophrenia: the past, present, and future. Neuropsychiatr-Dis-Treat, 2019: 15:2559-2569; doi: 10.2147/NDT.S209284.
23. Samara M., Lappas A.S., Pinioti E., Glarou E., Fober I., Christogiannis C., Siafis S., Christodoulou N., Helfer B., Mavridis D., Leucht S. Efficacy and tolerability of pharmacological interventions for schizophrenia non-responsive to prior treatment: a systematic review and network meta-analysis. eClinicalMedicine, 2025: 84: 103291; doi: 10.1016/j.eclinm.2025.103291.
24. Upadhyay B., Abdolmanafi S., Bhatnagar T., Al Jnainati, Al Jnainati J., Baral P., Shakir M.F. High-dose olanzapine versus clozapine for treatment-resistant schizophrenia: A systematic review and meta-analysis. Gen-Hosp-Psychiatry, 2025: 96: 140-150; doi: 10.1016/j.genhosppsych.2025.07.006.
25. Thomas K., Saadabadi A. Olanzapine. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025.
26. Römer N., Gaebler A.J., Neuner I., Haen E., Hiemke C., Schoretsanitis G., Paulzen M. Effects of the augmentation with quetiapine or olanzapine on the metabolism of duloxetine: a retrospective analysis. Expert-Rev-Clin-Pharmacol, 2025: 1-7; doi: 10.1080/17512433.2025.2486998.
27. Han R., Bian Q., Chen H. Effectiveness of olanzapine in the treatment of anorexia nervosa: A systematic review and meta-analysis. Brain-Behav, 2022; 12 (2): e2498; doi: 10.1002/brb3.2498.
28. Seeman P., Tallerico T. Antipsychotic drugs which elicit little or no parkinsonism bind more loosely than dopamine to brain D2 receptors, yet occupy high levels of these receptors. Mol-Psychiatry, 1998; 3 (2): 123-134; doi: 10.1038/sj.mp.4000336.
29. Seeman P. Atypical antipsychotics: mechanism of action. Can-J-Psychiatry, 2002; 47 (1): 27-38.
30. Leucht S., Cipriani A., Spineli L., Mavridis D., Orey D., Richter F., Samara M., Barbui C., Engel R.R., Geddes J.R., Kissling W., Stapf M.P., Lassig B., Salanti G., and Davis J.M. Comparative efficacy and tolerability of 15 antipsychotic drugs in schizophrenia: a multiple-treatments meta-analysis. Lancet, 2013; 382 (9896): 951-962.
31. Gao K., Muzina D., Gajwani P., Calabrese J.P. Efficacy of typical and atypical antipsychotics for primary and comorbid anxiety symptoms or disorders: a review. J-Clin-Psychiatry, 2006; 67 (9): 1327-40; doi: 10.4088/jcp.v67n0902.
32. Vieta E., Parramon G., Padrell E., Nieto E., Martinez-Arán A., Corbella B., Colom F., Reinares M., Goikolea J.M., Torrent C. Quetiapine in the treatment of rapid cycling bipolar disorder. Bipolar-Disord 2002; 4: 335–340; doi: 10.1034/j.1399-5618.2002.01204.x
33. Cinar B.R., Ligthart S.A., de Wit H.A.J.M., Schellekens A., Fleuren H.H.W.A., Kramers C., Batalla A., Kalkman G.A. Patterns and indications for quetiapine prescribing in Dutch primary care. BJGP-Open, 2025; BJGPO.2024.0219; doi: 10.3399/BJGPO.2024.0219.
34. Cleare A.J., Kerr-Gaffney J., Goldsmith K., Zenasni Z., Yaziji N., Jin H., Colasanti A., Geddes J.R., Kessler D., McAllister-Williams R.M., Young A.H., Barrera A., Marwood L., Taylor R.W., Tee H.; LQD Study Group. Clinical and cost-effectiveness of lithium versus quetiapine augmentation for treatment-resistant depression: a pragmatic, open-label, parallel-group, randomised controlled superiority trial in the UK. Lancet-Psychiatry, 2025; 12 (4): 276-288; doi: 10.1016/S2215-0366(25)00028-8.
35. Kreys T.-J.M., Phan S.V. A literature review of quetiapine for generalized anxiety disorder. Pharmacotherapy, 2015; 35 (2): 175-88; doi: 10.1002/phar.1529.
36. Li K.-Y., Lin B.-T., Hsu S.-T., Chien C.-F., Chang Y.-P., Yang Y.-H. Quetiapine Oral Solution in Alzheimer's Disease: Efficacy and Dosage Insights from a Real-World Retrospective Study. Quetiapine Oral Solution in Alzheimer's Disease: Efficacy and Dosage Insights from a Real-World Retrospective Study. J-Alzheimers Dis, 2024; 97 (2): 805-811; doi: 10.3233/JAD-231007.
30 декабря 2025
Количество просмотров: 116


