Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
1 Stavropol State Medical University, Ministry of Health, Russian Federation, Stavropol, str. Mira, 310, PO 355017;
2 Independent researcher in the field of psychopharmacology, Israel, Azur 5801726, str. Ben-Gurion 26/7
Abstract
The aim of this paper is to integrate contemporary biological hypotheses of electroconvulsive therapy (ECT), presenting it as a multi-level systemic intervention beyond classical neurotransmitter and neuroendocrine models. Based on neuroimaging, molecular, and multi-omics data, eight interrelated mechanisms are analyzed: epigenetic regulation (DNA methylation, miRNA, lncRNA), mitochondrial-immunometabolic cascades (AMPK-SIRT1-PGC-1α-NRF2), connectome resynchronization of neural networks (DMN, CEN, SN, limbic–thalamic and cerebellar circuits), glymphatic and neurovascular-glial regulation, the kynurenine pathway, the gut-brain axis, and Wnt/β-catenin signaling. A multi-level model is proposed, according to which these mechanisms form a unified cascade of neurobiological remodeling aimed at restoring the functional and energetic integrity of the brain. ECT is interpreted as a form of controlled cellular stress that triggers epigenetic reprogramming, metabolic adaptation, and network resynchronization, thereby establishing a new homeostatic equilibrium and opening perspectives for personalized neuromodulation in modern psychiatry.
Keywords: electroconvulsive therapy, neuromodulation, epigenetic regulation, mitochondrial stress response, immunometabolism, glymphatic system, neurovascular-glial unit, kynurenine pathway, gut–brain axis; Wnt/β-catenin signaling, neuroplasticity, connectome reset.
For citation: Bykov Yu.V., Bekker R.A. Brain Reset: An Integrative Multilevel Model of the Biological Effects of Electroconvulsive Therapy. Psychiatry and psychopharmacotherapy. 2026; 1: 4–14. DOI: 10.62202/2075-1761-2026-28-1-4-14
Введение
Электросудорожная терапия (ЭСТ) остается одним из наиболее изученных и эффективных биологических методов лечения психических заболеваний [1-5]. Она основана на индуцировании контролируемого кратковременного генерализованного судорожного припадка с помощью серии электрических импульсов, подаваемого на головной мозг пациента под общей анестезией и с применением миорелаксации [6-8].
Метод был впервые применен в 1938 году итальянскими психиатрами Уго Черлетти (Ugo Cerletti) и Лучо Бини (Lucio Bini), которые использовали электрическую стимуляцию для лечения больных шизофренией [7, 9]. В течение последующих десятилетий ЭСТ стала использоваться в терапии кататонии, маниакальных эпизодов, тяжелой депрессии и шизоаффективных состояний [1, 2, 7, 10].
Современная ЭСТ проводится в условиях блока интенсивной терапии с применением общей анестезии и миорелаксации, мониторинга жизненно важных функций и подбора индивидуальных параметров электростимуляции, что обеспечивает для пациентов высокий уровень безопасности и переносимости [7, 8, 11, 12]. Согласно международным клиническим рекомендациям, метод показан при фармакорезистентной депрессии, кататонии, острой суицидальности, при отдельных формах мании и шизофрении, ряде ургентных опасных для жизни состояний типа фебрильной шизофрении и злокачественного нейролептического синдрома [1-3, 13].
Клинические исследования достаточно давно подтверждают высокую эффективность ЭСТ при депрессии: частота терапевтического ответа превышает 70-80% даже у пациентов, не отвечающих на медикаментозное лечение [14, 15]. Наряду с традиционными психиатрическими показаниями, методика находит применение при неврологических и нейропсихиатрических расстройствах – болезни Паркинсона, обсессивно-компульсивном расстройстве, эпилепсии, посттравматическом стрессовом расстройстве [2, 16].
Эволюция техники позволила значительно повысить безопасность процедуры [7, 8]. Переход от стимуляции постоянным или синусоидальным током к импульсным стимулам, внедрение односторонних и билатеральных электродных конфигураций, а также использование коротких и ультракоротких импульсов снизили риск когнитивных побочных эффектов без потери эффективности [1, 4, 5, 11, 17]. Эти усовершенствования сделали ЭСТ одним из наиболее контролируемых и стандартизованных методов нейромодуляции в современной психиатрии.
Представленный обзор носит синтетический характер и объединяет данные различного уровня доказательности – от молекулярных и клеточных до системных и клинических. Целью работы является не установление прямых причинно-следственных зависимостей, а формирование целостного представления о многоуровневых механизмах ЭСТ как системного биологического вмешательства.
Классические механизмы действия электросудорожной терапии
За более чем 80 лет применения ЭСТ прошла путь от эмпирического метода до одного из наиболее исследованных нейромодуляционных вмешательств. В рамках настоящего обзора акцент сделан на наиболее изученных и воспроизводимых направлениях, подтвержденных в экспериментальных и клинических исследованиях: нейротрансмиттерное, нейроэндокринное, нейротрофическое, нейропластическое и иммунное. Эти системы формируют фундамент классических представлений о биологических эффектах ЭСТ и служат отправной точкой для анализа ее современных многоуровневых механизмов.
Нейротрансмиттерная модуляция
Классические работы достаточно давно продемонстрировали, что ЭСТ вызывает выраженные сдвиги в уровне моноаминовых медиаторов, включая серотонин, норадреналин и дофамин [1, 7]. Повышение серотонинергической активности и чувствительности постсинаптических 5-HT1A-рецепторов рассматривается как один из ключевых компонентов антидепрессивного эффекта [18]. Кроме того, ЭСТ нормализует баланс тормозных и возбуждающих систем, увеличивая активность ГАМК-ергических путей и снижая гиперглутаматергическую передачу [8, 19].
Нейроэндокринные и стресс-осевые эффекты
ЭСТ индуцирует кратковременную активацию гипоталамо-гипофизарно-надпочечниковой (ГГН) оси, сопровождающуюся выбросом кортизола, пролактина и адренокортикотропного гормона [7, 8, 18]. При повторных сеансах отмечается нормализация стресс-ответа и снижение исходной гиперактивации ГГН-оси [8, 19, 20]. Эти реакции рассматриваются как регулируемый нейроэндокринный «перезапуск» гомеостатических регуляторных систем.
Нейротрофические и пластические процессы
Одним из наиболее воспроизводимых открытий стало повышение экспрессии нейротрофинов – прежде всего Brain-Derived Neurotrophic Factor (BDNF, нейротрофический фактор, полученный из мозга), Vascular Endothelial Growth Factor (VEGF, сосудистый эндотелиальный фактор роста) и Glial cell line-Derived Neurotrophic Factor (GDNF, глиальный нейротрофический фактор, продуцируемый клетками глиального ряда) [1, 18]. Исследования на животных и у людей показали, что ЭСТ активирует транскрипцию генов нейротрофических факторов, усиливает синаптогенез и способствует восстановлению дендритных структур [1, 20]. Эти процессы коррелируют с клиническим улучшением и формируют основу так называемой «нейропластической гипотезы» ЭСТ.
Структурные и морфологические перестройки
Магнитно-резонансные исследования подтвердили, что курс ЭСТ приводит к увеличению объема гиппокампа, медиальной префронтальной коры и поясной извилины [1, 21, 22]. Эти изменения отражают не только нейрогенез, но и более комплексные формы нейро- и глиопластичности, включая ремоделирование сосудов и глиальных структур [4, 5]. Эти эффекты сохраняются после завершения курса и коррелируют с устойчивым клиническим ответом.
Иммунные и нейровоспалительные механизмы
Накоплены убедительные данные о положительном влиянии ЭСТ на иммунный статус [1, 18]. Систематический обзор [23] показал, что после курса ЭСТ снижаются уровни провоспалительных цитокинов (IL-6, TNF-α) и С-реактивного белка (СРБ). Данный эффект связывают с переключением активации микроглии в антивоспалительный фенотип и нормализацией взаимодействия иммунных и нейрональных сигнальных каскадов [20].
Интеграция классических механизмов
В совокупности классические исследования показывают, что ЭСТ действует многоуровнево – сочетая модуляцию моноаминовой передачи, нормализацию стресс-осевых и эндокринных систем, усиление нейротрофических каскадов и запуск пластических процессов, затрагивающих как нейрональные, так и глиальные элементы головного мозга. Современные обзоры подчеркивают, что эти эффекты не являются независимыми, а формируют единый каскад «нейробиологического ремоделирования», приводящего к восстановлению сетевой и метаболической целостности головного мозга [1, 19].
Несмотря на убедительную базу классических моделей, остается ряд нерешенных вопросов: каким образом эти процессы запускаются, какие из них являются первичными, а какие вторичными, и почему терапевтический эффект ЭСТ столь универсален? Ответы на эти вопросы формируют контуры новейших биологических гипотез, рассматривающих ЭСТ как многоуровневое системное вмешательство, выходящее далеко за рамки нейротрансмиттерных и эндокринных теорий.
К ним относятся восемь взаимосвязанных направлений: эпигенетическая регуляция, митохондриально-иммунометаболические каскады, коннектомная ресинхронизация нейросетей, глимфатическая и нейроваскулярно-глиальная регуляция, кинурениновый путь, ось «кишечник–мозг», а также сигнальный путь Wnt/β-катенина. Выбор именно этих восьми направлений не случаен. Они отражают наиболее активно развивающиеся и конвергентные линии исследований последних лет, в которых накоплены молекулярные, нейровизуализационные и клинические данные, демонстрирующие участие соответствующих механизмов в терапевтическом действии ЭСТ. Таким образом, рассмотренные направления представляют собой ядро современного представления о системной биологии ЭСТ, где каждая гипотеза дополняет другие, формируя целостную модель нейробиологического ремоделирования.
 Новые механизмы действия электросудорожной терапии
Новые механизмы действия электросудорожной терапии
Эпигенетические изменения, индуцируемые электросудорожной терапией
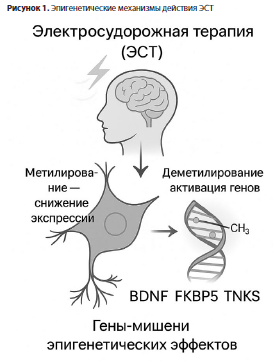
Исследования последних лет демонстрируют, что ЭСТ способна вызывать изменения в эпигенетических механизмах регуляции генной экспрессии, прежде всего в метилировании дезоксирибонуклеиновой кислоты (ДНК; Рис. 1). Эти изменения рассматриваются как возможное молекулярное звено, опосредующее терапевтический эффект ЭСТ при депрессии [1, 24].
В пилотном исследовании N. Moschny и соавт. (2020) был проведен анализ метилома (эпигенетических изменений метилирования ДНК) в периферических мононуклеарах крови у пациентов с депрессией, получавших курс ЭСТ. Авторы выявили восемь генов-кандидатов (RNF175, RNF213, TBC1D14, TMC5, WSCD1, LINC-ROR, ADARB2, RBMXL1) и два CpG-сайта в генах AQP10 и TRERF1, демонстрировавших значимые сдвиги уровня метилирования в процессе лечения [25]. Эти данные рассматриваются как потенциальные маркеры биологического отклика на ЭСТ, требующие дальнейшего подтверждения.
Результаты независимой группы L. Sirignano и соавт. (2021) дополнили эти наблюдения: изменения метилирования CpG-сайтов в генах TNKS и FKBP5 коррелировали с выраженностью клинического ответа по шкале Hamilton Depression Rating Scale (HDRS, Шкала Гамильтона для оценки выраженности депрессии) [26]. Систематический обзор S. Castro и соавт. [27], включивший девять исследований, показал, что наибольший интерес вызывают гены BDNF, FKBP5, S100A10, RNF213 и TNKS, однако все доступные данные остаются ограниченными малым числом выборок и разнородностью методик.
Помимо метилирования ДНК, все больше внимания привлекают некодирующие регуляторные РНК – прежде всего microRNA (miRNA), а также длинные и циркулярные некодирующие РНК (lncRNA, circRNA), участвующие в эпигенетической регуляции экспрессии генов.
Несмотря на ограниченность данных, ряд работ показал возможное участие miRNA в механизмах антидепрессивного эффекта ЭСТ. В частности, в пилотных исследованиях, включенных в обзор S. Castro и соавт. (2023), описаны сдвиги уровней miR-126, miR-106a и miR-24 у пациентов, ответивших на терапию [27]. Эти молекулы рассматриваются как потенциальные периферические биомаркеры ответа на ЭСТ, хотя авторы подчеркивают малый размер выборок и методическую гетерогенность.
MiRNA действуют как посттранскрипционные регуляторы, связываясь с 3´-UTR мРНК и ингибируя трансляцию или вызывая деградацию транскриптов [28]. Кроме того, они способны модулировать активность ключевых эпигенетических ферментов – ДНК-метилтрансфераз (DNMTs), гистон-деацетилаз (HDACs) и гистон-метилтрансфераз (HMTs), формируя двустороннюю связь между miRNA и эпигенетическим аппаратом клетки [29].
Эта взаимосвязь легла в основу концепции так называемых «epi-miRNA» – микроРНК, регулирующих ферменты, ответственные за метилирование ДНК и модификации гистонов [29, 30]. В свою очередь, экспрессия самих генов miRNA также может зависеть от метилирования их промоторных участков и ацетилирования гистонов, что формирует петлю эпигенетической обратной связи.
Гистоновые модификации – ацетилирование, метилирование, фосфорилирование – формируют еще один слой эпигенетической регуляции, влияющий на плотность упаковки хроматина и доступность генов для транскрипции [31]. Хотя прямых исследований влияния ЭСТ на гистоновые модификации пока нет, можно предположить, что кратковременный электрический стресс способен смещать баланс между HAT/HDAC и HMT/HDM в сторону открытого, транскрипционно активного хроматина, создавая условия для экспрессии генов нейропластичности, таких как BDNF и VEGF.
Дополнительное внимание заслуживают lncRNA и circRNA – длинные и кольцевые некодирующие транскрипты, участвующие в организации эпигенетического ландшафта. LncRNA способны связывать комплексы модификации хроматина (например, PRC2, HDAC) и направлять их к специфическим генам-мишеням, влияя на локальную структуру хроматина [30]. CircRNA, напротив, действуют как «губки» для miRNA, регулируя их доступность к мРНК-мишеням и тем самым косвенно влияя на эпигенетическую сеть.
Все доступные исследования эпигенетических эффектов ЭСТ, включающие анализ miRNA или других ncRNA, выполнены на периферических образцах (PBMC, плазма), и пока не подтверждены на уровне тканей головного мозга [27]. Отсутствуют также работы, оценивающие гистоновые модификации или экспрессию lncRNA и circRNA в центральной нервной системе (ЦНС) до и после ЭСТ. Эти ограничения делают раздел о некодирующих РНК и гистонах преимущественно концептуальным, но при этом подчеркивают перспективность дальнейших мультиомных исследований в этой области.
Но так или иначе, эпигенетические перестройки на фоне проведения ЭСТ формируют молекулярную основу для последующих системных изменений – прежде всего для перестройки нейросетевой активности и функциональной интеграции головного мозга, реализующихся в феномене коннектомного «reset».
 Коннектомный «reset» – перезапуск нейросетей
Коннектомный «reset» – перезапуск нейросетей
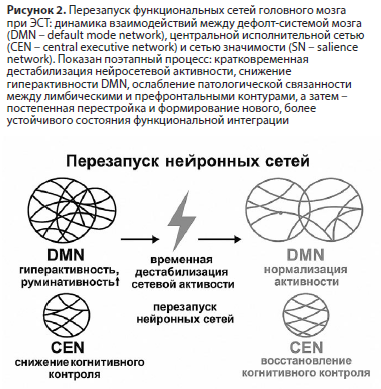
Современные исследования с использованием нейровизуализации показывают: ЭСТ воздействует на головной мозг не локально, а системно. Это не просто электрический стимул, а своего рода коннектомный «reset» – управляемая перезагрузка нейронных сетей. В момент проведения процедуры нарушаются патологические схемы функциональных связей, которые удерживают головной мозг в состоянии депрессии, и запускается процесс их перестройки в более здоровую и сбалансированную конфигурацию (Рис. 2).
Методы высокоразрешающей функциональной магнитно-резонансной томографии (фМРТ) и анализа коннектома показали, что ЭСТ уменьшает чрезмерную связанность между лимбическими и префронтальными областями, а также снижает гиперактивность Default Mode Network (DMN) – ключевой сети, активной в состоянии покоя. Именно она отвечает за внутренний диалог, размышления о себе, воспоминания и самоанализ. При депрессии DMN работает чрезмерно, удерживая человека в руминативных циклах – бесконечном прокручивании одних и тех же негативных мыслей [32].
Параллельно происходит перестройка взаимодействия между Central Executive Network (CEN) и Salience Network – сетями, регулирующими когнитивный контроль, внимание и способность оценивать значимость внешних и внутренних стимулов. После курса ЭСТ головной мозг постепенно переходит от хаотичной, рассогласованной работы к более организованной и скоординированной структуре [33].
Межцентровое исследование с использованием продольных данных фМРТ подтвердило: по мере проведения ЭСТ восстанавливается связность между ключевыми узлами DMN, а взаимодействие лобных и теменных зон возвращается к норме [34]. Изменения затрагивают не только стабильные (статические) связи, но и динамику сетевого взаимодействия, исследуемую методом динамической функциональной коннектомики (dynamic Functional Network Connectivity – dFNC).
Работа H. Dini и соавт. (2021) показала, что после ЭСТ снижается частота переходов между дезорганизованными состояниями головного мозга, усиливается преобладание устойчивых сетевых конфигураций и возрастает согласованность активности между фронтальными и теменными областями [35].
Терапевтический эффект ЭСТ во многом связан с восстановлением равновесия между DMN и CEN. Исследование Y. Pang и соавт. (2022) продемонстрировало: чем лучше восстанавливаются внутренние связи DMN и ее взаимодействие с CEN, тем выраженнее клиническое улучшение у пациентов с депрессией [36]. Аналогичные данные получили M. Moreno-Ortega и коллеги (2019), показавшие, что исходные параметры связности DMN могут предсказывать эффективность терапии [37].
ЭСТ также влияет на низкочастотные осцилляции и синхронность нейрональной активности. По данным S. Sun и соавт. (2022), во время процедуры возникает кратковременное расхождение фазовой активности между основными сетями покоя, после чего они стабилизируются на новом, более сбалансированном уровне [38]. Эти процессы сопровождаются нормализацией работы лобных отделов, ответственных за когнитивный контроль [39].
В целом совокупность данных свидетельствует: ЭСТ действует как сетевой «ресинхронизатор». Она разрушает патологические циклы активности и помогает головному мозгу самостоятельно перестроиться, находя новое устойчивое равновесие. С физиологической точки зрения это можно рассматривать как «жесткую перезагрузку» нейросетей, которая переводит головной мозг из застойного, дисфункционального режима в более оптимальное и согласованное состояние функциональной интеграции (Рис. 2).
Сетевые сдвиги устойчиво закрепляются при поддержании метаболического и ликворного гомеостаза; это выводит к рассмотрению роли глимфатической системы и обмена межклеточной жидкости в стабилизации новых паттернов активности.
 Глимфатическая и детоксикационная гипотеза
Глимфатическая и детоксикационная гипотеза
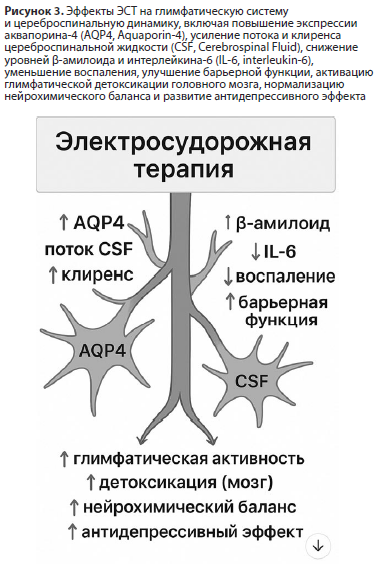
Растущие данные указывают, что эффект ЭСТ может включать не только нейромодуляцию, но и воздействие на процессы метаболического и ликворного гомеостаза головного мозга. Одним из возможных направлений обсуждения является связь ЭСТ с глимфатической системой – системой обмена спинномозговой и межклеточной жидкости, ответственной за удаление метаболитов и поддержание химического равновесия мозговой среды (Рис. 3).
Согласно концепции глимфатической системы, сформулированной L. Hablitz и M. Nedergaard (2021), транспорт ликвора осуществляется по периваскулярным путям с участием астроцитов и аквапориновых каналов (AQP4), обеспечивая «промывание» интерстициального пространства и выведение продуктов обмена, включая β-амилоид и цитокины [40]. Эта система функционирует как ключевой элемент детоксикации и метаболического очищения головного мозга, особенно во время сна, и нарушается при нейровоспалительных и нейродегенеративных процессах.
Исследование F. Mogensen и соавт. (2021) дополнило эти представления, показав, что активация или угнетение глимфатического тока тесно связаны с воспалительными процессами и проницаемостью астроцитарных мембран [41]. Авторы подчеркивают, что глимфатическая система реагирует на изменения в нейроваскулярной и иммунной регуляции, что делает ее потенциальным участником ответной реакции головного мозга на различные формы стрессорного воздействия, включая электрическую стимуляцию.
Прямых данных о влиянии ЭСТ на скорость тока ликвора или объем межклеточного пространства пока нет. Однако работа S. Mindt и соавт. (2020) показала, что после курса ЭСТ концентрация BDNF в спинномозговой жидкости достоверно возрастает, что можно рассматривать как косвенное свидетельство изменения барьерных и обменных свойств цереброспинальной среды [42]. Этот результат позволяет предположить, что судорожная активность, индуцированная ЭСТ, способна модифицировать обмен между нейрональной и ликворной системами, улучшая условия для метаболической «очистки» головного мозга.
Таким образом, гипотеза глимфатической активации при ЭСТ пока остается концептуальной, но имеет определенные предпосылки. Возможное улучшение транспорта ликвора, уменьшение нейровоспаления и нормализация микросреды головного мозга могут рассматриваться как дополнительные механизмы восстановления нейрохимического гомеостаза и антидепрессивного эффекта ЭСТ (Рис. 3).
Однако оптимизация клиренса метаболитов и ионного баланса формирует условия для адаптивного митохондриального ответа и иммунометаболической перенастройки (AMPK-SIRT1-PGC-1α-NRF2), снижая оксидативную и воспалительную нагрузку.
 Митохондриально-иммунометаболические механизмы действия электросудорожной терапии
Митохондриально-иммунометаболические механизмы действия электросудорожной терапии
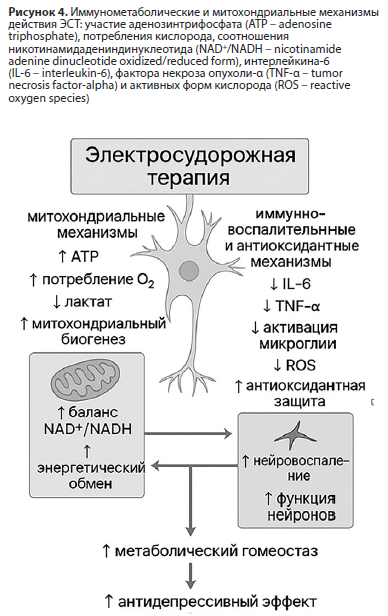
ЭСТ рассматривается как не просто нейромодуляционная, но и метаболически активирующая процедура, способная вызывать скоординированный клеточный ответ, направленный на восстановление энергетического гомеостаза и снижение воспаления (Рис. 4). Современные данные свидетельствуют, что ЭСТ запускает адаптивный митохондриальный стресс-ответ, активируя сигнальные каскады AMPK (5′ AMP-activated protein kinase, 5′-АМФ-активируемая протеинкиназа), SIRT1 (sirtuin 1, сиртуин-1), PGC-1α (peroxisome proliferator-activated receptor gamma coactivator 1-alpha, коактиватор γ-рецептора, активируемого пероксисомным пролифератором-1α) и NRF2 (nuclear factor erythroid 2-related factor 2, ядерный фактор, связанный с эритроидным фактором 2). Эти сигнальные пути играют ключевую роль в регуляции митохондриального биогенеза, антиоксидантной защиты и клеточного выживания [20].
Кратковременная электрическая стимуляция активирует сенсорные механизмы энергетического дефицита, прежде всего AMPK, которая усиливает катаболические процессы, повышая продукцию аденозинтрифосфата и стимулируя экспрессию коактиватора PGC-1α – основного регулятора митохондриального биогенеза [44]. Работы S. Goldfarb и соавт. (2020) показали, что электроконвульсивная стимуляция снижала микроглиальную нейротоксичность и уровень активных форм кислорода, демонстрируя нейропротективный и метаболически стабилизирующий эффект [44].
Иммунометаболические эффекты
ЭСТ влияет на взаимодействие энергетического и иммунного обмена. В клинических исследованиях наблюдалось снижение уровней IL-6, TNF-α и CРБ после курса терапии, что согласуется с переходом микроглии из провоспалительного (M1) в регенеративный (M2) фенотип [20, 24]. Этот эффект, вероятно, опосредован восстановлением митохондриального дыхания и снижением сигнала опасности DAMPs (damage-associated molecular patterns, молекулярные паттерны, ассоциированные с повреждением), поступающего от поврежденных митохондрий.
В совокупности активация каскадов AMPK-SIRT1-PGC-1α-NRF2 и нормализация воспалительных медиаторов формируют целостный адаптационный ответ, который можно рассматривать как биоэнергетическую перезагрузку. Таким образом, ЭСТ действует в режиме «мягкого клеточного стресса», усиливающего устойчивость, пластичность и метаболическую эффективность головного мозга (Рис. 4).
Энергетическая адаптация тесно сопряжена с микроциркуляцией и барьерной функцией; в связи с чем далее логично рассмотреть изменения нейроваскулярной единицы (VEGF/mTORC1, перициты, AQP4) как сосудисто-глиальный субстрат пластичности.
Нейроваскулярно-глиальные взаимодействия в механизмах действия электросудорожной терапии
В последние годы все больше данных указывает, что эффекты ЭСТ выходят за рамки чисто нейрональных процессов и включают активацию нейроваскулярной единицы (NVU – neurovascular unit) – функционального ансамбля, включающего нейроны, астроциты, перициты, эндотелиальные клетки и элементы базальной мембраны. ЭСТ можно рассматривать как системный модулятор нейро-глио-сосудистого обмена, влияющий на транспорт, микроциркуляцию и метаболическое сопряжение нейронов.
Одним из ключевых медиаторов этого эффекта является фактор роста эндотелия сосудов (VEGF). Его экспрессия усиливается после курса ЭСТ и коррелирует с пролиферацией нейральных предшественников и ангиогенезом в гиппокампе [45]. Параллельно активируется сигнальный путь mTORC1-VEGF, обеспечивающий синтез белков, необходимых для сосудистого ремоделирования [46]. Эти процессы создают основу для ангио- и нейрогенеза, способствуя структурной реабилитации гиппокампо-префронтальных контуров.
Однако данные последних лет расширяют понимание этого механизма, указывая на участие перицитов – клеток сосудистой стенки, регулирующих проницаемость гематоэнцефалического барьера (ГЭБ), тонус капилляров и трофическую поддержку эндотелия. Нарушения функции перицитов ассоциированы с депрессией, когнитивным дефицитом и микрососудистыми изменениями [47]. Предполагается, что ЭСТ, повышая VEGF-зависимую сигнализацию, способствует восстановлению перицитарной активности и целостности ГЭБ, что улучшает трофику и метаболический обмен между кровью и нервной тканью.
Особое место занимает астроцитарный компонент NVU. Исследования на животных моделях показали, что электроконвульсивная стимуляция повышает экспрессию аквапорина-4 (AQP4) и белков плотных контактов (claudin-5), а также восстанавливает покрытие капилляров астроцитарными ножками [48]. Эти эффекты ведут к нормализации глимфатического клиренса и регуляции ионного гомеостаза. Одновременно активируется астроцитарно-нейрональное метаболическое сопряжение (astrocyte–neuron lactate shuttle), при котором астроциты усиливают гликолиз и экспортируют лактат к нейронам в качестве субстрата для окислительного фосфорилирования [49]. Подобный энергетический обмен играет критическую роль в восстановлении нейрональной активности и синаптической пластичности после ЭСТ.
Таким образом, ЭСТ инициирует многоуровневую перестройку нейроваскулярно-глиального ансамбля: усиливает VEGF/mTOR-зависимый ангиогенез, стабилизирует ГЭБ и перицитарные связи, активирует астроцитарно-нейрональное сопряжение и оптимизирует локальную доставку метаболитов (Рис. 5). Эти процессы формируют благоприятные условия для нейропластического восстановления и устойчивой ремиссии депрессивного состояния.
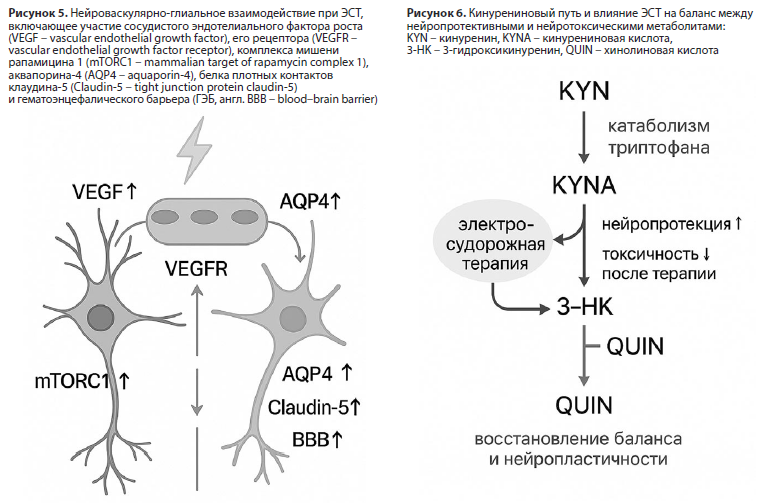
Ограничением остается недостаток прямых нейровизуализационных подтверждений перицитарных и метаболических изменений у человека после ЭСТ. Тем не менее конвергенция данных молекулярных, морфологических и метаболических исследований позволяет рассматривать NVU как центральную мишень системного действия ЭСТ, объединяющую сосудистую, глиальную и энергетическую регуляцию головного мозга.
Однако нормализация микроциркуляции и барьеров снижает провоспалительный фон и модифицирует триптофановый метаболизм, что отражается на балансе кинурениновых метаболитов между нейротоксическим и нейропротективным звеньями.
Кинурениновый путь и нейроиммунно-метаболические механизмы действия ЭСТ
Кинурениновый путь является основным направлением катаболизма триптофана, конкурирующим с серотониновым каскадом и обеспечивающим до 95% его метаболизма. В норме этот путь сбалансирован между нейропротективным и нейротоксическим звеньями, представленными, соответственно, кинурениновой кислотой (KYNA) и хинолиновой кислотой (QUIN) [50].
Под действием провоспалительных цитокинов (IFN-γ, IL-6, TNF-α) активируется фермент индоламин-2,3-диоксигеназа (IDO), что увеличивает превращение триптофана в кинуренин и смещает метаболизм в сторону образования нейротоксичных производных – 3-гидроксикинуренина (3-HK) и QUIN. Эти метаболиты усиливают NMDA-зависимую нейротоксичность, оксидативный стресс и микроглиальную активацию, что связывают с патогенезом депрессии [51, 52].
Метаанализы последних лет подтвердили наличие дисбаланса кинуренинового пути при большой депрессии – снижения уровней KYN и KYNA при повышении QUIN и 3-HK [53]. Эти изменения коррелируют с выраженностью воспалительного статуса и тяжестью симптоматики.
Интерес представляют работы, в которых ЭСТ рассматривается как модератор кинуренинового метаболизма. В пилотном исследовании L. Schwieler и соавт. (2016) показано, что курс ЭСТ у пациентов с резистентной депрессией подавляет нейротоксическую ветвь кинуренинового пути, снижая концентрации QUIN и повышая KYNA [54]. Это сопровождалось клиническим улучшением и снижением уровня воспалительных маркеров.
Результаты молекулярного анализа K. Ryan и соавт. (2025) продемонстрировали, что ЭСТ может модулировать экспрессию генов ферментов KP – IDO1, KMO и KYAT – в периферических мононуклеарах крови, что подтверждает системный характер этого эффекта [55]. Авторы предполагают, что восстановление баланса между IDO-зависимой и KAT-зависимой активностью является одним из звеньев антидепрессивного действия ЭСТ.
С учетом того, что конечные продукты кинуренинового пути вовлечены в синтез NAD+ (через QUIN), воздействие ЭСТ на этот путь может быть связано и с улучшением митохондриального метаболизма. Таким образом, кинурениновая система выступает как интегративное звено между воспалением, энергетическим обменом и нейропластичностью, а ее нормализация после ЭСТ отражает переход от воспалительно-токсического к адаптивно-пластическому фенотипу (Рис. 6).
Несмотря на обнадеживающие результаты, доказательная база остается ограниченной: большинство исследований проведено на периферических образцах, а динамика метаболитов в ЦНС не изучена. Перспективным направлением является мультиомный анализ метаболомов, транскриптомов и маркеров воспаления до и после ЭСТ, что позволит уточнить роль кинуренинового пути как биомаркера ответа на терапию.
Ось «кишечник–мозг» в системных эффектах электросудорожной терапии
Так как сдвиги кинуренинового каскада связаны с системным воспалением и доступностью триптофана, следующий рассматриваемый уровень – двунаправленная регуляция со стороны кишечного микробиома и барьерной функции ЖКТ.
Ось «кишечник–мозг» (gut-brain axis) представляет собой сложную двунаправленную систему взаимодействия между ЦНС, эндокринной, иммунной и энтеральной нервной системами [56, 57]. Ключевым элементом этого взаимодействия выступает микробиота кишечника, продуцирующая широкий спектр биологически активных соединений – короткоцепочечные жирные кислоты, нейротрансмиттеры, индольные метаболиты триптофана и цитокины, – влияющие на состояние ГЭБ, микроглии и стресс-оси ГГН [58].
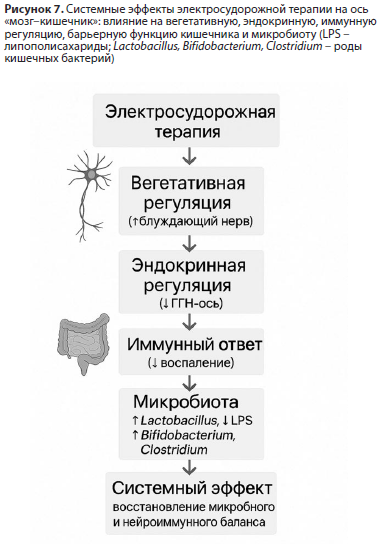 Накопленные данные указывают, что при депрессии и хроническом стрессе наблюдается дисбиоз кишечного микробиома – снижение доли Lactobacillus и Bifidobacterium, рост условно-патогенных таксонов (Clostridium, Ruminococcus, Alistipes), повышение проницаемости кишечного барьера и увеличение уровней липополисахаридов (LPS) в крови [59, 60]. Эти изменения сопровождаются активацией провоспалительных каскадов, повышением концентрации IL-6 и TNF-α, активацией индоламин-2,3-диоксигеназы (IDO) и усилением кинуренинового обмена, что связывает микробиоту с нейроиммунной дисрегуляцией и формированием депрессивного фенотипа [61].
Накопленные данные указывают, что при депрессии и хроническом стрессе наблюдается дисбиоз кишечного микробиома – снижение доли Lactobacillus и Bifidobacterium, рост условно-патогенных таксонов (Clostridium, Ruminococcus, Alistipes), повышение проницаемости кишечного барьера и увеличение уровней липополисахаридов (LPS) в крови [59, 60]. Эти изменения сопровождаются активацией провоспалительных каскадов, повышением концентрации IL-6 и TNF-α, активацией индоламин-2,3-диоксигеназы (IDO) и усилением кинуренинового обмена, что связывает микробиоту с нейроиммунной дисрегуляцией и формированием депрессивного фенотипа [61].
ЭСТ может опосредованно воздействовать на микробиоту через нормализацию нейровегетативных и нейроэндокринных контуров, улучшая барьерную функцию кишечника и снижая уровень системного воспаления. Восстановление симбиотического микробного профиля может, в свою очередь, способствовать снижению продукции LPS, модуляции цитокинового ответа и нормализации триптофанового метаболизма (Рис. 7).
Таким образом, ось «кишечник–мозг» может рассматриваться как одно из системных звеньев биологического ответа на ЭСТ. Нейровегетативная активация, горметическое воспалительное торможение и улучшение барьерной функции кишечника формируют условия для стабилизации нейроиммунного гомеостаза. Перспективными направлениями исследований являются метагеномные и метаболомные анализы до и после курса ЭСТ, а также изучение взаимосвязи изменений микробиоты с динамикой цитокинов и метаболитов кинуренинового пути.
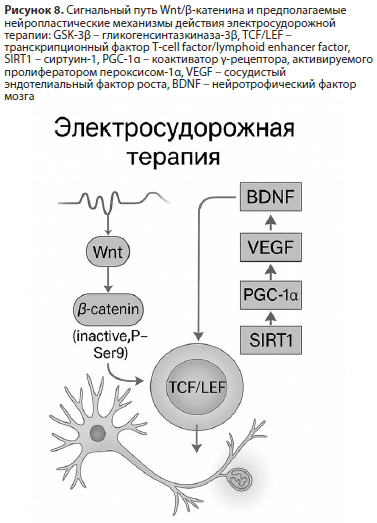 Сигнальный путь Wnt/β-катенина
Сигнальный путь Wnt/β-катенина
и нейропластические механизмы действия электросудорожной терапии
Через эндокринно-иммунные и метаболические сигналы ось «кишечник–мозг» опосредованно влияет на внутримозговые каскады нейропластичности; на этом фоне уместно рассмотреть роль Wnt/β-катенина как интегратора пластических программ.
Сигнальный путь Wnt/β-катенина является универсальным регулятором эмбрионального развития, нейрогенеза и синаптической пластичности, а также одним из ключевых каскадов, участвующих в поддержании структурной и функциональной целостности нервной ткани [62, 63].
В зрелом головном мозге активация Wnt-передачи обеспечивает выживаемость нейронов, стимулирует экспрессию BDNF и VEGF, способствует дендритогенезу и синаптическому ремоделированию [64].
При депрессии отмечается ингибиция Wnt-сигналинга и гиперактивация GSK-3β (glycogen synthase kinase-3β) – фермента, фосфорилирующего β-катенин и способствующего его деградации в протеасомах. Это приводит к снижению транскрипции генов, регулируемых β-катенином, и к ослаблению нейропластических процессов [65, 66].
Исследования на животных моделях показали, что электроконвульсивная стимуляция (аналог ЭСТ) активирует Wnt/β-катениновый путь в гиппокампе и префронтальной коре. В работе H. Okamoto и соавт. (2010) продемонстрировано, что после серии стимуляций повышается экспрессия β-катенина, а также фосфорилирование GSK-3β по Ser9 – маркер ее инактивации [62].
На молекулярном уровне ЭСТ, вероятно, инициирует фосфорилирование GSK-3β и стабилизацию β-катенина, что активирует транскрипцию пластичностных генов через TCF/LEF-комплексы. Эти изменения ведут к восстановлению синаптической архитектуры, аксонального роста и нейротрофического потенциала.
Интересно, что активация Wnt/β-катениновой передачи тесно взаимодействует с митохондриальными и эпигенетическими механизмами, ранее описанными при ЭСТ. β-катенин регулирует экспрессию антиоксидантных ферментов, участвует в контроле митохондриальной биогенезы (через взаимодействие с PGC-1α) и может быть мишенью для NAD+/SIRT1-зависимой деацетилации [67]. Эти перекрестные связи делают Wnt/β-катениновый путь интегративным центром клеточной адаптации при действии ЭСТ.
Таким образом, можно рассматривать ЭСТ как нейротрофическое и нейропластическое вмешательство, частично реализующее свои эффекты через активацию Wnt/β-катенинового каскада. Этот путь объединяет энергетические, эпигенетические и синаптические компоненты клеточного ответа, формируя основу для долговременного восстановления нейросетевой архитектуры и эмоционально-когнитивного гомеостаза.
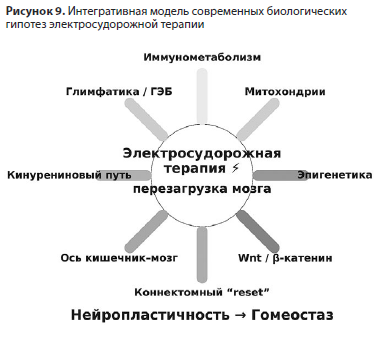 Интегративная многоуровневая модель биологических эффектов электросудорожной терапии
Интегративная многоуровневая модель биологических эффектов электросудорожной терапии
Современное понимание ЭСТ выходит за пределы нейротрансмиттерных и эндокринных моделей. На основании накопленных данных ее можно рассматривать как координированное многоуровневое вмешательство, в котором электрический стимул запускает серию взаимосвязанных процессов – от молекулярных и клеточных до системных и нейросетевых.
На молекулярном уровне эффект реализуется через эпигенетические перестройки: изменения метилирования ДНК, активности miRNA и lncRNA, что переопределяет экспрессию генов, связанных со стресс-ответом, пластичностью и энергетическим метаболизмом.
Клеточные и метаболические реакции включают активацию митохондриального стресс-ответа, усиление биогенеза, антиоксидантную защиту и восстановление NAD+-зависимых путей. Эти процессы обеспечивают энергетическую устойчивость нейронов и снижают воспалительный фон.
На уровне микроокружения мозга активируются глимфатические и нейроваскулярно-глиальные механизмы: оптимизируется ликворо-интерстициальный обмен, усиливается ангиогенез и астроцитарно-нейрональное сопряжение, что улучшает трофику и барьерные функции.
Иммунометаболическое звено проявляется нормализацией кинуренинового пути, снижением продукции нейротоксичных метаболитов и смещением иммунного профиля в сторону противовоспалительного фенотипа.
На висцерально-системном уровне происходят адаптивные изменения в оси «кишечник–мозг»: стабилизация микробиоты, улучшение барьерной функции кишечника и снижение системного воспаления, что поддерживает центральные процессы нейропластичности.
Завершающий контур модели связан с активацией сигнального пути Wnt/β-катенина, регулирующего синаптогенез, дендритогенез и экспрессию BDNF и VEGF. Именно этот каскад обеспечивает долговременную перестройку нейрональных сетей и интеграцию молекулярных и системных уровней ответа.
В совокупности эти процессы формируют единый феномен нейробиологического ремоделирования – переход головного мозга в новое состояние функциональной и энергетической целостности, при котором восстановление сетевых связей сочетается с биохимической и структурной стабилизацией нейроткани (Рис. 9).
Разумеется, предложенная автором модель – это не «новая аксиома нейронаук», а лишь попытка собрать воедино современные литературные данные и увидеть в них общую логику. Это гипотетическая, теоретическая конструкция, призванная помочь осмыслить феномен ЭСТ как системный биологический процесс, а не эмпирическую процедуру. Впрочем, если в ней окажется доля истины – пусть ею займутся уже будущие поколения нейробиологов.
Заключение
ЭСТ – не просто исторически сложившийся метод лечения депрессии, а точная нейромодуляционная технология, использующая потенциал контролируемого клеточного стресса. Кратковременная электрическая стимуляция активирует каскады адаптации и восстановления, приводя к нормализации энергетического обмена, снижению воспаления и перестройке нейросетевой динамики.
Эта способность запускать скоординированный стресс-ответ позволяет рассматривать ЭСТ как биологический триггер пластичности, восстанавливающий нарушенные связи между молекулярными, сосудистыми и нейрональными системами.
Будущее метода – в его персонализации. Использование объективных биомаркеров (метилирование FKBP5, экспрессия BDNF и VEGF, параметры NAD+/NADH, показатели связности DMN-CEN-SN) позволит подбирать оптимальные параметры стимуляции и прогнозировать терапевтический ответ.
Интеграция мультиомных, нейровизуализационных и физиологических подходов откроет путь к новой модели – точной нейромодуляционной психиатрии, в которой ЭСТ станет инструментом системного восстановления нейробиологического гомеостаза и индивидуальной нейропластической резилентности.
Информация об авторах
Быков Юрий Витальевич, к.м.н., доцент кафедры анестезиологии и реаниматологии с курсом ДПО, Ставропольский государственный медицинский университет
ORCID: 0000-0003-4705-3823. E-mail:
Беккер Роман Александрович, независимый исследователь в области психофармакотерапии, Израиль
ORCID: 0000-0002-0773-3405. E-mail:
Дата поступления: 21.11.2025
Received: 21.11.2025
Принята к печати: 06.02.2026
Accepted: 06.02.2026
Автор заявляет об отсутствии конфликта интересов.
Author declares no conflicts of interest
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№01 2026
Перезагрузка мозга: интегративная многоуровневая модель биологических эффектов электросудорожной терапии №01 2026
Номера страниц в выпуске:4-14
Резюме
Цель работы – интеграция современных биологических гипотез электросудорожной терапии (ЭСТ), раскрывающих ее как многоуровневое системное вмешательство, выходящее за рамки классических нейротрансмиттерных моделей. На основе данных нейровизуализации, молекулярной биологии и мультиомики рассмотрены восемь взаимосвязанных направлений: эпигенетическая регуляция (метилирование ДНК, miRNA, lncRNA), митохондриально-иммунометаболические каскады (AMPK-SIRT1-PGC-1α-NRF2), коннектомная ресинхронизация сетей (DMN, CEN, SN, лимбико-таламические и мозжечковые контуры), глимфатическая и нейроваскулярно-глиальная регуляция, кинурениновый путь, ось «кишечник–мозг» и сигнальный путь Wnt/β-катенина. Выдвигается многоуровневая модель, согласно которой данные механизмы формируют единый каскад нейробиологического ремоделирования, направленного на восстановление функциональной и энергетической целостности головного мозга. ЭСТ рассматривается как форма контролируемого клеточного стресса, инициирующая эпигенетическую репрограммировку, метаболическую адаптацию и сетевую ресинхронизацию, что открывает перспективы персонализированной нейромодуляционной терапии.
Ключевые слова: электросудорожная терапия, нейромодуляция, эпигенетическая регуляция, митохондриальный стресс-ответ, иммунометаболизм, глимфатическая система, нейроваскулярно-глиальная единица, кинурениновый путь, ось «кишечник–мозг»; сигнальный путь Wnt/β-катенина; нейропластичность; коннектомный reset.
Для цитирования: Быков Ю.В., Беккер Р.А. Перезагрузка мозга: интегративная многоуровневая модель биологических эффектов электросудорожной терапии. Психиатрия и психофармакотерапия. 2026; 1: 4–14. DOI: 10.62202/2075-1761-2026-28-1-4-14
Цель работы – интеграция современных биологических гипотез электросудорожной терапии (ЭСТ), раскрывающих ее как многоуровневое системное вмешательство, выходящее за рамки классических нейротрансмиттерных моделей. На основе данных нейровизуализации, молекулярной биологии и мультиомики рассмотрены восемь взаимосвязанных направлений: эпигенетическая регуляция (метилирование ДНК, miRNA, lncRNA), митохондриально-иммунометаболические каскады (AMPK-SIRT1-PGC-1α-NRF2), коннектомная ресинхронизация сетей (DMN, CEN, SN, лимбико-таламические и мозжечковые контуры), глимфатическая и нейроваскулярно-глиальная регуляция, кинурениновый путь, ось «кишечник–мозг» и сигнальный путь Wnt/β-катенина. Выдвигается многоуровневая модель, согласно которой данные механизмы формируют единый каскад нейробиологического ремоделирования, направленного на восстановление функциональной и энергетической целостности головного мозга. ЭСТ рассматривается как форма контролируемого клеточного стресса, инициирующая эпигенетическую репрограммировку, метаболическую адаптацию и сетевую ресинхронизацию, что открывает перспективы персонализированной нейромодуляционной терапии.
Ключевые слова: электросудорожная терапия, нейромодуляция, эпигенетическая регуляция, митохондриальный стресс-ответ, иммунометаболизм, глимфатическая система, нейроваскулярно-глиальная единица, кинурениновый путь, ось «кишечник–мозг»; сигнальный путь Wnt/β-катенина; нейропластичность; коннектомный reset.
Для цитирования: Быков Ю.В., Беккер Р.А. Перезагрузка мозга: интегративная многоуровневая модель биологических эффектов электросудорожной терапии. Психиатрия и психофармакотерапия. 2026; 1: 4–14. DOI: 10.62202/2075-1761-2026-28-1-4-14
Brain Reset: An Integrative Multilevel Model of the Biological Effects of Electroconvulsive Therapy
Bykov Yu.V.1, Bekker R.A.21 Stavropol State Medical University, Ministry of Health, Russian Federation, Stavropol, str. Mira, 310, PO 355017;
2 Independent researcher in the field of psychopharmacology, Israel, Azur 5801726, str. Ben-Gurion 26/7
Abstract
The aim of this paper is to integrate contemporary biological hypotheses of electroconvulsive therapy (ECT), presenting it as a multi-level systemic intervention beyond classical neurotransmitter and neuroendocrine models. Based on neuroimaging, molecular, and multi-omics data, eight interrelated mechanisms are analyzed: epigenetic regulation (DNA methylation, miRNA, lncRNA), mitochondrial-immunometabolic cascades (AMPK-SIRT1-PGC-1α-NRF2), connectome resynchronization of neural networks (DMN, CEN, SN, limbic–thalamic and cerebellar circuits), glymphatic and neurovascular-glial regulation, the kynurenine pathway, the gut-brain axis, and Wnt/β-catenin signaling. A multi-level model is proposed, according to which these mechanisms form a unified cascade of neurobiological remodeling aimed at restoring the functional and energetic integrity of the brain. ECT is interpreted as a form of controlled cellular stress that triggers epigenetic reprogramming, metabolic adaptation, and network resynchronization, thereby establishing a new homeostatic equilibrium and opening perspectives for personalized neuromodulation in modern psychiatry.
Keywords: electroconvulsive therapy, neuromodulation, epigenetic regulation, mitochondrial stress response, immunometabolism, glymphatic system, neurovascular-glial unit, kynurenine pathway, gut–brain axis; Wnt/β-catenin signaling, neuroplasticity, connectome reset.
For citation: Bykov Yu.V., Bekker R.A. Brain Reset: An Integrative Multilevel Model of the Biological Effects of Electroconvulsive Therapy. Psychiatry and psychopharmacotherapy. 2026; 1: 4–14. DOI: 10.62202/2075-1761-2026-28-1-4-14
Введение
Электросудорожная терапия (ЭСТ) остается одним из наиболее изученных и эффективных биологических методов лечения психических заболеваний [1-5]. Она основана на индуцировании контролируемого кратковременного генерализованного судорожного припадка с помощью серии электрических импульсов, подаваемого на головной мозг пациента под общей анестезией и с применением миорелаксации [6-8].
Метод был впервые применен в 1938 году итальянскими психиатрами Уго Черлетти (Ugo Cerletti) и Лучо Бини (Lucio Bini), которые использовали электрическую стимуляцию для лечения больных шизофренией [7, 9]. В течение последующих десятилетий ЭСТ стала использоваться в терапии кататонии, маниакальных эпизодов, тяжелой депрессии и шизоаффективных состояний [1, 2, 7, 10].
Современная ЭСТ проводится в условиях блока интенсивной терапии с применением общей анестезии и миорелаксации, мониторинга жизненно важных функций и подбора индивидуальных параметров электростимуляции, что обеспечивает для пациентов высокий уровень безопасности и переносимости [7, 8, 11, 12]. Согласно международным клиническим рекомендациям, метод показан при фармакорезистентной депрессии, кататонии, острой суицидальности, при отдельных формах мании и шизофрении, ряде ургентных опасных для жизни состояний типа фебрильной шизофрении и злокачественного нейролептического синдрома [1-3, 13].
Клинические исследования достаточно давно подтверждают высокую эффективность ЭСТ при депрессии: частота терапевтического ответа превышает 70-80% даже у пациентов, не отвечающих на медикаментозное лечение [14, 15]. Наряду с традиционными психиатрическими показаниями, методика находит применение при неврологических и нейропсихиатрических расстройствах – болезни Паркинсона, обсессивно-компульсивном расстройстве, эпилепсии, посттравматическом стрессовом расстройстве [2, 16].
Эволюция техники позволила значительно повысить безопасность процедуры [7, 8]. Переход от стимуляции постоянным или синусоидальным током к импульсным стимулам, внедрение односторонних и билатеральных электродных конфигураций, а также использование коротких и ультракоротких импульсов снизили риск когнитивных побочных эффектов без потери эффективности [1, 4, 5, 11, 17]. Эти усовершенствования сделали ЭСТ одним из наиболее контролируемых и стандартизованных методов нейромодуляции в современной психиатрии.
Представленный обзор носит синтетический характер и объединяет данные различного уровня доказательности – от молекулярных и клеточных до системных и клинических. Целью работы является не установление прямых причинно-следственных зависимостей, а формирование целостного представления о многоуровневых механизмах ЭСТ как системного биологического вмешательства.
Классические механизмы действия электросудорожной терапии
За более чем 80 лет применения ЭСТ прошла путь от эмпирического метода до одного из наиболее исследованных нейромодуляционных вмешательств. В рамках настоящего обзора акцент сделан на наиболее изученных и воспроизводимых направлениях, подтвержденных в экспериментальных и клинических исследованиях: нейротрансмиттерное, нейроэндокринное, нейротрофическое, нейропластическое и иммунное. Эти системы формируют фундамент классических представлений о биологических эффектах ЭСТ и служат отправной точкой для анализа ее современных многоуровневых механизмов.
Нейротрансмиттерная модуляция
Классические работы достаточно давно продемонстрировали, что ЭСТ вызывает выраженные сдвиги в уровне моноаминовых медиаторов, включая серотонин, норадреналин и дофамин [1, 7]. Повышение серотонинергической активности и чувствительности постсинаптических 5-HT1A-рецепторов рассматривается как один из ключевых компонентов антидепрессивного эффекта [18]. Кроме того, ЭСТ нормализует баланс тормозных и возбуждающих систем, увеличивая активность ГАМК-ергических путей и снижая гиперглутаматергическую передачу [8, 19].
Нейроэндокринные и стресс-осевые эффекты
ЭСТ индуцирует кратковременную активацию гипоталамо-гипофизарно-надпочечниковой (ГГН) оси, сопровождающуюся выбросом кортизола, пролактина и адренокортикотропного гормона [7, 8, 18]. При повторных сеансах отмечается нормализация стресс-ответа и снижение исходной гиперактивации ГГН-оси [8, 19, 20]. Эти реакции рассматриваются как регулируемый нейроэндокринный «перезапуск» гомеостатических регуляторных систем.
Нейротрофические и пластические процессы
Одним из наиболее воспроизводимых открытий стало повышение экспрессии нейротрофинов – прежде всего Brain-Derived Neurotrophic Factor (BDNF, нейротрофический фактор, полученный из мозга), Vascular Endothelial Growth Factor (VEGF, сосудистый эндотелиальный фактор роста) и Glial cell line-Derived Neurotrophic Factor (GDNF, глиальный нейротрофический фактор, продуцируемый клетками глиального ряда) [1, 18]. Исследования на животных и у людей показали, что ЭСТ активирует транскрипцию генов нейротрофических факторов, усиливает синаптогенез и способствует восстановлению дендритных структур [1, 20]. Эти процессы коррелируют с клиническим улучшением и формируют основу так называемой «нейропластической гипотезы» ЭСТ.
Структурные и морфологические перестройки
Магнитно-резонансные исследования подтвердили, что курс ЭСТ приводит к увеличению объема гиппокампа, медиальной префронтальной коры и поясной извилины [1, 21, 22]. Эти изменения отражают не только нейрогенез, но и более комплексные формы нейро- и глиопластичности, включая ремоделирование сосудов и глиальных структур [4, 5]. Эти эффекты сохраняются после завершения курса и коррелируют с устойчивым клиническим ответом.
Иммунные и нейровоспалительные механизмы
Накоплены убедительные данные о положительном влиянии ЭСТ на иммунный статус [1, 18]. Систематический обзор [23] показал, что после курса ЭСТ снижаются уровни провоспалительных цитокинов (IL-6, TNF-α) и С-реактивного белка (СРБ). Данный эффект связывают с переключением активации микроглии в антивоспалительный фенотип и нормализацией взаимодействия иммунных и нейрональных сигнальных каскадов [20].
Интеграция классических механизмов
В совокупности классические исследования показывают, что ЭСТ действует многоуровнево – сочетая модуляцию моноаминовой передачи, нормализацию стресс-осевых и эндокринных систем, усиление нейротрофических каскадов и запуск пластических процессов, затрагивающих как нейрональные, так и глиальные элементы головного мозга. Современные обзоры подчеркивают, что эти эффекты не являются независимыми, а формируют единый каскад «нейробиологического ремоделирования», приводящего к восстановлению сетевой и метаболической целостности головного мозга [1, 19].
Несмотря на убедительную базу классических моделей, остается ряд нерешенных вопросов: каким образом эти процессы запускаются, какие из них являются первичными, а какие вторичными, и почему терапевтический эффект ЭСТ столь универсален? Ответы на эти вопросы формируют контуры новейших биологических гипотез, рассматривающих ЭСТ как многоуровневое системное вмешательство, выходящее далеко за рамки нейротрансмиттерных и эндокринных теорий.
К ним относятся восемь взаимосвязанных направлений: эпигенетическая регуляция, митохондриально-иммунометаболические каскады, коннектомная ресинхронизация нейросетей, глимфатическая и нейроваскулярно-глиальная регуляция, кинурениновый путь, ось «кишечник–мозг», а также сигнальный путь Wnt/β-катенина. Выбор именно этих восьми направлений не случаен. Они отражают наиболее активно развивающиеся и конвергентные линии исследований последних лет, в которых накоплены молекулярные, нейровизуализационные и клинические данные, демонстрирующие участие соответствующих механизмов в терапевтическом действии ЭСТ. Таким образом, рассмотренные направления представляют собой ядро современного представления о системной биологии ЭСТ, где каждая гипотеза дополняет другие, формируя целостную модель нейробиологического ремоделирования.
 Новые механизмы действия электросудорожной терапии
Новые механизмы действия электросудорожной терапииЭпигенетические изменения, индуцируемые электросудорожной терапией
Исследования последних лет демонстрируют, что ЭСТ способна вызывать изменения в эпигенетических механизмах регуляции генной экспрессии, прежде всего в метилировании дезоксирибонуклеиновой кислоты (ДНК; Рис. 1). Эти изменения рассматриваются как возможное молекулярное звено, опосредующее терапевтический эффект ЭСТ при депрессии [1, 24].
В пилотном исследовании N. Moschny и соавт. (2020) был проведен анализ метилома (эпигенетических изменений метилирования ДНК) в периферических мононуклеарах крови у пациентов с депрессией, получавших курс ЭСТ. Авторы выявили восемь генов-кандидатов (RNF175, RNF213, TBC1D14, TMC5, WSCD1, LINC-ROR, ADARB2, RBMXL1) и два CpG-сайта в генах AQP10 и TRERF1, демонстрировавших значимые сдвиги уровня метилирования в процессе лечения [25]. Эти данные рассматриваются как потенциальные маркеры биологического отклика на ЭСТ, требующие дальнейшего подтверждения.
Результаты независимой группы L. Sirignano и соавт. (2021) дополнили эти наблюдения: изменения метилирования CpG-сайтов в генах TNKS и FKBP5 коррелировали с выраженностью клинического ответа по шкале Hamilton Depression Rating Scale (HDRS, Шкала Гамильтона для оценки выраженности депрессии) [26]. Систематический обзор S. Castro и соавт. [27], включивший девять исследований, показал, что наибольший интерес вызывают гены BDNF, FKBP5, S100A10, RNF213 и TNKS, однако все доступные данные остаются ограниченными малым числом выборок и разнородностью методик.
Помимо метилирования ДНК, все больше внимания привлекают некодирующие регуляторные РНК – прежде всего microRNA (miRNA), а также длинные и циркулярные некодирующие РНК (lncRNA, circRNA), участвующие в эпигенетической регуляции экспрессии генов.
Несмотря на ограниченность данных, ряд работ показал возможное участие miRNA в механизмах антидепрессивного эффекта ЭСТ. В частности, в пилотных исследованиях, включенных в обзор S. Castro и соавт. (2023), описаны сдвиги уровней miR-126, miR-106a и miR-24 у пациентов, ответивших на терапию [27]. Эти молекулы рассматриваются как потенциальные периферические биомаркеры ответа на ЭСТ, хотя авторы подчеркивают малый размер выборок и методическую гетерогенность.
MiRNA действуют как посттранскрипционные регуляторы, связываясь с 3´-UTR мРНК и ингибируя трансляцию или вызывая деградацию транскриптов [28]. Кроме того, они способны модулировать активность ключевых эпигенетических ферментов – ДНК-метилтрансфераз (DNMTs), гистон-деацетилаз (HDACs) и гистон-метилтрансфераз (HMTs), формируя двустороннюю связь между miRNA и эпигенетическим аппаратом клетки [29].
Эта взаимосвязь легла в основу концепции так называемых «epi-miRNA» – микроРНК, регулирующих ферменты, ответственные за метилирование ДНК и модификации гистонов [29, 30]. В свою очередь, экспрессия самих генов miRNA также может зависеть от метилирования их промоторных участков и ацетилирования гистонов, что формирует петлю эпигенетической обратной связи.
Гистоновые модификации – ацетилирование, метилирование, фосфорилирование – формируют еще один слой эпигенетической регуляции, влияющий на плотность упаковки хроматина и доступность генов для транскрипции [31]. Хотя прямых исследований влияния ЭСТ на гистоновые модификации пока нет, можно предположить, что кратковременный электрический стресс способен смещать баланс между HAT/HDAC и HMT/HDM в сторону открытого, транскрипционно активного хроматина, создавая условия для экспрессии генов нейропластичности, таких как BDNF и VEGF.
Дополнительное внимание заслуживают lncRNA и circRNA – длинные и кольцевые некодирующие транскрипты, участвующие в организации эпигенетического ландшафта. LncRNA способны связывать комплексы модификации хроматина (например, PRC2, HDAC) и направлять их к специфическим генам-мишеням, влияя на локальную структуру хроматина [30]. CircRNA, напротив, действуют как «губки» для miRNA, регулируя их доступность к мРНК-мишеням и тем самым косвенно влияя на эпигенетическую сеть.
Все доступные исследования эпигенетических эффектов ЭСТ, включающие анализ miRNA или других ncRNA, выполнены на периферических образцах (PBMC, плазма), и пока не подтверждены на уровне тканей головного мозга [27]. Отсутствуют также работы, оценивающие гистоновые модификации или экспрессию lncRNA и circRNA в центральной нервной системе (ЦНС) до и после ЭСТ. Эти ограничения делают раздел о некодирующих РНК и гистонах преимущественно концептуальным, но при этом подчеркивают перспективность дальнейших мультиомных исследований в этой области.
Но так или иначе, эпигенетические перестройки на фоне проведения ЭСТ формируют молекулярную основу для последующих системных изменений – прежде всего для перестройки нейросетевой активности и функциональной интеграции головного мозга, реализующихся в феномене коннектомного «reset».
 Коннектомный «reset» – перезапуск нейросетей
Коннектомный «reset» – перезапуск нейросетейСовременные исследования с использованием нейровизуализации показывают: ЭСТ воздействует на головной мозг не локально, а системно. Это не просто электрический стимул, а своего рода коннектомный «reset» – управляемая перезагрузка нейронных сетей. В момент проведения процедуры нарушаются патологические схемы функциональных связей, которые удерживают головной мозг в состоянии депрессии, и запускается процесс их перестройки в более здоровую и сбалансированную конфигурацию (Рис. 2).
Методы высокоразрешающей функциональной магнитно-резонансной томографии (фМРТ) и анализа коннектома показали, что ЭСТ уменьшает чрезмерную связанность между лимбическими и префронтальными областями, а также снижает гиперактивность Default Mode Network (DMN) – ключевой сети, активной в состоянии покоя. Именно она отвечает за внутренний диалог, размышления о себе, воспоминания и самоанализ. При депрессии DMN работает чрезмерно, удерживая человека в руминативных циклах – бесконечном прокручивании одних и тех же негативных мыслей [32].
Параллельно происходит перестройка взаимодействия между Central Executive Network (CEN) и Salience Network – сетями, регулирующими когнитивный контроль, внимание и способность оценивать значимость внешних и внутренних стимулов. После курса ЭСТ головной мозг постепенно переходит от хаотичной, рассогласованной работы к более организованной и скоординированной структуре [33].
Межцентровое исследование с использованием продольных данных фМРТ подтвердило: по мере проведения ЭСТ восстанавливается связность между ключевыми узлами DMN, а взаимодействие лобных и теменных зон возвращается к норме [34]. Изменения затрагивают не только стабильные (статические) связи, но и динамику сетевого взаимодействия, исследуемую методом динамической функциональной коннектомики (dynamic Functional Network Connectivity – dFNC).
Работа H. Dini и соавт. (2021) показала, что после ЭСТ снижается частота переходов между дезорганизованными состояниями головного мозга, усиливается преобладание устойчивых сетевых конфигураций и возрастает согласованность активности между фронтальными и теменными областями [35].
Терапевтический эффект ЭСТ во многом связан с восстановлением равновесия между DMN и CEN. Исследование Y. Pang и соавт. (2022) продемонстрировало: чем лучше восстанавливаются внутренние связи DMN и ее взаимодействие с CEN, тем выраженнее клиническое улучшение у пациентов с депрессией [36]. Аналогичные данные получили M. Moreno-Ortega и коллеги (2019), показавшие, что исходные параметры связности DMN могут предсказывать эффективность терапии [37].
ЭСТ также влияет на низкочастотные осцилляции и синхронность нейрональной активности. По данным S. Sun и соавт. (2022), во время процедуры возникает кратковременное расхождение фазовой активности между основными сетями покоя, после чего они стабилизируются на новом, более сбалансированном уровне [38]. Эти процессы сопровождаются нормализацией работы лобных отделов, ответственных за когнитивный контроль [39].
В целом совокупность данных свидетельствует: ЭСТ действует как сетевой «ресинхронизатор». Она разрушает патологические циклы активности и помогает головному мозгу самостоятельно перестроиться, находя новое устойчивое равновесие. С физиологической точки зрения это можно рассматривать как «жесткую перезагрузку» нейросетей, которая переводит головной мозг из застойного, дисфункционального режима в более оптимальное и согласованное состояние функциональной интеграции (Рис. 2).
Сетевые сдвиги устойчиво закрепляются при поддержании метаболического и ликворного гомеостаза; это выводит к рассмотрению роли глимфатической системы и обмена межклеточной жидкости в стабилизации новых паттернов активности.
 Глимфатическая и детоксикационная гипотеза
Глимфатическая и детоксикационная гипотезаРастущие данные указывают, что эффект ЭСТ может включать не только нейромодуляцию, но и воздействие на процессы метаболического и ликворного гомеостаза головного мозга. Одним из возможных направлений обсуждения является связь ЭСТ с глимфатической системой – системой обмена спинномозговой и межклеточной жидкости, ответственной за удаление метаболитов и поддержание химического равновесия мозговой среды (Рис. 3).
Согласно концепции глимфатической системы, сформулированной L. Hablitz и M. Nedergaard (2021), транспорт ликвора осуществляется по периваскулярным путям с участием астроцитов и аквапориновых каналов (AQP4), обеспечивая «промывание» интерстициального пространства и выведение продуктов обмена, включая β-амилоид и цитокины [40]. Эта система функционирует как ключевой элемент детоксикации и метаболического очищения головного мозга, особенно во время сна, и нарушается при нейровоспалительных и нейродегенеративных процессах.
Исследование F. Mogensen и соавт. (2021) дополнило эти представления, показав, что активация или угнетение глимфатического тока тесно связаны с воспалительными процессами и проницаемостью астроцитарных мембран [41]. Авторы подчеркивают, что глимфатическая система реагирует на изменения в нейроваскулярной и иммунной регуляции, что делает ее потенциальным участником ответной реакции головного мозга на различные формы стрессорного воздействия, включая электрическую стимуляцию.
Прямых данных о влиянии ЭСТ на скорость тока ликвора или объем межклеточного пространства пока нет. Однако работа S. Mindt и соавт. (2020) показала, что после курса ЭСТ концентрация BDNF в спинномозговой жидкости достоверно возрастает, что можно рассматривать как косвенное свидетельство изменения барьерных и обменных свойств цереброспинальной среды [42]. Этот результат позволяет предположить, что судорожная активность, индуцированная ЭСТ, способна модифицировать обмен между нейрональной и ликворной системами, улучшая условия для метаболической «очистки» головного мозга.
Таким образом, гипотеза глимфатической активации при ЭСТ пока остается концептуальной, но имеет определенные предпосылки. Возможное улучшение транспорта ликвора, уменьшение нейровоспаления и нормализация микросреды головного мозга могут рассматриваться как дополнительные механизмы восстановления нейрохимического гомеостаза и антидепрессивного эффекта ЭСТ (Рис. 3).
Однако оптимизация клиренса метаболитов и ионного баланса формирует условия для адаптивного митохондриального ответа и иммунометаболической перенастройки (AMPK-SIRT1-PGC-1α-NRF2), снижая оксидативную и воспалительную нагрузку.
 Митохондриально-иммунометаболические механизмы действия электросудорожной терапии
Митохондриально-иммунометаболические механизмы действия электросудорожной терапииЭСТ рассматривается как не просто нейромодуляционная, но и метаболически активирующая процедура, способная вызывать скоординированный клеточный ответ, направленный на восстановление энергетического гомеостаза и снижение воспаления (Рис. 4). Современные данные свидетельствуют, что ЭСТ запускает адаптивный митохондриальный стресс-ответ, активируя сигнальные каскады AMPK (5′ AMP-activated protein kinase, 5′-АМФ-активируемая протеинкиназа), SIRT1 (sirtuin 1, сиртуин-1), PGC-1α (peroxisome proliferator-activated receptor gamma coactivator 1-alpha, коактиватор γ-рецептора, активируемого пероксисомным пролифератором-1α) и NRF2 (nuclear factor erythroid 2-related factor 2, ядерный фактор, связанный с эритроидным фактором 2). Эти сигнальные пути играют ключевую роль в регуляции митохондриального биогенеза, антиоксидантной защиты и клеточного выживания [20].
Кратковременная электрическая стимуляция активирует сенсорные механизмы энергетического дефицита, прежде всего AMPK, которая усиливает катаболические процессы, повышая продукцию аденозинтрифосфата и стимулируя экспрессию коактиватора PGC-1α – основного регулятора митохондриального биогенеза [44]. Работы S. Goldfarb и соавт. (2020) показали, что электроконвульсивная стимуляция снижала микроглиальную нейротоксичность и уровень активных форм кислорода, демонстрируя нейропротективный и метаболически стабилизирующий эффект [44].
Иммунометаболические эффекты
ЭСТ влияет на взаимодействие энергетического и иммунного обмена. В клинических исследованиях наблюдалось снижение уровней IL-6, TNF-α и CРБ после курса терапии, что согласуется с переходом микроглии из провоспалительного (M1) в регенеративный (M2) фенотип [20, 24]. Этот эффект, вероятно, опосредован восстановлением митохондриального дыхания и снижением сигнала опасности DAMPs (damage-associated molecular patterns, молекулярные паттерны, ассоциированные с повреждением), поступающего от поврежденных митохондрий.
В совокупности активация каскадов AMPK-SIRT1-PGC-1α-NRF2 и нормализация воспалительных медиаторов формируют целостный адаптационный ответ, который можно рассматривать как биоэнергетическую перезагрузку. Таким образом, ЭСТ действует в режиме «мягкого клеточного стресса», усиливающего устойчивость, пластичность и метаболическую эффективность головного мозга (Рис. 4).
Энергетическая адаптация тесно сопряжена с микроциркуляцией и барьерной функцией; в связи с чем далее логично рассмотреть изменения нейроваскулярной единицы (VEGF/mTORC1, перициты, AQP4) как сосудисто-глиальный субстрат пластичности.
Нейроваскулярно-глиальные взаимодействия в механизмах действия электросудорожной терапии
В последние годы все больше данных указывает, что эффекты ЭСТ выходят за рамки чисто нейрональных процессов и включают активацию нейроваскулярной единицы (NVU – neurovascular unit) – функционального ансамбля, включающего нейроны, астроциты, перициты, эндотелиальные клетки и элементы базальной мембраны. ЭСТ можно рассматривать как системный модулятор нейро-глио-сосудистого обмена, влияющий на транспорт, микроциркуляцию и метаболическое сопряжение нейронов.
Одним из ключевых медиаторов этого эффекта является фактор роста эндотелия сосудов (VEGF). Его экспрессия усиливается после курса ЭСТ и коррелирует с пролиферацией нейральных предшественников и ангиогенезом в гиппокампе [45]. Параллельно активируется сигнальный путь mTORC1-VEGF, обеспечивающий синтез белков, необходимых для сосудистого ремоделирования [46]. Эти процессы создают основу для ангио- и нейрогенеза, способствуя структурной реабилитации гиппокампо-префронтальных контуров.
Однако данные последних лет расширяют понимание этого механизма, указывая на участие перицитов – клеток сосудистой стенки, регулирующих проницаемость гематоэнцефалического барьера (ГЭБ), тонус капилляров и трофическую поддержку эндотелия. Нарушения функции перицитов ассоциированы с депрессией, когнитивным дефицитом и микрососудистыми изменениями [47]. Предполагается, что ЭСТ, повышая VEGF-зависимую сигнализацию, способствует восстановлению перицитарной активности и целостности ГЭБ, что улучшает трофику и метаболический обмен между кровью и нервной тканью.
Особое место занимает астроцитарный компонент NVU. Исследования на животных моделях показали, что электроконвульсивная стимуляция повышает экспрессию аквапорина-4 (AQP4) и белков плотных контактов (claudin-5), а также восстанавливает покрытие капилляров астроцитарными ножками [48]. Эти эффекты ведут к нормализации глимфатического клиренса и регуляции ионного гомеостаза. Одновременно активируется астроцитарно-нейрональное метаболическое сопряжение (astrocyte–neuron lactate shuttle), при котором астроциты усиливают гликолиз и экспортируют лактат к нейронам в качестве субстрата для окислительного фосфорилирования [49]. Подобный энергетический обмен играет критическую роль в восстановлении нейрональной активности и синаптической пластичности после ЭСТ.
Таким образом, ЭСТ инициирует многоуровневую перестройку нейроваскулярно-глиального ансамбля: усиливает VEGF/mTOR-зависимый ангиогенез, стабилизирует ГЭБ и перицитарные связи, активирует астроцитарно-нейрональное сопряжение и оптимизирует локальную доставку метаболитов (Рис. 5). Эти процессы формируют благоприятные условия для нейропластического восстановления и устойчивой ремиссии депрессивного состояния.

Ограничением остается недостаток прямых нейровизуализационных подтверждений перицитарных и метаболических изменений у человека после ЭСТ. Тем не менее конвергенция данных молекулярных, морфологических и метаболических исследований позволяет рассматривать NVU как центральную мишень системного действия ЭСТ, объединяющую сосудистую, глиальную и энергетическую регуляцию головного мозга.
Однако нормализация микроциркуляции и барьеров снижает провоспалительный фон и модифицирует триптофановый метаболизм, что отражается на балансе кинурениновых метаболитов между нейротоксическим и нейропротективным звеньями.
Кинурениновый путь и нейроиммунно-метаболические механизмы действия ЭСТ
Кинурениновый путь является основным направлением катаболизма триптофана, конкурирующим с серотониновым каскадом и обеспечивающим до 95% его метаболизма. В норме этот путь сбалансирован между нейропротективным и нейротоксическим звеньями, представленными, соответственно, кинурениновой кислотой (KYNA) и хинолиновой кислотой (QUIN) [50].
Под действием провоспалительных цитокинов (IFN-γ, IL-6, TNF-α) активируется фермент индоламин-2,3-диоксигеназа (IDO), что увеличивает превращение триптофана в кинуренин и смещает метаболизм в сторону образования нейротоксичных производных – 3-гидроксикинуренина (3-HK) и QUIN. Эти метаболиты усиливают NMDA-зависимую нейротоксичность, оксидативный стресс и микроглиальную активацию, что связывают с патогенезом депрессии [51, 52].
Метаанализы последних лет подтвердили наличие дисбаланса кинуренинового пути при большой депрессии – снижения уровней KYN и KYNA при повышении QUIN и 3-HK [53]. Эти изменения коррелируют с выраженностью воспалительного статуса и тяжестью симптоматики.
Интерес представляют работы, в которых ЭСТ рассматривается как модератор кинуренинового метаболизма. В пилотном исследовании L. Schwieler и соавт. (2016) показано, что курс ЭСТ у пациентов с резистентной депрессией подавляет нейротоксическую ветвь кинуренинового пути, снижая концентрации QUIN и повышая KYNA [54]. Это сопровождалось клиническим улучшением и снижением уровня воспалительных маркеров.
Результаты молекулярного анализа K. Ryan и соавт. (2025) продемонстрировали, что ЭСТ может модулировать экспрессию генов ферментов KP – IDO1, KMO и KYAT – в периферических мононуклеарах крови, что подтверждает системный характер этого эффекта [55]. Авторы предполагают, что восстановление баланса между IDO-зависимой и KAT-зависимой активностью является одним из звеньев антидепрессивного действия ЭСТ.
С учетом того, что конечные продукты кинуренинового пути вовлечены в синтез NAD+ (через QUIN), воздействие ЭСТ на этот путь может быть связано и с улучшением митохондриального метаболизма. Таким образом, кинурениновая система выступает как интегративное звено между воспалением, энергетическим обменом и нейропластичностью, а ее нормализация после ЭСТ отражает переход от воспалительно-токсического к адаптивно-пластическому фенотипу (Рис. 6).
Несмотря на обнадеживающие результаты, доказательная база остается ограниченной: большинство исследований проведено на периферических образцах, а динамика метаболитов в ЦНС не изучена. Перспективным направлением является мультиомный анализ метаболомов, транскриптомов и маркеров воспаления до и после ЭСТ, что позволит уточнить роль кинуренинового пути как биомаркера ответа на терапию.
Ось «кишечник–мозг» в системных эффектах электросудорожной терапии
Так как сдвиги кинуренинового каскада связаны с системным воспалением и доступностью триптофана, следующий рассматриваемый уровень – двунаправленная регуляция со стороны кишечного микробиома и барьерной функции ЖКТ.
Ось «кишечник–мозг» (gut-brain axis) представляет собой сложную двунаправленную систему взаимодействия между ЦНС, эндокринной, иммунной и энтеральной нервной системами [56, 57]. Ключевым элементом этого взаимодействия выступает микробиота кишечника, продуцирующая широкий спектр биологически активных соединений – короткоцепочечные жирные кислоты, нейротрансмиттеры, индольные метаболиты триптофана и цитокины, – влияющие на состояние ГЭБ, микроглии и стресс-оси ГГН [58].
 Накопленные данные указывают, что при депрессии и хроническом стрессе наблюдается дисбиоз кишечного микробиома – снижение доли Lactobacillus и Bifidobacterium, рост условно-патогенных таксонов (Clostridium, Ruminococcus, Alistipes), повышение проницаемости кишечного барьера и увеличение уровней липополисахаридов (LPS) в крови [59, 60]. Эти изменения сопровождаются активацией провоспалительных каскадов, повышением концентрации IL-6 и TNF-α, активацией индоламин-2,3-диоксигеназы (IDO) и усилением кинуренинового обмена, что связывает микробиоту с нейроиммунной дисрегуляцией и формированием депрессивного фенотипа [61].
Накопленные данные указывают, что при депрессии и хроническом стрессе наблюдается дисбиоз кишечного микробиома – снижение доли Lactobacillus и Bifidobacterium, рост условно-патогенных таксонов (Clostridium, Ruminococcus, Alistipes), повышение проницаемости кишечного барьера и увеличение уровней липополисахаридов (LPS) в крови [59, 60]. Эти изменения сопровождаются активацией провоспалительных каскадов, повышением концентрации IL-6 и TNF-α, активацией индоламин-2,3-диоксигеназы (IDO) и усилением кинуренинового обмена, что связывает микробиоту с нейроиммунной дисрегуляцией и формированием депрессивного фенотипа [61].ЭСТ может опосредованно воздействовать на микробиоту через нормализацию нейровегетативных и нейроэндокринных контуров, улучшая барьерную функцию кишечника и снижая уровень системного воспаления. Восстановление симбиотического микробного профиля может, в свою очередь, способствовать снижению продукции LPS, модуляции цитокинового ответа и нормализации триптофанового метаболизма (Рис. 7).
Таким образом, ось «кишечник–мозг» может рассматриваться как одно из системных звеньев биологического ответа на ЭСТ. Нейровегетативная активация, горметическое воспалительное торможение и улучшение барьерной функции кишечника формируют условия для стабилизации нейроиммунного гомеостаза. Перспективными направлениями исследований являются метагеномные и метаболомные анализы до и после курса ЭСТ, а также изучение взаимосвязи изменений микробиоты с динамикой цитокинов и метаболитов кинуренинового пути.
 Сигнальный путь Wnt/β-катенина
Сигнальный путь Wnt/β-катенина и нейропластические механизмы действия электросудорожной терапии
Через эндокринно-иммунные и метаболические сигналы ось «кишечник–мозг» опосредованно влияет на внутримозговые каскады нейропластичности; на этом фоне уместно рассмотреть роль Wnt/β-катенина как интегратора пластических программ.
Сигнальный путь Wnt/β-катенина является универсальным регулятором эмбрионального развития, нейрогенеза и синаптической пластичности, а также одним из ключевых каскадов, участвующих в поддержании структурной и функциональной целостности нервной ткани [62, 63].
В зрелом головном мозге активация Wnt-передачи обеспечивает выживаемость нейронов, стимулирует экспрессию BDNF и VEGF, способствует дендритогенезу и синаптическому ремоделированию [64].
При депрессии отмечается ингибиция Wnt-сигналинга и гиперактивация GSK-3β (glycogen synthase kinase-3β) – фермента, фосфорилирующего β-катенин и способствующего его деградации в протеасомах. Это приводит к снижению транскрипции генов, регулируемых β-катенином, и к ослаблению нейропластических процессов [65, 66].
Исследования на животных моделях показали, что электроконвульсивная стимуляция (аналог ЭСТ) активирует Wnt/β-катениновый путь в гиппокампе и префронтальной коре. В работе H. Okamoto и соавт. (2010) продемонстрировано, что после серии стимуляций повышается экспрессия β-катенина, а также фосфорилирование GSK-3β по Ser9 – маркер ее инактивации [62].
На молекулярном уровне ЭСТ, вероятно, инициирует фосфорилирование GSK-3β и стабилизацию β-катенина, что активирует транскрипцию пластичностных генов через TCF/LEF-комплексы. Эти изменения ведут к восстановлению синаптической архитектуры, аксонального роста и нейротрофического потенциала.
Интересно, что активация Wnt/β-катениновой передачи тесно взаимодействует с митохондриальными и эпигенетическими механизмами, ранее описанными при ЭСТ. β-катенин регулирует экспрессию антиоксидантных ферментов, участвует в контроле митохондриальной биогенезы (через взаимодействие с PGC-1α) и может быть мишенью для NAD+/SIRT1-зависимой деацетилации [67]. Эти перекрестные связи делают Wnt/β-катениновый путь интегративным центром клеточной адаптации при действии ЭСТ.
Таким образом, можно рассматривать ЭСТ как нейротрофическое и нейропластическое вмешательство, частично реализующее свои эффекты через активацию Wnt/β-катенинового каскада. Этот путь объединяет энергетические, эпигенетические и синаптические компоненты клеточного ответа, формируя основу для долговременного восстановления нейросетевой архитектуры и эмоционально-когнитивного гомеостаза.
 Интегративная многоуровневая модель биологических эффектов электросудорожной терапии
Интегративная многоуровневая модель биологических эффектов электросудорожной терапииСовременное понимание ЭСТ выходит за пределы нейротрансмиттерных и эндокринных моделей. На основании накопленных данных ее можно рассматривать как координированное многоуровневое вмешательство, в котором электрический стимул запускает серию взаимосвязанных процессов – от молекулярных и клеточных до системных и нейросетевых.
На молекулярном уровне эффект реализуется через эпигенетические перестройки: изменения метилирования ДНК, активности miRNA и lncRNA, что переопределяет экспрессию генов, связанных со стресс-ответом, пластичностью и энергетическим метаболизмом.
Клеточные и метаболические реакции включают активацию митохондриального стресс-ответа, усиление биогенеза, антиоксидантную защиту и восстановление NAD+-зависимых путей. Эти процессы обеспечивают энергетическую устойчивость нейронов и снижают воспалительный фон.
На уровне микроокружения мозга активируются глимфатические и нейроваскулярно-глиальные механизмы: оптимизируется ликворо-интерстициальный обмен, усиливается ангиогенез и астроцитарно-нейрональное сопряжение, что улучшает трофику и барьерные функции.
Иммунометаболическое звено проявляется нормализацией кинуренинового пути, снижением продукции нейротоксичных метаболитов и смещением иммунного профиля в сторону противовоспалительного фенотипа.
На висцерально-системном уровне происходят адаптивные изменения в оси «кишечник–мозг»: стабилизация микробиоты, улучшение барьерной функции кишечника и снижение системного воспаления, что поддерживает центральные процессы нейропластичности.
Завершающий контур модели связан с активацией сигнального пути Wnt/β-катенина, регулирующего синаптогенез, дендритогенез и экспрессию BDNF и VEGF. Именно этот каскад обеспечивает долговременную перестройку нейрональных сетей и интеграцию молекулярных и системных уровней ответа.
В совокупности эти процессы формируют единый феномен нейробиологического ремоделирования – переход головного мозга в новое состояние функциональной и энергетической целостности, при котором восстановление сетевых связей сочетается с биохимической и структурной стабилизацией нейроткани (Рис. 9).
Разумеется, предложенная автором модель – это не «новая аксиома нейронаук», а лишь попытка собрать воедино современные литературные данные и увидеть в них общую логику. Это гипотетическая, теоретическая конструкция, призванная помочь осмыслить феномен ЭСТ как системный биологический процесс, а не эмпирическую процедуру. Впрочем, если в ней окажется доля истины – пусть ею займутся уже будущие поколения нейробиологов.
Заключение
ЭСТ – не просто исторически сложившийся метод лечения депрессии, а точная нейромодуляционная технология, использующая потенциал контролируемого клеточного стресса. Кратковременная электрическая стимуляция активирует каскады адаптации и восстановления, приводя к нормализации энергетического обмена, снижению воспаления и перестройке нейросетевой динамики.
Эта способность запускать скоординированный стресс-ответ позволяет рассматривать ЭСТ как биологический триггер пластичности, восстанавливающий нарушенные связи между молекулярными, сосудистыми и нейрональными системами.
Будущее метода – в его персонализации. Использование объективных биомаркеров (метилирование FKBP5, экспрессия BDNF и VEGF, параметры NAD+/NADH, показатели связности DMN-CEN-SN) позволит подбирать оптимальные параметры стимуляции и прогнозировать терапевтический ответ.
Интеграция мультиомных, нейровизуализационных и физиологических подходов откроет путь к новой модели – точной нейромодуляционной психиатрии, в которой ЭСТ станет инструментом системного восстановления нейробиологического гомеостаза и индивидуальной нейропластической резилентности.
Информация об авторах
Быков Юрий Витальевич, к.м.н., доцент кафедры анестезиологии и реаниматологии с курсом ДПО, Ставропольский государственный медицинский университет
ORCID: 0000-0003-4705-3823. E-mail:
Беккер Роман Александрович, независимый исследователь в области психофармакотерапии, Израиль
ORCID: 0000-0002-0773-3405. E-mail:
Дата поступления: 21.11.2025
Received: 21.11.2025
Принята к печати: 06.02.2026
Accepted: 06.02.2026
Автор заявляет об отсутствии конфликта интересов.
Author declares no conflicts of interest
Список исп. литературыСкрыть список1. Kritzer MD, Peterchev AV, Camprodon JA. Electroconvulsive Therapy: Mechanisms of Action, Clinical Considerations, and Future Directions. Harv Rev Psychiatry. 2023;31(3):101-113. doi: 10.1097/HRP.0000000000000365.
2. Smolarczyk J, Piłat P, Blanch J et al. Electroconvulsive Therapy and Hyperventilation: A Narrative Review. Life (Basel). 2025;15(9):1368. doi: 10.3390/life15091368.
3. Быков Ю.В., Беккер Р.А., Резников М.К. Депрессия и резистентность. Москва: Риор: инфра-М., 2013;374.
4. Быков Ю.В., Беккер Р.А. Минимизация когнитивных нарушений при электросудорожной терапии: реалии и перспективы (обзор литературы с комментариями и рекомендациями) (I часть: теоретическая). В мире научных открытий. 2016;(82):54-92.
5. Быков Ю.В., Беккер Р.А. Минимизация когнитивных нарушений при электросудорожной терапии: реалии и перспективы (Обзор литературы с комментариями и рекомендациями) (II часть: практическая). В мире научных открытий. 2016;12(84):200-272.
6. UK ECT Review Group. Efficacy and safety of electroconvulsive therapy in depressive disorders: a systematic review and meta-analysis. Lancet. 2003;361(9360):799-808. doi: 10.1016/S0140-6736(03)12705-5.
7. Нельсон А.И. Электросудорожная терапия в психиатрии, наркологии и неврологии. Москва БИНОМ. Лаборатория знаний. 2005;368.
8. Быков Ю.В. Электросудорожная терапия в практике анестезиолога. Издательство РИОР, 2013;220.
9. Endler NS. The origins of electroconvulsive therapy (ECT). Convuls Ther. 1988;4(1):5-23.
10. Fink M. Convulsive therapy: a review of the first 55 years. J Affect Disord. 2001;63(1-3):1-15. doi: 10.1016/S0165-0327(00)00352-8.
11. Sackeim HA. Modern electroconvulsive therapy: vast improvements yet still controversial. Nat Rev Neurol. 2017;13(1):47-58. doi: 10.1038/nrneurol.2016.164.
12. Rodek P, Mędrala W, Chrobak J et al. Around anesthesia: anesthetic aspects of electroconvulsive treatment in the light of the latest reports - review article. Psychiatr Pol. 2025;59(2):299-309. doi: 10.12740/PP/OnlineFirst/174768.
13. Grover S, Chakrabarti S, Mehta UM et al. Clinical Practice Guidelines for Electroconvulsive Therapy. Indian J Psychiatry. 2021;63(Suppl 2):S285-S307. doi: 10.4103/0019-5545.333471.
14. Kho KH, van Vreeswijk MF, Simpson S, Zwinderman AH. A meta-analysis of electroconvulsive therapy efficacy in depression. J ECT. 2003;19(3):139-147. doi: 10.1097/00124509-200309000-00001.
15. Jelovac A, Kolshus E, McLoughlin DM. Relapse following successful electroconvulsive therapy for major depression: a meta-analysis. Neuropsychopharmacology. 2013;38(12):2467-2474. doi: 10.1038/npp.2013.149.
16. Micallef-Trigona B. ECT for neuropsychiatric disorders other than depression: a review. J ECT. 2014;30(4):263-271. doi: 10.1097/YCT. 0000000000000134.
17. Loo CK, Schweitzer I, Pratt C et al. A comparison of RUL ultrabrief pulse (0.3 ms) ECT and standard RUL ECT. Int J Neuropsychopharmacol. 2008;11(7):883-890. doi: 10.1017/S1461145708009035.
18. Stojanović Z, Simić K, Tepšić Ostojić V, Gojković Z, Petković-Ćurčin A. Electroconvulsive therapy in the Fourth Industrial Revolution (Review). Biomed Rep. 2024;21(3):129. doi: 10.3892/br.2024.1817.
19. Cano M, Wainwright SR, Kerr JM et al. Understanding the mechanisms of action of electroconvulsive therapy: revisiting neuroinflammatory and neuroplasticity hypotheses. JAMA Psychiatry. 2023;80(5):467-479. doi: 10.1001/jamapsychiatry.2023.0001.
20. Rojas M, Barrera R, Peña F et al. Electroconvulsive Therapy in Psychiatric Disorders: Neurobiological, Endocrine, and Immune Mechanisms. Int J Mol Sci. 2022;23(13):6918. doi: 10.3390/ijms23136918.
21. Pirnia T, Joshi SH, Leaver AM et al. Electroconvulsive therapy and structural neuroplasticity in depressive disorders. Transl Psychiatry. 2016;6(9):e832. doi: 10.1038/tp.2016.103.
22. Abbott CC, Jones T, Lemke NT et al. Hippocampal structural and functional changes associated with electroconvulsive therapy response. Transl Psychiatry. 2014;4(11):e483. doi: 10.1038/tp.2014.123.
23. Yrondi A, Sporer M, Péran P, Schmitt L, Arbus C, Sauvaget A. Electroconvulsive therapy, depression, the immune system and inflammation: a systematic review. Brain Stimul. 2018;11(1):29-51. doi: 10.1016/j.brs.2017.10.013.
24. João RB, Daltro-Oliveira R, Oliveira LRM et al. Immune-inflammatory, neuroplastic, and epigenetic effects of electroconvulsive therapy in mood disorders. Front Psychiatry. 2025;16:1577530. doi: 10.3389/fpsyt.2025. 1577530.
25. Moschny N, Zindler T, Jahn K et al. Novel candidate genes for ECT response prediction – a pilot study analyzing the DNA methylome of depressed patients receiving electroconvulsive therapy. Clin Epigenetics. 2020;12:114. doi: 10.1186/s13148-020-00891-9.
26. Sirignano L, Gensous N, Lis A et al. Methylome-wide change associated with response to electroconvulsive therapy in depressed patients. Transl Psychiatry. 2021;11(1):547. doi: 10.1038/s41398-021-01474-9.
27. Castro SCC, Bicca C, Bicca B, Araujo S, Viola TW. A systematic mini-review of epigenetic mechanisms associated with electroconvulsive therapy in humans. Front Hum Neurosci. 2023;17:1143332. doi: 10.3389/fnhum.2023.1143332.
28. Chuang JC, Jones PA. Epigenetics and microRNAs. Pediatr Res. 2007;61(1):24-29. doi: 10.1203/pdr.0b013e3180457684.
29. Arif KMT, Elliott EK, Haupt LM, Griffiths LR. Regulatory mechanisms of epigenetic microRNAs: Effect of environmental factors. Cancers (Basel). 2020;12(10):2922. doi: 10.3390/cancers12102922.
30. Prabhakaran R, Gohil V, Patel S et al. Epigenetic frontiers: miRNAs, long non-coding RNAs and nanomaterials. Epigenetics Chromatin. 2024;17:31. doi: 10.1186/s13072-024-00554-6.
31. Kouzarides T. Chromatin modifications and their function. Cell. 2007;128(4):693-705. doi: 10.1016/j.cell.2007.02.005.
32. Gbyl K, Labanauskas V, Lundsgaard CC et al. Electroconvulsive therapy disrupts functional connectivity between hippocampus and posterior default mode network. Prog Neuropsychopharmacol Biol Psychiatry. 2024;132:110981. doi: 10.1016/j.pnpbp.2024.110981.
33. Guo Y, Wang Y, Chen X et al. Electroconvulsive therapy regulates brain connectome dynamics in major depressive disorder. Biol Psychiatry. 2024;95(12):1112-1123. doi: 10.1016/j.biopsych.2024.03.012.
34. Verdijk JPAJ, Dols A, Stek ML et al. Longitudinal resting-state network connectivity changes in ECT: a multicenter study. Brain Stimul. 2024;17(3):531-542. doi: 10.1016/j.brs.2024.05.001.
35. Dini H, Khazaie H, Sadeghi Bahmani D et al. Dynamic functional connectivity predicts treatment response in depression: a resting-state fMRI study of CCN/DMN. Front Hum Neurosci. 2021;15:689488. doi: 10.3389/fnhum.2021.689488.
36. Pang Y, Wei Q, Zhao S et al. Enhanced default mode network functional connectivity links with electroconvulsive therapy response in major depressive disorder. J Affect Disord. 2022;306:47-55. doi: 10.1016/j.jad.2022.02.013.
37. Moreno-Ortega M, Prudic J, Rowny S et al. Resting state functional connectivity predictors of treatment response to electroconvulsive therapy in depression. Sci Rep. 2019;9:5071. doi: 10.1038/s41598-019-41175-4.
38. Sun S, Yu H, Zhao X et al. Electroconvulsive therapy-induced changes in functional connectivity: a pilot resting-state fMRI study. Front Hum Neurosci. 2022;16:852657. doi: 10.3389/fnhum.2022.852657.
39. Perrin JS, Merz S, Bennett DM et al. Electroconvulsive therapy reduces frontal cortical connectivity in severe depression. Proc Natl Acad Sci U S A. 2012;109(14):5464-5468. doi: 10.1073/pnas.1117206109.
40. Hablitz LM, Nedergaard M. The glymphatic system: a novel component of fundamental neurobiology. J Neurosci. 2021;41(37):7698-7711. doi: 10.1523/JNEUROSCI.0619-21.2021.
41. Mogensen FLH, Hedelund-Mathiasen F, Delle C et al. The glymphatic system (en)during inflammation. Int J Mol Sci. 2021;22(14):7491. doi: 10.3390/ijms22147491.
42. Mindt S, Hellmann-Regen J, Steinacker P et al. Brain-derived neurotrophic factor in the cerebrospinal fluid during electroconvulsive therapy. J ECT. 2020;36(3):187-194. doi: 10.1097/YCT.0000000000000667.
43. Scarpulla RC. Metabolic control of mitochondrial biogenesis through the PGC-1 family regulatory network. Biochim Biophys Acta. 2011;1813(7): 1269-1278. doi: 10.1016/j.bbamcr.2010.09.019.
44. Goldfarb S, Eldar-Finkelman H, Gluck N et al. Electroconvulsive stimulation attenuates chronic neuroinflammation by reducing microglial neurotoxicity and oxidative stress. JCI Insight. 2020;5:e137028. doi: 10.1172/jci.insight.137028.
45. Segi-Nishida E, Warner-Schmidt JL, Duman RS. Electroconvulsive seizure and VEGF increase the proliferation of neural stem-like cells in rat hippocampus. Proc Natl Acad Sci U S A. 2008;105(32):11352-11357. doi: 10.1073/pnas.0710858105.
46. Elfving B, Wegener G. Electroconvulsive seizures stimulate the VEGF pathway via mTORC1. Synapse. 2012;66(4):340-345. doi: 10.1002/syn.21518.
47. Sweeney MD, Zhao Z, Montagne A et al. Blood–brain barrier: from physiology to disease and back. Physiol Rev. 2019;99(1):21-78. doi: 10.1152/physrev.00050.2017.
48. Azis AI, Horiguchi J, Minagaki T et al. Electroconvulsive shock restores the decreased coverage of brain blood vessels by astrocytic endfeet and ameliorates depressive-like behavior in rats. J Affect Disord. 2019;257:331-339. doi: 10.1016/j.jad.2019.07.008.
49. Magistretti PJ, Allaman I. Lactate in the brain: from metabolic end-product to signalling molecule. Nat Rev Neurosci. 2018;19(4):235-249. doi: 10.1038/nrn.2018.19.
50. Savitz J. The kynurenine pathway: a finger in every pie. Mol Psychiatry. 2020;25(1):131-147. doi: 10.1038/s41380-019-0414-4.
51. Maddison DC, Giorgini F. The kynurenine pathway and neurodegenerative disease. Semin Cell Dev Biol. 2020;99:97-106. doi: 10.1016/j.semcdb.2019.05.017.
52. Almulla AF, Maes M. The tryptophan catabolite or kynurenine pathway in major depressive and bipolar disorder: a systematic review and meta-analysis. Prog Neuropsychopharmacol Biol Psychiatry. 2022;127:110219. doi: 10.1016/j.pnpbp.2020.110219.
53. Marx W, Lane M, Gershon S et al. The kynurenine pathway in major depressive disorder, bipolar disorder and schizophrenia: a meta-analysis of 101 studies. Mol Psychiatry. 2021;26(8):4158-4178. doi: 10.1038/s41380-021-01055-2.
54. Schwieler L, Samuelsson M, Frye MA et al. Electroconvulsive therapy suppresses the neurotoxic branch of the kynurenine pathway in treatment-resistant depressed patients. J Neuroinflammation. 2016;13:51. doi: 10.1186/s12974-016-0510-4.
55. Ryan KM, Mathiassen A, Videbech P et al. Gene expression of kynurenine pathway enzymes in depression and following electroconvulsive therapy. Acta Neuropsychiatr. 2025;37(2):97-108. doi: 10.1017/neu.2025.3.
56. Cryan JF, O’Riordan KJ, Cowan CSM et al. The microbiota–gut–brain axis. Physiol Rev. 2019;99(4):1877-2013. doi: 10.1152/physrev.00018.2018.
57. Sharon G, Sampson TR, Geschwind DH, Mazmanian SK. The central nervous system and the gut microbiome. Cell. 2019;176(6):1232-1245. doi: 10.1016/j.cell.2019.02.044.
58. Dinan TG, Cryan JF. The microbiome–gut–brain axis in health and disease. Gastroenterol Clin North Am. 2017;46(1):77-89. doi: 10.1016/j.gtc.2016. 09.007.
59. Kelly JR, Borre Y, O’Brien C et al. Transferring the blues: depression-associated gut microbiota induces neurobehavioural changes in the rat. J Psychiatr Res. 2016;82:109-118. doi: 10.1016/j.jpsychires.2016.07.019.
60. Jiang H, Ling Z, Zhang Y et al. Altered fecal microbiota composition in patients with major depressive disorder. Brain Behav Immun. 2015;48:186-194. doi: 10.1016/j.bbi.2015.03.016.
61. Mayer EA, Tillisch K, Gupta A. Gut/brain axis and the microbiota. J Clin Invest. 2015;125(3):926-938. doi: 10.1172/JCI76304.
62. Okamoto H, Voleti B, Banasr M et al. Wnt2 expression and signaling is increased by different classes of antidepressant treatments. Biol Psychiatry. 2010;68(6):521-527. doi: 10.1016/j.biopsych.2010.05.013.
63. Inestrosa NC, Arenas E. Emerging roles of Wnts in the adult nervous system. Nat Rev Neurosci. 2010;11(2):77-86. doi: 10.1038/nrn2755.
64. Mao Y, Ge X, Frank CL et al. Disrupted in schizophrenia 1 regulates neuronal progenitor proliferation via modulation of GSK3β/β-catenin signaling. Cell. 2019;136(6):1017-1031. doi: 10.1016/j.cell.2019.02.041.
65. O’Brien WT, Harper AD, Jové F et al. Glycogen synthase kinase-3β haploinsufficiency mimics the behavioral and molecular effects of lithium. J Neurosci. 2004;24(30):6791-6798. doi: 10.1523/JNEUROSCI.1362-04.2004.
66. Li X, Zhu W, Roh MS et al. In vivo regulation of glycogen synthase kinase-3β (GSK3β) by serotonergic activity in mouse brain. Neuropsychopharmacology. 2010;35(5):1076-1087. doi: 10.1038/npp.2009.211.
67. Toledo EM, Colombres M, Inestrosa NC. Wnt signaling in neuroprotection and stem cell differentiation. Prog Neurobiol. 2020;196:101939. doi: 10.1016/j.pneurobio.2020.101939.
3 марта 2026
Количество просмотров: 57

