Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№03 2009
Когнитивные и психотропные эффекты препарата Кортексин при лечении больных эпилепсией №03 2009
Введение
Эпилепсия, являясь хроническим неврологическим заболеванием, приводит к развитию определенных психических нарушений, среди которых в первую очередь следует отметить мнестико-интеллектуальное снижение и широкую гамму психических расстройств пограничного уровня. Аффективная симптоматика в форме депрессий встречается наиболее часто, хотя в клинических условиях эти состояния своевременно не распознаются, что объясняется размытостью клинических и психопатологических проявлений этих расстройств у больных эпилепсией. При этом все многообразие аффективной симптоматики (преимущественно депрессивной) подразделяют на несколько подтипов в зависимости от времени появления депрессии по отношению к приступу. В соответствии с этим выделяют преиктальные, иктальные, постиктальные и интериктальные депрессии, среди которых наибольшее значение имеют последние. Картина депрессий при эпилепсии характеризуется отчетливой сопряженностью как с тревожной, так и дисфорической симптоматикой. Это часто затрудняет отнесение аффективных и тревожных расстройств к определенным диагностическим категориям, представленным в Международной классификации болезней 10-го пересмотра (МКБ-10). В соответствии с МКБ-10 в качестве самостоятельных диагностических категорий выделяют органическое аффективное расстройство и органическое тревожное расстройство, тогда как диагноза дисфорическое расстройство≫ в данной классификационной системе не существует. Мнестико-интеллектуальный дефект имеет не меньшее значение, поскольку именно в результате его развития у больных эпилепсией нарушается социальная адаптация, что заставляет переводить их на инвалидность. Дефект при этом часто сопряжен с личностными изменениями в виде вязкости, тугоподвижности мышления, брутальности, инертности аффектов, обстоятельности. Совокупность этих признаков ранее рассматривалась как атрибут эпилептической болезни и включалась психиатрами в диагностический алгоритм эпилепсии наряду с припадками. Более того, после Morel в психиатрии длительное время существовал термин epilepsia larvata, т.е. скрытая эпилепсия, когда при отсутствии припадков устанавливался диагноз эпилепсии на основании отмеченных признаков. В последние годы появились указания на то, что аффективная патология и когнитивные нарушения при эпилепсии часто связаны друг с другом, и это позволяет предположить общий патогенез, лежащий в основе столь разных на первый взгляд расстройств. В частности, подчеркивается, что обе эти группы расстройств могут иметь нарушения функций лобных долей, что получило в нейропсихологической литературе название гипофронтальности [1]. Исходя из сказанного, ясно, что устранение (снижение) клинических проявлений, как аффективных расстройств, так и когнитивных нарушений, при эпилепсии представляет актуальную задачу, что будет a priori способствоватьсохранению адаптации больных эпилепсией в обществе и повышению их качества жизни.
Общие критерии диагностики органических нарушений согласно МКБ-10 включают ряд признаков:
• наличие церебрального или соматического заболевания, которое может вызывать указанные расстройства;
• отчетливая связь во времени (от нескольких недель до нескольких месяцев) между развитием мозгового заболевания и психическими нарушениями;
• улучшение психического состояния после улучшения основного мозгового заболевания;
• отсутствие указаний на другие причины, в частности на наследственную отягощенность психическими заболеваниями, что могло бы объяснить их происхождение.
Следует отметить, что критерии отграничения отдельных категорий органических заболеваний головного мозга со временем подвергаются пересмотру, что привносит определенные трудности в процесс их диагностики и распознавания. Примером изменений в подходах к диагностике подобных состояний являются новые критерии диагностики деменции. При этом унифицированные диагностические критерии для деменции не разработаны, а предложенные МКБ-10 критерии противоречат традиционным представлениям классической психопатологии [2]. Деменция согласно МКБ-10 не является исключительно хроническим и необратимым процессом, поражающим интеллект и, напротив, может носить как острое, так и хроническое прогредиентное течение, иметь как обратимый, так и необратимый характер [2]. Из сказанного следует, что четкой демаркационной линии между деменцией и психоорганическим синдромом провести не представляется возможным и различия между ними носят скорее количественный, а не качественный характер. В свою очередь это может в значительной мере повлиять на результативность терапии ноотропными препаратами больных с органическими заболеваниями головного мозга. Понятно, что при расширении диагностических критериев деменции за счет включения в них случаев психоорганического синдрома можно ожидать более высокой эффективности препаратов и, напротив, при ужесточении диагностических критериев эффективность терапии будет менее высокой. Из этого следует, что оценка эффективности того или иного ноотропного препарата должна проводиться по строгим критериям эффективности в условиях контроля с применением плацебо, что не всегда возможно в клинических условиях.
Отечественный препарат Кортексин, выпускаемый компанией Герофарм, представляет собой комплекс низкомолекулярных белков, выделенных из коры головного мозга крупного рогатого скота [3, 4]. В отдельных исследованиях установлено, что Кортексин обладает ноотропным эффектом, оказывая благотворное влияние на показатели памяти, внимания, мышления, работоспособности, эмоциональное состояние, а также способен стимулировать процессы нейропластичности в нервной системе. Более того, его применение способствует нормализации обменных процессов нейромедиаторов. Препарат обладает несомненной антиоксидантной активностью, что снижает процессы перекисного окисления и уровень свободных радикалов [3, 4]. Сказанное позволяет предположить, что препарат должен оказывать позитивное влияние на когнитивные функции и аффективную сферу у больных эпилепсией, хотя специальных исследований в этом аспекте выполнено не было. Настоящее исследование проведено с целью изучения когнитивных и психотропных эффектов кортексина у больных эпилепсией. Наряду с этим поставлена задача по изучению влияния кортексина и на частоту припадков, поскольку учащение их может служить препятствием для его назначения лицам, страдающим эпилепсией.
Материалы и методы
В исследовании участвовали 78 больных (23 мужчины и 55 женщин) парциальной эпилепсией. Вся выборка из 78 человек в случайном порядке была разделена на 2 подгруппы: основную, получавших инъекции Кортексина (42 человека; 12 мужчин и 30 женщин) и контрольную – плацебо (36 человек; 11 мужчин и 25 женщин). Возраст больных в основной группе в среднем составлял 32,0Ѓ}11 лет (от 20 до 68 лет), в контроле – 31,0Ѓ}9,5 года (от 18 до 53 лет). Возраст дебюта заболевания эпилепсией в сравниваемых группах составлял 16,0Ѓ}7,6 и 17,0Ѓ}10,1 года соответственно. В основной группе диагноз симптоматическая эпилепсия установлен у 11 человек, диагноз криптогенная эпилепсия – у 31 больного. В контрольной группе симптоматическая эпилепсия диагностирована у 1 человека, криптогенная – у 35 человек. Все больные как основной, так и контрольной группы получали базисную терапию антиэпилептическими препаратами. Наряду с антиэпилептическими препаратами больные основной группы на протяжении 10 дней внутримышечно получали Кортексин в суточной дозе 10 мг, а больные контрольной группы препарат мильгамма в виде ежедневных внутримышечных инъекций в дозе 2,0 мл. Психический статус и состояние когнитивных функций узучали с помощью батареи формализованных шкал. Для оценки психопатологической симптоматики применялась шкала SCL-90 [5, 6]. Данная шкала заполняется самим больным. Это позволяет избежать субъективного искажения психопатологических показателей со стороны врача. В результате заполнения формируются 9 симптомокомплексов, отражающих разные психопатологические составляющие психического статуса больных. Они включают соматизацию, депрессию, тревогу, трудности межличностных контактов, фобическую тревогу, обсессивно-компульсивные переживания, враждебность, параноидные идеи и психотическую симптоматику. Наряду с этим применялась шкала Zung [7] для оценки выраженности соответствующей депрессивной симптоматики, а также госпитальная шкала тревоги и депрессии (HADS) у изучаемого контингента больных [8]. Для определения состояния исполнительских функций применялась шкала поведенческих функций (Executive Functions Behavioral Rating Scale), разработанная Sohlberg и Mateer (цитируется по H.Masur [9]), которая оценивает выраженность исполнительских функций в баллах. При нормальном уровне этих функций суммарная оценка состояния составляет не менее 85 баллов, тогда как более низкая величина указывает на снижение исполнительских способностей. Выраженность речевой беглости оценивали с помощью Thurstone’s Word Fluency Test (цитируется по A.Damasio и соавт. [10]). Суть данного теста сводится к подсчету воспроизведенных больным слов определенной категории в заданный интервал времени. Состояние памяти определяли с помощью Опросника памяти на повседневные события (Everyday Memory Questionnaire) [9, 11]. Наряду с этим исследовали частоту и тип эпилептических припадков. Эти показатели фиксировали до и в процессе терапии Кортексином (через 20, 40 и 90 дней с момента начала его применения). Применяли методы статистического анализа (программа Statistica 8). Для оценки возможных сдвигов в неврологических, когнитивных и психопатологических показателях использовали t-тест для зависимых и независимых переменных. Для анализа структуры психопатологической симптоматики до и во время терапии, а также для оценки ее динамики применялся факторный анализ (метод главных компонент).
Основные результаты исследования представлены в таблицах, основной (табл. 1) и контрольной (табл. 2) группах больных.
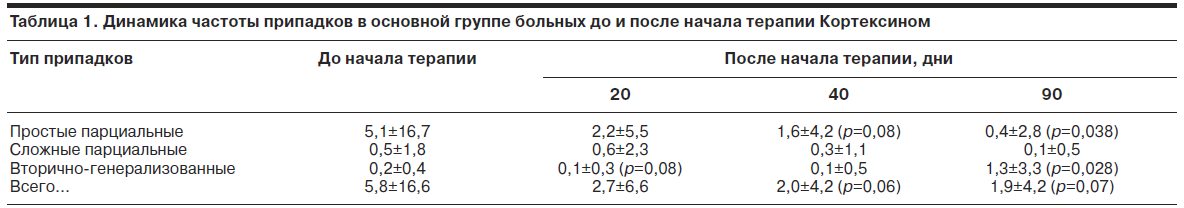
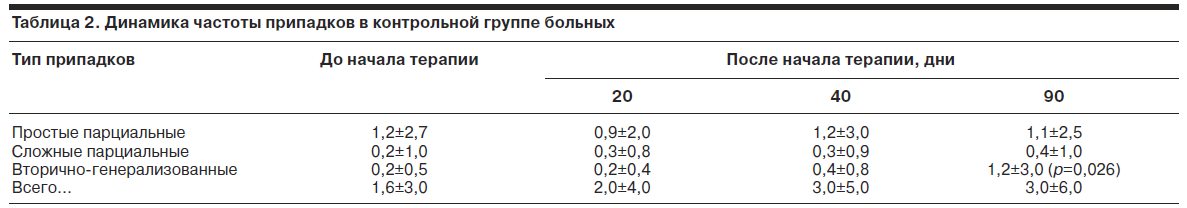
В процессе терапии Кортексином наблюдалась тенденция к редукции общего числа припадков, а также частоты простых парциальных, сложных парциальных и вторично-генерализованных припадков начиная с 20-го дня после начала курса терапии. К 90-му дню с момента начала терапии редукция простых парциальных припадков достигла статистически значимого уровня, тогда как частота вторично-генерализованных припадков к этому времени несколько увеличилась по сравнению с первоначальным фоном. Существенно, что в контрольной группе не отмечалось выраженной тенденции к снижению частоты приступов и наблюдалось возрастание частоты вторично-генерализованных приступов. Это не позволяет объяснить увеличение частоты приступов в основной группе исключительно влиянием Кортексина. В табл. 3 и 4 приведены данные по динамике нейропсихологических и некоторых психометрических показателей.
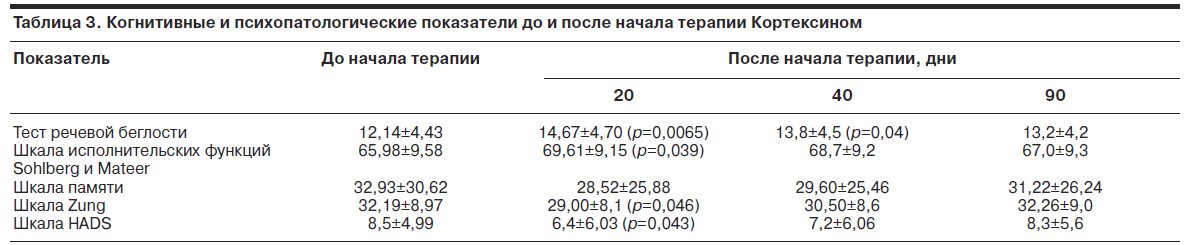
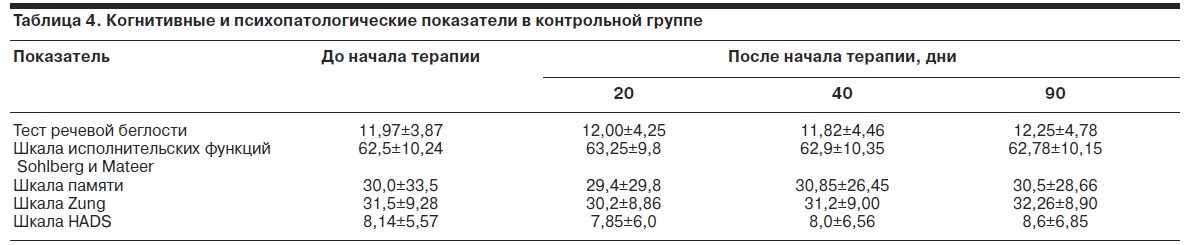
Следует подчеркнуть, что обе группы изначально не имели статистически значимых различий ни по одному из изучаемых показателей. Под влиянием Кортексина происходило повышение показателя теста речевой беглости на 20-й и 40-й день терапии и улучшение показателей исполнительских функций по шкале Sohlberg и Mateer на 20-й день после начала лечения. Наряду с этим отмечалось статистически значимое снижение выраженности депрессии по шкале Zung и тревоги по шкале HADS на 20-й день после начала терапии Кортексином. В то же время в контрольной группе не установлено заметных статистически значимых сдвигов по всем этим параметрам. С учетом того, что при заполнении врачом-исследователем психометрических шкал, возможны некоторая тенденциозность и, следовательно, искажение объективной информации, на следующем этапе работы было решено избежать этого с помощью анализа шкалы-самооценки SCL-90, заполняющейся больными.
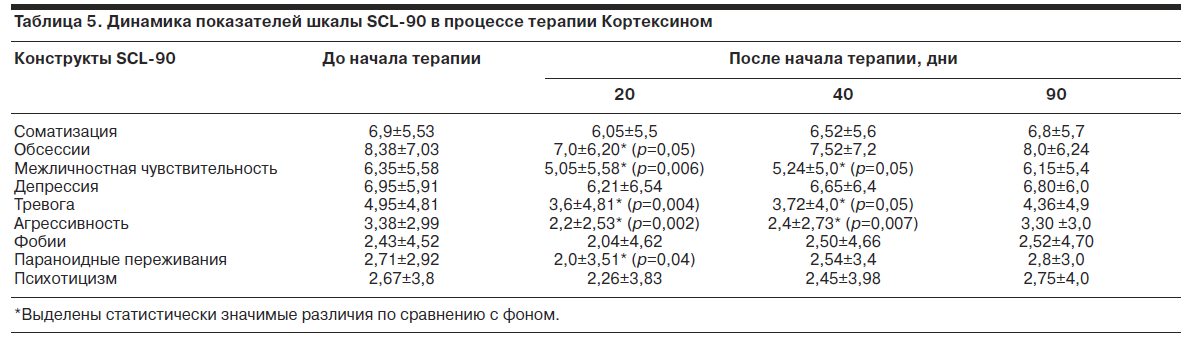
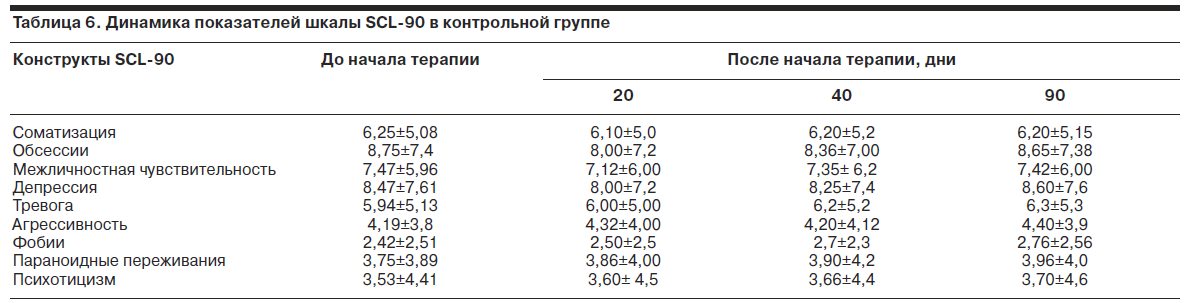
В процессе терапии Кортексином отмечались статистически значимые сдвиги в некоторых показателях шкалы SCL-90 в сторону снижения по сравнению с фоновым уровнем. Изменения затрагивали благоприятную динамику показателей обсессий, межличностной чувствительности, тревоги, агрессивности и параноидных переживаний. Наибольшие сдвиги по всем перечисленным параметрам наблюдались на 20-й день со дня начала терапии Кортексином (т.е. через 10 дней после прекращения курса инъекций). Интересно, что у показателей межличностной чувствительности, тревоги и агрессивности, данные сдвиги сохранялись и через 40 дней после начала терапии (т.е. через 30 дней после окончания курса инъекций Кортексина). К 90-му дню с момента начала терапии (через 80 дней после окончания курса терапии Кортексином) различия по сравнению с фоном стирались. В контрольной группе ни по одному показателю шкалы SCL-90 значимых различий по сравнению с фоном не отмечено. С учетом того, что в основной группе препарат Кортексин продемонстрировал многокомпонентный спектр клинического эффекта, на заключительном этапе исследования было решено более тщательно изучить основные векторы (составляющие) этого эффекта. Для этого применен факторный анализ (метод главных компонент). Следует отметить, что эта методика позволяет выделить среди всего многообразия явлений связанные между собой показатели, которые образуют факторы. Существенно, что в результате этой процедуры можно выделить факторы, которые не зависят друг от друга и представляют собой ортогональные векторы (т.е. расположенные в пространстве под углом в 90°). Соответственно, признаки, вошедшие в каждый из факторов со статистически значимыми весовыми нагрузками, будут указывать на структуру данного фактор, т.е. характеризовать его как симптомокомплекс, а признаки, включенные в разные факторы, не будут связаны друг с другом. В качестве изучаемых признаков на данном этапе исследования применялась разность между выраженностью 9 конструктов SCL-90 до и на 20-й день после начала терапии Кортексином. Иными словами, в качестве признаков служили показатели выраженности симптоматики, ушедшей в процессе лечения.
В результате анализа удалось выделить 2 фактора. Первый объяснял 44% дисперсии, второй – 14%, т.е. первый из факторов несет в 3 раза больше информации, чем 2-й. Со значимыми весовыми нагрузками в 1-й фактор вошли показатели личностной чувствительности, депрессии и психотицизма. Во 2-й фактор были включены лишь два признака со статистически значимыми нагрузками – тревога и агрессивность. Из этого следует, что редукция депрессии, межличностной сенситивности и психотических переживаний взаимосвязаны друг с другом, но происходит независимо от редукции тревоги и агрессивности, которые в свою очередь также взаимосвязаны между собой. Иными словами, первый вектор в клиническом эффекте Кортексина включает воздействие на депрессивно-сенситивную симптоматику и примыкающие к ним психотические переживания. Таким образом, данный компонент в действии препарата отражает своеобразный тимолептический (антидепрессивный) эффект, что проявляется не только в улучшении настроения, но и нормализации чрезмерной межличностной сенситивности и устранении психотических явлений пограничного уровня. Второй фактор фактически отражает анксиолитическое и антиагрессивное действие препарата, которое не зависит от антидепрессивного эффекта Кортексина.
Обсуждение результатов
Особенностью проведения терапевтического курса Кортексина является то, что его применяют в суточной дозе 10 мг внутримышечно не более 10 дней. В свою очередь дизайн исследования построен таким образом, что все возможные сдвиги в психическом и нейропсихологическом состоянии больных эпилепсией оценивались как минимум через 10, 30 и 80 дней после окончания курса Кортексина, что позволяет оценить стойкость эффектов Кортексина. Результаты исследования показали, что Кортексин действительно приводит к значимым изменениям как в нейропсихологической сфере, так и в психопатологической симптоматике у больных эпилепсией. Эффекты препарата затрагивают влияние на вербальную беглость, состояние исполнительских функций, а также на психопатологическую сферу больных (главным образом на аффективную и тревожную симптоматику). Немаловажно, что сразу после введения препарата не отмечалось учащения припадков, а неблагоприятные сдвиги в виде учащения вторично-генерализованных приступов возникали лишь через 80 дней после прекращения курса Кортексина, что не позволяет рассматривать эти явления как причинно-следственные. Исполнительские функции в нейропсихологии и нейропсихиатрии принято связывать с деятельностью лобных долей головного мозга, в частности дорсолатеральных отделов. Сохранность этих функций является необходимым условием для выполнения широкого круга задач, связанных с планированием деятельности, поведением, предвидением ошибочных решений и попыток исправить и не допустить ошибки [12–14]. Аналогично этому улучшение показателей речевой беглости также принято связывать с деятельностью лобных отделов головного мозга, хотя следует подчеркнуть, что статистически значимых связей между улучшением по тесту речевой беглости и тесту Sohlberg и Mateer получено не было. Это свидетельствует о независимости данных эффектов Кортексина. Иначе говоря, Кортексин наделен широким спектром эффектов и оказывает мультимодальное действие как на исполнительские функции, так и на речевую беглость и психопатологические феномены у больных эпилепсией. Полученные результаты показывают, что Кортексин в целом позитивно вмешивается в исполнительские функции и тем самым способствует их восстановлению. Можно предположить, что это позволит улучшить социальное функционирование больных эпилепсией по мере применения препарата, что в свою очередь обусловлено нормализацией деятельности лобных отделов мозга под влиянием Кортексина.
Результаты настоящего исследования показывают, что Кортексин оказывает позитивное влияние на больных эпилепсией в смысле снижения выраженности как аффективной, так и тревожной симптоматики. Важно подчеркнуть, что эти эффекты препарата не зависели друг от друга. Также они практически не зависели от влияния на нейропсихологические характеристики. Аффективную и тревожную симптоматику в психиатрии принято рассматривать в рамках отдельных и самостоятельных диагностических категорий. Тем не менее в последние 20 лет эти состояния изучают как коморбидные, т.е. допускается неслучайное совпадение депрессивных и тревожных расстройств у одних и тех же больных. Не углубляясь детально в эту проблему, следует подчеркнуть, что она пока далека от разрешения. Это касается как эндогенных аффективных расстройств, так и депрессивных и тревожных расстройств при органических поражениях головного мозга. Настоящее исследование продемонстрировало независимость антидепрессивного и противотревожного эффектов Кортексина у больных эпилепсией. Это, несомненно, указывает на широкие возможности препарата в плане устранения не только нейропсихологической несостоятельности у больных эпилепсией, но и благоприятного воздействия как на тревожную, так и депрессивную симптоматику.
Примечательно, что антидепрессивный эффект сочетался с устранением проявлений межличностной чувствительности и психотических проявлений и на долю устранения этих феноменов приходилось 44% от всей вариабельности фармакотерапевтических сдвигов. Напротив, на устранение тревожной симптоматики и сопряженной с ней агрессивности приходилось в 3 раза меньше дисперсии (14%) от всей динамики симптоматики. Из этого следует важный вывод о том, что собственно антидепрессивный эффект препарата и сопряженные с ним эффекты являются едва ли не основными в спектре действия Кортексина, поскольку на их долю приходится почти половина всех эффектов. В свою очередь доля анксиолитического и антиагрессивного эффектов Кортексина была в 3 раза меньше. Тем не менее не учитывать эту особенность действия препарата вряд ли было бы правильным. Важно, что препарат в состоянии устранить как собственно депрессивную, так и тревожную симптоматику и сопутствующие им феномены. Это лишний раз подчеркивает широту терапевтического диапазона Кортексина, который может рассматриваться не только как ноотропное соединение, но и как антидепрессант, транквилизатор и даже нейролептик (за счет устранения психотических переживаний и агрессивности). Очевидно, что все эти эффекты обязаны своим появлением воздействию препарата на функции лобных отделов головного мозга, что позволяет говорить о так называемом нормофронтальном эффекте Кортексина. Вместе с тем следует подчеркнуть, относительную нестойкость этих эффектов во времени при курсе терапии, не превышающем 10 дней. Очевидно, что для закрепления стойкости данных эффектов следует применять повторные курсы введения препарата через 2–3 мес, хотя это предположение нуждается в подтверждении в специальном исследовании.


