Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№04 2013
Антипсихотики off-label №04 2013
Номера страниц в выпуске:46-52
Традиции отечественной психиатрической школы предполагают необходимость проведения лечения на основании тщательного соотнесения клинических особенностей заболевания и спектров психотропной активности нейролептиков.
Резюме. Обзор литературы посвящен проблеме применения атипичных антипсихотиков off-label. Проводится анализ возможности и целесообразности, в том числе, с позиции соотношения риск/польза использования нейролептиков второй генерации в терапии тревожных, обсессивно-компульсивных, депрессивных, соматоформных расстройств, расстройств личности и пищевого поведения, деменции, бессоннице, при психических расстройствах у детей. Приводится доказательная сила эффективности различных препаратов (арипиразола, рисперидона, оланзапина, кветиапина, зипрасидона).
Ключевые слова: психические расстройства, терапия, нейролептики второй генерации.
Off-label antipsychotics
N.N.Petrova, M.V.Dorofeikova
Saint Petersburg State University
Summary. The literature review deals with the off-label use of atypical antipsychotics. The possibilities and expediency, including those in the context of a risk/benefit use of second-generation neuroleptics in the therapy of anxiety, obsessive-compulsive, depressive, somatoform, personality, and eating disorders, dementia, insomnia, in mental disorders in children are analyzed. There is evidence for the efficacy of different drugs (aripiprazole, risperidone, olanzapine, quetiapine, and ziprasidone).
Key words: mental disorders, therapy, second-generation neuroleptics.
Традиции отечественной психиатрической школы предполагают необходимость проведения лечения на основании тщательного соотнесения клинических особенностей заболевания и спектров психотропной активности нейролептиков [1, 2, 6, 7].
Было принято различать профили психотропной активности нейролептиков по выраженности преимущественно седативного, селективного или глобального антипсихотического, активирующего (дезингибирующего), депрессогенного, нейротропного действия. В соответствии с концепцией широкого и узкого спектра психотропного действия выделили препараты, которые эффективны при полиморфных, генерализованных психопатологических синдромах (галлюцинаторно-параноидных, кататоно-гебефренных и др.), а также препараты, которые способствуют редукции ряда более изолированных психопатологических синдромов [9].
Появление нейролептиков II поколения привело к условному выделению традиционных (классических) нейролептиков и атипичных антипсихотиков. D.Naber и М.Lambert (2009 г.), размышляя о вопросах систематики нейролептиков и анализируя эволюцию терминологии, отметили, что название «атипичные» было связано с предполагаемым отсутствием двигательных побочных эффектов. Однако было установлено, что и эти препараты в высоких дозировках вызывают экстрапирамидные нарушения, и понятие атипичности стало носить скорее количественный, чем категориальный характер. Последние исследования, по мнению авторов, показали, что подобный принцип разделения «псевдокатегоричен» [137].
Вместе с тем формируется приоритетность применения атипичных антипсихотиков по сравнению с традиционными нейролептиками, что обусловлено рядом факторов. Так, например, среди недостатков традиционной нейролептической терапии шизофрении выделяют резистентность к монотерапии, доходящую до 25–30% случаев, низкую эффективность коррекции негативных расстройств, высокий риск побочных эффектов, в частности нейролептических депрессий, широкий спектр неврологических, соматовегетативных, эндокринных нарушений [3, 5].
Бимодальный спектр действия на дофаминовые и серотониновые рецепторы указывает на перспективность использования атипичных антипсихотиков для преодоления резистентности к традиционным нейролептикам, коррекции негативных и когнитивных расстройств.
Из других преимуществ в ТоПеГзоп (1997 г.) отмечены особенности их фармакокинетики: быстрое достижение пика концентрации в крови (через 5 ч после поступления в организм); наличие пролонгированного эффекта (период полувыведения варьирует от 21 до 54 ч); возможность титрования дозы, которая достигается благодаря параллелизму между принимаемой дозой препарата и концентрацией его в плазме крови; безопасность применения в сочетании с другими психотропными и сомато-тропными препаратами [4].
В настоящее время получила распространение точка зрения, согласно которой все нейролептики различаются главным образом по спектру побочных эффектов и принципом выбора терапии должно служить соотношение «риск/польза». Предполагается, что это соотношение у атипичных антипсихотиков более благоприятно по сравнению с нейролептиками I поколения. Однако вопрос различий по этому параметру между препаратами внутри группы нейролептиков новой генерации, как, впрочем, и в отношении типичных нейролептиков, остается открытым.
Данный обзор посвящен анализу возможности и целесообразности применения атипичных антипсихотиков off-label – не по показаниям, в том числе с позиции соотношения «риск/польза». Следует отметить, что этот вопрос рассматривается в литературе последних лет именно в отношении нейролептиков II генерации.
Официальные показания для нейролептической терапии весьма ограниченны. Так, нейролептики одобрены Управлением по контролю пищевых продуктов и лекарств в США (FDA) для лечения шизофрении, биполярного аффективного расстройства (БАР) и некоторые из них – депрессии. При этом, например, 2-летнее исследование применения кветиапина в психиатрических больницах показало, что лишь 1/4 пациентов, получавших препарат, имели диагноз, при котором он одобрен, и только 1/3 пациентов получали его в стандартных дозах. Чаще всего кветиапин использовали при депрессии и в наркологической практике [154].
В зарубежной литературе имеются указания, что наиболее часто среди атипичных антипсихотиков применяются off-label рисперидон, кветиапин и оланзапин [13, 40, 91], а, например, в США, по данным 2009 г., – кветиапин и рисперидон [154].
В качестве мишеней применения нейролептиков помимо психозов выделяют бессонницу, тревогу, обсессивно-компульсивное расстройство (ОКР), возбуждение и другие поведенческие расстройства [123]. Высказано мнение, что наиболее распространенные психические расстройства для применения антипсихотиков off-label – посттравматическое стрессовое расстройство (ПТСР) и «малая депрессия» [115]. Данные канадских, британских, французских, австралийских, турецких, немецких, новозеландских и итальянских психиатров говорят об опыте применения атипичных антипсихотиков при тревоге [24, 40, 67, 91, 185], синдроме дефицита внимания и гиперактивности – СДВГ [19, 91], расстройствах личности – РЛ [185], депрессии [74, 91, 185], деменции [13, 81, 144, 166, 171, 198], расстройствах пищевого поведения – РПП [82].
Анализ использования атипичных антипсихотиков off-label с помощью англоязычных материалов PubMed, Embase, PsycINFO, CINAHL (Cumulative Index to Nursing and Allied Health Literature), Cochrane DARE (Database of Abstracts of Reviews of Effects) и Cochrane CENTRAL (Cochrane Central Register of Controlled Trials) на примере 170 статей, опубликованных до мая 2011 г. включительно, показал, что атипичные антипсихотики применялись при тревожном расстройстве, СДВГ, деменции и выраженной ажитации у пожилых, депрессии, РПП, бессоннице, ОКР, ПТСР, РЛ, зависимостях и синдроме Туретта [123].
В одном из плацебо-контролируемых исследований оланзапин оказался эффективнее плацебо [28], в 2 других – кветиапин не отличался от плацебо в терапии социальной фобии [68, 190].
Кветиапин в дозе 50 или 150 мг/сут оказался схожим по эффективности с пароксетином в дозе 20 мг/сут при терапии генерализованного тревожного расстройства (ГТР) в течение 8 нед, но при этом лечение кветиапином сопровождалось меньшей частотой побочных эффектов со стороны половой сферы [27]. Показано, что 150 или 300 мг/сут кветиапина равны по эффективности 10 мг/сут эсциталопрама в терапии ГТР в течение 8 нед [134]. При поддерживающей монотерапии кветиапином наблюдалось достоверное снижение риска рецидива эпизодов генерализованной тревоги [109].
Ряд активно контролируемых исследований, базировавшихся на наличии терапевтического ответа (снижение общего показателя по шкале тревоги Гамильтона – НАМ-А минимум на 50%), был направлен на оценку эффективности комбинированной терапии нейролептиками и различных лекарственных средств. Обнаружено, что аугментация кветиапином и кветиапином пролонг антидепрессивной терапии препаратами группы селективных ингибиторов обратного захвата серотонина (СИОЗС), в частности пароксетином, не дает преимуществ в преодолении терапевтической резистентности при ГТР [14, 111, 175].
В 8-недельном рандомизированном плацебо-контролируемом исследовании установлена эффективность сочетанной терапии рисперидоном в малых дозах и пароксетином при паническом расстройстве [156].
Результаты применения атипичных антипсихотиков при ПТСР противоречивы. Есть данные, которые свидетельствуют об эффективности рисперидона [29, 89, 136, 149, 158] и оланзапина [48, 180]. Анализ 5 работ, которые включали от 19 до 65 пациентов, получавших лечение в течение 5–16 нед [29, 89, 158, 162, 180], выявил умеренно значимую эффективность рисперидона в дозе 0,5–3 мг/сут (4 исследования) и оланзапина (15 мг/сут). Соответственно, относительный риск составил 6,47 (c 95% доверительным интервалом – ДИ 0,32–12,61) и 12,13 (95% ДИ 0,97–23,29), суммарно 7,79 (95% ДИ 2,40–13,17) [123]. Отмечена эффективность рисперидона в отношении отдельных симптомов ПТСР (раздражительности и навязчивых мыслей) [136].
Наряду с этим в метаанализе 2011 г. выявлен некоторый положительный эффект рисперидона и кветиапина, но не оланзапина [11]. В исследовании M.Butterfield и соавт. также было установлено, что оланзапин по эффективности не отличался от плацебо [48]. Небольшие (от 15 до 94 пациентов с ПТСР) исследования, в основном посвященные применению рисперидона, дали неоднозначные результаты [29, 89, 90, 136, 148, 149, 158, 162].
Метаанализы показали, что кветиапин и рисперидон весьма эффективны в качестве комбинированной терапии ОКР [123, 174]. Однако в отдельных работах повышение вероятности терапевтического ответа на основании результатов обсессивно-компульсивной шкалы Йеля–Брауна (Yale Brown Obsessive Compulsive Scale, Y-BOCS) достигло уровня статистической значимости для рисперидона, но не для кветиапина и оланзапина [37, 176].
Восемь работ, опубликованных с 2006 по 2011 г., 5 из которых – плацебо-контролируемые, свидетельствуют об эффективности аугментации кветиапином или рисперидоном антидепрессивной терапии циталопрамом либо ИОЗС: соответственно, 2,36 (95% ДИ 0,85–6,57), 3,92 (95% ДИ 1,27–12,13) [61, 63, 65, 114, 123, 125, 129, 194, 195]. Вместе с тем число пациентов, включенных в эти исследования, было невелико – от 18 до 66.
Применение при ОКР кветиапина в сочетании с СИОЗС
(в отличие от кломипрамина) оказалось эффективным, по данным Y-BOCS [65]. В сочетании с ИОЗС кветиапин показал себя как более эффективный препарат по сравнению с зипрасидоном (80 и 44,4% улучшение по шкале Y-BOCS соответственно) [164]. Следует отметить, что кветиапин эффективен как при лечении ОКР, так и ГТР: при ГТР кветиапин повысил вероятность ответа на терапию на 26% по сравнению с плацебо (минимум 50% улучшение по НАМ-А), при ОКР – в 3,9 раза (25–35% улучшение по шкале Y-BOCS).
При сравнении разных атипичных антипсихотиков в лечении ОКР было выяснено, что терапевтический эффект монотерапии оланзапином или рисперидоном существенно не различается [41].
В австралийском исследовании на примере 154 больных ОКР было показано, что 60,4% получали психотропную терапию, из них 59,1% – СИОЗС, а прием антипсихотических препаратов был ассоциирован с наличием хульных мыслей [123].
В метаанализе 2006 г., направленном на оценку возможностей применения атипичных антипсихотиков при большой депрессии, было выявлено отсутствие различий между атипичными антипсихотиками и плацебо в сочетании их с СИОЗС при длительности лечения 8 нед. В некоторых исследованиях, впрочем, атипичные антипсихотики способствовали более быстрой редукции депрессивной симптоматики (2–4 нед) [174].
В метаанализах Papakostas 2007 и 2009 гг. было выявлено положительное влияние аугментации атипичными антипсихотиками по числу ответов на терапию и достижению ремиссии при отсутствии различий в эффективности между отдельными препаратами (оланзапином, кветиапином, рисперидоном, арипипразолом) [138, 151]. Есть данные, что монотерапия кветиапином существенно увеличивает период до следующего эпизода депрессии [22].
С 2006 по 2011 г. вышло 26 статей о применении атипичных антипсихотиков при депрессии в качестве аугментации антидепрессивной терапии СИОЗС у пациентов с резистентной депрессией [30, 34, 35, 50, 72, 77, 80, 110, 113, 124, 126, 130, 132, 139, 157, 203]. При аугментации рисперидоном была выявлена большая дезактуализация суицидных мыслей по сравнению с монотерапией антидепрессантами [157]. Арипипразол в качестве аугментации антидепрессивной терапии позволял добиться терапевтического ответа (достоверная динамика по шкале Монтгомери–Асберга) [113].
Данные активно контролируемых исследований свидетельствуют о значительном улучшении состояния по шкале Монтгомери–Асберга у больных с депрессией, получавших сочетанную терапию оланзапином и флуоксетином, по сравнению с монотерапией одним из этих препаратов [188]. Добавление кветиапина в терапевтическую схему к пароксетину или венлафаксину усиливало антидепрессивный эффект (по данным шкалы депрессии Гамильтона – HAMD-17) [97]. Восьминедельное исследование эффективности зипрасидона в качестве аугментации терапии сертралином продемонстрировало максимальное улучшение состояния по общей клинической шкале CGI-S и шкале Монтгомери–Асберга при назначении 160 мг зипрасидона (по сравнению с 80 мг зипрасидона либо монотерапией сертралином) [71]. Впрочем, по HAMD-17 и HAM-A значительных различий найдено не было.
Данные литературы свидетельствуют о достижении ремиссии депрессии через 4–8 нед при сочетанной терапии антидепрессантами и атипичными антипсихотиками [80, 110, 124, 130, 132, 203]. Вероятность ремиссии (по HAMD) при применении антипсихотика была определена как 2,76 (95% ДИ 1,21–6,28) для кветиапина и 2,10 (95% ДИ 1,43–3,09) для рисперидона. Вероятность ответа на терапию (минимум 50% снижение по HAMD) составила 2,30 (95% ДИ 1,35–3,92) для кветиапина и 1,50 (95% ДИ 1,20–1,87) для рисперидона [123].
Ремиссия (уровень депрессии от 8 до 10 баллов по шкале Монтгомери–Асберга в зависимости от исследования) была зафиксирована в 8 исследованиях комбинированной терапии [30, 34, 35, 72, 77, 110, 126] – от 97 до 493 обследованных больных. Доказана эффективность арипипразола и кветиапина: арипипразол против плацебо – 1,57 (95% ДИ 1,24–2,00) и кветиапин против плацебо – 1,24 (95% ДИ 0,82–1,88) [123].
В ряде исследований, которые включали от 310 до 723 пациентов, подтверждена эффективность монотерапии депрессии кветиапином: в течение 6–9 нед терапии вероятность достижения ремиссии (по шкале Монтгомери–Асберга) составила 1,43 (95% ДИ 1,07–191) по сравнению с плацебо – 1,49 (95% ДИ 1,23–1,81) [21, 23, 39, 59, 123, 196]. Кветиапин оказался более эффективным по сравнению с препаратами лития при терапии в течение 56 дней (по шкале депрессии Гамильтона, Монтгомери–Асберга и Wildlocher Psychomotor Retardation Scales) [69].
Обзор 4 рандомизированных контролируемых исследований 2011 г. по применению антипсихотиков при соматоформном расстройстве показал эффективность сульпирида при диспепсии и неэффективность антипсихотиков при дисморфофобии [62].
Hagman и соавт. утверждает, что успешная психотропная терапия для страдающих анорексией все еще не найдена. Так, рисперидон (средняя доза 2,5 мг/сут, длительность приема 9 нед) при лечении 40 пациенток в возрасте от
12 до 21 года помог лишь снизить показатель «межличностное недоверие», но не привел к прибавке массы тела и иным существенным изменениям [103]. Аналогично нейтральные или негативные результаты демонстрируют и другие исследования нейролептической терапии анорексии [25, 57, 58, 86, 95, 127, 182]. Побочные эффекты, такие как седация и дислипидемия, которые, например, в австралийском исследовании 2011 г. встречались у 56% пациентов при приеме оланзапина, серьезно ограничивают возможность и усложняют нейролептическую терапию нервной анорексии [145].
Имеются данные о применении нейролептической терапии при некоторых РЛ. Антипсихотики широко используются при пограничном РЛ, поскольку считаются эффективными средствами против импульсивности, агрессии, тревоги [15, 31, 102, 146]. Их применение считается оправданным для коррекции расстройств мышления и восприятия у этих больных [92]. Однако побочные эффекты обусловливают применение антипсихотиков преимущественно при обострениях [33, 64, 141, 186].
Некоторые плацебо-контролируемые исследования указывают на эффективность при пограничном РЛ арипипразола [142, 143] (в дозе 5–10, но не 2,5 мг/сут), оланзапина [202], а также кветиапина, в том числе в отношении психотической симптоматики [191]. Другие свидетельствуют лишь о более быстром ответе на терапию при приеме зипрасидона или кветиапина [118, 152, 169]. Значительных различий в эффекте (улучшение настроения, снижение уровня тревоги) оланзапина и галоперидола не найдено [170]. Имеются данные, что клозапин нивелирует агрессию и психотическую симптоматику при пограничном РЛ [33, 51, 52, 75, 183].
Среди работ, посвященных применению при пограничном РЛ рисперидона, наиболее крупной является исследование Rocca и соавт. на 15 пациентах, у которых была отмечена положительная динамика агрессивного поведения, аффективных и других психических расстройств [93, 112, 160, 184].
Девять пациентов с коморбидными пограничным РЛ и дистимией через 8 нед применения оланзапина (средняя доза 3,3 мг/сут) обнаружили значительное снижение импульсивности, улучшение психического состояния и социального функционирования [168]. Zanarini и Frankenburg в полугодовом двойном слепом плацебо-контролируемом исследовании на 28 пациентках с пограничным РЛ показали эффективность оланзапина (5,33 мг/сут) в виде снижения тревоги, параноидных мыслей и улучшения коммуникабельности [201]. Также продемонстрирована эффективность оланзапина в дозе 5–10 [38] и 8,8 мг/сут в течение 12 нед в отношении импульсивного, агрессивного поведения, депрессии и тревоги [179]. Оланзапин в малых дозах уменьшает частоту самоповреждений [96]. Результаты исследования 2004 г. говорят о том, что сочетание флуоксетина и оланзапина более эффективны, чем монотерапия этими препаратами [12].
В нескольких исследованиях, посвященных кветиапину при пограничном РЛ, положительный результат был продемонстрирован при использовании от 25 до 400 мг/сут [10, 31, 32, 192].
Результаты лечения героиновых наркоманов с пограничным РЛ, проходящих поддерживающую терапию метадоном, свидетельствуют об успешном воздействии оланзапина на симптомы депрессии, тревоги и агрессии, обсессивную симптоматику, соматизированные расстройства [102, 147].
При шизотипическом РЛ рисперидон не отличался по эффективности от плацебо [131].
Рандомизированное контролируемое исследование, проведенное в Таиланде на 13 пациентах, не дает возможности судить об эффективности применения атипичных антипсихотиков для лечения бессонницы. Однако было показано, что применение кветиапина привело к удлинению сна на 125 мин по сравнению с 72 мин при приеме плацебо [123]. В 6 других описательных исследованиях оценивалась терапия кветиапином или оланзапином.
Последний оказал благоприятное воздействие на качество сна и «медленный» сон у 12 пациентов, получавших его на протяжении 3 нед [172], а также на длительность сна и количество ночных кошмаров у 8 из 9 пациентов на протяжении периода до 3 лет [73]. Рекомендуемые дозы составили от 2,5 до 10 мг на ночь в зависимости от самочувствия пациентов и данных полисомнографии. Накоплен опыт применения кветиапина при первичной бессоннице [197], бессоннице, связанной с абстинентным синдромом [187], у больных с опухолями [153] и с болезнью Паркинсона [105], однако данные недостаточно убедительны. Дозировки составляли от 12,5 до 225 мг ежедневно, курс лечения – от 6 нед до 3 мес. Обзор 2006 г. привел обнадеживающие результаты 3 плацебо-контролируемых исследований терапии расстройств сна оланзапином и 1 – арипипразолом [174].
Большое внимание исследователей уделяется применению атипичных антипсихотиков при деменции у пожилых пациентов, что связано с распространением их использования и связанного с этим повышения летальности среди этих больных [49]. Как показал метаанализ Maglione и соавт., эффективность в отношении психотических расстройств, ажитации у больных с деменцией установлена у арипипразола, оланзапина и особенно явно – у рисперидона, но не у кветиапина [123].
По данным метаанализов 2005–2006 гг., был обнаружен невыраженный, но статистически значимый терапевтический эффект рисперидона и арипипразола и тенденция к эффективности у оланзапина и кветиапина в отношении психотических расстройств и агрессии у больных с деменцией [26, 60, 147, 167]. В более позднем метаанализе не было выявлено существенного отличия между атипиками и плацебо в отношении поведенческих расстройств при деменции [200].
Результаты сравнения атипичных антипсихотиков и галоперидола показывают, что их воздействие на психотическую симптоматику и ажитацию при деменции различается несущественно. С другой стороны, не были найдены заметные различия между атипичными антипсихотиками (оланзапин, кветиапин, рисперидон) по терапевтической эффективности и исходам психозов при деменции [123].
По данным 129 крупных и/или плацебо-контролируемых исследований, у пациентов старшего возраста побочные эффекты терапии антипсихотиками включают повышенный риск смерти, инсульта, заболевания мочевой системы, развития экстрапирамидного синдрома. У взрослых лиц в возрасте до 64 лет отмечают прибавку массы тела (особенно при приеме оланзапина), повышенную утомляемость, седацию, акатизию (наибольший риск при приеме арипипразола), экстрапирамидные симптомы. Вместе с тем разница между побочными эффектами у пожилых пациентов с депрессией, принимавших рисперидон и антидепрессанты группы СИОЗС, не найдена [123].
Обзор 2006 г. продемонстрировал статистически значимую взаимосвязь между применением атипичных антипсихотиков и вероятностью смерти у пациентов с болезнью Альцгеймера (3,5%) по сравнению с 2,3% при приеме плацебо [174]. В то же время из 6 больших когортных исследований 4 выявили большую по сравнению с атипиками смертность среди больных, принимавших классические нейролептики [81, 101, 106, 119, 161, 166].
В 2004 г. почти 25% жителей домов престарелых в США получали нейролептики, преимущественно II поколения [123]. После предупреждения FDA в 2005 г. о повышенной смертности вследствие их употребления частота их использования уменьшилась, особенно среди пациентов, страдающих деменцией [70]. Впрочем, опрос профессионалов в сфере охраны здоровья показал, что лишь 49% врачей изменили свое отношение к назначению нейролептиков у пожилых: остальные не отреагировали на преду-преждение по причинам отсутствия альтернатив, недостатка руководств и доказательств [163].
В наркологии нейролептики используются при наличии коморбидных и метааддиктивных расстройств (отдельных формах психопатических и психопатоподобных нарушений, расстройствах невротического круга, дисфорических состояниях в ранней фазе опиоидной постабстиненции). Они улучшают прогноз заболевания, особенно у лиц шизоидного склада, и не вызывают зависимости.
Ю.П.Сиволап и В.А.Савченков в статье о применении нейролептиков в наркологической практике (2007 г.) указывают, что, несмотря на недостаточное и неоднозначное их влияние на аддиктивное влечение, эти препараты успешно нашли применение при психозах и пограничных расстройствах невротического, личностного и аффективного характера у злоупотребляющих психоактивными веществами [8].
Рисперидон оказался эффективным при многих состояниях, в том числе острых абстинентных и интоксикационных психозах и эндоморфных психотических синдромах у больных алкоголизмом. Этот препарат хорошо зарекомендовал себя в коррекции дисфории и психопатоподобных расстройств. Отмечено его положительное влияние на комплаенс наркологических пациентов. Имеются исследования, посвященные применению таких атипичных антипсихотиков, как арипипразол [17, 18, 128, 193], оланзапин [85, 98–100] и кветиапин [84, 108], при злоупотреблении алкоголем и алкогольной зависимости, а также арипипразола [117, 181], оланзапина [88, 107, 159] и рисперидона [83, 116, 120, 177, 178] при злоупотреблении кокаином и кокаиновой зависимости. Арипипразол оказался неэффективным лекарством при злоупотреблении амфетамином/метамфетамином [140, 189], а оланзапин – при лечении героиновой зависимости [79].
Опыт лечения алкоголизма с помощью атипичных антипсихотиков говорит о том, что наиболее частым результатом является достижение воздержания от алкоголя. Длительность воздержания от алкоголя и число пациентов, достигших полного воздержания от употребления алкоголя, не различались при лечении налтрексоном и арипипразолом [128]. Вместе с тем в плацебо-контролируемом исследовании было показано, что терапия арипипразолом не способствовала увеличению периода воздержания от алкоголя [17]. Однако аугментация кветиапином терапии налтрексоном оказалась эффективной [84].
Данные метаанализа 2006 г. о нейролептической терапии синдрома Туретта свидетельствуют о преимуществах рисперидона перед плацебо. Неоднозначные данные были получены об эффективности зипрасидона [174]. Описательные работы о лечении тиков (в возрасте до 18 лет) с помощью арипипразола свидетельствуют об улучшении состояния, однако довольно значительная часть пациентов (8 из 37 и 6 из 24) были вынуждены прервать курс лечения в связи с побочными эффектами [47, 199].
Рисперидон, как антипсихотик с антисеротониновым действием, в средней дозе 2,5 мг/сут показал положительный эффект при лечении синдрома Туретта в open-label-исследованиях и двойных слепых плацебо-контролируемых исследованиях, в частности Guy Chouinard, на 48 пациентах [16, 45, 46, 53, 54, 66, 76, 122, 165]. Так, 60,8% пациентов по сравнению с 26,1% пациентов, получавших плацебо, обнаружили улучшение общего функционирования. Влияния рисперидона на дистонию, дискинезии, акатизию обнаружено не было, притом что гипокинезия и тремор (в случаях его изначальной выраженности) наросли.
Особой проблемой является ограниченное применение нейролептической терапии у детей. Halloran и соавт. изучали паттерны назначения атипичных антипсихотиков частно застрахованным детям в США в возрасте от 2 до
18 лет в период 2002–2005 гг. и определили, что частота назначения нарастает (с 7,9 до 9,0 на 1 тыс. случаев). Мальчикам назначали почти в 2 раза больше препаратов, чем девочкам. Среди причин назначения преобладали поведенческие расстройства (67%), расстройства настроения (65%) и тревожные расстройства (43%), причем 75% детей имели более одного психиатрического диагноза. Чаще всего пациентам детского возраста назначали рисперидон (53%) и кветиапин (33%) [87].
Небольшое количество работ посвящено лечению антипсихотиками СДВГ. В одном из них все пациенты ответили на терапию рисперидоном, притом что на плацебо ответили 77% пациентов [20]. У детей с коморбидными СДВГ и умеренной умственной отсталостью рисперидон по сравнению с метилфенидатом оказался более эффективным [55]. Результаты 2 исследований, посвященных применению арипипразола при СДВГ в сочетании с БАР, не показали улучшения [123].
Клинический случай
Больная М. 55 лет, замужем, несколько лет не работает.
В течение примерно 10 лет постоянно безуспешно посещает различных специалистов-дерматологов в связи с убежденностью «заражения паразитами». Предъявляет жалобы на ощущение «передвижения насекомых» под кожей, неровность кожных покровов. Детально описывает размеры, строение, пути передвижения, жизненный цикл паразитов. Регулярно сдает для проведения микроскопического исследования «вещественные доказательства» – «частицы насекомых» представляются в лаборатории как личинки, яйца или продукты жизнедеятельности паразитов.
Занимается «вытравливанием» насекомых из организма. «Борьба» с паразитами включает такие методы самолечения, как механическое воздействие, едкие жидкости. Лицо, шея, плечи, грудь пациентки имеют выраженные дефекты кожного покрова (глубокие обезображивающие шрамы). Обрабатывает химическими веществами одежду, белье.
Таким образом, в клинической картине у пациентки дерматологической практики представлены монотематический паранойяльный зоопатический бред, тактильный галлюциноз, «симптом спичечного коробка», патомимия – кожные аутодеструктивные проявления, что соответствует дерматозойному бреду – инволюционной паранойе.
Назначен рисперидон (Торендо). Начальная доза составила 2 мг/сут, на 2-й день дозу повысили до 4 мг/сут. На фоне терапии рисперидоном (Торендо) в течение месяца наблюдались улучшение социальной адаптации, снижение актуальности патологических идей, редукция соматосенсорных феноменов восприятия.
Данный случай иллюстрирует применение рисперидона (Торендо) в психосоматике в режиме off-lable.
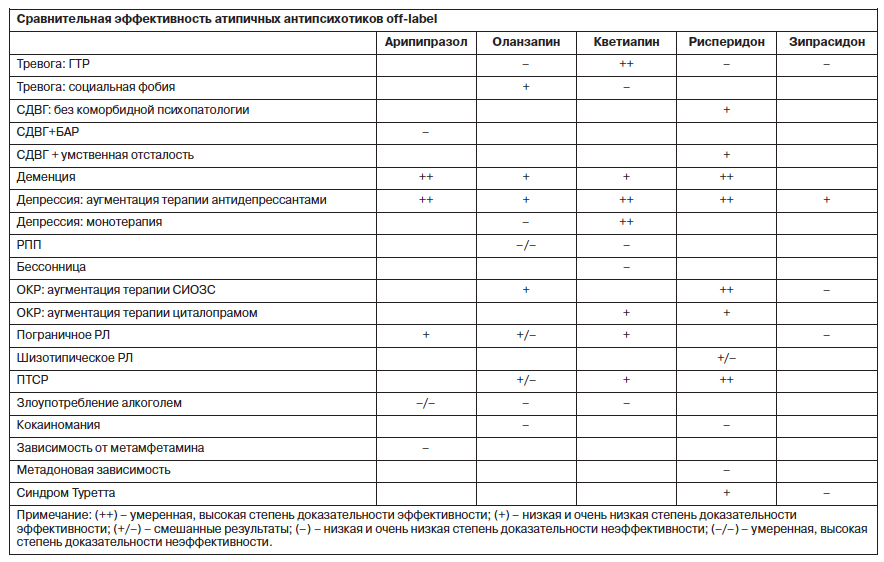
Доказательная сила эффективности различных препаратов приведена в таблице [123].
Таким образом, арипипразол, оланзапин и рисперидон оказывают не выраженный, но статистически значимый эффект в лечении психотических расстройств, возбуждения и поведенческих симптомов при деменции, однако следует учитывать значительный риск побочных эффектов. Зипрасидон не имеет достаточной доказательной базы для применения его off-label, за исключением депрессии. Умеренной силы доказательная база говорит об эффективности арипипразола, кветиапина и рисперидона в качестве аугментации антидепрессивной терапии: вероятность терапевтического ответа возрастает в 1,5–2 раза. Данных о применении оланзапина недостаточно, но они обнадеживают. Оланзапин продемонстрировал достаточную эффективность в терапии социальной фобии и ОКР. Умеренная доказательность наблюдается в отношении эффективности монотерапии депрессии кветиапином, аугментации терапии ОКР рисперидоном. Доказана эффективность и безопасность применения кветиапина при ГТР, рисперидона при ПТСР. Отсутствуют убедительные данные об эффективности атипичных антипсихотиков при РЛ, диссомнии, РПП и аддикции.
Сведения об авторах
Петрова Наталия Николаевна – д-р мед. наук, зав. каф. психиатрии и наркологии мед. фак. СПбГУ.
E-mail: petrova_nn@mail.ru
Дорофейкова Мария Владимировна – студентка 6 курса мед. фак. СПбГУ. E-mail: mvdorofeykova@mail.ru
Ключевые слова: психические расстройства, терапия, нейролептики второй генерации.
Off-label antipsychotics
N.N.Petrova, M.V.Dorofeikova
Saint Petersburg State University
Summary. The literature review deals with the off-label use of atypical antipsychotics. The possibilities and expediency, including those in the context of a risk/benefit use of second-generation neuroleptics in the therapy of anxiety, obsessive-compulsive, depressive, somatoform, personality, and eating disorders, dementia, insomnia, in mental disorders in children are analyzed. There is evidence for the efficacy of different drugs (aripiprazole, risperidone, olanzapine, quetiapine, and ziprasidone).
Key words: mental disorders, therapy, second-generation neuroleptics.
Традиции отечественной психиатрической школы предполагают необходимость проведения лечения на основании тщательного соотнесения клинических особенностей заболевания и спектров психотропной активности нейролептиков [1, 2, 6, 7].
Было принято различать профили психотропной активности нейролептиков по выраженности преимущественно седативного, селективного или глобального антипсихотического, активирующего (дезингибирующего), депрессогенного, нейротропного действия. В соответствии с концепцией широкого и узкого спектра психотропного действия выделили препараты, которые эффективны при полиморфных, генерализованных психопатологических синдромах (галлюцинаторно-параноидных, кататоно-гебефренных и др.), а также препараты, которые способствуют редукции ряда более изолированных психопатологических синдромов [9].
Появление нейролептиков II поколения привело к условному выделению традиционных (классических) нейролептиков и атипичных антипсихотиков. D.Naber и М.Lambert (2009 г.), размышляя о вопросах систематики нейролептиков и анализируя эволюцию терминологии, отметили, что название «атипичные» было связано с предполагаемым отсутствием двигательных побочных эффектов. Однако было установлено, что и эти препараты в высоких дозировках вызывают экстрапирамидные нарушения, и понятие атипичности стало носить скорее количественный, чем категориальный характер. Последние исследования, по мнению авторов, показали, что подобный принцип разделения «псевдокатегоричен» [137].
Вместе с тем формируется приоритетность применения атипичных антипсихотиков по сравнению с традиционными нейролептиками, что обусловлено рядом факторов. Так, например, среди недостатков традиционной нейролептической терапии шизофрении выделяют резистентность к монотерапии, доходящую до 25–30% случаев, низкую эффективность коррекции негативных расстройств, высокий риск побочных эффектов, в частности нейролептических депрессий, широкий спектр неврологических, соматовегетативных, эндокринных нарушений [3, 5].
Бимодальный спектр действия на дофаминовые и серотониновые рецепторы указывает на перспективность использования атипичных антипсихотиков для преодоления резистентности к традиционным нейролептикам, коррекции негативных и когнитивных расстройств.
Из других преимуществ в ТоПеГзоп (1997 г.) отмечены особенности их фармакокинетики: быстрое достижение пика концентрации в крови (через 5 ч после поступления в организм); наличие пролонгированного эффекта (период полувыведения варьирует от 21 до 54 ч); возможность титрования дозы, которая достигается благодаря параллелизму между принимаемой дозой препарата и концентрацией его в плазме крови; безопасность применения в сочетании с другими психотропными и сомато-тропными препаратами [4].
В настоящее время получила распространение точка зрения, согласно которой все нейролептики различаются главным образом по спектру побочных эффектов и принципом выбора терапии должно служить соотношение «риск/польза». Предполагается, что это соотношение у атипичных антипсихотиков более благоприятно по сравнению с нейролептиками I поколения. Однако вопрос различий по этому параметру между препаратами внутри группы нейролептиков новой генерации, как, впрочем, и в отношении типичных нейролептиков, остается открытым.
Данный обзор посвящен анализу возможности и целесообразности применения атипичных антипсихотиков off-label – не по показаниям, в том числе с позиции соотношения «риск/польза». Следует отметить, что этот вопрос рассматривается в литературе последних лет именно в отношении нейролептиков II генерации.
Официальные показания для нейролептической терапии весьма ограниченны. Так, нейролептики одобрены Управлением по контролю пищевых продуктов и лекарств в США (FDA) для лечения шизофрении, биполярного аффективного расстройства (БАР) и некоторые из них – депрессии. При этом, например, 2-летнее исследование применения кветиапина в психиатрических больницах показало, что лишь 1/4 пациентов, получавших препарат, имели диагноз, при котором он одобрен, и только 1/3 пациентов получали его в стандартных дозах. Чаще всего кветиапин использовали при депрессии и в наркологической практике [154].
В зарубежной литературе имеются указания, что наиболее часто среди атипичных антипсихотиков применяются off-label рисперидон, кветиапин и оланзапин [13, 40, 91], а, например, в США, по данным 2009 г., – кветиапин и рисперидон [154].
В качестве мишеней применения нейролептиков помимо психозов выделяют бессонницу, тревогу, обсессивно-компульсивное расстройство (ОКР), возбуждение и другие поведенческие расстройства [123]. Высказано мнение, что наиболее распространенные психические расстройства для применения антипсихотиков off-label – посттравматическое стрессовое расстройство (ПТСР) и «малая депрессия» [115]. Данные канадских, британских, французских, австралийских, турецких, немецких, новозеландских и итальянских психиатров говорят об опыте применения атипичных антипсихотиков при тревоге [24, 40, 67, 91, 185], синдроме дефицита внимания и гиперактивности – СДВГ [19, 91], расстройствах личности – РЛ [185], депрессии [74, 91, 185], деменции [13, 81, 144, 166, 171, 198], расстройствах пищевого поведения – РПП [82].
Анализ использования атипичных антипсихотиков off-label с помощью англоязычных материалов PubMed, Embase, PsycINFO, CINAHL (Cumulative Index to Nursing and Allied Health Literature), Cochrane DARE (Database of Abstracts of Reviews of Effects) и Cochrane CENTRAL (Cochrane Central Register of Controlled Trials) на примере 170 статей, опубликованных до мая 2011 г. включительно, показал, что атипичные антипсихотики применялись при тревожном расстройстве, СДВГ, деменции и выраженной ажитации у пожилых, депрессии, РПП, бессоннице, ОКР, ПТСР, РЛ, зависимостях и синдроме Туретта [123].
В одном из плацебо-контролируемых исследований оланзапин оказался эффективнее плацебо [28], в 2 других – кветиапин не отличался от плацебо в терапии социальной фобии [68, 190].
Кветиапин в дозе 50 или 150 мг/сут оказался схожим по эффективности с пароксетином в дозе 20 мг/сут при терапии генерализованного тревожного расстройства (ГТР) в течение 8 нед, но при этом лечение кветиапином сопровождалось меньшей частотой побочных эффектов со стороны половой сферы [27]. Показано, что 150 или 300 мг/сут кветиапина равны по эффективности 10 мг/сут эсциталопрама в терапии ГТР в течение 8 нед [134]. При поддерживающей монотерапии кветиапином наблюдалось достоверное снижение риска рецидива эпизодов генерализованной тревоги [109].
Ряд активно контролируемых исследований, базировавшихся на наличии терапевтического ответа (снижение общего показателя по шкале тревоги Гамильтона – НАМ-А минимум на 50%), был направлен на оценку эффективности комбинированной терапии нейролептиками и различных лекарственных средств. Обнаружено, что аугментация кветиапином и кветиапином пролонг антидепрессивной терапии препаратами группы селективных ингибиторов обратного захвата серотонина (СИОЗС), в частности пароксетином, не дает преимуществ в преодолении терапевтической резистентности при ГТР [14, 111, 175].
В 8-недельном рандомизированном плацебо-контролируемом исследовании установлена эффективность сочетанной терапии рисперидоном в малых дозах и пароксетином при паническом расстройстве [156].
Результаты применения атипичных антипсихотиков при ПТСР противоречивы. Есть данные, которые свидетельствуют об эффективности рисперидона [29, 89, 136, 149, 158] и оланзапина [48, 180]. Анализ 5 работ, которые включали от 19 до 65 пациентов, получавших лечение в течение 5–16 нед [29, 89, 158, 162, 180], выявил умеренно значимую эффективность рисперидона в дозе 0,5–3 мг/сут (4 исследования) и оланзапина (15 мг/сут). Соответственно, относительный риск составил 6,47 (c 95% доверительным интервалом – ДИ 0,32–12,61) и 12,13 (95% ДИ 0,97–23,29), суммарно 7,79 (95% ДИ 2,40–13,17) [123]. Отмечена эффективность рисперидона в отношении отдельных симптомов ПТСР (раздражительности и навязчивых мыслей) [136].
Наряду с этим в метаанализе 2011 г. выявлен некоторый положительный эффект рисперидона и кветиапина, но не оланзапина [11]. В исследовании M.Butterfield и соавт. также было установлено, что оланзапин по эффективности не отличался от плацебо [48]. Небольшие (от 15 до 94 пациентов с ПТСР) исследования, в основном посвященные применению рисперидона, дали неоднозначные результаты [29, 89, 90, 136, 148, 149, 158, 162].
Метаанализы показали, что кветиапин и рисперидон весьма эффективны в качестве комбинированной терапии ОКР [123, 174]. Однако в отдельных работах повышение вероятности терапевтического ответа на основании результатов обсессивно-компульсивной шкалы Йеля–Брауна (Yale Brown Obsessive Compulsive Scale, Y-BOCS) достигло уровня статистической значимости для рисперидона, но не для кветиапина и оланзапина [37, 176].
Восемь работ, опубликованных с 2006 по 2011 г., 5 из которых – плацебо-контролируемые, свидетельствуют об эффективности аугментации кветиапином или рисперидоном антидепрессивной терапии циталопрамом либо ИОЗС: соответственно, 2,36 (95% ДИ 0,85–6,57), 3,92 (95% ДИ 1,27–12,13) [61, 63, 65, 114, 123, 125, 129, 194, 195]. Вместе с тем число пациентов, включенных в эти исследования, было невелико – от 18 до 66.
Применение при ОКР кветиапина в сочетании с СИОЗС
(в отличие от кломипрамина) оказалось эффективным, по данным Y-BOCS [65]. В сочетании с ИОЗС кветиапин показал себя как более эффективный препарат по сравнению с зипрасидоном (80 и 44,4% улучшение по шкале Y-BOCS соответственно) [164]. Следует отметить, что кветиапин эффективен как при лечении ОКР, так и ГТР: при ГТР кветиапин повысил вероятность ответа на терапию на 26% по сравнению с плацебо (минимум 50% улучшение по НАМ-А), при ОКР – в 3,9 раза (25–35% улучшение по шкале Y-BOCS).
При сравнении разных атипичных антипсихотиков в лечении ОКР было выяснено, что терапевтический эффект монотерапии оланзапином или рисперидоном существенно не различается [41].
В австралийском исследовании на примере 154 больных ОКР было показано, что 60,4% получали психотропную терапию, из них 59,1% – СИОЗС, а прием антипсихотических препаратов был ассоциирован с наличием хульных мыслей [123].
В метаанализе 2006 г., направленном на оценку возможностей применения атипичных антипсихотиков при большой депрессии, было выявлено отсутствие различий между атипичными антипсихотиками и плацебо в сочетании их с СИОЗС при длительности лечения 8 нед. В некоторых исследованиях, впрочем, атипичные антипсихотики способствовали более быстрой редукции депрессивной симптоматики (2–4 нед) [174].
В метаанализах Papakostas 2007 и 2009 гг. было выявлено положительное влияние аугментации атипичными антипсихотиками по числу ответов на терапию и достижению ремиссии при отсутствии различий в эффективности между отдельными препаратами (оланзапином, кветиапином, рисперидоном, арипипразолом) [138, 151]. Есть данные, что монотерапия кветиапином существенно увеличивает период до следующего эпизода депрессии [22].
С 2006 по 2011 г. вышло 26 статей о применении атипичных антипсихотиков при депрессии в качестве аугментации антидепрессивной терапии СИОЗС у пациентов с резистентной депрессией [30, 34, 35, 50, 72, 77, 80, 110, 113, 124, 126, 130, 132, 139, 157, 203]. При аугментации рисперидоном была выявлена большая дезактуализация суицидных мыслей по сравнению с монотерапией антидепрессантами [157]. Арипипразол в качестве аугментации антидепрессивной терапии позволял добиться терапевтического ответа (достоверная динамика по шкале Монтгомери–Асберга) [113].
Данные активно контролируемых исследований свидетельствуют о значительном улучшении состояния по шкале Монтгомери–Асберга у больных с депрессией, получавших сочетанную терапию оланзапином и флуоксетином, по сравнению с монотерапией одним из этих препаратов [188]. Добавление кветиапина в терапевтическую схему к пароксетину или венлафаксину усиливало антидепрессивный эффект (по данным шкалы депрессии Гамильтона – HAMD-17) [97]. Восьминедельное исследование эффективности зипрасидона в качестве аугментации терапии сертралином продемонстрировало максимальное улучшение состояния по общей клинической шкале CGI-S и шкале Монтгомери–Асберга при назначении 160 мг зипрасидона (по сравнению с 80 мг зипрасидона либо монотерапией сертралином) [71]. Впрочем, по HAMD-17 и HAM-A значительных различий найдено не было.
Данные литературы свидетельствуют о достижении ремиссии депрессии через 4–8 нед при сочетанной терапии антидепрессантами и атипичными антипсихотиками [80, 110, 124, 130, 132, 203]. Вероятность ремиссии (по HAMD) при применении антипсихотика была определена как 2,76 (95% ДИ 1,21–6,28) для кветиапина и 2,10 (95% ДИ 1,43–3,09) для рисперидона. Вероятность ответа на терапию (минимум 50% снижение по HAMD) составила 2,30 (95% ДИ 1,35–3,92) для кветиапина и 1,50 (95% ДИ 1,20–1,87) для рисперидона [123].
Ремиссия (уровень депрессии от 8 до 10 баллов по шкале Монтгомери–Асберга в зависимости от исследования) была зафиксирована в 8 исследованиях комбинированной терапии [30, 34, 35, 72, 77, 110, 126] – от 97 до 493 обследованных больных. Доказана эффективность арипипразола и кветиапина: арипипразол против плацебо – 1,57 (95% ДИ 1,24–2,00) и кветиапин против плацебо – 1,24 (95% ДИ 0,82–1,88) [123].
В ряде исследований, которые включали от 310 до 723 пациентов, подтверждена эффективность монотерапии депрессии кветиапином: в течение 6–9 нед терапии вероятность достижения ремиссии (по шкале Монтгомери–Асберга) составила 1,43 (95% ДИ 1,07–191) по сравнению с плацебо – 1,49 (95% ДИ 1,23–1,81) [21, 23, 39, 59, 123, 196]. Кветиапин оказался более эффективным по сравнению с препаратами лития при терапии в течение 56 дней (по шкале депрессии Гамильтона, Монтгомери–Асберга и Wildlocher Psychomotor Retardation Scales) [69].
Обзор 4 рандомизированных контролируемых исследований 2011 г. по применению антипсихотиков при соматоформном расстройстве показал эффективность сульпирида при диспепсии и неэффективность антипсихотиков при дисморфофобии [62].
Hagman и соавт. утверждает, что успешная психотропная терапия для страдающих анорексией все еще не найдена. Так, рисперидон (средняя доза 2,5 мг/сут, длительность приема 9 нед) при лечении 40 пациенток в возрасте от
12 до 21 года помог лишь снизить показатель «межличностное недоверие», но не привел к прибавке массы тела и иным существенным изменениям [103]. Аналогично нейтральные или негативные результаты демонстрируют и другие исследования нейролептической терапии анорексии [25, 57, 58, 86, 95, 127, 182]. Побочные эффекты, такие как седация и дислипидемия, которые, например, в австралийском исследовании 2011 г. встречались у 56% пациентов при приеме оланзапина, серьезно ограничивают возможность и усложняют нейролептическую терапию нервной анорексии [145].
Имеются данные о применении нейролептической терапии при некоторых РЛ. Антипсихотики широко используются при пограничном РЛ, поскольку считаются эффективными средствами против импульсивности, агрессии, тревоги [15, 31, 102, 146]. Их применение считается оправданным для коррекции расстройств мышления и восприятия у этих больных [92]. Однако побочные эффекты обусловливают применение антипсихотиков преимущественно при обострениях [33, 64, 141, 186].
Некоторые плацебо-контролируемые исследования указывают на эффективность при пограничном РЛ арипипразола [142, 143] (в дозе 5–10, но не 2,5 мг/сут), оланзапина [202], а также кветиапина, в том числе в отношении психотической симптоматики [191]. Другие свидетельствуют лишь о более быстром ответе на терапию при приеме зипрасидона или кветиапина [118, 152, 169]. Значительных различий в эффекте (улучшение настроения, снижение уровня тревоги) оланзапина и галоперидола не найдено [170]. Имеются данные, что клозапин нивелирует агрессию и психотическую симптоматику при пограничном РЛ [33, 51, 52, 75, 183].
Среди работ, посвященных применению при пограничном РЛ рисперидона, наиболее крупной является исследование Rocca и соавт. на 15 пациентах, у которых была отмечена положительная динамика агрессивного поведения, аффективных и других психических расстройств [93, 112, 160, 184].
Девять пациентов с коморбидными пограничным РЛ и дистимией через 8 нед применения оланзапина (средняя доза 3,3 мг/сут) обнаружили значительное снижение импульсивности, улучшение психического состояния и социального функционирования [168]. Zanarini и Frankenburg в полугодовом двойном слепом плацебо-контролируемом исследовании на 28 пациентках с пограничным РЛ показали эффективность оланзапина (5,33 мг/сут) в виде снижения тревоги, параноидных мыслей и улучшения коммуникабельности [201]. Также продемонстрирована эффективность оланзапина в дозе 5–10 [38] и 8,8 мг/сут в течение 12 нед в отношении импульсивного, агрессивного поведения, депрессии и тревоги [179]. Оланзапин в малых дозах уменьшает частоту самоповреждений [96]. Результаты исследования 2004 г. говорят о том, что сочетание флуоксетина и оланзапина более эффективны, чем монотерапия этими препаратами [12].
В нескольких исследованиях, посвященных кветиапину при пограничном РЛ, положительный результат был продемонстрирован при использовании от 25 до 400 мг/сут [10, 31, 32, 192].
Результаты лечения героиновых наркоманов с пограничным РЛ, проходящих поддерживающую терапию метадоном, свидетельствуют об успешном воздействии оланзапина на симптомы депрессии, тревоги и агрессии, обсессивную симптоматику, соматизированные расстройства [102, 147].
При шизотипическом РЛ рисперидон не отличался по эффективности от плацебо [131].
Рандомизированное контролируемое исследование, проведенное в Таиланде на 13 пациентах, не дает возможности судить об эффективности применения атипичных антипсихотиков для лечения бессонницы. Однако было показано, что применение кветиапина привело к удлинению сна на 125 мин по сравнению с 72 мин при приеме плацебо [123]. В 6 других описательных исследованиях оценивалась терапия кветиапином или оланзапином.
Последний оказал благоприятное воздействие на качество сна и «медленный» сон у 12 пациентов, получавших его на протяжении 3 нед [172], а также на длительность сна и количество ночных кошмаров у 8 из 9 пациентов на протяжении периода до 3 лет [73]. Рекомендуемые дозы составили от 2,5 до 10 мг на ночь в зависимости от самочувствия пациентов и данных полисомнографии. Накоплен опыт применения кветиапина при первичной бессоннице [197], бессоннице, связанной с абстинентным синдромом [187], у больных с опухолями [153] и с болезнью Паркинсона [105], однако данные недостаточно убедительны. Дозировки составляли от 12,5 до 225 мг ежедневно, курс лечения – от 6 нед до 3 мес. Обзор 2006 г. привел обнадеживающие результаты 3 плацебо-контролируемых исследований терапии расстройств сна оланзапином и 1 – арипипразолом [174].

Большое внимание исследователей уделяется применению атипичных антипсихотиков при деменции у пожилых пациентов, что связано с распространением их использования и связанного с этим повышения летальности среди этих больных [49]. Как показал метаанализ Maglione и соавт., эффективность в отношении психотических расстройств, ажитации у больных с деменцией установлена у арипипразола, оланзапина и особенно явно – у рисперидона, но не у кветиапина [123].
По данным метаанализов 2005–2006 гг., был обнаружен невыраженный, но статистически значимый терапевтический эффект рисперидона и арипипразола и тенденция к эффективности у оланзапина и кветиапина в отношении психотических расстройств и агрессии у больных с деменцией [26, 60, 147, 167]. В более позднем метаанализе не было выявлено существенного отличия между атипиками и плацебо в отношении поведенческих расстройств при деменции [200].
Результаты сравнения атипичных антипсихотиков и галоперидола показывают, что их воздействие на психотическую симптоматику и ажитацию при деменции различается несущественно. С другой стороны, не были найдены заметные различия между атипичными антипсихотиками (оланзапин, кветиапин, рисперидон) по терапевтической эффективности и исходам психозов при деменции [123].
По данным 129 крупных и/или плацебо-контролируемых исследований, у пациентов старшего возраста побочные эффекты терапии антипсихотиками включают повышенный риск смерти, инсульта, заболевания мочевой системы, развития экстрапирамидного синдрома. У взрослых лиц в возрасте до 64 лет отмечают прибавку массы тела (особенно при приеме оланзапина), повышенную утомляемость, седацию, акатизию (наибольший риск при приеме арипипразола), экстрапирамидные симптомы. Вместе с тем разница между побочными эффектами у пожилых пациентов с депрессией, принимавших рисперидон и антидепрессанты группы СИОЗС, не найдена [123].
Обзор 2006 г. продемонстрировал статистически значимую взаимосвязь между применением атипичных антипсихотиков и вероятностью смерти у пациентов с болезнью Альцгеймера (3,5%) по сравнению с 2,3% при приеме плацебо [174]. В то же время из 6 больших когортных исследований 4 выявили большую по сравнению с атипиками смертность среди больных, принимавших классические нейролептики [81, 101, 106, 119, 161, 166].
В 2004 г. почти 25% жителей домов престарелых в США получали нейролептики, преимущественно II поколения [123]. После предупреждения FDA в 2005 г. о повышенной смертности вследствие их употребления частота их использования уменьшилась, особенно среди пациентов, страдающих деменцией [70]. Впрочем, опрос профессионалов в сфере охраны здоровья показал, что лишь 49% врачей изменили свое отношение к назначению нейролептиков у пожилых: остальные не отреагировали на преду-преждение по причинам отсутствия альтернатив, недостатка руководств и доказательств [163].
В наркологии нейролептики используются при наличии коморбидных и метааддиктивных расстройств (отдельных формах психопатических и психопатоподобных нарушений, расстройствах невротического круга, дисфорических состояниях в ранней фазе опиоидной постабстиненции). Они улучшают прогноз заболевания, особенно у лиц шизоидного склада, и не вызывают зависимости.
Ю.П.Сиволап и В.А.Савченков в статье о применении нейролептиков в наркологической практике (2007 г.) указывают, что, несмотря на недостаточное и неоднозначное их влияние на аддиктивное влечение, эти препараты успешно нашли применение при психозах и пограничных расстройствах невротического, личностного и аффективного характера у злоупотребляющих психоактивными веществами [8].
Рисперидон оказался эффективным при многих состояниях, в том числе острых абстинентных и интоксикационных психозах и эндоморфных психотических синдромах у больных алкоголизмом. Этот препарат хорошо зарекомендовал себя в коррекции дисфории и психопатоподобных расстройств. Отмечено его положительное влияние на комплаенс наркологических пациентов. Имеются исследования, посвященные применению таких атипичных антипсихотиков, как арипипразол [17, 18, 128, 193], оланзапин [85, 98–100] и кветиапин [84, 108], при злоупотреблении алкоголем и алкогольной зависимости, а также арипипразола [117, 181], оланзапина [88, 107, 159] и рисперидона [83, 116, 120, 177, 178] при злоупотреблении кокаином и кокаиновой зависимости. Арипипразол оказался неэффективным лекарством при злоупотреблении амфетамином/метамфетамином [140, 189], а оланзапин – при лечении героиновой зависимости [79].
Опыт лечения алкоголизма с помощью атипичных антипсихотиков говорит о том, что наиболее частым результатом является достижение воздержания от алкоголя. Длительность воздержания от алкоголя и число пациентов, достигших полного воздержания от употребления алкоголя, не различались при лечении налтрексоном и арипипразолом [128]. Вместе с тем в плацебо-контролируемом исследовании было показано, что терапия арипипразолом не способствовала увеличению периода воздержания от алкоголя [17]. Однако аугментация кветиапином терапии налтрексоном оказалась эффективной [84].

Данные метаанализа 2006 г. о нейролептической терапии синдрома Туретта свидетельствуют о преимуществах рисперидона перед плацебо. Неоднозначные данные были получены об эффективности зипрасидона [174]. Описательные работы о лечении тиков (в возрасте до 18 лет) с помощью арипипразола свидетельствуют об улучшении состояния, однако довольно значительная часть пациентов (8 из 37 и 6 из 24) были вынуждены прервать курс лечения в связи с побочными эффектами [47, 199].
Рисперидон, как антипсихотик с антисеротониновым действием, в средней дозе 2,5 мг/сут показал положительный эффект при лечении синдрома Туретта в open-label-исследованиях и двойных слепых плацебо-контролируемых исследованиях, в частности Guy Chouinard, на 48 пациентах [16, 45, 46, 53, 54, 66, 76, 122, 165]. Так, 60,8% пациентов по сравнению с 26,1% пациентов, получавших плацебо, обнаружили улучшение общего функционирования. Влияния рисперидона на дистонию, дискинезии, акатизию обнаружено не было, притом что гипокинезия и тремор (в случаях его изначальной выраженности) наросли.
Особой проблемой является ограниченное применение нейролептической терапии у детей. Halloran и соавт. изучали паттерны назначения атипичных антипсихотиков частно застрахованным детям в США в возрасте от 2 до
18 лет в период 2002–2005 гг. и определили, что частота назначения нарастает (с 7,9 до 9,0 на 1 тыс. случаев). Мальчикам назначали почти в 2 раза больше препаратов, чем девочкам. Среди причин назначения преобладали поведенческие расстройства (67%), расстройства настроения (65%) и тревожные расстройства (43%), причем 75% детей имели более одного психиатрического диагноза. Чаще всего пациентам детского возраста назначали рисперидон (53%) и кветиапин (33%) [87].
Небольшое количество работ посвящено лечению антипсихотиками СДВГ. В одном из них все пациенты ответили на терапию рисперидоном, притом что на плацебо ответили 77% пациентов [20]. У детей с коморбидными СДВГ и умеренной умственной отсталостью рисперидон по сравнению с метилфенидатом оказался более эффективным [55]. Результаты 2 исследований, посвященных применению арипипразола при СДВГ в сочетании с БАР, не показали улучшения [123].
Клинический случай
Больная М. 55 лет, замужем, несколько лет не работает.
В течение примерно 10 лет постоянно безуспешно посещает различных специалистов-дерматологов в связи с убежденностью «заражения паразитами». Предъявляет жалобы на ощущение «передвижения насекомых» под кожей, неровность кожных покровов. Детально описывает размеры, строение, пути передвижения, жизненный цикл паразитов. Регулярно сдает для проведения микроскопического исследования «вещественные доказательства» – «частицы насекомых» представляются в лаборатории как личинки, яйца или продукты жизнедеятельности паразитов.
Занимается «вытравливанием» насекомых из организма. «Борьба» с паразитами включает такие методы самолечения, как механическое воздействие, едкие жидкости. Лицо, шея, плечи, грудь пациентки имеют выраженные дефекты кожного покрова (глубокие обезображивающие шрамы). Обрабатывает химическими веществами одежду, белье.
Таким образом, в клинической картине у пациентки дерматологической практики представлены монотематический паранойяльный зоопатический бред, тактильный галлюциноз, «симптом спичечного коробка», патомимия – кожные аутодеструктивные проявления, что соответствует дерматозойному бреду – инволюционной паранойе.
Назначен рисперидон (Торендо). Начальная доза составила 2 мг/сут, на 2-й день дозу повысили до 4 мг/сут. На фоне терапии рисперидоном (Торендо) в течение месяца наблюдались улучшение социальной адаптации, снижение актуальности патологических идей, редукция соматосенсорных феноменов восприятия.
Данный случай иллюстрирует применение рисперидона (Торендо) в психосоматике в режиме off-lable.
Доказательная сила эффективности различных препаратов приведена в таблице [123].
Таким образом, арипипразол, оланзапин и рисперидон оказывают не выраженный, но статистически значимый эффект в лечении психотических расстройств, возбуждения и поведенческих симптомов при деменции, однако следует учитывать значительный риск побочных эффектов. Зипрасидон не имеет достаточной доказательной базы для применения его off-label, за исключением депрессии. Умеренной силы доказательная база говорит об эффективности арипипразола, кветиапина и рисперидона в качестве аугментации антидепрессивной терапии: вероятность терапевтического ответа возрастает в 1,5–2 раза. Данных о применении оланзапина недостаточно, но они обнадеживают. Оланзапин продемонстрировал достаточную эффективность в терапии социальной фобии и ОКР. Умеренная доказательность наблюдается в отношении эффективности монотерапии депрессии кветиапином, аугментации терапии ОКР рисперидоном. Доказана эффективность и безопасность применения кветиапина при ГТР, рисперидона при ПТСР. Отсутствуют убедительные данные об эффективности атипичных антипсихотиков при РЛ, диссомнии, РПП и аддикции.
Сведения об авторах
Петрова Наталия Николаевна – д-р мед. наук, зав. каф. психиатрии и наркологии мед. фак. СПбГУ.
E-mail: petrova_nn@mail.ru
Дорофейкова Мария Владимировна – студентка 6 курса мед. фак. СПбГУ. E-mail: mvdorofeykova@mail.ru
Список исп. литературыСкрыть список1. Авруцкий Г.Я., Гурович И.Я., Громова В.В. Фармакотерапия психических заболеваний. М.: Медицина, 1974.
2. Авруцкий Г.Я., Недува A.A. Лечение психически больных. М.: Медицина, 1988.
3. Вовин Р.Я. Шизофренический дефект (диагностика, патогенез, лечение). СПб.: Психоневрологический институт им. В.П.Бехтерева, 1991.
4. Костерин Д.Н. Оптимизация стационарной терапии больных шизофренией с применением атипичных антипсихотиков. Автореф. дис. … д-ра мед. наук, 2005.
5. Мосолов С.Н. Основы психофармакотерапии. М.: Восток, 1996.
6. Нуллер Ю..Л. Практические аспекты психофармакотерапии: трудности и ошибки. Психиатр. и психофармакотер. 2002; 4 (1): 16–8.
7. Пантелеева Г.П. Терапия основных форм шизофрении. В кн.: Руководство по психиатрии. Под ред. A.C.Тиганова. T. 1. М.: Медицина, 1999; с. 528–37.
8. Сиволап Ю.П., Савченков В.А. К проблеме рационального применения нейролептиков в наркологической практике. Наркология. 2007; 1: 32–7.
9. Смулевич А.Б., Пантелеева Г.П. Некоторые актуальные проблемы клинической психофармакологии. Журн. невропатол. и психиатр. 1983; 9: 1345–51.
10. Adityanjee A, Schulz SC. Clinical use of quetiapine in disease states other than schizophrenia. J Clin Psychiat 2002; 63 (Suppl. 13): 32–8.
11. Ahearn EP, Juergens T, Cordes T et al. A review of atypical antipsychotic medications for post-traumatic stress disorder. Int Clin Psychopharmacol 2011; 26 (4): 193–200.
12. Akerele E, Levin FR. Comparison of olanzapine to risperidone in, comparison of olanzapine to risperidone in abusing with schizophrenia. Am J Addict 2007; 16: 260–8.
13. Alessi-Severini S, Biscontri RG, Collins DM et al. Utilization and costs of antipsychotic agents: a Canadian population-based study, 1996–2006. Psychiat Serv 2008; 59 (5): 547–53.
14. Altamura AC, Serati M, Buoli M et al. Augmentative quetiapine in partial/nonresponders with generalized anxiety disorder: a randomized, placebo-controlled study. Int Clin Psychopharmacol 2011; 26 (4): 201–5.
15. American Psychiatric Association. Practice guideline for the treatment of patients with borderline personality disorder. Am J Psychiat 2001; 158: 1–52.
16. American Psychiatric Association. Diagnostic and statistical manual of mental disorders (DSM-III-R). 3rd ed. Washington: Association 1987.
17. Anton R, Breder C, Han J et al. Aripiprazole in the treatment of alcohol dependence: results from a multisite study. Neuropsychopharmacol 2006; 31 (Suppl. 1): 200.
18. Anton RF, Kranzler H, Breder C et al. A randomized, multicenter, double-blind, placebo-controlled study of the efficacy and safety of aripiprazole for the treatment of alcohol dependence. J Clin Psychopharmacol 2008; 28 (1): 5–12.
19. Aras S, Varol Tas F, Unlu G. Medication prescribing practices in a child and adolescent psychiatry outpatient clinic. Child Care Health Dev 2007; 33 (4): 482–90.
20. Armenteros JL, Lewis JE, Davalos M. Risperidone augmentation for treatment-resistant aggression in attention-deficit/hyperactivity disorder: a placebo-controlled pilot study. J Am Acad Child Adolesc Psychiat 2007; 46 (5): 558–65.
21. AstraZeneca. A multi-center, double-blind, randomized, parallel-group, placebo-controlled phase III study of the efficacy and safety of quetiapine fumarate extended-release (Seroquel XR™) as mono-therapy in the treatment of elderly patients with major depressive Disorder (SAPPHIRE STUDY). http://www.astrazenecaclinicaltrials.com/ _mshost800325/content/clinicaltrials/resources/pdf/8579646 ClinicalTrials.gov ID NCT00388973. Study code: D1448C00014
22. AstraZeneca. A multicenter, double-blind, randomized-withdrawal, parallel-group, placebo-controlled phase III study of the efficacy and safety of quetiapine fumarate extended release (SEROQUEL XR™) as monotherapy in the maintenance treatment of patients with major depressive disorder following an open-label stabilization period (AMETHYST STUDY) 2008.
23. AstraZeneca. A multi-centre, double-blind, randomised, parallel group, placebo-controlled and active controlled phase III study of the efficacy and safety of quetiapine fumarate extended release (SEROQUEL XR TM) as mono-therapy in the treatment of adult patients with major depressive disorder (AMBER STUDY). http://www.astrazenecaclinicaltrials.com/_mshost800325/content/clinicaltrials/resources/pdf/8579603 ClinicalTrials.gov ID NCT00351169. Study code: D1448COOO04
24. Atik L, Erdogan A, Karaahmet E et al. Antipsychotic prescriptions in a university hospital outpatient population in Turkey: a retrospective database analysis, 2005–2006. Prog Neuropsychopharmacol Biol Psychiat 2008; 32 (4): 968–74.
25. Attia E, Haiman C, Walsh BT, Flater SR. Does fluoxetine augment the inpatient treatment of anorexia nervosa? Am J Psychiat 1998; 155: 548–51.
26. Ballard C, Waite J. The effectiveness of atypical antipsychotics for the treatment of aggression and psychosis in Alzheimer's disease. Cochrane Database Syst Rev 2006; 1: CD003476.
27. Bandelow B, Chouinard G, Bobes J et al. Extended-release quetiapine fumarate (quetiapine XR): a once-daily monotherapy effective in generalized anxiety disorder. Data from a randomized, double-blind, placebo- and active-controlled study. Int J Neuropsychopharmacol 2009; 13 (3): 305–20.
28. Barnett SD, Kramer ML, Casat CD et al. Efficacy of olanzapine in social anxiety disorder: a pilot study. J Psychopharmacol 2002; 16 (4): 365–8.
29. Bartzokis G, Lu PH, Turner J et al. Adjunctive risperidone in the treatment of chronic combat-related post-traumatic stress disorder. Biol Psychiat 2004; 57 (5): 474–9.
30. Bauer M, Pretorius HW, Constant EL et al. Extended-release quetiapine as adjunct to an antidepressant in patients with major depressive disorder: results of a randomized, placebo-controlled, double-blind study. J Clin Psychiat 2009; 70 (4): 540–9.
31. Belli H, Ural C, Akbudak M. Borderline personality disorder: bipolarity, mood stabilizers and atypical antipsychotics in treatment. J Clin Med Res 2012; 4 (5): 301–8.
32. Bellino S, Paradiso E, Bogetto F. Efficacy and tolerability of quetiapine in the treatment of borderline personality disorder: a pilot study. J Clin Psychiat 2006; 67 (7): 1042–6.
